人工皮膚
背景
人体最大の臓器である皮膚は、病気や身体的損傷から体を守り、体温を調節するのに役立ちます。表皮と真皮の2つの主要な層で構成されています。表皮または外層は、主に細胞で構成されています:ケラチノサイト、メラノサイト、およびランゲルハンス。主にコラーゲンなどの結合組織繊維で構成される真皮は、表皮に栄養を供給します。
皮膚が病気や火傷によって深刻な損傷を受けた場合、体は必要な代替細胞を製造するのに十分な速さで行動することができません。糖尿病患者が苦しんでいる皮膚潰瘍などの傷は治癒しない可能性があり、手足を切断する必要があります。火傷の犠牲者は、感染と血漿の喪失で死亡する可能性があります。植皮は、そのような結果を防ぎ、変形を矯正する方法として開発されました。早くも6世紀 B.C。 、ヒンズー教の外科医は、患者の鼻から皮弁を移植して、鼻の再建に関与しました。イタリアの医師であるガスパーレタリアコッツォは、16世紀にこの技術を西洋医学にもたらしました。
20世紀後半まで、植皮は患者自身の皮膚(自家移植)または死体の皮膚(同種移植)から構築されていました。感染、または死体の皮膚の場合は拒絶反応が主な懸念事項でした。患者の体のある部分から別の部分に移植された皮膚は拒絶反応の影響を受けませんが、ドナーからレシピエントへの皮膚移植は他のどの組織移植や移植よりも積極的に拒絶されます。死体の皮膚は、火傷の犠牲者の最初の治癒期間中の感染および体液の喪失からの保護を提供することができるが、その後の患者自身の皮膚の移植がしばしば必要とされる。医師は、患者が利用できる皮膚に制限されており、重度の火傷の犠牲者の場合には明らかに不利です。
1980年代半ば、細胞生物学とプラスチック製造の分野で働く医学研究者と化学技術者が力を合わせて、感染と拒絶の発生を減らすための組織工学を開発しました。組織工学の触媒の1つは、移植に利用できる臓器の不足が拡大していることでした。 1984年、ハーバード大学医学部の外科医であるジョセフバカンティは、利用可能な肝臓がないことへの不満を、マサチューセッツ工科大学の化学技術者である同僚のロバートランガーと共有しました。一緒に、彼らは新しい器官が実験室で育てられることができるかどうか考えました。最初のステップは、体の組織の生成を複製することでした。ランガーは、割礼中に除去された提供された新生児包皮から抽出された細胞である線維芽細胞を使用して皮膚細胞を成長させることができる生分解性足場を構築するというアイデアを思いつきました。
他の研究者によって開発されたこの技術のバリエーションでは、抽出された線維芽細胞は、結合組織に見られる繊維状タンパク質であるコラーゲンに追加されます。化合物が加熱されると、コラーゲンはゲル化して線維芽細胞をトラップし、線維芽細胞はコラーゲンの周りに配置され、コンパクトで緻密で繊維状になります。数週間後、寄付された包皮から抽出されたケラチノサイトが新しい真皮組織に播種され、そこで表皮層が形成されます。
人工植皮は、患者や死体に由来するものに比べていくつかの利点があります。それはティッシュの必要性を排除します 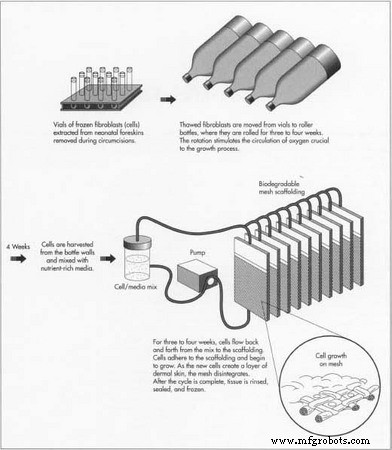 入力。人工皮膚は大量に作ることができ、保管や輸送のために冷凍して、必要に応じて利用できるようにします。各培養物は病原体についてスクリーニングされ、感染の可能性を大幅に削減します。人工皮膚には樹状細胞や毛細血管内皮細胞などの免疫原性細胞が含まれていないため、体に拒絶されることはありません。最後に、リハビリテーション時間が大幅に短縮されます。
入力。人工皮膚は大量に作ることができ、保管や輸送のために冷凍して、必要に応じて利用できるようにします。各培養物は病原体についてスクリーニングされ、感染の可能性を大幅に削減します。人工皮膚には樹状細胞や毛細血管内皮細胞などの免疫原性細胞が含まれていないため、体に拒絶されることはありません。最後に、リハビリテーション時間が大幅に短縮されます。
原材料
人工皮膚の製造に必要な原材料は、生物学的成分と必要な実験装置の2つのカテゴリーに分類されます。提供された皮膚組織のほとんどは、割礼中に除去された新生児の包皮から来ています。 1つの包皮は、4エーカーの接ぎ木材料を作るのに十分な細胞を生み出すことができます。線維芽細胞は、提供された組織の真皮層から分離されます。線維芽細胞は、ウイルスや、IIV、B型およびC型肝炎、マイコプラズマなどの他の感染性病原体について検査されている間、隔離されます。母親の病歴が記録されます。線維芽細胞はガラスバイアルに保存され、-94°F(-70°C)の液体窒素で凍結されます。培養物を成長させるために線維芽細胞が必要になるまで、バイアルは凍結状態に保たれます。コラーゲン法では、ケラチノサイトも包皮から抽出され、テストされ、凍結されます。
線維芽細胞をメッシュ足場で成長させる場合、溶解性縫合糸を作るために使用されるのと同じ要素である乳酸とグリコール酸の分子を組み合わせることによってポリマーが作成されます。化合物は化学反応を起こし、構造単位の繰り返しからなるより大きな分子を生成します。
コラーゲン法では、若い子牛の伸筋腱から少量のウシコラーゲンを抽出します。コラーゲンは酸性栄養素と混合され、39.2°F(4°C)の冷蔵庫に保管されます。
実験装置には、ガラスバイアル、チューブ、ローラーボトル、グラフトカートリッジ、金型、および冷凍庫が含まれます。
製造
プロセス
製造工程は一見シンプルです。その主な機能は、抽出された線維芽細胞をだまして人体にあると信じ込ませ、自然な方法で互いに通信して新しい皮膚を作成することです。
メッシュ足場法
- 1 線維芽細胞は解凍され、増殖します。 線維芽細胞は、バイアルから、リットルのソーダボトルに似たローラーボトルに移されます。ボトルは3〜4週間横向きに回転します。ローリングアクションは、成長プロセスに不可欠な酸素の循環を可能にします。
- 2 細胞を培養システムに移します。 細胞はローラーボトルから取り出され、栄養豊富な培地と組み合わされ、チューブを通って生分解性メッシュ足場を収容する薄いカセット状のバイオリアクターに流され、電子ビーム照射で滅菌されます。細胞がカセットに流れ込むと、細胞はメッシュに付着して成長し始めます。細胞は3〜4週間前後に流れます。毎日、残った細胞懸濁液を取り除き、新鮮な栄養素を加えます。酸素、pH、栄養素の流れ、および温度は、培養システムによって制御されます。新しい細胞が真皮の皮膚の層を作ると、ポリマーは崩壊します。
- 3 成長サイクルが完了しました。 メッシュ上での細胞増殖が完了すると、組織はより栄養豊富な培地ですすがれます。凍結防止剤が追加されます。カセットは個別に保管され、ラベルが付けられ、凍結されます。
コラーゲン法
- 4 細胞を培養システムに移します。 少量の冷たいコラーゲンと栄養培地、合わせた溶液の約12%が線維芽細胞に加えられます。混合物を型に分配し、室温に戻す。コラーゲンが温まると、コラーゲンはゲル化し、線維芽細胞を捕捉し、新しい皮膚細胞の成長を生み出します。
- 5 ケラチノサイトが追加されました。 コラーゲンが線維芽細胞に加えられてから2週間後、抽出されたケラチノサイトは解凍され、新しい真皮の皮膚に播種されます。それらは数日間成長させられ、次に空気にさらされ、ケラチノサイトが表皮層を形成するように誘導します。
- 6 成長サイクルが完了しました。 新しい皮膚は、必要になるまで滅菌容器に保管されます。
未来
医療専門家は、臓器再建の先駆者として人工皮膚技術を使用しています。このいわゆる人工構造組織は、たとえば、損傷した関節や骨の代わりに現在使用されているプラスチックや金属のプロテーゼに取って代わることが期待されています。耳と鼻は、ポリマーメッシュに軟骨細胞を播種することによって再構築されます。乳房および尿道組織の再生は現在、研究室で研究されています。この技術により、いつの日か肝臓、腎臓、さらには心臓さえも人間の組織から成長する可能性があります。
製造プロセス



