装填された薬物の化学的安定性に対するリポソームの微小環境pHの影響
要約
リポソームは、生物活性分子を送達するための有望な担体システムです。ただし、pHに敏感な分子の配信の成功は、生理学的環境におけるペイロードの本質的な不安定性によって依然として制限されています。ここでは、pHに敏感なペイロードの化学的安定性を向上させるために、内部の水性チャンバー内に酸性の微小環境を有する特別なリポソームシステムを開発しました。内部pH値(pH 2.5、5.0、または7.4)を変化させたクルクミンをロードしたリポソーム(Cur-LP)を準備しました。これらのCur-LPは、300 nmの同様の粒子サイズ、同等の物理的安定性、および類似のinvitro放出プロファイルを備えています。興味深いことに、50%ウシ胎児血清中のリポソームクルクミンの化学的安定性とin vitroでの抗がん効果は、どちらも微小環境のpHに依存します(Cur-LP-2.5> Cur-LP-5.0> Cur-LP-7.4)。この血清安定性には、Cur-LPの適用性を改善するためにさらに強化する余地があります。結論として、リポソームの内部チャンバーに酸性の微小環境を作り出すことは、pHに敏感なペイロードの化学的安定性を改善するために実行可能で効率的です。
背景
人工膜ビヒクルであるリポソームは、その薬物負荷能力、生分解性、および生体適合性により、薬物送達において大きな可能性を示しています[1,2,3,4]。古典的なリポソームは、構造が生細胞と類似しており、通常、リン脂質二重層と水性内部チャンバーで構成されています[5、6、7]。この構造により、リポソームは不溶性の薬物分子を可溶化し、負荷された薬物が過酷な生理学的環境から保護されるようにすることができます[8、9、10]。さらに、リポソームの表面を修飾して、血液循環時間を延長したり、特定の組織を標的にしたりすることができます[11、12、13、14、15]。これらの上記の利点により、さまざまなリポソームシステムが臨床的に承認されています[8、9、16]。
多くの薬物の送達はリポソームに組み込むことによって改善されましたが、一部のpH感受性薬物の送達は、生理学的環境(中性pH値)における薬物分子自体の不安定性によって依然として制限されています。一般に、リポソームは中性緩衝液中で調製されるため、ロードされた薬物分子もまた、リポソームに組み込まれた後、中性環境にある。したがって、酸性環境でのみ安定している分子は、リポソームの形でも依然として不安定である。したがって、pH感受性薬物の安定性を高めるための新しいアプローチの開発は、リポソームによるこれらのペイロードの送達を成功させるために非常に重要です。
上記のように、リポソームはその内部チャンバーに水性空間を持っており、これを使用して、酸性の微小環境を備えた薬物ペイロードを提供することができます(図1)。この現在の作業では、モデル薬物としてクルクミンを使用し、リポソームにロードされた薬物分子の化学的安定性を高めるための新しいアプローチを提供することを目指しています。クルクミンは親油性分子であり、そのさまざまな生物活性により、食品、医薬品、化粧品に広く使用されていることはよく知られています[17、18、19、20、21]。しかしながら、その送達は、体液におけるその不溶性および不安定性によって非常に制限されている[22、23、24、25]。これまでのところ、一部にはpHを介した不安定性のために、その臨床的期待はまだ果たされていません[26]。したがって、クルクミンはこの研究に適したモデル薬です。
内部水性チャンバー内のさまざまな微小環境酸性度を持つリポソームの概略図
メソッド
資料
リン脂質(注射用大豆レシチン)は、Shanghai Tai-Wei Pharmaceutical Co.、Ltd。(Shanghai、China)から購入しました。コレステロールはAmresco(Solon、OH、USA)から入手しました。ポロキサマー188(F68)は、BASF(China)Co.、Ltd。(上海、中国)から寄贈されました。クルクミンはSigma(St。Louis、MO、USA)から供給されました。ウシ胎児血清(FBS)は、HyClone(Logan、UT、USA)から購入しました。この研究で使用された他のすべての化学試薬は、分析グレード以上のものでした。
クルクミンをロードしたリポソーム(Cur-LP)の調製
さまざまな微小環境pH値を持つリポソームは、いくつかの変更を加えた以前の研究[27、28]に従って、蒸発法を使用して調製されました。簡単に説明すると、リン脂質(75 mg)とコレステロール(5 mg)を、2 mg / mlのクルクミンを含む0.5mlのエタノールに溶解しました。エタノール溶液を、1%( w )を含む5mlの0.001MPBSと混合しました。 / v )サイズ分布を狭めるための界面活性剤として機能したF68。 1分間磁気攪拌した後(恒温マグネチックミキサー、DF-101S、鄭州グレートウォールサイエンティフィックインダストリアルアンドトレード株式会社、鄭州、中国)、得られたエマルジョンを真空下で蒸発させ、35°Cで30分間暗くしました。エタノールを取り除きます。 Cur-LPの内部チャンバーの酸性度は、調製中に2.5、5.0、または7.4のさまざまなpH値を持つPBSを使用して調整しました。得られた懸濁液を低速(3000 rpm、5分)で遠心分離して、遊離のクルクミンを沈殿させました。次に、上清を高速(16 krpm、10分)で遠心分離し、さらに使用する前にペレットをPBS(pH 7.4)に再懸濁しました。この手順により、これらのLPに同一の外部環境が提供されました。異なる微小環境pH値で得られたリポソームは、それぞれCur-LP-2.5、Cur-LP-5.0、およびCur-LP-7.4として提示された。ブランクリポソームも上記のように作製した。
リポソームの特性評価
流体力学的サイズ、サイズ分布、およびゼータ電位は、リポソームシステムの3つの基本的なパラメーターです。 LPのサイズとゼータ電位は、25°CでZetasizerNano ZS90(Malvern Instruments Ltd.、Malvern、UK)を使用して、動的光散乱(DLS)と電気泳動光散乱(ELS)によってそれぞれ決定されました[29]。測定サイクルは、計測器システムによって自動的に決定されました。粒子サイズは強度分布によって表され、サイズ分布は多分散度指数(PDI)によって評価されました。
カプセル化効率(EE)の決定
品質管理の重要なパラメータであるEEは、リポソームベースのデリバリーシステムの開発において非常に重要です。 EEの決定は、高速遠心分離法に基づいていました。簡単に説明すると、100μlのCur-LPを低速(3000 rpm、5分)で遠心分離して非溶解の遊離クルクミンを沈殿させ、50μlの上清を高速遠心分離(16 krpm、10分)にかけてCur-を分離しました。小さな溶解したクルクミンからのLP。ペレットを500μlのPBSに再懸濁し(つまり、10倍希釈)、その10μlのアリコートを300μlのエタノールとボルテックスおよび30秒間の超音波処理によって混合しました。得られた溶液中のクルクミンの蛍光強度を測定し(励起波長(Ex)、458 nm、発光波長(Em)、548 nm)、 F として表示しました。 e 、すなわち、カプセル化されたクルクミンの蛍光強度。カプセル化された遊離クルクミンを含む別の50μlの新鮮なCur-LPもPBSで10倍に希釈し、10μlの希釈溶液を300μlのエタノールと混合しました。得られた溶液の蛍光強度を測定し、 F として示した。 t 、すなわち、総クルクミンの蛍光強度。したがって、EEは次の式で計算されました:EE = F e / F t 。
走査型電子顕微鏡(SEM)
LPの形態は、走査型電子顕微鏡(SEM、INSPECT F、FEI、オランダ)によって観察されました[30]。簡単に説明すると、LP懸濁液を蒸留水で100倍に希釈し、希釈した懸濁液を1滴きれいなガラスシートに置きました。風乾後、SEMの直前にサンプルを金でコーティングしました。
リポソームの物理的安定性
物理的安定性は、コロイド系の保管と輸送にとって非常に意味のあるパラメーターです。リポソームの物理的安定性はコロイド安定性によって示され、以前の方法[31]に従って調査されました。簡単に説明すると、100μlのLPをチューブに加え、37℃に保ちました。異なる時間間隔で、LPサイズを測定し、初期サイズと比較して、熱力学的安定性を示しました。さらに、さらに300μlのLPをチューブに追加し、37°Cに維持しました。同じ時間間隔で、100μlの上層の液体が収集されました。収集した標本の透過率を550nmで測定し、初期値と比較して、速度論的安定性を示しました。
インビトロリリース
リポソームの放出プロファイルは、リポソームのインビボでの運命および有効性を予測する上で重要な役割を果たす。 Cur-LPからのクルクミンのinvitro放出は、動的透析法を使用して研究されました[32]。簡単に説明すると、各Cur-LP 1 mlを透析バッグ(分子量カットオフ、10 kD)に追加しました。これは、リポソームを保持しながら、放出されたクルクミン分子の透過性を維持するために使用されました。検体を入れた透析バッグを4mlの放出培地(0.1%Tween80を含む0.001M PBS、pH 7.4)に浸し、光を避けて放出試験を行いました(37°C、100 rpm)。一定の時間間隔ごとに、放出培地を収集し、4 mlの新鮮な培地と交換して、沈下状態をシミュレートしました。収集した培地をPBSで5mlに希釈し、エタノールでさらに15倍に希釈しました。得られた溶液中のクルクミンは、蛍光分光光度法(Ex 458 nm、Em 548 nm)によって定量化されました。さらに、クルクミン粉末を上記の放出媒体に溶解し、クルクミン溶液の放出をpH 7.4で実施して、透析バッグがクルクミン分子を保持するかどうかを調査しました。
リポソームクルクミンの化学的安定性
化学的安定性は、薬物代謝、有効性、および毒性を予測するための重要なパラメーターです。 Cur-LPの化学的安定性を50%FBSで調べました。簡単に説明すると、100μlのCur-LPをPBS(pH 7.4)で10倍に希釈し、1mlのFBSと混合しました。標本は、光を避けて水平シェーカーで振とうされました(37°C、100 rpm)。一定の時間間隔で、10μlの検体を収集し、300μlのエタノールと混合した直後に遠心分離(16 krpm、5分)しました。上澄みに残っているクルクミンは上記のように定量化されました。
インビトロ抗がん効果
3つのCur-LPの予備的な抗癌効果は、ヒト肝肝細胞癌HepG2細胞を使用して調査されました。簡単に説明すると、HepG2細胞を96ウェル細胞培養プレートにウェルあたり10,000細胞の密度でプレーティングし、標準条件下(37°C / 5%CO 2 )で培養しました。 )10%FBSを添加したPRIM-1640培地で24時間。続いて、培地を除去し、細胞をPBSで洗浄した。 Cur-LPを無血清培地(4μg/ mlクルクミン)で希釈して細胞に添加した後、37°Cで1日間および3日間連続培養しました。生細胞のOD値はcck-8アッセイで測定しました。ブランク培地で処理された細胞はコントロールとして機能し、細胞生存率(%)はコントロールに対する検体のOD値のパーセンテージでした。
統計
すべてのデータは、平均±sd(標準偏差)として表されます。生徒の t によって分析された2つのグループ間の違い p の場合、検定は統計的に有意であると見なされました。 値は0.05未満でした。
結果と考察
リポソームの特性評価
リポソームの微小環境pHとは、リポソームの内部水性チャンバー内の酸性度を指し(図1)、外部環境のpHとは異なります。この研究では、特に明記しない限り、すべてのリポソーム懸濁液の外部環境pHは7.4でした。
粒子サイズ、ゼータ電位、およびカプセル化効率(EE)は、リポソームの品質管理のための重要なパラメーターです。 3つのCur-LPのサイズは互いに類似していました(約300 nm、図2a)。各製剤のPDIは0.2未満であり、サイズ分布が狭いことを示しています。興味深いことに、Cur-LP-7.4の負のゼータ電位(-9 mV)は、他の2つのCur-LPの負のゼータ電位(〜-18 mV)よりも大幅に低くなっています。通常、H + の増加により、分散相のpHが低下すると、負のゼータ電位が低下し、正の値に変換されます。 集中。 pH 2.5、5.0、および7.4の非バッファーHCl / NaOH溶液でCur-LPを調製したときに、この現象が実際に観察されました(図2b)。ただし、PBSの場合、PO 4 の存在 3- 、HPO 4 2- 、および/またはH 2 PO 4 − また、LPとの相互作用により、より複雑な状況や異なる結果が生じる可能性があります。ゼータ電位がナノスケール懸濁液のコロイド安定性を維持する上で重要な役割を果たすことはよく知られています。一般に、ゼータ電位の絶対値が高いほど、コロイド懸濁液システムがより安定します。
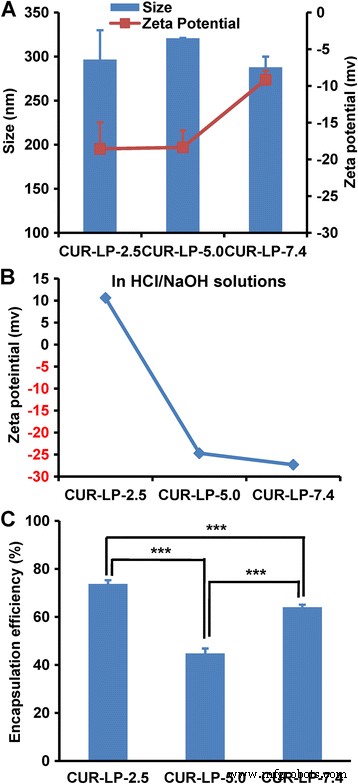
リポソームの物理化学的特性。 a それぞれpH2.5、5.0、7.4のPBSで製造されたCur-LPの流体力学的サイズとゼータ電位。 b それぞれpH2.5、5.0、7.4のHCl / NaOH溶液で製造されたCur-LPのゼータ電位。 c PBSで調製したCur-LPのカプセル化効率。データは平均±sd( n =3)。グループ間の統計的有意性:*** p <0.001
EEはリポソームの開発中に懸念されます。通常、EEを増やすことは、コストを削減し、有効性を高めるために重要です。この作業では、Cur-LP-2.5のEEは74%(図2c)であり、Cur-LP-5.0(45%)とCur-LP-7.4(64%)の中で最も高く、Cur-LP-2.5を示しています。 LP-2.5は、EEの観点からクルクミンを送達するための最良の製剤です。異なるpH値でのEEの多様性の理由はあまり明確ではありませんが、アルカリまたは極度に酸性の溶媒に可溶なクルクミンの溶解度に関連している可能性があります[33]。
SEMで調べたリポソームの形態を図3に示します。LP-2.5(図3a)とLP-5.0(図3b)の粒子は球形で、粒子分布が均一です。 LP-7.4も球のような形状を示しますが、粒子間の付着がはっきりと観察でき(図3c)、SEM試料調製中の乾燥プロセスがLP-7.4の凝集につながることを示しています。これは、LP-7.4のゼータ電位の絶対値が比較的低いことが原因である可能性があります(図2a)。さらに、SEMで測定された粒子サイズは、DLSで測定された流体力学的サイズよりも小さくなります。これは、SEMの乾燥プロセス後にリポソームの水和シェルが失われるためです。
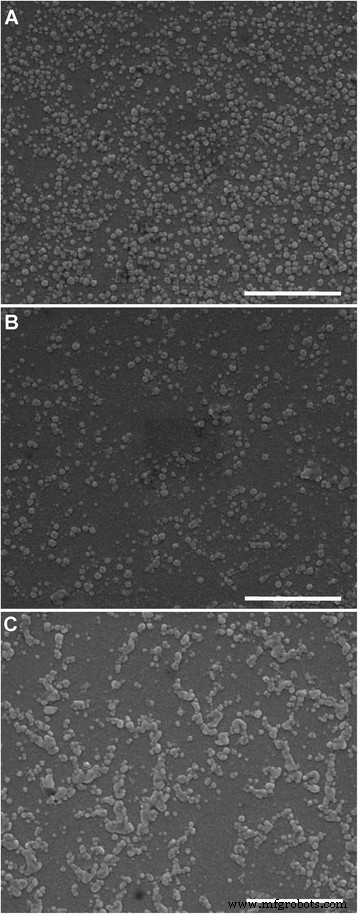
微小環境pHが a のリポソームのSEM画像 2.5、 b 5.0、および c 7.4。 スケールバー 、1μm
リポソームの物理的安定性
リポソームはコロイド系であり、その物理的安定性はコロイド安定性によって示され、リポソームの貯蔵およびさらなる用途に実質的な影響を及ぼします[34、35]。粒子の凝集(熱力学的不安定性)と沈降(速度論的不安定性)は、コロイド不安定性の2つの重要な側面です。凝集は見かけのサイズを大きくし、沈降は懸濁液の透過率の変化をもたらします。さらに重要なことに、粒子サイズは細胞取り込み、細胞毒性、薬物動態プロファイル、および組織分布に大きな影響を与えることが示されているため、サイズの増加はナノシステムの有効性に直接影響を与える可能性があります[36、37]。
ここでは、3つのリポソームシステムの凝集および沈降特性を調べて、それぞれの熱力学的および速度論的安定性を示しました。図4aに示すように、3つのLPは、72時間以内に流体力学的サイズに実質的な変化を示さず、これらすべてのLPが非常に高い熱力学的安定性を持っていることを示しています。一方、3つのLPすべての透過率の変化は10%未満であり(図4b)、粒子の沈降がほとんどなく、したがって高い速度論的安定性を示しています。これらの結果は、3つのLPが72時間以内に優れたコロイド安定性を示し、微小環境のpHがリポソームの物理的安定性に影響を与えないことを示唆しています。
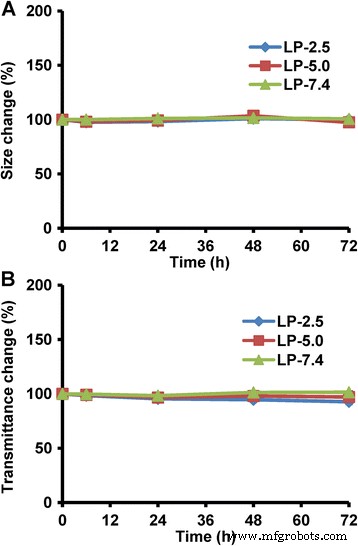
さまざまな微小環境pH値(pH 2.5、5.0、および7.4)でのリポソームの物理的安定性。 a 粒子の凝集を示す熱力学的安定性。 b 粒子の沈降を示す速度論的安定性。データは平均±sd( n )として表されます =3)
インビトロリリース
リポソームからの薬物放出プロファイルは、通常、製剤の品質を評価し、投与計画の参照を提供し、invivoでの有効性を予測するために検査されます。一般に、ほとんどすべてのリポソームシステムは持続的な薬物放出特性を持っています。ここでは、PBS(pH 7.4)中の3つのCur-LPのinvitro放出挙動を調べました。一方、透析膜がクルクミンの拡散に影響を与えるかどうかを確認するために、クルクミン溶液の放出も調べた。図5aに示すように、クルクミンはその溶液から非常に速く放出され(6時間で> 80%)、透析バッグがクルクミンの拡散に影響を与えなかったことを示しています。クルクミン溶液の急速放出とは対照的に、すべてのCur-LPは明らかな徐放性を示し(図5b)、放出プロファイルは互いに非常に類似しており、微小環境のpHがクルクミンに有意な影響を与えなかったことを示していますリリース速度。詳細には、クルクミンは最初の8時間で少し早く放出されましたが、これはおそらく最初のバースト放出によるものです(累積放出率は約5%でした)。 8時間後、クルクミンの放出は少し遅くなり、72時間以内の累積放出率は約30%でした。インビボまたは血清の存在下での放出速度は、部分的に脂質の代謝のために実質的に速いと想定されている。
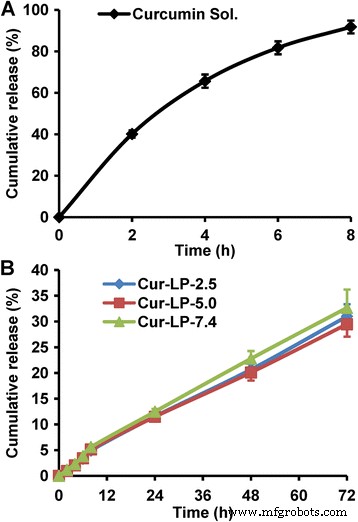
PBS(pH 7.4)中のさまざまなクルクミン製剤のinvitro放出プロファイル。 a 0.1%Tween 80(pH 7.4)を含むPBSにクルクミンを溶解したクルクミン溶液。 b それぞれ2.5、5.0、および7.4のさまざまな微小環境pHを持つCur-LP。データは平均±sd( n )として表されます =3)
興味深いことに、3つのCur-LPすべてのリリースプロファイルは直線に近いです。したがって、3つのリリースプロファイルへの線形フィッティングが実行されました。表1に示すように、これらのプロファイルはすべて、0.99を超える適合度で非常に良好な直線性を示し(回帰式も表示されています)、ゼロ次反応速度に適合したCur-LPの放出を示唆しています。他の同様の研究では、リポソームからのクルクミンの放出は非線形であることがわかりました[38、39]。薬物の研究開発の観点から、ゼロ次放出動態は、一定の薬物放出速度を提供し、したがって治療効果を長期間維持し、投与時間を短縮し、副作用を低減することができるため、最も理想的な放出プロファイルです。 。したがって、この研究で調製されたLPは、制御されたドラッグデリバリーのための有望な担体である可能性があります。
<図>Cur-LPの化学的安定性に対する微小環境pHの影響
FBSにおけるリポソームクルクミンの化学的安定性を図6に示します。2時間のインキュベーション後、Cur-LP-2.5では89%のクルクミンが残り、Cur-LP-5.0では74%、Cur-LPでは61%を大幅に上回りました。 -7.4( p <0.001)。インキュベーションの4時間後、Cur-LP-2.5では69%のクルクミンが残り、Cur-LP-5.0では53%、Cur-LP-7.4では40%を大幅に上回りました( p <0.01)。インキュベーション後6時間で、55%のクルクミンがCur-LP-2.5で残っていましたが、Cur-LP-5.0では43%、Cur-LP-7.4では34%を大幅に上回っています( p <0.05)。 Cur-LPの化学的安定性が微小環境のpHに依存することは明らかです:Cur-LP-2.5> Cur-LP-5.0> Cur-LP-7.4。 Cur-LPのこのpH依存性の化学的安定性は、遊離クルクミンのpH依存性の安定性を示した別の研究と一致しています[26]。 in vitro放出は無血清培地で行われ、累積放出は72時間で30%になる可能性があります。しかし、化学的安定性の研究は、血清酵素が放出されたクルクミンを分解し、リポソームを破壊して未放出のクルクミンを分解する可能性がある血清含有溶液で実施されました。これが、in vitro放出試験では72時間で30%のクルクミンが放出されたが、血清安定性試験ではCur-LP-2.5では55%しか6時間で放出されなかった理由です。
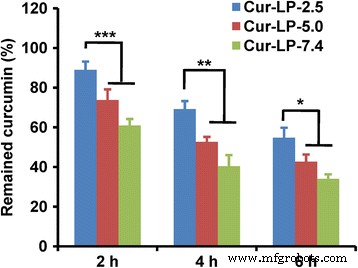
さまざまな微小環境pH値(pH 2.5、5.0、および7.4)でのリポソームクルクミン(Cur-LP)の化学的安定性。安定性は、Cur-LPを50%FBSとインキュベートした後に残ったクルクミンを定量化することによって調べられました。データは平均±sd( n )として表されます =3)。グループ間の統計的有意性:*** p <0.001、** p <0.01、* p <0.05
リポソームは構造の2つの部分で構成されています。1つは疎水性脂質二重層で、もう1つは親水性の内部水性チャンバーです。 pH感受性の親水性薬物が内部の水性チャンバーに配置され、その安定性は、緩衝容量と緩衝能力がはるかに高い水性チャンバー内の微小環境のpHによって大きく影響されることは容易に理解できます。脂質二重層のそれより。対照的に、クルクミンは疎水性分子であり、脂質二重層に位置します。このため、リポソームクルクミンの微小環境のpH依存性の化学的安定性を見つけることは非常に興味深いことです。脂質二重層の空間は疎水性ですが、完全に無水ではないと考えられます。私たちが知っているように、生細胞膜はその脂質二重層で完全に無水ではありません。代わりに、水溶性分子やイオンを輸送するための少量の水溶液が含まれています。同様に、リポソームの調製が成功した後、内部チャンバーと同じ成分を有する特定の少量の緩衝液も疎水性脂質二重層に存在するであろう。したがって、脂質二重層に位置する疎水性薬物は、リポソームの微小環境pHによって直接影響を受ける可能性があります。さらに、酸性の微小環境は、通常の生理学的状態で最高の活性を示すいくつかの酵素の活性を低下させる可能性があります。これはまた、より低い微小環境pHでのリポソームクルクミンのより高い化学的安定性に貢献します。卵ホスファチジルコリン(EPC)で構成されるリポソームは、バッファー(pH 7.4)で内部pH勾配を急速に失い、pH勾配維持能力はEPC(相転移温度( T m )≈-5°C) T が高い m (41°C)脂質DPPC(ジパルミトイルホスファチジルコリン)およびコレステロールの添加による[40]。この現在の研究では、リポソームは大豆レシチン( T )で構成されています m 約238.2°C [41])とコレステロールです。したがって、この研究で調製されたリポソームの微小環境pH勾配は、長期間維持することが期待できます。これは、上記の結果と仮定を強力にサポートしています。
インビトロ抗がん効果
上記のリポソームクルクミンの微小環境のpH依存性化学的安定性を示しました。ここでは、これらのリポソームクルクミンの抗がん効果を調査するための予備的なinvitro研究を実施しました。興味深いことに、ブランクLPは、コントロールグループと比較して、1日目で細胞増殖を促進し、3日目までこの機能をある程度維持することができました(図7)。これは、ブランクLPが細胞に栄養を提供する可能性があることを示しており、これは以前の報告[27]と一致しています。遊離クルクミンは、溶解度が非常に限られているため、抗がん効果はほとんどありませんでした。対照的に、Cur-LPは、微小環境のpH依存的に有意な抗癌効果を示しました。 1日間の処理後、Cur-LP-2.5およびCur-LP-5.0は、Cur-LP-7.4よりもHepG2細胞の増殖を阻害する有意に強い能力を示しました(Cur-LP-2.5およびCur-LPの細胞生存率は80%でした)。 -5.0、Cur-LP-7.4の場合は90%)。治療後3日目に、細胞生存率は大幅に低下し、Cur-LP-2.5およびCur-LP-5.0は同等の抗癌効果を示し、Cur-LP-7.4よりも有意に高かった。 Cur-LP-2.5( p )の細胞生存率は24%でした <0.05 vs Cur-LP-7.4)、Cur-LP-5.0では21%( p <0.01 vs Cur-LP-7.4)、Cur-LP-7.4では39%。これらの結果は、リポソームクルクミンの抗癌効果が微小環境のpHおよび時間に依存することを示しています。 Cur-LP-5.0よりもCur-LP-2.5のEEと化学的安定性が高いことを考慮すると、微小環境pHが2.5のリポソームは実用化の可能性が最も高いでしょう。
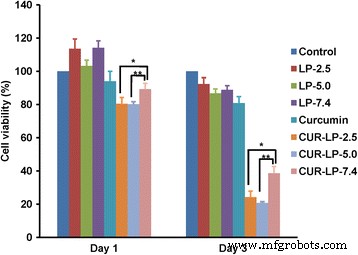
さまざまな微小環境pH(2.5、5.0、および7.4)でのリポソームクルクミンの抗がん効果。ブランクLP、遊離クルクミン、およびCur-LPによる処理後1日目および3日目のHepG2細胞の生存率を、cck-8アッセイで調べました。血清を含むブランク培地で処理された細胞は、コントロールとして機能しました。データは平均±sd( n )として表されます =3)。グループ間の統計的有意性:** p <0.01、* p <0.05
結論
広く使用されている薬物送達システムとしてのリポソームは、水不溶性薬物の溶解性を改善し、薬物ペイロードを過酷な生理学的環境から保護し、標的組織にペイロードを送達することができる。ただし、pH感受性薬物の送達は、生理学的条件(中性環境)での自然な不安定性によって依然として制限されています。この現在の作業では、リポソームの微小環境の酸性度を調節することにより、pH感受性薬物ペイロードの化学的安定性を高めるための新しいアプローチを提案します。調査結果は、モデルpH感受性薬物クルクミンの化学的安定性とin vitro有効性が、リポソームの微小環境を酸性化することによって大幅に強化されることを示しています。結論として、リポソームの微小環境pHの調節は、脂質二重層にある疎水性薬物の場合でも、pH感受性薬物ペイロードの化学的安定性を高めるために実行可能です。
ナノマテリアル



