ナノ結晶ストロンチウムフェライトの構造、微細構造、および磁気特性に及ぼすゾル-ゲル修飾のpH調整パラメータの影響
要約
ナノ結晶ストロンチウムフェライト(SrFe 12 O 19 )ゾルゲル法は、その修飾パラメータに敏感です。したがって、この研究では、SrFe 12 の調製中にゾル-ゲル修飾パラメーターとしてpHを調整する試みが行われました。 O 19 900°Cの低い焼結温度で焼結されたナノ粒子が紹介されています。 SrFe 12 の構造、微細構造、および磁気的挙動に対するさまざまなpH(pH 0〜8)の関係 O 19 ナノ粒子は、X線回折(XRD)、電界放出型走査顕微鏡(FESEM)、および振動試料型磁力計(VSM)によって特徴づけられました。前駆体のpHを変化させると、SrFe 12 の焼結密度、結晶構造、および磁気特性に強い影響が見られました。 O 19 ナノ粒子。 pHが0なので、SrFe 12 O 19 比較的最大の密度、飽和磁化、 M を生成しました s 、および保磁力、 H c 、900°Cの低い焼結温度で。 SrFe 12 の粒径 O 19 73.6〜133.3nmの範囲で取得されます。サンプルの多孔性は、SrFe 12 の密度と磁気特性に影響を与えました。 O 19 フェライト。低温焼結SrFe 12 O 19 pH0で M が表示されました s 44.19 emu / gおよび H c 6403.6 Oeの、低温同時焼成セラミック永久磁石に適用するための大きな可能性を持っています。
ハイライト
-
ストロンチウムフェライト(SrFe 12 O 19 )ゾルゲル自動燃焼技術を使用したナノ粒子。
-
SrFe 12 O 19 ナノフェライト相は、900°Cの低い焼結温度で得られました。
-
飽和磁化の磁気パラメータ M s 、残りの M r 、および保磁力 H c pHが上がると減少します。
背景
ストロンチウムフェライト(SrFe 12 O 19 )は、マイクロ波デバイス、高密度磁気記録、電子デバイス、および永久磁石での潜在的なアプリケーションについて広く研究されてきました。永久磁石フェライトは、そのいくつかの利点[1]と、高い電気抵抗率[2]、大きなヒステリシス損失、高い固有保磁力[3]などの優れた特性により、電気製造業界で広く使用されています。優れた耐熱性と耐食性として最もよく知られており、多くの用途に役立ちます。ストロンチウムフェライトは、結晶構造の高い保磁力の原因となる高い磁気異方性により、近年、より多くの科学的研究を引き付けており[4、5]、粒子のサイズをナノスケールに縮小した場合でも高い保磁力を確保できます。シングルドメイン構造。 SrFe 12 が示す強磁性 O 19 Fe 3+ に起因します 構造内に存在するイオン副格子。それらは3つの八面体(12 k、2a、4f 2 )、1つの四面体(4f 1 )、および1つの両錐型サイト(2b)。これらのサイトから、12 k、2a、および2bは高スピン状態および4f 1 として表されます。 および4f 2 低スピン状態と見なされます[6、7]。 Fe 3+ の磁気モーメント イオンは、O 2- によって媒介される超交換相互作用によって互いに結合されます。 イオン。 Sr 2+ イオンは、結晶格子の摂動を引き起こすため、大きな磁気一軸異方性の原因となります[8]。ストロンチウムヘキサフェライト(SrFe 12 O 19 )ナノ粒子の平均粒子サイズは0.1μm未満で、均一な粒子サイズ分布でできています[9]。粒子サイズが小さいほど表面積が大きくなり、SrFe 12 が大幅に向上します。 O 19 化学的、物理的、機械的、磁気的特性などのナノ粒子の特性により、ナノフェライト用途に興味深い特性がもたらされます。
従来のセラミック固体法では、ナノ粒子やモノサイズの粒子を得るのは困難です[4、5]。約1300°Cの高い焼結温度での長い加熱スケジュール、得られる粒子/粒子サイズの増加、時間の消費の増加などの制限があります。フェライトナノ粒子の製造に関係する実験条件は、フェライトナノ粒子の粒子サイズだけでなく、得られる特性にも重要な役割を果たします。均質性の高いSrFe 12 を実現するため O 19 低い焼結または焼成温度での単一ドメイン構造からなるナノ粒子は、焼結中に促進される異常な粒子成長を伴う広い粒子サイズ分布を回避できるように、さまざまな方法が導入されてきた。この方法には、共沈法[9、10]、塩溶解法[11]、熱水[12、13]、マイクロエマルジョン[14]、およびゾルゲル法[1、4、15]が含まれます。これらの方法の中で、ゾルゲル法は、化学量論を制御し、ナノ結晶フェライトを生成するための、低コストでシンプルで信頼性の高い方法です。ゾルゲルプロセスは、焼成温度を下げ、結晶子サイズを小さくすることができる均一な混合酸化物を生成します[3]。単相サンプル、超微粒子、およびより低い焼成温度を生成するには、FeとSrのモル比(Fe / Sr)を最適化することが非常に重要です[1]。この比率は、出発原料の変更や製造方法の変更によって異なります[1]。高い焼成温度では、粒子サイズと交換相互作用の両方が増加します。これらは、高品質の永久磁石を得るのに不利になります[16]。一般に、金属アルコキシドはゾルゲル法の原料として使用されることが多いですが、大気中の水分に対する感度が高いため、多くのアルコキシドの入手や取り扱いは非常に困難です。さらに、多成分セラミックを調製する場合、アルコキシドの加水分解速度を制御することは容易ではありません。金属塩は非常に有用で、安価で、取り扱いが簡単なため、この研究で使用されています。さらに、金属塩は多くの種類の有機溶媒に溶解することができるため、金属イオンを有機配位子でキレート化することによって金属錯体を形成します[17]。 pH調整[1、18]、塩基性剤[3]、界面活性剤[1]、カルボン酸[2]、出発金属塩[3]など、いくつかのゾルゲル修飾プロセスが報告されています。 SrFe 12 の最終的な焼成温度、結晶子サイズ[2]、および高い異方性 O 19 ナノ粒子[12]。ゾルゲル法では、水酸化物および/または酸化物を形成する能力は、溶液のpHおよび金属カチオンの荷電/半径比に強く依存します[17]。さらに、ゾルのpHはH + の量を制御します またはOH − 金属-酸素結合の重合を効果的に決定するゾル中のイオン。また、ゾルゲルプロセス中、クエン酸との錯化プロセスはpH値に敏感であることが知られています[19、20]。したがって、相形成に不可欠なゾルの均一性は、溶液のpHによって決定されます。 SrFe 12 の磁気特性はよく知られています O 19 合成パラメータを変更することにより、その形態、粒子/粒子サイズ、形状、配向、およびドメイン構成に強く依存します。したがって、この作業では、ゾルゲル法の変更パラメータとして溶液のpHを調整し、より低い焼成温度でかなりの値の磁気特性を持つナノ結晶フェライトを生成する予定です。
メソッド
この研究の実験シーケンスは、ゾルゲル法によるストロンチウムフェライトナノ粒子の合成(「ストロンチウムフェライトナノ粒子の合成」セクション)と、それに続く構造、微細構造、および磁気特性の特性評価という2つの主要な段階で構成されていました。調製したストロンチウムフェライトの分析(「ストロンチウムフェライトの特性評価」セクション)
ストロンチウムフェライトナノ粒子の合成
ストロンチウムフェライトナノ粒子は、ゾルゲル法によって合成されています。この方法では、硝酸ストロンチウム無水粒状Sr(NO 3 ) 2 (98%、Alfa Aeser)、硝酸鉄(III)Fe(NO 3 ) 3 (99%、HmbG)、クエン酸C 3 H 4 (OH)(COOH) 3 (99%、Alfa Aeser)、アンモニアNH 4 サンプル調製の出発物質として、OH(25%、SYSTERM)と脱イオン水を使用しました。適切な量のSr(NO 3 ) 2 およびFe(NO 3 ) 3 を100mlの脱イオン水に60°Cで数分間溶解し、250rpmの一定の攪拌機で回転させて水溶液を作成します。クエン酸と硝酸塩のモル比(C / N =0.75)のキレート剤としてクエン酸を添加し、温度を80°Cに上げました。混合物を連続的に攪拌し、NH 4 pHをpH0からpH8に変化させるために、OHを添加しました。pHは、HI2211 pH / ORPメーター(HANNA機器)で測定しました。溶液を継続的に攪拌し、90°Cで数時間加熱すると、溶液はゆっくりと緑色の粘着性のあるゲルに変わりました。緻密な粘着性のあるゲルが形成されたら、ホットプレートの温度を200°Cまで上げ、脱水プロセスのためにゲルを1時間燃焼させます。得られた粉末を900℃で6時間、5℃/分の加熱速度で煆焼した。 SrFe 12 の合成手順の段階的な説明 O 19 ナノ粒子を図1に示します。
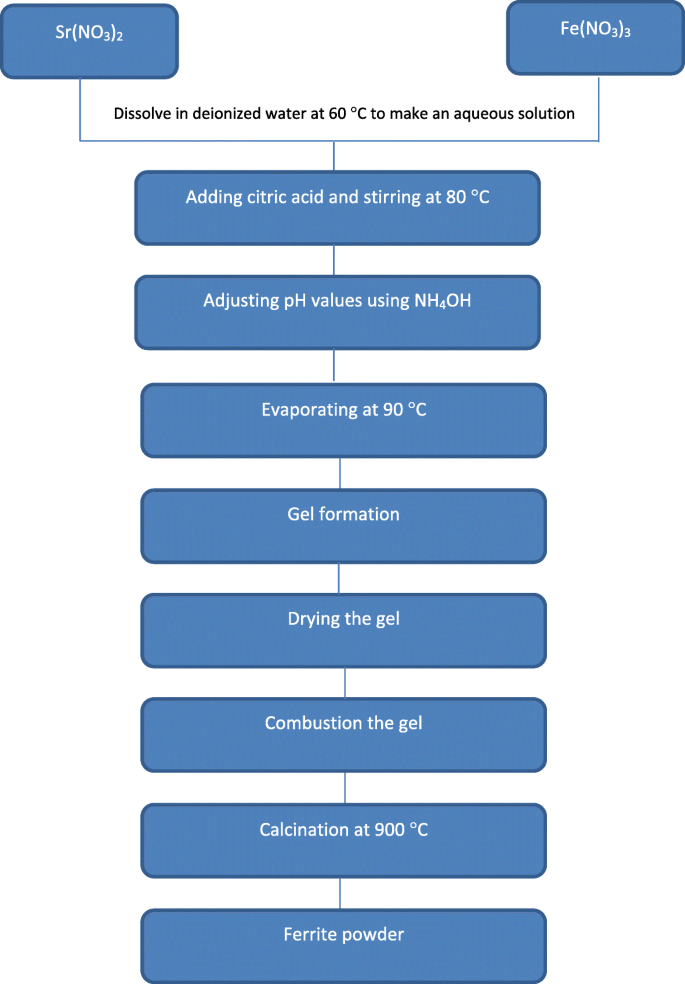
SrFe 12 を準備するためのフローチャート O 19 ゾルゲル法によるナノ粒子粉末
ストロンチウムフェライトの特性評価
ストロンチウムフェライトの特性測定は、その構造、微細構造、および磁気特性の観点から実施されています。詳細な説明は、次のサブセクションに示されています。
構造プロパティ
サンプルの構造特性は、フィリップスX’pertX線回折計モデル7602EAアルメロと1.5418ÅのCuKα放射線を使用したX線回折(XRD)技術によって特性評価されました。使用する回折角の範囲は、室温で20°から80°です。加速電流と動作電圧はそれぞれ35mAと4.0kVでした。 X’Pert High ScorePlusソフトウェアを使用してデータを分析しました。
フーリエ変換赤外(FTIR)の特性評価は、サンプルの吸収および発光バンドの赤外スペクトルを決定するために、パーキンエルマーフーリエ変換赤外分光計モデル1650によって実行されました。 280〜4000 cm -1 の赤外線スペクトル間で実行されました 。
微細構造のプロパティ
微細構造の観察は、FEI Nova NanoSEM 230マシンを使用して電界放出型走査電子顕微鏡(FESEM)によって実行されました。粒子サイズ画像の分布は、5.0kVの加速電圧で100kxの倍率で固定されました。粒子サイズの分布は、サンプルの200の異なる粒子画像を取得し、imageJソフトウェアを使用して個々の粒子の平均直径を推定することによって得られました。粒度分布は、平均線形切片法によって測定されました。
密度
密度は、ヒルデブランド濃度計モデルH-300 Sを使用して測定しました。焼結ペレットの密度は、流体媒体として水を使用したアルキメデスの原理を使用して、式(1)によって得られました。 1、
$$ {\ rho} _ {\ mathrm {exp}} =\ left(\ frac {W _ {\ mathrm {air}}-{W} _ {\ mathrm {water}}} {W _ {\ mathrm {water} }} \ right)\ times {\ rho} _w $$(1)ρ exp 測定されたサンプルの密度、ρ w は水の密度、 W 空気 は空気中のサンプルの重量であり、 W 水 は水中でのサンプルの重量です。
磁気特性
サンプルの磁気特性は、振動試料型磁力計(VSM)モデル7404LakeShoreによって測定されました。測定は室温で行った。 12kOeの外部フィールドがサンプルと平行に適用されました。
結果と考察
構造解析
図2は、SrFe 12 のX線回折(XRD)スペクトルを示しています。 O 19 pHを変えることによるナノ結晶。 XRDピークの構造は、標準のSrFe 12 を参照しました。 O 19 JCPDS参照コードは98-004-3603です。 SrFe 12 の特徴的なピークとミラー指数 O 19 図にも示されています。最高強度は2θ(34.218°)で観察でき、ミラー指数は[1 14]です。単相SrFe 12 の形成 O 19 900°Cの比較的低い煆焼温度で得られました。微量のヘマタイトFe 2 がpH 8で調製されたサンプルを除いて、試薬前駆体または他の二次相と中間生成物の一部に対応するピークは観察されませんでした。 O 3 相が検出され、図に示すように、すべてのサンプルの結晶化度が良好です。二次Fe 2 の形成 O 3 pH 8で調製されたサンプルで観察された相により、SrFe 12 の純度が低下しました。 O 19 87.8%に。 Fe 2 O 3 パターンは、98-004-1067のICSD参照コードにインデックス付けされました。 Fe 2 の存在 O 3 相は、pH8で調製されたサンプルの不十分な煆焼温度によるものです[21]。 pH 0から3までの中溶液での高い酸性度は、高い結晶化度のSrFe 12 の形成に有利であることがわかりました。 O 19 段階。ゾルのpHの上昇は、負に帯電した鉄ゲルの形成と、鉄ゲルへの正に帯電したSrイオンの吸着を助けました。その結果、より均質な溶液が得られ、SrFe 12 が容易に形成されます。 O 19 フェーズ[3] 。 SrFe 12 の形成にもかかわらず O 19 pHを上げると容易になり、重合中の複合体のすぐ近くに局所的なシフトがあるため、不均一なセラミック凝集体が形成される可能性があります[22]。したがって、結晶成長が阻害され、pH4以降の結晶化度が低下する可能性があります。これは、SrFe 12 の結晶化度の改善によるXRDピーク強度の増加によって示されました。 O 19 pH1からpH3を使用して調製しましたが、pH値を4から8に上げるとゆっくりと減少しました。結晶性SrFe 12 O 19 900°Cで煆焼した後は、組成の均一性が高いことと、硝酸塩とクエン酸の発熱反応から発生する熱が大きいことが原因です[21]。
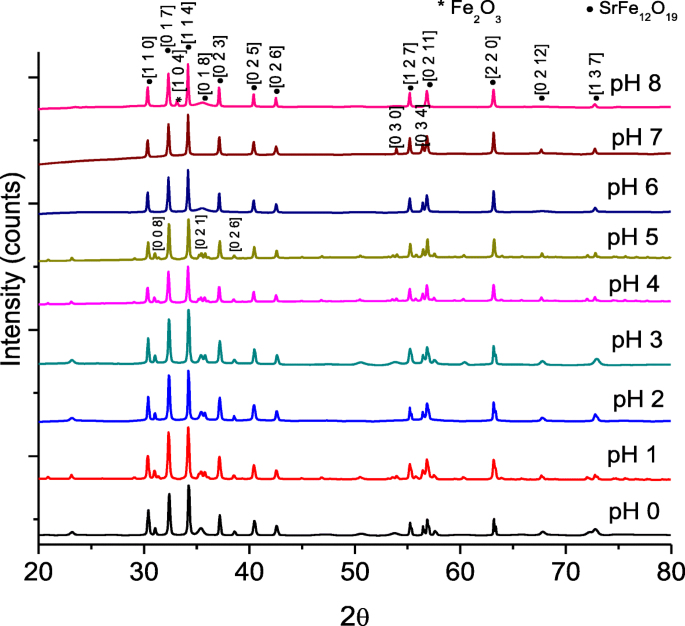
SrFe 12 のX線回折スペクトル O 19 pH0からpH8の場合、900°Cで焼結
格子定数 a および c 観測された値は、理論上のSrFe 12 と比べてそれほど違いはありませんでした。 O 19 a の格子定数 =5.8820Åおよび c =23.0230Å[23](図3)。 a および c 観察されたパラメータは、Masoudpanah etal。のパラメータと類似しています。 [3]およびDangetal。 [12]。ボリュームセル V セル XRDの密度ρ xrd この研究で使用されるのは、 P63 / mmc の空間群を持つ六角形の結晶系を持つ結晶学的パラメーターに依存します。 。 V セル 式を使用して計算されました。 (2);
$$ {V} _ {\ mathrm {cell}} =\ frac {\ sqrt {3}} {2} {a} ^ 2c $$(2)ここで a および c は格子定数です。理論密度ρ 理論 サンプルの量は、式(1)を使用して計算されました。 (3)、
$$ {\ rho} _ {\ mathrm {theory}} =\ frac {2M} {N_AV} $$(3)ここで M はSrFe 12 の分子量です O 19 これは1061.765gに相当します。 1つのユニットセル内の2つの分子の重量は2×1061.765 =2123.53gです。 N A アボガドロの数(6.022×10 23 mol -1 。
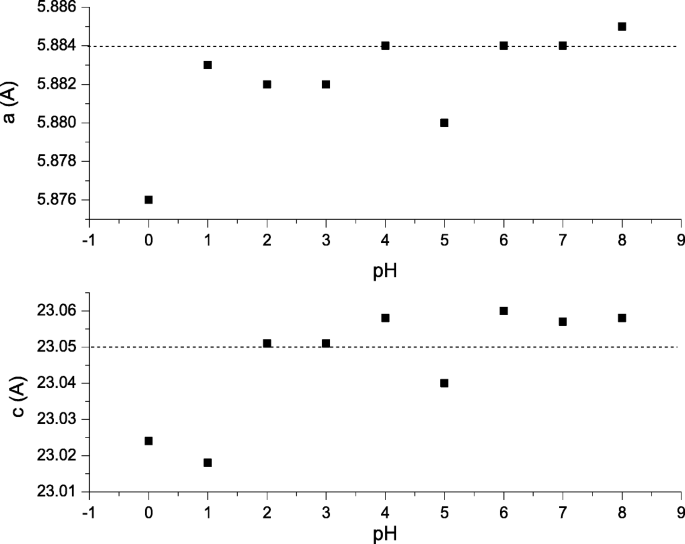
格子定数 a および c SrFe 12 の O 19 pH0からpH8のナノ粒子、900°Cで焼結。破線は、格子定数 a の参照値です。 および c
気孔率 P サンプルの数は、式(1)を使用して計算できます。 (4);
$$ P =\ left(\ frac {1-{\ rho} _ {\ mathrm {exp}}} {\ rho _ {\ mathrm {theory}}} \ right)\ times 100 \%$$(4)pH値が増加するにつれて、サンプルの実験密度ρ exp 実験密度の最適値でpH4、6、および7で調製されたサンプルで観察されたいくつかの変動を除いて減少し、pH4で調製されたサンプルで得られた気孔率は少なくなりました。最適密度と気孔率は4.693g / cm として記録されました。 3 それぞれ8.15%(図4、表1)。表1に示されているX線密度は、焼結プロセス中に作成された細孔の存在が原因である可能性がある実験密度よりも高くなっています。凝集体の多孔性の特徴は、NH 3 などの大量のガスの放出にも起因します。 燃焼プロセス中[24]。
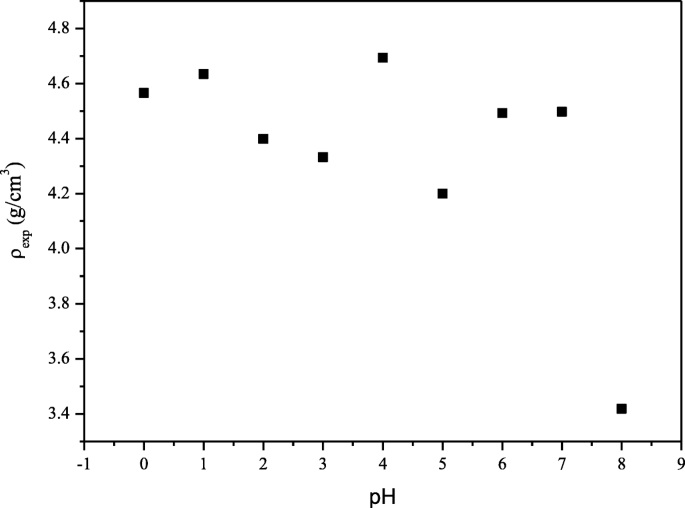
SrFe 12 の実験密度 O 19 pH0からpH8のナノ粒子、900°Cで焼結
焼結SrFe 12 のFTIRスペクトル O 19 pH0からpH8までのさまざまなpHでの様子を図5に示します。前駆体のFTIRスペクトルは、430、583、904、および1446 cm -1 の範囲で顕著に現れました。 IR特性バンドの。 436 cm -1 の吸収帯 CH 2 の伸縮バンドとして示されました 、CH飽和化合物の存在を証明します[25]。 583 cm ‑1 のバンド 特徴的な金属酸素振動Sr–O Fe–Oを示します[20]。 443〜600 cm -1 の範囲の吸収帯 金属-酸素結合の伸縮振動としてのストロンチウムフェライトの形成に起因するとされた[26、27、28、29]。これにより、SrFe 12 O 19 900°Cの焼結温度で形成されました。ピーク904cm -1 の比較的強くて広いバンド NH 3 の分解によるN–H振動のアミン官能基があることを明らかにしました 。一方、ペレイラ等。 [29]はまた、Sr–O伸縮の幅広い振動は、ストロンチウムナノフェライトの形成を示していると述べています。 1446 cm -1 の吸収帯 酸化物バンドによる金属の分解によるFe–O–Feバンドの振動バンドを示します[25]。
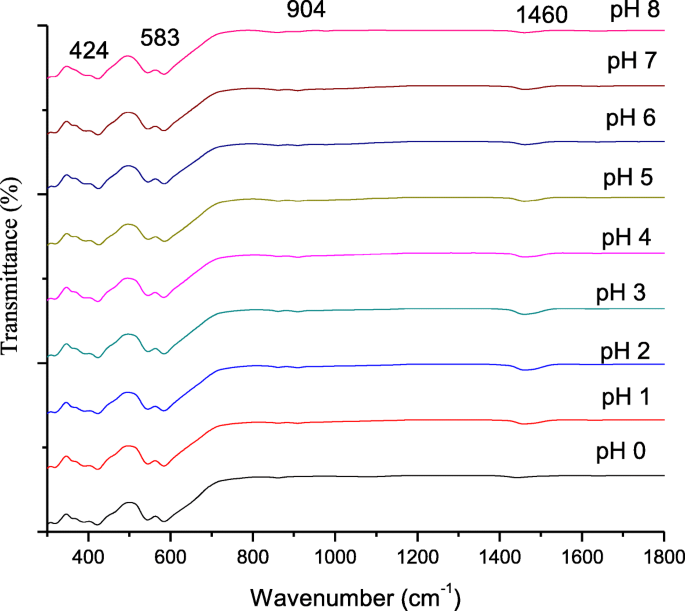
SrFe 12 のFTIRスペクトル O 19 pH0からpH8の場合、900°Cで焼結
微細構造分析
バルクSrFe 12 の微細構造画像 O 19 とEDXスペクトルを図6に示し、サンプルの粒子サイズ分布を図7に示します。平均粒子サイズは73.6〜133.3nmの範囲で見つかりました。サンプルの平均粒子サイズは、pH4およびpH8のサンプルを除いて、大きな変動を示していません。粒子サイズは、pH値の増加に伴って凝集しました。 pH 0では、平均73.6 nmの比較的小さく、充填された粒度分布が観察されました。粒度は、pH値がpH0からpH3に増加するにつれて増加し、pH 4で減少し、さらに増加するまで増加しました。 pH8。結果は、図2に示すXRDスペクトルと一致しており、pH 4のサンプルでは結晶化度が低下しています。図6eから、pH 4で調製したサンプルでは、粒子が均一ではないことがわかります。分散していて均一に形成されていません。

pHを変化させて900°Cで焼結したサンプルのFESEM顕微鏡写真: a pH 0、 b pH 1、 c pH 2、 d pH 3、 e pH 4、 f pH 5、 g pH 6、 h pH 7、および i pH 8
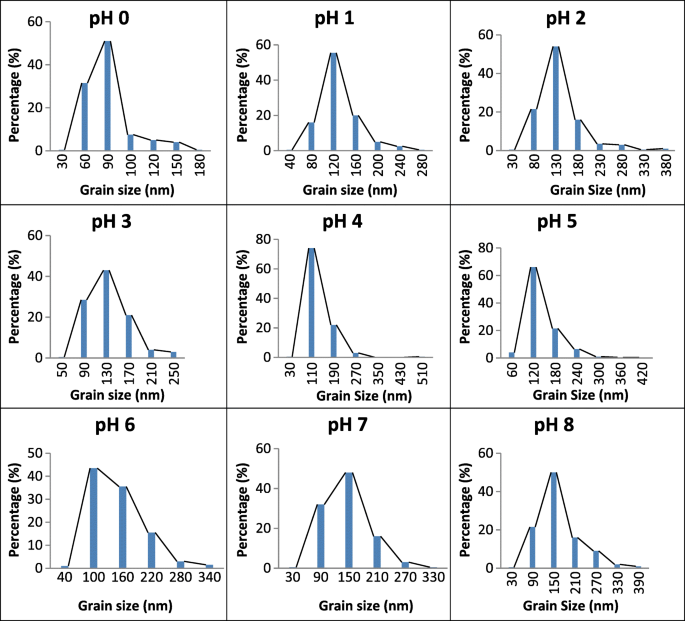
SrFe 12 の粒度分布 O 19 pHを変えて900°Cで煆焼: a pH 0、 b pH 1、 c pH 2、 d pH 3、 e pH 4、 f pH 5、 g pH 6、 h pH 7、および i pH 8
最高の粒径は最高の M を示しました s 、 M r 、および H c 。 pH 0のサンプルの粒子は球形であり、別の粒子と接触してネッキング構造を形成していました。接触はpH値の増加とともに明白であり、したがってより細長い粒子構造を示した。 pH値が高くなるにつれて、粒子サイズ/形状の分布は大きくなり、不均一になりました。粒度分布のヒストグラムは、小さい粒度から大きい粒度を示すようにシフトしました。燃焼速度と反応から放出される熱の増加は、結晶子サイズも増加させる可能性があります[30]。ヒストグラムの赤い点線(図7)は、サンプルの平均粒径を示しています。微細構造は、バルクSrFe 12 の調製中にポリビニルアルコールが存在するため、一部のサンプルが大きな多孔性を示したことを示しました。 O 19 ペレット状のナノフェライト、およびサンプル準備中のガスの放出。
磁気的振る舞い
M の開発 – H さまざまなpHでのヒステリシスループを図8に示します。この変化のさらなる確認は、飽和磁化の変化 M から見ることができます。 s 、残留磁気、 M r 、直角度比、 M r / M s 、および保磁力、 H c 、表1に示すpHの関数として。単位質量あたりの磁化は、サンプルの微細構造に直接関係していません。したがって、単位体積あたりの磁化は、単位質量あたりの磁化に実験密度ρを掛けて計算されています。 exp 。 M s 、 M r 、および H c ゾルゲル前駆体にアンモニアを添加することにより、pHの上昇とともに一般的に減少することがわかっています。 pHが上昇するにつれて磁気パラメータが減少するのは、アンモニアNH 3 の反磁性相が大量に存在するためである可能性があります。 。反磁性NH 3 の主な効果は Sr-フェライトナノ粒子を互いに分離することで、それらの間の交換相互作用を低減し、 M に悪影響を与えることが知られています。 s および M r 。 「微細構造分析」のセクションで前述したように、SrFe 12 の微細構造 O 19 pH値を上げることによって影響を受けました。これは、Yangらによって報告された調査結果と一致しています。 [31]、ここで粒子はpHが5から11に増加するにつれて大きくなりました[32]。大きい粒子は粒子内のFeの磁性原子間の強い磁気相互作用の影響を強く受けました[33]。
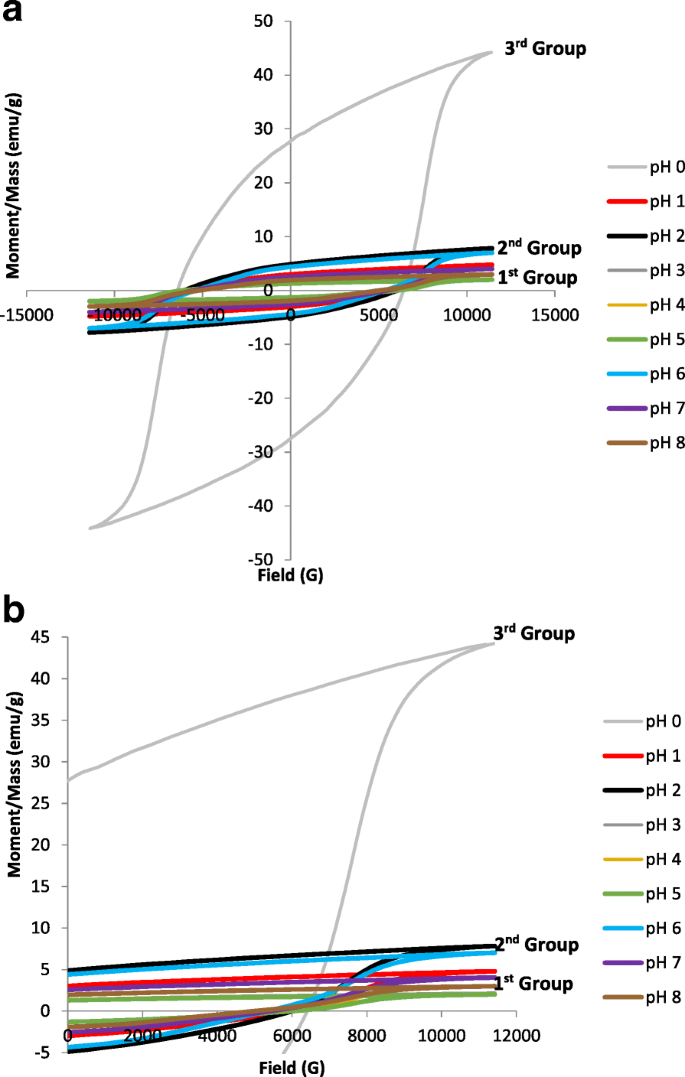
M – H SrFe 12 のヒステリシスループ O 19 a の場合 pH0からpH8および b クローズアップグラフ、900°Cで焼結したさまざまなpH
M – H 図8のヒステリシスループが精査され、微分されたグループの形状と値によって特徴付けられるヒステリシスループの3つの重要なグループが観察されました。最初のグループは、pH 1、3、4、5、7、および8を使用して調製されたサンプルである調製サンプルの大部分で構成されていました。このグループは、 M の値が低い弱い強磁性特性に対応していました。 s および M r 。 M s 特にサンプルの結晶化度に依存します。これは、pH 4、5、7、および8を使用して調製されたサンプルで見られ、サンプルの結晶化度が低下したため、 M の値が低くなりました。 s 。さらに、28.2%のα-Fe 2 O 3 pH 8を使用して調製したサンプルで、二次相としての不純物が検出され、サンプルの結晶化度が低下し、その結果、 M が低下しました。 s 価値。図2で観察されたXRDスペクトルは、pH 3を使用して調製されたサンプルで高度の結晶化度を示しましたが、結果として得られる低い磁気特性値は、細孔の存在により密度が低下し(表1を参照)、影響を与える可能性があります。サンプルの保磁力。 M 以降 s H に関連しています c 式に示すように。 (5)[34]、 M s H が減少すると c 増加しました。
$$ {H} _c =\ frac {2 {K} _1} {M_s} $$(5)細孔は反磁界の発生器として機能するため、多孔性が磁化プロセスに影響を与えることも知られています[35]。
サンプルのヒステリシスパラメータが中程度である2番目のグループでは、pH2とpH6が低下したことがわかります(図8)。このグループのサンプルは、最初のグループと同様のヒステリシスループの形状を示しましたが、 M の値がわずかに高くなっています。 s および M r 。 H c pH2とpH6を使用して準備されたサンプルで記録された値は、それぞれ6005.8と5377.0Oeでした。 M s pH2とpH6の値は、7.8 emu / g(226.2 emu / cm 3 )と観測されました。 )および7.0 emu / g(35.8 emu / cm 3 )、それぞれ、 M r pH2とpH6の値は、それぞれ4.9 emu / gと4.4emu / gとして与えられました。サンプルには大きな粒子サイズが存在していましたが、pH 2および6を使用して調製したサンプルで細長い粒子の存在が検出されたため(図6c、gの赤い点線の円を参照)、記録された値は依然として低かった。総異方性エネルギー障壁は体積と表面異方性エネルギー密度に依存することが知られているため、粒子の特定の体積に対して、表面積は細長い形状の粒子の方が大きくなります。したがって、表面から有効異方性への主な寄与と H の増加 c 細長い粒子でも予想される[36]ため、 M が減少します。 s 。
3番目のグループは、pH 0を使用して準備された唯一のサンプルで検出されました。2番目と3番目のグループの間に有意なギャップが観察され、このグループ内のサンプル、特に M での特性の変化を示しています。 s 値。 pH0のヒステリシスループは最大の M s 、 M r 、および H c 有意な値は44.19emu / g(226.2 emu / cm 3 )、27.59 emu / g、6403.6Oe。通常、 M s SrFe 12 の値 O 19 74〜92 emu / gの範囲で、単結晶の形で測定されることがよくあります[8]。 M の値 s pH 0を使用して調製されたサンプルの場合、指定された値よりも比較的低く、以前に報告された56 emu / g [37]および53emu / g [38]の研究でも、どちらもゾルゲル法による合成でした。 M の値が期待されます s この研究では、焼結温度をさらに上げると増加します。ただし、 H c 値は、5000 Oe [37]および5200Oe [38]であった以前の研究よりも比較的高い値を示し、Pullar [8]によると、 H の正確な値は示されていません。 c 加工方法や粒度によって大きく異なります。一方、 M の有意差はありません r 以前に報告されたように、30 emu / gであると見なされていました[38]。明らかな直立した、より大きく、明確に定義されたヒステリシスループが観察されました。これは、完全な結晶性SrFe 12 の高体積分率の形成に起因する強い強磁性挙動によるものです。 O 19 図2に示すように、位相。したがって、ドメイン内の磁気モーメントの強い相互作用は、交換力によって発生しました。この観察された現象は、サンプルの秩序ある磁性と見なすことができます。実際、秩序だった磁性と整形式の M を得るために – H ヒステリシスループ、重要なドメイン形成、十分に強い異方性場、 H が存在する必要があります a 、および粒界や細孔などの欠陥に起因するオプションの添加寄与[39]。このグループの広いループは、実質的な磁気ストレージを意味することに注意するのは興味深いことです。したがって、サンプルは実際のアプリケーションに役立つ可能性のある特性を備えています[40]。
H c 図1と図2のバリエーション。 9aと10は言及に値するはずです: H c pHが上昇するにつれて一般的に減少することが観察されます。 H の減少 c pHの上昇に伴い、異方性Fe 2+ による結晶磁気異方性の低下に起因する可能性があります。 2aサイトに位置するイオンと粒子サイズの拡大は、FESEM顕微鏡写真で明らかです(図6)。さらに、pH 8では、保磁力 H c これは、28.2%のα-Fe 2 が存在するため、5117.7Oeが記録されました。 O 3 不純物(図2)。 H の減少 c 不純物α-Fe 2 の存在によるものでした O 3 H が報告されているため、結晶粒界と結晶粒界に影響を与えました。 c 粒子サイズ、イオン置換、形態、界面構造、結晶欠陥、結晶磁気異方性、ひずみなどの重要なパラメータの影響を受ける可能性があります[41]。直角度比、 M r / M s 、は磁気データから計算され、表1にまとめられています。通常、大きな M r / M s 値は、高密度の磁気記録媒体や永久磁石などの多くのアプリケーションで好まれます[42]。計算された M r / M s この研究では、0.63から0.65の範囲にあることがわかりました。これは、すべてのサンプルが主に単一の磁区構造にあることを示しています[43]。 M r / M s 0.5以上は、粒子が単一の磁区にあり、0.5未満はマルチドメイン構造の形成に起因する可能性があることを示します[43、44]。
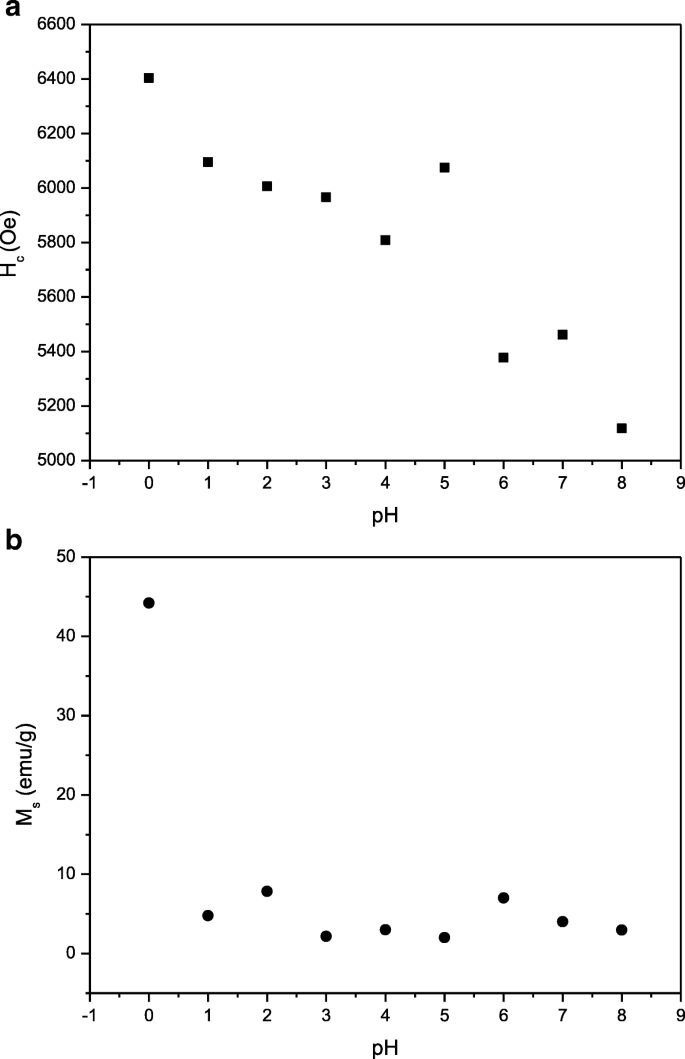
a H c および b M s SrFe 12 の O 19 900°Cで焼結したさまざまなpHで
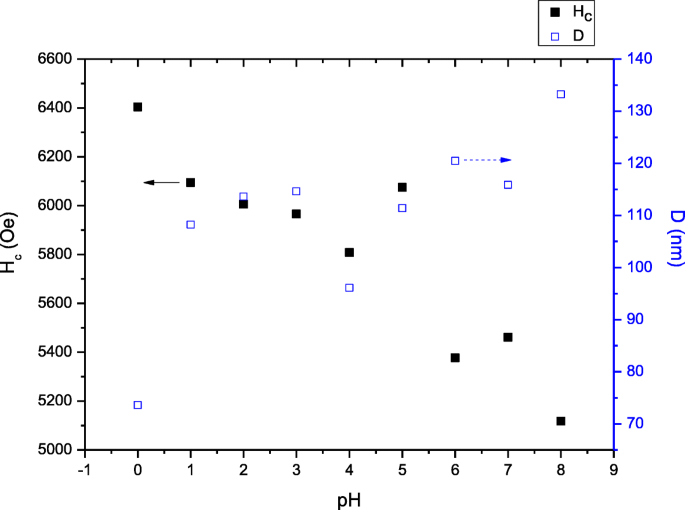
H の関係 c SrFe 12 の粒径と粒径 O 19 900°Cで焼結したさまざまなpHで
結論
SrFe 2 の単相ナノ粒子 O 19 異なるpHを使用して調製されたものは、ゾルゲル法によって首尾よく合成されました。 SrFe 2 の構造的、微細構造的、および磁気的挙動の影響 O 19 900°Cの固定焼結温度でpH値を変更することによって研究されました。この研究から、pH値は単相SrFe 12 の形成に重要な役割を果たしていると結論付けることができます。 O 19 これには7以下のpHが必要であり、pHを0から3に上げることにより、SrFe 12 が形成されます。 O 19 支持されています。 SEM顕微鏡写真は、SrFe 2 の円形結晶タイプを示しました。 O 19 平均粒径は73〜133nmの範囲です。単相SrFe 2 O 19 最適な磁気特性を備えたサンプルがpH0で観察され、面内飽和磁化は44.188 emu / g、残留磁化は27.593 emu / g、保磁力は6403.6Oeと最高でした。
略語
- ρ exp :
-
測定されたサンプルの密度
- ρ 理論 :
-
理論密度
- ρ w :
-
水の密度
- ρ xrd :
-
XRDの密度
- a :
-
格子定数
- C:
-
カーボン
- c :
-
格子定数
- C / N:
-
クエン酸塩から硝酸塩
- C 3 H 4 (OH)(COOH) 3 :
-
クエン酸
- EDX:
-
エネルギー分散型X線
- Fe:
-
鉄
- Fe(NO 3 ) 3 :
-
硝酸鉄(III)
- Fe 2 O 3 :
-
ヘマタイト
- FESEM:
-
電界放出型走査顕微鏡
- FTIR:
-
フーリエ変換赤外
- H:
-
水素
- H a :
-
異方性フィールド
- H c :
-
保磁力
- IR:
-
赤外線
- K 1 :
-
異方性定数
- M :
-
分子量
- M r :
-
残留性
- M r / M s :
-
直角度比
- M s :
-
飽和磁化
- N:
-
窒素
- N A :
-
アボガドロの番号
- NH 3 :
-
アンモニア
- NH 4 OH:
-
アンモニア
- O:
-
酸素
- P :
-
気孔率
- Sr:
-
ストロンチウム
- Sr(NO 3 ) 2 :
-
硝酸ストロンチウム無水粒状
- SrFe 12 O 19 :
-
ストロンチウムフェライト
- V セル :
-
ボリュームセル
- VSM:
-
振動試料型磁力計
- W 空気 :
-
空気中のサンプルの重量
- W 水 :
-
水中のサンプルの重量
- XRD:
-
X線回折
ナノマテリアル
- コバルトをドープしたFeMn2O4スピネルナノ粒子の調製と磁気特性
- 構造的および光学的性質を改善するためのH2 / NH3混合ガス中のGaNベースの多重量子井戸の原子転位
- MnХFe3−XО4スピネルの構造的および磁気的特性に及ぼす接触非平衡プラズマの影響
- グラフェン/ MnZnフェライト/ p-Siヘテロ接合の赤外線特性とテラヘルツ波変調
- 微結晶およびナノセルロースの構造と誘電特性に及ぼす水の影響
- In VivoCTイメージングおよび腎クリアランス特性のための新しい生体適合性AuNanostars @PEGナノ粒子
- Cu / Ti3SiC2 / Cナノコンポジットの微細構造と機械的性質に及ぼすグラフェンとMWCNTの相乗効果
- 着色された低温顔料用のCrドープTiO2の構造的および可視近赤外光学特性
- Ag n V(n =1–12)クラスターの構造的、電子的、および磁気的特性の調査
- 強化された光触媒評価と抗菌分析のためのZnOナノ粒子に対するMgドーピングの影響
- リチウムイオン電池用のザクロ型Fe2O3 / Cアノードの調製と電気化学的性質



