酸化亜鉛/多孔質陽極酸化アルミナ複合膜の調製とアンチバイオフィルム特性
要約
PAA(多孔質陽極酸化アルミナ)膜は、異なる時間の後に2段階の陽極酸化によって調製され、次いで、ZnO / PAA複合膜は、それらの表面上にゾルゲル法によって調製された。一方、ZnO / PAA複合フィルムは、X線回折(XRD)、熱重量/示差熱分析装置(TG / DTA)、フーリエ変換赤外分光計(FT-IR)、走査型電子顕微鏡(SEM)、透過型電子顕微鏡によって特徴づけられました。 (TEM)、選択領域電子回折(SAED)、および水接触角(CA)。 Shewanella putrefaciens 上のZnO / PAA複合フィルムの抗バイオフィルム特性 同時に測定されました。結果は、PAAおよびZnO / PAA複合フィルムの微細形態が2回目の陽極酸化時間の影響を受けることを示しています。 ZnOは六角形のウルツ鉱型構造であり、直径10〜30nmのZnO粒子がPAAの内面または外面に付着します。 Si69によって修飾された後、ZnO膜は親水性から疎水性に変化します。最適なアンチバイオフィルム特性を備えたZnO / PAAフィルムは、40分間の2段階陽極酸化によってPAA表面に作成されます。 Shewanella putrefaciens の順守 はその超疎水性によって抑制され、バイオフィルム細菌の増殖はその豊富なZnO粒子によって抑制されます。
背景
私たちが知っているように、バクテリアは固体表面に付着し、適切な環境で滑りやすいバイオフィルムを形成する可能性があります[1]。通常、バクテリアのバイオフィルムは、ステンレス鋼[2]、ゴム[3]、ガラス[4]、ポリスチレン[5]などの材料の表面にしっかりと付着します。バイオフィルムは、機器の腐食[6]と食品汚染[7]を引き起こし、莫大な経済的損失をもたらします。多くの研究は、バイオフィルムの接着が、粗さ[8,9,10,11]、微細構造[12,13]、親水性[14,15,16,17]、抗生物質成分などの材料表面の特性によって影響を受けることを示しています。 [18、19、20]。 Bohinc etal。 [10]は、ガラスの表面粗さとともに細菌の付着が増加することを指摘しました。シンら。 [12]は、高い表面粗さがタンパク質の吸着を改善し、細菌の付着とバイオフィルムの形成を促進できることを示しました。 Bonsaglia etal。 リステリア菌が見つかりました 疎水性の表面(ポリスチレンなど)よりも親水性の表面(ステンレス鋼やガラスなど)によく接着します[14]。他の研究でも、疎水性表面がバイオフィルムの接着に適していないことが証明されました[16、17]。いくつかの研究は、抗生物質成分がバイオフィルム形成を阻害する可能性があることを示しています[18、19、20]。 34個のCu含有ステンレス鋼表面は、Cu元素の抗菌活性を利用して、優れた抗菌性と抗菌性を備えています[18]。要するに、表面特性は、材料のアンチバイオフィルム特性にとって非常に重要です。
アルミニウム材料が広く使用されており、近年、光電気機能、触媒機能、センシング機能の分野で多孔質陽極酸化アルミナ(PAA)が注目されており[21、22、23、24]、その抗菌作用は報告。 Ferraz etal。 [24]は、PAAがそれらのマトリックス相とナノ多孔性のために単球/マクロファージの付着活性化を誘発する可能性があることを報告しました。
さらに、酸化亜鉛(ZnO)薄膜は、抗菌および抗真菌のための優れた材料として研究されてきました。 緑膿菌の順守 ナノロッド表面構造を有するZnO膜に対しては、ガラスおよびスパッタされたZnOのそれよりも弱く、より多くの P。緑膿菌 ZnO膜で死滅します[25]。一方、ある研究では、ZnOでコーティングされた表面がバイオフィルムの形成を劇的に制限し、ヒドロキシルラジカルの生成がアンチバイオフィルムの活性に重要な役割を果たしましたが、亜鉛イオンの存在には影響しなかったことが指摘されました[26]。さらに、ZnO複合フィルムは、バイオフィルムの形成を制限するために多くの分野で使用でき、水産物の保存に良い応用の見通しがあります[27]。 ZnOは親水性ですが、疎水性フィルムはバイオフィルムの付着を抑えるのに優れています。したがって、ZnO膜の疎水性を向上させる必要があります。
水生製品は、微生物による腐敗のために非常に腐りやすい[28]。好気性貯蔵条件下では、シュードモナス spp。および Shewanella putrefaciens 優勢な腐敗生物として知られています[29]。 シュワネラプトレファシエンス 精神栄養性があり、トリメチルアミンを減らすことができます- N -酸化物からトリメチルアミン[30]。つまり、 Shewanella putrefaciens この論文では、指標細菌として使用されます。
ZnO膜の微細構造は、PAAベースのために異なり、アンチバイオフィルムの特性が影響を受けます。この作業では、ZnO膜を異なる形態のPAAで調製し、疎水性を改善するために変更しました。 Shewanella putrefaciens の抗バイオフィルム特性 ZnO / PAA複合膜の構造を研究した。この結果は、食品包装、食品加工機器、およびその他の抗菌機能材料分野でのアプリケーションに潜在的な価値を提供します。
材料と方法
資料
この研究で使用されたすべての試薬は分析的に純粋でした。脱イオン水と滅菌水を使用して、導電率が0.5 mS / cm未満の溶液を調製しました。 シュワネラプトレファシエンス ATCC8071はアメリカンタイプカルチャーコレクションから購入しました。厚さ0.3mm、アルミニウム純度99.99%以上のアルミニウム箔は、Shengshida Metal Materials Co.、Ltd。(中国)から購入しました。
ZnO / PAA複合フィルムの準備
多孔質陽極酸化アルミナ(PAA)フィルムの準備
高純度のアルミホイルを10×30mm 2 の小さな寸法にカットしました。 研磨機(WV80、Positec Machinery Co.、Ltd。、中国)によって50 nmシリカの研磨ペーストで研磨し、アセトン中で53 kHz、280 Wで15分間超音波脱脂しました(SK8210HP、Kudos Ultrasonic Instruments Co. Ltd 。、上海)。次に、フォイルをエタノールと水でそれぞれ2回洗浄しました。前処理されたアルミニウム箔がアノードとして使用され、等面積のグラファイトシートがカソードとして使用され、0.3 mol / Lシュウ酸溶液が電解質として使用されました。最初の陽極酸化は、30°Cおよび40Vの条件下で90分間行いました。その後、アルミニウムシートを6.0 wt%H 3 の混合溶液に浸しました。 PO 4 および1.8wt%H 2 CrO 4 60°Cで4時間、アルミナ層を除去します。次に、2回目の陽極酸化を同じ条件下で、それぞれ0、40、60、80分間実行しました。異なるポートモデルの多孔質陽極酸化アルミナ(PAA)フィルムが得られました。
ZnO / PAA複合フィルムの準備
まず、等量の0.02 mol / L酢酸亜鉛エタノール溶液と0.04mol / L NaOHエタノール溶液を70°Cで5分間急速に攪拌しながら混合し、次にPAAフィルム(アルミニウム箔)を混合溶液に浸しました。 − 0.085MPaの真空度で。その後、溶液を沸騰するまで加熱した。薄い青色のゾルになった後、アルミホイルを取り出し、脱イオン水ですすいだ。次に、サンプルを-0.085 MPa、80°Cで6時間真空乾燥し、空気雰囲気中で480°Cで2時間焼成した後、ZnO / PAA複合膜を作成しました。酸化亜鉛粉末は同時に調製された。最後に、ZnO / PAA複合フィルムと粉末を、1.0 wt%Si69エタノール溶液で65°Cで2時間修飾した後、-0.085 MPa、40°Cで12時間真空乾燥しました。
ZnO / PAA複合フィルムの特性評価
酸化亜鉛粉末のX線回折は、X線粉末回折計(Rigaku Ultima IV、Rigaku、Japan)を使用して、0.02°および2 θのステップで実行されました。 40 kV、50mAのCuKa放射で10°〜80°の範囲。サンプルの熱変化と重量損失は、熱重量分析/示差熱分析装置(TG / DTA、Perkin Elmer Diamond)によって分析されました。フーリエ変換赤外(FT-IR)スペクトルは、Scimitar 2000 Near FT-IR Spectrometer(Agilent、American)を使用して4000〜400 cm -1 の範囲で記録されました。 。 PAAフィルムおよびZnO / PAA複合フィルムの表面顕微鏡写真は、電界放出走査型電子顕微鏡(FESEM、S−4800、日立、日本)によって画像化された。 ZnO / PAA複合フィルムから削り取られたナノ粒子の形態は、電界放出透過型電子顕微鏡(FETEM、Jem-2100F、JEOL、日本)、および選択された領域の電子回折(SAED、Jem-2100F、EOL、日本)によって測定されます。サンプルを調べた。複合フィルムの水接触角(CA)(変更前/変更後)は、3.0μLの脱イオン水滴(SL200B、米国)を使用して、各サンプル表面のいくつかの異なる位置で液滴法によって測定されました。
ZnO / PAA複合フィルムのアンチバイオフィルム特性
Shewanella putrefaciens の栽培 バイオフィルム
二次活性化 Shewanellaputrefaciens の細菌懸濁液 (OD 595 ≈0.5)と3%(m / v)NaClのアルカリ性ペプトン水(APW)を、1:200( v )の比率で均一に混合しました。 / v )。 ZnO / PAA複合フィルム(0.5×0.5 cm)を3 mLの希釈接種液に浸し、28°Cで一定時間インキュベートしました。この条件下で、 Shewanella putrefaciens よく成長し、強い増殖能力を示しました。
Shewanella putrefaciens の接着アッセイ ZnO / PAA複合フィルム上のバイオフィルム
Shewanella putrefaciens の細菌懸濁液で培養した後 一定時間、バイオフィルムを含むZnO / PAA複合フィルムを別の滅菌遠心分離管に移し、1 mLの0.85%(m / v)滅菌NaCl溶液で3回洗浄して、遊離細菌を除去しました。バイオフィルムは1mLの0.2% w / w で染色されました クリスタルバイオレットを室温で15分間、1 mLの0.85%(m / v)滅菌NaCl溶液で3回洗浄して、余分なクリスタルバイオレットを除去しました。次に、染色されたバイオフィルムを33%( v )超音波で剥ぎ取りました。 / v )53 kHz、280Wで10分間200μLの酢酸。 OD 595 上記の溶液の(595 nmでの光学密度)は、VICTOR™X3マイクロプレートリーダー(Perkin Elmer、America)によって96ウェルマイクロタイタープレートで記録されました。結果は、3回の並行実験の「平均±標準偏差」として示されました。
Shewanellaputrefaciens の総細菌数アッセイ ZnO / PAA複合フィルム上のバイオフィルム
バイオフィルムを含むZnO / PAA複合フィルムを、滅菌リン酸緩衝生理食塩水(PBS、pH 7.4、137 mmol / L NaCl、2.7 mmol / L KCl、10 mmol / L Na 2 )で3回洗浄しました。 HPO 4 、および1.8 mmol / L KH 2 PO 4 )浮遊細菌を除去し、染色されたバイオフィルムを10 mLの滅菌PBSで、53 KHz、280Wで10分間超音波で除去しました。続いて、バイオフィルム中の総細菌数をプレートカウント法によって測定した。 3回の並行実験では、結果は「平均±標準偏差」として示され、バイオフィルム細菌のコロニー成長曲線が描かれました。
Shewanella putrefaciens の顕微鏡写真測定 バイオフィルム
浮遊細菌を除去した後、バイオフィルムを含むZnO / PAA複合フィルムを2.5%( w / v )4°Cで4時間のグルタルアルデヒド。その後、サンプルは30分ごとに、50、70、80、および90%( v )で脱水されました。 / v )それぞれエタノール。無水エチルアルコールに1時間浸した後、サンプルをクリーンベンチで自然乾燥させました。サンプルの表面顕微鏡写真は、3 kVで40秒間金のスパッタコーティングを施した後、FESEM(S-4800、日立、日本)によって画像化されました。
Shewanella putrefaciens のCLSM測定 バイオフィルム
バイオフィルムを含むZnO / PAA複合フィルムをリン酸緩衝生理食塩水(PBS、pH =7.4)で3回洗浄して浮遊細菌を除去し、サンプルを0.01wt%の混合溶液で15分間暗所で染色しました。アクリジンオレンジ(AO、Sigma、アメリカ)および0.1wt%ヨウ化プロピジウム(PI、Sigma、アメリカ)。その後、サンプルをPBSで3回洗浄して余分な染色液を取り除き、余分な水分を取り除きました。 10マイクロリットルの抗蛍光消光シール剤(Biosharp BL701A、中国)をバイオフィルムに滴下し、サンプルを光なしで4°Cで保存しました。バイオフィルムの生細胞と死細胞の比率は、共焦点レーザー走査顕微鏡(CLSM、TCS-SP5 II、ドイツLeica Instrument Co.、Ltd。)を使用して観察されました[31、32]。
結果と考察
ZnO膜の特性評価
ゾルゲル法で調製されたZnO粉末のXRD特性評価
酸化亜鉛の抗菌性と抗菌性は、その結晶構造の影響を受けます[33、34]。図1は、サンプルの結晶構造が煆焼後に変形していることを示しています。煆焼前のサンプルは、ZnOの六方晶ウルツ鉱型構造に含まれています。 2 θの31.70°、34.52°、36.31°、47.68°、56.82°、62.92°、および67.92°に回折ピークがあります。 酸化亜鉛の(100)、(002)、(101)、(102)、(110)、(103)、および(112)結晶面に対応します(PDF#36-1451、 a = b =3.250および c =5.207)、それぞれ。広い回折ピークは、結晶化度が低く、ZnOの粒子が小さいことを示しています。一方、不純なピークが少ないと、サンプルの中間体が明らかになります。 230°Cで煆焼した後、不純なピークは消え、測定されたノイズは減少しますが、回折ピークの幅は不変です。これは、中間体が消え、結晶の次数が増加することを意味します。煆焼温度の上昇に伴い、ZnOの回折ピークが鋭くなり、結晶化度が上昇し、結晶粒子が成長していることを示しています。
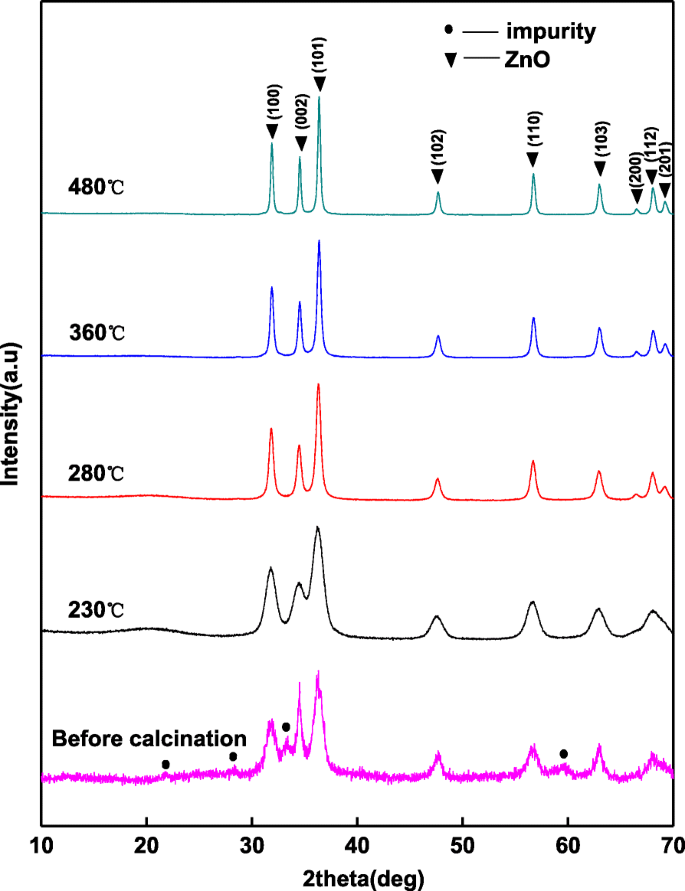
さまざまな温度で焼成された酸化亜鉛粉末のXRDパターン
Zn(CH 3 COO) 2 ・2H 2 OはZn(CH 3 のエタノール溶液で生成されます COO) 2 、およびCH 3 の加水分解 COO − 禁止されています。まず、Zn(CH 3 COO) 2 加水分解されて中間生成物が生成されます。
4Zn(CH 3 COO) 2 ・2H 2 O→Zn 4 O(CH 3 COO) 6 + 2CH 3 COOH + 3H 2 O(1)
加熱プロセスでは、NaOHのエタノール溶液とCH 3 の空間立体効果によってコロソルが促進されます。 COO − ZnOコロソルの安定性にとって非常に重要です。一方、CH 3 の中性反応 NaOHとのCOOHが起こります。
5Zn 4 O(CH 3 COO) 6 + 22NaOH + 13H 2 O→4Zn 5 (OH) 8 (CH 3 COO) 2 ・2H 2 O + 22CH 3 COONa(2)
CH 3 COOH + NaOH→CH 3 COONa + H 2 O(3)
SpanhelとAnderson [35]は、酸化亜鉛アルコゲルが凝集とオストワルド成長(老化)によってZnO粒子から形成されることを示しました。次に、Zn 5 の中間体 (OH) 8 (CH 3 COO) 2 ・2H 2 Oは加熱されてZnO相に分解されます[36、37]。したがって、ZnOの六方晶ウルツ鉱構造は、煆焼前の乾燥ゼラチンの基礎となります。
Zn 5 (OH) 8 (CH 3 COO) 2 ・2H 2 O→5ZnO + 2CH 3 COOH + 5H 2 O(4)
細野ほか[37]この反応メカニズムを確認しました。 Zn(CH 3 のエタノール溶液 COO) 2 ・2H 2 Oは60°Cでの加熱中にコロイド生成物になり、XRDの結果は、ゼラチンの乾燥生成物が結晶性ZnOとZn5(OH) 8 の混合物であることを示しています。 (CH 3 COO) 2 ・2H 2 O. 48時間還流した後、粒子はウルツ鉱型ZnOに変換されます。
TG / DTA分析
酸化亜鉛ゼラチンのTG / DTAの結果を図2に示します。TG曲線は、3つの段階に分けることができます。最初の段階では、質量損失は室温から100°Cまで68.6%であり、62°Cに吸熱ピークが存在しました。これは、酸化亜鉛ゼラチン中の失われたエタノール溶媒と水に対応します。第2段階では、100〜400°Cでの質量損失はわずか3.8%です。 XRDの結果は、230、280、および360°Cでそれぞれ焼成した後、不純物が消失し、結晶化度が増加し、結晶粒子が成長したことを示しています。少量の質量損失は、間隙水の損失と不純物の遷移である可能性があります。 400〜850°Cでは、質量損失や吸熱ピークはなく、この段階では結晶変態がないことを示しています。一方、XRDの結果は、480°Cでの煆焼後に結晶が成長することを示しています。 TG / DTAの結果はXRDの結果と一致しています。
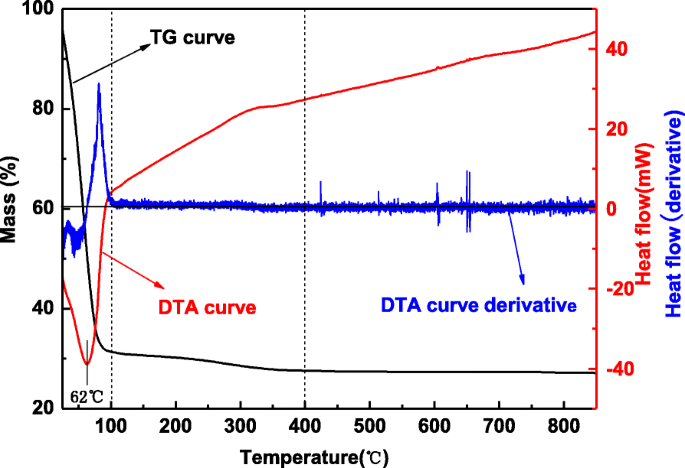
酸化亜鉛ゼラチンのTG / DTAグラフ
未修飾/修飾酸化亜鉛フィルムのFT-IR特性評価
図3は、未修飾および疎水性修飾ZnOフィルムのFT-IRスペクトルを示しています。 3600〜3300 cm -1 の広いピーク -OHの伸縮振動と、1651 cm -1 のピークに起因します。 は、それぞれ–OHの曲げ振動に起因し、サンプルに吸収された水と毛細管水を示します[38]。 2360および2328cm -1 のピーク 空気中の二酸化炭素に起因します。 2943および2864cm -1 のピーク -CH 2 の非対称および対称伸縮振動によるものです。 、 それぞれ。 1475 cm -1 の強いピーク -CH 2 の面内曲げ振動またはシザリング振動によるものです。 グループ[39]、および895 cm -1 のピーク Si-O基の伸縮振動によるものです[40]。約440および414cm -1 のピーク 未修飾/修飾ZnOのZn-O基のフレームワーク振動に起因します[41]。結果は、修飾によりSi69の–S–S–結合が破壊され、トリエトキシシリルプロピルがサンプルにグラフトされるため、ZnO膜の疎水性が向上することを示しています。 Wang [42]は、化学反応によってナノZnO粒子の表面にグラフトされたSi69およびSi69をその場で修飾することにより、ナノZnO分散を改善できると報告しました。これは、分析結果と一致しています。
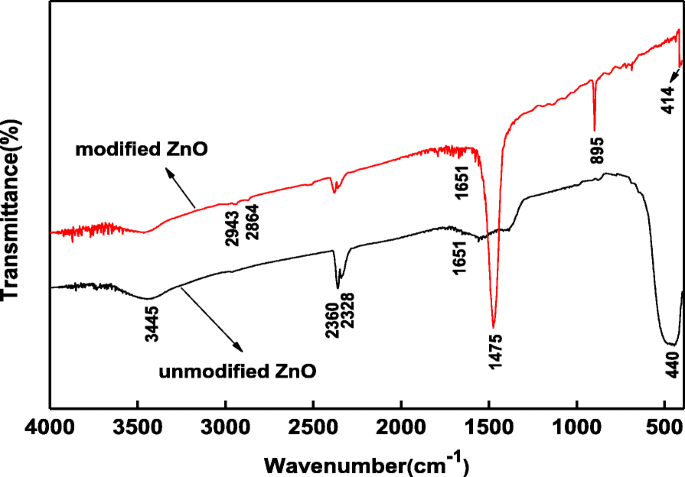
未修飾/修飾酸化亜鉛膜のFT-IRスペクトル
PAAフィルムの微細形態分析
PAAフィルムの形態は、2回目の陽極酸化酸化時間の影響を受けます。図4に示すように、最初の陽極酸化処理のアルミナ層を除去した後、PAAフィルムは、5〜10 nmのナノポアを備えた鋸歯状の六角形のハニカムフレームになります(図4a)。 40分間の2段階の陽極酸化の後、ナノポアは多層シェルフレームに変換されます(図4b)。 60分間の2段階の陽極酸化後、多層シェルフレームはフェードアウトし、ナノポアの直径は20〜40 nmに拡大します。その間、表面に隆起があります(図4c)。 2段階の陽極酸化時間を80分に延長すると、ナノポアは60〜70 nmに拡大し、隆起は消えます(図4d)。

2回目の陽極酸化期間が異なる多孔質陽極酸化アルミナ(PAA)のSEM画像 a 0分、 b 40分、 c 60分、 d 80分
酸性電界支援溶解(AFAD)の理論[43]によれば、陽極酸化プロセスでは、バリア層の酸化膜が不均一になり、隆起が形成されます。これらの時点で、ミクロポーラスの形成と発達は、悪化したAFADによって促進されます。 2回目の陽極酸化時間が長くなると、表面に規則正しい貫通穴が徐々に形成され、多層シェルフレームと隆起が消えました(図4b–d)。結果は、0.3 mol / Lシュウ酸で2段階の陽極酸化プロセスを介してPAAを調製したReddyの結果と似ています[44]。
ZnO膜の微細形態分析
材料表面のアントバイオフィルム特性は、それらの形態と物質によって影響を受けます[12]。図5に示すように、ZnO膜の形態は大きく異なり、2回目の陽極酸化期間が異なるPAA膜で作成されます。 5〜10 nmのナノポアを持つPAAフィルムの表面には、20〜30 nmの凝集した大きな粒子が密に付着し、厚いZnOフィルムを形成します(図5a)。 2段階の陽極酸化期間40分で作成されたPAAフィルムの表面では、多層シェルフレームがZnOフィルム上に残ります(図5b)。図5cに示すように、ZnO粒子はPAAフィルムの骨格に付着し、より大きな穴を形成しています。 60〜70 nmのナノポアを持つサンプルでは、10〜20 nmのZnO粒子がPAAホールのエッジに付着し、粒子の一部がナノポアに入りました(図5d)。これは、真空条件下で大きな穴に入り、次にZnO粒子を形成するコロソルである可能性があります。上記の結果は、PAAのナノポア径が小さいほど、ZnOの付着率が高いことを示しています。ウーら[45]ゾル粒子の負とPAA細孔壁の正のために、コロソル粒子が穴の壁に容易に形成されると考えてください。この発見は、Bousslamaらによる研究とも一致しています。 [46]。コロソルは、PAAフィルムを亜鉛ゾルに24時間浸したときに穴の壁に付着するだけで、その後、穴は48時間いっぱいになります。これは、コロソル粒子が穴の壁に優先的に付着したことを示しています。

2段階の陽極酸化期間の異なる時間でPAA上に調製されたZnO膜のSEM画像 a 0分、 b 40分、 c 60分、 d 80分
上記の結果は、コロソル粒子が真空条件下で大きな穴に入り、内面に付着しやすいことを示しています。ただし、コロソル粒子は、PAAの外面の骨格に小さな穴でしか付着しません。
ZnO / PAA複合フィルムから削り取られたZnOフィルムのTEM画像を図6に示します。1段階の陽極酸化のみで作成されたPAA表面では、層間剥離したZnO粒子は約10 nmですが、粒子は20〜30 nmはSEM画像(図5a)に示され、ZnO粒子が凝集していることを示しています。 2段階の陽極酸化によって作成されたPAA表面では、剥離したZnO粒子は約20 nmであり、粒子の一部は個々の場所に凝集しています。 ZnO粒子が最初にPAA穴の端に付着していることが明らかになります(図6c、e、f)。

TEM画像( a 、 c 、 e 、 f )およびSAEDパターン( b 、 d )2段階の陽極酸化期間の異なる時間でPAA上に調製されたZnO膜の a 、 b 0分 c 、 d 40分; e 60分;および f 80分
六方晶ウルツ鉱構造ZnOの格子面(100)、(101)、(102)、(110)、(103)をSAEDパターンで示し(図6b、d)、ZnOが六方晶ウルツ鉱であることを示しています。結果はXRD分析と一致しています。
ZnOフィルム表面の疎水性-親水性の特性評価
材料の細菌付着を減らすために、異なる微細形態で調製されたZnOフィルムを処理して疎水性を改善し、修飾前後の薄膜表面の水接触角を表1に示します。
<図>修飾前は、ZnO粒子の表面ヒドロキシル基のためにZnOフィルムは親水性です。親水性は、PAA表面に40分の2段階の陽極酸化期間で準備された多孔質構造のために最高です。 2段階の陽極酸化期間が60分と80分である他のサンプルでは、ZnOの接着量が少ないため、親水性は徐々に低下します。ワンステップの陽極酸化期間のサンプルの場合、水媒花が少ないのは、その非多孔質構造によるものです。
修飾後、ZnO膜は疎水性に変換されます。 FT-IR分析によると、トリエトキシシリルプロピルは、Si69の–S–S–結合が破壊された後にサンプルにグラフトされます。一方、それはその多孔質構造とより多くのZnO粒子の結果である可能性があります。フィルムの疎水性は最も高く、2段階の陽極酸化時間は40分です。
Shewanella putrefaciens の特性 バイオフィルム
Chi etal。 [47]は、陽極酸化アルミニウムにはグラム陰性菌( Escherichia coli )に対する抗菌活性がないことを報告しました。 および P。緑膿菌 )およびグラム陽性菌( Streptococcus faecalis および黄色ブドウ球菌 )。しかし、ZnOは優れた抗菌および抗菌活性を持ち[25、26、27]、抗菌活性と抗菌活性の間には正の相関関係があります[48、49]。さらに、ZnOの抗菌特性はその微細構造の影響を受けます[50、51]。優れたアンチバイオフィルム活性表面を得るために、異なる微細構造のZnOフィルムを、2回目の陽極酸化時間の異なるPAAフィルム上に調製し、アンチバイオフィルムの特性を測定しました。
バイオフィルムの付着とバイオフィルム細菌の増殖曲線
バクテリアのバイオフィルムの形成と発達は、5つの段階で終わらせることができます。可逆的接着から不可逆的接着への変換;バイオフィルムの最初の形成;成熟したバイオフィルムの開発;バイオフィルムとバクテリアの退化は浮遊状態に戻ります[52]。
図7(1)に示すように、2時間で、 Shewanella putrefaciens の付着 ZnOフィルム上のバイオフィルムは急速に増加し、細菌の可逆的付着から不可逆的付着への変換を示しています。 2時間から12時間まで、バイオフィルムの付着は徐々に増加します。これは、バイオフィルムの成長段階です。 12〜24時間で、バイオフィルムの付着はわずかに増加または減少し、バイオフィルムの成熟段階を示します。 24時間後、バイオフィルムの付着は低下し、バイオフィルムは変性段階に入ります。図7(2)は、バイオフィルム細菌の変動傾向がバイオフィルムの付着と一致していることを示しており、バイオフィルムの発達はバイオフィルム細菌に依存していることを示しています。
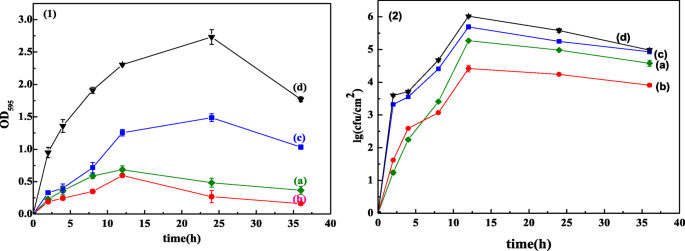
Shewanella putrefaciens の付着 バイオフィルム( 1 )およびバイオフィルム細菌のコロニー増殖曲線( 2 )2段階の陽極酸化時間の異なる時間でPAA上に調製されたZnOフィルム(a)0分、(b)40分、(c)60分、および(d)80分
さらに、PAA表面に80分間の2段階の陽極酸化期間で調製されたZnOフィルムの場合、バイオフィルムの付着とバイオフィルム細菌の総量の両方が4つのサンプルの中で最も高くなっています。ただし、PAA表面に2段階の陽極酸化時間を40分間かけて作成したZnO膜の場合、アンチバイオフィルムの特性が最適です。これは、最高の疎水性によって阻害されるバイオフィルムの付着、次にバイオフィルム細菌の増殖に対するエキソポリサッカライド(EPS)および他の栄養素の減少が原因である可能性があります。 PAA表面に80分間の2段階の陽極酸化期間で調製されたZnOフィルムの場合、その親水性はバイオフィルムの初期付着に適しており、ZnO粒子が少ないとバイオフィルム細菌の増殖が阻害されません。一方、より多くのバイオフィルム接着剤がバイオフィルムバクテリアに栄養を与え、バイオフィルムバクテリアは急速に増殖します。私たちの研究と一致して、バイオフィルムの付着は、バイオフィルム形成の初期段階でのZnOフィルムのより高い疎水性によって阻害されます[49]。バイオフィルムの付着は、材料の疎水性と親水性の特性に影響されます[14、53、54]。 Bonsaglia etal。 [14]は L。リステリア・モノサイトゲネス 疎水性表面よりも親水性表面に付着しやすい。多くの研究は、細菌の付着が疎水性の表面によって減少または阻害されることを発見しました[47、54]。 Shaer etal。 [54]は、機能化整形外科用ハードウェアでのバイオフィルムのコロニー形成は、疎水性のポリカチオンによって防ぐことができることを示しました。 Chen etal。 [55]はまた、バイオフィルムが低い表面自由エネルギーによって阻害される可能性があることを示唆した。結果は私たちの結果と一致しました。
Shewanella putrefaciens の形態的特徴 バイオフィルム
Shewanella putrefaciens のミクロトポグラフィー さまざまな段階のバイオフィルムを図8に示します。

2段階の陽極酸化期間の異なる時間でPAA上に調製された酸化亜鉛膜上のバイオフィルムのSEM画像 a 0分、 b 40分、 c 60分、 d 80分
2時間培養した後、PAAで調製されたZnOフィルムには、2段階の陽極酸化処理を行わず(a)、2段階の陽極酸化処理を40分間行った場合(b)の接着剤は少なくなりますが、接着剤は多くなり、バクテリアはわずかになります。他の2つ(c、d)。前者の2つの付着防止特性は後者の2つよりも優れていることが示され、図7と一致しています。12時間培養した後、ますます多くのEPSとバクテリアがZnOフィルムに付着し、急速な成長を示しています。バイオフィルムの。 24時間で、EPSフィルムは徐々に厚くなり、バイオフィルムバクテリアはよく成長し、成熟したバイオフィルムを示します。 36時間の時点で、落葉性EPSフィルムと死菌は、バイオフィルムの変性段階を示しています。
溶存金属イオンの抗菌メカニズムによれば、溶存亜鉛イオンはバクテリアの活性プロテイナーゼと結合し、プロテイナーゼの生物活性を失い、バクテリア細胞を死に至らしめます[34、56]。したがって、前者の2つ(a、b)の抗菌特性は、フィルム上に豊富なZnO粒子があるため、後者の2つ(c、d)よりも優れています。 Xie [57]とJones [58]も、ZnO粒子の投与量を増やすと抗菌能力が強化されると考えました。一方、 Shewanella putrefaciens の接着分析によると、サンプル(d)の接着剤とバクテリアはすべて他のものよりも多いです。 バイオフィルムおよびバイオフィルム細菌のコロニー成長曲線(図7)。 Feng etal。 [59]は、 Escherichia coli の菌糸が 直径50および100nmのPAA細孔に容易に到達し、バイオフィルムが蓄積してPAAの表面に付着しました。ただし、 Shewanella putrefaciens の菌糸はありません。 私たちの研究で観察することができます。最適な抗バイオフィルム特性は、バイオフィルム形成の初期段階でのZnOフィルムの疎水性が低いことに起因すると推測できます。
ZnO / PAA複合バイオフィルムのCLSM特性
CLSM画像に示されているように、ライブの Shewanella putrefaciens バクテリアは緑色で、死んだバクテリアは赤色です(図9)。黒い画像は、2時間のバイオフィルム培養後、表面の生きた細菌の数が少ないことを示しています。バイオフィルム菌は急速に増殖し、培養時間とともに生菌数が大幅に増加します。前の2つ(a、b)では24時間で、すべてのサンプルで36時間でより多くの死菌が観察されます。後者の2つ(c、d)の死菌数は、前者の2つ(a、b)よりも少なくなっています。結果は、前の2つ(a、b)の抗菌特性が、前の分析によると、後の2つ(c、d)の抗菌特性よりも優れていることを示しています。
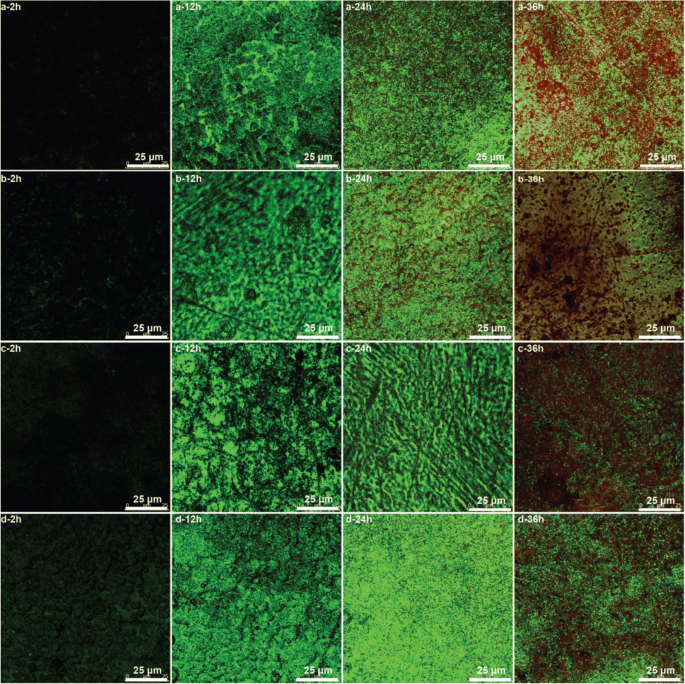
CLSMは、2段階の陽極酸化期間の異なる時間でPAA上に作成された酸化亜鉛膜上に形成されたバイオフィルムを画像化します a 0分、 b 40分、 c 60分、 d 80分
結論
この作業では、最初に2段階の陽極酸化によって微細構造の異なるPAAフィルムを作成し、次にゾルゲル法によってZnO / PAA複合フィルムを作成します。 ZnO膜は、ZnO粒子の表面ヒドロキシル基のために親水性である。 Si69によって修飾された後、ZnO膜は、その疎水性基のために疎水性に変換されます。 ZnOフィルムのアンチバイオフィルム特性は、疎水性とZnO粒子の量に影響されます。疎水性は、バイオフィルムの初期付着を阻害し、バイオフィルム細菌の増殖に対するEPSおよび他の栄養素を減少させます。そのため、ZnO / PAAフィルムのアンチバイオフィルム特性は最適であり、超疎水性と大量のZnO粒子により、PAA表面に40分間の2段階の陽極酸化期間で調製されます。
略語
- AO:
-
アクリジンオレンジ
- CA:
-
水接触角
- EPS:
-
エキソポリサッカライド
- FT-IR:
-
フーリエ変換赤外分光計
- PAA:
-
多孔質陽極酸化アルミナ
- PBS:
-
リン酸緩衝生理食塩水
- PI:
-
ヨウ化プロピジウム
- SAED:
-
選択領域電子回折
- SEM:
-
走査型電子顕微鏡
- TEM:
-
透過型電子顕微鏡
- TG / DTA:
-
熱重量分析/示差熱分析
- XRD:
-
X線拡散
ナノマテリアル
- コバルトをドープしたFeMn2O4スピネルナノ粒子の調製と磁気特性
- TiO2ナノ流体に向けて—パート1:準備と特性
- ゾル-ゲル法によるナノ構造シリカ/金-セルロース結合アミノ-POSSハイブリッド複合材料とその特性
- チタン酸塩ナノチューブで装飾された酸化グラフェンナノコンポジット:調製、難燃性、および光分解
- 圧力センサーおよび調整可能な感度を備えたガスセンサーとしての多層多孔質ポリアニリン複合材料の容易な製造
- Al2O3 / ZnOナノラミネートの形態的、光学的、および電気的特性に及ぼす二重層の厚さの影響
- 界面層の設計によるZnO膜の表面形態と特性の調整
- 超循環原子層堆積によるZnO膜のフェルミ準位調整
- 分子線エピタキシー法を用いたGeBi膜の作製と光学的性質
- GeSiSnナノアイランドと歪み層を備えた半導体膜の形態、構造、および光学特性
- 赤外領域におけるAlドープZnO膜の光学的性質とそれらの吸収への応用



