アニーリングされた酸化スズナノ構造の光触媒、殺菌および分子ドッキング分析
要約
ナノサイズの酸化スズは、シンプルで費用対効果の高い沈殿技術で製造され、X線粉末回折(XRD)、フーリエ変換赤外線(FT-IR)分光法、高分解能透過型電子顕微鏡(HR-TEM)顕微鏡法を実行して分析されました。 、エネルギー分散型X線(EDX)およびUV-Vis分光法。 XRDの結果から、酸化スズ粒子は典型的な斜方晶構造を持ち、アニーリングによって結晶化度が向上することが明らかになりました。 250°Cでの煆焼により、主に斜方晶系のSnOが生成され、SnO 2 に変換されました。 500および750°Cの高温で。 HRTEMおよびFESEM画像は、酸化スズの粒子内に凝集が存在することを示しました。吸収は特定のアニーリング温度まで増加し、その後減少することがわかりました。これは、UV-Vis分光法によって記録されました。合成された光触媒の染料分解挙動に及ぼすアニーリング温度の影響を研究した。アニーリング温度は、合成された粒子のサイズ、バンドギャップ幅、および酸化スズの光活性に影響を与えることに注意してください。 500°Cで調製されたサンプルは、一次反応速度に従い、メチレンブルーに対して最大の光触媒反応性を示しました。本研究から得られた実験結果は、SnO 2 は、廃水や環境から汚染物質を除去するための有望で有益な触媒です。 Eなどの選択されたターゲットに対して500°CでアニーリングされたSnOの抗菌評価。コリ および S。アウレウス 250および750°Cのサンプルと比較して、有意な抑制ゾーンが示されています。さらに、SnO 2 の分子ドッキング予測 ナノ粒子(NP)は、βのアクティブポケットに対して実行されました。 -それぞれ細胞壁と核酸生合成経路に属するラクタマーゼとDNAジャイレース酵素。作製されたNPは、βに対して良好な結合スコアを示しました。 -両方の Eのラクタマーゼ。コリ (− 5.71 kcal / mol)および S。アウレウス (− 11.83 kcal / mol)DNAジャイレース(− 9.57 kcal / mol; E. coli および− 8.61 kcal / mol; S。アウレウス )。これらのインシリコ予測は、SnO 2 を示唆しました 選択されたタンパク質標的の潜在的な阻害剤としてのNPは、新しい抗生物質の発見に寄与する可能性のある作用機序の明確な理解を促進します。
はじめに
従来の金属酸化物に関連する卓越した特性と幅広い技術的応用は、これらの材料をナノ構造の形で探索するきっかけとなりました。これらの中で、酸化スズ(SnO 2 )は、室温で3.6eVのワイドバンドギャップを示す重要な金属酸化物[1]であると考えられています[2]。これは、ドナー(n型キャリア)と相互作用する格子間スズ原子を含む酸素空孔の形で固有の欠陥を持つn型半導体材料です。伝導帯の自由電子の数が増えると、材料の導電率が上がります[3]。
SnO 2 の使用 酸化触媒として、光触媒、ガスセンサー、透明導体は、この材料をさらに調査するための基礎を提供します[4,5,6,7,8,9]。可燃性、爆発性、および有毒ガスを検出する機能があります[10]。工業化により、COやSO 2 などの有害な大気汚染物質や水質汚染物質の排出が増加しています。 大気中および廃水中の有害なアゾ染料。約500トンのさまざまな染料が工業廃水に排出されていると推定されており、それらの大部分(〜80%)は繊維産業からのものです[11]。化学毒素と有機燃料は大気汚染の一部を形成し、水域からの危険な染料は地球の生態系に影響を与えるため、そのような汚染物質が環境に害を及ぼすのを検出して防止するために使用される技術の重要性が増しています。その独特の物理化学的特性により、SnO 2 低温で動作する能力があります。固有の非化学量論により、表面への酸素の吸着を容易にすることで有害ガスを低減します。さらに、同様の用途に使用される他の利用可能な材料と比較した場合、コストが低くなります。また、実質的な光学的透明性と導電性を備えているため、オプトエレクトロニクスコンポーネントでの使用に適しています[12]。パネルやいくつかのエレクトロクロミックデバイスで使用するための透明電極や太陽電池の製造に使用されています[13、14、15、16、17]。
水系感染症を予防するために、飲料水や衛生システムでは、廃水からバクテリアを除去することが重要です。米国では2003年から2005年の間に、4つの水系感染症が報告されました。これらの病気は、約282人の人間に影響を与える飲料水中の病原体に現れました。水域を消毒するための従来の技術は、嚢胞を形成する原生動物(GiardiaおよびCryptosporidium)に対して効果が低い化学薬品に依存しています。また、これらの技術は有害な副産物を生成することがあります。ナノテクノロジーは、新しい消費者製品、材料の使用法、製造方法を通じて世界経済に影響を与えることができる新世代の技術です[18]。金属酸化物ナノ構造は、表面積対体積比、安定性、および生体適合性が高いことに起因する抗菌特性の向上を示しています。それらは、細胞膜構造を貫通し、細菌の細胞部分を破壊する独自の能力を持っています[19]。
SnOとSnO 2 などの2つの基本的な酸化スズが主に研究されています 、およびこれらの酸化物の存在は、二重のSnバランス度(酸化あり)+2および+4に起因します。これらの2つの酸化物は、酸化スズの場合はPbO構造、SnO
SnOおよびSnO 2 材料はリチウムイオン電池にも使用されています[23、24、25]。報告された文献は、ナノ材料の電気化学的性能は、そのサイズを制御することによって改善できることを示しています[26]。木田ほか粒子サイズの減少がH 2 のセンサーの応答の増加を引き起こしたことを報告しました 検出;ただし、H 2 への応答 SとCOは、粒子サイズの増加とともに増加しました[27]。 SnO 2 を生成するためのさまざまな方法 文献で報告されています。 Merlin [28]は、キャッピングおよび還元剤として機能するエタノール性ステビアレバウディアナ植物抽出物を使用したグリーン合成により、サイズ範囲が20〜30nmのナノ粒子を合成しました。 Janardhan etal。 [29]希塩酸とSnCl 2 を使用して、平均サイズが50nmのSnOナノ粒子を調製しました。 ・2H 2 O.セルバクマリ他[30]製造されたSnO 2 鶏の卵殻膜を使用した平均結晶サイズが13〜40nmの粒子。
一般に、ナノ材料は、電気化学的還元[31]、ゾル-ゲル[32]、熱水[33]、共沈[34]などのさまざまな方法を使用して合成できます。本研究では、ナノ構造を合成するための便利で費用効果の高い技術を構成するため、沈殿法が好まれました。この研究の目的は、合成中に使用されるさまざまな温度(250、500、および750°C)が、調製された非構造材料の結晶子サイズ、形態、およびバンドギャップエネルギーに及ぼす影響を観察することでした。さらに、合成された生成物の光触媒挙動は、世界中の産業で一般的に遭遇する汚染物質であるメチレンブルー染料の分解にそれを使用することによって研究された。 SnO 2 の殺菌活性に関与するメカニズムを明らかにするために、インシリコ分子ドッキング予測が実行されました。 β-に対して 細胞壁生合成経路に属するラクタマーゼおよび Eからの核酸生合成経路のDNAジャイレース。コリ および S。アウレウス 。
メソッド
現在の研究は、SnO 2 を合成することを目的としていました 簡単で簡単な沈殿プロセスによってナノ粒子をさまざまな温度でアニールします。アニーリングされたSnO 2 廃水と抗菌力から有機汚染物質を除去するために使用されました。
化学薬品
塩化スズ(II)二水和物(SnCl 2 ・2H 2 O)および分析グレードのエタノールはSigma-Aldrich(ドイツ)から直接入手しました。水酸化ナトリウム(NaOH)とメチレンブルー(MB)は、それぞれMerk(ドイツ)とBDH(英国)から調達しました。蒸留水は、酸化スズナノ構造を製造するために地元の市場から購入しました。この研究で使用された汚染物質(つまり、MB染料)の化学構造を図1に示します。
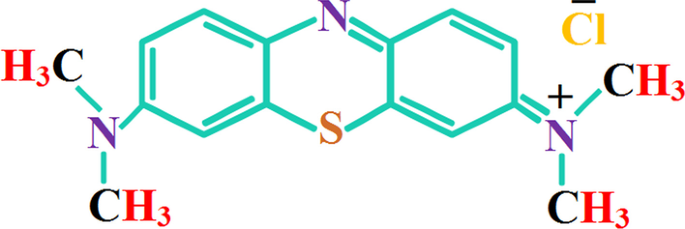
MB汚染物質の化学構造
酸化スズナノ構造の調製
この研究では、高純度の分析グレードの市販化学物質を使用して、沈殿手順を使用して酸化スズナノ材料を調製しました(図2を参照)。 SnCl 2 の水溶液 ・2H 2 O(19 g)とNaOH(8 g)は、50mLの蒸留水で別々に調製しました。 NaOHの水溶液をSnCl 2 に滴下した。 .2H 2 400 mLフラスコを使用して、70°Cで一定に攪拌しながらO溶液(〜10滴/分)。溶液を滴下すると白い沈殿物が現れた。得られた生成物を、遠心分離機で蒸留水およびエタノールを使用して数回洗浄した。得られた材料をさらに室温で48時間乾燥させて、水分を除去しました。最後に、乾燥した固形物を乳鉢と乳棒を使用して微粉末の形に粉砕した。 3つのサンプルをマッフル炉でさまざまな温度(250、500、750°C)で3時間、加熱速度0.5°C /分でアニーリングしました[35]。
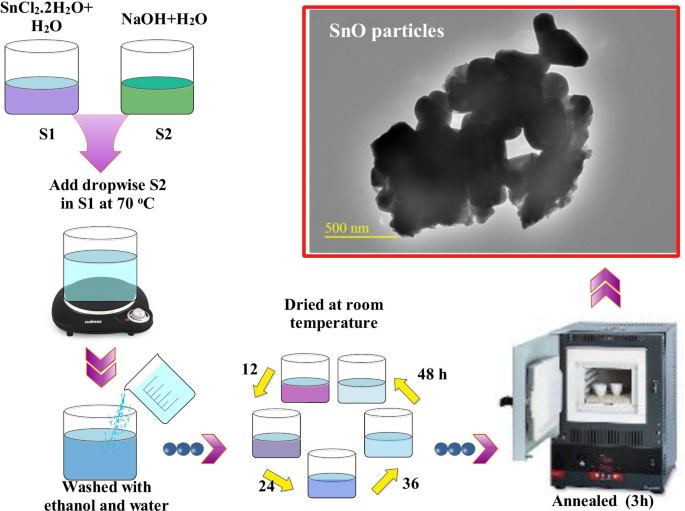
酸化スズサンプルの合成の概略図
光触媒活性プロセス
アニールされた酸化スズサンプルの光活性ポテンシャルは、光源下でのMB水溶液の光分解を監視することによって評価されました。図3に示されているメカニズム[36、37、38]。各光活性実験では、既知の質量のナノマテリアル(10 mg)を60 mLの染料水溶液(10 mg / L)に添加しました。光を照射する前に、懸濁液を暗所で5分間磁気的に攪拌して[38]、光触媒の表面での色素の吸着/脱着平衡を取得しました。懸濁液に水銀ランプ(400Wおよびλ)を80分間照射しました。 =400–700 nm)攪拌下(220 rpm)。 〜5 mLのMBサンプルをテスト溶液から抽出し、300〜750nmの範囲のUV-Vis分光光度計を使用してMBの残留量を監視しました。 MB色素の光分解を研究するために、放射線時間に対するMB最大吸収波長(〜665 nm)の変化を記録しました。合成された生成物の活性は、以下の関係を使用して色素分解%を計算することによって評価されました:
$$ \ hbox {Degradation} \、\%=[{({C}} _ {0}-{C})/ {{C}} _ {0}] \ times 100 $$(1)ここで C 0 初期MB濃度と C を示します 照射後の濃度を示します。光触媒なしで、対照実験も同じ条件下で実施された。ナノマテリアルの再利用性を調べるために、分解されたMB溶液を10分間遠心分離(6000 rpm / min)して、光触媒を回収しました。その後、回収した製品を80°C(2時間)で乾燥させ、MB分解実験に再利用しました。触媒の耐久性をテストするために、リサイクル光活性実験を最大4サイクル実行しました。各サイクルの後、製品を遠心分離し、乾燥させ、次の光実験に使用しました。
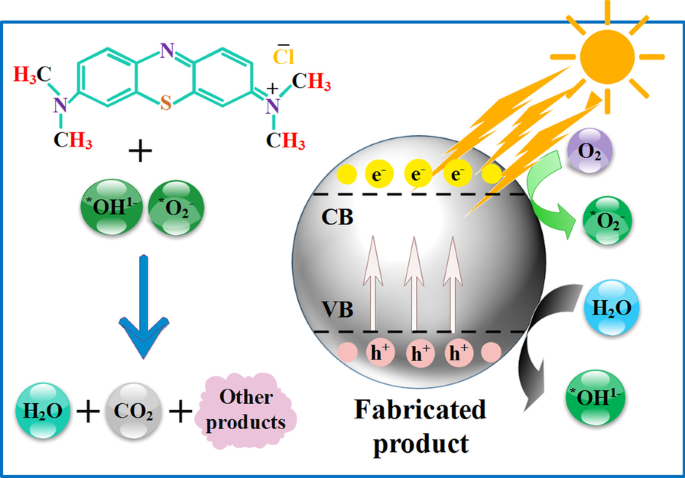
光触媒によるメチレンブルーMBの分解の図解
抗菌作用
さまざまな温度処理での製造されたSnOのinvitro抗菌作用は、最も一般的な病原菌 Eに対して評価されました。コリ および S。アウレウス ウェル拡散アッセイを使用してヤギ乳房炎から分離。固化したマッコンキー寒天培地とマンニット食塩寒天培地でバクテリア活性化増殖(0.5マクファーランド標準)を含むペトリ皿を、滅菌コルクボーラーを使用して直径6 mmのウェルを調製した後、37°Cでインキュベートしました。異なる濃度の合成ナノ構造(500および1000μg/50μl)を低用量および高用量として適用し、対照の陽性および陰性としてそれぞれシプロフロキサシン(5μg/50μl)およびDIW(50μl)を適用しました。 37°Cで一晩インキュベートしたペトリ皿は、ノギスを使用して測定された抑制ゾーン(mm)を宣言しました。阻害ゾーン(mm)で測定された抗菌活性は、SPSS 20.0を使用した一元配置分散分析(ANOVA)を使用して統計的に有意であると宣言されました。
分子ドッキング研究
細胞壁合成は、ベータラクタム系抗生物質や糖ペプチド系抗生物質など、さまざまな作用機序を持つさまざまな抗生物質を発見するための効果的な標的と見なされてきました。ベータラクタム系抗生物質は、最も市場に出回っている薬として報告されており、細菌感染症の最も一般的な治療法です[39、40]。それらは、ペニシリン結合タンパク質(PBP)およびβと結合することにより、細胞壁の生合成を阻害します。 -ラクタマーゼ[41]。同様に、核酸合成に属する酵素(すなわち、DNAジャイレース)も抗生物質発見の効果的な標的と見なされてきました[42]。ここでは、SnO 2 の分子ドッキング研究を行いました。 βに対するNP -両方の EのラクタマーゼおよびDNAジャイレース酵素。コリ および S。アウレウス 考えられる作用機序についての洞察を得る。
Eに属する選択されたタンパク質標的の3D結晶構造。コリ および S。アウレウス アクセッションコードが4KZ9のタンパク質データバンクから取得されました。解像度:1.72Å[43]、1MWU;解像度:βの場合は2.6Å[44] -ラクタマーゼ、6KZX;解像度:2.1Å[45]および5CTU; Res:図4に示すように、DNAジャイレースの場合は1.45Å[46]。
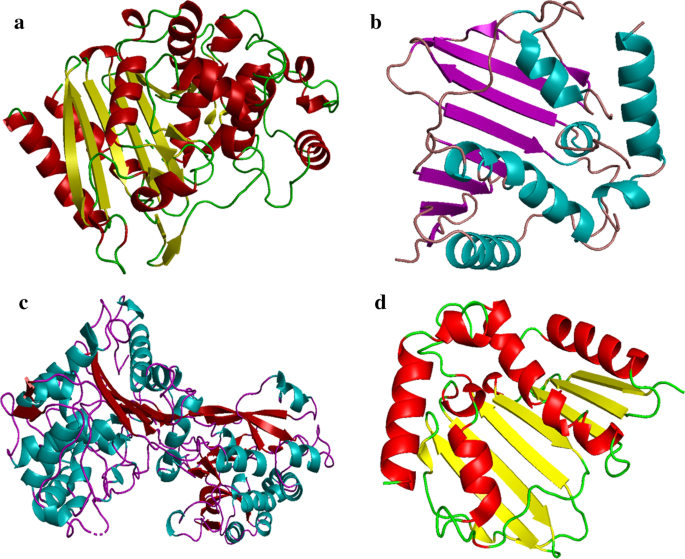
a の3D構造 ベータラクタマーゼ(PDB:4KZ9)、 b EからのDNAジャイレース(PDB:6KZX)。コリ 、 c ベータラクタマーゼ(PDB:1MWU)および d SのDNAジャイレース(PDB:5CTU)。アウレウス
分子ドッキング研究は、ICM Molsoftソフトウェア(Molsoft L.L.C.、カリフォルニア州ラホーヤ)ソフトウェアを使用して実施されました[47]。 ICMの受容体調製ツールは、極性水素原子の追加、水分子の除去、および共結晶化リガンドを含むタンパク質構造に利用されました。タンパク質構造は、デフォルトのパラメーターでエネルギー最小化ツールを使用して最適化され、グリッドボックスは結晶化したリガンドの周りのアクティブなポケットを識別するために使用されました。後で、SnO 2 の方向を指定する10の最良のコンフォメーション 酵素のアクティブポケット内のNPは、それぞれの場合に生成されました。これらの選択された酵素に対する作製されたNPの結合パターンと阻害傾向を明らかにしたさらなる分析のために、最も低い結合スコアのコンフォメーションが選択されました。
SnO 2 構造はICMのligeditツールを使用して生成され、ドッキングされたコンフォメーションの3DビューはICMとディスカバリースタジオビジュアライザーを介して生成されました[48]。
材料の特性評価
BRUKER D2 Phaser X線回折(XRD)の範囲は2 θです。 =10°–70°(CuKα(λ) =1.540Å)を使用して、格子構造を調べ、相構成に関するデータを取得しました。合成された生成物の官能基は、PerkinElmerフーリエ変換赤外(FTIR)分光計によって評価されました。 JEOL JSM-6610LV電界放出型走査電子顕微鏡(FESEM)とINCAソフトウェアを備えたOxford XMax EDS検出器を使用して、準備したサンプルの形態と元素組成を分析しました。 PhilipsCM30とJEOLJEM 2100F高分解能透過型電子顕微鏡(HR-TEM)を使用して、SAED、HRTEM画像、および格子縞パターンを記録しました。調製した酸化スズサンプルの光学特性は、GENESYS-10S UV-vis分光計を介して300〜800nmで記録されました。
結果と考察
図5(a)は、さまざまな温度で合成およびアニールされた酸化スズサンプルから得られたXRDスペクトルを示しています。相組成分析では、デバイとシェラーの関係でCuKα放射を使用しました。\(D =K \ lambda / \ beta {\ mathrm {Cos}} \ theta \)ここで、λ =1.54Åおよび k =0.9を使用して、材料の結晶子サイズを計算しました。 250°Cでは、XRDパターンは2θ値が29.12°(112)、31.60°(020)、33.57°(113)、40.15°(023)、45.54°(024)、51.35°(222)、64.57のピークを示しています。 °(225)これらはすべてSnO斜方晶相(JCPDS:01–077-2296)に起因します。 26.66°(112)で記録された1つのピークのみがSnO 2 に属します 斜方晶構造(JCPDS:01–078-1063)。サンプルを500および750°Cでアニーリングすると、SnOに関連する回折ピークが消失し、得られた生成物は斜方晶系SnO 2 として識別されました。 JCPDSファイルNo.01-078-とよく一致する結晶面24.81°(110)、29.12°(113)、31.23°(020)、41.59°(211)、46.90°(117)、59.57°(135) 1063 [49]。観察されたXRDの結果は、準備された材料が最初に250°CでSnOに酸化されたことを示しています。その後、500°C以上で、SnO 2 に完全に変換されました。 [50]。結果はまた、サンプルの結晶化度が温度の上昇とともに向上したことを示しています。さらに、250°Cと750°Cでアニールされたサンプルから得られたSAEDパターンは、それぞれ図5b、cに示すように明るいスポットリングを示しています。格子面(020)、(023)、(024)、(112)で分析されたパターンは、斜方晶系SnOに割り当てられ(図5b)、(020)、(110)、(117)、(135)の回折面はSnO 2 に起因 それぞれ250°Cと750°Cでアニールされたサンプル用のナノマテリアル(図5c)。製品の結晶性は、XRDの観察結果と一致するSAED画像によっても確認されました。
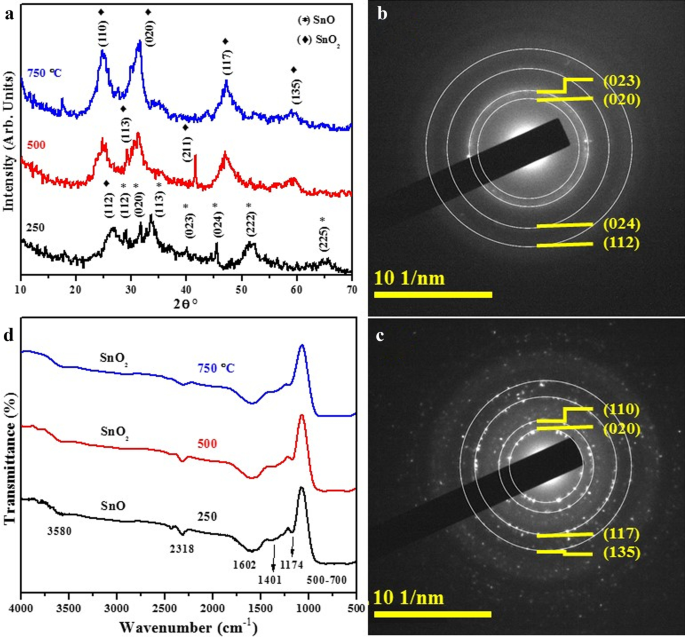
a 250、500、750°CでアニールされたSnOから得られたXRDスペクトル b 、 c それぞれ250°Cと750°CのサンプルのSAEDリング、および d FTIRパターン
250、500、および750°Cで加熱された製造された酸化スズナノ材料のFTIRスペクトルを図5dに示します。約3580cm -1 を中心とする吸収ピーク ほぼ1602cm -1 バンドは、酸化スズが周囲の大気から一定量の水を吸収するという事実のために、O–H基とSn-OH結合の伸縮/屈曲に起因していました[51]。低吸収ピークは2300〜2400 cm -1 の範囲でした 大気にさらされたときに生成物に生成された二酸化炭素に割り当てられます[52]。 1174 cm -1 に現れる結合 さまざまな種類の表面ヒドロキシル基の振動に対応し、1401 cm -1 でピークになります これはC–H曲げ振動によるものです[53、54]。特徴的なピークは500〜700 cm -1 の範囲でした 表面層のSn–O振動に起因します[55]。アニーリングされた温度の上昇は、ピークの青方偏移を引き起こしますが、特徴的なピークはより強く、より強く見えます。これは、ナノ材料の原子がナノ粒子原子の位置を変えるのに十分なエネルギーを獲得して再結晶化するアニーリングプロセスが原因である可能性があります[56]。
FESEMおよびHRTEM分析は、製造された製品の形態およびナノ構造の詳細な情報を収集するために実行されました。図6a〜cに示すように、250、500、および750°Cでアニールされた酸化スズのHRTEM画像が記録されました。これらの画像は、ほぼ球形で粒子サイズがランダムに分布しているナノ粒子内に凝集が形成されている証拠を示しています(図6a、cを参照)。図6bでは、大きなサイズで、わずかに透明で、凝集の少ない単分散粒子が観察されました。粒子分布の同じ振る舞いは、高倍率の挿入画像から観察することができます。 500°Cでの形態学的挙動の急激な変化が顕著です。この温度は、酸化プロセス中の特徴的な特徴である可能性があります[22]。さらに、図6d–fは、平面間距離を検出するために、それぞれ250、500、および750°Cでアニールされたサンプルから得られたHRTEM顕微鏡写真を示しています。結晶子では、SnOの斜方晶相の(023)回折面に対応する図6dの挿入IFFTプロファイル画像に示されているように、格子縞の間隔は〜0.225 nmです(JCPDS:01-077-2296)。 500および750°Cで処理されたサンプルの格子縞から計算されたd間隔は、約0.364および0.367 nmであり、SnO 2 の(110)面に起因します。 JCPDSNOによる斜方晶構造。 01-078-1063。これらの結果は、XRDの結果とよく一致しています[49、57、58]。提供されたIFFT画像は、温度の上昇に伴うd間隔の増加を明確に示しています。
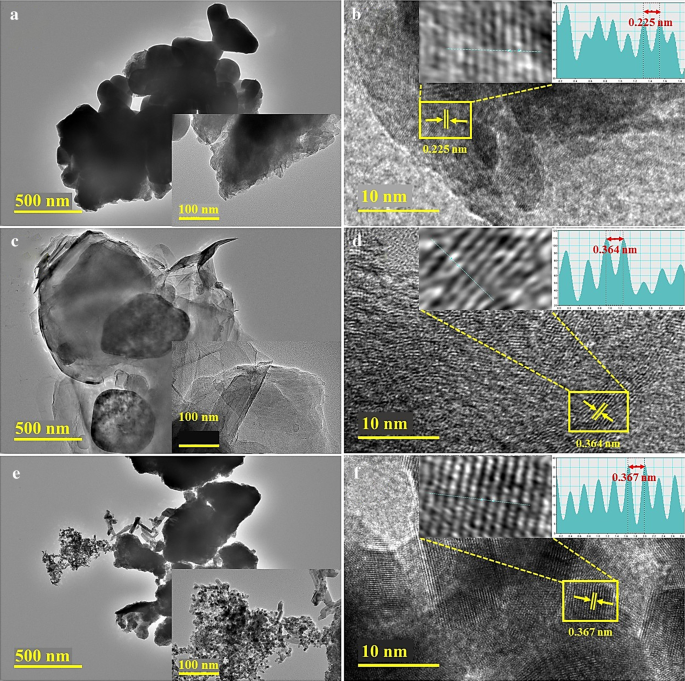
a – c HR-TEMおよび d – f それぞれ250、500、750°Cのアニーリング温度で得られたナノ構造の格子縞
250°C(図7a)および750°C(図7b)でアニールされた酸化スズのFESEM画像は、凝集に伴う大小の個々の粒子を含む粒子の不均一またはランダムな形状など、格子構造の形状とサイズの変化を示しています。 。図7bは、750°CでアニールされたサンプルのFESEM顕微鏡写真を示しています。これは、粒子がランダムに分布している低温でアニールされたサンプルと比較して、小さな凝集粒子と十分に成長した構造を示しています。粒子の凝集は、それらのサイズの増加による表面自由エネルギーの減少をもたらし、それらの表面積の減少をもたらす。ナノ粒子の凝集は、(サブ)ミクロンサイズのエンティティにつながる弱い力による粒子の相互の付着によるものです。 [59]。
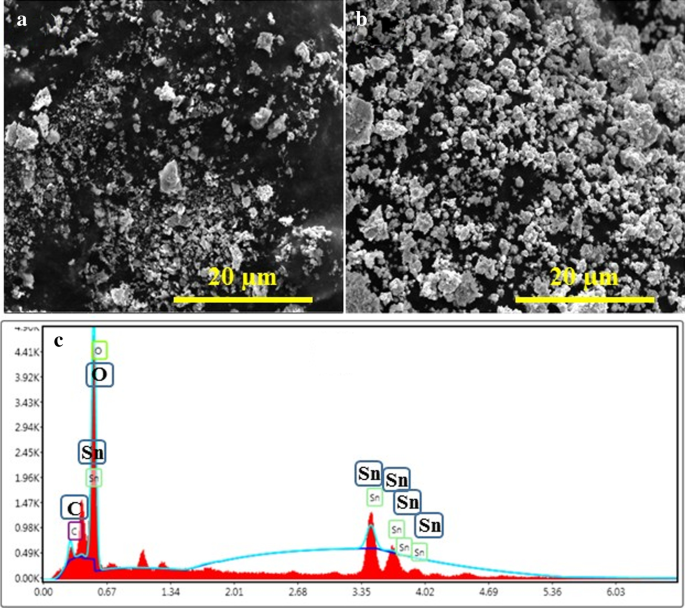
a でアニールされたサンプルからのFESEM顕微鏡写真 250および b 750°Cおよび c 750°CでアニールされたサンプルからのEDXスペクトル
図7cに示すように、750°Cでアニールされた製造された酸化スズの組成をEDX技術で分析しました。サンプルスペクトルは、重量%がそれぞれ53.7、42.2、4.0%のSn、O、Cの存在を明確に示しました。製品には不純物成分が含まれておらず、SnO 2 の純度が高いことが示唆されました。 ナノマテリアル、C含有量は、サンプルを保持するために使用されるカーボンタブに由来する可能性があります。
非破壊吸収分光法を使用して、導電性および半導体性ナノ材料の光学特性を研究しました。さまざまな温度でアニールされた酸化スズから得られた吸収スペクトルを図8aに示します。酸素欠乏、エネルギーバンドギャップ、不純物の性質、表面粗さなど、いくつかの要因が予想される吸光度に影響を与えます。アニールされた酸化スズから得られたスペクトルは、300〜365 nmで紫外線カットオフを示しました[60]。これは、価電子帯から伝導帯への電子の光励起が原因である可能性があります。図8aに示すように、吸収スペクトルは温度の上昇とともに300〜365nmの間でわずかに減少しました。バンドギャップを計算するには、Tauc関係\(\ alpha h \ nu =A {(h \ nu- {E} _ {\ mathrm {g}})} ^ {n} \)ここで、α 吸収係数の略で、 A n の間、定数を表します 直接バンドギャップの場合は=1/2。 \({(\ alpha h \ nu)} ^ {2} \)対hνプロットの外挿により、光学バンドギャップ値 E が得られます。 g (図8b)。測定されたバンドエネルギーは、250、500、および750°Cでアニールされたサンプルでそれぞれ3.51、3.32、および3.71 eVでした[61、62]。製品のバンドギャップは、文献で報告されている値と一致しています[61]。全体として、温度が上昇すると、ナノ粒子の原子はより多くのエネルギーを獲得して再結晶の位置を変更し、形態を変化させ、粒子サイズを縮小します(HRTEMデータから分析できます)。粒子サイズが小さくなると、バンドギャップ値が増加します。これは、通常の量子閉じ込め効果に起因します。同様の傾向がマリクらによって観察されました。 [63]。 500°Cでアニールされたナノ材料によって示される最も低いバンドギャップは、ユニークなナノ構造または多結晶酸化スズのアモルファス合成、および赤方偏移を生成する酸素空孔の生成に起因していました。 Taucモデルは、アモルファスまたは無秩序な表面半導体は、より低いバンドエネルギーで局所的なバンドテール状態を持っていると述べています[64]。
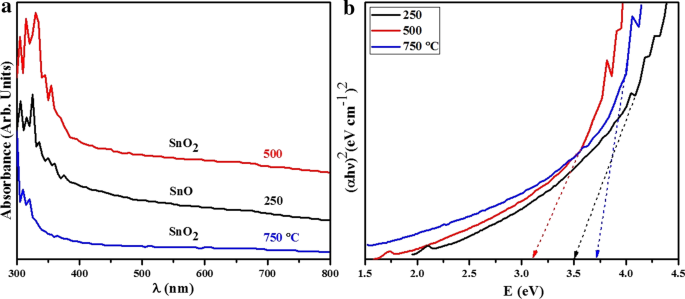
a UV-Vis吸光度スペクトルと b それぞれ250、500、750°Cでアニールされたサンプルから得られたエネルギーギャップ値
さまざまな温度でアニールされた酸化スズ製品の光活性を、光照射下でMB色素の光分解を行うことによって調べました(図9)。 λでのMB溶液の吸光度の変動 max =光分解中の665nmを図9aに示します。作製したサンプルを追加すると、MB吸収帯が時間とともに減少します。最大の光触媒性能は、500°C( E )でアニールされたサンプルによって示されました。 g =3.32 eV)これは、特定の形態と低い電子正孔再結合率に起因します。 250、500、750°Cで80分でアニーリングして調製した酸化スズ光触媒による86.0、92.4、71.6%のMB劣化が観察されました(図9b)。半導体材料の光活性は、MB劣化プロセス中に光生成された電子正孔対の酸化還元電位に影響を与えるバンドギャップエネルギーにも関係しています。ここでテストした3つのサンプルの中で、500°Cでアニールされた光触媒は最低のバンドギャップエネルギー(3.32 eV)を示しましたが、この製品によって示される大幅に向上した劣化率は、図9bに示すようにその独特の構造と高度な凝集によるものです。疑似一次色素分解は、ln( C o / C )対照射時間プロット:ln( C o / C )= kt 図9cに示すように、 k 速度定数、 C を示します o Cは、それぞれ染料の初期濃度と最終濃度(MB)を表します[63、65、66、67]。 500°Cで調製されたナノ材料を使用したkの値は0.59分 -1 250および750°Cで合成されたサンプルの大幅な減少が約0.50および0.31分 -1 で観察されました。 、それぞれ(図9d)。
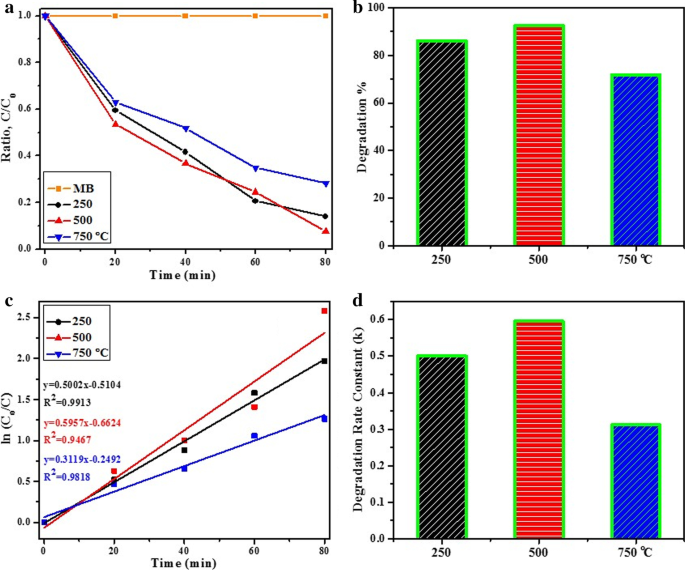
a 作製した光触媒が示すMB劣化の結果 b 劣化%棒グラフ c ln(C o / C)対照射時間プロットおよび d 計算された劣化速度定数グラフ
汚染された水を処理するために、光触媒は、プロセスを経済的に実現可能にするために、長期間にわたって安定性と再利用性を示す必要があります。本研究では、製造された酸化スズ光触媒を使用してMBを除去するために、4サイクルのテストを実行して、それらの安定性を判断しました。色素分解の4つの連続したサイクルの観察結果を図10a、bに示します。 500°Cでアニールされたナノマテリアルは、4サイクル後にMB光分解のわずかな減少を示しました(6%の減少)。この研究で報告された水からの汚染物質除去の結果は、Prakashらによって報告された結果と同等です。 [65]。
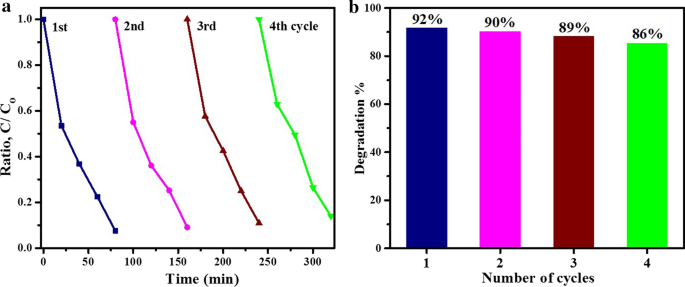
a 500°Cおよび b でアニールされた酸化スズ光触媒の再利用性 劣化率棒グラフ
さまざまな温度処理で製造されたSnOナノ構造を、阻害ゾーン(mm)と比較有効性%ageの観点から測定したin vitro抗菌活性を、図11a〜dと表1に示します。グラフは、ナノ構造濃度と阻害ゾーンの直接的な比率を示しています。形成された。 EのSnO(250、500、および750°C)サンプルで記録された重要な抑制ゾーン。コリ および S。アウレウス 低濃度と高濃度で、それぞれ2.85〜3.5 mm、3.35〜3.75 mm、3.25〜4.75 mm、4.55〜5.35 mmの範囲でした(図11a、b、表1)。合成されたナノ材料の有効率は67.0〜82.3から増加しました。 Eの場合は78.8〜88.2%になります。コリ 同様に、 Sの場合は45.4〜66.4%および63.6〜74.8%です。アウレウス 、それぞれ、図11c、d。すべての測定結果をDIW(0 mm)と比較しました。ポジティブコントロールは、 Eの4.25mmおよび7.15mmの抑制ゾーンを示しています。コリ および S。アウレウス 、それぞれ、図11a、b。全体的なSnO 2 500°Cで最適化されたナノ構造は、両方の濃度でより強力であり、より広く、SnO 2 グラム陰性菌(G –ve) Eに対してより強力であることがわかりました。コリ グラム陽性(G + ve) Sと比較。アウレウス 。
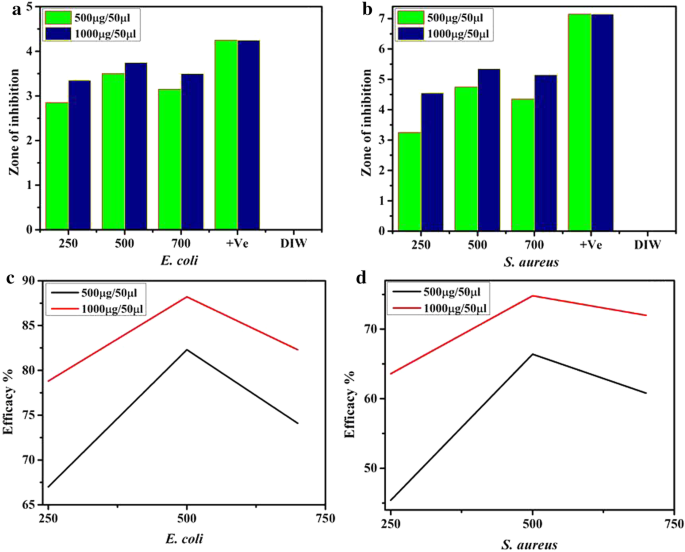
a Eのために異なる温度でアニーリングされたSnOのinvitro殺菌作用。コリ b S。アウレウス c Eのために作製されたNPのinvitro殺菌効果%年齢。コリ (d) および S。アウレウス 、それぞれ
ナノ構造のサイズ、濃度、および形態は、生成される酸化ストレスに直接影響します。サイズと濃度を阻害する抗菌活性は、サイズと反比例の関係を示します[68,69,70]。ナノ構造は、細菌の膜に存在する活性酸素種(ROS)をより効率的に生成し、細胞小器官の押し出しと細菌の死をもたらします[71]。 SnO 2 過酸化水素(H 2 )を含むROSをより効率的に生成します O 2 )、OH基およびスーパーオキシドイオン[72]。 Eの様々な温度処理での製造されたSnOの抗菌効果の増加。コリ Sと比較して。アウレウス 細菌の細胞壁構造の違いに起因する可能性があります。 G –veバクテリアの細胞壁は、タンパク質とリン脂質を含む外膜を備えたペプチドグリカンの薄層で構成され、G + veの細胞壁は、リポテイコ酸とテイコ酸を含むペプチドグリカンの厚い層を含みます。両方の細菌の細胞壁構造におけるこの大きな違いは、G + ve細菌と比較してG-veに向けて作製されたナノ構造の最大の有効性につながります[18]。
さまざまな抗生物質に対する微生物病原体によって獲得された耐性、特に多剤耐性は、世界中の公衆衛生に大きな脅威をもたらし、新しい作用機序を備えたより多くの抗生物質が緊急に必要とされています[73]。さまざまなクラスに属する抗生物質は、細菌の生存に不可欠なそれらの活性と標的経路について異なるメカニズムに従います。たとえば、ペプチドグリカン合成に関与するペニシリン標的酵素などのベータラクタム抗生物質(すなわち、細胞壁合成の重要な前駆体)[74]一方で、よく知られている抗生物質標的酵素であるリファンピシンは、核酸生合成経路[42]に属し、新しい抗生物質発見の標的としての細胞壁と核酸生合成経路の両方[75]。さまざまなナノ粒子の殺菌活性が近年報告されていますが、それらの作用の正確なメカニズムはまだわかっていません[76、77]。 SnO 2 の優れた抗菌活性を視野に入れて Eに対して。コリ および S。アウレウス 、分子ドッキング研究を実施して、βに対する可能な作用機序を特定しました。 -潜在的なターゲットとしてのラクタマーゼおよびDNAジャイレース酵素。
βの場合 - Eからのラクタマーゼ。コリ 観察された最高の結合スコアは-5.71kcal / molで、図12a、bに示すように、Gln35との金属接触相互作用に加えてLys239(1.80Å)およびGly235(1.66Å)との水素結合相互作用を示しています。同様に、 EからのDNAジャイレースについて得られた最高の結合スコア。コリ 図12c、dに示すように、Thr163(1.46Å)、Gly77(1.43Å)、およびGlu50(3.36Å)との水素結合相互作用と、Gly75との金属接触相互作用を有する-9.57 kcal / molでした。
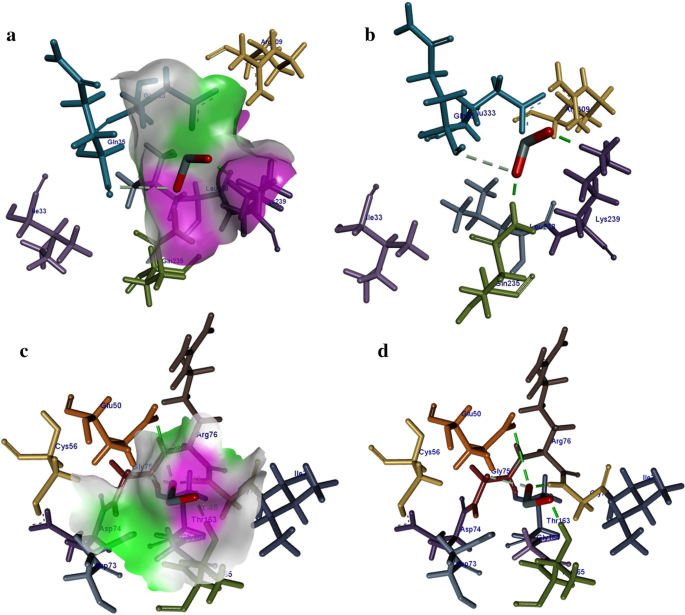
a 、 b SnO 2 の結合相互作用パターン βの活性部位残基を持つナノ粒子 -ラクタマーゼと c 、 d EからのDNAジャイレース。コリ
βで得られた最高の結合スコア - Sのラクタマーゼ。アウレウス -11.83 kcal / molでした。 SnO 2 の結合パターン アクティブポケットの内側には、Ser400(2.16Å)、Gly522(1.99Å)、Ileu524(1.90Å)との水素結合相互作用が含まれていました。さらに、SnO 2 間で金属接触相互作用が観察されました。 図13a、bに示すようにGln521。 SのDNAジャイレースの場合。アウレウス 得られた最良のコンフォメーションは、結合スコアが-8.61 kcal / molのGly85(2.55Å)およびThr173(1.54Å)との水素結合相互作用を示しました(図13c、d)。
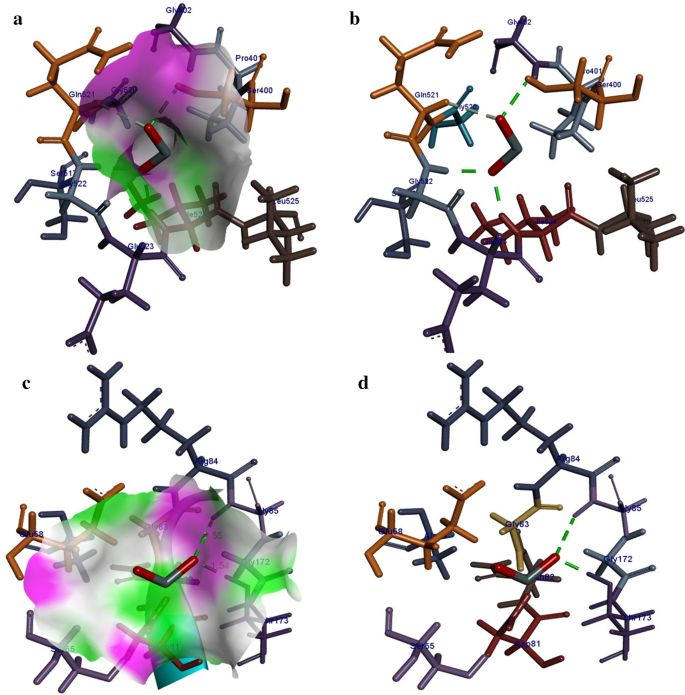
a 、 b SnO 2 の結合相互作用パターン βの活性部位残基を持つナノ粒子 -ラクタマーゼと c 、 d SからのDNAジャイレース。アウレウス
結論
要約すると、さまざまな温度でアニールされた酸化スズナノ粒子は、簡単で単純な沈殿プロセスによって合成されました。合成中に250°Cでサンプルをアニーリングすると、主に斜方晶系のSnOが生成され、SnO 2 に変換されました。 500および750°Cで。 XRDおよびHRTEM分析により、ナノ粒子は斜方晶構造を持っていることが明らかになりましたが、粒子サイズは、温度が500°Cに上昇すると最初は増加し、続いて750°Cで減少しました。 500°Cでの大きな粒子サイズは、その温度でアニールされたサンプルによって示される独特の構造に起因していました。製造されたナノ構造は、凝集とともに十分に結晶化された挙動を示した。モデル有機汚染物質として使用されたMB色素を分解することにより、アニールされた酸化スズナノ材料の光活性を評価し、アニールされたサンプル間の比較を実現しました。 500°Cで合成された製品は、MBの分解中に250°Cでアニーリングされたサンプルと比較して6%高い活性を示しました。この研究で達成された最大MB劣化は、500°Cのサンプルによる80分の照射時間後に92%でした。ラジカル(* OH 1- および* O 2 − )と穴は、光触媒プロセスの主要なアクティブエンティティです。インシリコの予測は、SnO 2 のinvitro殺菌活性とよく一致しています。 NP。 SnO 2 の分子ドッキング研究 選択された酵素、つまりベータラクタマーゼとDNAジャイレースに対するNPは、これらの酵素の活性を妨げる傾向があることを示唆しており、酵素阻害アッセイの研究を通じてさらに調査および確認する必要があります。
データと資料の可用性
すべてのデータは制限なしで完全に利用可能です。
略語
- EDS:
-
エネルギー分散型X線分光法
- FTIR:
-
フーリエ変換赤外分光法
- G + ve:
-
グラム陽性
- G −ve:
-
グラム陰性
- HR-TEM:
-
高分解能透過型電子顕微鏡
- JCPDS:
-
粉末回折基準に関する合同委員会
- NP:
-
ナノ粒子
- SnO:
-
酸化スズ
- UV–Vis:
-
紫外可視分光法
- XRD:
-
X線回折
ナノマテリアル
- 回路とネットリストの例
- ポリマーナノ構造上のU2OS細胞におけるアクチンと接着斑組織の分析
- セリウムのダイヤモンドカッティングの分子動力学モデリングとシミュレーション
- invitroおよびinvivoでのグラフェンおよび酸化グラフェンのバイオセーフティおよび抗菌能力
- 中空構造LiNb3O8光触媒の調製と光触媒性能
- 蒸発誘起自己組織化と強化されたガス検知特性によるワームホールのようなメソポーラス酸化スズの容易な合成
- Cu2ZnSnSe4ナノプレートのワンポット合成とそれらの可視光駆動光触媒活性
- 銀ナノ構造の合成方法と応用における最近の進歩
- ニオブ酸スズ光触媒の操舵電荷速度論:相構造と電子構造の重要な役割
- 新規SrTiO3 / Bi5O7Iナノコンポジットの製造と光触媒特性
- 酸化亜鉛ナノ粒子の特性と微生物に対するそれらの活性



