分子ドッキング研究で評価された抗生物質耐性菌の有望な殺菌剤としての多濃度Cu:Ag二金属ナノ粒子の開発
要約
本研究は、抗生物質耐性菌に対する有望な抗菌剤として使用するために開発されたCu:Agバイメタルナノ粒子内のさまざまな濃度のAgの影響を評価することに関するものです。ここでは、1:0.025、1:0.050、1:0.075、および1:0.1とラベル付けされた一定量のCu中のAgのさまざまな濃度比(2.5、5.0、7.5、および10 wt%)のCu:Agバイメタルナノ粒子が合成されました。溶媒として水酸化アンモニウムと脱イオン水、キャッピング剤としてポリビニルピロリドン、還元剤として水素化ホウ素ナトリウムとアスコルビン酸を使用した共沈法を使用します。これらの配合製品は、さまざまな技術によって特徴づけられました。 XRDは相の純度を確認し、Cu相とAg相に属する明確なfcc構造の存在を検出しました。 FTIR分光法により、さまざまな官能基に対応する振動モードの存在が確認され、バイメタルから発生する特徴的なピークが記録されました。紫外可視分光法により、Ag含有量の増加に伴うバンドギャップの減少が明らかになりました。 SEMおよびHR-TEM顕微鏡写真は、小規模および大規模な凝集を伴うAgドープCuバイメタルの球状形態を明らかにしました。サンプルは、さまざまな寸法と層間間隔を示しました。合成されたCu:AgバイメタルNPの殺菌作用は、統計的に有意であることが示されています( P <0.05)黄色ブドウ球菌に対するさまざまな濃度のAgドーパントについて記録された阻害ゾーン (黄色ブドウ球菌 )、Escherichia coli ( E.coli )、 および Acinetobacter baumannii ( A. baumannii )それぞれ(0.85〜2.8 mm)、(0.55〜1.95 mm)、(0.65〜1.85 mm)の範囲です。概して、Cu:AgバイメタルNPは、グラム陰性菌と比較してグラム陽性菌に対してより強力であることがわかりました。 βに対してAg–CuバイメタルNPの分子ドッキング研究を実施しました -両方の Sからの細胞壁生合成経路の重要な酵素であるラクタマーゼ。アウレウス (結合スコア:− 4.981 kcal / mol)および A。バウミンニー (結合スコア:− 4.013 kcal / mol)。同様に、 Aからの脂肪酸生合成経路に属するFabIに対する結合相互作用分析。バウミンニー (結合スコア:− 3.385 kcal / mol)および S。アウレウス (結合スコア:− 3.012 kcal / mol) EのFabHとともに。コリ (結合スコア:− 4.372 kcal / mol)が実施されました。これらの理論的計算は、選択された酵素の可能な阻害剤としてCu-AgバイメタルNPを示しています。これらの材料のinvitro阻害の可能性を探求することは、抗生物質の発見のための新しい道を開くかもしれないことが示唆されています。
はじめに
バクテリア、菌類、ウイルス、寄生虫からなるさまざまな微生物が地球とその環境の中に存在しています。これらの種は、医療機器、ヘルスケア商品、加工食品、浄水システム、および家庭用衛生製品の製造と使用に問題を引き起こします[1、2]。抗生物質は、人間や動物に病気を引き起こす細菌を殺すために医師によって日常的に使用されています。抗生物質を頻繁に使用することの不利な点は、細菌が時間とともに薬剤耐性になることです。抗生物質は、感染症と戦う体内に存在する「善玉菌」の数を減らすのにも役立ちます。抗生物質耐性菌による感染症に起因する病気は、今日の医学の分野で懸念される主な原因となっています。この点で、多くの細菌が薬剤耐性であることが確認されています[3,4,5,6,7]。薬剤耐性菌の問題に取り組み、現在の抗菌剤をより効率的で補完的な治療法に置き換えるための新しい取り組みが進行中です。この点で、ナノテクノロジーは、金属および金属酸化物NP(つまり、Ag、Cu、CuO、TiO 2 )などのナノ材料の製造に大きく貢献しています。 、SiO 2 、MgO、およびZnO)は、ますます多くの抗菌剤耐性微生物と戦うために使用されます。これらの中で、CuおよびAg NPは、有望な抗菌特性を示しています[8,9,10,11,12]。
近年、バイメタルNPが開発され、化学、材料科学、バイオテクノロジー、環境保護の分野でさまざまな用途に使用されています。表面原子の割合が高く、比表面積が大きい銅(Cu)と銀(Ag)を含むバイメタルNPが広く研究されています[13]。これらのバイメタルNPは、化学的、光学的、触媒的、生物学的、プラズモン的、そして特に抗菌性が強化されているため、非常に興味深いものです[14、15、16、17、18、19、20]。 Agイオンは、800〜1000°Cの大気条件下でエタノールによって還元され、銀NPが得られます[21、22]。銀のNPは優れた抗菌効果を持っているため、日焼け止めクリームの製造や水処理に使用されます[23]。 Cu NPは、マイクロ波照射下でエチレングリコール中の硫酸銅をヒドラジンで還元することによって製造され、抗菌剤としても使用できます[24、25、26]。
CuやAgなどの金属は、個別に有望な光学的、触媒的、構造的特性を持たず、バイメタルに変換することはできません。一方、両方の金属(Cu:Ag)を組み合わせると、結果として得られる製品の構造と形態を目的の用途に合わせて調整する新しい機会が得られます。その最終的な構造、例えば、コアシェル、ダンベル構造、2界面構造、ランダムに混合された構造、または花の形の構造に基づいて、バイメタルNPはさまざまな抗菌活性を示すことができます[27、28、29、30 、31]。共沈法、ゾルゲル法、熱水法、還元法、マイクロエマルジョン法、ポリオール法など、さまざまな方法でバイメタルNPを合成できます[32、33、34、35、36、37]。
この研究では、Cu:AgバイメタルNPを、水酸化アンモニウムと脱イオン水を溶媒として、ポリビニルピロリドンをキャッピング剤として、水素化ホウ素ナトリウムとアスコルビン酸を還元剤として使用する共沈法によって合成しました。さまざまな濃度の4つのサンプルを準備しました。準備されたバイメタルNPのAg濃度が高くなると、サンプルはバクテリア acinetobacter baumannii に対して強化された活性を示しました。 それは発熱と吐き気を引き起こします。合成された材料は、急速な成長中に赤い外観を呈し、抗菌活性がバイメタルNP中のAgの濃度の増加とともに強化されたことを示唆しています。さらに、分子ドッキング研究を使用したインシリコ予測を実行して、βに対するCu:AgバイメタルNPの相互作用パターンを特定しました。 -脂肪酸生合成経路のFabIおよびFabH酵素と並んで細胞壁生合成経路のラクタマーゼ酵素。
メソッド
現在の研究は、抗生物質耐性菌に対する抗菌剤の有効性を調査するために、熱水経路を介してCu:Agバイメタルナノ粒子内でさまざまな濃度のAgを合成することを目的としていました。
資料
塩化銅(II)(CuCl 2 0.2 H 2 O、98.9%)、および硝酸銀(AgNO 3 )前駆体として、キャッピング剤としてポリビニルピロリドン(PVP、平均分子量40,000)、水素化ホウ素ナトリウム(NaBH 4 、99.9%)およびL-アスコルビン酸(C 6 H 8 O 6 、99.0%)還元剤および水酸化アンモニウム(NH 4 OH)は、米国のSigma Aldrichから取得した後、本研究で使用されました。
バイメタルCu:AgNPの合成
バイメタルCu:Ag NPは、図1に示すように、共沈法を使用して調製しました。脱イオン水中に、1.25gのPVPと0.5gのアスコルビン酸を添加し、100°Cで激しく攪拌しました。 40mLの水酸化アンモニウムの2つの溶液を個別に調製しました。一方の溶液では、1.7 gの塩化銅を添加し、もう一方の溶液では、1.7gの硝酸銀を添加しました。次に、これら2つの溶液を、最初に調製した溶液に0.5gのNaBH 4 を加えて次々に注ぎます。 。その後、最終溶液を100°Cで4時間撹拌して均一にし、後で6000rpmで遠心分離してNPを完全に抽出しました。得られたバイメタルNPを100°Cで乾燥させて水分と不純物を完全に除去し、調製したバイメタル製品が純粋な形であることを確認しました[12]。同様に、さまざまなAg濃度(mol 2.5%、5%、7.5%、および10%)の4つのサンプルが、固定されたCu比で準備されました。
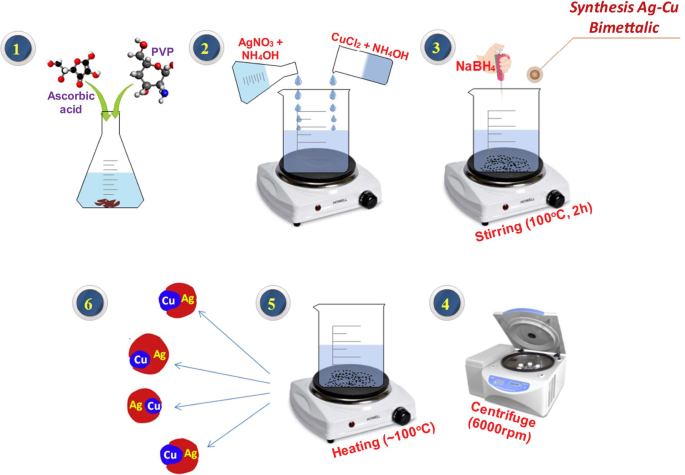
Cu:AgバイメタルNPの合成を示す図
抗菌作用
Cu:AgバイメタルNPのinvitro殺菌能力を病原菌 Sに対して評価した。アウレウス、大腸菌 および A。バウマニ ウェル拡散法を使用してウシ乳房炎乳から得られた分離株。マンニット食塩寒天培地、マッコンキー寒天培地、およびローリアベルタニ寒天培地を、分離された細菌活性化増殖1.5×10 8 で拭き取りました。 CFU / ml。メディアが固化した後、直径15 mm、10マイクロリットル(5 µg / mL)の寸法の黄色いピペットを使用して5つのウェルを準備しました。ポジティブコントロールとして10マイクロリットルのアモキシシリン(5 µg / mL)、ネガティブコントロールとして50 µlのDIWと比較して、新たに調製したCu:AgバイメタルNPをさまざまな比率でウェルにロードしました。合成されたCu:AgバイメタルNPの殺菌活性は、37°Cで15時間のインキュベーション後に形成された阻害ゾーン(mm)を測定することによって決定されました。
統計分析
阻害ゾーン(mm)の測定値を持つ合成NPの殺菌活性は、SPSS 20.0、一元配置分散分析(ANOVA)を使用して統計的に有意であると見なされました[57]。
分子ドッキング研究
抗生物質は細菌の増殖を減少させ、細胞壁の損傷、生化学的プロセスの破壊、細胞膜の損傷、およびバイオフィルムへの浸透を通じて細菌の死を引き起こします[38]。ここ数十年で、潜在的な殺菌活性を持つ多くのナノ粒子が報告されており、細胞壁の破壊または既知の抗生物質と同様のメカニズムによって食物源を遮断することによって細菌を殺します[39、40、41]。したがって、これらの生化学的経路に属する酵素は、抗生物質の発見にとって重要で魅力的な標的であると考えられています[12]。ここでは、細胞壁生合成経路からの重要な酵素(すなわち、β -ラクタマーゼ)および脂肪酸生合成経路(すなわち、FabHおよびFabI)が、Cu:AgバイメタルNPと阻害剤としてのアクティブポケットとの相互作用のメカニズムを評価するための可能なターゲットとして選択されました(図2を参照)。
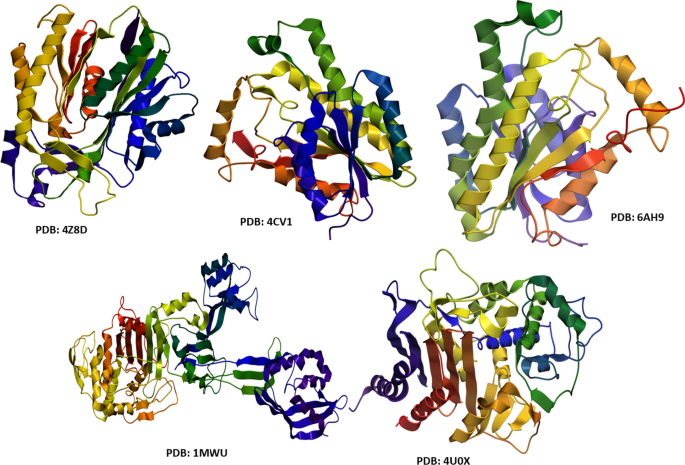
タンパク質ターゲットの3D構造β -ラクタマーゼ、FabI( A. bauminnii から & S。アウレウス )および EのFabH。コリ
選択した酵素の3D構造パラメーターは、PDBコード:βの4U0X(2.03Å解像度)でタンパク質データバンクから取得されました。 -ラクタマーゼ[42]および6AH9; Aのエノイル-[アシルキャリアタンパク質]レダクターゼ(FabI)の分解能1.74Å[43]。バウミンニー 。 β -PDB IDが1MWUのラクタマーゼ(3D構造)。解像度2.6Å[44]およびPDBコードを使用したFabI:4CV1; Sからの解像度1.95 [45]。アウレウス EのFabHの場合。コリ PDBコード:4Z8D;解像度2.0Å[46]。
Cu:AgバイメタルNPの分子ドッキング研究は、ICM Molsoft v3.8–4a以上(Molsoft L.L.C.、カリフォルニア州ラホーヤ)ソフトウェアを使用して行われ、活性部位の重要な残基との結合相互作用を特定しました[47]。 ICMのタンパク質/受容体調製ツールは、選択された酵素ターゲットの最適化と構造調製に使用されました。含まれるステップは、極性H原子の追加、水分子の削除、およびデフォルトパラメータを使用したエネルギー最小化でした。共結晶化したリガンド分子を除去して、NPのドッキングの余地を提供しました。結合ポケットは、結晶化したリガンドの位置を指定するグリッドボックスを使用して定義されました。アクティブポケット内のAg–CuバイメタルNPの相互作用パターンと結合傾向を分析するために、ドッキングされた上位10個のコンフォメーションのうち結合エネルギーが最も低いコンフォメーションがそれぞれの場合に選択されました。 Pymolとdiscoverystudioビジュアライザーソフトウェアは、結合相互作用の分析と3Dビュー描写に使用されました[48]。 Cu:AgバイメタルNPの構造は、PubChemin.sdf形式から取得されました。
特性評価
構造解析と相純度は、XRD(PAN分析X’pert pro XRD)をCu-Kα放射線(λ)と組み合わせることによって観察されました。 =0.154 nm、20°〜80°)。さまざまな官能基に対応する振動モードの存在は、フーリエ変換赤外分光法-パーキンエルマー分光計を備えたFTIRを使用して評価されました。吸収スペクトルは、UV-visible-Genesys10S分光光度計を使用して取得しました。 FESEMとEDS分光計(JSM-6610LV)およびHR-TEM(JEOL JEM 2100F)を組み合わせて、表面形態を視覚化しました。 ICM v3.8-4a以降(Molsoft L.L.C.、カリフォルニア州ラホーヤ)ソフトウェアを分子ドッキング分析に使用しました。
結果と考察
XRD分析は、配合された製品の相の構成と結晶構造を評価するために行われました。図3aは、20°から80°の間にプロットされたXRDパターンを示しています。バイメタルCu:Agでは、〜38.2°、46°、64.4°、および77.1°付近で観測された反射は、JCPDS No. 。04-0783[32、49、50、51、52]。一方、Cuの場合、32.6°、44.2°、51°に現れる回折は、それぞれ(110)、(111)、(200)格子面を示し、fcc構造のCuOと金属Cuの存在を確認しました。 JCPDS No. 04-0836 [32、53,54,55,56]とよく一致します。抽出されたパターンでは、AgとCuの両方のピークが観察されました。これは、AgとCuの両方の相を構成するNPの存在を示しています。さらに、Ag含有量が少ないサンプル(たとえば、1:0.025、1:0.050、および1:0.075)にCuOが存在することは、Cu NPが酸化され、Ag濃度が低いために高温で非保護挙動を示したことを示しています[ 52]。逆に、Ag含有量が最も高い(1:0.1)サンプルでは、CuOピークの強度が低く、部分的に酸化物を含まない生成物が形成されていることを示しています[57]。これは、Agの添加によりバイメタルNPの耐酸化性が向上することを示唆しています[52]。各結晶面は原子密度に基づいてエネルギー的に異なるサイトを含みますが、機器の検出限界内で不純物の追加のピークは検出されませんでした。 CuとAgの両方のNPは、(111)に高い原子密度のファセットを持ち、平面の最大配向を明らかにするのに役立ちました[51、58]。ブラッグの法則を使用すると、AgとCuのd間隔はそれぞれ0.24nmと0.21nmであることがわかりました。これは、両方の元素の異なる平面(111)に対応し、HR-TEMの結果と一致していました(図6)[51、59 、60、61、62]。準備されたバイメタル製品から得られた対応するSAEDリング(図3b–d)は、十分に結晶化された製品を示し、XRDパターンとよく一致する明確なリングパターンを示します。
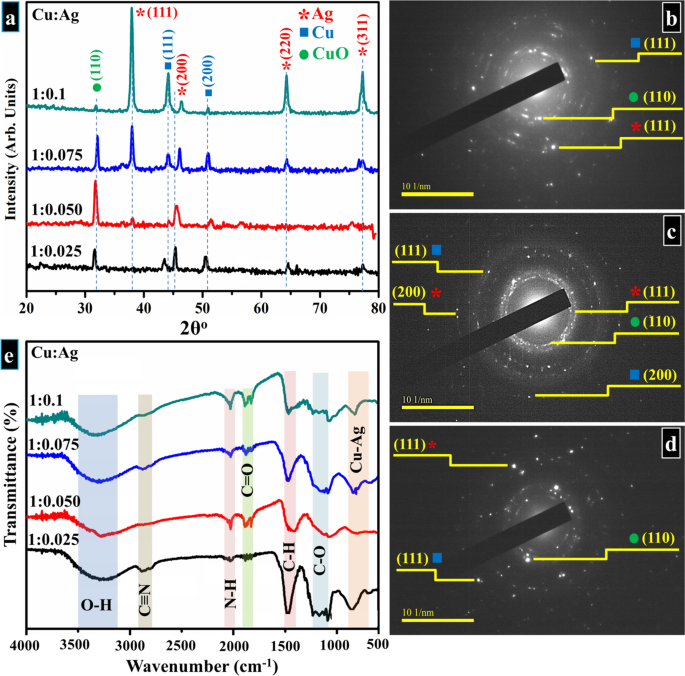
a Cu:AgバイメタルNP、 b から得られたXRDプロファイル – d サンプルのHR-TEMを使用して得られたSAEDリング b 1:0.025、 c 1:0.050、および d 1:0.10、 e 調製したサンプルのFTIRスペクトル
FTIRスペクトルは、500〜4000 cm -1 で記録されました。 図3eに示すように。 600〜900 cm -1 の間に配置された送信帯域 Cu:Ag結合の形成によって引き起こされます[63]。 〜1200および1400 cm -1 付近で観測されたバンド それぞれC–OとC–Hに起因します。 〜1800および2100 cm -1 に現れるピーク PVPとNH 4 によるC =OとN–H結合に対応します OH [64]。 〜2800 cm -1 付近で観測された透過率 および3400cm -1 C≡Nとヒドロキシル基(O–H)の存在に起因します[64]。
図4aは、340、410、および500 nmに明確な吸収帯が存在するAg–CuバイメタルNPの吸収スペクトルを示しています。これは、金属AgおよびCuの表面プラズモン共鳴吸収によるものです[52]。通常、410 nmに現れるバンドは、Ag NPの存在が原因で発生し、510 nmに位置する後者のピークは、Cu NPの存在に起因します[52、57、58、59、65、66、67]。以前に議論されたようにXRDの結果によっても確認されたバイメタルの発達の代わりに、バイメタルのNPが別個のAgおよびCu相で発達することが示唆されるかもしれません[52]。 410 nmでの吸収帯のわずかな赤方偏移と、Ag含有量の増加に伴う最大吸収の増加が観察されました[58]。 Tauc方程式を使用して
$$ [\ alpha h \ nu =K \ left({h \ nu --Eg} \ right)^ {n}] $$(1)ここでα 吸収係数と見なされます[2.303log( T / d )、 T 透過光と d サンプルセルの厚さを示します]、 h プランク定数(6.62607015×10 −34 )を象徴します Js)、\(\ nu \)は光の周波数、 K は吸収指数を示し、 E g eV単位のバンドギャップエネルギーに等しい。 「 n 」の値 」は、バンドギャップの電子遷移タイプに関連しています[13、26、68、69]。図4b–eに示すように、準備されたバイメタル製品のバンドギャップが計算され、3.2、2.9、2.7、および2.6eVであることがわかりました。
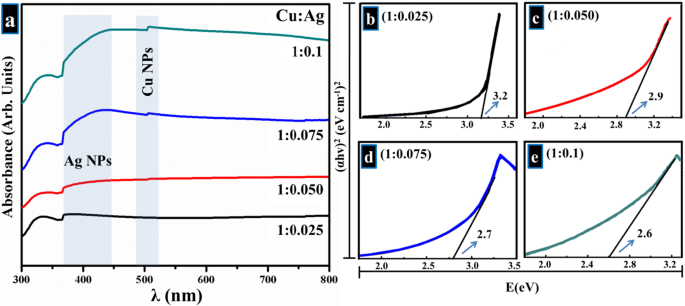
バイメタル b から得られたUV-Visスペクトル – e Taucプロット分析
合成されたままのCu:AgバイメタルナノコンポジットのSEM画像(図5a〜d)から、小さなサイズの粒子が大きな粒子の表面に堆積していることが観察されました。 Ag含有量が2.5%から7.5%に増加すると、さまざまな形態のさまざまな粒子が形成され、最終的には分厚いCu:AgNPになりました。さらに、不均一で小さなAg粒子の蓄積は、ドーパント濃度の増加に伴って増大し、その表面により多くの散乱ブロックが出現することを示唆しています。これは、CuへのAgドーピングが形態に与える主な影響を示しており、HR-TEM顕微鏡写真でさらに確認されました(図5e–hを参照)。

a–d 準備された製品から得られたSEM画像、 e–h HR-TEM顕微鏡写真
準備されたバイメタルの形態とd間隔をさらに詳しく説明するために、10nmの分解能を持つHR-TEMを使用しました。図6aでは、Cu NPのd間隔(0.21 nm)は、XRDの結果(図3a)でも明らかなように、Cuの(111)ファセットに対応しています。図6bは、層間隔のわずかな増加(0.21〜0.22 nm)を示しており、(111)面と一致する0.24nmの面間距離を持つAgNPを示しています。同様に、図6c、dは、計算された層間隔とバイメタルの別々の相を示し、図6eは、AgおよびCuNPの粒子形状を示しています。 HR-TEM画像の粒子はコアシェル構造を持っているように見えます。単一粒子内の図6dでは、CuとAgから発生する格子縞が記録されています。これは、Cu:Ag比が異なるコアシェルバイメタルNPが形成され、不規則な準球形NPが生成されることを強く示唆しています。さらに、TEM画像は粒子が暗くて明るい領域のように見えることを示しました。単一粒子内のコントラストのこの変化は、バイメタルCu:Ag粒子の作成を示唆する2つの異なる構成材料の存在を示している可能性があります[70、71]。

a–d 準備されたすべてのサンプルのd間隔測定用のHR-TEM(10 nm)画像、 e バイメタル粒子を示す低倍率画像
バイメタルに由来するEDSスペクトルと元素組成に明確なピークが存在することで、Cu:AgNPの形成が成功したことが確認されました。図7aは、1:0.050サンプルから得られたEDSスペクトルを表しており、CuとAgの明確なピークを示しています。図7bは、ドープされたサンプルでCとOのピークが検出された1:010サンプルから取得されたものです。これらは、カーボンタブがSEM検査中のサンプルを保持するために使用されているため、および/またはSEM-EDSセンサーのバックグラウンドカウントのために表示されます。
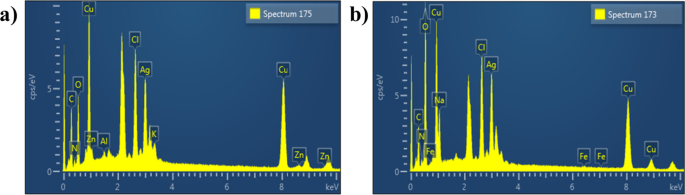
バイメタルNPから得られたEDSプロファイル
寒天ウェル拡散アッセイを使用したCu:AgバイメタルNPのin vitro殺菌効果を表1に示します。結果は、合成NP濃度と阻害ゾーン(mm)の間に直接的な比例関係があることを示しています。統計的に有意( P <0.05) Sに対する(2.5、5、7.5、および10 wt%)Agドーパントについて記録された抑制ゾーン。アウレウス、大腸菌 および A。バウマニ それぞれ0.85〜2.8 mm、0.55〜1.95 mm、0.65〜1.85 mmの範囲でした。表1を参照してください。すべての結果を、それぞれ陰性対照および陽性対照としてDIW(0 mm)およびアモキシシリン(4 mm)と比較しました。同様に、ドープされたNPの有効性%は、 Sに対して(21.2–70%)、(13.7–48.7%)、および(16.2–46.2%)増加しました。アウレウス、大腸菌 および A。バウマニ 、 それぞれ。全体として、Cu:AgバイメタルNPは Sに対してより強力であることがわかりました。アウレウス (つまり、グラム+ ive) Eと比較。コリ および A。バウマニ (つまり、グラム-ive)。
<図>NPのサイズ、濃度、および形状は、ナノ構造によって生成される酸化ストレスに直接影響します。カチオン(++)の利用可能性の増加により、AgドープCuバイメタルNPのwt%ドーピングが増加したため、抑制ゾーン(mm)の形での殺菌効果が向上しました。サイズと濃度に関する殺菌作用は、サイズと逆の関係を示しています[58、59]。ナノサイズの構造は、細菌の細胞膜に存在する活性酸素種(ROS)を効率的に生成し、細胞小器官の押し出しと最終的には細菌の死をもたらします[60]。 ROS生成に加えて、Ag + のカチオン相互作用 およびCu ++ バクテリアの細胞膜の負に帯電した部分を使用すると、細胞溶解とバクテリアの崩壊により、濃度を上げると殺菌効果が向上します[58、61]。
さまざまなクラスのナノ粒子の生物学的応用は、過去数十年以来広く研究されてきました。 NPの独自の特性により、従来の抗生物質を代替する能力を備えた殺菌剤としての可能性のために広く利用されてきました。 NPは細菌細胞と相互作用し、細胞膜の透過を妨害し、重要な代謝経路を破壊します[72]。細菌に対するナノ粒子毒性の特定のメカニズムを調査する必要があります。 NPは、静電力、ファンデルワールス力、または疎水性相互作用を伴う細菌細胞と相互作用し、最終的に細菌を死に至らしめると考えられています。酵素は、細菌感染に関与する主要な病原性因子として報告されており、それらの活性を阻害するようにそれらを標的にして、引き起こされた感染に取り組むのを助けます[73]。ここでは、脂肪酸生合成経路に沿った細胞壁の酵素標的に対するCu:Ag NPの分子ドッキング研究により、アクティブポケット内のこれらのNPの結合相互作用パターンが特定されました。 Aに対するこれらのNPのinvitro抗菌能を視野に入れておく。バウミンニー 、 S。アウレウス および E。コリ 、これらの微生物から酵素標的を選択して、殺菌活性の背後にある考えられるメカニズムについての洞察を得ました。
βを含むCu:AgバイメタルNPの場合に観察される最良のドッキングコンフォメーション - Aからのラクタマーゼ。バウミンニー ドッキングスコアが-4.013kcal / molであるのに対し、Glu272(2.8Å)およびSer286(3.2Å)との水素結合相互作用とVal292との金属接触相互作用が明らかになりました(図8a)。同様に、βに対して観察されたAg–CuバイメタルNPの結合スコア - Sからのラクタマーゼ。アウレウス 図8bに示すように、Ser403(3.2Å)、Tyr519(3.6Å)、Gln521(3.0Å)、Asn464(3.1Å)との水素結合相互作用を有する− 4.981 kcal / molでした。
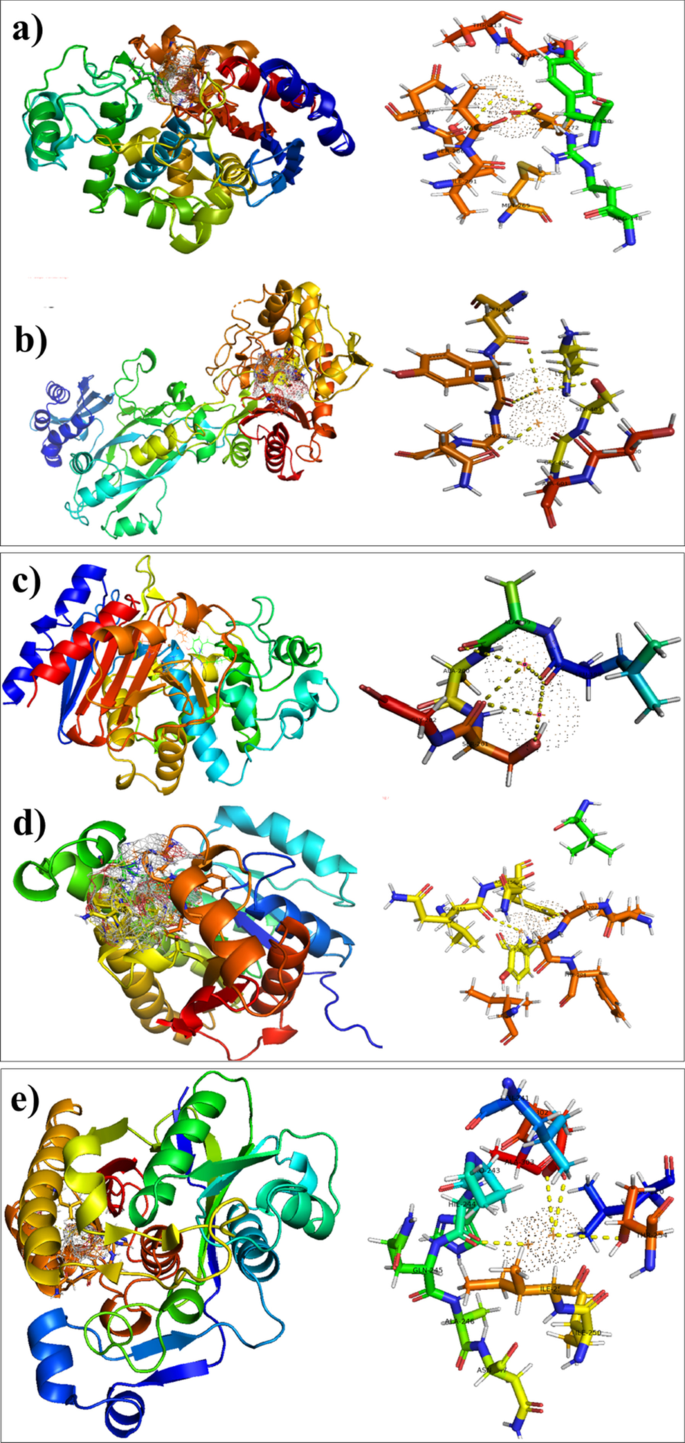
アクティブポケット内のAg–CuバイメタルNPの結合相互作用パターン。 a β - Aからのラクタマーゼ。バウミンニー 、 b β - Sからのラクタマーゼ。アウレウス 。 c 、 d アクティブポケット内のAg–CuバイメタルNPの結合相互作用パターン c Aからのエノイル-[アシルキャリアタンパク質]レダクターゼ(FabI)。バウミンニー 、 d Sからのエノイル-[アシルキャリアタンパク質]レダクターゼ(FabI)。アウレウス 、 e EからのFabHのアクティブポケット内のAg–CuバイメタルNPの結合相互作用パターン。コリ
現在の研究で選択された2番目の酵素標的FabIは脂肪酸生合成経路に属し、分子ドッキング予測は、この標的に対する潜在的な阻害剤としてCu:Ag二金属NPを示唆しました。 Cu:AgバイメタルNPは、 AのFabIに対して良好な結合スコア(-3.385 kcal / mol)を示しました。バウミンニー 図8cに示すように、Ser201(2.7Å)、Ala199(3.5Å)、およびLeu198(3.3Å)と水素結合しています。同様に、 SのFabIの活性部位を持つAg–CuNPの最良のドッキングコンフォメーション。アウレウス 結合スコアが-3.012kcal / molのGly202(2.5Å)およびGln155(2.5Å)との水素結合を示しました(図8d)。
さらに、 E.coli のFabHに対するCu:AgバイメタルNPの結合能力 も評価され、観察された結合スコアは-4.372 kcal / molで、図8eに示すThr254(3.5Å)、HIE244(2.6Å)、およびGlu302(3.0Å)と水素結合相互作用があります。
結論
Cu:Agバイメタルナノ粒子は、細菌関連の病気と戦うためのアプリケーションで使用するために、共沈法によって調製されました。 XRDプロファイルにより、fcc構造のCuOと金属のCuおよびAg粒子の存在が確認されました。 AgとCuの両方のピークが観察されました。これは、AgとCuの相を伴うバイメタルNPを意味します。 XRD分析で観察された平面は、SAEDリングによく対応しています。配合された製品と600〜900 cm -1 の特徴的な透過率バンドを持つ結合化学基 Cu:Ag結合の形成によって引き起こされました。プロットされたUV-visのスペクトルは、通常AgNPの存在が原因で発生する410nmでの吸収を示し、510nmに位置する後者のピークはCuNPの存在に起因していました。 HR-TEM画像の粒子はコアシェル構造を持っているように見えました。 Cu:Ag NPは、異なるCu:Ag比のバイメタルNPの形成を明確に示し、不規則な準球形NPを生成しました。さらに、Cu NPのd間隔、つまり0.21 nmは、XRD結果で検出されたCuの(111)ファセットに対応します。層間隔のわずかな増加(0.21から0.22 nm)は、0.24nmの層距離を持つAgNPが(111)面と一致していることも示しています。分子ドッキング研究は、invitro殺菌活性との良好な一致を示しました。 βに対するCu:AgバイメタルNPの結合傾向 -脂肪酸生合成経路のFabIおよびFabH酵素と並んで細胞壁生合成経路のラクタマーゼ酵素は、酵素阻害研究を通じてさらに調査する必要がある阻害の可能性を示しました。
データと資料の可用性
すべてのデータはオンデマンドで完全に利用できます。
略語
- EDS:
-
エネルギー分散型X線分光法
- FTIR:
-
フーリエ変換赤外分光法
- G + ve:
-
グラム陽性
- G −ve:
-
グラム陰性菌
- HR-TEM:
-
高分解能透過型電子顕微鏡
- JCPDS:
-
粉末回折標準に関する合同委員会
- Ag:
-
シルバー
- UV–Vis:
-
紫外可視分光法
- XRD:
-
X線回折
ナノマテリアル
- 化学療法センサー用の金ナノ粒子
- 化学センシング用の貴金属ナノ粒子で装飾されたエレクトロスピニングポリマーナノファイバー
- 非常に効果的な標的膵臓腫瘍治療のための、血液循環が延長され、生体適合性が改善されたレスベラトロール負荷アルブミンナノ粒子
- ポリ(4-スチレンスルホン酸-co-マレイン酸)による金磁性ナノ粒子の安定性の向上:タンパク質検出用に調整された光学特性
- 分子動力学法によるアブレシブナノメートル切削プロセスに及ぼす衝撃方向の影響の研究
- 抗菌剤として銀ナノ粒子で装飾された酸化グラフェンベースのナノコンポジット
- Auナノ粒子で調整されたシリカ珪藻殻により、生物学、安全、環境アプリケーション向けの分子の高感度分析が可能になります
- 非常に濃縮された亜鉛源を用いた水/グリセロール中のナノサイズの酸化亜鉛の調製のための簡単なアプローチ
- トランスフェリン受容体による細胞内在化が増強されたパクリタキセルベースの標的脂質ナノ粒子の抗増殖およびアポトーシス誘発能—白血病細胞での研究
- Fe3 +イオンの高効率検出のためのAgナノ粒子を備えた十分に整列したTiO2ナノチューブアレイ
- 高い触媒活性と耐水性を備えたCO酸化とメタン燃焼のためにPdOナノ粒子で修飾されたロッド状のナノポーラスCeO2



