酸化スズナノ粒子のグリーンで費用効果の高い合成:合成方法論、形成のメカニズム、およびそれらの潜在的な用途に関するレビュー
要約
ナノテクノロジーは、科学のすべての分野でその重要な応用により、最も有望な研究分野になりました。近年、酸化スズはその魅力的な特性により大きな注目を集めており、ナノメートル範囲でこの材料を合成することで改善されています。酸化スズナノ粒子を製造するために、最近、多くの物理的および化学的方法が使用されています。しかし、これらの方法は高価であり、高エネルギーを必要とし、合成中にさまざまな有毒化学物質を利用します。人間の健康と環境への影響に関連する懸念の高まりは、その生産のための費用効果が高く環境に優しいプロセスの開発につながりました。最近、酸化スズナノ粒子は、植物抽出物、細菌、天然生体分子などのさまざまな生物学的実体を使用したグリーン法によって首尾よく合成されています。しかし、グリーン合成アプローチを使用した工業規模の生産は、合成中に発生する反応と形成のメカニズムの解明を困難にする生物学的基質の複雑さのために、依然として課題となっています。したがって、本レビューは、酸化スズナノ粒子のグリーン合成に使用される生物学的実体と方法論のさまざまなソースとそれらの特性への影響をまとめたものです。この研究では、文献で報告されている形成メカニズムの理解の進歩と、これらのナノ粒子の特性評価に使用されるさまざまな分析技術についても説明しています。
はじめに
過去数十年の間に、ナノテクノロジーは、薬剤学、食品産業、化粧品、繊維産業、医学、光学、電子機器、エネルギー科学および電気化学アプリケーション[1,2,3,4]。ナノマテリアルは、1〜100nmのサイズ範囲で1つの寸法を持つマテリアルです。これらの材料の表面積対体積比が非常に大きく、サイズが非常に小さいと、バルク材料と比較して、電気的、光学的、磁気的、触媒的、および抗菌性の活性が完全に新しくなるか、向上する可能性があります[5、6、7]。これらのユニークな特性により、ナノ粒子は、ナノメディシン、光触媒、バイオセンサー、洗浄剤、繊維産業など、現代の科学と工学のさまざまな分野で応用されています[1,8]。ナノ粒子の中で、酸化スズ(IV)(SnO 2 )特に、オプトエレクトロニクスデバイス[9]、固体ガスセンサー[10]、リチウムイオン電池用電極[11]、電界放出ディスプレイ[12]、発光ダイオードなどの用途が広いため、大きな注目を集めています。 [13]、触媒作用[14]、染料ベースの太陽電池[15]、薬[16]、光センサーおよび帯電防止コーティング[17]。
材料科学では、SnO 2 は酸素不足のn型半導体と見なされ、格子定数 a の正方晶ルチル構造として結晶化します。 = b =4.7374Åおよび c =3.1864Å。ユニットセルは、2つの6倍に配位したスズと4つの3倍に配位した酸素原子で構成されています[18、19]。広いエネルギーギャップ(3.6〜3.8 eV)、強力な熱安定性(最大500°C)、可視スペクトルの高度な透明性、吸着種との強力な化学的および物理的相互作用により、SnO 2 > リチウムイオン電池、センサー、触媒作用、エネルギー貯蔵、ガラスコーティング、医学および環境修復における潜在的な用途の有望な候補[20,21,22,23]。 SnO 2 は、比表面積が高く、化学的安定性が高く、電気抵抗が低く、密度が低いため、応答時間と感度を向上させるセンサーとして使用されます[24]。過去数年から、SnO 2 CO、NO、NO 2 などの可燃性ガスを検出するための太陽電池[25]およびガスセンサーでのアプリケーションについて徹底的に調査されました。 、H 2 S、およびC 2 H 5 OH [26,27,28,29]。ナノ粒子(NP)のユニークな物理化学的特性と潜在的な用途のために、科学界はナノ粒子を生成するためのいくつかの方法を開発してきました。しかし、金属および金属酸化物ナノ粒子の合成に使用される化学的および物理的方法は非常に高価であり、環境および人間の健康に有害な有毒物質を使用します[30]。近年、ほとんどの研究者は、費用効果が高く、製造手順が簡単で、製造の再現性があり、多くの場合、より安定したナノ粒子が得られるなど、多くの利点があるため、NPのグリーン合成に関心を変えています[31]。過去10年間に、SnO 2 のグリーン合成に関するいくつかの研究 NPが報告されました。しかし、合成の方法論と形成のメカニズムを実証する単一の総説は、文献で利用できません。したがって、このペーパーでは、SnO 2 のグリーン合成、形成メカニズム、特性評価手法、および潜在的なアプリケーションについて説明します。 NP。
酸化スズナノ粒子のグリーン合成
SnO 2 NPは、さまざまな物理的、化学的、および環境に優しい方法で合成されます。化学的方法には、ゾルゲル法、熱水法、沈殿法、メカノケミカル法、マイクロエマルジョンなどが含まれます[31、32、33、34、35、36、37]。化学的方法の中で、最も広く使用されている手法は、ゾル-ゲル合成です。これは、スズ前駆体塩と、スズ含有ゲルの形成を制御する化学試薬を利用します。その後、ゲルを800°Cまでの温度で熱処理してSnO 2 を取得します。 NP [32、38]。 SnO 2 の合成中に、シュウ酸やエチレングリコールなどの化学安定剤やキャッピング剤を添加することができます。 ナノ粒子のサイズを制御し、凝集を禁止するためのNP [32、39]。溶液のpH、化学物質の濃度、反応時間、および焼成温度も、ナノ粒子のサイズと形態に影響を与える可能性があります[31、34、35、36、37]。 SnO 2 を合成する前述の方法 NPは、さまざまな危険な化学試薬、溶媒、および界面活性剤を利用しており、環境と人間の健康に深刻な脅威をもたらします[4、30]。
SnO 2 NPは、スプレー熱分解、熱酸化、化学蒸着、レーザーアブレーション、超音波処理などの物理的手法によっても合成できます[40、41、42、43、44]。これらの方法の中で、レーザーアブレーションは、液体中で金属および金属酸化物ナノ粒子を合成するための費用効果が高く簡単な方法と考えられています[44、45]。他の従来の方法とは対照的に、この方法は、キャッピング/還元剤、高温、または高圧を必要とせず、高純度のナノ粒子を生成することができます[44、45]。レーザービームから印加されるパルスのパラメーターの変動とアブレーション時間は、ナノ粒子の粒子サイズ、形態、および表面化学を定義する重要なパラメーターです[44]。ただし、ほとんどの物理的方法には、複雑な機器、高エネルギー、および熟練した人的資源が必要です[46]。したがって、環境に優しく、安価で、効率的で、周囲条件で機能する合成方法を開発することが非常に重要です。そのような解決策の1つはグリーン合成であり、多くの研究者が酸化スズナノ粒子を合成するためのグリーンケミストリーアプローチを開発しました。グリーン合成戦略では、植物抽出物、微生物、その他のグリーンソースなどの生物学的実体を、従来の物理的および化学的方法の代替として使用できます[47]。最近では、生物学的に着想を得た合成方法は、グリーンケミストリーの12の原則と一致しているため、グリーン合成としても知られています[48]。生物学的合成が物理的および化学的方法に勝る明確な利点のいくつかは、(a)無毒の化学物質が使用されるため、クリーンで環境に優しい方法、(b)再生可能な供給源の使用、(c)酵素自体のような活性な生物学的成分植物化学物質は還元剤およびキャッピング剤として機能し、それによって合成プロセスの全体的なコストを最小限に抑えます。(d)高圧や高温などの外部実験条件は不要であり、大幅なエネルギー節約をもたらします[49、50]。
過去10年間で、SnO 2 の合成への関心 このプロセスは、環境に悪影響を与えることなく、信頼性が高く、環境に優しく、費用効果が高く、投入量が少なく、収率が高く、手順が簡単であるため、生物学的手法によるNPは大幅に増加しています。 SnO 2 のグリーン合成には、植物抽出物、細菌、天然生体分子などのさまざまな生物学的基質がうまく利用されています。 NP。さまざまな植物の植物化学物質とバクテリアからの酵素が主にグリーン合成に関与しています。グリーンソースに存在する活性化合物は、合成中に還元剤、キャッピング剤、安定剤としても機能します。望ましいNPは、特定の温度での煆焼またはアニーリング後に得られることがよくあります[51、52、53、54]。
植物を介した酸化スズナノ粒子の合成
植物を介した合成は、有毒な化学物質を含まず、天然のキャッピングと還元剤を提供するため、従来の物理化学的方法よりも優れた合成プラットフォームになっています。さらに、それは簡単で環境に優しく、不純物のない量が豊富な製品を提供します。この方法では、高温高圧の高価な設備を使用する必要がありません。さらに、植物を介した合成は、さまざまな形状とサイズのより安定したナノ粒子の大規模生産につながります[55、56]。 SnO 2 のグリーン合成には、さまざまな植物種の多数の部分の抽出物が利用されています。 NP。一般に、SnO 2 の植物媒介合成 NPは、前もって調製した抽出物に薄い塩を加える非常に単純なプロセスです。反応後、溶液を遠心分離にかける。最後に、ペレットは熱処理にかけられ、フーリエ変換赤外分光法(FTIR)、X線回折計(XRD)、エネルギー分散型X線分析(EDS)、走査型電子顕微鏡法(EDS)などのさまざまな分析技術を使用して特性評価されます。 SEM)、透過型電子顕微鏡(TEM)、粒子サイズ分析器(PSA)、および動的光散乱(DLS)。ナノ粒子の形成を監視するために、UV-可視分光法(UV-Vis)が使用されます。 SnO 2 の植物媒介合成のための詳細なプロトコル NPは図1に概略的に示されています。Dialloetal。 SnO 2 のグリーン合成を報告しました Aspalathuslinearis を使用したNP および塩化スズ五水和物(SnCl 4 ・5H 2 O)前駆体として[51]。塩は植物抽出物に溶解し、10分後に白い沈着物の形成が観察されました。遠心分離プロセス後に白い堆積物を収集し、約80°Cで乾燥させました。粉末をさまざまな温度で約4時間アニールし、高分解能透過型電子顕微鏡(HR-TEM)、EDS、XRD、X線光電子分光法(XPS)などのさまざまな分析技術にかけました。 NPは準球形で、平均サイズは2.5〜11.40nmの範囲でした。 NPの粒子サイズおよび結晶性は、アニーリング温度の上昇とともに増加することが観察された。さらに、植物抽出物に存在するアスパラチン、ノトファギン、アスパラリニンなどの生物活性成分は、キレート剤と還元剤の両方として機能します。 Camellia sinensis 葉の抽出物は、SnO 2 の合成にも使用されました NP [53]。葉の抽出物に含まれるポリフェノールは、安定剤とキャッピング剤の両方として機能します。高解像度走査型電子顕微鏡(HR-SEM)およびXRD分析により、球形のSnO 2 が明らかになりました。 サイズが5〜30nmの範囲のNP。さらに、NPのバンドギャップはアニーリング温度の上昇とともに減少することがわかりました。 Catunaregam spinosa 媒介グリーン合成SnO 2 NPは、コンゴーレッド色素に対して優れた光触媒活性を示しました[57]。生合成されたNPは球形で、平均サイズは47nmです。
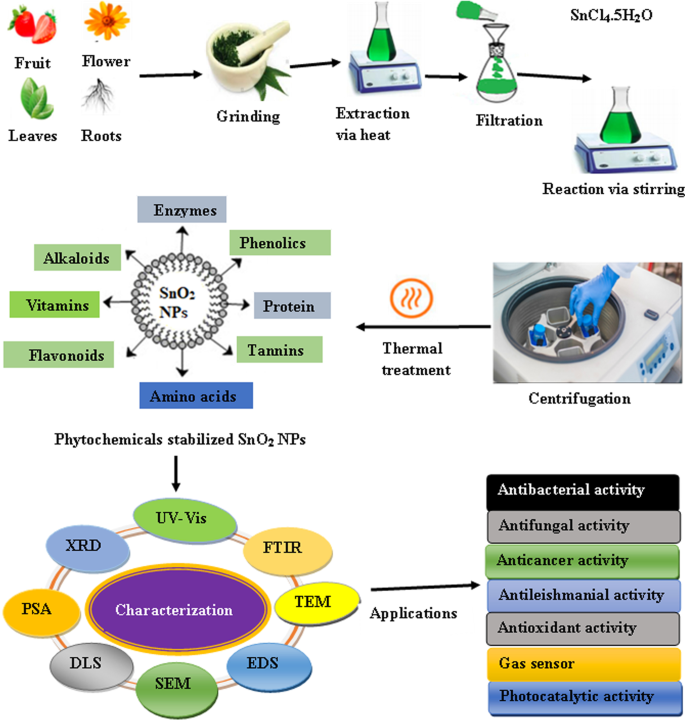
植物抽出物を介したSnO 2 の合成の概略図 NP
アロエベラミラーの葉の抽出物 SnO 2 の合成に使用されています SnCl 2 からのNP ・2H 2 前駆体としてのO [58]。得られたNPは球形で、平均サイズは50〜100nmの範囲で変化することがわかりました。さらに、合成されたナノ粒子は、 Sに対して優れた抗菌活性を示した。アウレウス および E。コリ。
別の研究では、SnO 2 のグリーン合成 NPは、 Plectranthus amboinicus を使用した効率的で安価な方法で行われました。 葉の抽出物とSnCl 2 ・2H 2 出発物質としてのO [59]。植物抽出物は、還元剤および安定剤として機能します。得られたNPは、SEM、EDX、XRD、およびPSAによって特徴づけられました。 NPは正方晶の形状で、平均粒度は63nmでした。さらに、著者らは、生合成されたNPが、市販のSnO 2 と比較して、ローダミンBに対してより大きな光触媒活性を示すことを明らかにしました。 。 SnO 2 のグリーン合成 NPは、 Nyctanthes arbor-tristis を使用して報告されました。 (パリジャタカ)花エキス[60]。 SEMおよびPSA分析から明らかなように、合成されたナノ粒子は、小さな凝集段階と2〜8nmの平均粒径を持つ微細な顆粒の形態を示しました。この研究では、植物抽出物の加水分解とキャッピングの可能性についても調査しました。
SnO 2 のグリーン合成 NPは、 Psidium guajava を使用して、低コストで環境に優しいプロセスによって実行されました。 葉の抽出物[61]。 UV-Visの結果は、314 nmに表面プラズモン共鳴ピークを示し、SnO 2 の形成を確認しました。 NP。さらに、NPは球形で、サイズは8〜10nmの範囲でした。この研究では、NPが太陽光照射下で180分以内に反応性黄色186の90%の分解を示すことも示されました。 Bhosale etal。 [62] Calotropis gigantea の葉の抽出物を特定しました SnO 2 の合成のための天然源として NP。抽出物の二次代謝産物は、塩化スズのSnO 2 への変換において安定剤とキャッピング剤の両方として機能します。 NP。著者らは、NPは球形であり、平均サイズは30〜40nmであると示唆しています。合成されたNPは、120分以内にメチルオレンジ色素を最大80%分解します。シンら。 [63]はSnO 2 の生合成を報告しました キンマを使用するNP 葉の抽出物。 SEMおよびTEM分析により、平均サイズが8.4nmの球状NPの形成が明らかになりました。 NPは、92.17%の効率で疑似一次で反応性黄色186を分解する。さらに、NPは、リアクティブレッド120およびリアクティブグリーン119と比較して、リアクティブイエロー186の除去に対して優れた選択性を示しました。文献では、SnO 2 の調製にさまざまな植物および植物抽出物が使用されています。 (表1)。表から、植物種の性質と反応条件がSnO 2 のサイズと形状に影響を与えることがわかります。 NP。
<図>バクテリアを介した酸化スズナノ粒子の合成
微生物は、環境に優しく費用効果の高いツールとして計り知れない可能性を秘めた重要なナノファクトリーであり、有毒な化学物質や物理化学合成に必要な高エネルギーを回避します。細菌、真菌、酵母などのさまざまな微生物が、細胞内または細胞外のいずれかで金属および金属酸化物ナノ粒子の合成に使用されてきました。細胞内合成には、金属イオンを微生物細胞に輸送し、細胞内の酵素、補酵素、およびその他の生体分子の存在下でNPを形成することが含まれます。細胞外合成では、金属イオンが微生物細胞の表面にトラップされます。表面で利用可能な酵素とタンパク質は金属イオンを還元し、NPに安定化を提供する役割を果たします[73]。ただし、細胞外合成は、大量のNPを製造するために使用でき、NPの回収に必要な合成のさまざまなステップを排除するため、細胞内経路と比較してより有利です[74]。
バクテリアを利用した生物学的合成は、化学合成と比較して環境に優しく、費用効果の高いアプローチです。ただし、この方法にはいくつかの欠点があります。(a)微生物のスクリーニングは時間のかかるプロセスであり、(b)培養液とプロセス全体を注意深く監視する必要があり、(c)のサイズと形態を制御することは困難です。 NP。固有の代謝プロセスと酵素活性のために、すべての細菌がNPを合成できるわけではありません。したがって、明確なサイズと形態のNPを生成するには、適切な細菌を慎重に選択する必要があります[74]。たとえば、SrivastavaとMukhopadhyay [54]が実施した研究では、SnO 2 を合成するための、低コストで環境に配慮した最も簡単な手順が報告されています。 新鮮で清潔な Erwinia herbicola を使用するNP 細菌細胞と塩化スズ(II)水溶液。合成されたSnO 2 NPはほとんど球形で、サイズは10〜42nmの範囲でした。 SnO 2 の合成中に、細菌タンパク質およびその他の生体分子が還元剤および安定剤として機能することが報告されました。 NP。これらの生体分子は、SnO 2 のサイズと凝集の制御にも役立ちました。 NP。
生体分子およびその他のグリーンソースを介した酸化スズナノ粒子の合成
植物および細菌を介したSnO 2 の合成は別として NP、研究者は、アミノ酸、ビタミン、酵素、糖などの他の生体分子を利用することにより、無毒で環境に優しいグリーンケミストリーアプローチを開発しました(表2)。ヤンら。 [75]合成されたSnO 2 天然に利用可能な生体分子であるビタミンC(アスコルビン酸)を使用した、低コストで環境に優しい方法を使用したNP。 TEM分析では、平均サイズが約30nmの球状NPの形成が示されました。ビタミンCは、合成中にキャッピング剤と還元剤の両方として機能します。この研究は、SnO 2 の表面にビタミンCがキャップされていることを示唆しています NPはSnO 2 によって引き起こされる酸化ストレスを減少させました 細胞上のNPは、新生児マウスの体重減少を減らします。球状SnO 2 13 nmの平均粒子サイズ内のNPは、炭水化物(デンプン)を使用して調製されました[76]。炭水化物がテンプレートとして機能し、それらの官能基を介していくつかの金属カチオンを結合できることが示唆され、したがって、カチオンの均一な分散が観察された。別の研究では、浸したベンガルグラム豆( Cicer arietnum )から集めた残りの水 L.)は、ドープされていないSnO 2 の合成に使用されました。 、およびNi、Fe、およびAuをドープしたSnO 2 NP [77,78,79]。著者らは、抽出物中のペクチンがSnO 2 の合成に関与していることを示唆しました NP。球形のドープされていないSnO 2 の平均結晶子サイズ 、NiドープSnO 2 、およびAuをドープしたSnO 2 NPは、それぞれ11 nm、6 nm、25nmであることがわかりました。
<図>別の研究では、SnO 2 を合成するための環境に優しいアプローチが示されています 鶏の卵殻からの天然のバイオ廃棄物である卵殻膜(ESM)[80]を使用するNP。 ESMは、合成中に還元剤として作用する、ウロン酸やアルデヒド部分を含む糖類などの生体分子を構成することが示唆されました。形態素解析により、SnO 2 の棒状、六角形、球形の形成が示されました。 粒子サイズが13〜40nmのNP。
SnO 2 のグリーン合成には、グリシン、アルギニン、アスパラギン酸、リジン、チロシンなどのさまざまなアミノ酸が使用されています[81,82,83,84,85]。 優れたキャッピング剤または錯化剤によるNP。アミノ酸を介した合成により、合成中に有毒な化学物質を使用する必要がなくなります。球状SnO 2 NPはアルギニンを使用して合成されました[81]。形態学的研究は、合成されたSnO 2 NPは球形で、平均サイズは4〜5nmの範囲でした。 Bhattacharjee etal。 [83]はグリシンを使用してSnO 2 を生成しました 塩化第一スズからのNP。 200°C、400°C、および600°Cで形成されたNPは、球形、多結晶、および単分散であり、それぞれ平均サイズが6、16、および33nmであることが示唆されました。さらに、400°Cで得られたナノ粒子は発光性でした。同様に、Begum etal。 [84]は、正方晶のルチル構造SnO 2 の合成を示しました。 サイズが4〜17nmの範囲のL-リジンを使用するNP。
グリーン合成による酸化スズナノ粒子の形成メカニズム
過去数年間で、さまざまな植物抽出物、微生物、およびその他の生物学的誘導体が、金属および金属酸化物NPのグリーン合成に使用されてきました。研究によると、植物抽出物に存在するフェノール、フラボノイド、タンニン、サポニン、テルペノイド、炭水化物などの二次代謝産物は、金属または金属酸化物NPの合成において還元剤と安定剤の両方として作用することにより重要な役割を果たします[87]。さらに、微生物を介した合成は、NPが形成される場所に応じて細胞内または細胞外のいずれかで達成することができます。細胞外合成では、表面で利用可能な酵素の存在下で微生物細胞の表面で生物還元が起こります。さらに、細胞内生合成では、金属イオンが微生物細胞に輸送され、細胞内の酵素の存在下でNPがそこで容易に形成されます[73]。セルバクマリ他[53]利用された Camellia sinensis SnO 2 の生合成のための抽出物 NP。彼らは彼らの研究から、抽出物中に存在するポリフェノール化合物(エピカテキン、エピガロカテキン、エピカテキンガレート、およびエピガロカテキンガレート)がキャッピング剤と安定剤の両方として機能することを実証しました。 SnO 2 この方法で形成されたNPは、(i)Sn 2+ の還元を含むいくつかの主要なステップで構成されます。 Sn 0 へ 、(ii)抽出物のフェノール化合物(–OH)の還元効果によるSn種の形成、および(iii)Sn種のSnO 2 への熱変換 NP。 SnO 2 Calotropis gigantean を使用して合成されたNP 葉の抽出物であるポリフェノール化合物は、スズイオンの生化学的変換に関与しています[62]。球状SnO 2 3.62〜6.34 nmの範囲のサイズのNPは、カリフラワー抽出物を使用して合成されました[52]。抽出物のポリフェノールとフラボノイドが金属イオンと配位し、Sn(OH) 2 が形成されることが示唆されました。 煆焼するとSnO 2 の形成につながる中間体 NP。別の研究では、SrivastavaとMukhopadhyay [54]は、球状のSnO 2 の細胞内合成と細胞外合成の両方を報告しました。 細菌 Eによって分泌される酵素によるNP。ハービコラ 。この方法では、Sn 2+ イオンは、細菌細胞によって分泌される細胞外酵素または細胞表面の膜関連タンパク質によってトラップされ、還元はデヒドロゲナーゼ酵素によって開始されました。 Sn 2+ イオンは、2つの電子とNAD + の分子を獲得することによって還元されます。 酸化されてNADHを形成し、最終的に細胞外SnNPが生成されます。次に、生合成されたSnナノ粒子は、溶液中に存在する酸素によって酸化され、SnO 2 が形成されます。 NP。 FTIR分析により、表面にタンパク質のような分子が存在することが明らかになりました。これは、SnO 2 の自然なサポートと安定性を提供します。 NP。さらに、アミノ酸はキャッピング剤または錯化剤として機能し、それによって合成中の有毒化学物質の使用を最小限に抑えます。 SnO 2 のグリーン合成の可能なメカニズム NPを図2に示します:
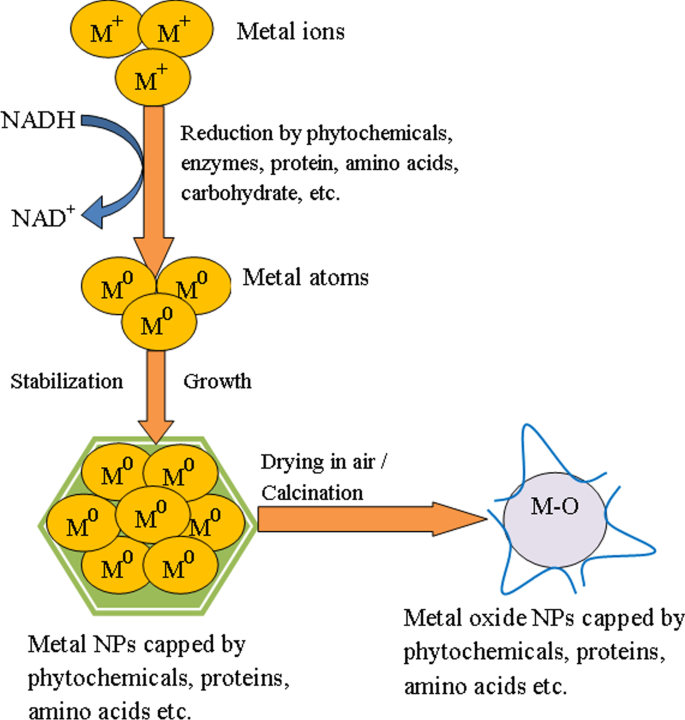
金属酸化物(SnO 2 )の生物学的に媒介された合成の可能なメカニズムを示す図 )NP
酸化スズナノ粒子の特性評価
NPの特性評価は、合成手順とアプリケーションを理解して制御するために非常に重要です。合成されたNPのサイズ、形状、結晶化度、および表面積に関する表面形態とコンフォメーションの詳細は、さまざまな手法を利用して研究されます。緑で合成されたSnO 2 の特性を明らかにするために使用される手法のいくつか NPは、UV-Vis、FTIR、XRD、EDS、SEM、およびTEMです。 UV-Vis分光法は、ナノ粒子の光学特性を研究することにより、ナノ粒子の形成を監視するために使用されます。 SnO 2 のUV-Visスペクトル Catunaregam spinosa を使用して合成されたNP 抽出物は、その表面プラズモン共鳴により、223nmの最高の吸収ピークを示しました[57]。 XRDは、材料の結晶構造を研究するために使用される強力な手法です。 Bhattacharjee etal。 [81]特性化されたSnO 2 回折角(2 θ)にXRDピークを持つNP )(110)、(101)、(200)、(211)、(220)、(002)に対応する26.7、34.2、38.07、51.9、54.9、58.1、62.1、64.9、66.08、71.6、および79.07のそれぞれ(310)、(112)、(301)、(202)、および(321)平面(図3)。標準の回折ピークは、SnO 2 の正方晶ルチル構造を示しています。 Debye-Schererの式[81]を使用して計算された平均結晶子サイズ4.6nmのNP。
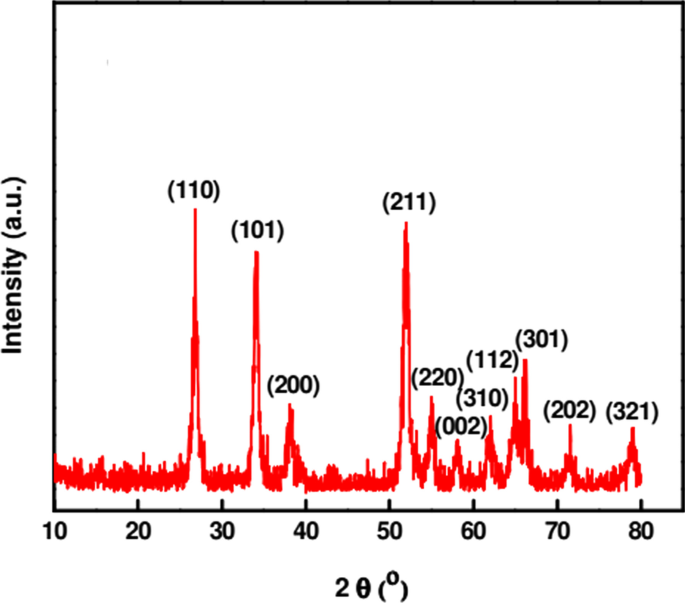
SnO 2 のXRDパターン マイクロ波照射下でアルギニンを使用して合成されたNP [81]
FTIR分光法は、表面化学を調査し、NPの表面に存在する官能基を特定するために使用されます。これは、NPの還元、キャッピング、および安定化に関与している可能性があります[88]。 SnO 2 のFTIR分析 Pruni flos を使用して合成されたNP 抽出物は、3308、2153、1634、423、403、および383 cm -1 に主要な吸収帯を示しました。 。 3308、2153、および1634 cm -1 で観察された強いバンド SnO 2 に吸着された水分子によるSn–OH基の伸縮振動に割り当てられています それぞれ、表面、アルキンのC–H伸縮、およびフラボノイドのC =O振動。 423〜383 cm -1 のバンド 反対称Sn–O–Sn伸縮に起因します[70]。ナノ粒子の形態学的特性を決定するために、SEMやTEMなどの顕微鏡ベースの技術が広く採用されています。ただし、TEMは、SEMと比較して、結晶構造や形態などの内部構造に関するより優れた解像度と情報を提供します。表面特性のより正確な結果は、FE-SEMを使用して取得できます。これらの手法は、合成されたナノ粒子の平均サイズを推定するのにも役立ちます[89]。 FE-SEMおよびTEM分析により、わずかに凝集した球形のSnO 2 の形成が明らかになりました。 平均サイズが30〜40 nmのNP(図4)[62]。

a 生合成されたSnO 2 のTEM画像 NP; b SnO 2 のHR-TEM画像 NP; c SnO 2 のFE-SEM画像 NPと d SnO 2 のSAEDパターン NP
さらに、選択的領域電子回折(SAED)分析は、粒子が本質的にナノ結晶であることを示しました(図4)[62]。球形のSnO 2 の形成 キンマを使用して合成されたNP 水性抽出物はFE-SEMによって確認されました[63]。 TEMおよびXRD分析から、NPの平均サイズは8.4nmであることがわかりました。
EDSは、サンプルの元素組成を分析するために使用される分析技術です。 SnO 2 のEDSスペクトル Psidium Guajava を使用して合成されたNP 葉の抽出物は、SnおよびOピークの存在を明らかにしました。これは、純粋なSnO 2 の形成を確認します。 NP [61]。
緑色で合成された酸化スズナノ粒子の生物学的応用
緑で合成されたSnO 2 NPは、バルク形態と比較して、強化された光触媒、抗菌、抗酸化、および抗癌活性を示しました。このセクションでは、グリーン合成されたSnO 2 のアプリケーションについて説明しました。 将来の展望のための新しい研究者へのガイダンスとしてのさまざまな分野のNP。
抗菌作用
多くの研究者が抗菌活性SnO 2 を観察しています NP。たとえば、SnO 2 の抗菌活性 アロエベラを使用して合成されたNP 植物抽出物は、 Eを使用して研究された。コリ および S。アウレウス 。 NPは Sに対してより活性であることが示唆された。アウレウス Eより。コリ [58]。これは、 Eの細胞壁が原因である可能性があります。コリ Sよりも複雑です。アウレウス 。 S。アウレウス 厚いペプチドグリカンで構成された膜を持っています。ただし、 Eの細胞壁。コリ ペプチドグリカン層に加えて、リポ多糖で構成される外膜があります。 Eの外膜。コリ 細胞へのROSの浸透レベルを下げるバリアとして機能します[90,91,92]。別の理由は、それらの細胞膜の極性の違いである可能性があります。 黄色ブドウ球菌の膜 Eよりも正の電荷を持っています。コリ 、その結果、負に帯電したフリーラジカルの浸透レベルが高くなり、 Sでより多くの細胞損傷と死を引き起こします。アウレウス Eより。コリ [93、94] 。 SnO 2 の抗菌活性 ザクロを使用して合成されたNP シード抽出物は Eに対してテストされています。コリ。 殺菌効果は、ナノ粒子の濃度を上げると増加しました[95]。 SnO 2 Trigonella foenum-graecum を使用して合成されたNP 種子抽出物はまた、 Eに対して同様の抗菌活性を示した。コリ [72]。最近の研究では、 Clerodendrum inerme 葉抽出物は、ドープされていないおよび共ドープされたSnO 2 の合成に使用されました NP [96]。緑で合成された非ドープおよびCoドープSnO 2 NPは、 Eなどの5つの病原菌に対する抗菌活性にさらされました。コリ 、 B。 subtillis 、 A。ニジェール 、 A。 flavus 、および C。アルビカンス、 、およびそれらの阻害ゾーン(ZOI)、最小発育阻止濃度(MIC)、および最小殺菌濃度(MBC)を計算しました。共ドープされたSnO 2 NPは Eに対して実質的な抗菌活性を示した。コリ および B。 subtillis ドープされていないSnO 2 と比較して濃度依存的に NP、植物抽出物、およびMIC(22±0.7、18±0.8 mg / mL)およびMBC(31±0.9、21±0.6 mg / mL)、およびZOI(30±0.08、26±それぞれ0.06nm)。著者らは、CoドープSnO 2 の広域スペクトル抗菌活性を示唆しました。 NPはコバルトドーピングによるものであり、ドープされていないSnO 2 と比較して、NPの粒子サイズと表面積が増加します。 NP。粒子サイズが小さい表面積が大きいほど、抗菌活性は大きくなります。フラボノイドやフェノール化合物などの生体分子とCoドープSnO 2 との結合 NPは、抗菌活性の強化にも関与しています。さらに、緑色で合成されたCoドープSnO 2 NPは、 Aに対して17±0.04、23±0.08、および26±0.06 nmの最大ZOIで、並外れた抗真菌活性を示しました。ニジェール 、 A。 flavus、 および C。アルビカンス、 それぞれ、植物抽出物と比較して、ドープされていないSnO 2 NP、および標準薬[96]。
SnO 2 の実際の作用機序 微生物株に対するNPはまだ不明です。しかし、ナノ粒子の分解、ナノ粒子と微生物の細胞壁との静電相互作用、光放射の影響による活性酸素種(ROS)の形成など、細菌に対するいくつかの作用メカニズムが金属酸化物ナノ粒子に対して示唆されています[ 97,98,99]。 SnO 2 の抗菌効果の考えられる原因の1つ NPは、細菌の細胞膜の表面にNPが蓄積している可能性があります。 SnO 2 の存在により生成されたROS NPは細胞膜と相互作用し、細菌の膜透過性と呼吸系を乱し、細胞死を引き起こします[72、95、100]。たとえば、カーン等。 Sn 4+ のリリースを提案しました およびCo 2+ バクテリアのDNAとミトコンドリアの損傷の原因であり、バクテリアの酵素を不活性化し、最終的に細胞死を引き起こします[96]。
抗酸化作用
多くの研究者は、安定したDPPH(2,2-ジフェニル-1-ピクリルヒドラジル)ラジカルを非ラジカル型(DPPH-H)に消光する能力を監視することにより、NPの抗酸化活性を調べました。カマラジら[101]はSnO 2 の抗酸化活性を報告しました Cleistanthus Collinus を使用して生合成されたNP 葉エキス。 SnO 2 の抗酸化作用 NPは、SnO 2 の濃度の増加とともに増加しました NPと反応時間。別の研究[95]では、緑色で合成されたSnO 2 のフリーラジカル捕捉活性 NPは用量依存的に増加した。しかしながら、アニーリングされたサンプルは、調製されたままのサンプルと比較して、より低い捕捉活性を示した。アニーリング温度の上昇に伴うスカベンジング活性の低下は、NPの表面積対体積比の低下に起因する可能性があります。さらに、SnO 2 の抗酸化効果 DPPHに対するNPは、NPとDPPHの窒素にあるフリーラジカルとの間の電子密度の移動によるものです。 SnO 2 でも同様の結果が見つかりました Trigonelle foenum-graecum を使用して合成されたNP 水性抽出物[72]。 Hong etal。 [67]は、生合成されたSnO 2 の重要な抗酸化特性を報告しました NP。生合成されたSnO 2 の抗酸化活性 IC 50 で、NPの濃度の増加とともに増加しました (最大阻害濃度の半分)2257.4 µg / mlの値。最近、Khan et al 。 CoドープSnO 2 の有意な抗酸化活性を報告 ドープされていないSnO 2 と比較したNP NPと植物抽出物[96]。
細胞毒性活性
SnO 2 Annonasquamosa の乾燥果皮の農業廃棄物の水性抽出物を使用して合成されたNP 肝細胞癌細胞株(HepG2)に対する細胞毒性試験について評価された[64]。 TEMの結果は、細胞体積の減少、細胞のかなりの腫れ、および核凝縮を明らかにしました。 SnO 2 で見られる核凝縮 NP処理されたHepG2細胞は、核内のクロマチンの分解が原因である可能性があります。 SnO 2 NPは、IC 50 を使用して、用量および時間に依存して細胞増殖を阻害しました。 148 µg / mLの値。 SnO 2 piper nigrum を使用して合成されたNP 種子抽出物は、結腸直腸(HCT116)および肺(A549)の癌細胞株に対してより高い細胞毒性活性を示しました[69]。両方の癌細胞株の増殖は、NPサイズの増加とともに増加しました。さらに、SnO 2 の投与量を増やすと、細胞生存率の段階的な低下が観察されました。 NP。著者らは、細胞毒性効果は活性酸素種(ROS)からの酸化ストレスの発生に関連していると結論付けました。 SnO 2 Pruni spinosae flos を使用して作成されたNP 水性抽出物は、非小細胞肺癌細胞A549および肺線維芽細胞CCD-39Lu細胞に対して、濃度および時間依存的に優れた細胞毒性効果を示しました[70]。最近、カーン等。 [96]は、緑色で合成されたドープされていないSnO 2 のinvitro細胞毒性効果を調査しました。 NPと共ドープSnO 2 比色法による乳腺乳がん(MCF-7)、ヒト羊膜(WISH)、およびヒト肺線維芽細胞(WI38)細胞株に対するNP 3-(4,5-ジメチルチアゾール-2イル)-2,5-ジフェニルテトラズジウムブロミド(MTT)アッセイ。緑で合成されたCoドープSnO 2 NPは、ドープされていないSnO 2 と比較して、有意かつ実質的な死亡率を示しました。 NP、植物抽出物、および標準薬5-FU(5-5-5-フルオロウラシル)、ドープされていないSnO 2 NPは標準薬と同様の死亡率を示しましたが、乳がん細胞株に対する細胞毒性が最も低いのは植物抽出物でした。植物抽出物の細胞毒性効果、緑色で合成されたドープされていないSnO 2 、および共ドープされたSnO 2 NPはIC 50 で実行されました MCF-7の場合は31.56±1.4、26.99±1.9、18.15±1.0 µg / mL、WI38の場合は40.69±0.9、38.97±0.8、36.80±0.6 µg / mL、WI38、38.56の値。それぞれ31.10±0.7µg / mLであり、CoドープSnO 2 の細胞毒性を示しています。 NPは、植物抽出物およびドープされていないSnO 2 と比較してより熟練していました。 NPのみ。さらに、著者らは、濃度および用量依存的に乳がんMCF-7細胞株のinvitro阻害が大きいことを示す優れた観察結果を報告しました。緑で合成されたNPは、CoをドープしたSnO 2 を含むWI38およびWISHの正常細胞株と比較して、MCF-7に対して強力な細胞毒性も示しました。 ドープされていないSnO 2 よりも高いROS生成を明らかにするNP NP。図5は、緑色で合成されたSnO 2 の細胞毒性メカニズムの可能性を示しています。 NP。
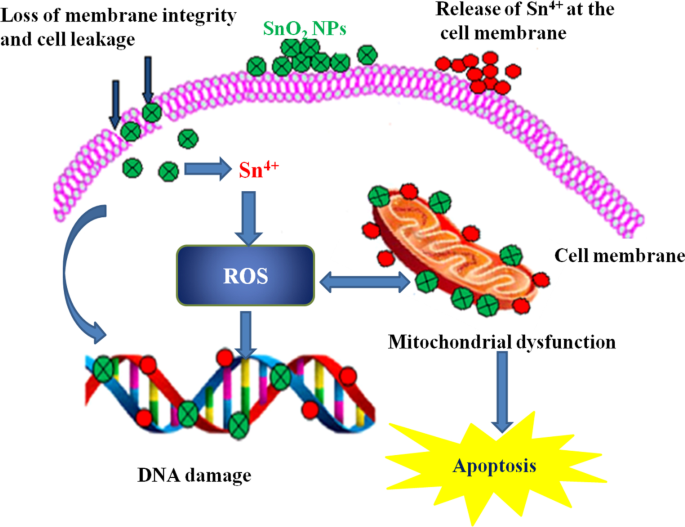
緑で合成されたSnO 2 の細胞毒性中のメカニズム NP
光触媒活性
さまざまな産業から流水への有毒化学物質、危険な繊維染料、および農薬の制御されていない放出は、深刻な環境問題を引き起こしました。これらの過剰な水質汚染物質は、長期的な悪影響を引き起こし、水生生物と人間の生命に深刻な脅威をもたらします。その上、いくつかの有機染料は発癌性で毒性があります。したがって、有毒化学物質を含む水を環境に廃棄する前に処理することは、環境汚染を減らすために非常に重要です。最近の研究では、ナノ構造の半導体金属酸化物が、さまざまな水質汚染物質を除去するための優れた光触媒として機能することが示されています[102、103、104、105]。半導体金属酸化物の中で、SnO 2 物理的および化学的安定性、高い表面反応性、高い光触媒効率、低コスト、低毒性などの有益な特性により、一般的な繊維染料や有機化合物の除去に広く使用されています[68、106]。 Manjula etal。 [107]合成されたSnO 2 グルコースを使用したナノ粒子。 NPは、メチルオレンジ(MO)色素を分解する際の触媒として効果的に使用されました。 NPの光触媒活性に対する煆焼温度(150〜500°C)の影響を調査した結果、合成されたままのSnO 2 150°Cで煆焼されたNPは、研究対象の材料の中で研究中の反応に最適な光触媒です。さらに、準備されたままのSnO 2 ナノ粒子はメチルオレンジを30分で完全に分解しました。また、ナノ材料は最低5倍の効率でリサイクルできます。別の研究[108]では、SnO 2 の光触媒活性 セリンを使用して合成された量子ドット(量子ドット)は、直射日光の下でエオシンY溶液の光吸収スペクトルを監視することによって評価されました。 SnO 2 を使用したエオシンYの分解速度が観察されました。 QD(98%)は、市販のSnO 2 を使用した場合よりも高くなっています。 (96%)およびP25(88%)。 Begum etal。 [84]はSnO 2 の合成を報告しました アミノ酸、L-リジン一水和物を使用するNP。合成されたナノ粒子は、有毒な有機染料、すなわち直射日光下でのマラカイトグリーンシュウ酸塩(MGO)とビクトリアブルーB(VBB)に対する光触媒挙動について評価されました。これらの色素の吸収ピークは減少し始めており、発色団の構造が破壊されていることを示しています(図6)。さらに、準備されたままのSnO 2 NPは、120分以内にMGO(97.3%)およびVBB(98%)色素の顕著な光触媒分解を示しました。緑で合成されたSnO 2 の光触媒活性に関する文献報告 NPは表3にまとめられています。
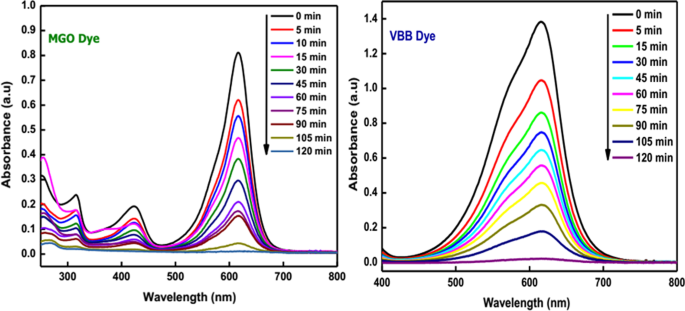
SnO 2 を使用した太陽照射下でのマラカイトグリーンシュウ酸塩染料の光触媒分解 NP
ガス検知プロパティ
多くの金属酸化物ベースのガスセンサーは、ガス検知アプリケーションに広く使用されています。ただし、SnO 2 NPは、高感度、高選択性、容易な可逆性、安価な製造コストなどの有益な特性により、大気条件下でのガス検知で大きな注目を集めています。グリーン合成された多孔質SnO 2 ナノスフェアは優れたガス検知能力を示しました[107]。 0.5 wt%PdのSnO 2 への同化が観察されました。 マトリックスは感度を向上させ、低温水素検出に対して高度に選択的にしました。さらに、ファブリックは50 ppm H 2 にも対応できました。 N 2 で 室温で10秒間隔で。これらの検知特性は、SnO 2 の両方の多孔質構造の相乗効果によるものです。 ナノスフェアとPdナノ粒子の触媒特性。 Gattu et al 。 [77]は、生合成および化学合成されたNiドープSnO 2 のガス検知挙動を報告しました。 NPs薄膜。生合成されたNiドープSnO 2 NPs薄膜はより高いNO 2 を示した 化学合成されたものと比較したガス検知応答。センサー応答は、生合成および化学合成されたNiドープSnO 2 の両方で、Niドーピングによって増加することがわかりました。 NP。これは、Niドーピングによる粒子サイズの減少が原因である可能性があり、その結果、NO 2 の吸着表面積が増加します。 ガス。さらに、NiドープSnO 2 薄膜はNO 2 に対して優れた選択性を示した NH 3 のような他のガスの隣に置かれたときのガス 、LPGおよびH 2 S.別の研究[78]では、ドープされていないSnOとFeをドープされたSnO 2 のガス検知特性 Cicer arietnum を使用して合成されたNP L.抽出物が報告されました。 100 ppm NH 3 の存在下でのガス応答 ドープされていないSnO 2 の場合、200°Cの動作温度でのガスは28%であることがわかりました。 鉄をドープしたSnO 2 の場合は46% 薄膜。さらに、FeをドープしたSnO 2 ベースのセンサーはNH 3 に対してより選択的であることがわかりました ドープされていないSnO 2 と比較したガス センサー。生合成されたAuドープSnO 2 NPはNO 2 に非常に敏感であることがわかりました 200°Cの動作温度のガス[79]。ガスセンサーはAuドープSnO 2 をサポート NPは、100 ppmのNO 2 に対して〜30%のガス応答を示しました。 ガス。さらに、AuをドープしたSnO 2 のガスセンサー NPはNO 2 に対して優れた選択性を示しました H 2 のような他のガスの隣に置いたときのガス S、LPG、およびNH 3 。 NO 2 に対するガス応答と選択性の向上 ガスは、Auドーピングによって引き起こされる格子歪みと、SnO 2 内での酸素空孔の生成によるものです。 格子。
結論
NPの生産にグリーン法を使用することは、環境に優しく、安価で、毒性がなく、持続可能な方法であるため、焦点を絞った研究分野となっています。多くの研究がSnO 2 を生成する可能性を報告しています さまざまな植物材料、バクテリア、および天然生体分子を使用したグリーンプロトコルによるNP。文献調査によると、緑色の基質は、その供給源に関係なく、還元剤および安定剤またはキャッピング剤として機能します。 SnO 2 のさまざまなグリーンメソッドの中で 合成、植物媒介合成は費用効果が高く、処理が簡単で、微生物よりも危険性が少ないです。しかし、植物抽出物は、異なる組成の多数の活性化合物で構成されているため、金属イオンの還元に関与する分子の正確な量を知ることは困難です。この複雑さのために、ナノ粒子の合成を評価することは困難です。したがって、SnO 2 の形成メカニズムに関するさらなる研究 NPは、合成中に発生する化学反応を理解するために必要です。実際の反応メカニズムの知識があれば、SnO 2 の大規模生産に不可欠な生合成プロセスを監視および最適化することが可能になります。 NP。したがって、ここで説明する急速に成長している合成方法を理解することは、SnO 2 に関する将来の研究の進歩を促進するのに役立ちます。 NPと、近い将来の工業規模の生産に対するその大きな可能性。
データと資料の可用性
利用できません。
略語
- NP:
-
ナノ粒子
- SnO 2 NP:
-
酸化スズナノ粒子
- UV-Vis:
-
紫外可視分光法
- SEM:
-
走査型電子顕微鏡
- FE-SEM:
-
電界放出型走査電子顕微鏡
- TEM:
-
透過型電子顕微鏡
- HR-TEM:
-
高分解能透過型電子顕微鏡
- FTIR:
-
フーリエ変換赤外分光法
- EDS:
-
エネルギー分散型X線分析
- PSA:
-
粒子サイズアナライザー
- XPS:
-
X線光電子分光法
- SAED:
-
選択領域電子回折
ナノマテリアル
- 特殊酸化物耐火物とその用途
- 改善された診断および治療用途のための多機能金ナノ粒子:レビュー
- ICAをロードしたmPEG-ICAナノ粒子の調製とLPS誘発性H9c2細胞損傷の治療におけるそれらの応用
- Escherichia coliに対する酸化銅ナノ粒子の生体合成、特性評価、および抗菌力の評価
- マウスにおける二酸化チタンナノ粒子の潜在的な肝臓、脳、および胚の毒性
- フェニルトリメトキシシランで修飾されたアルミナナノ粒子をベースにしたAl2O3:SiOCナノコンポジットの形成と発光特性
- Au @ TiO2卵黄シェルナノ構造の調製とメチレンブルーの分解および検出へのその応用
- 蒸発誘起自己組織化と強化されたガス検知特性によるワームホールのようなメソポーラス酸化スズの容易な合成
- 銅ナノ粒子の合成と安定化におけるグリーン熟達度:触媒、抗菌、細胞毒性、および抗酸化活性
- 金および銀ナノ粒子のグリーン合成のためのPlatycodiRadix(Platycodon grandiflorum)からのPlatycodonサポニン
- 金属および金属酸化物ナノ粒子のグリーン合成と単細胞藻類Chlamydomonasreinhardtiiに対するそれらの効果



