原子価と結晶構造
原子価: 最も外側の殻、または原子価殻の電子は、原子価として知られています。 電子。これらの価電子は、化学元素の化学的性質に関与しています。他の元素との化学反応に関与するのはこれらの電子です。単純な反応に適用できる過度に単純化された化学規則は、原子が8個の電子(Lシェルの場合は2個)の完全な外殻を形成しようとすることです。原子は、下にある完全なシェルを露出させるために、いくつかの電子を放出する場合があります。原子は、シェルを完成させるためにいくつかの電子を受け入れる場合があります。これらの2つのプロセスは、原子からイオンを形成します。原子は、外殻を完成させようとして、原子間で電子を共有することさえあります。このプロセスは分子結合を形成します。つまり、原子が結合して分子を形成します
指揮者
たとえば、グループIの元素:Li、Na、K、Cu、Ag、およびAuは単一の価電子を持っています。 (下の図)これらの元素はすべて同様の化学的性質を持っています。これらの原子は、他の元素と反応するために1つの電子を容易に放出します。電子を簡単に放出できるため、これらの元素は優れた導体になります。
周期表のグループIA元素:Li、Na、およびK、およびグループIB元素:Cu、Ag、およびAuは、外殻または原子価殻に1つの電子を持ち、容易に供与されます。内殻電子:n =1、2、3、4の場合; 2n 2 =2、8、18、32。
絶縁体
グループVIIA元素:Fl、Cl、Br、およびIはすべて、外殻に7つの電子を持っています。これらの元素は電子を容易に受け入れて、外殻を完全な8個の電子で満たします。 (下の図)これらの元素が電子を受け入れる場合、中性原子から負イオンが形成されます。電子をあきらめないこれらの元素は絶縁体です。
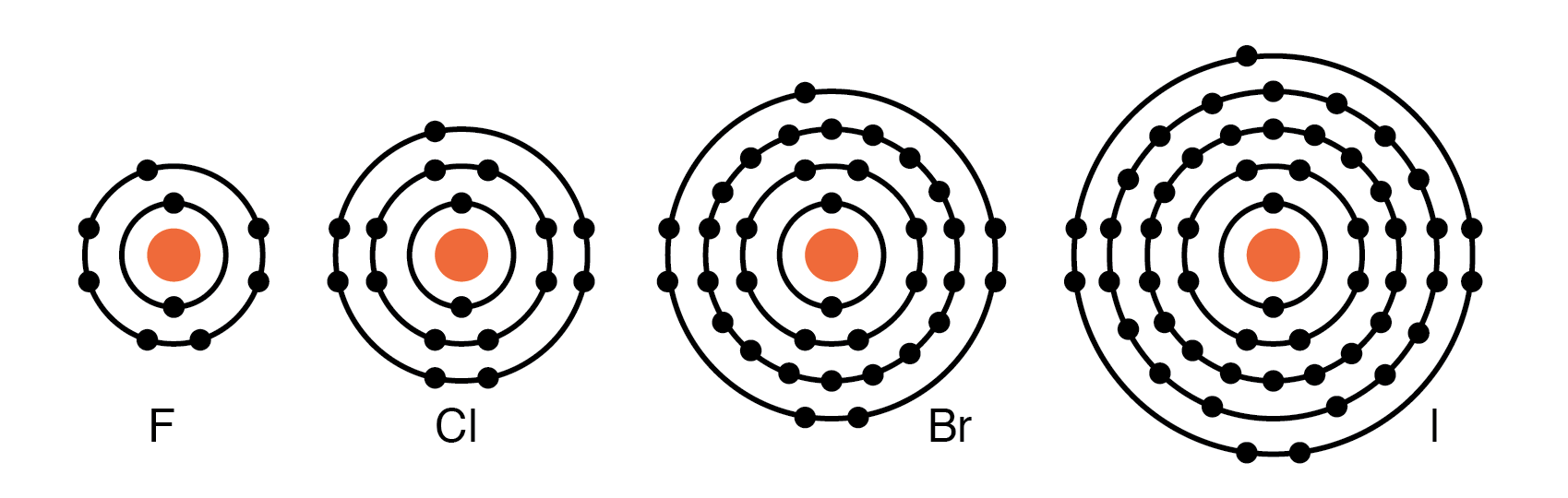
周期表グループVIIA元素:7つの価電子を持つF、Cl、Br、およびIは、他の元素との反応で電子を容易に受け入れます。
たとえば、Cl原子はNa原子からの電子を受け取り、Cl - になります。 下の図に示すようにイオン。 イオン は、電子を供与または受容することによって原子から形成される荷電粒子です。 Na原子が電子を提供すると、Na +イオンになります。これは、Na原子とCl原子が結合してNaCl、実際にはNa + である食卓塩を形成する方法です。 Cl - 、イオンのペア。 Na + およびCl - 反対の電荷を帯びて、お互いを引き付けます。
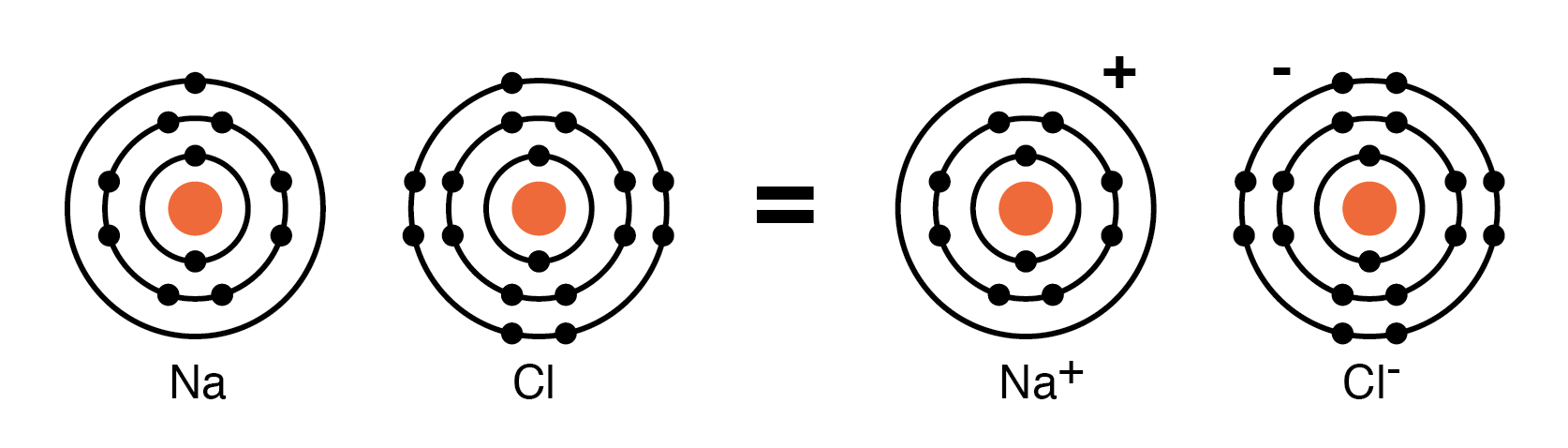
中性ナトリウム原子は中性塩素原子に電子を供与してNaを形成します + とCl - イオン。
塩化ナトリウムは、下の図に示す立方構造で結晶化します。このモデルは、3次元構造を示すために縮尺どおりではありません。 Na + Cl - イオンは実際には積み重ねられたビー玉の層のように詰め込まれています。簡単に描画できる立方晶構造は、固体結晶に荷電粒子が含まれている可能性があることを示しています。
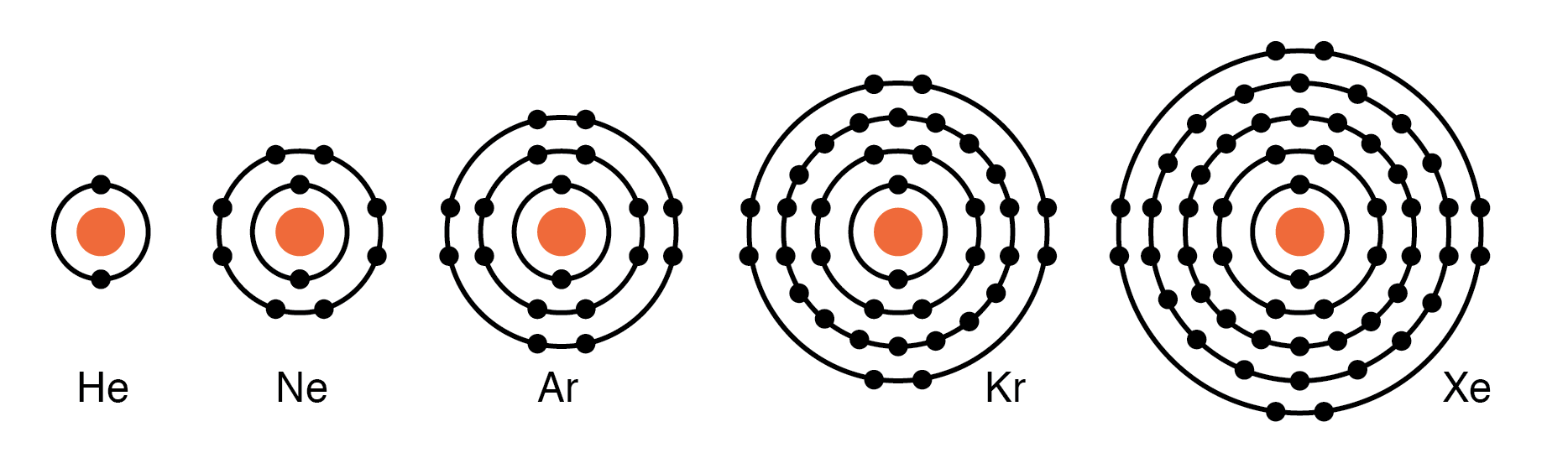
グループVIIIAの元素:He、Ne、Ar、Kr、Xeはすべて、原子価殻に8つの電子を持っています。 (下の図)つまり、原子価殻は完全であり、これらの元素は電子を供与も受容もしません。また、グループVIIIAの元素は他の元素と容易に結合しないため、化学反応に容易に関与することもありません。近年、化学者はXeとKrにいくつかの化合物を形成させるように強制しましたが、私たちの議論の目的のために、これは適用できません。これらの要素は優れた電気絶縁体であり、室温ではガスです。

グループVIIIA元素:原子価殻が完成しているため、He、Ne、Ar、Kr、Xeはほとんど反応しません。
半導体
グループIVA元素:下の図に示すように原子価殻に4つの電子を持つC、Si、Geは、イオンを形成せずに他の元素と電子を共有することによって化合物を形成します。この共有電子結合は、共有結合として知られています。 。中心原子(および拡張により他の原子)は、電子を共有することによってその原子価殻を完成させていることに注意してください。この図は結合を2次元で表したものであり、実際には3次元であることに注意してください。私たちがその半導体特性に関心を持っているのは、このグループ、IVAです。
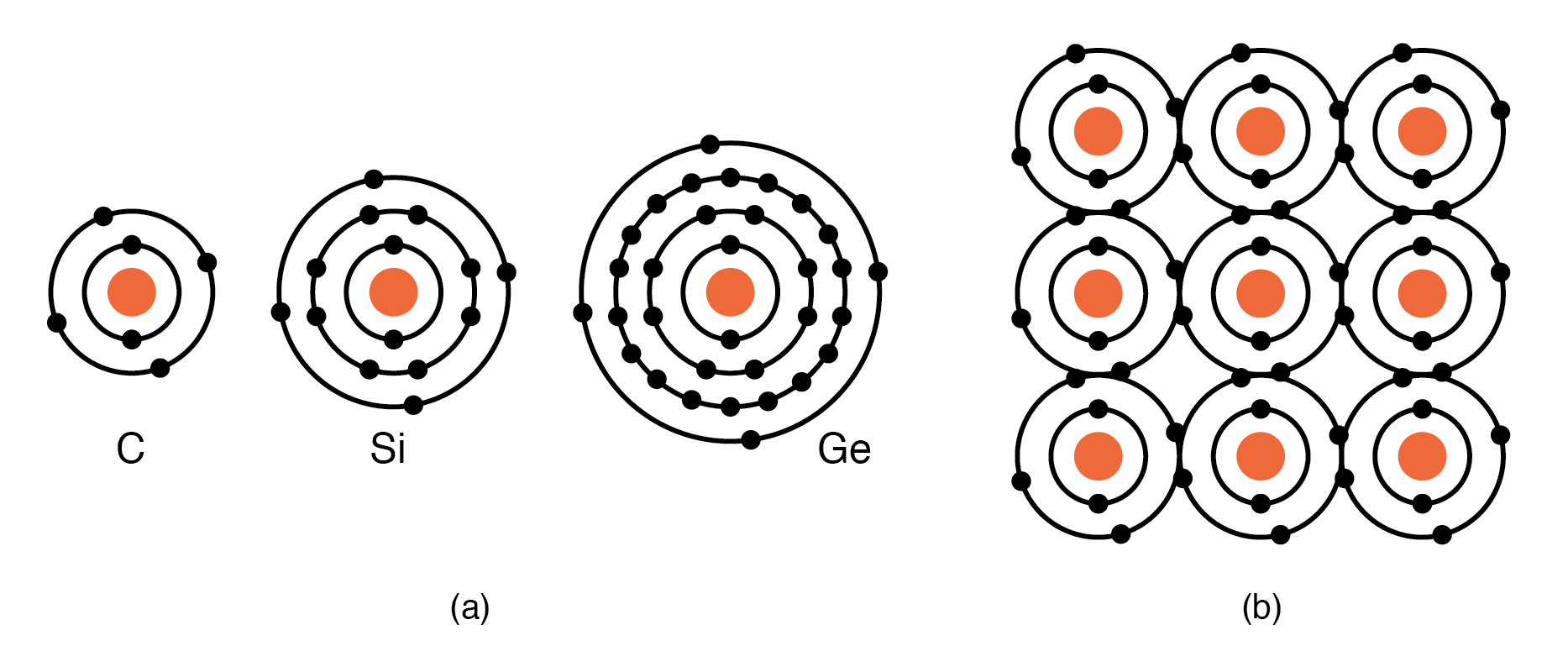
(a)グループIVA元素:原子価殻に4つの電子を持つC、Si、Ge、(b)他の元素と電子を共有することによって原子価殻を完成させます。
結晶構造: ほとんどの無機物質は、原子(またはイオン)を形成して、結晶と呼ばれる規則正しい配列にします。 。原子の外側の電子雲は規則正しく相互作用します。金属でさえ、微視的なレベルで結晶で構成されています。金属サンプルに光学研磨を施してから酸エッチングすると、微視的な微結晶 構造は下図のようになります。専門業者から金属単結晶試料をかなりの費用をかけて購入することも可能です。そのような試験片を研磨およびエッチングすることは、微結晶構造を明らかにしない。事実上、すべての工業用金属は多結晶です。一方、最新の半導体のほとんどは単結晶デバイスです。私たちは主に単結晶構造に関心があります。
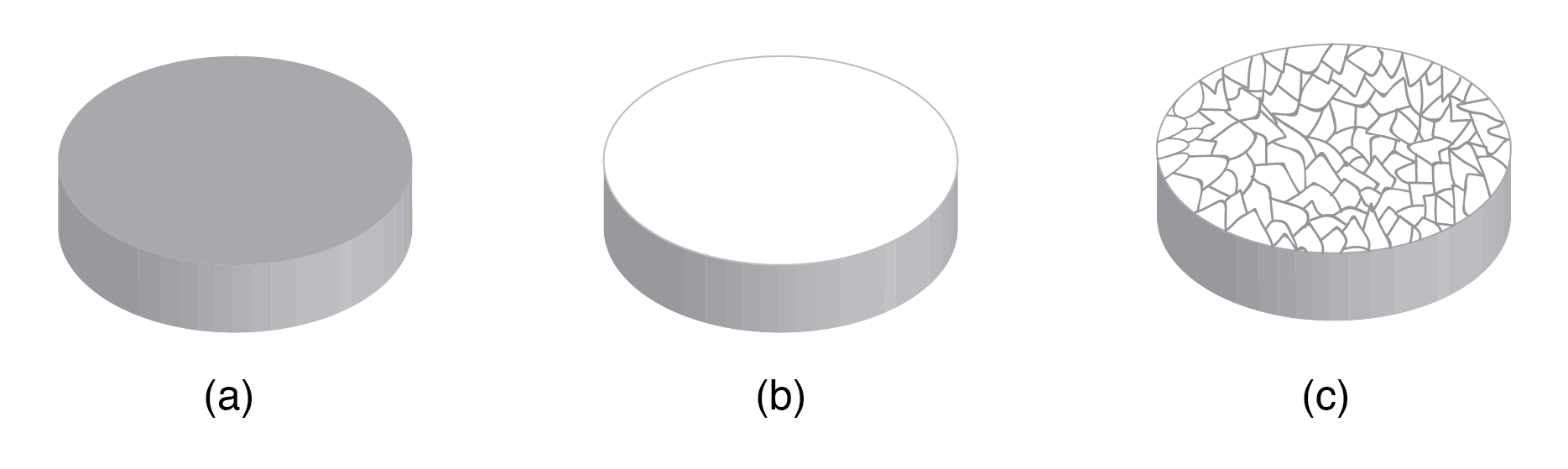
(a)金属サンプル、(b)研磨、(c)微結晶構造を示すための酸エッチング。
多くの金属は柔らかく、さまざまな金属加工技術によって簡単に変形します。微結晶は金属加工で変形します。また、価電子は結晶格子の周りを自由に動き、結晶から結晶へと自由に動きます。価電子は特定の原子に属しているのではなく、すべての原子に属しています。
下の図の剛直な結晶構造は、正のNaイオンと負のClイオンの規則的な繰り返しパターンで構成されています。 NaおよびCl原子はNa + を形成します およびCl - 自由電子なしで、NaからClに電子を移動することによってイオン。電子は結晶格子の周りを自由に移動できません。これは金属との違いです。また、イオンは含まれていません。イオンは結晶構造内の所定の位置に固定されています。ただし、NaCl結晶が水に溶解している場合、イオンは自由に動き回ることができます。しかし、クリスタルはもう存在しません。通常の繰り返し構造はなくなりました。水の蒸発によりNa + が堆積します およびCl - 反対に帯電したイオンが互いに引き合うため、新しい結晶の形のイオン。イオン性材料は、反対に帯電したイオンの強い静電引力により結晶構造を形成します。
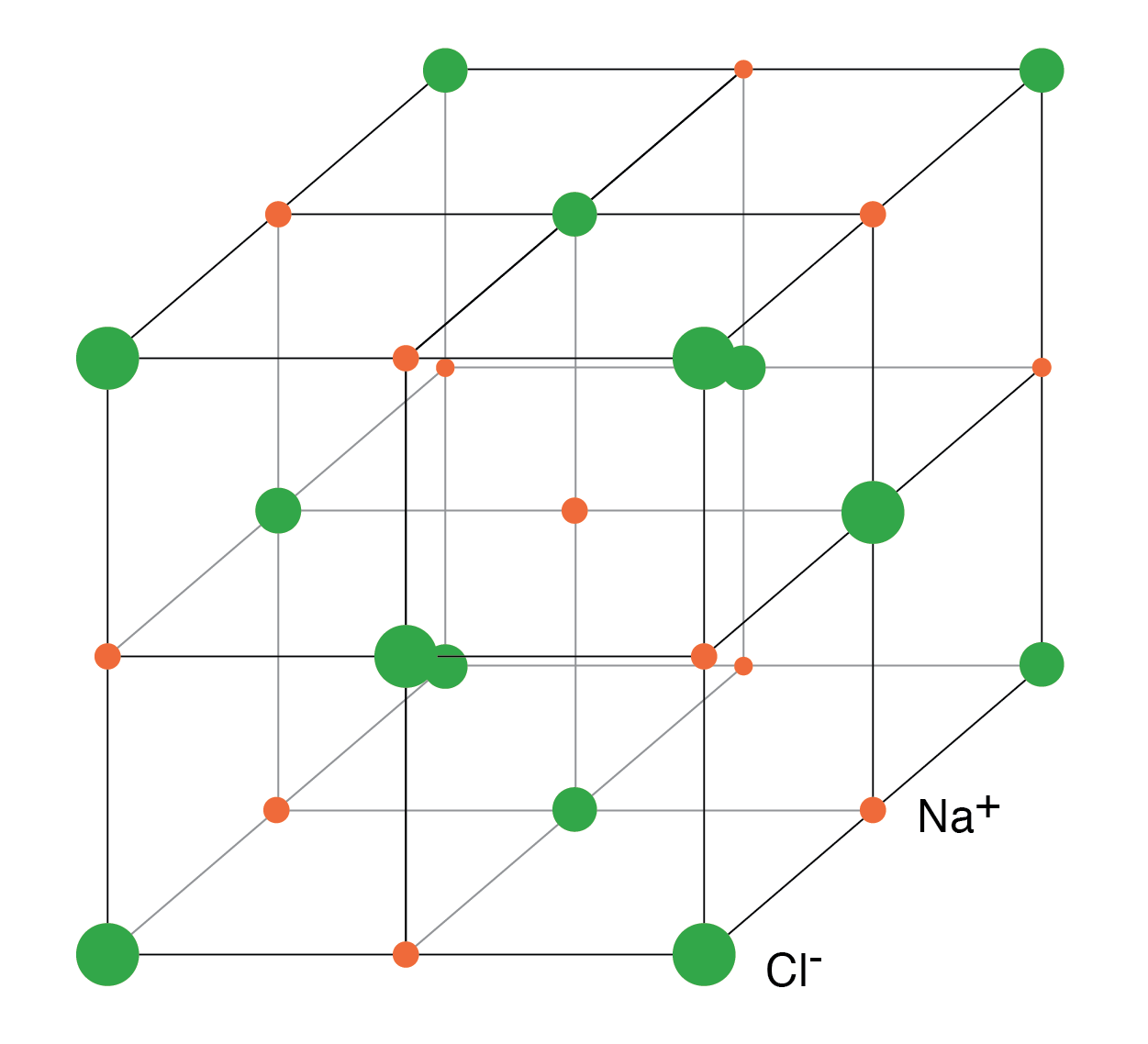
立方晶のNaCl結晶 グループ14(以前はグループIVの一部)の半導体は、原子の周りのsおよびp軌道電子を利用して四面体結合パターンを形成し、4つの隣接する原子と電子対結合を共有します。 (下の図(a))。グループ14の元素には、4つの外部電子があります。2つは球形のs軌道にあり、2つはp軌道にあります。 p軌道の1つが空いている。 3つのp軌道はs軌道と混成して、4つのsp 3 を形成します。 分子軌道。これらの4電子雲は、下の図に示すように、正の原子核に引き付けられて、Si原子の周りに等距離の四面体間隔で互いに反発します。
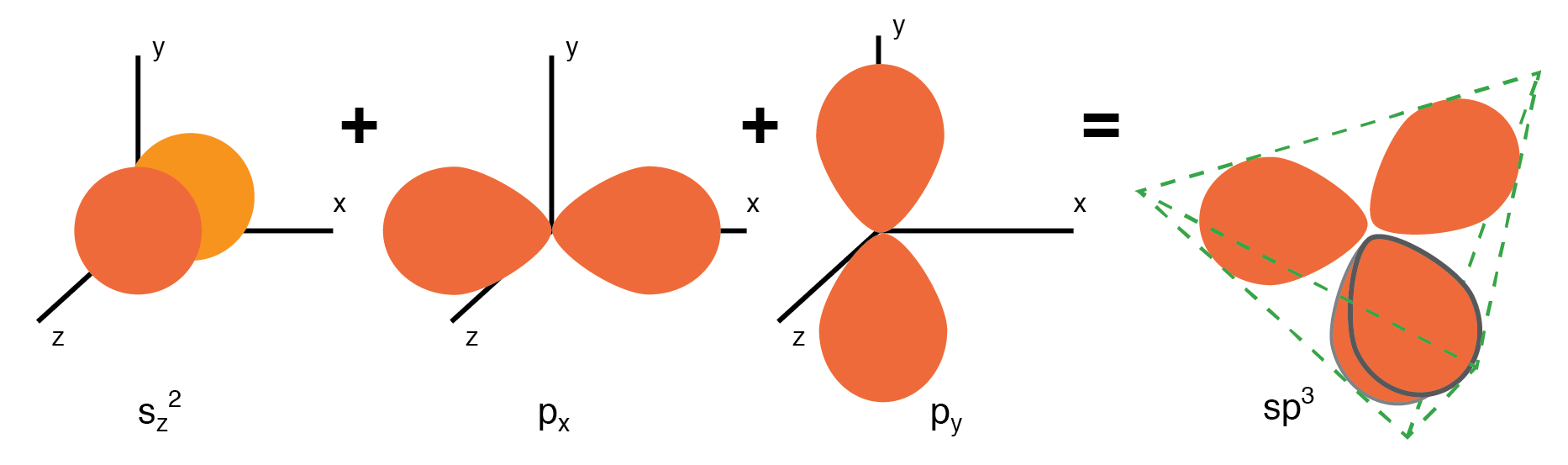
1つのs軌道電子と3つのp軌道電子が混成して4つのsp 3 を形成します。 分子軌道。
すべての半導体原子、Si、Ge、またはC(ダイヤモンド)は、共有結合によって他の4つの原子に化学的に結合しています。 、共有電子結合。それぞれが反対のスピン量子数を持っている場合、2つの電子は軌道を共有する可能性があります。したがって、不対電子は別の原子からの電子と軌道を共有する可能性があります。これは、下の(a)電子雲の重なり合った図または結合に対応します。下の図(b)は、下の図に示すダイヤモンド結晶構造ユニットセルの原点の体積の4分の1です。結合はダイヤモンドで特に強く、IV族からシリコンとゲルマニウムに向かって強度が低下します。シリコンとゲルマニウムはどちらもダイヤモンド構造の結晶を形成します。
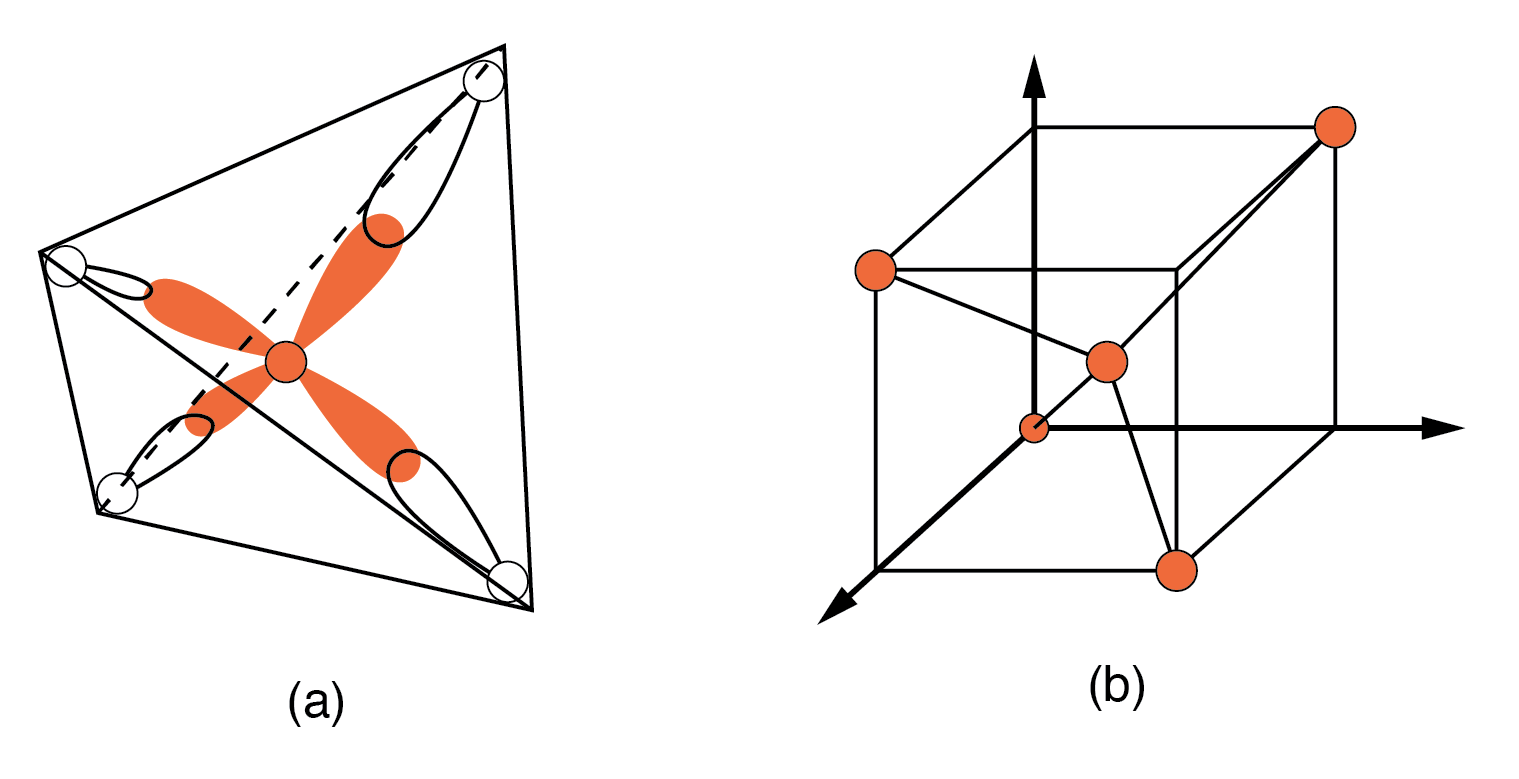
(a)Si原子の四面体結合。 (b)立方単位セルの1/4につながる
ダイヤモンドユニットセル 基本的な水晶の構成要素です。下の図は、セルのボリューム内で他の4つの原子に結合した4つの原子(暗い)を示しています。これは、上の図(b)の1つを下の図の原点に配置し、さらに3つを隣接する面に配置して、立方体全体を埋めるのと同じです。 6つの原子が6つの立方体の面のそれぞれの中央にあり、2つの結合を示しています。わかりやすくするために、隣接するキューブへの他の2つの結合は省略されています。 8つの立方体の角のうち、4つの原子が立方体内の原子に結合します。他の4つの原子はどこに結合していますか?他の4つは、結晶の隣接する立方体に結合します。四隅の原子は立方体に結合を示していませんが、結晶内のすべての原子は1つの巨大な分子に結合していることに注意してください。このユニットセルのコピーから半導体結晶が構築されます。
Si、Ge、およびC(ひし形)は、面を中心に配置された立方体を形成します。
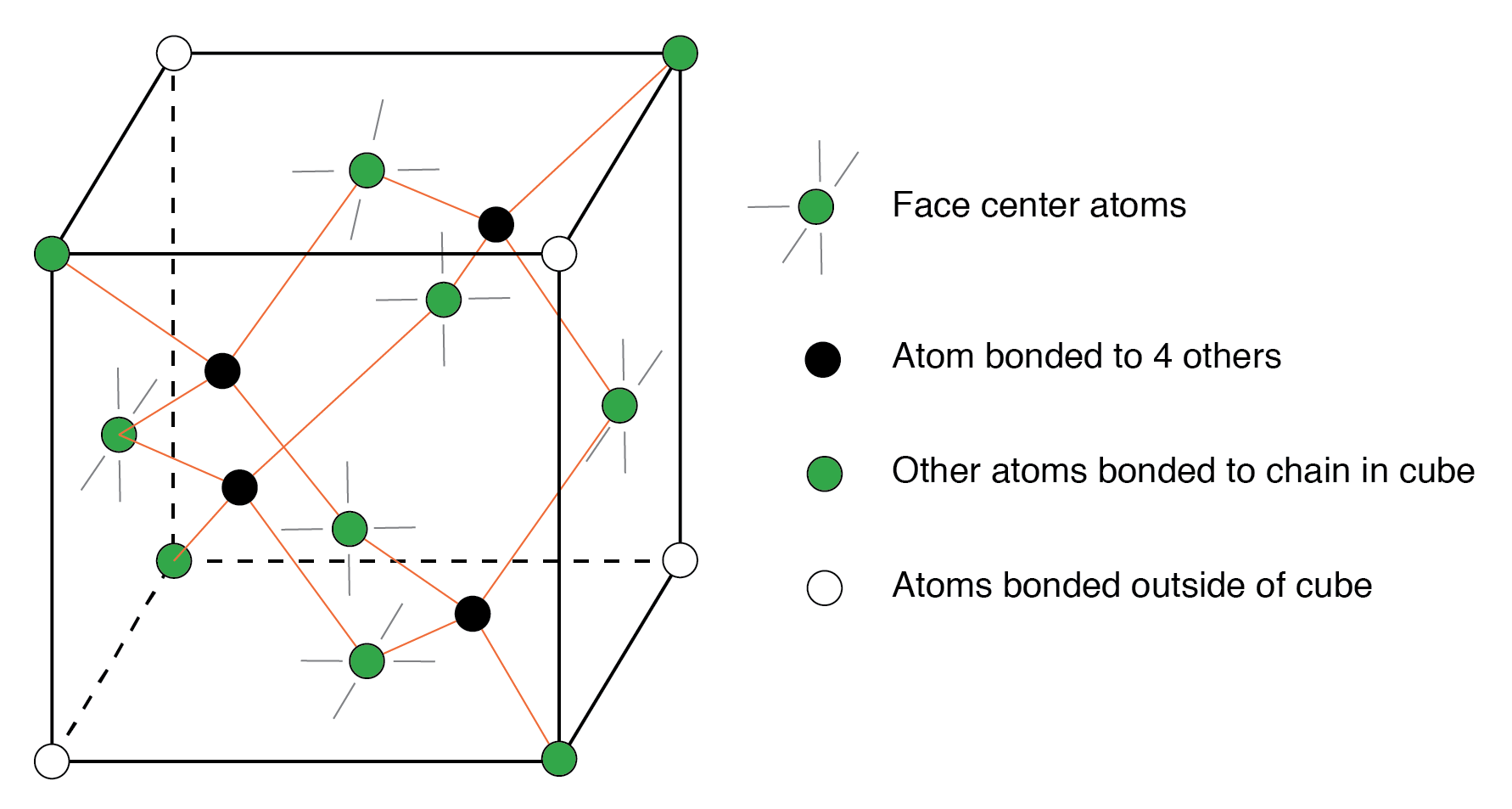
結晶は事実上1つの分子です。原子は他の4つに共有結合し、次に他の4つに結合します。結晶格子は比較的硬く、変形に抵抗します。結晶の周りの伝導のために自由になる電子はほとんどありません。半導体の特性は、電子が解放されると、正に帯電した空の空間が発達し、それが伝導にも寄与することです。
レビュー
- 原子は、8電子の完全な外側の原子価の殻(最も内側の殻の場合は2電子)を形成しようとします。原子は、数個の電子を寄付して、下にある8個の殻を露出させるか、数個の電子を受け入れて殻を完成させるか、電子を共有して殻を完成させることができます。
- 原子は、結晶と呼ばれる剛直な構造でイオンまたは原子の規則正しい配列を形成することがよくあります。
- 中性原子は、電子を提供することによって陽イオンを形成する場合があります。
- 中性原子は、電子を受け入れることによって負イオンを形成する可能性があります
- グループIVA半導体:C、Si、Geは結晶化してダイヤモンド構造になります。結晶内の各原子は巨大な分子の一部であり、他の4つの原子に結合しています。
- ほとんどの半導体デバイスは単結晶から製造されています。
関連ワークシート:
- 半導体ワークシートの電気伝導
産業技術



