超高感度グルコースセンシング用のメソポーラス酸化ニッケル(NiO)ナノペタル
要約
FTOコーティングされたガラス基板上に熱水成長したナノペタル(NP)形状のメソポーラスでよく整列した高密度酸化ニッケル(NiO)ナノ構造(NS)のグルコース検知特性が実証されています。 NiO-NPの構造研究に基づく調査は、X線回折(XRD)、電子および原子力顕微鏡、エネルギー分散型X線(EDX)、およびX線光電子分光法(XPS)によって実施されています。表面分析に使用されるBrunauer–Emmett–Teller(BET)測定は、表面活性ベースのグルコース検知アプリケーションに対するNiOの適合性を示唆しています。 NiO-NPs @ FTO電極にグルコースを固定化したグルコースセンサーは、3.9μA/μM/ cm 2 の高い直線性と高感度で、広範囲のグルコース濃度の検出を示します。 0.5Vの動作電位で。 1μMという低い検出限界と1秒未満の高速応答時間が観察されました。グルコースセンサー電極は、優れた干渉防止能力、安定性、再現性、再現性を備えており、アスコルビン酸(AA)、尿酸(UA)、ドーパミン酸(DA)に対して不活性な挙動を示すため、完全な非酵素的グルコースセンサーになります。
背景
糖尿病は、血糖値が血中で上昇し、診断も治療もされていない場合、健康に非常に危険であり、最終的には死に至る可能性がある慢性疾患です[1、2]。糖尿病の管理におけるさまざまな治療法には、病気の主な原因であるインスリンレベルの低下の結果としての血中のブドウ糖のレベルに応じた薬の投与量の調整が含まれます。したがって、血中レベルを感知するための正確で信頼性の高いグルコースセンサーは、糖尿病を管理する上で最も重要なパラメーターです。一般に、グルコースセンサーは、グルコースをグルコン酸とH 2 に変換する酵素であるグルコースオキシダーゼ(GOx)の使用に作用します。 O 2 [3,4,5,6,7]。グルコースの濃度は、過酸化物の形で水素が形成されるかどうか電極を流れる電子の数を監視することによって決定されます[8]。酵素バイオセンサーでは、作用電極上の物質(センサーとして機能する)の活性領域と反応する物質(検知される)の結果として電位を制御し、電流を測定することによって、定量的検知が行われます。同じ原理で動作する酵素グルコースセンサーは、グルコースに対して高い感度を示します。これらのセンサーの制限には、寿命の短さ、温度、pH値などの環境条件、使用する化学物質の毒性などがあります。これらの問題に対処するために、最近、多くの金属酸化物ベースの非酵素的グルコースセンサーが開発されました[9、10、11、12、13、14]。これらの非酵素的グルコースセンサーの検知メカニズムは、電極表面近くの金属酸化物イオンによるグルコースのグルコノラクトンへの酸化に基づいています。電気化学的センシングでは、サイクリックボルタンメトリー(CV)は、低い検出限界での高感度、正確な定量分析、および高速で明確な特性評価により、効率的な手法であることが証明されています[15、16]。これらの酸化物ベースのグルコースセンサーは確かに実際の診断に使用される可能性があり、さらなる研究が必要です。
NiO、CuO、TiO 2 などの低コストの金属酸化物材料を使用した電極の製造に対する関心が高まっています。 、ZnO、および電気触媒活性を改善することによってグルコースに対して高い感度を示すことができる複合材料[17、18、19、20、21、22、23、24]。反応ベースのセンシングに関しては、ナノマテリアルは反応のためにより多くの表面積を提供し、したがってより良いセンシングを提供できるため、興味深い可能性があります。最近では、ナノ構造のさまざまな材料が、センシング、エレクトロニクス、オプトエレクトロニクスにおいて大きな可能性を示しています[25、26、27]。ナノ構造について確立された事実は、そのサイズおよび/または形態を変更することによって物理的特性を調整する能力であり、多様な用途で使用されるナノ材料に多様性を与えます。したがって、センサーの場合、電極表面の設計も重要なパラメーターの1つです。中でも、Niベースのナノ材料は、触媒作用[28,29,30]や、表面積対体積比が大きいために高い感度など、優れた特性を示します。経済的でありながら感度の高いグルコースセンサーは、デバイスを適切に設計し、材料を合成することにより、NiOナノ構造ベースのセンサーで実現できます。この論文では、電気化学的研究によるグルコース検知のための花びらのようなNiOナノ構造からなる作用電極を、活性化合物として使用するために作製しました。フルオレンをドープした酸化スズ(FTO)でコーティングされた導電性ガラス基板は、熱水技術によってNiOナノ構造(NS)を成長させるために使用されてきました。
実験的
少量のアンモニウム溶液の存在下で過硫酸カリウムと混合された硝酸ニッケル前駆体は、これらのNiONSの調製中の配向に使用されてきました。 150°Cで5時間連続加熱した後、堆積したフィルムを脱イオン水ですすぎ、空気中で乾燥させました。続いて、NiO-NSsフィルムを250°Cで2時間アニールしました。 FTOコーティングされたガラスの導電性表面上に均一でよく整列したNiONSが得られました。フィルムの微細構造は、XRD(単色Cu-Kα放射線を使用したRigaku SmartLabX線回折計λによって調査されました。 =1.54Å)と電子顕微鏡(Supra55 Zeiss)。元素の確認には、エネルギー分散型X線分光法(Oxford Instrument)とAlKα線(1486.6 eV)を使用したX線光電子分光計(ESCA System、SPECS GmbH、ドイツ)を使用しました。原子間力顕微鏡はBruker(MultiMode 8-HR)マシンで実行され、高解像度ナノ構造の分析はWSxMソフトウェアを使用して実行されました[31]。 NiO-NSを使用したグルコース検知では、Keithley2450-EC電気化学ワークステーションを使用して適切な電気化学測定が実行されています。 Brunauer–Emmett–Teller(BET)メソッドは、Autosorb iQバージョン1.11(Quantachrome Instruments)でも表面分析に使用されました。
結果と考察
NiO NSの微細構造の詳細と形態は、電子顕微鏡と原子間力顕微鏡(AFM)を使用して研究されています。図1aは、FTOコーティングされた導電性ガラス基板上に成長した非常に高密度のバラの花びらのような構造を示しています。これらの花びらの厚さは約25〜30 nmで、その上に構造物のような非常に細いとげがあります。フィルムは緻密で、100ミクロン以上にわたって均一です。より広い領域にわたる均一性により、センシングアプリケーションに適しています。 NiO NSの断面図は、図1aの挿入図で見ることができます。これは、垂直方向の配置と花びらの高さを示しています。これらのNiONSのTEM顕微鏡写真は、追加ファイル1:図S1で確認できます。図1bは、NiOナノペタルのSEM画像を示しており、均一なNiONPが広範囲に成長していることを示しています。これらのナノペタルの形状とサイズの詳細は、図1c–eのAFM画像を使用して調査されています。図1c、dは、それぞれ2次元および3次元のAFM画像を示しています。高密度のナノペタル(NP)が垂直に並んだ、ほぼ均一に分布したペタルを示しています。図1eと図1cの挿入図のAFM画像は、より高い解像度のNiONSを示しています。図1eの黒い線は、ナノ構造のラインプロファイリングを示しており、NPの平均厚さに関する情報を提供します。ナノペタルの幅が約25〜30nmの範囲にあることは明らかです。図1fのエネルギー分散型X線(EDX)スペクトルは、適切なNi / O比を持つ高純度のNiONSを示唆するNiONPの化学組成を示しています。元素スズ(Sn)に対応するいくつかのピークは、基板として使用されるFTOコーティングされたガラスからも見ることができます。図1は、花びら状の高密度NiO NSが、FTOコーティングされたガラス基板上にある程度の多孔性を伴って均一に製造されていることを明確に示しています。

a 、 b 断面図(挿入図)で花びらのような構造を示すNiOナノ構造の表面形態。 c – e ラインプロファイリングを使用したAFM画像。 f 元素配座のEDXスペクトル
X線光電子分光法(XPS)は、NiOナノペタルの成分と表面化学組成の分析のために実行されます。 XPSサーベイスキャン(図2a)は、EDXの結果と一致するスズ(Sn)の基質ピークを持つニッケルと酸素の組成を示しています。約855.7eV(2p 3/2 )に2つの特徴的なNi2pピークが観察されます。 )および873.4 eV(2p 1/2 )高解像度スキャンで(図2b)。デコンボリューションされたスペクトルには7つのピークが含まれ、855.7と873.4eVに2つの強いピークがあり、Ni 2+ に対応します。 Ni–O結合では、2つの衛星(弱い)ピークがあります[32]。図2cのXRDパターンは、XRDピーク強度の降順で、それぞれ43°、37°、63°、76°、79°の回折ピークを明確に示しています。ピーク位置とそれらの相対強度は、NiO-NSの面心立方(FCC)構造とよく一致しており、NPの結晶性を示しています[33]。準備された基板の上記の形態学的および構造的特性は、NiOの低次元の花びらのような構造の存在を予測し、同じことが可能なグルコース検知特性について調査されます。
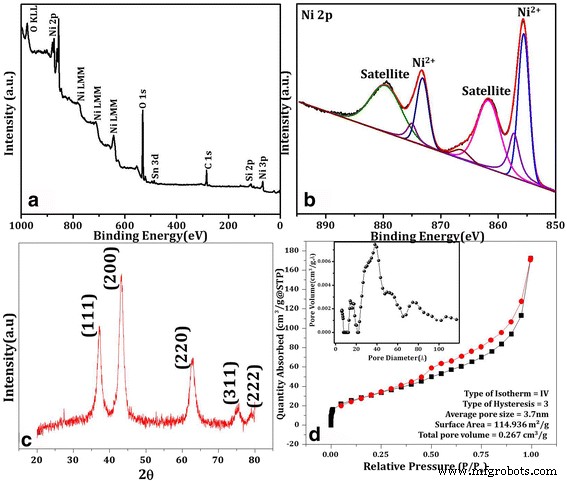
XPS a を使用して製造されたNiOナノペタルの成分分析 調査スキャン、 b 2p Niのディープスキャン、 c 構造解析用のXRD、および d N 2 によるBET等温線測定を使用した表面積とテキストの研究 吸着/脱着
先に述べたように、検知メカニズムの基礎は、グルコースとNiOの反応性であるため、より高い表面積が必要です。これは、検知特性を調査する前に分析する必要があります。比表面積および等温線のタイプ、平均細孔サイズ、総細孔容積などの他のパラメータは、 N によって取得されています。 2 BET法による吸着・脱着。図2dは、相対圧力範囲0.025≤ P で77Kで測定した場合の、タイプIVの等温線とタイプH3のヒステリシスを示しています。 / P 0 ≤1.00[18]。 P でBETおよびLangmuirメソッドによって推定された測定表面積 / P 0 0.05〜0.30の範囲は、114.936 m 2 であることがわかります。 / gおよび約3.7nmの細孔径分布。これは、NiONPがメソポーラスで細孔径分布が比較的均一であることを示しています。サンプルの総細孔容積は0.267cm 3 であることがわかります。 / g相対圧力( P )で推定 / P 0 )0.99。
NiO-NPのグルコース検知に利用できる適切な表面は、図3に示すように電気化学的CV測定を使用して以下で調査されました。CV測定には、NiO-NPs @FTOサンプルを作用電極として使用する3電極システムが採用されています。 、Ag / AgCl(1 M KCl)および白金線をそれぞれ参照電極および対極として使用します。図3aは、 I を示しています – V 10〜100 mV / sの間で変化するさまざまな電圧掃引速度の曲線。 CVスキャンを3000サイクル繰り返すことでテストしたところ、電極は非常に安定しています(追加ファイル1:図S2)。図3aから明らかなように、電流は〜0.25 mA / cm 2 10 mV / sのスキャン速度で流れていて(黒い曲線)、〜2.5 mA / cm 2 に増加します スキャン速度を100mV / sに上げたとき(薄緑色の曲線)。スキャンレートを10倍に増やすことによる電流の10倍の増加は、2つの間の線形変化を意味します。図3aの挿入図に示されているように、スキャンレートの関数としての電流のこのような線形変化は、ほとんどの場合、表面制御された反応に起因するものとして割り当てられ、センシングアプリケーションに適しています。
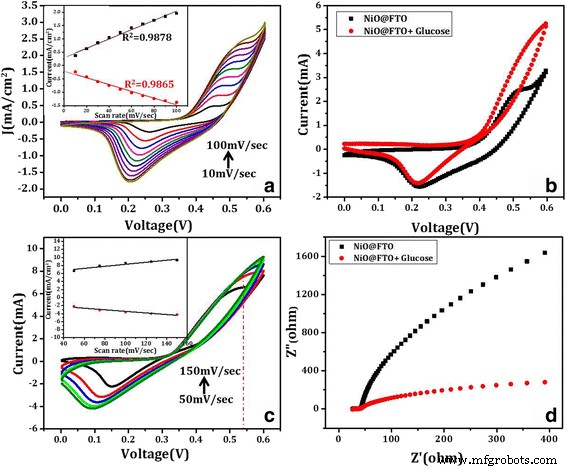
a さまざまなスキャンレートでのNiO-NPs @ FTOのサイクリックボルタンメトリー(CV)。 b CV技術を使用した電気化学グルコース(10μM)センシング。 c さまざまなスキャンレートでのグルコース固定化NiO-NPs @ FTO電極のCVスキャン。 b グルコースセンシングを示すための電気化学インピーダンス分光法(EIS)。 a の挿入図 および c スキャンレートの関数としての電流の線形変化を示します
センシング研究のために、CV測定は、作用電極としてNiO NSsフィルム(NiO-NPs @ FTO)を使用し、50 mV / sのスキャン速度で、グルコース(5 mM)を使用した場合と使用しない場合(黒)で実行されました。図3bに示すように、0.1 MNaOH電解質の存在。グルコースの存在下でさまざまなスキャンレートで記録されたCVプロットも図3cに示されています。これは、非グルコースの場合と比較して電流値が増加し、スキャンレートが増加するとさらに増加することを示しています。図3cのこのスキャン速度に依存するCV曲線は、グルコース検知と表面制御反応に関する上記の説明と一致しています。図3bの黒と赤の曲線からわかるように、反応のピーク電流が観察されます。これは、NiO-NPs @ FTO電極が0.0〜0.6Vの電位範囲でレドックス反応を起こすことを示しています。ピーク電流値は2倍になります。グルコースの存在下、すなわち、グルコースを含むNiO-NPs @ FTO電極の電流は、グルコースを含まないものよりも大きく、これは、NiONSのより大きな表面積内に固定化されたグルコース分子の酸化に起因する可能性がある。これは、適切な部位で起こる以下の酸化還元反応によってサポートできるように、グルコース感知の最も可能性の高いメカニズムであるように思われます。
$$ \ mathrm {NiO} + {\ mathrm {H}} _ 2 \ mathrm {O} \ to \ mathrm {NiO} \ mathrm {OH} $$(1)$$ \ mathrm {NiO} \ mathrm {OH} + \ mathrm {glucose} \ to \ mathrm {NiO} + {\ mathrm {H}} _ 2 {\ mathrm {O}} _ 2 + \ mathrm {gluconolactone} $$(2)$$ \ mathrm {Gluconolactone} \ to \ mathrm {gluconic} \ \ mathrm {acid} $$(3)$$ \ mathrm {Gluconic} \ \ mathrm {acid} + {\ mathrm {H}} _ 2 \ mathrm {O} \ to {\ mathrm {gluconate} } ^ {\ hbox {-}} + {\ mathrm {H}} ^ {+} $$(4)CV測定中、Ni 2+ 酸化してNi 3+ NiO-NPs @ FTO電極のセルに存在する電解質水溶液による(反応1)。酸化されたNi 3+ ブドウ糖の触媒として働き、それ自体を還元することによってブドウ糖を酸化します(反応2)。酸化すると、グルコースはグルコノラクトンに変換され、その結果、すぐにグルコン酸に変換され(反応3)、この化合物は水分子と反応してグルコン酸塩とヒドロニウムイオンを形成します(反応4)。作用電極の表面近くにあるこれらのイオンは、3.9μA/μM/ cm 2 という非常に優れた比感度で検出可能な信号として電流を増加させます。 。
「グルコースドーピング」によって誘発される電気伝導率の向上をさらにサポートするために、NiO NPで製造された作用電極の電気化学インピーダンス分光法(EIS)が、グルコースの有無で測定されました(図3d)。図3dのナイキスト(コールコール)プロットでは、高周波領域の単一の凹んだ半円と低周波領域の傾斜した線を見ることができます。一般に、高周波の半円は電解液中に存在するグルコースとNiOナノ構造界面との間の電気化学的反応インピーダンスを示し、低周波領域の傾斜線は活物質(NiO)と導電性電極の界面インピーダンスを示します[34]。図3dのコールコールプロットに対するグルコースの影響は明確に区別できるため、同じ測定値を使用してグルコースの存在を検出できます。これは、ナノペタル型のNiONSである材料のグルコース検知特性を明確に示しています。
デバイスの再現性は、実際のセンサーとして効果的なパフォーマンスを実現するための重要なパラメーターの1つです。図4aは、CVおよびアンペロメトリー技術を使用したグルコース検知用の電気化学セルです。図4bは、100μM〜1.2mMのさまざまなグルコース濃度が存在する場合のNiO-NPs @ FTOのCVスキャンに対応しています。図4cは、線形フィッティングファクター( R )を持つ電流密度とグルコース濃度の線形関係を示しています。 2 )0.9948の。図4dは、+ 0.5Vで検出された0.1M NaOH電解質中のさまざまな量のグルコース水溶液の添加時のNiO-NPs @ FTO電極のアンペロメトリー挙動を示しています。このバイアスでは、NiO-NPs @FTO電極は電流の系統的な変化を示します濃度の50μLのグルコース溶液の場合、1μMが電解質に追加されます。さらに、排他的なグルコース感知挙動を説明するために、グルコース様尿酸(UA)、アスコルビン酸(AA)、および葉酸(FA)とともに存在する他の化合物の効果を、対照実験を実施することによってチェックした。さまざまな濃度での言及された種の応答は、57秒と65秒でこれらの酵素を追加することによって研究されました(図4dでマークされた矢印)。これは、アンペロメトリー測定中に電流に有意な変化を示さないのに対し、グルコースは60秒の間に追加されたときに検出されました。 2番目。他の化合物と比較したグルコースセンシングの選択性は、追加ファイル1:図S3でより明確に確認できます。もう1つの重要な観察結果は、グルコースによって誘発されたスパイク後の電流の減少です。これにより、センサーが再利用可能になります。 NiO NS電極は、最近のグルコース検知電極のいくつかをまとめた表1に示されているように、他のさまざまなセンサー電極と比較して非常に優れた感度を示しています。 NiO NSベースの電極の優れた感度(表1の下の行)は、必要に応じて血液や食品などの実際のサンプルでさらに研究を行うことができるグルコース検知アプリケーションの優れた候補になります。
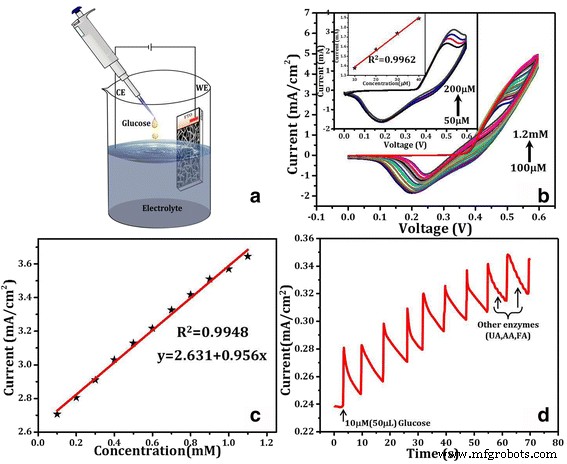
a 支持電解質NaOH(0.1 M)を備えた作用電極としてNiO-NPs @FTOを使用した電気化学的グルコース検知セットアップの概略図。 b 挿入図の拡大図を使用したCVスキャン中の50μMの連続グルコース添加。 c グルコース濃度と電流の線形関係 d 10μMのグルコース添加でのアンペロメトリー応答(+ 0.5Vで)
結論
要約すると、高表面積対体積比を備えた、熱水成長した高密度の整列したNiOナノ構造(NS)を備えた電極を使用することにより、感度が向上した優れたグルコース検知挙動が達成されました。単純な技術によって成長したNiONSは、他のいくつかの技術によって成長した対応物と比較して、安定性と感度の点で優れたグルコース検知能力を示します。提案されたセンサー電極は、3.9μA/μM/ cm 2 の高い比感度でグルコース濃度の幅広い検出を示します。 1秒未満の高速応答時間。これに加えて、アスコルビン酸、葉酸、尿酸などのグルコースに存在する他の酵素に対して不活性な応答を示し、効率的な非酵素的グルコースセンサーになります。これらすべての得られた結果は、提案されたグルコースセンサーが薬物、ヒト血清中のグルコース濃度をモニタリングするための効率的な分析ツールであり、生物医学関連のアプリケーションで使用できることを示しています。
ナノマテリアル
- 化学センシング用の貴金属ナノ粒子で装飾されたエレクトロスピニングポリマーナノファイバー
- 薄膜トランジスタ用の酸化インジウムナノフィルムの原子層堆積
- 中空多孔質NiOに基づく高感度の非酵素的電気化学的グルコース検出
- 非酵素的グルコースセンサーの長期保存のためのα-NiSナノスフェアフィルムを合成するための硫化温度の操作
- 潜在的な創傷治癒用途のためのエレクトロスピニングされたキトサン-ポリエチレンオキシド/フィブリノーゲンバイオコンポジットの開発
- 高性能スーパーキャパシタ用の2次元VO2メソポーラスマイクロアレイ
- ミルストーン剥離:大型の数層酸化グラフェンの真のせん断剥離
- ナトリウムイオン電池の高性能アノード材料用の酸化ケイ素のその場磁気熱還元から生成されたメソポーラスシリコンミクロスフェア
- 人間の発汗感知のための澱粉紙ベースの摩擦電気ナノ発電機
- 超高感度バイオセンサー用のグラフェンベースのデバイス
- ニッケル合金 400 の用途



