ポリオール媒介プロセスによるZnOナノクリップの製造と特性評価
要約
酢酸亜鉛水和物(Zn(OAc) 2 を使用して、単分散性の高いZnOナノクリップを正常に調製しました。 ・nH 2 O)単純な溶液ベースの経路-ポリオールプロセスによるZn源および溶媒としてのエチレングリコール(EG)として。溶液濃度がZnOナノクリップの形成に及ぼす影響が深く研究されています。まず、0.01 M Zn(OAc) 2 ・nH 2 Oは、水やアルカリを添加しなくてもEGと反応し、170°Cで多結晶ウルツ鉱構造のZnOナノクリップを生成します。合成されたままのZnOナノクリップには、88 m 2 の高い比表面積を持つ多数の凝集ナノ結晶(〜5〜15 nm)が含まれています。 / g。 ZnOナノクリップの形状は基本的に一定に保たれ、400〜600°Cでアニーリングした後の結晶化度が向上します。より低い溶液濃度とわずかな量のH 2 OはZnOナノクリップの形成に決定的な役割を果たします。溶液濃度が≤0.0125Mの場合、Zn(OAc) 2 間の錯化および重合反応 ・nH 2 OとEGが優勢であり、主にZnOナノクリップを作り上げています。溶液濃度が≥0.015Mの場合、Zn(OAc) 2 のアルコール分解および重縮合反応 ・nH 2 OとEGが優勢になり、球形と楕円形のZnO粒子が形成されます。 Zn(OAc) 2 の錯化とアルコール分解の競合に基づく可能な成長メカニズム ・nH 2 OとEGが提案されています。
背景
直接ワイドバンドギャップが3.37eV、励起結合エネルギーが60 meVの酸化亜鉛(ZnO)は、光触媒、太陽電池、電気・光学デバイスへの応用により、近年大きな注目を集めています[1,2 、3,4,5,6,7,8,9,10]。 ZnOには、ナノスフェア、ナノロッド、ナノワイヤー、ナノフラワーなどの非常に豊富なナノ構造があります[11、12、13、14、15、16]。 ZnOナノ構造を生成するためにさまざまな合成方法が利用されてきました[17、18、19、20、21、22]。これらの方法の中で、溶液ベースのポリオールプロセスは、高沸点(最大250°C)や錯化、還元、界面活性剤などの独自の溶媒特性により、無機化合物(金属、酸化物、ヒドロキシアセテート)の調製に優れた利点を示します。それらの両親媒性の特徴に加えて、特性[23,24,25]。過去数十年の間に、ポリオールを介したアプローチから派生したさまざまなサイズと形態のZnOナノ粒子が広く研究されてきました。ポリオール、反応温度と濃度、陰イオン、加水分解またはアルカリ比、および添加剤の処理パラメーターは、ZnO粒子のサイズと形態に大きな影響を及ぼします[11、12、13、14、15、16、17、18、19、 20,21,22,23,24,25,26,27,28,29,30,31]。 20〜500 nmのサイズの球状酸化物粒子は、エチレングリコール(EG)を溶媒として使用し、Zn(OAc) 2 を使用すると、頻繁に形態が変化します。 ・2H 2 亜鉛源としてのO [23、28、30]。多結晶球を形成するためのZnOナノ結晶ユニットの凝集挙動が確認されています[18、24、26、27]。
この作業では、酢酸亜鉛水和物(Zn(OAc) 2 を使用した単純なポリオールプロセスにより、初めてZnOナノクリップを作成することに成功しました。 ・nH 2 O、 n <2)および追加のH 2 なしのEG Oまたは他の添加剤。溶液濃度が形態に及ぼす影響を深く調査し、考えられる成長メカニズムを提案しました。
メソッド
すべての試薬は分析グレードであり、さらに精製することなく使用しました。酢酸亜鉛水和物9.2mg(Zn(OAc) 2 ・nH 2 O、 n <2)を5 mLのエチレングリコール(EG)に溶解し、約0.01 mol / L(M)の無色の溶液を得ました。次に、溶液をホットプレート上でマグネチックスターラーで1〜3時間170°Cに加熱しました。溶液は6〜7分後に濁り始め、乳白色の凝集塊が形成された。反応が終了する間、沈殿物を遠心分離し、エタノールと脱イオン水(体積比4:1)で2000〜3000 rpmで数回洗浄し、構造的および形態学的特性評価のために室温で一晩乾燥させました。一部のサンプルは、管状炉内で400および600°Cで2時間、空気中で2°C /分のランプ速度でアニーリングされました。さまざまなZn(OAc) 2 を含むソリューション ・nH 2 溶液濃度の影響を調べるために、0.005、0.125、0.015、0.05、および0.2MのO濃度も準備しました。
サンプルの結晶化度と位相は、Cukα放射線(λ)を使用したX線回折計(D / max 2000、リガク)によって評価されました。 =1.5405Å)。形態学的観察は、走査型電子顕微鏡法(SEM; Quanta(商標)50、FEI)および透過型電子顕微鏡法(TEM; Tecnai G2 F20、フィリップス)によって実施された。準備されたままのサンプルの熱安定性は、20°C /分の加熱速度での空気流における熱重量分析-微分熱重力分析(TG-DTG; STA 409 PC、Netszch)によって特徴づけられました。調製およびアニーリングされたままのサンプルのフーリエ変換赤外スペクトル(FTIR)は、4000〜400 cm − 1 で収集されました。 プレスされたKBrペレットを使用したFTIR分光計(FTIR; Spectrum、PerkinElmer)による範囲。 Brunauer-Emmett-Teller(BET)の比表面積は、表面積装置(TriStar-3000、Micromeritics)によって推定されました。さらに、アニールされたサンプルの光学特性は、紫外可視近赤外光線(UV-可視-NIR)分光光度計(UV-3600、島津製作所)を介して測定されました。
結果と考察
ZnOナノクリップの形態
いくつかの文献[23、28、30]に基づいて、球状または楕円形のZnOナノ粒子は、Zn(OAc) 2 を使用してEG溶媒中で形成できます。 ・2H 2 160または198°CでのZn源としてのO。ただし、5 mL 0.01 M Zn(OAc) 2 の処理条件下では ・nH 2 追加のH 2 を追加せずに、170°Cの反応温度で2時間のO溶液 図1に示すように、単分散性の高いO、ZnOナノクリップは、単純なポリオールプロセスによって製造されています。調製したままのサンプルは、大量のクリップとわずかなナノ粒子を含む明確なクリップのような形態を示します(図1a)。 600°Cのアニーリング後、形態は基本的に変化しません(図1b)。また、図1cに示すように、400°CでアニールしたZnOサンプルに対してTEMおよび高分解能TEM(HRTEM)観察を行いました。そして、ナノクリップの形態を再び観察することができます。 400°Cのサンプルの局所倍率のHRTEM写真に基づくと、ZnOクリップは多結晶構造を持つ多数の凝集したナノ結晶(〜3〜15 nm)で構成されていることがわかります。図1dは、幅(W)が50〜100 nm、長さ(L)が〜1〜3μm、直径(D)が10〜30nmの1つのZnOナノクリップのスケッチ図を示しています。 ZnOは非常に豊富なナノ構造を持っていますが、ナノクリップのような形態は、特に単純なポリオール媒介アプローチでは報告されていない、私たちの知る限り、依然として非常にユニークで斬新です。

( a のSEM画像 )準備済みおよび( b )600°CでアニールされたZnOナノクリップサンプル。 ( c のTEM画像 )400°CでアニールされたZnOナノクリップ。 ( c の挿入図 )は、局所倍率の対応するHRTEM画像です。 ( d )ZnOナノクリップのスケッチ図
ZnOナノクリップの構造
図2aは、準備されたままの400および600°CでアニールされたZnOナノクリップのX線回折(XRD)パターンを示しています。準備されたままのZnOクリップは、ほとんどが六角形のウルツ鉱相(JCPDS36-1451)で結晶化されています。かなりの数のXRDピークが(100)、(002)、(101)、(102)、(110)、(103)、(112)、および(201)面に由来し、ZnOナノクリップの多結晶性を示しています、上記のHRTEM結果とよく一致しています(図1c)。 400および600°Cのアニーリング後、これらのXRDはより強く、より鋭くなり、結晶化度が向上したことを証明します。 (101)、(100)、および(002)の3つの強いピークの半値全幅(FWHM)に基づいて、合成されたままの400および600°Cのナノクリップの平均結晶子サイズは次のように計算されます。 Scherrerの式を使用すると、それぞれ約11.5、21.0、および24.8nmになります。明らかに、アニーリングはZnOナノクリップの結晶化度を大幅に改善し、ナノクリップを形成するナノ結晶の平均サイズを増加させます。ただし、大量のSEM観察に基づくと、ナノクリップの形態とサイズに大きな変化はありません。
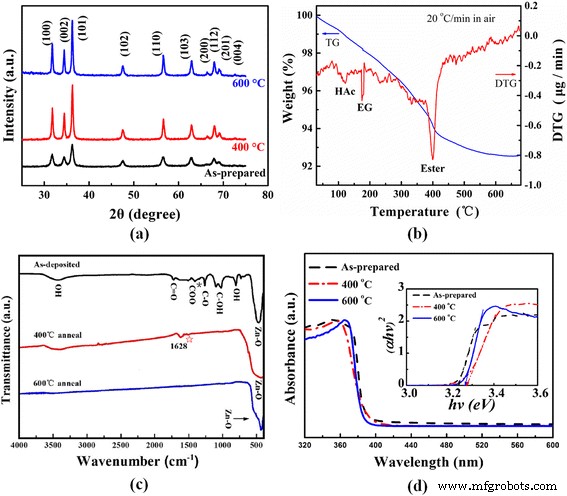
( a )準備されたままの400および600°CでアニールされたZnOナノクリップサンプルのXRDパターン。 ( b )空気中で加熱された調製されたままのZnOナノクリップのTG-DTG曲線。 ( c )準備されたままの400および600°CでアニールされたZnOナノクリップサンプルのFTIRスペクトル。 ( d )調製したままの400および600°CでアニールしたZnOナノクリップサンプルのUV-可視吸収スペクトル。 ( d の挿入図 )は(αhvの対応する曲線です ) 2 hv への依存
図2bは、700°Cまでの空気中で20°C /分の加熱速度で調製されたままのZnOナノクリップのTG-DTG曲線を記録しています。 DTG曲線は、酢酸とEGの揮発、およびエステルの激しい分解と燃焼にそれぞれ関連する、118、180、および400°C付近に3つの重量損失ピークを示しています。 TG曲線は、室温から600°Cまでの少量(〜7%)の重量減少を確認します。 600°C後、600°CでアニールされたZnOサンプルの次のFTIR結果に従って、ZnOナノクリップ内の有機種が完全に除去されるため、重量は基本的に変化しません(図2c)。
図2cは、調製したままの400および600°CでアニールしたZnOナノクリップサンプルのFTIRスペクトルを示しています。調製されたままの生成物は、いくつかの有機基またはZnOに起因するいくつかの吸収帯を示す。 400〜600cmの強い吸着帯 − 1 低波数領域でのZn–Oの伸縮振動モードに由来し、ZnOの形成を示しています。 800cm付近のピーク − 1 はアルコール中のOH結合の伸縮振動モードに割り当てられ、吸収帯は1020〜1090 cm − 1 の範囲にあります。 C–OH結合に属します。これは、調製したままのサンプルに少量のポリオールが含まれていることを示しています。 1260および1727cm − 1 のピーク これは、C–OおよびC =O結合の伸縮振動に起因します。これは、調製されたままの状態でエステルまたはグリコレートが存在することを意味します。約1587および1413cmの2つの吸収帯 − 1 アセテート(COO)グループのC =OとC–Oの非対称および対称伸縮振動にそれぞれ対応します[3、20、26]。 130〜200 cm − 1 の範囲での非対称および対称カルボン酸塩伸縮バンド(Δ)間の分割 架橋錯体の典型です[32]。ここで、174cm − 1 のΔ値 は、合成されたままのZnOナノクリップのブリッジングボンディングモードを示唆しています。さらに、1343 cm − 1 にある小さな吸収ピーク(*で示される) これは、弱く結合した酢酸分子によるものであり、以前の報告[11、26]と一致して、合成されたままのZnOナノクリップの表面にわずかな酢酸が吸着されていることを示唆しています。
400°Cのアニーリング後、1587 cm − 1 の非常に弱い吸収ピーク(☆で示される)を除く 図2bのTG-DTGの結果と一致して、C =Oの場合、HAc、エステル、およびEGからの他のIR吸収帯は消失しています。さらに、1628cm − 1 の吸収帯 水和または水吸着の曲げ振動に起因します[26]。 3440cmの高波数範囲の弱い広帯域 − 1 400°Cのアニーリングの前後の両方で、金属酸化物の表面にヒドロキシル基が存在することを確認します。 600°Cのアニーリング後、有機化合物とヒドロキシル基が完全に除去されます。 434cmの強いバンドのみ − 1 Zn–Oによる伸縮振動が観察され、600°Cでの純粋なZnO形成を示しています。 400および600°Cのアニーリング後のZn–Oピークシフトと広がりは、結晶化度の改善、結晶子サイズ、および有機種/不純物の減少に関連している可能性があります。
ZnOナノクリップの光学特性と比表面積
図2dは、調製したままの400および600°CでアニールしたZnOナノクリップサンプルのUV-可視吸収スペクトルを示しています。 (d)の挿入図は、(αhvの対応する曲線です。 ) 2 hv への依存 。強い吸収は約390nm以下で発生します。
ZnOの直接バンドギャップ(Eg)は、(αhvによって推定できます。 ) 2 = c ( hv − 例 )[33]、ここでα は吸収係数であり、 hv は放出光子エネルギーです。調製されたままの400および600°CのZnOサンプルの計算されたバンドギャップは、それぞれ3.24、3.28、および3.27 eVであり、ポリオール合成によるZnOナノ粒子の3.2eVと一致しています[28]。バンドギャップが最初に増加し、その後アニーリング温度とともにわずかに減少するのはなぜですか?これにはいくつかの要因があると思います。一方では、ナノ材料のバンドギャップは、ナノ結晶のサイズが大きくなるにつれて減少します。一方、結晶性粉末は非晶性粉末よりもバンドギャップが大きくなります。一方、金属酸化物中の炭素不純物の減少は、バンドギャップを高める可能性があります。 XRDおよびFTIRの結果に基づくと、400°CのZnOサンプルは、より優れた結晶化度とより低い炭素含有量を示しています。 400°CのZnOナノクリップのナノ結晶サイズは大きくなりますが、明らかに改善された結晶化度と炭素不純物の減少が優勢であり、バンドギャップの増加につながります。 600°Cでさらにアニーリングすると、バンドギャップがわずかに減少するのは、主に粒子サイズの影響によるものです。
調製したままのZnOナノクリップの比表面積は約88m 2 です。 / g。 400°Cのアニーリング後、約59 m 2 に減少します。 / gは、結晶子サイズの増加、粒子密度の増加、および熱処理後の細孔と欠陥の減少に関連しています[26]。
ZnO形態に対する溶液濃度の影響
ポリオールプロセスによるZnOサンプルの形成と形態に対する反応物濃度の影響を調査するために、Zn(OAc) 2 ・nH 2 O溶液濃度は、他の反応パラメーターを固定することにより、0.005から0.01、0.0125、0.015、0.05、および0.2Mまで変化しました。 Zn(OAc) 2 ・nH 2 O溶液濃度は0.005、0.01、および0.0125 Mであり、図1bに示すように、ZnOナノクリップはわずかなナノ粒子で作成できます。溶液濃度を0.015Mに上げると、ZnOナノクリップが消え、楕円形(〜435×200 nm)のZnOナノ粒子のみが図3aに形成されます。これは、以前の文献の結果と同様です[25、28、30]。溶液濃度をさらに0.05Mに上げると、SEM画像は、図3bに、楕円形(〜220–260×100–140 nm)または球状(100–260 nm)の粒子と数マイクロメートルの不規則な凝集体の混合物を示します。また、溶液濃度が高くなると反応が速くなります。溶液の濁り時間は、0.01Mの7分から0.2Mの4.5分に短縮されます。0.2MのZnO生成物は、約30nmの小さな球体でより乱雑な凝集形態を示します。

( a のさまざまな条件下でのZnOサンプルのSEM画像 )0.015 M、5 mL、170°Cおよび( b )0.05 M、5 mL、および170°C
ZnOナノクリップの可能な成長メカニズム
ZnOナノクリップ形成の可能な成長メカニズムを解明するために、170°Cの0.01M溶液から12分の反応時間で得られた初期のZnO沈殿についてもSEM観察を行いました。図4は、12分と2.5時間のさまざまな反応時間でのZnOサンプルのSEM画像を示しています。

0.01 M Zn(OAc)2・nH 2 からのZnOサンプルのSEM画像 ( a の反応時間で170°CのO溶液 – c )12分および( d – f )2.5時間。 ( c の挿入図 )は、ナノリング形態の局所倍率です
低倍率ビュー(×5000)では、12分と2.5時間で得られたZnOサンプルは、図4a、dの羽のような凝集体と同様の形態を示します。倍率をさらに上げると(×50,000)、12分のサンプルの場合、図4bの明確な特徴と詳細を観察することはできません。ただし、2.5時間のサンプルの場合、蓄積されたナノクリップは図4eではっきりと見ることができます。ナノリングやハーフリングなどのナノクリップの初期の形態が、図4cの12分のサンプルで見つかったことは注目に値します。これは、ZnOナノクリップの形成メカニズムを説明するための重要なヒントです。さらに、2.5時間のサンプルでは、図4fのナノワイヤー、ナノスティック、閉じていないクリップなど、ナノクリップの一部も認識されます。
当社のZnOナノクリップ調製プロセスでは、Zn(OAc) 2 ・nH 2 O溶液濃度は0.01Mであり、ほとんどの参考文献[23、24、28、29、30]よりも明らかに低くなっています。一方、NaOHやポリビニルピロリドン(PVP)のキャッピング剤などの余分な水やアルカリは、5 mLEG溶媒に添加されません。さらに、使用したZn源には、比較的少ない水和水が含まれています( n <2)長期保管による水分損失による。 ZnOナノクリップの形成の可能性は次のように説明できます:
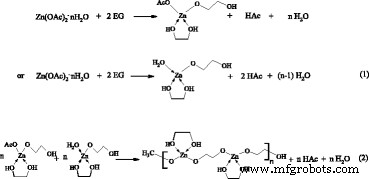
まず、Zn(OAc) 2 ・nH 2 Oは170°Cで約1分でEG溶媒に溶解します。酢酸亜鉛水和物はEGと反応し、Zn(OAc)(OCH 2 などの酢酸アルコキシ複合体の中間前駆体を形成します。 CH 2 OH) x 図2cのFTIRスペクトルで確認されたように、酢酸アニオンと水分子を部分的に置き換えることによって(式1)。 Zn 2+ 間の配位結合の形成 また、ジエチレングリコール(DEG)とEGの溶媒は、以前のいくつかの研究でも観察されています[24、28、29]。ポール等。 Zn(OAc) 3 のアルコキシアセテート複合体の存在を検出しました (OCH 2 CH 2 OH)およびZn 3 (OAc) 4 (O(CH 2 ) 2 O(CH 2 ) 2 O)[34、35]。その後、アルコキシアセテート錯体は重合を続け、線状ポリマーを形成します(式2)。アセテートとEGは、重合を可能にする架橋配位子として機能します。調製されたままのZnOナノクリップのFTIRスペクトルも、図2cの架橋結合モードを示しています。ここでは、テンプレートのような線状ポリマーが、熱分解またはゆっくりとした加水分解によって長鎖に沿ってZnOナノ結晶の成長を誘発し、ZnOナノワイヤーとナノリングを取得します。十分な反応時間(≥1時間)の後、図5aに示すように、ZnOナノワイヤーとナノリングからのZnOナノクリップが最終的に形成されます。
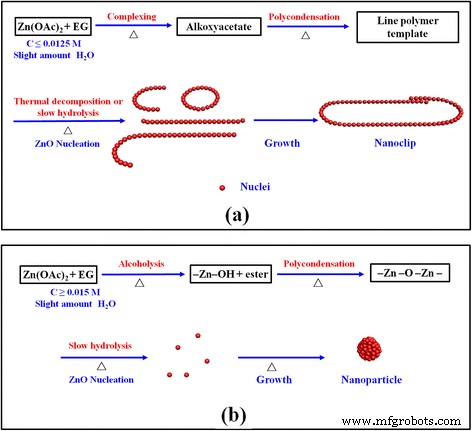
( a)の進化の概略図 ZnOナノクリップおよび( b )2つの可能なポリオール媒介経路によるZnO粒子形成
ZnOナノクリップの形成に対する反応温度、添加剤、PVPなどの溶媒、およびZn源などの他の処理パラメーターの影響は、追加ファイル1に示されています。Zn(OAc) 2間の非加水分解アルコール分解反応 ・nH 2 OとEGは、ZnOナノ結晶の製造において優勢になり始めます[36、37]。 H 2 O量とOH − 濃度は、ポリオールを介したZnO生成物の形態と粒子サイズに重要な影響を及ぼします[23、24、27、28、29、30]。 EGの高い加水分解比(> 50)はヒドロキシアセテートの形成につながります[23]。文献報告[23、24、26]に基づくと、ヒドロキシアセテートはこれらの条件下でのZnOナノ粒子の形成に有利に働きます。 –Zn–OHは、エステル脱離反応に基づくアルコール分解経路によって形成され(式3)、その後、–Zn–OHと–Zn–O–Acまたは–Zn–OHの重縮合により、酢酸またはH 2 を分離することによるZnO核 O(式4および5)、これは遅い加水分解反応を伴う可能性があります[28]。式5は、Gaudon etalによって提案された強制水素化凝縮に等しい。 [27]。最後に、ZnO核は大きくなり、ZnOナノ結晶を形成します。これらのナノ結晶は、図5bに示すように、球状または楕円形のナノ粒子に凝集します。処理パラメータの変更に伴い、2種類のポリオール反応経路間で競合します。
結論
より良い単分散性を備えた興味深いZnOナノクリップは、初めて単純なポリオール媒介経路によって調製されました。溶液濃度がZnOナノクリップの形成に及ぼす影響が深く研究されています。 Zn(OAc) 2 ・nH 2 Oは、水やアルカリを添加しなくてもEGと反応し、170°Cで多結晶ウルツ鉱構造の純粋なZnO相を生成します。 ZnOナノクリップの形状は一定に保たれ、400〜600°Cでのアニーリング後の結晶品質が向上します。 Zn(OAc) 2 間の錯化とアルコール分解の競合に基づく可能な成長メカニズム ・nH 2 OとEGが提案されています。 170°Cの5mL溶液で溶液濃度が≤0.0125Mの場合、錯化反応と重合反応が優勢になり、主にZnOナノクリップが生成されます。溶液濃度が≥0.015Mの場合、アルコール分解および重縮合反応が支配的になり、球形または楕円形のZnO粒子が形成されます。特殊なナノ構造と比表面積が大きいため、ZnOナノクリップは、廃水やガス中の有害な汚染物質を分解するための光触媒、電気化学エネルギー貯蔵用のリチウム電池またはスーパーキャパシタのアノード材料、および危険なガスを検出するためのセンサーとして有望な材料です。
略語
- ベット:
-
ブルナウアー-エメット-テラー
- DEG:
-
ジエチレングリコール
- EG:
-
エチレングリコール
- FTIR:
-
フーリエ変換赤外スペクトル
- FWHM:
-
半値全幅
- HRTEM:
-
高分解能透過型電子顕微鏡
- NIR:
-
近赤外線
- PVP:
-
ポリビニルピロリドン
- SEM:
-
走査型電子顕微鏡
- TEM:
-
透過型電子顕微鏡
- TG-DTG:
-
熱重量分析-微分熱重力
- UV:
-
紫外線
- XRD:
-
X線回折
ナノマテリアル



