可視光下での304ステンレス鋼の光生成陰極保護用のBi2Se3増感TiO2ナノチューブフィルム
要約
二酸化チタン(TiO 2 )ナローギャップ半導体と結合したナノチューブアレイ—セレン化ビスマス(Bi 2 Se 3 )—可視光下での304ステンレス鋼の光陰極保護特性の顕著な向上を示しました。 Bi 2 Se 3 / TiO 2 ナノコンポジットは、純粋なTiO 2 を調製するための電気化学的陽極酸化法を含む、単純な2段階の方法を使用して正常に合成されました。 およびBi 2 を合成するための化学浴堆積法 Se 3 ナノフラワー。複合フィルムの形態および構造は、走査型電子顕微鏡法、エネルギー分散型分光法、X線光電子分光法およびX線回折によって研究された。さらに、Bi 2 の影響 Se 3 複合フィルムの光電気化学的および光陰極保護特性に関する含有量も研究された。 Bi 2 の光電流密度 Se 3 / TiO 2 ナノコンポジットは、純粋なTiO 2 よりも大幅に高かった 可視光の下で。増感剤Bi 2 Se 3 光生成された電子正孔対の効率的な分離とTiO 2 の光陰極保護特性を強化しました 。可視光照明下で、Bi 2 Se 3 / TiO 2 Bi 3+ を使用した化学浴堆積法によって合成されたナノコンポジット (0.5 mmol / L)は、304ステンレス鋼に対して最適な光生成陰極防食性能を示しました。
背景
重要なエンジニアリング材料として、ステンレス鋼はその優れた耐食性により、多くの分野で重要なプロジェクトに広く適用されてきました。ただし、ステンレス鋼は、酸性環境などの特定の攻撃的な環境や、塩化物を含むまたは高温の条件下で使用すると、深刻な腐食を引き起こす可能性があります[1,2,3,4]。コーティング[5、6]、犠牲陽極の使用[7]、印象的な電流陰極防食法[8、9]など、従来の防食方法の広範な研究と応用が過去数十年の間に開発されてきました。しかし、環境に優しく長持ちする防食技術は依然として主要な目標です。新しい防食技術として、光陰極保護は、腐食研究者から注目される前に、1995年に元と辻川によって最初に提案されました[10]。
二酸化チタン(TiO 2 )は、優れた光電変換と光触媒特性を備えた重要な光電材料であり、低コスト、非毒性、安定した化学的特性により、触媒[15]、太陽電池[16]、ガスセンサー[17]で広く使用されています。 TiO 2 およびTiO 2 ベースの複合材料は、光生成陰極防食法に使用されます。これは、近年急速に発展している腐食防止の有望な技術です[18、19、20、21、22、23]。ただし、TiO 2 のバンドギャップ(3.2 eV) 光応答を紫外線領域のみに制限し、太陽光発電の利用率を大幅に低下させます。さらに、裸のTiO 2 の光誘起電荷キャリア ナノ粒子は、光励起された電子正孔対の急速な再結合により非常に短い寿命を示し、純粋なTiO 2 の光陰極保護効果を低下させます。 映画。したがって、TiO 2 の上記の欠陥を克服する方法 広く研究されているトピックになっています。 TiO 2 の配合について多くの研究が行われています。 非金属元素(F、N、S)[12、24、25]、金属原子(Fe、Co、Cu、Ce)[26、27、28、29]、およびいくつかの狭いバンドギャップナノ半導体(Ag 2 O、ZnSe、WO 3 、CdS、Ag 2 S、CdSe、Bi 2 S 3 )[30,31,32,33,34,35,36] TiO 2 のキャリア分離と光利用を改善する 。
セレン化ビスマス(Bi 2 Se 3 )は直接バンドギャップ層状半導体であり、V 2 の重要なメンバーです。 VI 3 複合ファミリー。可視および近赤外光領域で高い吸収係数を持ち、バンドギャップが狭い(0.35 eV)[37]。重要なn型カルコゲニドとして、Bi 2 Se 3 高い電気伝導率[38]、かなりの熱電特性[39]、感光性[40]、電気化学的特性[41]、光伝導性[42]など、多くの重要な特性を備えています。さらに、Bi 2 Se 3 は人気のあるトポロジカル絶縁体[43,44,45]であり、導電性の表面状態と絶縁されたバルク状態という独自の特性を備えています。高品質のBi 2 Se 3 ナノ構造は、高真空物理蒸着法、化学蒸着、原子層堆積、パルスレーザー堆積、および高温での気液固技術を使用して調製されています[44、45、46、47、48、49]。 Bi 2 のこれらの合成方法 Se 3 難しい製造が必要であり、高い製造コストにつながります。この論文では、上記の問題は、Bi 2 に低コストで簡単な化学浴堆積法を採用することによって克服されます。 Se 3 TiO 2 へのナノフラワーの堆積 。 n-Bi 2 の組み合わせ Se 3 / n-TiO 2 効率的な光アノードとしてのヘテロ接合は、304ssの光生成陰極防食法に初めて適用されました。 Bi 2 の形態、構造、および吸光度 Se 3 / TiO 2 ナノコンポジットは、走査型電子顕微鏡(SEM)、X線回折(XRD)、エネルギー分散型X線分光法(EDS)、X線光電子分光法(XPS)、およびUV-可視(UV-Vis)拡散反射スペクトルによって研究されました。 、それぞれ。
メソッド
この研究で使用されたすべての化学物質は分析グレードであり、さらに精製することなく受け取ったままの状態で使用されました。すべての水溶液は脱イオン水を使用して調製しました。
TiO 2 の準備 映画
NH 4 を含む混合物を使用して、Ti箔(20mm×10mm×0.3mm、純度> 99.9%)を研磨しました。 F(2.25 g)、H 2 O(12.5 mL)、H 2 O 2 (30 wt%、30 mL)およびHNO 3 (68 wt%、30 mL)次に、Ti片を脱イオン水とエタノールで洗浄しました。 TiO 2 フィルムは、文献[50]で報告されている陽極酸化法によってTi箔上に作成されました。カソードとしてPtプレートを選択し、NH 4 を含むエチレングリコール溶液中でTiフォイルを20Vで1時間アノードにしました。 F(0.22 g)、H 2 周囲温度でのO(4 mL)およびエチレングリコール(40 mL)。その後、サンプルを脱イオン水とエタノールですすいだ。最後に、試験片を450°Cで2時間アニールし、周囲空気中で冷却してTiO 2 を得ました。 映画。
Bi 2 の合成 Se 3 TiO 2 映画
Bi 2 Se 3 化学浴堆積法により調製した。実験手順では、8ミリモルのニトリロ三酢酸(H 3 NTA)および0.4ミリモルのBi(NO 3 ) 3 ・5H 2 Oを脱イオン水(400 mL)に加えて、Bi 3+ のビスマスキレートを形成しました。 混合溶液中の濃度は1.0mmol / Lです。上記の溶液に還元剤としてアスコルビン酸2ミリモルを加えた後、水酸化アンモニウムを注意深く滴下し、混合物のpHが約8.6〜8.9に調整され、混合溶液が無色透明に見えるようにした。最後に、Na 2 SeSO 3 (20 mL、30 mmol / L)を上記の溶液に注入しました。上記のすべての実験において、水溶液をマグネチックスターラーで完全に攪拌して、均質な溶液を得た。次に、TiO 2 基板をビーカー(100 mL)の最終溶液(40 mL)に浸しました。次に、ラップフィルムで覆われたビーカーを80°Cの温度に200分間加熱したオーブンに移し、Bi 2 を得ました。 Se 3 TiO 2 上のナノフラワー 基板。最後に、サンプルをビーカーから取り出し、脱イオン水とエタノールで数回洗浄した後、周囲空気中で乾燥させました。このように、Bi 2 Se 3 増感されたTiO 2 フィルムを入手し、Bi 2 でラベル付けしました Se 3 / TiO 2 -1.0。簡単にするために、さまざまな量のBi 2 Se 3 TiO 2 基板はBi 2 として指定されます Se 3 / TiO 2 -この論文のγ。ここで、γはBi 3+ の濃度を示します。 H 3 で NTAおよびBi(NO 3 ) 3 ・5H 2 Oソリューション。他の試薬の量を一定に保った状態で、Bi 2 Se 3 / TiO 2 -0.5およびBi 2 Se 3 / TiO 2 Bi 3+ では-0.25が得られました それぞれ0.5ミリモル/ Lと0.25ミリモル/ Lの濃度。さまざまな量のBi 2 の影響 Se 3 この論文では、複合フィルムの光電気化学的および光陰極保護特性について調査しました。
形態と組成の分析
走査型電子顕微鏡(SEM、日立S-4800、日本)を使用して、調製されたフィルムの形態を調査した。エネルギー分散型X線分光法(EDS、Oxford Energy 350 X線エネルギースペクトル分析装置)およびX線光電子分光法(XPS、Thermo Scientific ESCALAB 250Xi)を使用して、Bi 2 Se 3 / TiO 2 ナノコンポジット。サンプルの吸光度を測定するために、UV-Vis DRS(Japan Hitachi UH4150)を使用しました。サンプルの結晶相組成は、CuK αを使用したX線回折計(XRD、ドイツBruker AXSD8)によって特徴づけられました。 10°から80°までの放射(γ=1.54056Å)。
光電気化学測定
図1に示すように、光分解セルと電解セルで構成されるカップリングシステムを光電気化学測定に使用し、プロトン交換膜を使用して2つのセルを結合しました。光分解セルには0.1mol / L Na 2 が含まれていました Sと0.2mol / LのNaCl混合溶液は、電子と正孔の分離を促進するための犠牲剤の役割を果たしましたが[33、51]、電解セルの電解質として0.5 mol / LのNaCl溶液を使用しました。電解槽では、対極(CE)にPt箔、参照電極(RE)に飽和カロメル電極、作用電極(WE)に304ssの3電極方式を採用しました。 Bi 2 Se 3 / TiO 2 光分解セルに配置されたナノコンポジットサンプルは、銅線によって電解セルに浸された304ss電極に接続されました。可視光範囲の光源は、高圧キセノンランプ(PLS-SXE 300 C、北京パーフェクトライト社、中国)によって照射されました。開回路電位(OCP)と光電流曲線の変化は、光照射前と照射中にGamryポテンシオスタット/ガルバノスタット/ ZRAシステム(GAMRY 3000、Gamry Instruments、米国)を使用して測定されました。
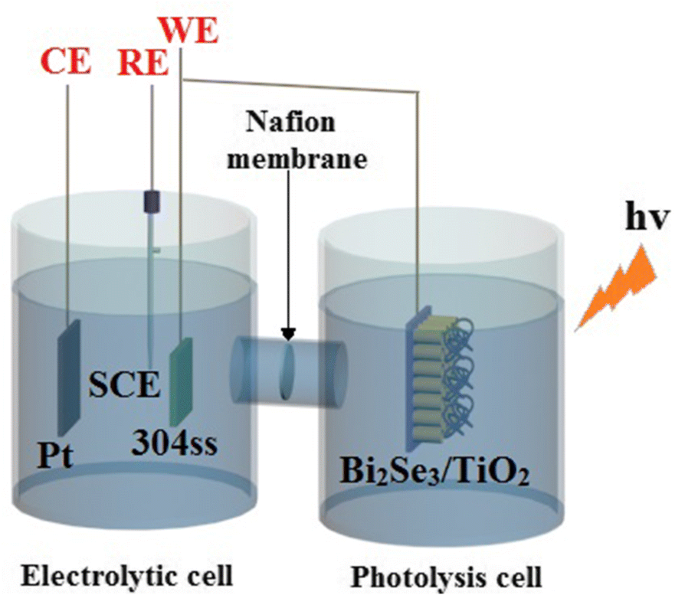
光電気化学分析に使用される実験装置の概略スケッチ
結果と考察
純粋なTiO2とBi2Se3 / TiO2の特性評価
図2aは、TiO 2 の典型的な上面図と断面図を示しています。 陽極酸化法で作製したフィルム。 TiO 2 ナノチューブアレイは、平均内径と長さがそれぞれ約55nmと680nmの、秩序だった高密度のナノチューブで構成されるナノポーラス構造を示しています。図2b–dに示すように、TiO 2 ナノチューブ表面はBi 2 によって正常に修飾されました Se 3 さまざまな濃度のBi 3+ の化学浴堆積法による 。 Bi 2 の場合 Se 3 / TiO 2 -0.25、Bi 2 Se 3 ナノフレークは散発的に分布し、TiO 2 全体に不均一に凝集しました。 ナノチューブ(図2b)。 Bi 3+ の濃度が 0.5ミリモル/ L、Bi 2 Se 3 TiO 2 のノズルを塞ぐことなく、直径約800nmの柔軟な極薄ナノフレークの花のようなパターンでほぼ完全に構成されていました。 ナノチューブまたはそれらに損傷を与える(図2c)。 Bi 2 Se 3 TiO 2 の表面に均一に分布していることが観察されたナノフラワー 図2cに示すように、は極薄ナノフレークの内部架橋構造を示しました。これにより、ラメラの凝集が効果的に防止され、アーキテクチャの寿命が長く維持されました。 Bi 3+ の濃縮後 Bi 2 の量と直径である1.0mmol / Lに増加しました Se 3 図2dに示すように、ナノフラワーは大幅に増加し、ナノフラワーの凝集によりナノチューブがブロックされました。 Bi 2 の対応するEDSスペクトル Se 3 / TiO 2 -図2eに示す0.5フィルムは、Ti、O、Bi、およびSeの特徴的なピークが、それぞれ0.9%および1.3%のBiおよびSeの原子百分率でマークされていることを示しています。試験元素の含有量が少なくなると、EDS試験の測定誤差が大きくなることはよく知られています。したがって、BiとSeの原子比が2:3に近いことは許容されます。

a のSEM画像 純粋なTiO 2 、 b Bi 2 Se 3 / TiO 2 -0.25、 c Bi 2 Se 3 / TiO 2 -0.5および d Bi 2 Se 3 / TiO 2 -1.0; e Bi 2 のEDSスペクトル Se 3 / TiO 2 -0.5フィルム
図3aは、純粋なTiO 2 のXRDスペクトルを示しています。 (曲線a)およびBi 2 Se 3 / TiO 2 -1.0ナノコンポジット(曲線b)。 Ti基板のピークを除いて、25.38°、38.03°、48.01°、54.05°、55.17°、62.71°および70.44°の回折ピークは、格子面(101)、(004)、(200)、アナターゼ型TiO 2 の(105)、(211)、(204)および(220) 、それぞれ(JCPDS 21-1272)。 TiO 2 を除く ピーク、29.35°および74.90°の特徴的な回折ピークは、菱面体晶Bi 2 の格子面(015)および(0216)にインデックス付けされました。 Se 3 (JCPDS 33-0214)。ただし、Bi 2 の明らかなピークはありません。 Se 3 / TiO 2 -コンテンツが少ないため1.0Bi 2 Se 3 TiO 2 に堆積 XRDスペクトルはSEMおよびEDSの結果に適合しました。 X線光電子分光法(XPS)を使用して、Bi 2 の化学組成と状態をさらに決定しました。 Se 3 / TiO 2 ナノコンポジット。図3bに示すように、XPSは、偶発的な炭化水素汚染によるC汚染物質に加えて、Bi、Se、Ti、およびO成分の存在を明らかにしました。図3cは、458.7および464.5eVでのTi2pのピーク位置を示しています。これは、酸化チタンが主にTiO 2 で構成されていることを示しています。 [52]。図3dに示すように、O 1sセマフォは2つのガウスピークと一致しました。低い結合エネルギー(530.0 eV)での最大値は、格子酸素(O L )に起因していました。 )Bi 2 で Se 3 / TiO 2 ナノコンポジットと、より高い結合エネルギー(531.5 eV)の2つ目は、吸着された酸素(O A )、弱い結合の酸素またはヒドロキシル基を含む。 O A の存在 これは、ナノコンポジットの表面に酸素空孔が生成されたためであり、Bi 2 の光電変換特性が向上する可能性があります。 Se 3 / TiO 2 光陰極保護におけるナノコンポジット[53]。図3eは、4f 7/2 Biの非対称ピークは2つのピーク(157.5と159.4 eV)に分解され、Bi 4f 5/2 同様に、スペクトルはそれぞれ162.8eVと164.7eVの2つのバンドに分割されます。低い方のピーク(157.5eVと162.8eV)の位置は、Bi 2 の位置とよく一致していました。 Se 3 、159.4eVおよび164.7eVの酸化ビスマスに対応する高いピークがあります[54、55]。 Bi 2 を使用した合成プロセス中に、一握りのビスマス金属が酸化されたと結論付けることができます。 Se 3 純粋なTiO 2 の変更 。図3fに示すように、2つのピークは3d 3/2 に割り当てられました。 および3d 5/2 Seのコアレベルはそれぞれ55.1および54.2eVであり、SeがSe 2- の形で存在したことを示しています。 [56]。
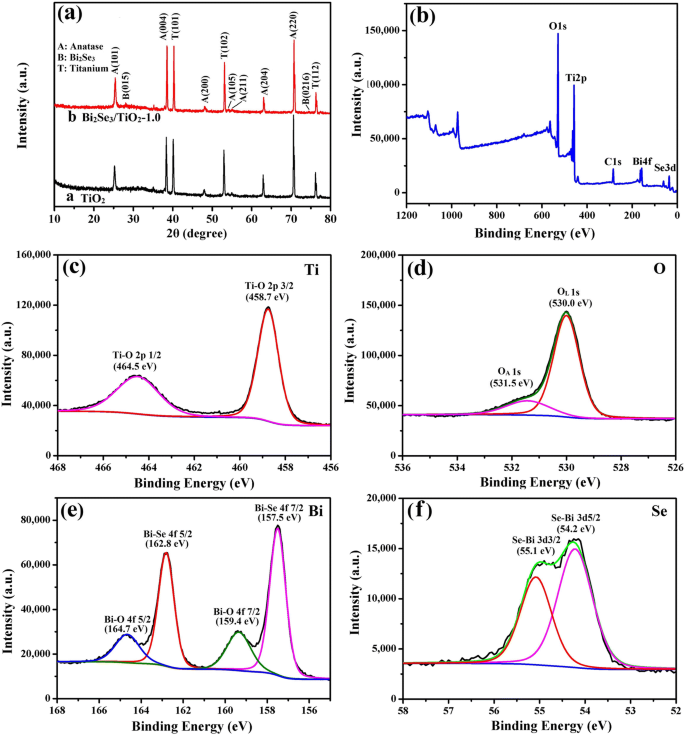
a 純粋なTiO 2 のXRDパターン およびBi 2 Se 3 / TiO 2 -1.0ナノコンポジット; b 総調査スペクトル、 c Ti 2p、 d O 1s、 e Bi4fおよび f Bi 2 のSe3dXPSスペクトル Se 3 / TiO 2 -1.0ナノコンポジット
図4は、純粋なTiO 2 の光吸収能力を示しています。 およびBi 2 Se 3 / TiO 2 -1.0ナノコンポジット。純粋なTiO 2 の特徴的な吸収端 アナターゼ型TiO 2 のバンドギャップエネルギーにより、UV領域内で約380nmでした (3.2 eV)(曲線a)。 Bi 2 では顕著な吸着が観察されました Se 3 / TiO 2 可視光領域(350〜800 nm)のナノコンポジット(曲線b)、純粋なTiO 2 よりも高い可視光吸収能力 Bi 2 が組み込まれているため Se 3 ナノフラワー。この現象は、Bi 2 Se 3 バンドギャップが狭い(0.35 eV)ため、可視光下で励起され、伝導帯(CB)と価電子帯(VB)で電子と正孔が生成されます。したがって、Bi 2 の追加 Se 3 Bi 2 の可視光吸収能力を効果的に高めます Se 3 / TiO 2 ナノコンポジット。
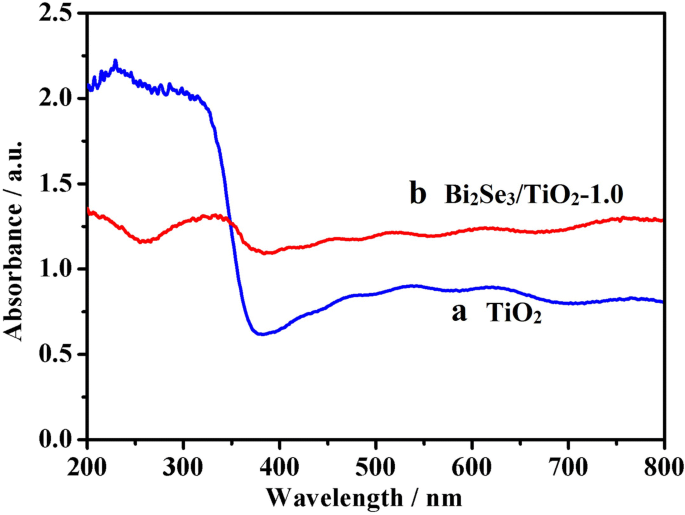
TiO 2 のUV-可視吸収スペクトル (a)およびBi 2 Se 3 / TiO 2 -1.0(b)
純粋なTiO2およびBi2Se3 / TiO2の光陰極保護性能
図5に示すように、純粋なTiO 2 と結合した304ssのOCP曲線 およびBi 2 Se 3 / TiO 2 ナノコンポジットフォトアノードは、断続的な可視光の下で測定され、照明に対するOCP応答が促され、結合されたすべての電極の負の電位にシフトしました。点灯の初期段階で、結合されたすべての電極のOCPは、短時間で負のシフトを示しました。これは、純粋なTiO 2 からの励起された光電子の移動によるものです。 およびBi 2 Se 3 / TiO 2 304ss電極へのナノコンポジット[1,57]。その後、比較的安定したOCP値は、光生成された電子の生成と再結合の間の平衡速度に起因する可能性があります[32]。照射をオフにした後、Bi 2 のOCP値 Se 3 / TiO 2 ナノコンポジットは、純粋なTiO 2 と比較して遅い速度で元の値に戻りました 。この現象は、Bi 2 の電子プール効果に起因する可能性があります。 Se 3 / TiO 2 光照射下で光誘起電子を蓄積し、光照射なしでこれらの電子をゆっくりと放出することができるナノコンポジット。可視光照射下で、304ssのOCP値は、TiO 2 と組み合わせた場合に約-450mVでした。 (曲線a)、およびBi 2 と結合した304ssのOCP値 Se 3 / TiO 2 -0.25(曲線b)、Bi 2 Se 3 / TiO 2 -0.5(曲線d)およびBi 2 Se 3 / TiO 2 -1.0(曲線c)は、それぞれ-905 mV、-996 mV、-958mVに達しました。これらの結果は、Bi 2 と結合すると、304ssが陰極分極したことを示しています。 Se 3 / TiO 2 ナノコンポジットと、304ssの優れた陰極防食がBi 2 によって提供される可能性があること Se 3 / TiO 2 フォトアノード。図5dに示すように、Bi 2 に結合された304ss Se 3 / TiO 2 -0.5が最も負の電位を持っていたということは、304ssで最高の光陰極保護性能を示しています。この結果は、Bi 2 の増加に伴って活性部位と光収穫が増加したためである可能性があります。 Se 3 コンテンツ。ただし、過剰な量のBi 2 Se 3 粒子は電子と正孔の再結合サイトとして機能し、Bi 2 からの電荷移動を妨げました。 Se 3 / TiO 2 304ssへのナノコンポジット。
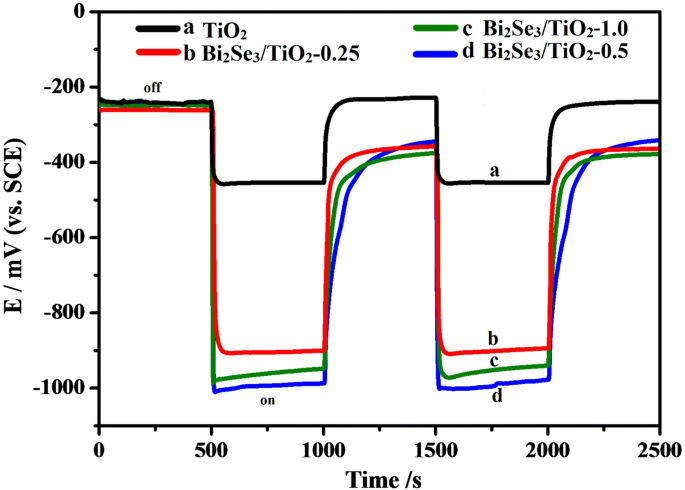
純粋なTiO 2 と組み合わせた304ss用OCP およびBi 2 Se 3 / TiO 2 0.5molのNaCl溶液中のナノコンポジット
図6に示すように、TiO 2 の光電流密度と時間の曲線 およびBi 2 Se 3 / TiO 2 ナノコンポジットは、断続的な可視光照明下で迅速かつ再現性のある光応答を示しました。これは、材料の光電変換性能を反映しています。光生成電流は、可視光の吸収が弱いため、可視光下では比較的小さかった(曲線a)。しかし、光生成電流は、TiO 2 の増感に続いて、可視光照明下で著しく増加しました。 Bi 2 による Se 3 ナノフラワー(曲線bからd)。データは、Bi 2 Se 3 / TiO 2 ナノコンポジットは可視光を利用することができ、TiO 2 間のヘテロ接合 およびBi 2 Se 3 光生成された電子と正孔の分離を促進しました[58]。さらに、Bi 2 の伝導帯で生成された光電子 Se 3 ナノフラワーは、TiO 2 のより正の伝導帯に簡単に移動できます。 可視光照射下のナノチューブ。 3回の照射間隔の後、光電流は比較的安定した値を維持し、光電流の劣化は検出されませんでした。これは、Bi 2 の良好な光化学的安定性を示しています。 Se 3 / TiO 2 ナノコンポジットフィルム。さまざまな濃度のBi 3+ 、Bi 2 Se 3 / TiO 2 ナノコンポジットは、光電流応答に対して異なる強度を示しました。特に、Bi 2 の過渡光電流密度 Se 3 / TiO 2 -0.5(415μA/ cm 2 )はBi 2 よりも高かった Se 3 / TiO 2 -0.25(85μA/ cm 2 )およびBi 2 Se 3 / TiO 2 -1.0(160μA/ cm 2 )、Bi 2 であることを示します Se 3 / TiO 2 -0.5は、光生成された電子正孔対の理想的な分離効率を備えていました。 Bi 2 の不足により、活性部位と光収穫が減少しました Se 3 Bi 2 のナノフラワー Se 3 / TiO 2 ナノコンポジットフィルム、電子と正孔の再結合サイトは、過剰な量のBi 2 の存在下で増加しました Se 3 ナノフラワー。可視光照明下で、Bi 2 の最大の光誘起電流密度 Se 3 / TiO 2 -0.5光アノードは、図5に示す最大の光誘起電位降下と一致しており、Bi 2 の最適な光陰極保護性能をさらに検証しています。 Se 3 / TiO 2 -304ssの場合は0.5。
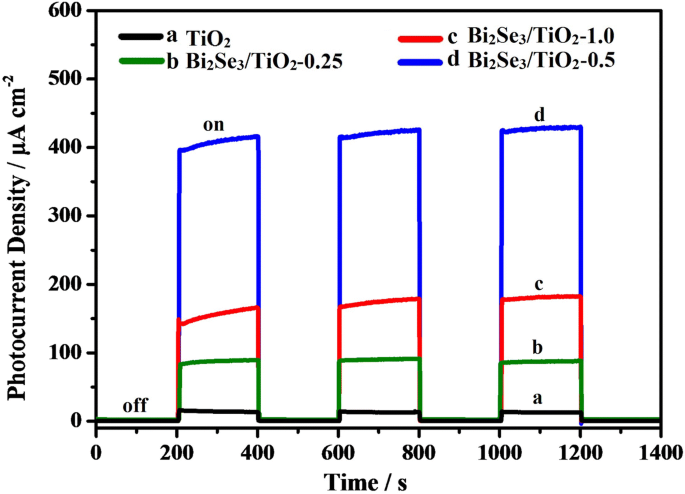
純粋なTiO 2 の光電流密度対時間曲線 およびBi 2 Se 3 / TiO 2 0.1 mol / L Na 2 のナノコンポジット Sと0.2mol / LのNaOH混合溶液
図7は、Bi 2 の光電変換および輸送プロセスを示しています。 Se 3 / TiO 2 ナノコンポジット。可視光の下で、Bi 2 Se 3 ナノフラワーは、吸着した酸素(O A )を含んでいるため、光子を容易に吸収できます。 )、バンドギャップ幅が狭い(0.35 eV)。光子がBi 2 によって吸収されるとき Se 3 ナノフラワー、光励起電子は、Bi 2 の価電子帯(VB)からの励起によって生成されます Se 3 Bi 2 の伝導帯(CB)へ Se 3 。 Bi 2 のCB内の光励起電子 Se 3 TiO 2 のCBにシフトされます 、TiO 2 のVBに光生成された穴 Bi 2 のVBに転送されます Se 3 、その後、S 2- によってキャプチャされます 電解質中で光アノード膜の表面でSに変わります。光励起された電子が光アノードを出て304ssに移動すると、それらは酸素ガスおよび水と反応してOH - に変換されます。 。さらに、Na + は、プロトン交換膜によって電解セルから光分解セルに輸送されるため、カップリングシステムは全体として電気的に中性です。結果として、光生成された電荷は効果的に分離され、光生成された電子正孔対の再結合確率が低下します。 304ssがBi 2 から光励起された電子を受け取ると Se 3 / TiO 2 ワイヤーを介したナノコンポジットでは、304ssの電位が負にシフトします。可視光照明下では、Bi 2 Se 3 / TiO 2 ナノコンポジットは304ssの腐食速度を低下させる可能性があります。したがって、Bi 2 の光励起された電子正孔対の効率的な分離 Se 3 / TiO 2 ナノコンポジットはレドックス反応を加速し、304ssの効果的な光陰極保護を生成します。
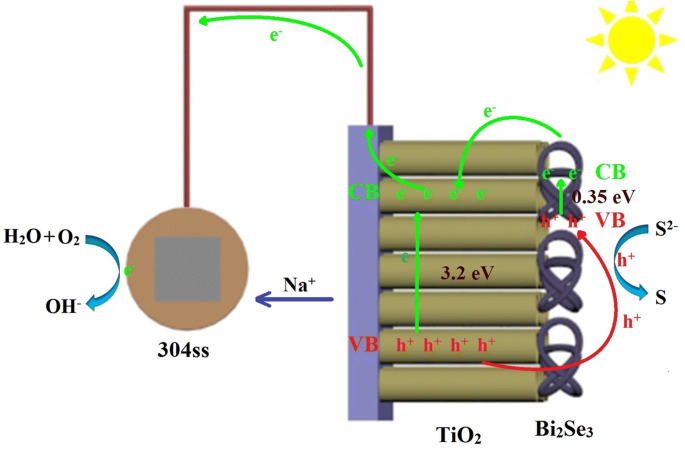
Bi 2 での電子移動プロセスの概略図 Se 3 / TiO 2
結論
この論文では、TiO 2 ナノチューブアレイは、陽極酸化法とBi 2 によって調製されました。 Se 3 ナノフラワーはTiO 2 で育てられました 化学浴堆積によるナノチューブ。 Bi 2 Se 3 / TiO 2 ナノコンポジットは、均一な分布と秩序だった特性を示しました。ナノコンポジットと純粋なTiO 2 の電気化学的試験 304ssと組み合わせると、Bi 2 の光生成陰極防食性能が示されました。 Se 3 / TiO 2 ナノコンポジットは、純粋なTiO 2 の場合と比較して優れていました 。 Bi 2 と組み合わせた304ssのOCP値 Se 3 / TiO 2 -0.5は、活性部位とTiO 2 の光収穫により、可視光照明下で-996mVへの負のシフトを示しました。 Bi 2 によって感作 Se 3 。 3つのBi 2 の電気化学的試験の結果を比較することによって Se 3 / TiO 2 ナノコンポジット、0.5 mmol / L Bi 3+ を使用して調製されたナノコンポジット 電解液中で最適な性能を示しました。
略語
- 304ss:
-
304ステンレス鋼
- CB:
-
伝導帯
- CE:
-
対極
- EDS:
-
エネルギー分散型X線分光法
- H 3 NTA:
-
ニトリロ三酢酸
- OA:
-
吸着酸素
- OCP:
-
開回路電位
- OL:
-
ラティス酸素
- RE:
-
参照電極
- SCE:
-
飽和カロメル電極
- SEM:
-
走査型電子顕微鏡
- UV-Vis:
-
紫外可視拡散反射スペクトル
- VB:
-
価電子帯
- WE:
-
作用電極
- XPS:
-
X線光電子分光法
- XRD:
-
X線回折
ナノマテリアル
- 高温用途向けのステンレス鋼の選択
- 304&316ステンレス鋼の差別化
- MoO3でコーティングされたTiO2ナノチューブ光電極上のAu-プラズモンナノ粒子によって強化された光触媒活性
- 着色された低温顔料用のCrドープTiO2の構造的および可視近赤外光学特性
- 陽極酸化チタンナノチューブアレイにCeO2ナノ粒子をロードするための簡単な方法
- Fe3 +イオンの高効率検出のためのAgナノ粒子を備えた十分に整列したTiO2ナノチューブアレイ
- 可視光下での光触媒活性を高めるための単斜晶BiVO4へのCu2-xSe修飾
- 静電容量が強化されたスーパーキャパシタ電極用の原子層堆積によって製造されたTiO2ナノメンブレン
- ステンレス鋼部品およびエンクロージャーの不動態化
- ステンレス鋼の最も一般的な用途
- メーカー向け精密金属



