蛍光半導体ナノ粒子でコード化された高分子電解質マイクロカプセルに基づくバイオイメージングツール:蛍光特性の設計と特性評価
要約
蛍光イメージングは、現代の診断およびその他の生物医学アプリケーションにおいて、分子、細胞、および組織レベルでの分布、相互作用、および変換プロセスを検出および監視するために広く使用されている手法です。蛍光半導体ナノ結晶のユニークな光物理的特性「量子ドット」(QD)は、生体分子の蛍光標識または微粒子の光学的符号化のための高度なフルオロフォアであり、標的送達、可視化、診断、およびイメージングでバイオイメージングおよびセラノスティック剤として使用されます。この論文は、多機能ポリエチレングリコール誘導体水溶性量子ドットで覆われた、安定した高分子電解質マイクロカプセルの光学的符号化への改善されたアプローチの開発の結果、ならびに符号化されたマイクロカプセルの光学的特性、形態学的および構造的特性の特性評価について報告する。 。事前に形成された高分子高分子電解質シェルへの層ごとの堆積によるポリマーマイクロカプセル膜へのQDの埋め込みにより、フローサイトメトリーによって個々の均質な集団として明確に識別できる、適応した電荷とサイズ分布を持つ明るい蛍光粒子を得ることができます。開発された蛍光マイクロカプセルは、光励起とともにさまざまな外部刺激に敏感なバイオイメージングおよびセラノスティック剤をさらに設計する際に使用できます。
はじめに
薬物、タンパク質、および核酸分子の標的化送達のための担体として使用される蛍光ポリマーのマイクロおよびナノ粒子の開発は、バイオイメージングおよびセラノスティック剤の設計の分野で特に興味深い[1,2,3]。量子ドット(QD)は、物理的なサイズに応じて蛍光ピーク波長を持つ2〜10nmの半導体コロイド結晶です。広い吸収スペクトルと、ナノ粒子のサイズに応じた位置を持つ狭く対称的な蛍光スペクトルにより、単一の放射線源を使用して、多重検出に使用できるさまざまな蛍光バンドを持つ一連のQDで蛍光を励起できます。したがって、QDは非常に魅力的で有望な診断およびイメージング用の高度なフルオロフォアです[4]。
高分子電解質マイクロカプセルをさまざまな機能コンポーネントのキャリアとして使用すると、さまざまな物理的(超音波、磁場、レーザー、または光放射)または化学的(pH、微小環境のイオン強度、および溶媒の極性)に応答するシステムの開発が可能になります。刺激[5、6]。高分子電解質マイクロカプセルは、球形マトリックス上に反対に帯電した高分子高分子電解質を層ごとに堆積させることによって得られます。その後のマトリックスの溶解により、中空構造が生成され、その安定した高分子膜は高分子電解質の高分子複合体で構成されます[7、8、9]。高分子電解質の層ごとの吸着技術により、磁性、金属(金または銀)、または蛍光(QDなど)ナノ粒子を含むさまざまな機能成分を高分子膜に組み込み、膜の厚さを制御することができます形成される[10、11]。
蛍光標識されたマイクロカプセルは、invitroおよびinvivoでの輸送と送達を監視するために使用できる有望なバイオイメージング剤です[12、13]。マイクロカプセルの蛍光標識(光学的符号化)の利用可能な方法では、ポリマーは蛍光標識と結合または物理的に混合されます[14、15]。マイクロカプセルの光学的性質を決定する蛍光成分は、マトリックス微粒子、例えば炭酸カルシウムマイクロスフェロライトの調製中に蛍光色素で標識されたポリマーの共沈を介してそれらの内部に組み込むこともできる[16]。マトリックスが削除された後にカプセル化することもできます。この目的のために、高分子膜を介した低分子量および高分子量の化合物の拡散は、微小環境のイオン強度またはpHを増加させることによって保証されます。ただし、蛍光ナノ結晶を使用した高分子電解質マイクロカプセルの光学的符号化は、その独自の光学特性とバイオイメージングにおける有効性により、より有望です[17]。
高分子電解質マイクロカプセルの高分子膜にQDを組み込むことによってコード化する既知の方法は、低分子量リガンド、例えば、チオグリコール酸またはシステインで水溶化されたQDを使用する[18、19]。この研究の目的は、水溶性CdSe / ZnS(コア/シェル)QDで光学的にコード化された非常に安定した蛍光高分子電解質マイクロカプセルを開発することでした。得られた蛍光マイクロカプセルの蛍光および構造特性を推定します。
メソッド
調査の目的、設計、設定
QDでエンコードされた高分子電解質マイクロカプセルの製造
トリオクチルホスフィンオキシド(TOPO)でコーティングされた590nmで最大蛍光を発するCdSe / ZnS(コア/シェル)QDは、NRNU MEPhI(モスクワ、ロシア)のナノバイオエンジニアリング研究所のP.Samokhvalov博士によって合成されました。 QDの精製と可溶化は、前述のように実行されました[20、21]。 QDをクロロホルムに溶解し、続いてメタノールで沈殿させることにより、TOPOをQD表面から除去しました。手順を3回繰り返した。その後、QDを再びクロロホルムに溶解し、QDとシステインの質量比が1:0.13になるようにメタノール中のシステイン溶液で沈殿させました。 QD沈殿物をメタノールで過剰のシステインを洗浄し、真空濃縮器で乾燥させた。乾燥したQDを、0.1M水酸化ナトリウムを添加して水に再懸濁しました。その後、分散液を超音波浴を使用して超音波処理し、ろ過しました(孔径、0.22μm)。得られた分散液に、末端カルボキシル基を含むPEGのチオール誘導体を1:4.6の質量比で添加した。混合物を4°Cで一晩インキュベートし、PEG化QDをゲルろ過クロマトグラフィーを使用して精製しました。 得られたサンプルのQD含有量は、最初の励起子の波長で分光光度的に決定されました。可溶化された量子ドットは、動的光散乱とZetasizer Nano ZS(Malvern、UK)によるレーザードップラー微小電気泳動を使用した流体力学的直径とζ電位によって特徴づけられました。
QDエンコーディングは、前述のように得られた炭酸カルシウム微粒子の表面に、反対に帯電したポリカチオンおよびポリアニオンポリマー、ならびにPEGのカルボキシル化チオール誘導体で官能化された水溶性QDの層ごとの堆積の修正された技術を使用して実行されました。 [22]。高分子高分子電解質層は、ポリカチオンポリ(アリルアミン塩酸塩)(PAH)とポリアニオンポリ(4-スチレンスルホン酸ナトリウム)(PSS)またはポリアクリル酸(PAA)から形成されました。フルオロフォアは水溶性のPEG化CdSe / ZnS QDであり、波長590 nm、ゼータ電位-26.7±0.8 mV、流体力学的直径18.7〜23.3nmに蛍光ピークがあります。 QDでエンコードされたマイクロカプセルの間に、各層の堆積後の製造プロセスは、レーザードップラー微小電気泳動を使用して微粒子の表面電荷(ζ電位)を制御しました。
炭酸カルシウム微粒子を超純水に再懸濁し、0.5 MNaCl中の2mg / mLPAH溶液0.5mLを添加しました。懸濁液を超音波浴で超音波処理し、室温で攪拌しながら20分間インキュベートしました。その後、遠心分離、続いてMilliQ水に再懸濁することにより、過剰なポリマーを洗い流した。高分子ポリアニオンからなる次の層を適用するために、マイクロビーズを0.5 mLの超純水に再懸濁し、懸濁液を0.5 MNaCl中の2mg / mLPSS溶液0.5mLと混合し、超音波浴で超音波処理しました。 60秒間、室温で攪拌しながら20分間インキュベートし、上記のように過剰なポリマーを洗い流します。高分子電解質塗布の各段階後の微粒子の洗浄を3回繰り返した。符号化の前に、5つの高分子電解質層が炭酸カルシウム微粒子に適用され、5番目の層はポリカチオンで構成されていました。その後、可溶化したQDを添加し、80分間恒久的に攪拌しながら混合物をインキュベートしました。次に、反対に帯電したポリマーの6つの連続した層が適用され、6番目の層はポリアニオンPSSまたはPAAで構成されています。 QDでエンコードされた中空高分子電解質マイクロカプセルは、得られた殻付きマイクロビーズの炭酸カルシウムコアを0.2 Mエチレンジアミン四酢酸二ナトリウム(EDTA)(pH 6.5)で洗浄して溶解することで得られました。その後、マイクロカプセルの表面をウシ血清アルブミン(BSA)(Sigma-Aldrich、USA)でさらに修飾し、微粒子を1%のBSAを含む50 mMリン酸緩衝液(pH 7.4)に分散させ、その後4°Cでインキュベートしました。暗闇の中で12時間。使用直前に、中空マイクロカプセルの懸濁液を50 mMリン酸緩衝液(pH 7.4)で5回過剰なBSAで洗浄しました。得られた高分子電解質マイクロカプセルは、暗所で4℃で保存しました。
QDでエンコードされた高分子電解質マイクロカプセルの光学および蛍光顕微鏡
微粒子の形態およびサイズ分布は、光学および蛍光顕微鏡を使用して分析された。微粒子のサイズ分布を推定するために、5 µLの微粒子懸濁液を10 µLの50%グリセロールでスライドに固定しました。サンプルは、ライトフィールドにLD A-Plan 40x / 0.55M27レンズを備えたAxioObserver 3顕微鏡(Carl Zeiss、ドイツ)を使用して検査しました。蛍光画像は、HBO 100水銀イルミネーター(Burner Mercury)とXF115-2 FITCロングパスフィルターセット(505DRLPダイクロイックフィルター、475AF40励起フィルター、510ALP発光フィルター(Omega Optical、USA)、EC Planを含む)を使用して取得しました。 -Neofluar 100x / 1.30オイルアイリスM27レンズ(WD =0.20 mm)、開口数は0.7から1.3まで調整可能、Immersol 518Fイマージョンオイル(Carl Zeiss、ドイツ)。
得られたマイクロカプセルの形態学的特徴を、エポキシ包埋媒体に固定されたBSAフリー表面を有する光学的にコード化された高分子電解質マイクロカプセルの切片で研究した。この目的のために、マイクロカプセル懸濁液を30、50、70、および95%エタノール水溶液で順次脱水し、次に無水エタノール(Acros Organics、USA)で3回処理して、完全に脱水させました。脱水の各段階は15分間続きました。マイクロカプセルの脱水サンプルを1:1エポキシ-エタノール混合物に12時間移し、次に3:1エポキシ-エタノール混合物に3時間移しました。次に、サンプルをきれいな埋め込みエポキシ媒体に移し、エポキシブロックを45°Cで12時間、60°Cで72時間重合させました。次に、幅2.0mmのUltraAFM35ダイヤモンドナイフ(Diatome、スイス)を備えたLeica EM UC6ウルトラミクロトーム(Leica Microsystems、オーストリア)を使用して、蛍光QDでエンコードされた高分子電解質マイクロカプセルを含むこれらのブロックから150nmの切片を切り出しました。切片をスライドに移し、励起用のHBO 100水銀イルミネーター(Burner Mercury)と45 HQ TexasRed蛍光フィルターセット( d =25シフトフリー(E)、560/40励起BP、FT 585ビームスプリッター、および630/75発光BP)(Carl Zeiss、ドイツ)。蛍光画像は、Carl Zeiss EC Plan-Neofluar100x /1.30オイルPh3レンズとImmersol518F浸漬オイル(Carl Zeiss、ドイツ)を使用して取得しました。画像は、Zen(Carl Zeiss、ドイツ)およびImage J 1.48 v(米国)ソフトウェアを使用して分析および処理されました。
QDでエンコードされたマイクロカプセルの蛍光特性
エンコードに使用された元のQDおよびQDエンコードされたマイクロカプセルの蛍光特性は、Infinite 200 PROマルチモーダルプレートリーダー(TECAN、スイス)を使用して分析されました。測定前に、QDでエンコードされたマイクロカプセルとミクロスフェアの懸濁液を含むウェルのあるプレートを、2630× g のА-2-DWPローターを備えた5810R遠心分離機(Eppendorf、USA)を使用して遠心分離しました。 20分間。高分子電解質マイクロカプセルのポリマーシェルに埋め込まれた遊離QDおよびQDの蛍光最大値は、励起波長480nmで測定されました。サンプルの分析にはボトムスキャンモードを使用しました。
フローサイトメトリー
励起源として青色(488 nm)アルゴンレーザーを備えたFACSCanto IIフローサイトメーター(Becton Dickinson、USA)を使用して、元の炭酸カルシウム微粒子、QDを含む高分子電解質シェルを備えた微粒子、およびQDでエンコードされた中空マイクロカプセル。 10 6 を含む懸濁液の0.5mLアリコートを分析しました マイクロビーズ/マイクロカプセル;収集されたイベントの数は2500でした。蛍光強度は、標準の前方散乱光(FSC)、側方散乱光(SSC)、およびフィコエリトリン(PE、585/42 nm)チャネルで記録されました。データは、FACSDivaソフトウェア(Becton Dickinson、米国)を使用して処理されました。
資料
12モノマーのPEGスペーサー(Thermo Fisher Scientific、米国)、Mw≈15,000Daのポリ(アリルアミン塩酸塩)(PAH)、ポリ(4-スチレンスルホン酸ナトリウム)を含むPEGのカルボキシル化チオール誘導体を使用しました。 (PSS)Mw≈70,000Da(Sigma-Aldrich、米国)、およびポリアクリル酸(PAA)Mw≈15,000Da(Sigma-Aldrich、米国)。炭酸ナトリウム、塩化カルシウム、エチレンジアミン四酢酸二ナトリウム塩二水和物、ウシ血清アルブミン(BSA)、エポキシ包埋剤、およびその他の試薬は、Sigma-Aldrich(USA)から入手しました。すべての作業溶液は、Direct-Q浄水システム(フランス、ミリポア)を使用して得られたMilliQ水(18.2mΩcm)を使用して調製され、孔径0.22μmのフィルターでろ過されました。
統計分析
データの統計分析には、MS Office Excel2007およびOriginPro2015ソフトウェアパッケージを使用しました。結果は、3つの独立した実験の平均と標準偏差として示されています。
結果と考察
QDでエンコードされた高分子電解質マイクロカプセルの開発
提案された方法は有機溶媒を必要とせず、生体適合性ポリマーの使用を可能にし[23、24]、効率的な固定化を保証したため、QDエンコード蛍光微粒子の形でバイオイメージング剤を取得するためにレイヤーバイレイヤー堆積技術を使用しましたポリマーシェル内のQD [21]。水溶性の表面修飾QDで光学的にエンコードされた蛍光高分子電解質マイクロカプセルの製造は、最初のステップとしてマトリックスとして機能する炭酸カルシウム微粒子の表面に5つの反対に帯電した高分子電解質層を適用し、続いて高分子電解質シェルを負にエンコードすることで構成されます。帯電したQD、反対に帯電した高分子電解質の保護層でQD層をコーティングし、微粒子のコアマトリックスを溶解し、最後にマイクロカプセル表面をBSAで修飾します(図1)。炭酸カルシウム微粒子の負の表面電荷は、ポリカチオンと微粒子表面との静電相互作用によるPAHの吸着を保証します。粒子へのPAH吸着から生じる表面の正のゼータ電位により、PSSポリアニオンの後続の適用、およびHS-PEG 12 で修飾されたQDが可能になります。 -COOHは、カルボキシル基のために負の表面電荷を持っているため、PAHポリカチオン層に吸着することができます。図1a、bに示すように、高分子高分子電解質膜へのQDの埋め込みは、追加の被覆高分子電解質層(少なくとも4〜6層)を適用することによって実行されます。
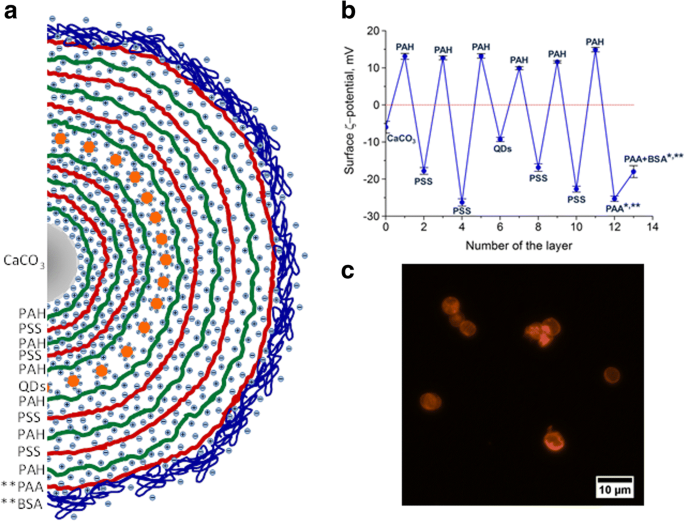
量子ドット(QD)でエンコードされた高分子電解質マイクロカプセルの設計と構造: a ポリマーマイクロカプセル膜の層の配置の概略図。 b 高分子電解質の層状化およびQDエンコーディング中の炭酸カルシウム微粒子の表面のζ電位の変化。 c HS-PEG 12 で可溶化されたCdSe / ZnSQDでエンコードされた高分子電解質マイクロカプセルの蛍光顕微鏡写真 -COOH。 *コアが除去された後のマイクロカプセル表面のζ電位。 ** BSAで修飾された表面を備えたQDエンコード高分子電解質マイクロカプセルの製造における追加の段階
ポリマー膜に固定化されたQDを含む中空マイクロカプセルは、炭酸カルシウム微粒子を0.2 M EDTA(pH 6.5)で溶解し、エチレンジアミン四酢酸のカルシウム塩の水溶性複合体を形成することによって得られます。マイクロカプセル内の空洞。 BSAで修飾された表面を備えたQDエンコード高分子電解質マイクロカプセルを得るために、PAAポリアニオンはPAHポリカチオンの11番目の層に層状になっています。マイクロカプセル表面との相互作用の際の解離定数の値のために、PAAが使用されます。 PAAのpKa値(pKa≈4.7)はPSS(pKa≈7.5)と比較して低く、したがってより酸性であり[25、26]、その結果、マイクロカプセル表面のζ電位が高くなります。 PAAで修飾された表面の電荷は、BSAとPAAの間の静電相互作用により、BSAの受動吸着を促進します。ただし、PAAとBSAの間で組み立てると、マイクロカプセルの負の表面電荷が減少します(図1b)。マイクロカプセル表面へのBSAの沈着後、BSAの静電的に正のアミノ基による負に帯電したPAA層の遮蔽が発生します。したがって、BSAでコーティングされたQDでエンコードされたマイクロカプセルのζ電位は、BSAの静電挙動によって主に決定されます。外側のマイクロカプセルコーティング[26]。
水溶性のPEG化QDは、サイズ分布が狭く、分散液に凝集がなく、コロイド安定性が高いという特徴があります。これにより、マイクロビーズ表面へのQDの均一な吸着が保証され、効果的なエンコードが容易になり、明るい蛍光マイクロカプセルが得られる可能性があります(図1c)。
表面修飾にBSAなどのタンパク質を使用すると、ポリマーマイクロカプセルの生体適合性が高まり、相互の接着に対する耐性が高まります。これにより、マイクロカプセル表面の一時的な不動態化も保証されます。これは、細胞とのinvitro相互作用およびinvivo挙動の観点から、PAH-PSSまたはPAH-PAAインターポリマー複合体によって形成されるマイクロカプセルのその後の研究にとって重要です[27,28,29]。 。
得られたQDエンコードマイクロカプセルは球形であり(図1c)、平均サイズが4.45±0.65μmの狭いサイズ分布(図2)が特徴です。このサイズは赤血球のサイズに匹敵し、それよりもさらに小さい[30]。さらに、先に示したように、マイクロカプセルの高分子膜は変形しやすい柔軟な構造です。静脈内に注射されると、このサイズのマイクロカプセルは血液組織の障壁を越えて浸透することができず、これにより、体内で光学的にコード化されたマイクロカプセルの輸送と分布を追跡することができます[31、32]。しかし、炎症や腫瘍増殖領域など、血管壁の透過性が向上した局在化では、マイクロカプセルが血管外空間に浸透する可能性があり、これにより、標的化送達のイメージングとモニタリングが確実になります[33,34,35 、36]。
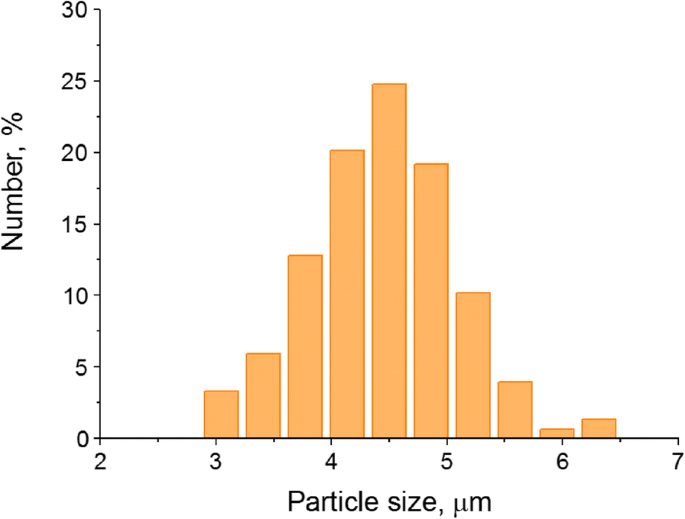
量子ドットで光学的にエンコードされた高分子電解質マイクロカプセルのサイズ分布。分析されたマイクロカプセルの数は600でした。
QDでエンコードされた高分子電解質マイクロカプセルの蛍光および構造特性
製造されたマイクロカプセルは、波長590 nmの蛍光ピークを特徴としています。これは、マイクロカプセルの光学的符号化に使用された元の水溶性QDの蛍光ピークに対応します。これは、マイクロカプセル膜を構成する高分子高分子電解質が、マイクロビーズおよびそれらから調製されたマイクロカプセルのQDの蛍光特性、特に蛍光の最大値に影響を与えないことを示しています(図3)。
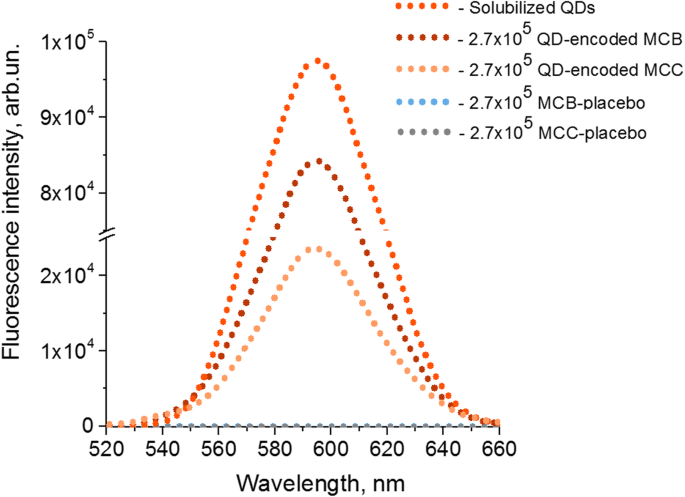
マイクロビーズ(MCB)およびマイクロカプセル(MCC)の高分子膜への量子ドット(QD)の取り込みが、それらの蛍光特性に及ぼす影響:2.241mgのQDを含むQD溶液の蛍光スペクトルが示されています。これは、MCBの光エンコーディングに使用されるQDの量に対応します
図4は、PE(575/25 nm)蛍光チャネルとFSC-AおよびSSC-A(488/10 nm)における、QDでエンコードされたマイクロカプセルとプラセボマイクロカプセルの集団からの信号強度の分布ヒストグラムを示しています。 )フローサイトメーターのチャネル。データは、PE(575/25 nm)チャネルでのプラセボと光学的にエンコードされたマイクロカプセルの効果的な区別を示しています(図4a、b)。 PE(575/25 nm)チャネルのマイクロカプセルからの蛍光シグナルの強度は〜10 4 です。 、QDでエンコードされたマイクロカプセルの高い蛍光容量を示しています。 FSC-AチャネルとSSC-A(488/10 nm)チャネルでは、2つのマイクロカプセル集団の分布が重なり合っています。これは、プラセボとエンコードされたマイクロカプセルの相対的なサイズと粒度のパラメータが類似していることを示しています(図4c、d)。 、集団の均質性。明らかに、これは、マイクロカプセル膜が同数のポリマー層からなり、コード化されたマイクロカプセルの膜がQDの1つの層のみを含むという事実によるものである。したがって、得られたマイクロカプセルは、均一なサイズ分布と最適な蛍光特性によって特徴付けられ、フローサイトメーターの対応するチャネルでの検出を保証します。
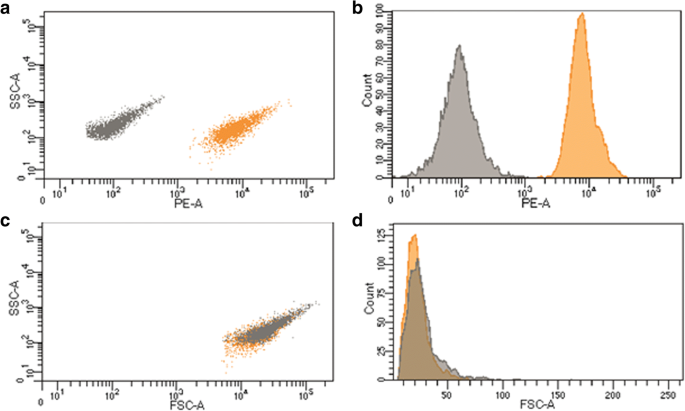
フローサイトメトリーによるQDエンコード高分子電解質マイクロカプセルの検出可能性: a SSC-PEチャネルのマイクロカプセルドットプロットプロファイル。 b PEチャネルのマイクロカプセル分布ヒストグラム。 c SSC-FSCチャネルのマイクロカプセルドットプロットプロファイル。 d FSCチャネルのマイクロカプセル分布ヒストグラム。 QDフリーのマイクロカプセル(プラセボ)をコントロールとして使用し、灰色で示しています。一方、CdSe / ZnS量子ドット(最大590 nmでの蛍光発光)でエンコードされたものはオレンジ色で示しています。分析されたイベントの数は2500でした。ドットプロットとヒストグラムの軸は、SSC-A、FSC-A、PE-Aとして表示されます。ここで、Aはデータが信号領域で表されることを意味します
図5に示すQDでエンコードされた高分子電解質マイクロカプセルの断面の顕微鏡写真は、マイクロカプセルが中空であり、検出された明るい蛍光信号がQDを含む高分子膜から放出されていることを示しています。これらのデータは、コアを溶解するために使用される手順の効率を確認し、製造されたマイクロカプセルの明るい蛍光シグナルを示します。これは、対応するフィルター、蛍光顕微鏡およびフローサイトメトリーの場合にそれぞれテキサスレッドおよびPEを使用して検出できます。ポリマーシェルにQDを含む調製された高分子電解質マイクロカプセルは、フルオレセインイソチオシアネート(FITC)やアミノフルオレセインなどの従来の色素で標識された高分子電解質マイクロカプセルと比較して、より高い蛍光特性を備えています[14、37]。そうでなければ、レイヤーバイレイヤーアプローチを使用してQDでエンコードされたマイクロカプセルは、膨潤技術を使用して有機色素でエンコードされたマイクロビーズの明るさに匹敵するか、それよりも劣る明るさを持ちます。明るさは、吸光係数と量子収率の積によって決まります。室温での水溶性QDの量子収率は約40%であり、有機色素の量子収率に匹敵します[22、38、39]が、QDの吸光度は有機色素の約100倍です。そうしないと、QDのサイズが大きいため、マイクロカプセルシェル内の量が有機色素分子の量と比較できない場合があります。したがって、有機色素分子をコード化する量は、QDの場合よりもはるかに優れているため、同等の明るさが保証されます。反対に、QDを使用してマイクロカプセルをエンコードすると、光退色がまったくないなどの重要な比較優位が得られます。さらに、異なる色(サイズ)のQDは、同じ波長の励起で励起される場合があります。したがって、マイクロカプセルのエンコードに異なる色のQDを使用すると、スペクトル分解された光コードの数が実質的に無制限になる可能性があります[21]。
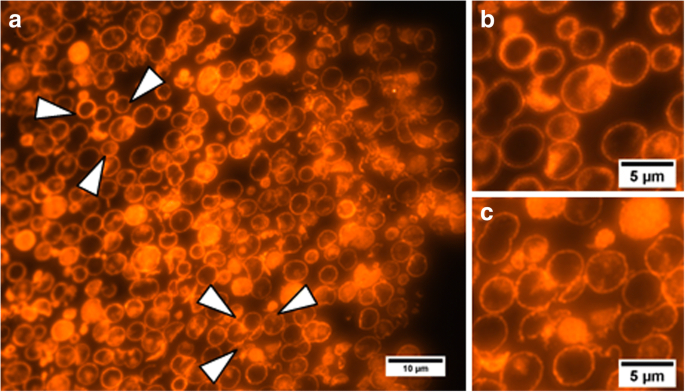
量子ドットでエンコードされた高分子電解質マイクロカプセルの切片の顕微鏡写真。 ( a の矢印 )( b に示されている領域を示します 、 c )高倍率で
結論
QDでエンコードされた高分子電解質マイクロカプセルを取得するために開発された技術は、効果的な光エンコードを保証します。製造されたポリマーマイクロカプセルは、市販のフローサイトメーターおよび共焦点顕微鏡による効率的な検出に使用される最適なサイズ分布および高い蛍光強度によって特徴付けられます。したがって、設計されたマイクロカプセルは、invitroおよびinvivoバイオイメージングのための潜在的な蛍光剤です。用途の広いマイクロカプセルベースのプラットフォームのさらなる開発は、光励起とともにさまざまな外部の物理的または化学的刺激に応答する蛍光QDエンコード微粒子に基づく新しいバイオイメージングおよびセラノスティックツールの提案を目的としています。
略語
- BSA:
-
ウシ血清アルブミン
- EDTA:
-
エチレンジアミン四酢酸二ナトリウム
- PAA:
-
ポリアクリル酸
- PAH:
-
ポリカチオンポリ(アリルアミン塩酸塩)
- PEG:
-
ポリエチレングリコール
- PSS:
-
ポリアニオンポリ(4-スチレンスルホン酸ナトリウム)
- QD:
-
量子ドット
- TOPO:
-
トリオクチルホスフィンオキシド
ナノマテリアル
- ヒューズを使用したジェンダーに配慮した個別化された製品の製造1
- 半導体ナノ粒子
- コバルトをドープしたFeMn2O4スピネルナノ粒子の調製と磁気特性
- グラファイトナノプレートレットを備えた多層カーボンナノチューブに基づくハイブリッド複合材料の電気的性質
- フェニルトリメトキシシランで修飾されたアルミナナノ粒子をベースにしたAl2O3:SiOCナノコンポジットの形成と発光特性
- 界面層の設計によるZnO膜の表面形態と特性の調整
- Ag n V(n =1–12)クラスターの構造的、電子的、および磁気的特性の調査
- ポリオール媒介プロセスによるZnOナノクリップの製造と特性評価
- 半導体ナノ結晶でコード化された高分子電解質マイクロカプセルに基づく次世代セラノスティック剤:開発と機能特性評価
- GeSiSnナノアイランドと歪み層を備えた半導体膜の形態、構造、および光学特性
- スマート業界の新しいツールを使用して技術者とエンジニアを準備する



