ヒト肝ミクロソームにおけるテストステロン代謝に対する金ナノ粒子の影響
要約
金ナノ粒子(AuNP)-タンパク質コロナ複合体は、それらの物理化学的特性を変化させることにより、シトクロムP450(CYP)を介したテストステロン(TST)代謝を変化させることができます。分岐ポリエチレンイミン(BPEI)、リポ酸(LA)、およびポリエチレングリコール(PEG)で機能化された40および80 nm AuNPを使用して、プールされたヒト肝ミクロソーム(pHLM)のTST代謝におけるNPサイズ、表面化学、およびタンパク質コロナの影響を調査しました。 )およびヒト血漿タンパク質コロナ(PC)。 AuNPを介したTST代謝の個人差は、異なるレベルのCYP活性を含む単一ドナーHLM間でも特徴づけられました。 40 nmAuNPおよび程度は低いが80nm AuNPの阻害効果は、pHLMで合計5つのTSTのヒドロキシル化代謝物の生成に対して発生しましたが、PCはそれらを軽減しました。一方、裸のAuNPはアンドロステンジオンの生成を増加させました。 TST代謝の個人間変動は、単一ドナーHLM内で発生しました。ほとんどの場合、40および80nmの裸およびPCAuNPは、非阻害濃度でTST代謝を本質的に抑制しましたが、PCPEG-AuNPはアンドロステンジオンを増加させました。これらの研究は、TST代謝を変化させることにより、TSTかく乱物質としてのAuNPの役割の理解を深めるのに役立ち、潜在的な内分泌かく乱物質として他のNPをスクリーニングするために利用できます。
はじめに
金ナノ粒子(AuNP)は、その独特の光学的および物理的特性により、ドラッグデリバリー、医療診断、癌治療薬、および消費者製品、つまり化粧品、食品包装に広く使用されています[1,2,3]。タンパク質の混合物にさらされると、NPはタンパク質と結合し、タンパク質コロナを形成します。これにより、表面化学、吸着タンパク質のコンフォメーション、およびその後の生物学的応答、すなわちNP毒性、細胞NP取り込み、シトクロムP450(CYP )薬物に対する酵素[4,5,6,7]。初代上皮細胞と癌細胞株を用いたinvitro研究は、AuNPがヒト肝細胞、肝細胞株C3A、および精子細胞に対して毒性があることを示唆しています[6,7,8]。しかし、NPの周りのタンパク質コロナの形成は、表面化学に依存する方法でAuNP毒性を集中的に弱めたり増強したりしました[6、7]。タンパク質コロナは、サイズや表面電荷に関係なく、ヒト肝細胞、腎近位尿細管細胞、HepG2細胞、C3A細胞株におけるAuNPの細胞取り込みを妨害しました[6、7、9、10、11、12]。
肝CYP酵素は、主に内因性および外因性化合物の合成および/または代謝に関与しますが、広範囲の薬剤、すなわち、薬物、農薬、またはNPは、ステロイドホルモンの合成、代謝、および/または解毒に逆に影響を及ぼし、薬理学的効果をもたらしますそして生理学的機能[13,14,15,16,17]。テストステロン(TST)は、位置選択的および立体選択的に重要なアンドロゲンおよびCYP3A4特異的基質(6β-OHTSTへの主な変換)です[18]。フェーズI代謝中、TSTはCYP3A4によって2β-OHTSTにヒドロキシル化され、CYP2D6によってアンドロステンジオン(AD)に脱アルキル化されます[17、19]。ヒト肝細胞、C3A細胞株、ヒト肝ミクロソーム(HLM)、および組換えCYP酵素を用いたin vitro研究では、裸のタンパク質コロナ被覆AuNPが、CYP1A2、2C9、2C19、2D6、2E1を含む広範囲のCYP酵素を調節することが示唆されました。および3A4 [6、7、20、21]。他の金属NPである裸のAgNPも、HLMにおけるCYP3A4を介した6β-OHTSTの産生を抑制しました[22]。分岐ポリエチレンイミン(BPEI)とリポ酸(LA)で機能化されたAuNPは、C3A細胞株のCYP3A4活性を低下させましたが、ヒト血漿タンパク質コロナ(PC)はそれを弱めました[7]。対照的に、裸(PCなし)およびPC BPEI-AuNPは、NPサイズに関係なく、ヒト肝細胞のCYP2C9および3A4を阻害しました[6]。
インビボ研究では、小さなサイズのAuNP(4および13 nm)が主に雄のBALB / cマウスの肝臓および脾臓に蓄積し、肝臓のCyp1a1および2b遺伝子の発現を誘導したことが報告されています[23]。他の金属NP、酸化亜鉛NPは、雄のSprague Dawleyラットの肝臓のCYP1A2、2C11、および3A2活性を阻害し、肝臓の病理学的変化が増加しました[24]。
今日まで、生物学的に関連するタンパク質コロナの非存在下および/または存在下で、AuNPがCYPを介したTST代謝(TSTのヒドロキシル化および脱アルキル化)をどのように関連付けるかはほとんどわかっていません。この研究の目的は、40および80nmのカチオン性BPEIAuNP、アニオン性LA AuNP、および中性ポリエチレングリコール(PEG)AuNPの物理化学的特性に対するPCの影響を調査することです。 PCを使用した場合と使用しない場合のCYPを介したTST代謝に対するAuNPの影響は、pHLMを使用して特徴付けられます。 TST代謝の個人差も、さまざまな程度のCYP酵素を含む単一ドナーHLM内で研究されます。
メソッド/実験
化学薬品
2,3,4- 13 C 3 テストステロン(CAS#327048-83-9)および6β-ヒドロキシテストステロン(6β-OHTST、CAS#62-99-7)は、MilliporeSigma(セントルイス、ミズーリ州)から入手しました。テストステロン(TST、CAS#58-22-0)、2α-ヒドロキシテストステロン(2α-OHTST、CAS#004075-14-3)、2β-ヒドロキシテストステロン(2β-OHTST、CAS#10390-14-4)、6α -ヒドロキシテストステロン(6α-OHTST、CAS#2944-87-8)、11β-ヒドロキシテストステロン(11β-OHTST、CAS#1816-85-9)、15β-ヒドロキシテストステロン(15β-OHTST、CAS#39605-73- 7)、16α-ヒドロキシテストステロン(16α-OHTSTCAS#63-01-4)、16β-ヒドロキシテストステロン(16β-OHTST、CAS#17528-90-4)、11-ケトテストステロン(CAS#564-35-2) 、アンドロステンジオン(AD、CAS#63-05-8)、4-ヒドロキシアンドロステンジオン(CAS#566-48-3)、および11β-ヒドロキシアンドロステンジオン(CAS#382-44-5)は、Steraloids(Newport、RI)から購入しました。 )。 LC-MSグレードのアセトニトリルと-ホルム酸はFisherScientific(ニュージャージー州フェアローン)から入手し、超純水はMerck KGaA(ドイツ、ダルムシュタット)のSynergy®UV-Rシステムによって社内で製造しました。特に明記されていない限り、他のすべての試薬はMilliporeSigma(ミズーリ州セントルイス)から購入しました。
ヒト肝ミクロソーム
プールされたヒト肝ミクロソーム(pHLM)(200人のドナー、100人の男性、および100人の女性)および単一ドナーの肝ミクロソームは、Corning Inc.(Charlotte、NC)から入手しました。 pHLMはサプライヤーによってプールされますが、単一ドナーHLMのプールではありません。この研究で使用されたシングルドナーHLMの特性と選択されたシトクロムP450(CYP)酵素活性は、追加ファイル1:表S1に示されています。
金ナノ粒子の合成
カチオン性分岐ポリエチレンイミン(BPEI)、アニオン性リポ酸(LA)、および中性ポリエチレングリコール(PEG)で官能化されたBiopure™40および80 nm球状AuNPは、nanoComposix(San Diego、CA)から購入しました。コア材料は、テトラクロロ金酸水素(III)水和物(HAuCl 4 )の還元によって合成されました。 3H 2 O)炭酸カリウム水溶液中で、エージングプロセスとタンジェンシャルフローろ過(TFF)を行いました。 AuNP表面は、ジヒドロリポ酸(0.2:1、 w )を添加することにより、LAまたはPEGで機能化されました。 / w )またはチオール-メトキシ末端PEG(Laysan Bio Inc.、アラバマ州アラブ)(0.5:1、 w / w )、それぞれ、TFF洗浄と滅菌ろ過を使用します。 BPEIで官能化された表面は、LAのカルボン酸をBPEIのアミンに結合することにより、EDC / NHS化学を介して合成されました。未結合のBPEIは、TFF洗浄とそれに続く遠心分離で除去されました。
ヒト血漿タンパク質コロナの調製
プールされたヒト血漿(HP、 n =5)Biological Specialty Corp.(Colmar、PA)から入手しました。 40および80nmのAuNPは、総血液量の生理学的血漿量が55%( v )のヒト血漿とインキュベートされました。 / v )軌道振とう/回転インキュベーター内、37°C、250rpmで1時間。インキュベーションの最後に、NPを取り巻くヒト血漿タンパク質コロナ(PC)を、20,000× g での遠心分離によって収集しました。 20°Cで20分間、続いてリン酸緩衝生理食塩水(PBS)で3回洗浄します。未結合および緩く結合したタンパク質を遠心分離によって廃棄した。得られたPCAuNPをPBSに分散させ、物理化学的特性とTSTとの相互作用の特性評価に使用しました。
AuNPの物理的特性評価
粒子サイズと表面特性は、動的光散乱(DLS)と透過型電子顕微鏡(TEM)によって測定されました。流体力学的直径(D H )、および脱イオン(DI)水中の40および80 nm裸(PCなし)BPEI-、LA-、およびPEG-AuNPとPBS中のPC AuNPのゼータ電位を、Zetasizer Nano-Zs(Malvern Instruments、英国ウスターシャー)、25°Cで0時間。 D H 、多分散度指数(PDI)、およびゼータ電位は、ミクロソームインキュベーションバッファー(pH 7.4)中の裸およびPC AuNPについて、0分および37°Cで45分でも得られました。サンプルは、それぞれ10秒の11回のサブランで5回測定されました。 TEMは、裸およびPCAuNPの形態を特徴づけました。すべてのAuNPは、formvarでコーティングされた銅グリッド上に配置され、加速電圧120 kVでオックスフォード検出器(FEI Company、オレゴン州ヒルズボロ)を備えたTecnai G2 SpiritBioTWINで表示されました。 GATAN顕微鏡スイート(GATAN Inc.、カリフォルニア州プレザントン)は、AuNPの直径を測定しました。光学吸収スペクトルは、Spectra Max i3マルチモードマイクロプレートリーダー(Molecular Devices、カリフォルニア州サニーベール)を使用して測定しました。
裸およびPCAuNPの非存在下および存在下でのテストステロンのinvitro代謝
予備研究を実施して、インキュベーション時間とミクロソームタンパク質濃度を決定し、TSTの線形代謝率(最終濃度10μM)を提供しました。 TST代謝物の生成は、1.3〜9.3mgのミクロソームタンパク質mL -1 で直線的でした。 最大60分間。代謝アッセイは完全に記載されているように実施された[25]。簡単に説明すると、ミクロソームインキュベーションバッファー中のpHLMを10μMTSTで処理した後、40および80 nmの裸(PCなし)のAuNPを0、7、32、63、143、250、400、および571μgmLで添加しました -1 ; PC AuNP pHLM 0、7、32、63、および143μgmL -1 の場合 。ミクロソームインキュベーションバッファーには、100 mMリン酸バッファー、3.3 mM MgCl 2 が含まれていました。 、および1 mM EDTA(pH 7.4)。代謝反応は、0.25 mM NADP、2.5 mMグルコース-6-リン酸、および2 U mL -1 を含むNADPH再生システムの有無にかかわらず開始されました。 グルコース-6-リン酸デヒドロゲナーゼ。 37°Cで45分間インキュベートした後、4%( v / v )リン酸水溶液(1:1、 v / v )。 3500 rpmで20分間遠心分離した後、サンプルの上清を収集し、さらに使用するまで-20°Cで保存しました。さらに、ミクロソームインキュベーションバッファー中のシングルドナーHLMを10μMTSTで処理した後、63μgmL -1 でインキュベートしました。 すべての裸およびPCAuNPの37°Cで45分間。インキュベーションの最後に、サンプルを処理し、上記のように-20°Cで保存しました。
標準とサンプル準備
TST、その代謝物、および 13 の一次標準原液 C 3 -内部標準(ISTD)としてラベル付けされたTSTは、1 mMの濃度でメタノールで調製され、さらに使用するまで-20°Cで保存されました。 TSTとその代謝物の標準溶液の濃度は、一次原液の段階希釈で0.01、0.05、0.1、0.5、1、5、10、50、100、および200μMでした。標準キャリブレータの場合、各作業標準溶液の50μLアリコートを450μLの反応バッファーに加えて1:10に希釈し、0.1μMのISTD溶液も4%リン酸水溶液を使用して調製しました。品質管理(QC)サンプルは、0.01、0.05、および0.1μMの濃度で調製されました。
解凍後、サンプルを3500 rpmで20分間、室温で遠心分離しました。上清に50μLの0.1μMISTDを添加し、Oasis PRIME HLB 96ウェルμ溶出プレートと収集プレートをWaters陽圧-96プロセッサーで、80 psiで1〜2分間処理しました。 (ウォーターズコーポレーション、マサチューセッツ州ミルフォード)。 5%メタノールを含む300μLの水で洗浄し、50μLのアセトニトリル/メタノール混合液(90/10、 v )で溶出した後 / v )、得られた溶離液を50μLの水(最終容量100μL)で希釈し、液体クロマトグラフィー-質量分析(LC-MS / MS)にかけました。
液体クロマトグラフィー-質量分析
すべてのサンプルは、Waters Acquity Ultra Performance Liquid Chromatography system with Triple Quadrupole Detector(UPLC TQD)(Waters Corp.、Milford、MA)を備えたWaters UPLC HSS T3カラム(2.1×50 mm、1.8μm)で分離されました。移動相AとBは、それぞれ水中の0.1%ギ酸とメタノール中の0.1%ギ酸でした。 600μLmin -1 の流量でグラジエントLCメソッドを使用しました 0〜8.4分。勾配は、0〜1分(30%B)、1〜3分(50%Bまで)、3〜3.5分(50%B)、3.5〜7分(80%Bまで)、7〜7.01分( 〜98%B)、7.01〜7.5分(98%B)、および7.51〜8.4分(30%B)。 MSの状態を以下に簡単に説明しました。イオン化源はエレクトロスプレーポジティブ(ESI + )キャピラリー電圧4000Vのモード。ソース温度150°Cの場合。脱溶媒和温度は450°Cです。脱溶媒ガスの流量(N 2 )、コーンガス(N 2 )、および衝突ガス(アルゴン)は900 L h -1 、100 L h -1 、および0.1 mL min -1 、 それぞれ。スキャンタイプはマルチプルリアクションモニタリング(MRM)で、MSの実行時間は8.4分でした。分析に使用したMRMトランジションは、追加ファイル1:表S2および図2にまとめられています。注入量は2 µLで、分析中はカラムを50°Cに維持しました。すべての定量メソッドは、0.001〜20μMの濃度範囲にわたる7点の検量線に基づいています。 TSTおよびターゲット代謝物について、0.001μMおよび0.005μMの検出限界(LOD)および定量限界(LOQ)が確立されました。
統計分析
D H に対する分散剤の影響 裸のPDIとAuNP上のPCは、学生の t を使用して評価されました。 両側分布でテストします。最大阻害濃度の半分(IC 50 )および最大活性化濃度の半分(EC 50 )pHLMでのCYP依存性TST代謝物の生成に向けたAuNPの量は、GraphPadPrism®を使用して観測データに可変勾配のヒル方程式を当てはめることによって決定されました。一元配置分散分析(ANOVA)は、GraphPadPrism®を使用して実施され、シングルドナーHLMのTST代謝に対するAuNP治療の効果を評価しました。効果が有意である場合、5%の有意水準でテューキーの正直有意差(HSD)検定を使用して多重比較を実行しました。ピアソン相関係数( r )シングルドナーHLMのCYP活性と、CYP依存性TST代謝物の生成との間は、GraphPadPrism®バージョン6.07(La Jolla、CA)を使用して決定されました。
結果と考察
裸およびヒト血漿タンパク質コロナAuNPの物理化学的特性評価
NPサイズ、表面電荷、形態、およびスペクトル特性におけるヒト血漿タンパク質コロナ(PC)の影響は、DLS、TEM、およびUV-Vis分光法を使用して特徴付けられています(図1)。 TEM画像は、40nmと80nmのPCBPEI-AuNPを除くすべての裸(PCなし)とPC AuNPが単分散であり、安定したサイズ分布と固有のUV-Visスペクトル範囲(520〜557 nm)を示しました(図1a、b) 。 PBS中のAuNP周辺の明確なPCもTEMによって発見されました。 25°Cで0分でのPBS中の40および80nm PCコーティング分岐ポリエチレンイミン(BPEI)-AuNPの凝集は、サイズ分布の複数のピークと、裸のBPEI-AuNPと比較した吸収スペクトルの赤方偏移を相関させました(図1b)。流体力学的直径(D H )25°Cで0分でPBSに溶解し、37°Cで0および45分でミクロソームインキュベーションバッファーに溶解した40および80 nm PC BPEI-AuNPの値は、サイズ分布の複数のピークとともにDLSによって決定されませんでした。 D H ミクロソームインキュベーションバッファー中の40nmの裸のBPEI-およびLA-AuNPとPCPEG-AuNP、および80 nmの裸のBPEI-AuNPの値は、37°Cで45分まで大幅に増加しましたが、80nmのPCLAでは値が減少しました。 -AuNP(表1)。 40nmの裸およびPCPEG-AuNPと80nmのPCPEG-AuNPの多分散度指数(PDI)は、37°Cで45分で増加しました。さらに、40nmおよび80nmの裸のBPEI-AuNPと40nmの裸のPEG-AuNPのゼータ(z)電位値は、時間の経過とともに大幅に減少しました。以前の研究では、ヒト肝ミクロソームタンパク質に関連するAuNP(7および70 nm)が、UV-可視範囲で最大の特徴的な吸光度を変化させたことが報告されています[21]。これらの結果は、PCおよびヒト血清アルブミンコロナが、溶解媒体およびインキュベーション時間に関係なく、NPサイズ、最大吸光度の赤方偏移、および形態を変化させたという最近の研究によって裏付けられました[6、7、10、26]。 PCを介したNPの物理化学的特性とCYP活性の酵素機能の変化に基づいて[6、7]、CYPを介したヒト肝ミクロソームTST代謝に対する40および80nmのAuNPの潜在的影響をより生物学的に調査しました。関連するPC。

( a の透過型電子顕微鏡写真 )脱イオン水中の40nmおよび80nmの裸のAuNPおよび b 25°Cで0時間のPBS中の40および80nm PC AuNP、UV吸収スペクトル(上の挿入図)、および動的光散乱分布(下の挿入図)。矢印はPCの形成を示します。 BPEI 分岐ポリエチレンイミン、 LA リポ酸、 PEG ポリエチレングリコール、 ND 未定、 PC ヒト血漿タンパク質コロナ、裸 PCなし
プールされたヒト肝ミクロソームにおけるAuNPを介したテストステロン代謝
TSTの合計11の代謝物がスクリーニングされ、6つの代謝物が10μMTSTのプールされたヒト肝ミクロソーム(pHLM)で検出されました。 TSTと6つの選択された代謝物のターゲットLC-MS / MS分析を図2に示します。選択された代謝物のリストには、5つのヒドロキシル化TST代謝物(2β-OHTST、6β-OHTST、15β-OHTST、16α)が含まれています。 -OH TST、16β-OHTST)および脱アルキル化代謝物(アンドロステンジオン、AD)。これは、TSTが主に6β-OHTSTにヒドロキシル化され、程度は低いが2β-OHTST、15β-OHTST、16α-OHTST、および16β-OHTSTにヒドロキシル化されたというヒト肝細胞およびHLMを使用した以前の研究と相関しています。脱アルキル化代謝物、AD [17、19、27]。
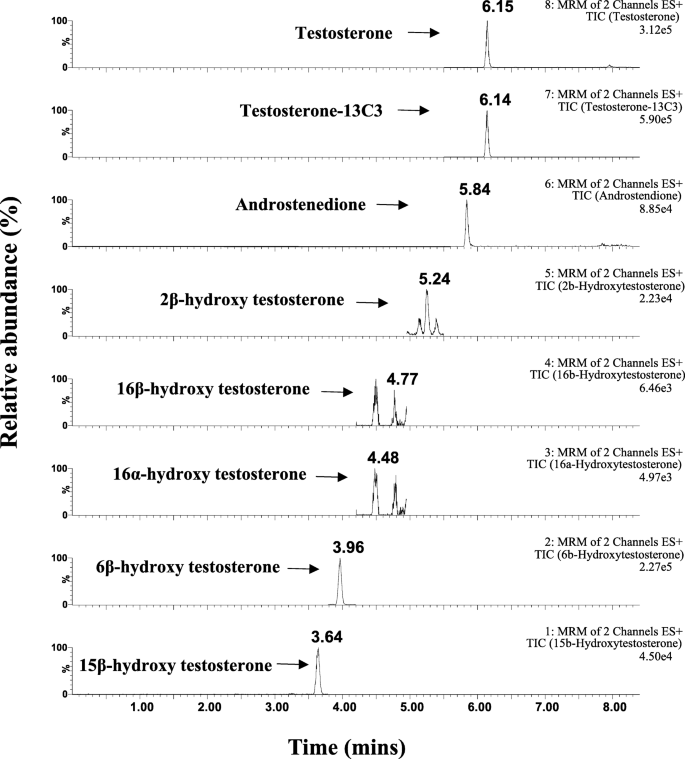
テストステロン(TST)の抽出イオンクロマトグラム(XIC)、 13 C3標識TST、アンドロステンジオン、2β-ヒドロキシテストステロン(2β-OHTST)、16α-ヒドロキシテストステロン(16α-OHTST)、16β-ヒドロキシテストステロン(16β-OHTST)、6β-ヒドロキシテストステロン(6β-OHTST)、および15β -ヒドロキシテストステロン(15β-OHTST)は、NADPHの存在下で37°Cで45分間、最終濃度10μMのテストステロンでプールされたHLMで生成されます。 HLM ヒト肝ミクロソーム、 NADPH 還元型ニコチンアミドアデニンジヌクレオチドリン酸
pHLMで40および80nmの裸のAuNPとTSTを共培養した結果を、図1および2に示しました。 3および4。すべての40および80nmの裸のAuNPは、pHLMでの2β-OHTST、6β-OHTST、および15β-OHTSTの生成を、さまざまな阻害の程度で変化させました(図3a–f)。最大阻害濃度の半分(IC 50 )6β-OHTSTを生成するための40 nmBPEI-AuNPの値は416μgmL -1 ; 80 nmBPEI-AuNPの場合438μgmL -1 ; 80 nmPEG-AuNPの場合387μgmL -1 (図3c、d)。 15β-OHTST生産の場合、IC 50 40nmのBPEI-AuNPの値は1113μgmL -1 でした; 80 nmBPEI-AuNPの場合415μgmL -1 ; 80 nmPEG-AuNPの場合480μgmL -1 (図3e、f)。これらの結果は、金属NP、AgNP、および多孔質シリコンNPがヒト上皮結腸直腸腺癌Caco2細胞、肝細胞癌HepG2細胞、およびヒト肝ミクロソームにおける6β-OHTST産生を阻害したというヒト癌細胞株および肝臓組織を用いたinvitro研究によって裏付けられました。 [22、28]。 40および80nmの裸のAuNPは、最高濃度(517μgmL - 1 )(図4a–d)。 40および80nm BPEI-AuNPは、最高濃度でアンドロステンジオン(AD)の生成を増加させ、対応する代謝率は4.3および2.1 pmolmgタンパク質 -1 でした。 min -1 、それぞれ対照と比較(0.7 pmolmgタンパク質 -1 min -1 )(図4e、f)。しかし、80 nm LA-AuNPは、IC 50 によるAD産生を阻害しました。 233μgmL -1 の値 。これらの結果は、裸のAuNPが、表面コーティングおよびサイズに依存する方法で、選択されたTST代謝物の生成を媒介したことを示しています。さらに、40および80nmのPCAuNPはすべて、最大143μgmL -1 のpHLMでTSTから選択された6つの代謝物の生成を阻害しませんでした。 、表面コーティングに関係なく(図5および6)。特に、PCは、40 nmの裸のBPEI-AuNPを介した6β-OHTSTおよび15β-OHTST産生の高濃度(32μgmL -1 )での阻害を軽減しました。 〜143μgmL -1 )(図3c、eおよび5c、e)。この結果は、40および80 nmの裸のBPEI-、LA-、およびPEG-AuNPがTSTヒドロキシル化(2β-OHTST、6β-OHTST、および15β-OHTST)を用量依存的に減少させることを示しました(図7 )。さらに、40nmと80nmの裸のBPEI-AuNPはAD産生を増加させましたが、前者は16β-OHTSTを減少させました。インビトロ研究は、主にCYP3A4によって媒介される6β-OHTST産生が、用量依存的に単層カーボンナノチューブ(SWCNT)によって阻害されたが、ウシ血清アルブミンコロナがそれを軽減したことを報告した[17、29]。私たちの研究室は最近、40および80nmの裸およびPCBPEI-AuNPが、細胞および転写レベルでCYP1A2、2C9、および3A4の阻害剤として機能したことを報告しました[6、7]。インビボ研究では、PEG-AuNP(4および13 nm)は主に雄のBALB / cマウスの肝臓に蓄積され、肝臓のCyp1a1および2b遺伝子の転写レベルが変化したことが報告されています[23]。静脈内投与された雄のICRマウスPEG-NH 2 の注入 -AuNPは、精子の形態や出産することなく、NPが増加した血漿TSTレベルを示しました[30]。その他の金属NP、二酸化チタン(TiO 2 )はCD1雄マウスの精巣に蓄積し、cyp1b1および2e1の発現を減少させました[31]。疫学研究によると、マサチューセッツ州の不妊クリニックの成人男性は、内分泌かく乱物質として知られているクロルピリホス(CFS)の高曝露に由来する、高レベルの3,5,6-トリクロロ-2-ピリジノール(TCP)と相関する低血漿TSTレベルを示しました。 CYPを介したTST代謝の阻害剤[32]。以前の研究では、既知の内分泌かく乱物質、CFS、CFSオキソン、ホノホス、ホレート、ジエチルトルアミド(DEET)、およびペルメトリンが、ヒドロキシル化および/または脱アルキル化TST代謝物、すなわち2β-OHの生成を実質的に阻害および/または活性化したことが報告されました。ヒト肝臓におけるTST、6β-OHTST、15β-OHTST、ADおよび4-ヒドロキシAD [17]。そうは言っても、AuNPは、CYPを介したTSTの代謝に対する阻害および/または活性化の効力を媒介することにより、潜在的な内分泌かく乱物質である可能性があると仮定するのは合理的です。
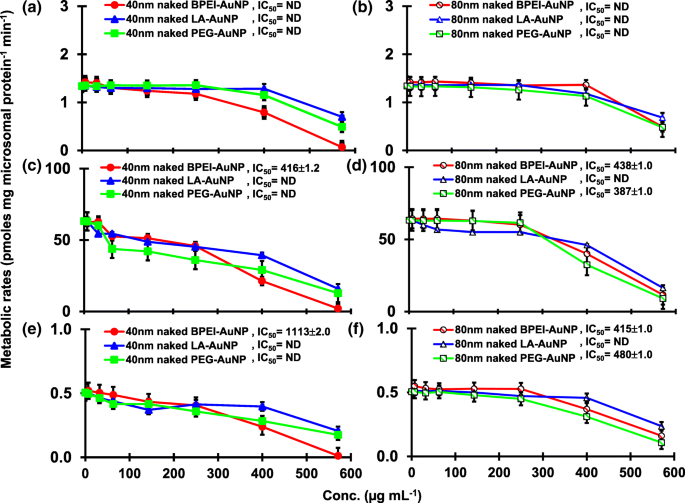
2β-OHTST( a )の生成に対する裸(PCなし)AuNPの阻害効果 、 b )、6β-OHTST( c 、 d )および15β-OHTST( e 、 f )pHLMで。データは平均±S.D。を表します( n =3)。 IC 50 、最大抑制濃度の半分; pHLM 、プールされたヒト肝ミクロソーム; ND 、GraphPadPrism®を使用して観測データに可変勾配のヒルの式を当てはめることによって決定されません。 PC 、ヒト血漿タンパク質; BPEI 、分岐ポリエチレンイミン; LA 、リポ酸; PEG、ポリエチレングリコール;濃度、濃度; 2β-OHTST、2β -ヒドロキシテストステロン; 6β-OHTST、6β -ヒドロキシテストステロン; 15β-OHTST、15β -ヒドロキシテストステロン
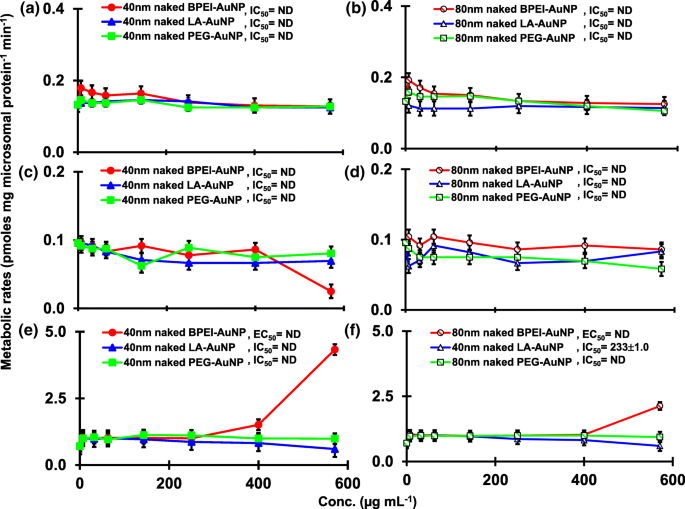
16β-OHTST( a )の生成に対する裸(PCなし)AuNPの抑制および刺激効果 、 b )、16β-OHTST( c 、 d )およびAD( e 、 f )pHLMで。データは平均±S.D。を表します( n =3)。 IC 50 、最大抑制濃度の半分; EC 50 、最大活性化濃度の半分; pHLM 、プールされたヒト肝ミクロソーム; ND 、GraphPadPrism®を使用して観測データに可変勾配のヒルの式を当てはめることによって決定されません。 PC 、ヒト血漿タンパク質; BPEI 、分岐ポリエチレンイミン; LA 、リポ酸; PEG 、 ポリエチレングリコール;濃度、濃度; 16α-OHTST、16α -ヒドロキシテストステロン; 16β-OHTST、16β -ヒドロキシテストステロン; AD 、アンドロステンジオン。
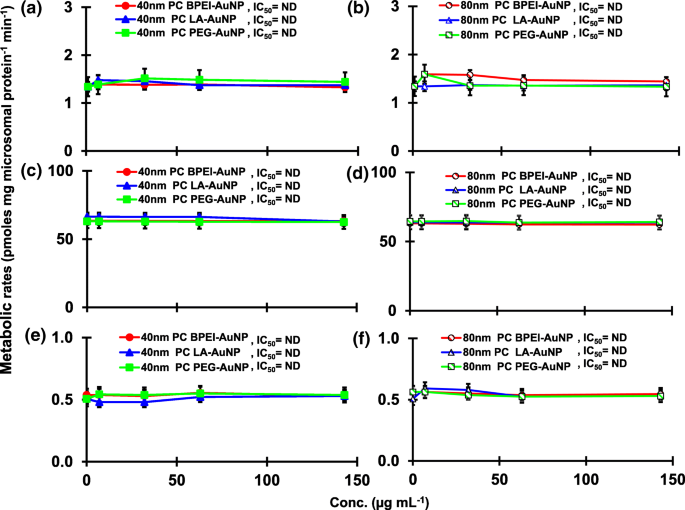
2β-OHTST( a )の生成に対するPCAuNPの影響 、 b )、6β-OHTST( c 、 d )および15β-OHTST( e 、 f )pHLMで。データは平均±S.D。を表します( n =3)。 IC 50 、最大抑制濃度の半分; pHLM 、プールされたヒト肝ミクロソーム; ND 、GraphPadPrism®を使用して観測データに可変勾配のヒルの式を当てはめることによって決定されません。 PC 、ヒト血漿タンパク質コロナ; BPEI 、分岐ポリエチレンイミン; LA 、リポ酸; PEG 、 ポリエチレングリコール;濃度、濃度; 2β-OHTST、2β -ヒドロキシテストステロン; 6β-OHTST、6β -ヒドロキシテストステロン; 15β-OHTST、 15β-ヒドロキシテストステロン。
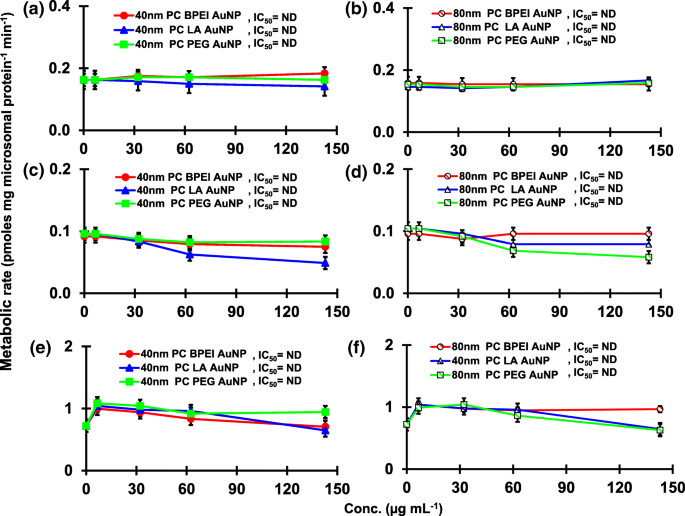
16α-OHTST( a )の生成に対するPCAuNPの影響 、 b )、16β-OHTST( c 、 d )およびAD( e 、 f )pHLMで。データは平均±S.D。を表します( n =3)。 IC 50 、最大抑制濃度の半分; pHLM 、プールされたヒト肝ミクロソーム; ND 、GraphPadPrism®を使用して観測データに可変勾配のヒルの式を当てはめることによって決定されません。 PC 、ヒト血漿タンパク質コロナ; BPEI 、分岐ポリエチレンイミン; LA 、リポ酸; PEG 、 ポリエチレングリコール;濃度、濃度; 16α-OHTST、16α -ヒドロキシテストステロン; 16β-OHTST、16β -ヒドロキシテストステロン; AD 、アンドロステンジオン。
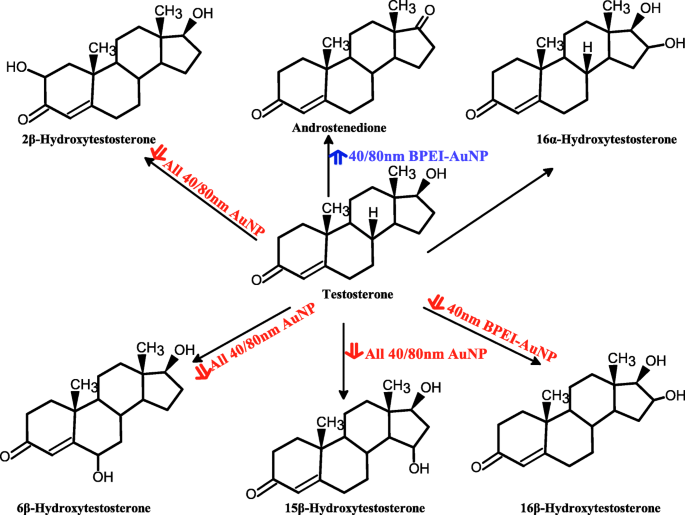
プールされたヒト肝ミクロソームおよびAuNPを介したその代謝産物産生におけるテストステロン代謝の提案されたスキーム。 AuNP 金ナノ粒子、 BPEI 分岐ポリエチレンイミン、 LA リポ酸、 PEG ポリエチレングリコール、 PC ヒト血漿タンパク質コロナ。赤い矢印、抑制効果;青い矢印、刺激効果
シングルドナーヒト肝ミクロソームにおけるTST代謝とAuNPによるその調節
6つの選択された代謝物の生成は、40および80nmの裸のpHLMベースの非阻害濃度およびPCAuNP(10μgmL -1 )。 3つの異なるシングルドナーHLMの間で、TST代謝の個人差が観察されました(追加ファイル1:図S1)。各CYP酵素の触媒活性とTST由来代謝物の生成との関係は、低、中、高のCYP触媒活性を含む3つの異なるシングルドナーHLM内で特徴づけられました(追加ファイル1:表S1)。 6β-OHTSTの産生は、CYP2C19の活性と正の相関がありました( r =0.99および p =0.01)およびCYP3A4( r =0.99および p =0.03)個人内(追加ファイル1:図S2)。 AD産生はCYP4A11と負の相関がありました( r =−0.98および p =0.04)(追加ファイル1:図S3)。これらの結果は、CYP3A4とCYP2D6がそれぞれ主要なTST代謝物である6β-OHTSTとADの生成に重要な役割を果たしたと報告された以前の研究と一致していました[17]。この研究はまた、TSTのCYP依存性代謝の個人差がCYP酵素の遺伝子型とそれらの表現型活性に依存することを示唆しました。以前の研究では、CYP多型と表現型がCYP機能の重要な特徴であり、薬物副作用および/または薬物の有効性と用量を示唆する個々の感受性に寄与する、貧弱、中程度、広範囲、および超高速の代謝物としての分類的薬理遺伝学表現型をもたらすことが報告されましたCYP酵素の代謝が不十分な場合、つまりCYP3A4は、CYP阻害剤であるAuNPへの曝露によるTST代謝の影響を受けやすい可能性があります[33]。
図1と図2に示すように。図8および9では、非阻害濃度でのTSTとAuNPの共培養により、サイズおよび表面変化の変化に応じて、単一ドナーHLM間でCYPを介したTSTの代謝が増加および/または減少しました。 ANOVAは、AuNPサイズ( p )による有意な変化を示しました <0.0001)、表面コーティング( p <0.0001)、およびPC形成( p <0.0001)は、シングルドナーHLM(HDA1、HDB2、およびHDC3)でのTSTの6つの選択された代謝物の生成で観察されました。
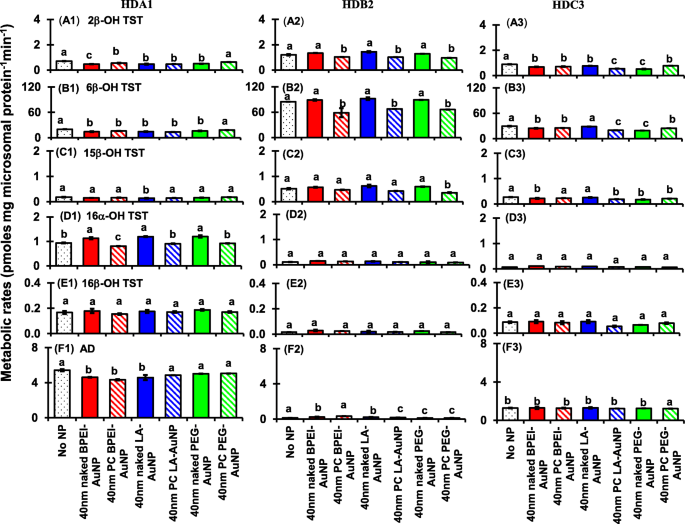
2β-OHTST(A1–A3)、6β-OHTST(B1–B3)、15β-OHTST(C1–C3)、16α-OHTST(D1–D3)の生成に対する40nmネイキッドおよびPCAuNPの影響)、16β-OHTST(E1–E3)、およびAD(F1–F3); 3つの異なるシングルドナーHLM(HDA1、HDB2、およびHDC3)で。同じ文字が続く平均は、各ナノ粒子で有意差はありませんでした(テューキーの正直な有意差=5%)。 裸 PCなし、 PC ヒト血漿タンパク質コロナ、 HLM ヒト肝ミクロソーム、 BPEI 分岐ポリエチレンイミン、 LA リポ酸、 PEG ポリエチレングリコール、2β - OH TST 2β-ヒドロキシテストステロン、6β - OH TST 6β-ヒドロキシテストステロン、15β - OH TST 15β-ヒドロキシテストステロン、16α - OH TST 16α-ヒドロキシテストステロン、16β - OH TST 16β-ヒドロキシテストステロン、 AD アンドロステンジオン
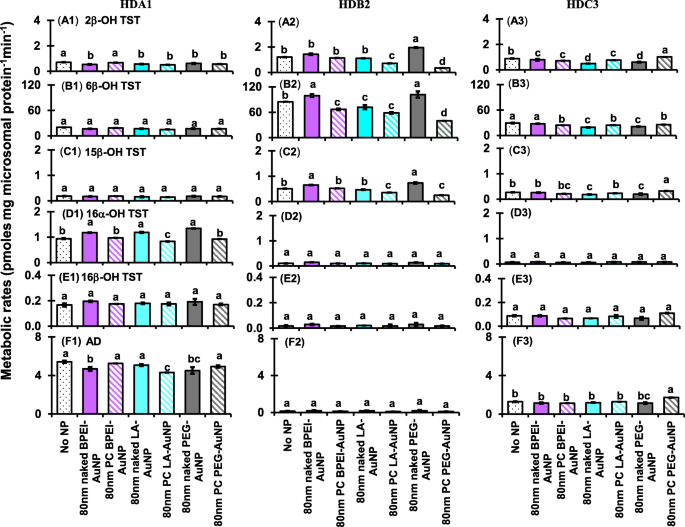
2β-OHTST(A1–A3)、6β-OHTST(B1–B3)、15β-OHTST(C1–C3)、16α-OHTST(D1–D3)の生成に対する80nmネイキッドおよびPCAuNPの影響)、16β-OHTST(E1–E3)、およびAD(F1–F3); 3つの異なるシングルドナーHLM(HDA1、HDB2、およびHDC3)で。同じ文字が続く平均は、各ナノ粒子で有意差はありませんでした(テューキーの正直な有意差=5%)。 裸 PCなし、 PC ヒト血漿タンパク質コロナ、 HLM ヒト肝ミクロソーム、 BPEI 分岐ポリエチレンイミン、 LA リポ酸、 PEG ポリエチレングリコール、2β - OH TST 2β-ヒドロキシテストステロン、6β - OH TST 6β-ヒドロキシテストステロン、15β - OH TST 15β-ヒドロキシテストステロン、16α - OH TST 16α-ヒドロキシテストステロン、16β - OH TST 16β-ヒドロキシテストステロン、 AD アンドロステンジオン
前者のPCPEG-AuNPと後者の裸のLC-AuNPを除いて、すべての40nmの裸およびPCAuNPは、HDA1およびHDC3の2β-OHTSTと6β-OHTSTの両方の生成を減少させましたが、HDB2では、PCAuNPのみが阻害を増強しました表面コーティングに関係なく、それらの製品の一部です(図8(A1–B3))。 40 nmの裸のLA-AuNPは、HDA1での15β-OHTST生成の阻害剤でした。 HDB2 PCPEG-AuNPの場合。また、HDC3ネイキッドBPEI-およびPEG-AuNPとPCLA-およびPCPEG-AuNPの場合(図8(C1–C3))。 40 nmの裸のAuNPはすべて、HDA1での16α-OHTST産生の活性化因子でしたが、阻害を増強したPC BPEI-AuNPを除いて、PCはそれを弱めました(図8(D1))。すべての40nmの裸およびPCAuNPは、個人内の16β-OH生成に影響を与えませんでした(図8(E1–E3))。 ADの生成は、HDC3で活性化因子として機能するPC PEG-AuNPを除いて、さまざまな程度の阻害を伴う40nmの裸およびPCAuNPによって調節されました(図8(F1–F3))。
2β-OHTST産生に対する80nmの裸およびPCAuNPを介した阻害は、HDB2およびHDC3でそれぞれ活性化因子として機能した80nmの裸およびPCPEG-AuNPを除いて、個体内で観察されました(図9(A1–A3) )。これらの結果は、表面コーティングに関係なく、2β-OHTSTに対するすべての裸およびPC 40 nm AuNPを介した阻害と一致していませんでした(図8(A1–A3))。 6β-OHTSTの場合、80 nmの裸のAuNPはLA-AuNPを除いて活性化因子でしたが、PCはHDB2での阻害を増強しました(図9(B2))。これは40nmの裸およびPCのAuNPを介した阻害と同様でした。 /またはそれぞれアクティベーション(図8(B2))。 15β-OHTSTの場合、80 nmの裸のBPEI-およびPEG-AuNPとPCPEG-AuNPが、それぞれHDB2とHDC3の活性化因子でした(図9(C2とC3))。 80 nmの裸のAuNPは、表面コーティングに関係なく、HDA1で16α-OHTSTの生成を増加させましたが、阻害剤であるPC LA-AuNPを除いて、PCはそれを減衰させました(図9(D1))。これは、HDA1での16α-OHTST生成の40nmネイキッドおよびPCAuNPを介したアクティブ化と減衰に似ています(図8(D1))。表面コーティングに関係なく、すべての80 nmの裸およびPCは、すべての個体内で16β-OHTSTの生成を阻害しませんでした(図9(E1〜E3))。これらの結果は、40 nmの裸で、PCを介した個体内での生成と一致していました(図8(E1–E3))。 AD生成では、80 nmの裸のBPEI-およびPEG-AuNPが阻害剤でしたが、HDA1の裸およびPC LA-AuNPではPCが弱毒化し、その逆も同様でした(図9(F1))。 80nmのネイキッドおよびPCAuNPは、アクティベーターであるPC PEG-AuNPを除いて、HDC3での生成を減少させました(図9(F3))。この研究は、HLMにおけるCYP酵素とのAuNP相互作用が、個人内のヒドロキシル化および脱アルキル化代謝物へのTST変換の減少および/または増加を引き起こし、PCの存在が阻害または保護の役割を果たしたことを強く示唆しています。インビボ研究は、非競合的CYP3A4阻害剤であるケトコナゾールを経口投与された雄CD-1マウスが、血清TSTレベル、性腺TST分泌、および6β-OHTST、15α-OHTSTを含む肝臓TSTヒドロキシル化活性の低下を示したことを報告した。 15β-OHTST、および16β-OHTST[34]。ヒト肝細胞、C3A細胞株、HepG2細胞株、HLM、および組換えCYP酵素を用いたin vitro研究では、AuNPがCYP1A2、2C9、2C19、2D6、2E1、および3A4を含むさまざまなCYP酵素の活性を調節することが示唆されました[6、7 20、21]。 PCおよびヒト血清アルブミンコロナは、ヒト肝細胞およびC3A細胞株におけるCYP1A2、2C9、および3A4酵素活性に対するBPEI-およびLA-AuNPの阻害効果を軽減しました[6、7]。とはいえ、CYP酵素に対するAuNPの干渉が、内分泌かく乱物質および/または同じCYP酵素を共有する薬物間相互作用に関連する循環TSTレベルの変化をもたらす可能性のある、予期しない毒物学的影響に対する個人の感受性を関連付けることを提案することは合理的かもしれません。 35]。
結論
これらの研究は、PCとのAuNPの相互作用が、平均的なアメリカ人の人口をよりよく表す大規模なドナープールに由来するHLMにおけるTSTのCYP依存性代謝を確実に調節することを示しています。 40 nmの裸(PCなし)のAuNPと、程度は低いが80 nmの裸のAuNPは、TSTのヒドロキシル化を抑制しましたが、高濃度でTSTの脱アルキル化を活性化しました。カチオン性BPEI-AuNPは、プールされたHLMでの6β-OHTSTおよび15β-OHTSTの生成を差し控えましたが、より生物学的に関連性のあるPCの存在により、サイズおよび表面電荷の変化の関数としての悪影響が軽減されました。ほとんどの場合、40nmと80nmの裸およびPCAuNPは、非阻害濃度で表面化学に依存する方法で、シングルドナーHLMのTST代謝を本質的に阻害します。さらに、PC PEG-AuNPは、サイズに関係なく、HDC3でAD産生の活性化を引き起こしました。これらの結果は、AuNPを介したTST代謝の個人差が毒性の要因であり、TSTを破壊するNPに対する脆弱なサブグループを特定するために利用できる可能性があることを示している可能性があります。
データと資料の可用性
この調査中に生成または分析されたすべてのデータは、この記事とその補足情報ファイルに含まれています。
略語
- 11β-OHTST:
-
11β-ヒドロキシテストステロン
- 15β-OHTST1:
-
5β-ヒドロキシテストステロン
- 16α-OHTST:
-
16α-ヒドロキシテストステロン
- 16β-OHTST:
-
16β-ヒドロキシテストステロン。
- 2α-OHTST:
-
2α-ヒドロキシテストステロン
- 2β-OHTST:
-
2β-ヒドロキシテストステロン
- 6α-OHTST:
-
6α-ヒドロキシテストステロン
- 6β-OHTST:
-
6β-ヒドロキシテストステロン
- AD:
-
アンドロステンジオン
- AgNP:
-
銀ナノ粒子
- ANOVA:
-
一元配置分散分析
- AuNP:
-
金ナノ粒子
- BPEI:
-
分岐ポリエチレンイミン
- CFS:
-
クロルピリホス
- CYP:
-
シトクロムP450
- DEET:
-
ジエチルトルアミド
- D H :
-
流体力学的直径
- DI:
-
脱イオン水
- DLS:
-
動的光散乱
- EC 50 :
-
最大活性化濃度の半分
- EDC / NHS:
-
1-エチル-3-(3-ジメチルアミノプロピル)カルボジイミド/ N-ヒドロキシスクシンイミド
- ESI + :
-
エレクトロスプレーポジティブ
- HLM:
-
ヒト肝ミクロソーム
- HSD:
-
テューキーの正直な有意差
- IC 50 :
-
最大阻害濃度の半分
- ISTD:
-
内部標準
- LA:
-
リポ酸
- LC-MS / MS:
-
液体クロマトグラフィー-質量分析
- LOD:
-
検出限界
- LOQ:
-
定量限界
- MRM:
-
複数の反応の監視
- NADP:
-
ニコチンアミドアデニンジヌクレオチドリン酸
- NADPH:
-
NADPの削減
- 裸:
-
PCなし
- NP:
-
ナノ粒子
- PBS:
-
リン酸緩衝生理食塩水
- PC:
-
ヒト血漿タンパク質コロナ
- PDI:
-
多分散度指数
- PEG:
-
ポリエチレングリコール
- pHLM:
-
プールされたヒト肝ミクロソーム
- QC:
-
品質管理
- SWCNT:
-
単層カーボンナノチューブ
- TEM:
-
透過型電子顕微鏡
- TFF:
-
タンジェンシャルフローろ過
- TiO 2 :
-
二酸化チタン
- TST:
-
テストステロン
- UPLC TQD:
-
トリプル四重極検出器を備えた超高速液体クロマトグラフィーシステム
ナノマテリアル
- 半導体ナノ粒子
- プラズモンナノ粒子
- 化学療法センサー用の金ナノ粒子
- 改善された診断および治療用途のための多機能金ナノ粒子:レビュー
- 局在表面プラズモン共鳴に基づく金ナノバイオセンサーは、ヒトブルセラ症を診断することができ、迅速で手頃な方法を導入します
- マウスにおける二酸化チタンナノ粒子の潜在的な肝臓、脳、および胚の毒性
- ポリ(4-スチレンスルホン酸-co-マレイン酸)による金磁性ナノ粒子の安定性の向上:タンパク質検出用に調整された光学特性
- 炭化水素中の金ナノ粒子のサイズ制御と安定化のための分散剤としての修飾ハイパーブランチポリグリセロール
- 6-メルカプトプリンとニューロン透過性ペプチドで修飾された金ナノ粒子によるSH-SY5Y細胞増殖の促進
- 金および銀ナノ粒子のグリーン合成のためのPlatycodiRadix(Platycodon grandiflorum)からのPlatycodonサポニン
- 金ナノ粒子で作られたタトゥーは医療診断に革命をもたらします



