炭化水素中の金ナノ粒子のサイズ制御と安定化のための分散剤としての修飾ハイパーブランチポリグリセロール
要約
ハイパーブランチポリグリセロール(HPG)は、「チオール-エン」クリック反応を介してドデカンチオール(DS)で修飾され、両親媒性生成物DSHPGが得られます。 DSHPGサンプルの分子構造は、NMR、FTIR、およびGPCによって特徴付けられ、熱挙動は、DSCおよびTGAによって特徴付けられます。金ナノ粒子(Au NP)は、安定剤および表面修飾試薬としてDSHPGを使用して調製されます。 HPGの分子量を変更することにより、AuNPのサイズを調整できます。 HPGの分子量が1123、3826、55,075の場合、NPの直径はAu @ DSHPG-1では4.1nm、Au @ DSHPG-2では9.7nm、Au @ DSHPG-3では15.1nmになります。 。 Au NPの形態とサイズは、TEMとDLSによって特徴付けられます。特に、さまざまな純粋な溶媒および共溶媒混合物におけるAuNPの分散能力が調査されます。 DSHPGの長いアルキル鎖により、AuNPが非極性溶媒に十分に分散することができます。炭化水素ベースのナノ流体は、一連の炭化水素に分散した疎水性AuNPから取得できます。炭化水素中のAuNPの分散安定性は、UV-Vis分光法によって監視され、Au NPの相対濃度は3600時間後も80%以上維持されることが観察されています。
背景
エネルギー密度が高く、ヒートシンクが高いため、吸熱性炭化水素燃料は航空宇宙分野で重要な役割を果たしてきました。それらは、航空機に再生冷却効果を提供するために、エンジンの可燃性冷却剤として使用できます。接触分解は、炭化水素燃料の吸熱能力を向上させるための効果的なアプローチであり[1,2,3]、通常、貴金属NPが触媒として使用されます[4、5]。ゴードンは最初に、従来の燃料に金属粉末を加えるというアイデアを提案しました[6]。 Zhangは、PtおよびPd NPがJP-10の分解を著しく促進し、PtNPが分解反応の開始温度を650から600°Cに下げる可能性があることを発見しました[7]。 Yueはデカリンと航空灯油にPdNPを適用し、これらの炭化水素燃料の変換、ガス収量、およびヒートシンクが大幅に増加しました[8、9]。私たちの以前の研究では、疑似均質系としてJP-10に分散したAu NPの触媒活性も調査され、Au NPによって触媒されるJP-10の変換は、熱からの純粋なJP-10の変換よりも高いことがわかりました。ひび割れ[10]。しかし、安定した固液懸濁液の取得は、ナノ粒子を含む燃料を調製するための主要な課題です[11]。
実用的な手法として、研究者はNPに保護層を与えるコーティング方法を考案しました[12]。ハイパーブランチポリマーは、一種の効果的なコーティング材料と見なされています。独自の構造と特性を備えた球状高分子は、金属NPの合成と安定化のための優れたプラットフォームを提供できます[13、14]。ハイパーブランチポリグリセロール(HPG)は、ハイパーブランチポリエーテル「コア」を持ち、ヒドロキシル基で終端されています。これは、金属NPをホストおよび安定化するための完璧な媒体を提供します[15、16、17]。 HPG安定化アプローチは、優れた安定性と生体適合性を備えた多種多様な無機ナノ結晶を調製するために使用できます[18]。さらに、HPGは、炭化水素燃料の分解を促進するための有望な開始剤として開発されました[19、20]。パルミトイルクロリド修飾HPG(PHPG)は、炭化水素燃料の「ラジカルパッケージ」として適用され、PHPGの存在下でのトリデカンと灯油の変換、ガス収率、およびヒートシンクに対する有意な促進効果が観察されました[21]。
硫黄はエステルやアセチルなどの酸素含有シェルと比較して軟質金属イオンの普遍的な配位部位であるため、チオエーテル構造を持つHPGは金属NPに長期安定性を提供する可能性があります[22、23、24]。チオール-エンクリックケミストリーは、チオエーテル構造を導入するための効果的な方法です。チオエーテル構造には、穏やかな条件下で効率の高い、選択性の高い単純な直交反応が含まれています[25]。フリーラジカル連鎖メカニズムによって重合されたチオール-エン系は、二重結合へのチオール基の付加をもたらす可能性があります[26]。残念ながら、これまでに報告されているのは、チオエーテル置換ハイパーブランチポリマーのいくつかの例だけです[16]。
この作業では、チオエーテル構造を持つ両親媒性HPG(DSHPG)は、修飾HPGと1-ドデカンチオールのクリックケミストリーによって合成されます。長いアルキル鎖は、DSHPGに炭化水素燃料への良好な溶解性を与えます。 DSHPGは、Au NPの表面修飾試薬として使用され、十分に分散されたAu @DSHPGを取得します。 AuNPのサイズとHPGの分子量との関係を体系的に調査します。さまざまな純粋な溶媒および共溶媒混合物におけるAuNPの分散安定性も調べられます。
メソッド
資料
(±)グリシドール(96%)、メチラートカリウム(95%)、1,1,1-トリス(ヒドロキシメチル)プロパン(TMP、98%)、4-( N 、 N ' -ジメチルアミノ)ピリジン(99%)、1,4-ジオキサン(99%)、グリシジルメタクリレート(97%)、ベンゾフェノン(99%)、クロロ金酸(48〜50%、Au塩基性)、テトラオクチルアンモニウムブロミド(98% )、および水素化ホウ素ナトリウム(98%)は、Aladdin Chemical Reagent Corporation(上海、中国)から購入しました。トルエン(99.5%)、メタノール(99.5%)、クロロホルム99%)、ジエチルエーテル(99.7%)、ジクロロメタン(99.5%)、ジメチルスルホキシド(99%)、トルエン(99.5%)、ヘキサン(97%)、シクロヘキサン(97%)、デカヒドロナフタレン(98%)、1-ドデカン(98%)、およびオクタン(98%)は、Sinopharm Chemical Reagent Corporation(Jiangsu、China)から購入しました。 1-テトラデカンは上海新蘭化学技術公社から購入しました。 HPG、HPG-MA、DSHPG、およびAu @ DSHPGのサンプルは、スキーム1に示されている手順に従ってこのラボで準備されました。
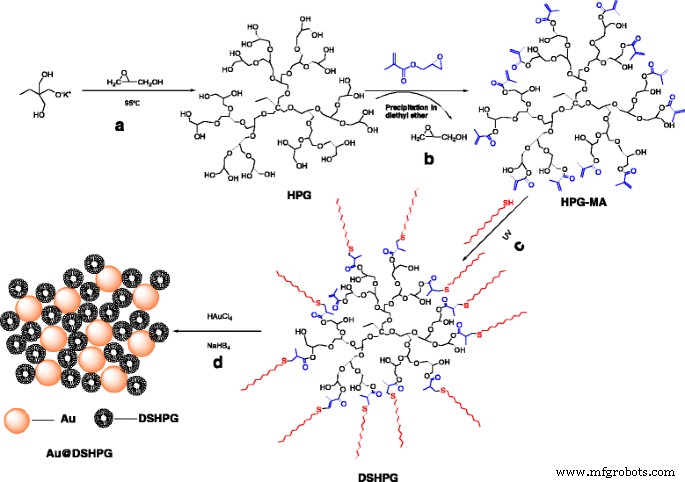
HPG、HPG-MA、DSHPG、およびAu @DSHPGの準備
HPGの準備
HPGは、以前に[27]で説明されている開環アニオン重合法によって調製されました。 1,1,1-トリス(ヒドロキシメチル)プロパン(TMP、0.278 g、1.5 mmol)は、0.1 mLのメチラートカリウム溶液(1.25 mmolのCH 3 )で部分的に脱プロトン化されました。 メタノール中でOK)、続いて溶融物から過剰のメタノールを蒸留します。次に、シリンジポンプを使用して、グリセロール(50 mL、真空蒸留で精製)を95°Cで12時間かけて滴下しました。生成物を陽イオン交換樹脂で濾過することにより中和し、アセトン中で2回沈殿させた。最後に、HPGを85°Cの真空中で24時間乾燥させました。 HPGの分子量は、モノマー/開始剤の比率と、溶融物への1,4-ジオキサンの添加によって制御されました(スキーム1a)。
メタクリレート化HPG-MAの調製
HPG-MAの合成は、Marion [28]によって記述された手順に基づいて実行されました。 HPG(1 g)および4-( N 、 N ' -ジメチルアミノ)ピリジン(2 g)を、窒素雰囲気下、室温でジメチルスルホキシド(9 mL)に溶解しました。次に、メタクリル酸グリシジル(10 mL)を滴下しました。室温で24時間撹拌した後、HPG-MAをジエチルエーテルで沈殿させ、続いて一晩乾燥させました(スキーム1b)。
クリックケミストリーによるDSHPGの準備
乾燥したHPG-MA(4 mL)とクロロホルム(4 mL)を管状光反応器に加えました。 HPG-MAの溶解後、1-ドデカンチオール(2 mL)と適切な量のベンゾフェノンを添加しました。紫外線下で1時間撹拌した後、ポリマーをクロロホルム透析で精製し、室温で乾燥させました(スキーム1c)。
Au @DSHPGの準備
Au NPは、以下の手順で作製した。 HAuCl 4 水溶液(20 mL、0.59 mmol)をトルエン(120 mL)中のテトラオクチルアンモニウムブロミド(0.42 g)と混合しました。混合物を激しく撹拌し、有機層を収集した。次に、DSHPG(0.2 g)を追加しました。その後、新鮮なNaBH 4 の溶液 水(20 mL)中の(0.15 g、3.97 mmol)を滴下し、混合物を0.5時間撹拌し続けた。混合物を2日間静置して、両親媒性ポリマーに金が完全に移動するようにしました。沈殿物を廃棄し、透明な溶液を回転蒸発にかけてトルエンを除去した。最後に、茶色がかった固体を室温で真空乾燥しました(スキーム1d)。
HPG、HPG-MA、DSHPG、およびAu @DSHPGの特性評価
HPG、HPG-MA、およびDSHPGの核磁気共鳴(NMR)スペクトルは、 d のBrukerAdvance400分光計で取得されました。 4 -メタノール、 d 6 -ジメチルスルホキシド、および d -それぞれクロロホルム。スペクトルは、重水素化溶媒の残留シグナルを基準にしています。フーリエ変換赤外(FTIR)スペクトルは、Thermo Fisher ScientificCorp。のNicoletiS10分光計(フィルムまたはKBrディスク)で記録されました。
数平均分子量(\(\ overline {M_n} \))とHPGサンプルの分布は、1.0 mLの流量で蒸留水を溶離液として使用するゲル浸透クロマトグラフィー(GPC)(Waters、USA)で測定しました。 min − 1 。システムは、狭いサイズ分布の線形ポリ(メチルメタクリレート)標準を使用してキャリブレーションされました。各HPG水溶液は、1.0 mg mL − 1 の濃度で調製されました。 。
HPG、HPG-MA、DSHPG、およびAu @ DSHPG-2の示差走査熱量測定(DSC)測定は、Q2000示差走査熱量計(TA Instruments、米国)で実行されました。温度範囲は、スキャン速度3.0°Cmin − 1 <で、− 70〜100°C(HPG)または− 70〜150°C(HPG-MA、DSHPG、Au @ DSHPG-2)に設定しました。 / sup> 。 HPGおよびAu @ DSHPG-2の熱重量分析(TGA)は、Q50熱重量分析装置(TA Instruments、米国)で実行されました。温度範囲は、窒素雰囲気下、加熱速度10°C分 − 1 で、室温から600°Cに設定しました。 。
Au @ DSHPGの形態は、透過型電子顕微鏡(TEM、CM-200、PHILIPS)を使用して観察されました。平均サイズは、動的光散乱法(DLS、ZEN 3600、Malvern Instruments)によって監視されました。 Auナノ流体の安定性は、1.0 cmの石英セルを備えたUV-Vis分光計(島津製作所、日本、UV-1750)によって検出された吸光度によって評価されました。
結果と考察
HPG、HPG-MA、およびDSHPGの分子構造
1 Hと 13 HPG、HPG-MA、およびDSHPGのCNMRスペクトルを図1に示します。 1 の3.3〜3.9ppmのピーク HPGのHNMRスペクトル(図1a)は、メチル、メチレン、およびメチンの水素の信号です。 13 HPGのCNMR(図1b)は、文献[29]のCNMRと一致しています。 1 で HPG-MAのHNMRスペクトル(図1c)、メタクリロイル基の水素の信号は1.8 ppmで表示され、C =C結合に接続された水素は5.6および6.0ppmで表示されます。クリック反応後、C =C結合に結合している水素の信号は大幅に減少し、ドデシル基の信号は0.8〜2.0 ppmで表示されます(図1d)。
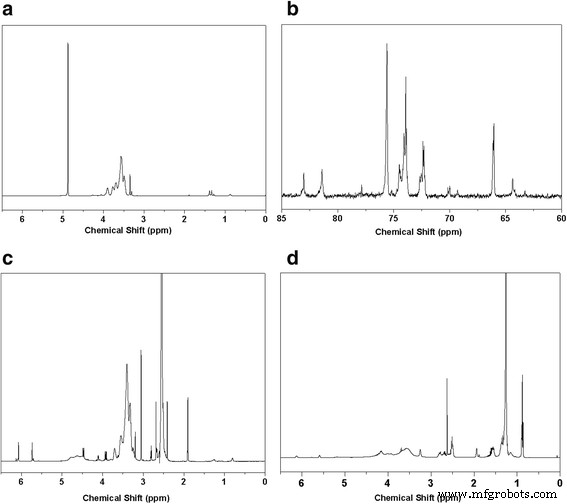
HPG、HPG-MA、およびDSHPGのNMR特性評価 a 1 HPGのHNMRスペクトル、 b 13 HPGのCNMRスペクトル、 c 1 HPG-MAのHNMRスペクトル、 d 1 DSHPGのHNMRスペクトル
図2に示すフーリエ変換赤外(FTIR)スペクトルでは、C =C伸縮振動ピークの強い吸収帯が1562cm − 1 に明らかに現れています。 HPGのエステル化後、3003 cm − 1 で=C-HとC =Oのバンドが観察されます。 および1652cm − 1 、 それぞれ。二重結合基のシグナルは、クリック反応生成物DSHPGのFTIRスペクトルで大幅に減少します。構造的特徴は、HPGのエステル化とS-アルキル化が成功し、HPG-MAとDSHPGの生成物が得られることを示しています。
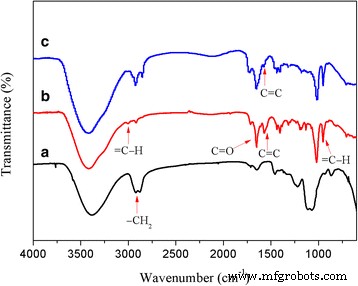
a のFTIRスペクトル HPG、 b HPG-MA、および c DSHPG
HPG、HPG-MA、DSHPG、およびAu @DSHPGの熱的挙動
HPG、HPG-MA、DSHPG、およびAu @ DSHPG-2のDSC結果を図3に示します。ガラス転移点の温度( T g )のHPGは、-37.5°Cで観察できます(図3a)。これは、主鎖の単結合の動きによって達成される「凍結」または「解凍」プロセスのポリマー鎖セグメントの動きに対応します。 HPG-MAの架橋点は110°Cであり、 T の値は g は− 20.8°Cです(図3b)。これは、ポリマー鎖の柔軟性に影響を与える可能性のある要因が T に影響を与えることを示しています。 g 。 HPG-MAでのC =C結合の架橋は、鎖セグメントの動きを制限し、 T g 値はHPGの値よりはるかに高いです。 DSHPGの長いアルキル鎖はよく整列しているため、DSHPGは結晶化しやすいです。 DSHPGでは、− 4.7°Cでの融解ピークと− 12.34°Cでの低温結晶化ピークが観察されます(図3c)。ただし、これらのピークはAu @ DSHPGでは観察されなくなりました(図3d)。これは、Au @DSHPGにAuNPを導入すると、おそらくポリマー鎖が崩壊し、分子鎖の整然とした配置が破壊されることを意味します。
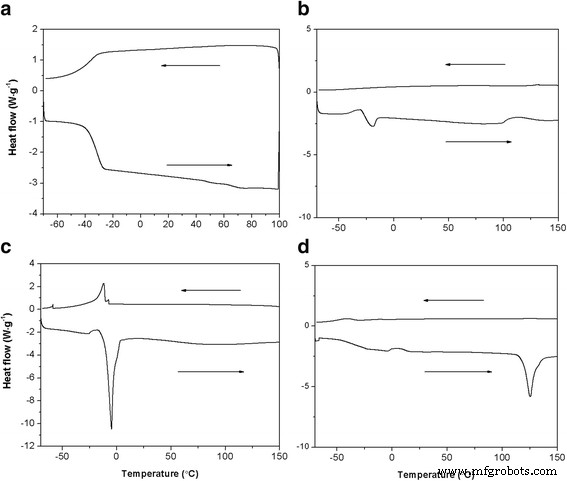
a のDSC曲線 HPG、 b HPG-MA、 c DSHPG、および d スキャン速度3°CminのAu @ DSHPG-2 − 1
HPGおよびAu @ DSHPGの熱安定性は、TGAによって検出され、結果は図4に示されています。これは、HPGコアの亀裂が425°C付近で発生していることを示しています(図4a)。したがって、Au @ DSHPGの亀裂(図4b)の場合、400°Cでの重量損失のピークはHPGの亀裂に起因し、他の重量損失のピークはDSHPGのポリマーシェルの亀裂に起因するはずです。 Au @ DSHPG-2サンプルのAu含有量は27.2wt%です。
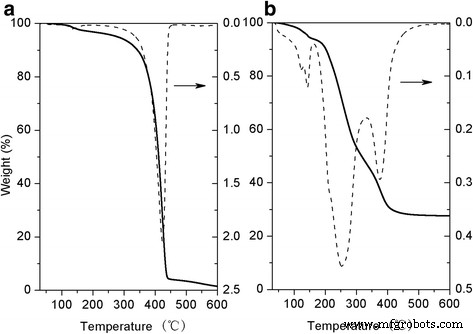
a のTGAおよびDTG曲線 HPGと b Au @ DSHPG-2、加熱速度10°C分 − 1
Au @DSHPGのサイズ制御
一連のHPGサンプルは、\(\ overline {M_n} \)の値を1123から57,000まで変化させて取得されます(表1)。より大きなモノマー(グリセロール)/開始剤(TMP)比は、ポリマーのより高分子量を生成できると推測されます。さらに、得られたポリマーの分子量は、乳化剤の作用を受け、アニオン重合を保護するための陽イオン交換に役立つ微小環境を作り出すことができる1,4-ジオキサンの存在下ではるかに高いレベルに増加します[ 30]。
<図>動的光散乱(DLS)の結果は、水中のHPGのサイズがHPG分子量の増加とともに増加することを示しています。次に、コアHPG分子のさまざまなサイズまたは分子量に基づいて、Au NPのサイズ制御がドデカンチオール修飾HPG(DSHPG)によって実行されます。 Au @DSHPGのTEM画像を図5に示します。
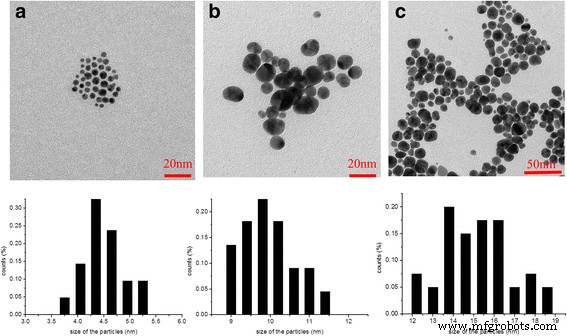
Au @DSHPGのTEM画像とサイズ分布。 a Au @ DSHPG-1(HPG \(\ overline {M_n} \)=1123)、 b Au @ DSHPG-2(HPG \(\ overline {M_n} \)=3826)、および c Au @ DSHPG-3(HPG \(\ overline {M_n} \)=55,075)
Au @ DSHPG-1、Au @ DSHPG-2、およびAu @ DSHPG-3の4.1、9.7、および15.1 nmのサイズは、1123、3826、および1123、3826、およびの\(\ overline {M_n} \)値に対応して観察されます。 HPGの場合はそれぞれ55,075。明らかに、AuNPのサイズはHPGコアのサイズに強く影響されます。 HPGの分子量とAuNPのサイズの間には正の関係があります。高分子量のHPGは、より大きなポリエーテル「コア」を持ち、より大きなサイズのNPを形成する可能性があります。 HPGとNPの観察されたサイズから、1つだけではなくHPGのいくつかの高分子が1つのナノ粒子の安定化に影響を与えると推測できます。 HPG分子が小さいほど、さまざまなナノ粒子の接触や融合に対する保護(または分離)効果が高くなります。
さまざまな溶媒でのAu @ DSHPGの分散能力
UV-Vis分光光度法を使用して、さまざまな純粋な溶媒および共溶媒混合物におけるAu @DSHPGの分散能力を調査します。 Au @ DSHPG-2は、トルエン、ジエチルエーテル、酢酸エチル、アセトニトリル、水など、極性の異なるいくつかの純粋な溶媒に分散しています。 Au @ DSHPG-2の飽和溶液のUV-Visスペクトルを図6に示します。トルエンおよびジエチルエーテル中のAuNPの飽和溶液の吸収値は高すぎて検出できないため、システムはUV-Vis測定用の溶媒。非極性溶媒中でDSHPGで安定化されたAuNPの分散能力は、DSHPGの非極性アルキル鎖により、極性溶媒での分散能力よりも大幅に優れていることが示されています。
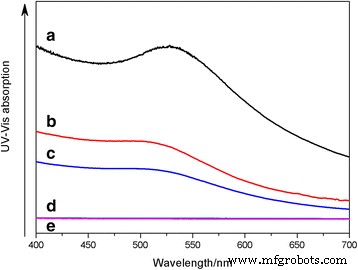
Au @ DSHPG-2の飽和溶液のUV-Vis吸収曲線。 a メチルベンゼン(100倍希釈)、 b ジエチルエーテル(6倍希釈)、 c 酢酸エチル、 d アセトニトリル、および e 水
Au @ DSHPGの分散能力と溶媒極性の関係をさらに明らかにするために、トルエンとアセトニトリルの混合物中の一連のAu @ DSHPG-2含有溶液を調製します。極性は、2つの成分の比率によって調整されます。これらの溶液のUV-Vis吸収曲線を図7に示します。トルエンの割合を増やすと、AuNPの分散能力が徐々に向上します。トルエンとアセトニトリルのさまざまな混合物における飽和溶液の521nmでの吸収値を図8に示します。結果は、溶媒の極性が弱いほど、Au @DSHPGの分散がより実現可能であることを示しています。
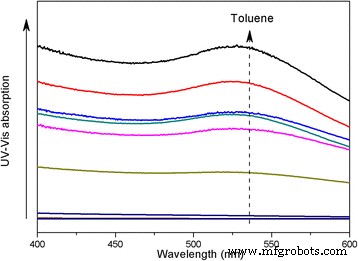
トルエンとアセトニトリルのさまざまな混合物中のAu @ DSHPG-2の飽和溶液のUV-Vis吸収曲線。破線の矢印は、0.1間隔でトルエンの体積分率が0から1に増加することを示しています
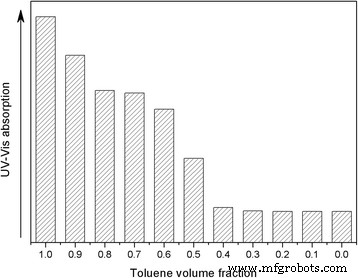
トルエンとアセトニトリルのさまざまな混合物中のAu @ DSHPG-2の飽和溶液の521nmでのUV-Vis吸収
溶解プロセスは、溶解係数から理論的に評価することができます。ポリマーDSHPGの場合、溶解係数は次の式[31]で計算できます。
$$ \ delta =\ frac {\ sum F} {\ overline {V}} =\ frac {\ rho \ sum G} {\ overline {M}} $$(1)ここで、ρ はDSHPGの密度、\(\ overline {M} \)はDSHPGの反復単位のモル質量、 G はモル重力定数です。
δ間のわずかな違い 1 およびδ 2 2つの液体の混和性が向上します。 δの詳細データ 1 (溶媒)[32]およびδ 2 (DSHPG)25°Cおよび101.3 kPaで表2に示します。トルエンの溶解係数がDSHPGの溶解係数に最も近く、次に酢酸エチル、ジエチルエーテル、アセトニトリル、および水が続くことに注意してください。これは、溶媒の極性を上げると、室温で溶解プロセスがより困難になることを意味します。理論計算の結果は、UV-Vis分析の結果と一致しています。これは、DSHPGがAu NPに親油性と疎水性を与えることに成功し、炭化水素へのAu @DSHPGの適用を可能にすることを証明しています。
<図>炭化水素中のAu @ DSHPGの安定性
一般に、ブーゲ-ランベルト-ベールの法則[33]によれば、上澄み濃度と浮遊粒子の吸光度の間には線形の関係があります。ナノ流体の相対的な安定性を明らかにするために、Au @ DSHPG-2をヘキサン、シクロヘキサン、オクタン、デカリン、ドデカン、およびテトラデカンに分散させ、堆積時間に対するUV-Vis吸収を調べます。これらの炭化水素燃料におけるAuNPの吸収と沈降時間の変化を図9に示します。DSHPGの変更により、Au NPは親水性のハイパーブランチポリマーDSHPGのネットワークに囲まれ、AuNPの吸収が弱まりました。 Au @ DSHPGを炭化水素と混合すると、炭化水素分子がポリマーにゆっくりと浸透し、ポリマーが溶解するまで膨潤し、Au NPがかさばる分子から徐々に放出され、吸収が増加します。このプロセスは、Au NPが完全に露出するまでに数百時間かかる、周囲条件下ではかなり時間がかかります。図9に示すように、さまざまな溶媒中のNPの相対濃度は、0〜750時間の間に増加します。堆積時間が750時間から3600時間にさらに増加すると、ヘキサン、オクタン、およびデカリン中のAuNPの相対濃度はほぼ一定に保たれます。ただし、それらはドデカンとテトラデカンでわずかに低下します。システムが3600時間維持された後も、Au NPの相対濃度は80%を超えて維持されます。したがって、DSHPGによる変更により、AuNPが炭化水素ベースの燃料で長期貯蔵安定性を持つことが可能になると提案できます。
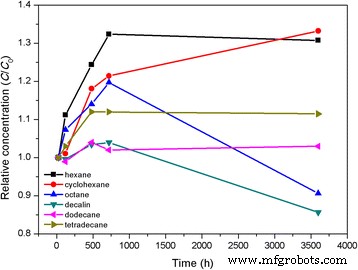
さまざまな炭化水素中のAu @ DSHPG-2の相対的な上澄み粒子濃度
結論
数平均分子量の異なる一連のハイパーブランチポリグリセロール(HPG)が用意されています。それらは、ドデカンチオール修飾HPG(DSHPG)およびDSHPG修飾Au NP(Au @ DSHPG)の調製にうまく使用されています。 Au @ DSHPGのサイズは、HPGの分子量を調整することで制御でき、HPGの分子量が大きいほど、AuNPのサイズが大きくなります。 UV-Vis観察結果は、非極性溶媒(トルエンやジエチルエーテルなど)でのAu @ DSHPGの分散能力が、極性溶媒(水やアセトニトリルなど)での分散能力よりも大幅に優れていることを示しています。これは、DSHPGの強力な効果を証明しています。溶媒中のAuNPの分散。堆積物の測定結果は、Au @DSHPGが炭化水素に著しく沈着することなく3600時間以上安定化できることを示しています。このような種類の炭化水素ベースのナノ流体は、Au NPの触媒効果により、熱分解プロセス中に高いヒートシンク値に達する可能性があります。
略語
- Au @ DSHPG-1:
-
直径4.1nmのDSHPGによって安定化された金ナノ粒子
- Au @ DSHPG-2:
-
直径9.7nmのDSHPGによって安定化された金ナノ粒子
- Au @ DSHPG-3:
-
直径15.1nmのDSHPGによって安定化された金ナノ粒子
- DS:
-
ドデカンチオール
- DSHPG:
-
ドデカンチオール(DS)で修飾されたハイパーブランチポリグリセロール(HPG)
- HPG:
-
ハイパーブランチポリグリセロール
ナノマテリアル
- 遮断と制御が難しいバルブ
- プラズモンナノ粒子
- 化学療法センサー用の金ナノ粒子
- 改善された診断および治療用途のための多機能金ナノ粒子:レビュー
- 癌治療のためのナノ粒子:現在の進歩と課題
- 生体適合性FePO4ナノ粒子:ドラッグデリバリー、RNA安定化、および機能的活性
- 非常に効果的な標的膵臓腫瘍治療のための、血液循環が延長され、生体適合性が改善されたレスベラトロール負荷アルブミンナノ粒子
- In VivoCTイメージングおよび腎クリアランス特性のための新しい生体適合性AuNanostars @PEGナノ粒子
- 光熱治療および光音響イメージングのためのポリピロール被覆鉄-白金ナノ粒子の合成およびinvitro性能
- 6-メルカプトプリンとニューロン透過性ペプチドで修飾された金ナノ粒子によるSH-SY5Y細胞増殖の促進
- 金および銀ナノ粒子のグリーン合成のためのPlatycodiRadix(Platycodon grandiflorum)からのPlatycodonサポニン



