改善された診断および治療用途のための多機能金ナノ粒子:レビュー
要約
金属の医学的特性は、感染症や病気の治療のための伝統医学で何世紀にもわたって探求されてきましたが、今でも実践されています。プラチナベースの薬剤は、40年以上前に米国食品医薬品局(FDA)によってシスプラチンが承認された後、抗がん剤として臨床的に使用される最初のクラスの金属ベースの薬剤です。それ以来、健康に役立つより多くの金属が臨床試験に承認されています。興味深いことに、これらの金属が金属ナノ粒子に還元されると、バルクの対応物よりも優れたユニークで斬新な特性を示しました。金ナノ粒子(AuNP)は、FDAが承認した金属ナノ粒子のひとつであり、医学におけるさまざまな役割において大きな期待を示しています。それらは、ドラッグデリバリー、光熱(PT)、造影剤、治療、放射線増感剤、および遺伝子トランスフェクション剤として使用されました。それらの生物医学的応用は、病気の診断と治療におけるそれらの潜在的な使用をカバーして、ここでレビューされます。臨床試験で承認されているAuNPベースのシステムのいくつか、AuNPの潜在的な健康上の脅威、および生体適合性を改善するために使用できるいくつかの戦略についても説明します。レビューされた研究は、AuNPベースのシステムを単独で、または従来のシステムと組み合わせて使用して、その有効性を改善できる可能性があるという原理の証明を提供します。
はじめに
医学は、ナノテクノロジーの恩恵を受けてきた多くの分野の1つです。ナノテクノロジーは、ナノ材料の使用を通じて新しい診断薬および治療薬を改善および開発する多くの機会とともに出現しました[1、2]。特にAuNPは、独特の物理化学的特性と優れた化学的安定性を示します。それらは、さまざまな化学作用を通じて、またはチオール化分子に対する強い親和性に基づいて、ほぼすべてのタイプの電子供与分子で簡単に機能化できます[3、4]。サイズが小さいため、AuNPは表面積が大きく、薬物負荷容量が高くなっています。生物医学的応用のために、複数の部分をAuNPに組み込むことができます。これらには、特異性を高めるための標的分子、バイオイメージングのための造影剤、および薬物に対する疾患反応をリアルタイムで監視するための造影剤、および疾患治療のための治療薬が含まれます[5、6]。興味深いことに、生体分子を追加しなくても、AuNPは疾患の標的化、イメージング、および治療を行うことができます。サイズに依存する特性に基づいて、さまざまな生物医学アプリケーションで使用するための新しいAuNPベースのシステムを作成できます[7]。
AuNPは、熱安定性であるため非常に安定で非生分解性の金属前駆体から作られています。バルクゴールドは医学で使用されており、生体不活性で無毒であることが証明されています[8、9]。したがって、AuNPのゴールドコアは基本的に同様の特性を示します[3、10]。 AuNPとその応用は、50年以上にわたって広く研究されており、前臨床[5、11、12、13]および臨床研究[14、15、16、17、18]のセラノスティック剤として大きな期待が寄せられています。このレビューで説明したように、新しいAuNPベースのシステムにはさらに多くの機会があります。 AuNPは、後期がんの治療のための薬物担体[16、17]として、また前立腺がん[19]およびにきび[18]の治療におけるPT剤として、すでに臨床試験で検討されています。 AuNPの使用を取り巻く健康と規制の問題を損なうことなく[20]、生物医学におけるこれらのシステムの将来は間近に迫っています。局所的かつ改善された有効性で薬剤耐性と戦うことができる多機能AuNPベースのシステムが可能です[11、21、22]。このレビューでは、診断薬と治療薬の両方としてのバイオアプリケーションを反映することにより、前臨床および臨床研究におけるAuNPの生物学的特性を強調しています。それらの限界を克服するために使用されたそれらの潜在的な健康上の脅威と戦略も説明されています。最後に、医学におけるAuNPの将来の展望が強調されています。
金ナノ粒子
医療用途でのAuNPの人気は、その独特の化学的および物理的特性のために大きな勢いを得ています。 AuNPは、サイズが1〜100nmの範囲の固体コロイド粒子です[23]。生物学におけるAuNPの用途は、そのサイズ、表面プラズモン共鳴(SPR)、形状、および表面化学に限定されない、それらの物理化学的特性に根ざしています[3、10]。これらのパラメータはそれらの活動に影響を及ぼし、送達、感作、造影剤、または治療薬のいずれかとして、疾患の診断および治療に使用するための完璧な候補になります。それらの小さいサイズは、より大きな表面積に関連しており、これにより、標的化、画像化、および治療薬などの複数のペイロードの表面修飾および付着が可能になる[4、24、25、26]。サイズが小さいため、NPとその貨物は、他の方法では到達して侵入するのが難しい生物学的障壁を通過することもできます[11]。
AuNPは、従来の治療法に関連するオフターゲット効果に対処する可能性のある、実行可能な診断、治療、およびセラノスティック(疾患の診断と治療に同時に使用できる薬剤)としてますます認識されています。ただし、AuNPは、生体適合性のあるバルク対応物とは異なる特性と機能を備えており、人の健康に害を及ぼす可能性があります[27、28、29]。病気の治療のためのバルク金化合物の臨床使用は古代の慣習であり、安全であると認定されています[8]。近年、研究により、AuNPは同様または改善された医学的特性を持っていることが示されています[29]。独自の光学的、化学的、物理的特性により、AuNPはバルク金と比較して新しい特性を示すことが多く[30、31]、診断および治療薬として機能します[5]。
AuNPの合成
AuNPは、トップダウンまたはボトムアップのアプローチに従って、いくつかの方法で作成できます。トップダウンアプローチでは、物理的および化学的方法を使用してバルク材料から目的のサイズを生成しますが、ボトムアップアプローチでは、化学的方法を使用して、ナノサイズのシステムを形成するためのビルディングブロックを組み立てます[32、33]。物理的手法(フライス盤、光化学、放射線、リソグラフィーなど)は、大量のエネルギーと圧力を使用して、バルク材料を10 –9 にスケールダウンします。 サイズが10億分の1メートル[10、32、34]。物理的方法を使用する場合、核形成プロセスは容易に制御され、還元剤は必要ありません。これらの方法のいくつかでは、合成はNPの滅菌と同時に行われます。ただし、物理的な技術はコストがかかり、すぐに利用できず、特殊な機器が必要になることがよくあります。さらに、キャッピング剤と安定剤は、これらのプロセスに含まれる高エネルギープロセスに耐えられない可能性があります[34]。
ボトムアップアプローチは、迅速で、簡単で、高度な機器を使用する必要がないため、AuNPの合成に最も適しています[33、34、35]。これは、1951年にTurkevichによって開発された化学的方法(図1A)に基づいており、金前駆体の還元と安定化にクエン酸塩を使用して、15 nmの球状AuNPを生成します[3、10、23、33、36 、37]。クエン酸塩と金の前駆体含有量の比率を変えることでこの方法をさらに変更し、15〜150 nmのAuNPのサイズ直径範囲を実現しました(図1B)[10、24]。水素化ホウ素ナトリウム、臭化セチルトリメチルアンモニウム(CTAB)、アスコルビン酸などの多くの還元剤も導入されました。化学還元剤の中には、残念ながら毒性があり[33、34、36]、通常、ポリエチレングリコール(PEG)、アラビアゴム、多糖類、生理活性ペプチドなどの安定剤を表面に添加することで不動態化されます[37、38]。
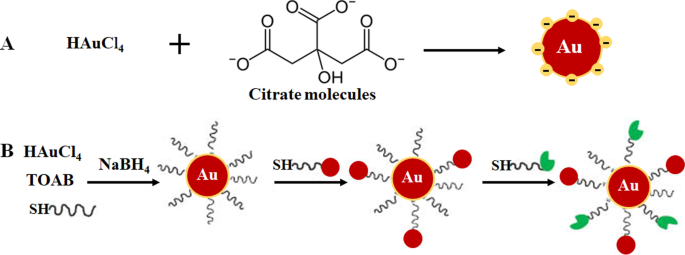
クエン酸塩還元による単相系によるAuNP製剤( A )および二相系還元とそれに続く配位子交換反応による安定化と官能化、Brust-Schiffrin法( B )。許可を得て複製[36]。 Copyright 2013、DeGruyter。 TOAB 臭化テトラブチルアンモニウム、 SH チオール化分子
マイクロ波誘導液体中プラズマプロセス(MWPLP)やグリーンナノテクノロジーなどのより環境に優しいアプローチが、有毒な化学還元剤の使用を回避するために、AuNPの合成で検討されてきました。 MWPLPは、マイクロ波を使用して金属NPの核生成を生成し、還元剤を必要とせず、合成に必要なエネルギーは非常に低くなります[34]。一方、グリーンナノテクノロジーは、植物や微生物に由来する天然化合物を、生体AuNPの合成における還元剤の供給源として使用します[12、33、39、40、41]。グリーンナノテクノロジーは、環境に優しく、環境にやさしいと考えられているため、生物医学的用途により適しています。植物を介した合成は、微生物を使用するよりも経済的です。さらに、合成はたった1つのステップで実行でき、NPはより簡単に精製できます。さらに、植物は再生可能です。葉、茎、樹皮、根、花、果実などの植物のさまざまな部分は、植物を殺すことなく収穫し、合成に使用することができます。植物材料から調製された抽出物には、還元剤、安定剤、およびキャッピング剤として機能できる植物化学物質、タンパク質、および酵素が含まれています[10、12、24、34、35、40、42]。緑茶のエピガロカテキン[42]とマンゴーのマンギフェリン(MGF)[12、43]は、AuNPの合成に広く使用されている植物由来の化合物の1つです[34]。これらの方法の詳細については、次の参考文献[10、24、34、35]で詳しく説明されています。
AuNPの生物学的応用
医学におけるAuNPの役割と重要性は、間違いなくより明白になりつつあります。これは、幅広い生物医学分野での多面的な応用を実証する研究の数の増加に支えられています。 AuNPの生体適合性は、紀元前2500年から2600年にまで遡る、人間の病気の治療における金の長い歴史に起因しています。中国人とインド人は、男性の無力、てんかん、梅毒、リウマチ性疾患、結核の治療に金を使用していました。中国は赤いコロイド金の寿命効果を発見しました。これは、若返りと活性化のためのアーユルヴェーダ医学の一部としてインドで今でも実践されています。辰砂-金(マカラドワジャとしても知られています)は、インドの出産を改善するために使用されます。西欧諸国では、金は神経障害やてんかんの治療に使用されてきました。 invitroおよびinvivo研究の両方での使用について毒性は報告されていません[8、44、45]。それ以来、経口および注射可能な金化合物は関節炎の治療として使用され続け[9、46]、また抗癌効果があることが示されています[8]。同様の、場合によっては改善された効果が、疾患診断[47,48,49]および治療[3、29、50、51]の有望な薬剤として浮上しているAuNPについても報告されました。
AuNPは、目的の機能に合わせてさまざまな生体分子を結合することにより、生物医学的用途に利用できるより大きな表面積を持っています。これらには、疾患特異的バイオマーカーの認識に役立つターゲティング部分、バイオイメージング用の造影剤、および疾患治療用の治療薬が含まれます[24、25]。他のナノ材料よりもAuNPを使用する利点は、図2 [4、26]に示すように、さまざまな化学物質を使用して簡単に機能化できることです。 AuNPはチオール化分子に対して高い親和性を持ち、チオール-金結合は分子をNP表面に吸着するために最も一般的に使用される方法です[4]。ビオチン-ストレプトアビジン結合やカルボジイミドカップリングなどの親和性ベースの化学物質も使用されます。 AuNPは、医薬品の送達、診断および治療目的の3つの主要な生物医学分野で使用されており[24、35]、以下で説明するように、これらの分野で大きな可能性を示しています。
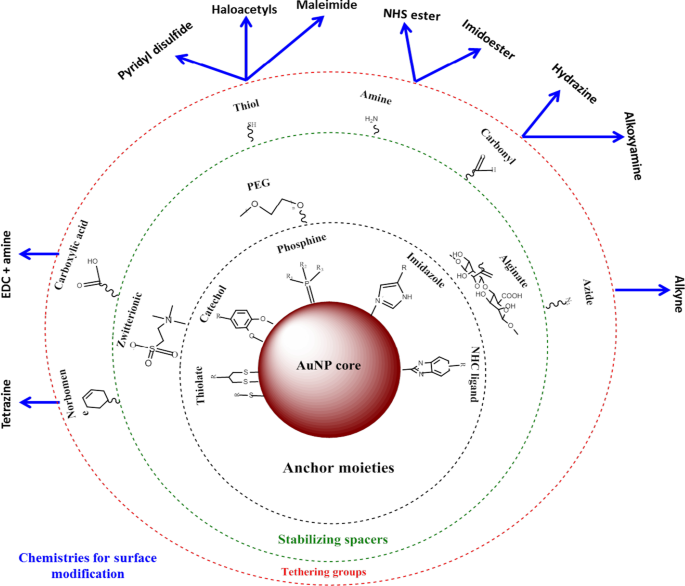
AuNPの合成と機能化。官能基を持つ生体分子は、最初に金-チオール親和性を介してNP表面に吸着されます。次に、アミン基などの他の官能基を使用して、分子をカルボキシル基と結合させて、ターゲティングまたは薬物部分を結合させることができます。 [32]
から適応ドラッグデリバリーエージェントとしてのAuNPs
AuNPの最も一般的な用途は、薬物[11、18、52]、ワクチン[53]、および遺伝子治療[24、32]の送達媒体としてです。 AuNPは、薬剤耐性、低薬物分布、生分解、早期薬物クリアランスなど、従来の治療法に関連する問題のほとんどを解決できる特性を備えています[11]。 AuNPは、薬物の投与量、治療頻度を大幅に削減し、疎水性および不溶性の薬物を輸送することができます。それらは生体不活性であると考えられており、免疫細胞による攻撃から貨物を覆い隠し、循環系を通過する際のタンパク質分解から薬物を保護し、したがって薬物循環時間を増加させることができます。これらの要因は、正常組織にほとんどまたはまったく影響を与えることなく、病変組織に薬物を集中させて保持することにより、薬物の有効性を容易に高めることができます[25]。
癌治療におけるAuNPの使用は広く研究されており[17、37、54]、長年にわたって肥満[50、55、56]やにきび[18]などの他の疾患にも拡大されています。ナノベースのシステムは、ほとんどの細胞成分よりも小さく、病変組織の血管系に対する強化された透過性と保持(EPR)効果を利用することにより、細胞バリアを受動的に通過できます[25]。病的状態のEPRは、過剰な血管新生と透過性メディエーターの分泌の増加を特徴とし、病変組織によるAuNPの取り込みを促進する可能性があります。これらの特徴は病的状態にのみ関連しており、正常組織には関連しておらず、AuNPコンジュゲートを選択的に標的化する機会を提供します[25]。 AuNPは、複数の分子を同時に運ぶことができ、その特性をさらに多様化できるため、薬物担体として魅力的です。 AuNPは特定の生物医学的機能に合わせて調整できるため、これは、AuNPバイオアプリケーションのほとんどが根付いている医学における望ましい特性です。これは、細胞小器官との相互作用の方法を制御するのに役立ち、したがって、さまざまな疾患の効果的な診断および治療法の将来の開発に有望です[4]。
AuNPベースの診断システム
ナノテクノロジーの出現により、従来の診断テストと比較して、迅速で、堅牢で、感度が高く、競争力の高い検出システムを開発する姿勢が高まっています[48]。ナノマテリアルは通常、疾患の発症に関与するガス、DNA、およびタンパク質マーカーを検出するための既存のバイオセンシングプラットフォームに統合されています[47]。診断に使用されるさまざまなナノ材料(金属、高分子、磁気、半導体のNPを含む)の中で、AuNPは、疾患バイオマーカーの存在を検出または感知するためのバイオセンサー、電気化学センサー、および発色アッセイで広く使用されています[49]。それらの局在化SPR(LSPR)、蛍光共鳴エネルギー移動(FRET)、表面増強ラマン散乱、導電率、レドックス活性、および量子化された帯電効果により、ターゲット分子のイメージングと検出に理想的なツールになります[10、24]。それらの電子的および光学的特性、ならびに可視および近赤外(NIR)光を散乱する能力は、顕微鏡技術(電子、共焦点および暗視野光散乱)[57]、コンピューター断層撮影(CT)などのさまざまな技術と互換性があり測定可能です。 、PTヘテロダインイメージング技術、UV-Visおよびラマン分光法[24、35]。
AuNPベースの診断システムの開発には、たとえば、疾患のバイオマーカーを認識する生体分子の付着によるAuNP表面の修飾が含まれます[3、24、58]。イムノクロマトグラフィー(LFA)は、おそらくナノテクノロジーベースの診断ツールの最もよく知られた例です。 LFAは通常、約30〜40 nmのAuNPを使用します。これは、小さい粒子の消光断面積が非常に小さいのに対し、大きい粒子は通常、これらのアッセイで使用するには不安定であるためです[59]。さらに、AuNPのSPR、導電率、酸化還元の変化を引き起こす可能性のある他の分子/酵素が含まれています。これらのインジケーターは、分析物がAuNPコンジュゲートに結合した後に検出可能なシグナルを提供し[24]、シグナルの欠如または存在は、標的分子または疾患の有無を反映します。 AuNPによって生成される信号は、化学的に安定しており、長持ちし、さまざまなテスト形式(試験管、ストリップ、invitroおよびinvivo)で使用した場合に一貫性があります[24]。したがって、それらのアプリケーションは、診断アッセイの速度と成功を著しく向上させました。
比色AuNPベースのアッセイ
比色分析では、AuNPは、高度な機器を使用せずに肉眼で検出できる視覚信号(通常は色の変化)を生成します。一般に、AuNPのコロイド溶液は、粒子間の距離に大きく依存するルビーレッドからブドウの色を持っています[60、61]。分子生物学的認識要素(例えば、抗体、ペプチド、アプタマー、酵素など)で修飾されたAuNPへの分析物の結合は、LSPRの明確なシフトを誘発し、その結果、ルビーレッドからブルーへの色の変化をもたらします[60 、62、63]。色の濃さは分析物の濃度に正比例し、病気の存在と状態を確認するために使用されます。 AuNPベースの比色診断は、インフルエンザAウイルス[64]、ジカウイルス[65]、T7バクテリオファージ[66]、結核菌の検出に使用されています。 [67]、そして最近、重症急性呼吸器症候群の検出のために-コロナウイルス-2(SARS-CoV-2)[60、68]。
比色分析AuNPベースのアッセイの例は、SARS-CoV-2 [60]、高感染性コロナウイルス病2019(COVID-19)[60、68]を引き起こすウイルスの検出のために実証されました。このアッセイでは、ウイルスの存在は単純な色の変化によって報告されました。診断を行うために機器は必要ありませんでした。このウイルスの現在の臨床診断テストでは、逆転写酵素リアルタイムポリメラーゼ連鎖反応(RT-PCR)アッセイを使用します。これには、4〜6時間かかりますが、迅速なポイントオブケア(PoC)システムでは、かかる可能性のある抗体を検出します。血中に現れるまで数日。比較すると、比色AuNPベースのアッセイは、図3に示すように、より堅牢で高速でした。SARS-CoV-2RNAサンプルの存在下でアンチセンスオリゴヌクレオチド(ASO)とタグ付けされたAuNPをインキュベートすると、 〜10分。 SARS-CoV-2陽性試験では、ウイルスのヌクレオカプシドリン酸化タンパク質のN遺伝子にASOが結合すると、青色が誘発され、視覚的に検出されました。このテストは非常に感度が高く、SARS-CoV-2RNAの検出限界は0.18ng /μLでした[60]。
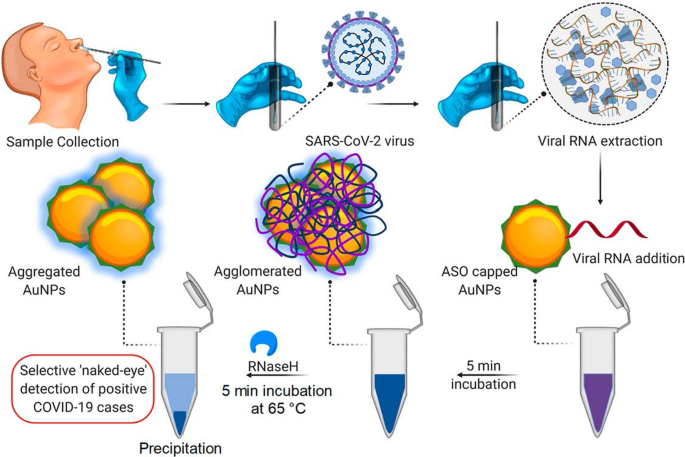
AuNPベースの比色診断システム。 ASOでキャップされたAuNPによるSARS-CoV-2RNAの選択的な肉眼検出。許可を得て複製[60]。 Copyright 2020、ACS Nano
AuNPベースのLFAは、図3に示されているものと同じ原理に従います。ただし、分析物が存在する場合、溶液の色の変化の代わりに、テストストリップ上に目に見える線が形成されます。分析物の存在下で、AuNPはテストライン上でキャプチャされ、肉眼で視覚化された明確な赤いラインを形成しました。線の強度は、吸着されたAuNPの数によって決まります[69]。 ニューモシスチスジロベシイを検出するための、シンプルで迅速なAuNPベースのLFAの例を図4に示します。 ( P. jirovecii )ヒト血清中のIgM抗体。 40 nmのAuNPは、 Pの組換え合成抗原(RSA)と結合しました。 jirovecii 、主要な表面糖タンパク質またはケキシン様セリンプロテアーゼのいずれか。これらは、 Pの有無の指標として使用された。 jirovecii 。陽性テストでは、 P。 jirovecii IgMは、コンジュゲートパッドでAuNP-RSAコンジュゲートによって捕捉されました。次に、AuNP-RSA / IgM複合体は分析膜に流れ、そこで抗ヒトIgM(テストライン)に結合し、過剰なものは抗RSA抗体(コントロールライン)に移動し、2本の赤い線が生じます。ネガティブテストは、コントロールライン[70]でのみ赤色になります。独立した研究では、AuNPベースのLFAを使用して、テストラインとコントロールラインの両方で赤い線が現れることで確認されたSARS-CoV-2IgMを選択的に検出しました[68]。 2つのシステムで15分以内に肉眼で色が視覚的に検出され、テストごとに必要な血清サンプルは10〜20μLのみでした[68、70]。
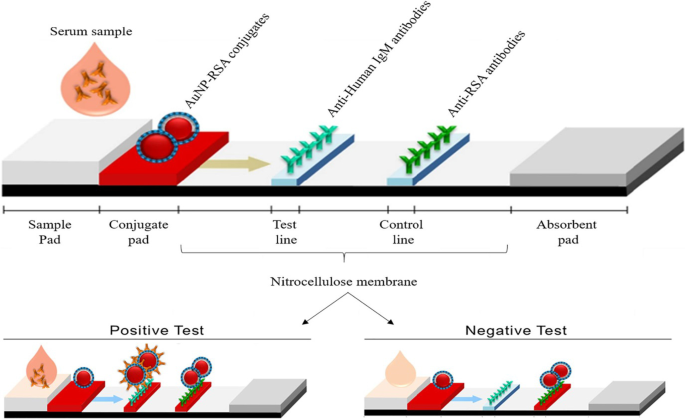
IgM Pを検出するためのAuNPベースのLFA。 jirovecii 抗体。 Pの存在(陽性テスト)または不在(陰性対照)。 jirovecii 抗体は、テストラインとコントロールラインの両方で、またはコントロールラインでのみ、AuNPの赤みがかった色で区別できます。許可を得て複製[70]。 Copyright 2019、微生物学のフロンティア
LFAのシグナルプローブとしてAuNPを使用した最初の例の1つは、Ramos細胞の検出でした。 TE02アプタマーを捕捉プローブとして使用し、TD05アプタマーを検出プローブとして使用した。アプタマー-AuNPバイオセンサーは、機器を使用せずに最低4,000個のRamos細胞を視覚的に検出し、ポータブルストリップリーダーを使用して15分以内に800個のRamos細胞を視覚的に検出できます。このサンドイッチ検出バイオセンサーを使用して、アッセイはヒトの血液にスパイクされたラモス細胞を検出することに成功し[71]、循環癌細胞の定性的および定量的検出のための迅速、高感度、低コストのシステムを開発するための概念実証として使用されました。それ以来、さまざまなAuNPベースのLFAが、ニューモシスチス肺炎によって引き起こされる疾患を含む、多数の感染症の診断のために設計されてきました。 [70]、エボラウイルス[72]、HIV、C型肝炎ウイルス、および結核菌 [73]そして最近ではSARS-CoV-2ウイルス[68]。
AuNPベースのイメージングシステム
AuNPは、最大10 5 の共鳴波長に一致する光を吸収および散乱する能力があるため、バイオイメージングでのアプリケーションについて集中的に調査されてきました。 従来のフルオロフォアの2倍[74]。 AuNPは、原子番号と電子密度が高くなります(79および19.32 g / cm 3 )従来のヨウ素ベースの薬剤(53および4.9 g / cm 3 )と比較して )、したがって、より優れた造影剤であることが証明されています[24]。 AuNPは、罹患した細胞または組織に蓄積し、強力なX線減衰を誘発して、標的部位を非常に明確にし、容易に検出できるようにします。 AuNPは、化学部分と分子生物学的認識剤に結合しており、特定の抗原を選択的に標的にして、CTイメージング用の明確で標的特異的なコントラストを誘導することができます[75]。
前立腺特異的膜抗原(PSMA)に結合するRNAアプタマーで機能化されたAuNPを使用することにより、invitroで標的化された分子CTイメージングシステムが実現されました。 AuNP-PSMAアプタマーコンジュゲートは、標的受容体を欠くPC-3前立腺細胞と比較して、PSMA発現前立腺(LNCaP)細胞に対して4倍を超えるCT強度を示しました[76]。同様に、AuNP-ジアトリゾ酸-AS1411アプタマーコンジュゲートは、CL1-5(ヒト肺腺癌)細胞およびCL1-5担癌マウスに局在していた。 AS1411アプタマーは、細胞表面のCL1-5細胞によって発現されるヌクレオリン(NCL)受容体を標的としますが、ジアトリゾ酸はヨウ素ベースの造影剤です。 AuNP-ジアトリゾ酸-AS1411アプタマーコンジュゲートは、0.027 mM Auハウンズフィールド単位(HU -1 )の傾きを持つ線形減衰曲線を持っていました。 )腫瘍部位でのAuNPの蓄積を示す[77]。 AuNPはより長い血管滞留時間を示し、血液中の循環時間を延長し[77,78,79]、ジアトリゾ酸のCT信号を改善しました[77]。
図5は、齧歯類の心筋梗塞でコラーゲンIを標的とするために、コラーゲン結合接着タンパク質35(CNA35)に結合したAuNPを使用した冠状動脈のin vivoCT血管イメージングを示しています。 AuNP信号は、静脈内(i.v)投与の6時間後も血中に検出されました。これは、ヨウ素ベースの薬剤の半減期(5〜10分)よりも有意に長かった[79]。これらの効果は、マンノース発現(DC2.4およびRAW264.7)細胞で受容体を介した取り込みと非毒性を示した、緑色で合成されたマンナンでキャップされたAuNPを使用して再現されました。マンナンでキャップされたAuNPは、マウスの後肢に注射した後、invivoで膝窩リンパ節を選択的に標的としました[38]。 AuNPベースのCTイメージングは、冠状動脈や癌に限らず、さまざまな疾患の診断に重要な情報を提供できます[76、77、79、80、81]。造影剤としてのAuNPの使用は、光音響、核イメージング、超音波、磁気共鳴イメージングなどの他のイメージングシステムでの可能性を示しています。これらのシステムは他の場所で広範囲にレビューされています[82、83]。
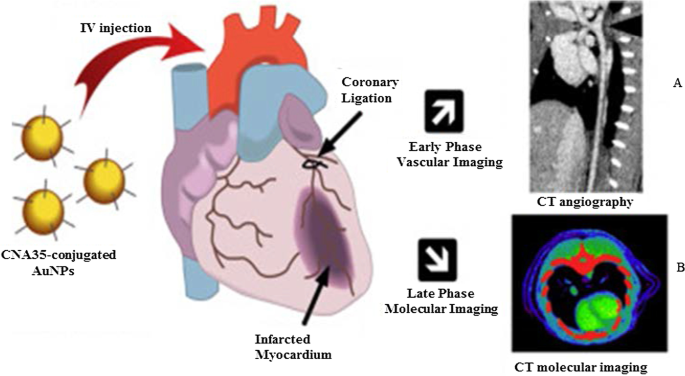
CT造影剤としてAuNPを使用したinvivoCTイメージング。マンナンでキャップされたAuNPとリンパ節のCTイメージング( A )、および心筋瘢痕負荷のCNA35結合AuNPs CTイメージング( B )。許可を得て複製[79]。 Copyright 2018、Elsevier
蛍光ベースの検出システムにおけるAuNPs
AuNPは、蛍光ベースの検出システムで、蛍光剤または蛍光消光剤として使用されます。サイズ≤5nmでは、AuNPは量子ドット(QD)の特性を示し、代わりに使用できます。 Au 55 (PPh 3 ) 12 Cl 6 1981年に導入されたナノクラスターは、その量子サイズの振る舞いのために、おそらく最も集中的に研究されています[7]。それ以来、Au 25 などのさまざまな量子サイズのAuNP(AuNPsQ) (SR) 18 、Au 38 (SR) 24 およびAu 144 (SR) 60 [84]は、優れた電子導体およびレドックスメディエーターであるため、主に電気化学センシングで研究されてきました[85]。
AuNPsQフィルム電極は、前立腺特異抗原(PSA)を検出するための超高感度電気化学免疫センサーの製造に使用されました。免疫センサーの感度は31.5μAmL/ ngで、10μLの未希釈ヒト血清中のPSAの検出限界は0.5 pg / mLでした。イムノアッセイは、癌の存在に関連するレベルよりも低いバイオマーカー濃度で、複数の部分を含む以前に報告されたカーボンナノチューブフォレスト免疫センサーよりも8倍優れた性能を示しました。このように、それは正常な状態と病気の状態の両方でテストバイオマーカーを測定するために使用することができます。免疫センサーの性能は、参照ELISA法[86]と同等でした。 AuNPsQは、多孔質構造のCaCO 3 にも組み込まれました。 球体を形成して蛍光CaCO 3 外傷性脳損傷および肺癌の診断および予後バイオマーカーであるニューロン特異的エノラーゼの検出のための/ AuNPsQハイブリッド。センサーの検出限界は2.0pg mL -1 でした [87]。これまで、B型肝炎[73、88]、インフルエンザA [89]、癌[90]、心臓損傷[91]に関連する分析物を検出するためのAuNPベースの蛍光検出システムがいくつか報告されています。
AuNPは、優れたFRETベースのクエンチャーでもあります[92]。それらのユニークな光学特性(安定した信号強度と光退色抵抗)、サイズ、および変更可能な能力により、蛍光センシングプラットフォームで魅力的なプローブになっています[93、94]。より大きなAuNP(≥10–100 nm)は量子収率が低く、直接蛍光センシングには適していません。しかし、比較的高い励起エネルギー状態で蛍光色素を消光する能力により、効果的なフォトルミネッセンス消光剤になっています[94]。原則として、蛍光ナノプローブはドナーフルオロフォア(色素またはQD)とアクセプターAuNPで構成され、近接すると、選択されたフルオロフォアの蛍光はAuNPによって消光されます[94、95]。蛍光シグナルの欠如によって示されるように標的が存在しない場合、核酸プローブはハイブリダイズし、ループ構造を形成し、その両端にあるフルオロフォアとクエンチャーを近接させる。一方、分析物が核酸プローブに結合すると、AuNPからフルオロフォアが移動し、蛍光シグナルが発生します[24、94、96]。上記の特性を利用して、AuNPは、腫瘍細胞でのマトリプターゼ発現のin vitro(金ナノスフェア、AuNS)およびin vivo(金ナノロッド、AuNR)検出用の分子ビーコンに組み込まれました。 2つの分子ビーコンは、AuNPとフルオロフォアの間のリンカーとしてのマトリプターゼ切断部位で構成されていました。 AuNS分子ビーコンはフルオレセインイソチオシアネート(FITC)で構成され、AuNR分子ビーコンはNIR蛍光色素(メルカプトプロピオン酸、MPA)で構成されていました。ターゲットがない場合、AuNSとAuNRは、それぞれFITCとMPAの蛍光をブロックしました。マトリプターゼの存在下でのAuNP分子ビーコンからのFITCまたはMPAの切断は、定量化可能な蛍光シグナルを示しました。 HT-29腫瘍を有するヌードマウスのMPA–AuNR–ビーコンの蛍光シグナルは、腫瘍部位で14時間持続しましたが、シグナルは時間の経過とともに非腫瘍部位から徐々に消失しました[97]。
AuNPは、4-((4 '-(ジメチル-アミノ)フェニル)アゾ)安息香酸(DABCYL)[94、98]やブラックホールクエンチャー-2 [などの有機消光剤と同等またはそれ以上の蛍光消光効率を示すことが報告されています。 99]。 1.4 nm AuNPの蛍光消光効率は、一般的に使用される4つの有機フルオロフォア(FITC、ローダミン、テキサスレッド、Cy5)と互換性がありました。 AuNPの蛍光消光効率はDABCYLのそれと類似しており、DABCYLとは異なり、AuNPは低塩緩衝液と高塩緩衝液の両方で一貫性を示しました[98]。競合ハイブリダイゼーションアッセイでは、10 nmのAuNPは、市販のブラックホールクエンチャー-2(〜50%)よりもCy3色素に対して優れた(> 80%)蛍光消光効率を示しました。このアッセイでは、ヒト血清中のmiRNA-205の検出限界が3.8 pMで、検出範囲が3.8pMから10nMであり、ヌクレオチド配列が異なるmiRNAを区別することができました[99]。競合するセンサーアレイは感度が高いだけでなく[96、99]、正常細胞と罹患細胞、および良性癌と転移性癌を区別することができました[96]。
AuNPベースのバイオバーコーディングアッセイ
AuNPベースのバイオバーコーディングアッセイ(BCA)テクノロジーは、従来のアッセイよりも最大5桁の標的タンパク質および核酸を検出するための非常に特異的で超高感度な方法の1つになりました[100]。このアッセイは、特定の標的に結合する抗体で機能化された磁性微粒子プローブと、特定のタンパク質標的および抗体を認識するDNAでコードされたAuNPプローブに依存しています。ターゲットDNAと相互作用すると、磁性微粒子とAuNPsプローブの間にサンドイッチ複合体が形成されます。次に、サンドイッチは磁石によって分離され、続いて熱脱ハイブリダイズされて遊離のバーコードDNAが放出され、ターゲットの検出と定量化が可能になります[101、102]。
AuNPベースのBCAアッセイは、従来のELISAよりも100〜150倍高いレベルでHIV-1p24抗原を検出することができました[103]。これらのシステムを使用したPSAの検出限界は330fg / mLでした[104]。 BCAベースのプラットフォームの開発のためのAuNPsの多様性は、脳脊髄液(CSF)に見られる潜在的なアルツハイマー病(AD)マーカーであるアミロイドベータ由来の拡散性リガンド(ADDLs)の濃度を測定することによってさらに実証されました。 ADDL濃度は、認知症ではない年齢をマッチさせた対照よりも、ADと診断された被験者から採取したCSFで一貫して高かった[105]。これらの結果は、AuNPを使用して、実験室での研究や臨床診断のための迅速で高感度なテストプラットフォームを提供することで、ユニバーサルラベリングテクノロジーを改善できることを示しています。
AuNPベースの治療法
金属ベースの薬は医学にとって新しいものではありません。実際、それらはさまざまな病気の臨床治療に使用されている既存の金属薬に触発されています[9、106、107、108、109]。広く研究され、臨床的に使用されている金属ベースの薬剤は、プラチナ(例、進行がんの治療用のシスプラチン、カルボプラチン、テトラプラチナ)、ビスマス(感染症および胃腸疾患の治療用)、金(関節炎の治療用)、およびガリウム(がん関連の高カルシウム血症の治療用)[108、109]。癌の臨床治療のためのFDAによる1978年のシスプラチンの承認[107]は、他の金属(パラジウム、ルテニウム、ロジウムなど)の研究をさらに刺激しました[32、106、110]。
抗リウマチ、抗菌、抗癌効果を含む生物活性、およびバルク金の生体適合性[8、9、46、111]により、AuNPはいくつかの疾患の治療のために広く研究されています。 AuNPは、バルクの対応物よりも優れたユニークで斬新な特性を示しました。 AuNPは非常に安定しており、ドラッグデリバリーおよび治療薬としての医療への応用を導く明確なSPRを備えています[112]。 AuNPには、従来の治療法に比べて多くの利点があります。それらはより長い貯蔵寿命を持ち、[11、49、113]または標的分子なし[14、15、24、25、114]でそれらの標的[25]に到達するのに十分長くシステム内を循環することができます。 AuNPは、局所的かつ選択的な治療効果を提供できます。 AuNPが治療に使用された分野のいくつかを以下に説明します。
非標的AuNPの治療効果
合成されたままの(すなわち、修飾されていない、またはキャップされていない)AuNPは、多くの感染症[115、116]、代謝性および慢性疾患[3、29、50、51]に対して多様な治療効果を有することが示されています。それらの抗酸化作用、抗癌作用、抗血管新生作用[3、32]、抗炎症作用[3、51]、および体重減少[29、50、112]効果は、癌、関節リウマチ、黄斑変性症、肥満などの疾患に有益です[5 、25、113、117]。上記の疾患は、漏出性血管系および高度に血管新生された血管を特徴とし[5、113]、これにより、NPが病変組織に容易に通過し、細胞の影響に対する感受性が高まります。 EPR効果により、キャップのないAuNPは、罹患した細胞または組織の血管系に受動的に蓄積する可能性があります。したがって、AuNPは、血管新生(既存の血管からの血管の成長と伸長)が癌、関節リウマチ、黄斑変性症、肥満などの制御不能になる疾患で抗血管新生効果を発揮するように特別に設計されています[5、25 、113、117]。欠陥のある血管を標的にして破壊することで、酸素と栄養素が病気の細胞に到達するのを防ぎ、その結果、それらの細胞が死に至ります。患部(特に癌や肥満)の血管の毛穴は200〜400 nmであり、このサイズ範囲の物質が血管系から患部の組織や細胞に通過する可能性があります[14、15、25、114]。 。
キャップのないAuNPの細胞への取り込み、局在化、生体内分布、循環、および薬物動態は、サイズと形状に強く依存します[49]。これらの効果はすべてのAuNPに適用できますが、クエン酸塩でキャップされたAuNP(cAuNP)の生物学的効果は、広範囲にわたって研究およびレビューされています。球状cAuNPは、マウスおよびヒトの細胞株に依存するサイズおよび濃度の選択的なin vitro抗癌活性を示しました[3、51]。さまざまなサイズ(10、20、および30 nm)のcAuNPは、ヒト子宮頸癌(HeLa)、マウス線維芽細胞(NIH3T3)、およびマウス黒色腫(B16F10)細胞で異なる効果を示しました。 20および30nmのcAuNPは、2.2 µg / mLの最低濃度で開始するHeLa細胞で有意な細胞死を示しましたが、10nmのNPは≥8.75µg / mLの濃度で毒性がありました。これらのNPの活性は、非癌性のNIH3T3細胞、特に10nmと20nmではごくわずかでした。 20 nmは、最高濃度(35 µg / mL)で生存率を≤5%低下させ、10および30 nmでは〜20%低下させました。 IC 50 Hela細胞の10、20、および30 nm cAuNPの値は、それぞれ35、2.2、および4.4μg/ mLでしたが、IC 50 非癌性細胞の値は35µg / mLより高かった[3]。 0.002〜2 nMの濃度範囲を使用すると、13 nmのcAuNPはウサギの関節軟骨細胞にアポトーシスを誘導し、同じ条件下で3および45nmのcAuNPに影響は観察されませんでした。 13 nmのcAuNPは、ミトコンドリアの損傷を誘発し、活性酸素種(ROS)を増加させました。これらの作用は、ROSスカベンジャーであるN-アセチルシステインによる前処理では阻止できませんでした[51]。さまざまなサイズ(3、5、8、12、17、37、50、100 nm)のcAuNPをマウス(8 mg / kg /週)に4週間注射した後、サイズ依存性の影響もinvivoで観察されました。 8、17、12、37 nmはマウスにとって致命的であり、14日間の治療後に組織の損傷と死亡を引き起こしました。他のサイズは毒性がなく、マウスは実験期間を生き延びました。それどころか、0.4 mMまでの濃度の同じサイズのAuNPは、24時間の曝露後にHeLa細胞に対して毒性がありませんでした[118]。
cAuNPは、体内のさまざまな組織や臓器、特に細網内皮系(RES)臓器(血液、肝臓、脾臓、肺)内で非特異的に相互作用して蓄積する可能性があります[55、119]。これは、高脂肪(HF)食餌誘発性肥満ウィスターラット[55]およびスプラーグドーリーラット[119]で、急性(24時間に1回投与)[55]および慢性(1回投与; 0.9、9、および90)後に明らかでした。 µg /週(7週間)[119]それぞれ14 nmcAuNPへの曝露。静脈内注射されたcAuNPの大部分は、ラットの骨格と死骸を含む肝臓、脾臓、膵臓、肺、腎臓[55、119]で検出されました[119]。 Chen etal。痩せたC57BL / 6マウスに21nm cAuNPを単回腹腔内(ip)注射した後(7.85 µg / g体重)、24〜72時間後に腹部脂肪組織と肝臓に蓄積することが観察されました[29]。 9週間毎日同じ用量を注射されたHF誘発性肥満マウスの脾臓、腎臓、脳、心臓として[50]。 cAuNPは、注射後72時間で腹部WAT(後腹膜および腸間膜)の質量と血糖値を低下させました[29]。食餌誘発性肥満マウスでは、21nmのcAuNPが抗炎症作用と抗肥満作用を示しました[50]。それらはまた、耐糖能を改善し、後腹膜WATおよび肝臓における炎症および代謝マーカーの発現を増強した[50]。 14nmと21nmのcAuNPはどちらも、腎臓と肝臓の損傷に関連するマーカーに毒性や変化の兆候は見られませんでした[29、55、119]。
植物を介したAuNPについても、アクセスできる分子を標的とせずに、げっ歯類の腫瘍[40、120]および肥満WAT [121]を切除するという同様の所見が報告されました。生体AuNPの異なる取り込み、分布、および活性も、NPのサイズと形状によって異なります。特定のサイズが血管網を通過し、病気の部位に保持される可能性がありますが、他のものは、図6 [15、114]に示すように、RES器官と単核食細胞系を介してシステムから簡単にフィルターで取り除くことができます。 NPは、疾患細胞に到達する前に、組織に存在するマクロファージ(TRM)によって除去できます。 TRMを逃れ、疾患部位に到達しないもの、特に小さいNP(≤5nm)は、腎臓での糸球体濾過によって排泄されます[25、114]。クロドロネートリポソームによる前処理は、50、100、および200 nmのAuNPに曝露する前に、肝臓と脾臓のTRMを枯渇させました。これにより、肝臓によるAuNPの取り込みが減少し、血中の半減期と腫瘍部位への蓄積が増加しました[122]。ただし、取り込みをEPR効果に依存するAuNPが克服しなければならない障害はTRMだけではありません。 EPR効果だけでは、≤1%のAuNP取り込みしか確認できず[15、114]、治療前のTRMの枯渇により、NPのわずか≤2%がターゲットに到達しました[122]。非標的化AuNPの成功は、病変組織に到達して蓄積する能力に依存しますが、EPR効果による受動的標的化は効率的ではない可能性があります。 NPはまた、より長く循環し、早期のクリアランスを逃れる必要があり、最も重要なことに、傍観者効果の減少を示す必要があります[25、123]。これらの品質は、バイオアベイラビリティを高め、AuNPの選択性と有効性を確保することができます。これらは、以下で説明するようにAuNPの表面化学を変更することでさらに改善できます[15、124]。
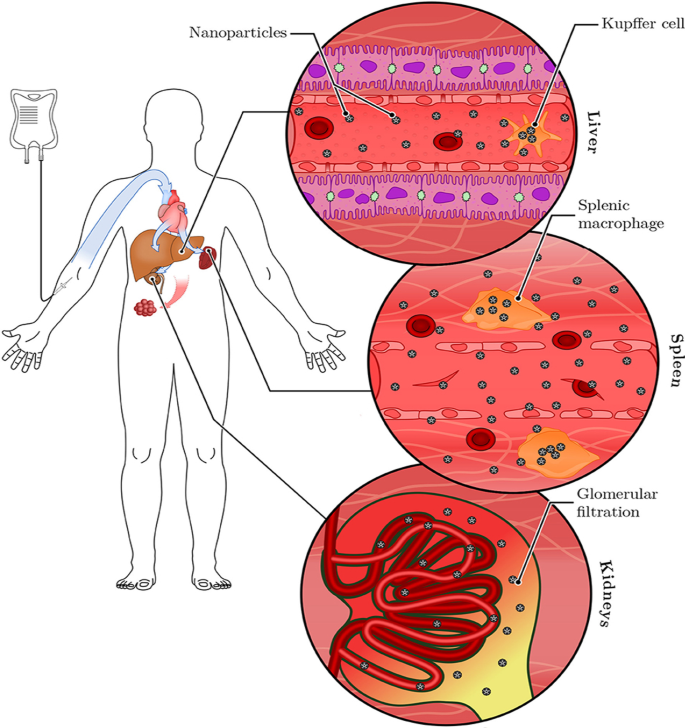
全身投与されたAuNPのRESベースのクリアランスはそれらのサイズに依存します。大きなAuNPは肝臓に蓄積しますが、小さなAuNPは最終的に脾臓に到達するか、糸球体濾過によって尿中に排泄される可能性があります。 TRMを逃れるAuNPは、病変組織に蓄積する可能性があります。許可を得て複製[114]。 Copyright 2019、バイオエンジニアリングとバイオテクノロジーのフロンティア
表面機能化AuNPの治療効果
AuNPベースの治療法の一般的な戦略には、AuNP表面を治療薬で修飾することが含まれます[3、124、125、126]。治療薬は、特定の疾患の治療にすでに使用されている薬物、または細胞シグナル伝達に対する既知の阻害効果を有する生体分子である可能性があります。場合によっては、治療用AuNPは、特定の細胞や組織へのAuNPのアクティブなターゲティングを容易にする分子を持つようにも設計されています。分子は、チオール化、1-エチル-3-(3-ジメチルアミノプロピル)カルボジイミド(EDC)などの化学を使用した化学修飾、ストレプトアビジン/ビオチン結合[3、124、125、126、127]、および反対の電荷に基づくイオン相互作用によって、AuNP表面に容易に吸着できます。 NP表面と生体分子の間[124,125,126]。 AuNP表面の機能化は、それらの物理化学的特性に影響を与え、それらの安全性、生体適合性、および移動性に影響を与える可能性があります。したがって、AuNPによって運ばれる貨物が目的の場所に確実に配達されるようにするには、AuNPの物理的および化学的特性の両方を考慮する必要があります[124、125、126]。特に、AuNPコンジュゲートの機能に重要な役割を果たし[124]、AuNPベースの治療薬の薬物動態を完全に変えることができるのは、AuNPのサイズ、形状、電荷、およびキャッピング剤です。
機能化により、カスタマイズされたナノシステムの開発が可能になり、伝統医学にしばしば伴う望ましくない傍観者効果を減らすことができます。 AuNPの機能化は、AuNP表面へのタンパク質の非特異的吸着を防ぐこともでき、その結果、タンパク質コロナが形成され、食細胞によるオプソニン作用によってAuNPが早期にクリアランスされます[49、123]。 NPの表面電荷は、生物学的環境内のNPの動作に大きな影響を与える可能性があります。中性の表面電荷を持つAuNPは非反応性であり、荷電したAuNPよりもオプソニン化を逃れる率が高くなります。親水性のNPは、疎水性の表面を持つNPとは異なる動作をします[49、123]。 PEGは、食細胞からAuNPをマスクするために最も頻繁に使用されるポリマーの1つであり、多くのin vivo研究でAuNPの生体適合性を安定化および強化することが示されています[49、55、123]。ペグ化は、中性および負に帯電したAuNPが細胞膜に結合したり、アフリカングリーンモンキー腎臓(COS-1)細胞の細胞成分に局在したりするのを防ぐことにより、8.2 nmAuNPの生体適合性を改善しました[49]。そして、ペグ化されたAuNPがポリアルギニン細胞透過部分で機能化されたとき、AuNPは細胞膜上およびCOS-1細胞内で視覚化されました[49]。 SV40ウイルスからの核局在化シグナル、HIVからのTat、およびポリアルギニンペプチドなどの細胞透過性ペプチドは、正常または疾患のあるすべての細胞型内のAuNPの転座で調査されています。ただし、臨床応用には高い特異性が必要であり、悪性細胞と正常細胞の生理学的差異を利用することで達成できます。これは、標的細胞の表面で排他的または過剰発現される細胞特異的受容体を認識する標的分子でAuNPを機能化することによって達成されました。このようにして、AuNPは、標的受容体を発現する細胞にのみ誘導および送達することができます。したがって、AuNPへのターゲティング部分の結合(アクティブターゲティング)は、AuNPが標的受容体を発現する悪性組織にのみ限定されるため、より多くの選択性、傍観者毒性の低減、および有効性の向上をもたらします[49、55、57、113、126、 127]。
AuNPの多様性を示す良い例を図7に示します。ここでは、4つの異なる分子がAuNPに結合され、2つの独立したマーカーとメカニズムをターゲットにしています[11]。多機能AuNPは、ドキソルビシン(Dox)に耐性のある白血病(K562DR)細胞の治療に使用されました。 40 nmのAuNPは、2つのターゲティング部分(葉酸とAS1411アプタマー)と2つの治療薬(Doxとanti-miRNA分子/ anti-221)で修飾されています。葉酸分子とAS1411アプタマーはそれぞれ、細胞表面で過剰発現している葉酸受容体とNCL受容体を認識し、受容体を介したエンドサイトーシスによってAuNPコンジュゲートを細胞に輸送します。 AS1411アプタマーは、細胞内で発現するNCL受容体も標的とすることにより、2つの機能を持っていました。 AuNPコンジュゲートがセルにシャトルされた後、貨物(AS1411アプタマー、anti-221、およびDox)がオフロードされ、セルの消滅を相乗的にもたらす3つのメカニズムに独立して作用します。 AS1411アプタマーと抗221は、NCL / miR-221経路の内因性NCLおよびmiR-221機能を抑制し、それによって細胞をDoxの効果に感作させることで白血病誘発を予防しました[11]。
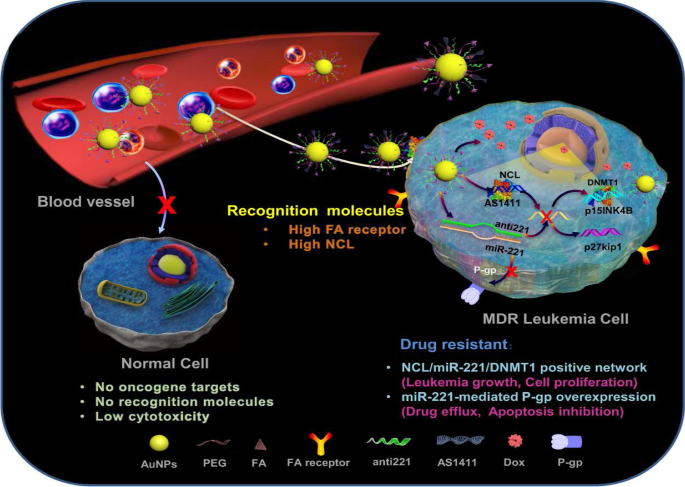
Doxに対する細胞の感受性を高めることによる多剤耐性(MDR)白血病細胞の治療における多機能AuNP。許可を得て複製[11]。 Copyright 2019. SpringerNature。葉酸(FA)受容体
興味深いことに、同様の二重のターゲティングと治療効果は、追加の分子なしでグリーン合成されたAuNPで達成されました。天然物が還元剤として作用するため、生体AuNPは、化学的に合成されたNPよりも生体適合性が高い可能性があります[12、40、41、43、120]。 MGF-AuNPは、前立腺(PC-3)およびトリプルネガティブ乳がん(MDA-MB-231)細胞のラミニン受容体、およびこれらの腫瘍を有する重症複合免疫不全症(SCID)マウスの異種移植片を選択的に標的としました[12、40、120 ]。通常のSCIDマウスでは、静脈内注射されたMGF-AuNPの大部分(30分で85%が24時間後に95%に増加)が肝臓に蓄積しました。血液(2.7%)、脾臓(5%)、肺(0.6%)、胃、腸、腎臓で検出されたのは10%未満でした。前立腺腫瘍を有するSCIDマウスに腫瘍内注射した場合、注射の24時間後に肝臓で検出されたMGF-AuNPはわずか11%でしたが、腫瘍では〜80%でした。胃、死骸、小腸にはごくわずかな量が見られました。一部のAuNPは、24時間後に尿と糞便の腎臓と肝臓の経路から排泄されました[40、120]。 Nano Swarna Bhasmaは、マンゴーの皮の抽出物から合成されたAuNPと、マンゴー、ターメリック、グーズベリー、アラビアガムの植物化学物質からなる混合物で、MDA-MB-231細胞と比較して48時間後に正常な内皮細胞に対する毒性が低下しました[12]。
いくつかの研究は、AuNPが臨床応用の可能性を秘めていることを示しています。従来の薬剤と組み合わせて、疾患細胞を薬剤効果に感作させ[12、128]、また薬剤関連の傍観者効果を防止または低減するために使用することができます[12]。 AuNPは、Dox [43、129]や5-フルオロウラシル(5-FU)[128]などの化学療法薬の薬物動態を改善しました。病気の細胞における薬物の透過性と保持に大きな改善が主に見られ、その結果、有効性が向上しました[130]。正常なマウス線維芽細胞(L929)細胞に対して非毒性であったDox負荷AuNPも、マウスの線維肉腫腫瘍に対して選択的な毒性を示しました[129]。 cAuNPに結合した5-FUは、結腸直腸癌細胞において、それ自体で5-FUよりも優れた活性を示しました[128]。化学療法薬とのAuNPの併用治療は、化学療法薬の有効性を改善するのに非常に効率的でした[12、43、128、129、131]。 Doxおよびシクロホスファミドと組み合わせて経口摂取されたNanoSwarna Bhasmaは、SCIDマウスを有する乳房腫瘍細胞の腫瘍体積を減少させ、IIIA / B期の転移性乳癌患者における化学療法薬の許容可能な安全性プロファイルおよび傍観者効果の減少も示しました[12]。アクティブターゲティングのみで、AuNPを目的のターゲットに直接送達し、健康な組織への損傷を最小限に抑えながら、有効性と毒性のバランスをとることができます[14、15、49]。制御された薬物放出は、AuNPベースのシステムによって提供される多くの利点の1つであり、局所的かつ選択的な毒性を可能にするため重要です[49]。 AuNPは、コンジュゲートが内部(グルタチオン置換、酵素切断可能リンカー、pH)または外部(光、熱)刺激に応答して機能するように設計できます[24、25、34、128]。
遺伝子治療におけるトランスフェクション剤としてのAuNPs
遺伝子治療におけるAuNPの使用は、特定の遺伝子の発現を抑制または増強するための細胞への遺伝物質の送達を促進することにより、有望な結果を示しています[24、32、132]。したがって、AuNPは、癌やその他の遺伝性疾患の治療のための遺伝子治療におけるトランスフェクション試薬として使用できます。 AuNPコンジュゲートは、臨床使用が承認されているポリカチオン試薬を含む実験的なウイルスおよび非ウイルス遺伝子送達ベクターよりも高いトランスフェクション効率を示しています[24]。
AuNPは導電性が高く、疾患治療のための生体分子の細胞内送達のためのエレクトロポレーション中の微小電極としての使用に適しています。 AuNPはエレクトロポレーションシステムの性能を大幅に向上させ、K562細胞などのトランスフェクションが困難な細胞へのDNAの送達に成功裏に使用されてきました[133]。エレクトロポレーションに関連することが多い細胞喪失を防ぐために、ターゲティング部分をAuNPに結合させて、受容体を介したメカニズムを介したAuNP結合体の細胞取り込みを促進することができます[133]。オリゴヌクレオチド分子で細胞をトランスフェクトするためのAuNPの使用には、これらの生体分子の半減期とその有効性を高めるという追加の利点もあります[24、32]。
非標的AuNPコンジュゲートは受動的に細胞に輸送され、効率的なトランスフェクションのために表面電荷とAuNP形状に依存します[24、36、134、135]。 AuNP表面に結合した生体分子の電荷は、トランスフェクション効率に重要な役割を果たします。たとえば、カチオン性分子で機能化されたAuNPは、アニオン性分子で機能化されたAuNPよりも高いトランスフェクション効率を示します。正に帯電したアミノ酸(リジン)をNP表面に付着させて、トランスフェクションの速度を上げることができます。 AuNS [24]およびAuNR [36、134、135]はトランスフェクションに一般的に使用され、従来のトランスフェクション試薬(X-tremeGENEおよびsiPORT)と比較して、invitroで標的遺伝子の発現を> 70%阻害しました[134]。およびinvivo [135]。これらの研究では、トランスフェクション効率は、RT-PCRと免疫染色を使用したターゲット発現に基づいて定量化されました[134、135]。トランスフェクション試薬として、AuNPは長期的な効果、局所的な遺伝子送達、およびより高い有効性を提供します[36、134、135]。他の種類のナノ材料(例えば、ポリマー、リポソーム、セラミック、カーボンナノチューブ)は、AuNPよりも遺伝子治療での使用に大きな注目を集めていました。固形腫瘍におけるsiRNAの送達にポリマーまたは脂質ベースのナノ材料を使用した6つの臨床試験が完了しました[36、134、136]。これらはすべて、低い積載効率、低い安定性、および不十分なペイロード放出に悩まされています[36、136]。一方、AuNPに基づくトランスフェクションシステムは、効率的なローディング容量と安定した複合体の形成を保証する簡単な化学反応を利用します[36、135]。それらの安全性は、それらの形状、サイズ分布、および表面組成を操作することによって制御できます[36]。
AuNPの抗菌効果
MDR微生物は、世界中で主要な健康上の懸念であり、死亡の主な原因です[21、137、138、139、140、141]。これらの微生物は、これらの薬剤の過剰処方と誤用により、従来の抗菌剤に耐性を示しています[142]。主に大手製薬会社がインセンティブの欠如のために抗生物質研究プログラムから撤退したため、40年以上にわたって新しい抗生物質は生産されていません[143]。そのため、次のパンデミックとなる可能性のある抗菌剤耐性に対抗し、薬剤耐性感染の急増を回避するために、新しく効果的な抗菌剤が緊急に必要とされています。
AuNPは、検討中の新世代の抗菌剤の1つです。それらは、多くの病原性およびMDR微生物に対して幅広い抗菌(殺菌、殺菌および殺ウイルス)効果を示しており、したがって微生物の薬剤耐性を克服する可能性があります[21、142、144]。それらの抗菌効果は、それらの物理化学的特性、特にそれらのサイズ、表面組成、電荷および形状に依存します[21、144]。 AuNPはサイズが小さいため、細菌の細胞膜を容易に通過し、生理学的機能を破壊し、細胞死を誘発する可能性があります[35]。 AuNPの正確な抗菌メカニズムはまだ完全には解明されていません。それにもかかわらず、さまざまなナノ構造材料(NSM)と細菌細胞との相互作用から生じる報告された作用機序のいくつかを図8に示します。強調表示されたメカニズムは、AuNPの抗菌活性にも関係しており、微生物の誘導が含まれます。膜損傷による死、ROSと酸化ストレスの発生、細胞小器官の機能不全、遺伝子発現と細胞シグナル伝達の変化[141]。
NSMの抗菌作用モード。さまざまなNSMは、さまざまな生物学的機能を変化させることによって細胞死を誘発する可能性があります。Xは、メカニズムの1つとして、タンパク質のチロシン残基の脱リン酸化による細胞シグナル伝達の変化を表します。許可を得て複製[141]。 Copyright 2018、微生物学のフロンティア
AuNPは、それ自体が抗菌剤であることに加えて、抗菌剤の開発に向けて果たすべき複数の役割を持っています。それらは、薬物増感剤および薬物送達媒体として機能することができます[35、58、132、145]。これらの機能は、化学合成されたAuNPとグリーン合成されたAuNPの両方に適用でき、多くのヒト[21、145、146、147]および水系[148]の病原性株に対して抗菌効果があると報告されています。一般に、試験細菌は、化学的に合成されたAuNP、すなわちcAuNP [21、146、147]およびNaBH 4 に対して低い感受性を示しました。 -AuNPの削減[149]。これは、AuNP表面の負電荷と細菌細胞の間の反発力によるものであり、AuNPと細菌の間の相互作用を妨げていました[21]。化学的に合成されたAuNPの活性は、そのサイズ、形状、濃度、および曝露時間に基づいています。例として、ある研究ではNaBH 4 -還元されたAuNPは、黄色ブドウ球菌に対して活性がありませんでした (黄色ブドウ球菌 )および Escherichia coli ( E.coli )500 µg / mLで6時間[149]。対照的に、別の研究では、NaBH 4 の有意な用量(1.35、2.03、2.7μg / mL)とサイズ(6〜34 nm対20〜40 nm)に依存する抗菌効果が示されました。 -クレブシエラ肺炎のAuNPの減少 、 E。コリ 、 S。アウレウス および枯草菌 [145]。
AuNPは、微生物感染症を治療するために、単独で、または他の抗菌剤と組み合わせて使用されます[35、58、132、145]。他の抗菌剤と組み合わせて使用すると、AuNPコンジュゲートは、AuNPおよび薬剤の個々の効果を超える相乗的な抗菌効果をもたらしました[21、35、58、132、150]。これらの薬物は、化学的方法[4、151]または還元剤およびキャッピング剤[21、149]のいずれかによってAuNPに結合されました。そうすることにより、AuNPはドラッグデリバリー、取り込み、感度、および有効性を改善しました。 AuNPにロードされたFDA承認の抗生物質および非抗生物質のいくつかを表1に示します[4、21、149、152]。シプロフロキサシン[152]、セファクロル[149]、リンコマイシン[4]、カナマイシン[21]、バンコマイシン、アンピシリン[151]、リファンピシン[32]は、AuNPに搭載されている抗生物質のひとつであり、AuNPの多様性を示しています。これらの戦略は、金シリカナノシェル[152]、AuNPで組み立てられたロゼットナノチューブ[151]、マルチブロック共重合体にカプセル化されたAuNP [153]など、さまざまなサイズと形状のAuNPで成功しました。例えば、セファクロルが減少したAuNSは Sの成長を阻害した。アウレウス および E。コリ 濃度(10〜50 µg / mL)に応じて2〜6時間以内ですが、薬剤のみによる完全な細菌増殖阻害は、6時間後の50 µg / mLでのみ観察されました。 The minimum inhibitory concentration (MIC) of the treatments was 10 µg/mL and 50 µg/mL for cefaclor-AuNPs and cefaclor, respectively [149].
AuNPs have presented properties that make them ideal candidates as alternative antimicrobial agents; the most important being their broad antimicrobial activity [21, 35, 58, 132, 150]. Owing to their biocompatibility and easily modifiable surface, microorganisms are less prone to developing resistance toward AuNPs [21]. For example, the kanamycin (Kan)-resistant bacteria (S 。 bovis , S 。 epidermidis , E 。 aerogenes , P 。 aeruginosa and Y 。 pestis ) showed increased susceptibility toward Kan-reduced AuNPs. The MIC values for Kan-AuNPs on the test bacteria were significantly reduced to < 10 µg/mL when compared to the MIC values for Kan alone at 50–512 µg/mL. This shows that AuNPs can restore the potency of antibiotics toward the drug-resistant strains by facilitating the uptake and delivery of the antimicrobial agents [21]. AuNPs can enhance drug-loading capacity and control the rate at which the drugs are released. AuNP hybrids with the multi-block copolymers increased the loading capacity of rifampicin and the drug’s half-life to 240 h. By sustaining the drug in the system for that long, ensured slow release of rifampicin from AuNPs at the target sites after oral administration of the AuNP conjugates to rats for 15 days. The drug on the surface was released within 24 h followed by the drug trapped in the polymer matrix after 100 h. And lastly, the drug entrapped between the AuNPs and the polymer matrix took over 240 h to be released in the interstitial space [153].
The AuNP hybrids also allow for the conjugation of multiple molecules with independent but synergistic functions. This was demonstrated by co-functionalization of the AuNPs with antimicrobial peptide (LL37) and the pcDNA that encode for pro-angiogenic factor (vascular endothelial growth factor, VEGF) and used in the treatment of MRSA-infected diabetic wounds in mice [132]. The AuNPs served dual functions, as a vehicle for the biomolecules, and also as transfection agent for the pcDNA. After topical application of the AuNP conjugates on the wound, the LL37 reduced MRSA colonies, while the pcDNA promoted wound healing by inducing angiogenesis through the expression of VEGF [132].
AuNPs have been shown to confer activity and repurpose some non-antibiotic drugs toward antimicrobial activity. The examples of repurposed drugs, which were used for the treatment of diseases other than bacterial infections, include 5FU [58], metformin [147] and 4,6-diamino-2-pyrimidinethiol (DAPT) [13, 112]. AuNPs as drug carriers are able to transport the drugs into the cells and allow direct contact with cellular organelles that resulted in their death [58, 147]. 5FU is an anti-leukemic drug, when attached to AuNPs was shown to kill some bacterial (Micrococcus luteus , S. aureus , P. aeruginosa , E. coli ) and fungal (Aspergillus fumigatus , Aspergillus niger ) strains [58]. While bacteria are resistant to DAPT, DAPT-AuNPs displayed differential antibacterial activity against the Gram-negative bacteria. Furthermore, conjugation of non-antibiotic drugs (e.g., guanidine, metformin, 1-(3-chlorophenyl)biguanide, chloroquine diphosphate, acetylcholine chloride, and melamine) as co-ligands with DAPT on AuNPs exerted non-selective antibacterial activity and a two–fourfold increased activity against Gram-negative bacteria [13]. When used in vivo, orally ingested DAPT-AuNPs showed better protection by increasing the intestinal microflora in E. coli -infected mice. After 4 weeks of treatment, the DAPT-AuNPs cleared the E. coli infection with no sign of mitochondrial damage, inflammation (increase in firmicutes ) or metabolic disorders (reduction in bacteroidetes ) in the mice [112].
The virucidal effects of the AuNP-based systems have been reported against several infectious diseases caused by influenza, measles [154], dengue [155, 156] and human immunodeficiency [115] viruses. Their anti-viral activity was attributed to the ability of AuNPs to either deliver anti-viral agents, or the ability to transform inactive molecules into virucidal agents [154, 156]. AuNPs synthesized using garlic water extracts inhibited measles viral growth in Vero cells infected with the measles virus. When the cells were exposed to both the virus and AuNPs at the same time, they blocked infection of Vero cells by the measles virus [154]. The AuNPs were nontoxic to the Vero cells up to a concentration of 100 µg/mL but inhibited viral uptake by 50% within 15–30 min at a concentration of 8.8 μg/mL [154]. Based on the Plaque Formation Unit assay, the viral load was reduced by 92% after 6 h exposure to 8.8 μg/mL of the AuNPs. The AuNPs interacted with the virus directly and blocked its transmission into the cells [154]. Modification of the AuNP surface with ligands that bind to the virus [156] or anti-viral agents [115, 155] protected them from degradation, enhanced their uptake and delivery onto the cells. The charge of the AuNPs also played a role, with cationic AuNPs being more effective in the delivery and efficacy of the AuNPs than the anionic and neutrally charged NPs. Cationic AuNPs complexed with siRNA inhibited dengue virus-2 replication in dengue virus-2-infected Vero and HepG-2 cells and also the virus infection following pre-treatment of the virus with AuNPs [155]. Inactive molecules are transformed into highly potent anti-viral agents after conjugation to AuNPs. One such example is the transformation of SDC-1721 peptide, a derivative of TAK-779, which is an antagonist of CCR5 and CXCR3 receptors for HIV-1 strain. SDC-1721 has no activity against the HIV-1, but when conjugated to the AuNPs it inhibited HIV-1 infection of the human phytohemagglutinin-stimulated peripheral blood mononuclear cells. The inhibitory effects of SDC-1721-AuNPs were comparable to the TAK-779 [115].
AuNPs as PT Agents
Diseased cells are sensitive to temperatures above 40 °C; cancer cells in particular appear to be even more sensitive to these high temperatures. Studies have shown that high fevers in cancer patients either reduced the symptoms of cancer or completely eradicated the tumors as a result of erysipelas infections [33, 157, 158]. Historically, fevers induced by bacterial infections, hot desert sand bath, or hot baths were used to increase the body temperature in order to kill the cancer cells [157]. These findings gave birth to PT therapy (PTT), which is mostly used for the treatment of cancer. PTT makes use of organic photosensitizers (indocyanine green, phthalocyanine, heptamethine cyanine) that are irradiated by the external source to generate heat energy that will increase the temperature to 40–45 °C (hyperthermia) in the target cells. Hyperthermia then triggers a chain of events (such as cell lysis, denaturation of the genetic materials and proteins), resulting in the destruction of the diseased cells [57, 158,159,160].
The organic dyes are used alone, or in combination with chemotherapy and radiotherapy for enhanced efficacy [157, 160]. Ideally, the effects of the PT agents must be confined to target cells and display minimal bystander effects. However, the organic PT dyes have several limitations such as toxic bystander effects, susceptibility to photobleaching and biodegradation [159]. In recent years, AuNPs are being explored as alternative PT agents as they exhibit strong plasmonic PT properties, and depending on their shape, they can absorb visible or NIR light. Absorption of light in the NIR spectrum is an added advantage that can allow deep tissue PTT [158, 161, 162]. Unlike organic dyes, AuNPs operate in an optical window where the absorption of light by interfering biological PT agents such as hemoglobin, melanin, cytochromes and water is very low [158, 161, 162].
The practicality of AuNP-based PTT has been demonstrated through in vitro and in vivo studies [158, 162, 163]. When the AuNPs are exposed to light, they can convert the absorbed light energy into thermal energy within picoseconds [57, 158, 159], consequently activating cell death via necrosis or apoptosis in the target cells or tissues. AuNP-based hyperthermia in diseased cells has been reported to occur at half the amount of the energy required to kill normal cells, thus perceived to be safer and better PT agents than the conventional dyes [33, 160]. AuNPs can be easily modified to have localized and enhanced PT activity by targeting and accumulating in only diseased cells through either active or passive targeting. And since the tumor environment is already hypoxic, acidic, nutrient starved and have leaky vasculature, the tumors will be most sensitive to the AuNP-based hyperthermia than the surrounding healthy cells and tissues [33, 160].
AuNP-based PTT has been extensively studied [158, 161, 162] and established that AuNPs (e.g., AuNRs, nanocages and nanoshells) that absorb light in the NIR spectrum are best for in vivo and deep tissue PTT [161]. While the ones that absorb and emit light in the visible spectrum (AuNSs and hollow AuNPs) have been demonstrated to treat diseases that affect shallow tissues (up to a depth of 1 mm), which could be of benefit to superficial tumors [158, 161, 162], ocular surgery [164, 165], focal therapy and vocal cord surgery [158, 165]. Although the PTT effects of AuNSs are limited in vivo or for use in deep tissues, combination therapy or active targeting can be incorporated to facilitate target-specific effects [158, 161, 163]. The AuNPs in the combination therapy will serve dual functions as both drug sensitizer and a PT agent, and was shown to enhance anticancer effects of chemotherapeutic drugs [158, 162, 163]. AuNS-Dox combination demonstrated enhanced cancer cell death after laser exposure when compared to the individual effects of the AuNSs and Dox with and without laser treatment [158].
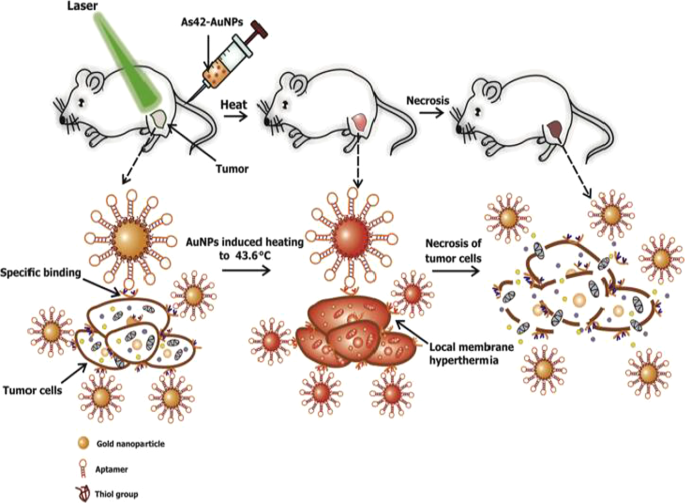
Active targeting on its own can also improve AuNP uptake, localization and target-specific PT effects, which can be viewed in real time by adding fluorophores. AuNSs (25 nm) loaded with transferrin targeting molecules and FITC were shown to accumulate and destroy human breast cancer cells at a higher rate than in non-cancer cells and had better efficacy than the untargeted AuNSs [57]. An independent study also demonstrated that DNA aptamers (As42)-loaded AuNSs (As42-AuNP) induced selective necrosis in Ehrlich carcinoma cells that express HSPA8 protein, a receptor for the aptamers. None of these effects were observed in blood and liver cells mixed with target cells, or cells treated with the AuNSs without laser treatment [163]. The PT effects of the As42-AuNP were replicated in mice transplanted with Ehrlich carcinoma cells in their right leg. As shown in Fig. 9, tail-vein injections of As42-AuNPs followed by laser irradiation resulted in targeted PT destruction of the cancer cells. The As42-AuNPs reduced tumor size in a time-dependent manner; cell death was attributed to increased temperature up to 46 °C at the tumor site. The tumor in mice treated with As42-AuNPs without laser treatment and the AuNPs conjugated with nonspecific DNA oligonucleotide continued to grow but at the lower rate compared to mice injected with PBS. This suggests that the AuNPs were also localized in the tumor [163]. In cases where AuNSs are not efficient for deep tissue PTT, other shapes such as nanocages, nanoshells and AuNRs can be used [158]. Alternately, the visible light absorption of the AuNSs can be shifted to NIR by using processes such as two-photon excitation [57].

In vivo plasmonic PT therapy of cancer cells using targeted AuNSs. As42-AuNPs localized in HSPA8-expressing tumor cells after i.v injection. Exposure to laser treatment resulted in hyperthermia that caused cancer cell death. Reproduced with permission [163]. Copyright 2017, Elsevier
The PT effects of the AuNPs have also been reported for the reversal of obesity [52, 56], using hollow AuNSs (HAuNSs) [52] and AuNRs [56] for the PT lipolysis of the subcutaneous white adipose tissue (sWAT) in obese animals. The HAuNSs were modified with hyaluronate and adipocyte targeting peptide (ATP) to produce HA–HAuNS–ATP conjugate [52]. Hyaluronate was used to ensure topical entry of the HA–HAuNS–ATP through the skin [52, 166], while ATP will recognize and bind to prohibitin once the HAuNSs are internalized. Prohibitin is a receptor that is differentially expressed by the endothelial cells found in the WAT vasculature of obese subjects [5, 52, 55]. The HA–HAuNS–ATP was topically applied in the abdominal region of the obese mice, and through hyaluronate were transdermally shuttled through the epidermis into the dermis where the ATP located the sWATs (Fig. 10) 。 Illumination of the target site with the NIR laser selectively induced PT lipolysis of the sWAT in the obese mice and reduced their body weight [52]. The AuNRs were used in the photothermolysis-assisted liposuction of the sWATs in Yucatan mini pigs. The untargeted PEG-coated AuNRs (termed NanoLipo) were injected in the sWATs through an incision, followed by laser illumination to heat up the sWATs, which was then aspirated using liposuction. The amount of fat removed from NanoLipo-treated porcine was more than the one removed with conventional suction-assisted lipectomy (SAL). NanoLipo-assisted fat removal had several advantages over the conventional SAL; it took less time (4 min) for liposuction compared to 10 min for SAL, the swelling in the treated site healed faster, and the weight loss effects lasted over 3 months post-liposuction [56].
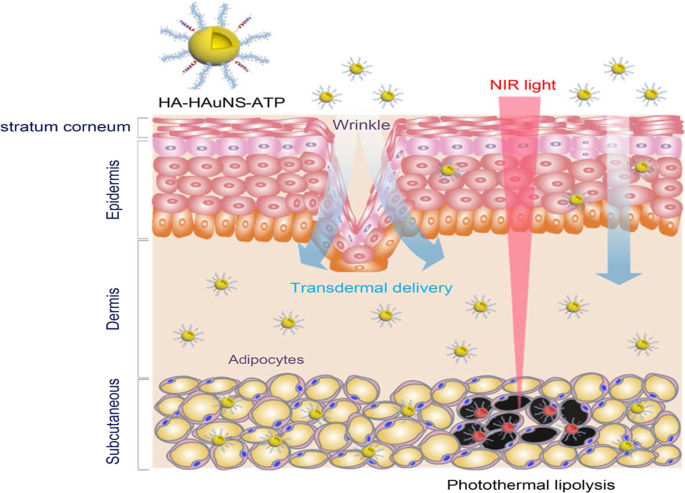
PT lipolysis of the sWATs using HA-HAuNS-ATP. The ATP was conjugated to the AuNSs for targeted delivery and destruction of the prohibitin-expressing sWATs after NIR laser exposure. Reproduced with permission [52]. Copyright 2017, American Chemical Society
AuNP-based PTT clearly offers a lot of advantages compared to the conventional agents. Their biocompatibility allows for broader applications both in vitro and in vivo. Moreover, they can be customized based on their shapes for shallow (AuNSs) [158, 161, 162] or deep tissue (AuNRs and stars) PTT [158, 161]. At 1–100 nm diameter, AuNPs and its conjugates can circulate long enough to reach and accumulate in the target tissues, with or without targeting moieties [159, 167]. Active targeting can be used to ensure localized PT effects through various routes of administration and might be effective for solid and systemic diseases. AuNP-based PTT can also be used to sensitize cancer cells when administered in combination with chemotherapy, gene therapy and immunotherapy [159]. Therefore, AuNP-based PTT has potential for treatment of chronic diseases [161].
Toxicity of AuNPs
AuNPs can play an important role in medicine, as demonstrated by the preclinical and clinical studies under review. Their full potential in clinical application as both diagnostic and therapeutic agents can only be realized if they do not pose any health and environmental hazards. While their use in vitro appears to be inconsequential, in vivo application can be hampered by their potential toxicity, which could be detrimental to human health. A major concern with their clinical use is that AuNPs are non-biodegradable and their fate in biological systems has not been fully studied [5, 30]. Although AuNPs are considered to be bio-inert and compatible, their properties (size, shape, charge and composition) raise concerns as they can alter their pharmacokinetics when used in biological environment [27, 34, 118]. The toxicity of AuNPs of varying sizes and shapes has been demonstrated in animals [27, 118]. These NPs can accumulate in the RES organs where they induce damage.
AuNPs are 1–100 nm in diameter which makes them smaller than most of the cellular components. At these sizes, AuNPs can passively transverse cellular barriers and blood vessels by taking advantage of the EPR effect in pathological cells. AuNPs with smaller diameters (1–2 nm) can easily penetrate cell membranes and biologically important cellular organelles such as mitochondria and nuclei [7, 168]. Accumulation of AuNPs in these organelles induces irreversible damage that can cause cellular demise. On the contrary, AuNPs larger than 15 nm are restricted to the cytoplasmic spaces and unable to penetrate internal organelles [168]. These features are desirable for targeting pathological cells, however, AuNPs can also be taken up by healthy cells and alter their physiology [118]. Administration of AuNP-based therapeutics can be done via different routes (i.e., intranasal, oral, transdermal, i.p or i.v) and transported through blood vessels into different tissues and organs [34, 118]. They are able to pass through the blood brain barrier and the placental barrier [34]. Toxicity is size dependent, with certain sizes of AuNPs being well tolerated, while others could be lethal to healthy tissues. Unfunctionalized AuNSs at 8, 17, 12, 37 nm caused physical changes (i.e., change the fur color, loss of bodyweight, camel-like back and crooked spine) within 14 days of treatment (2 doses of 8 mg/kg/week) in rats [118]. Most (> 50%) of the rats died within 21 days (i.e., after 3 doses), and abnormalities in the RES organs (liver, lungs and spleen) were observed. On the contrary, mice treated with 3, 5, 50 and 100 nm AuNPs were not affected by the NPs and no adverse effects or death occurred throughout the duration (50 days) of the study [118]. In diet-induced obese rats that received i.v injections of 14 nm cAuNPs, the NPs were detected in various tissues after 24 h and were mostly confined to the RES organs [55].
The shape, charge and surface chemistry of AuNPs can influence their toxicity. These factors can determine how AuNPs will interact with the biological systems, their cellular uptake and effects on the cells. AuNSs are readily taken up by cells and proven to be less toxic than other shapes such as rods and stars. AuNP surfaces are charged and will influence how they interact and behave within a biological environment [169]. Cationic AuNPs are likely to be more toxic compared to neutral and anionic AuNPs, as their charge allows these NPs to easily interact with negatively charged cell membranes and biomolecules such as DNA. Both the positively and negatively charged AuNPs have been associated with mitochondrial stress, which was not observed with the neutrally charged AuNPs [34, 35].
The shell that forms on the surface of the AuNP core can also influence the functioning of the NPs. These are usually reducing and/ or stabilizing agents such as citrate and CTAB, and once subjected to a biological environment, these molecules can cause either the desorption or absorption of biomolecules found in the biological environment. This can result in the formation of a corona or cause the NPs to become unstable. Citrate- and CTAB-capped AuNPs are highly reactive, which can facilitate the attachment of biocompatible polymers such as PEG, polyvinyl-pyrrolidone, poly (acrylic acid), poly(allylamine hydrochloride), and polyvinyl-alcohol) or biomolecules such as albumin and glutathione to prevent the formation of AuNP-corona with serum proteins. These molecules serve as a stabilizing agent and form a protective layer that can mask the AuNPs from attacks by phagocytes [7, 29, 34, 170] and prevent off-target toxicity [7]. As discussed in “AuNP-Based Therapies” section, AuNPs can be functionalized with targeting and therapeutic agents to define their targets and effects [34].
In addition to their physicochemical properties, the dosage, exposure time and environmental settings also influence the activity of AuNPs. Lower doses and short-term exposure times might render AuNP as nontoxic, while increasing these parameters will lead to cytotoxic effects [34]. Moreover, in vitro studies do not always simulate in vivo studies. At times, AuNPs that seem to be nontoxic in cell culture-based experiments end up being toxic in animal experiments. Many factors could be responsible for these discrepancies [118], and some steps have been identified that can guarantee the safety of AuNPs in biomedical applications. The biocompatibility and target specificity of AuNPs can be improved by modifying the surface of the NPs. Attaching targeting moieties on the AuNPs can channel and restrict their effects to specific targets or pathological cells [5, 55, 127]. Modification of AuNP surface with bio-active peptides provides a platform for developing multifunctional AuNPs with enhanced specificity, efficacy and potentially sustainable effects [11, 127]. All of these effects will be instrumental in the design and development of AuNP-based systems for clinical applications.
Clinical Application of AuNPs
Nanotechnology has the potential to shape the future of healthcare systems and their outcomes. Its promise of creating highly sensitive and effective nanosystems for medicine has been realized with the introduction of organic nanoformulations for cancer treatment. These systems have already paved the way for nanomaterials into clinical applications:doxil and abraxane have been in the market for over two decades and demonstrated the potential of nanotechnology in medicine [1, 2]. More recently, this technology has been used for the development of the SARS-CoV-2 lipid NP-based vaccine to fight against the COVID-19 pandemic [171]. Inorganic nanosystems such as AuNPs offer many advantages over their organic counterparts, yet few of these systems are used clinically (Table 2) [19, 32].
While several AuNP-based drugs are some of the inorganic nanomaterial-based drugs that were tested in clinical trials, they are not progressing at the same rate as organic liposome-based nanodrugs. Aurimune (CYT-6091) and aurolase were the first of AuNP-based formulations to undergo human clinical trials for the treatment of solid tumors. CYT-6091 clinical trials started in 2005 for delivery of recombinant TNF-α as an anticancer therapy in late-stage pancreatic, breast, colon, melanoma, sarcoma and lung cancer patients. CYT-6091 consists of 27-nm cAuNPs loaded with TNF-α and thiolated PEG. The CYT-6091 nanodrug has achieved safety and targeted biologic response at the tumor site at a dose lower than that required for TNF-α alone [16, 17]. CYT-6091 is approved and yet to start phase II clinical trials in combination with chemotherapy. Based on phase II clinical trial strategy, several variants of CYT-6091 have been developed and tested in preclinical studies. All the nanosystems contain TNF-α with either chemotherapy (paclitaxel, dox and gemcitabine), immunotherapy (Interferon gamma) or apoptosis inducing agents attached to the 27 nm cAuNPs [14,15,16]. The AuNP conjugates preferentially accumulated in the tumor sites after systemic administration through the EPR effect and vascular targeting effects of the TNF-α. The AuNPs were not detected in the healthy tissues, and the anti-tumor effects of TNF-α were restricted to the tumor environment [14, 16, 19].
The first clinical trial for the PT treatment with AuroLase® for refractory and/or recurrent head and neck cancers was completed. Information on the outcome of this trial is still pending. The second trial is set to evaluate the effects of AuroLase® on primary and/or metastatic lung tumors in patients where the airway is obstructed [19]. The number of human trials based on AuNP-based formulation is increasing, covering the treatment of a wide range of medical conditions including skin, oral, heart and neurological diseases. AuNP-formulation (150 nm silica-gold nanoshells coated with PEG), which is similar to AuroLase®, was approved for PT treatment of moderate-to-severe inflammatory acne vulgaris. The nanoshells were topically applied on the acne area and transdermally delivered into the follicles and sebaceous ducts through low-frequency ultrasound or massage. Nanoshells applied through massage were effective in penetrating the shallow skin infundibulum (90%) and the sebaceous gland (20%), while the low-frequency ultrasound can penetrate both shallow and deep skin tissues. NIR laser treatment resulted in focal thermolysis of the sebaceous glands in the affected area and disappearance of the acne [18, 167]. The gold–silica nanoshells were well-tolerated, showed no systemic toxic effects with minor side effects (reddiness and swelling) at the treatment site [18]. AuNPs offer many health benefits based on their unique properties but at the same time have raised a lot of political and ethical issues, and resulted in termination of some clinical studies (NCT01436123).
Conclusion and Future Perspectives
Applications of AuNPs in biomedicine are endorsed by their unique physicochemical properties and have shown great promise as theranostic agents. The increasing interest in biomedical applications of AuNPs is further encouraged by the biocompatibility and medical history of bulk gold, which suggests that the gold core in AuNPs will essentially display similar or improved properties [3]. But at the same time their small size can infer unique properties that will completely change their pharmacokinetics [144]. The diverse biomedical applications of AuNPs in diagnostics and therapeutics herein discussed demonstrate their potential to serve as adjunct theranostic agents. They can be used as drug delivery, PTT, diagnostic and molecular imaging agents [12, 33, 128]. In time, and with better knowledge of mechanisms of action, more AuNP-based systems will obtain approval for clinical use. However, the excitement of these biomedical applications of AuNPs should unequivocally be balanced with testing and validation of their safety in living systems before any clinical applications.
In conclusion, more work needs to be done to taper the toxicity of AuNPs. This can be achieved by introducing biocompatible molecules on their surface [14, 15, 58, 159], and developing new and better synthesis methods, such as the use of green chemistry to produce biogenic NPs. All these developments may further broaden the applications of AuNPs in nanomedicine. AuNPs are non-biodegradable, and off-target distribution could result in chronic and lethal effects. All these concerns must be addressed before clinical translation; the existing trials will soon provide some clarity on their impact in human health. Should their health benefits outweigh their potential risks as is the case with the existing clinical drugs, it is a matter of time before they are approved for clinical use.
Availability of Data and Materials
All the information in this paper was obtained from the studies that are already published and referenced accordingly.
Abbreviations
- 5-FU:
-
5-Fluorouracil
- AD:
-
Alzheimer's disease
- ADDLs:
-
Amyloid-beta-derived diffusible ligands
- ASOs:
-
Antisense oligonucleotides
- AuNPs:
-
Gold nanoparticles
- AuNPsQ:
-
Quantum-sized AuNPs
- AuNRs:
-
Gold nanorods
- AuNSs:
-
Gold nanospheres
- BCA:
-
Bio-barcoding assay
- cAuNPs:
-
Citrate-capped AuNPs
- COVID-19:
-
Corona virus disease 2019
- CSF:
-
Cerebrospinal fluid
- CT:
-
Computed tomography
- CTAB:
-
Cetyltrimethylammonium bromide
- DABCYL:
-
4-((4′-(Dimethyl-amino)-phenyl)-azo)benzoic acid
- DAPT:
-
4,6-Diamino-2-pyrimidinethiol
- Dox:
-
Doxorubicin
- EDC:
-
1-Ethyl-3-(3-dimethylaminopropyl) carbodiimide
- EPR:
-
Enhanced permeability and retention
- FA:
-
Folate
- FDA:
-
Food and Drug Administration
- FITC:
-
Fluorescein isothiocyanate
- FRET:
-
Fluorescence resonance energy transfer
- HAuNSs:
-
Hollow AuNSs
- HF:
-
High-fat
- HU −1 :
-
Hounsfield unit
- LFAs:
-
Lateral flow assays
- LSPR:
-
Localized surface plasmon resonance
- MDR:
-
Multidrug resistant
- MGF:
-
Mangiferin
- MPA:
-
Mercaptopropionic acid
- MWPLP:
-
Microwave-induced plasma-in-liquid process
- NCL:
-
Nucleolin
- NIR:
-
Near-infrared
- NSMs:
-
Nanostructured materials
- P. jirovecii :
-
Pneumocystis jirovecii
- PEG:
-
Polyethylene glycol
- PSA:
-
Prostate-specific antigen
- PSMA:
-
Prostate-specific membrane antigen
- PT:
-
Photothermal
- PTT:
-
Photothermal therapy
- QDs:
-
Quantum dots
- RES:
-
Reticuloendothelial system
- ROS:
-
Reactive oxygen species
- SARS-CoV-2:
-
Severe acute respiratory syndrome-coronavirus-2
- SCID:
-
Severe combined immunodeficiency
- SPR:
-
Surface plasmon resonance
- sWAT:
-
Subcutaneous white adipose tissue
- TOAB:
-
Tetrabutylammonium bromide
- TRMs:
-
Tissue-resident macrophages
- VEGF:
-
Vascular endothelial growth factor
- WAT:
-
White adipose tissue
ナノマテリアル
- 化学療法センサー用の金ナノ粒子
- 癌治療のためのナノ粒子:現在の進歩と課題
- 合成および生物医学的応用のための蛍光ナノ材料の進歩と挑戦
- スーパーキャパシター用途向けのグラフェンおよびポリマー複合材料:レビュー
- Au @ TiO2卵黄シェルナノ構造の調製とメチレンブルーの分解および検出へのその応用
- 炭化水素中の金ナノ粒子のサイズ制御と安定化のための分散剤としての修飾ハイパーブランチポリグリセロール
- PPy被覆MnO2ハイブリッドマイクロ材料の調製とリチウムイオン電池のアノードとしてのそれらの改善されたサイクル性能
- 生物医学的応用のための球形の共役金-ザルガイ殻由来炭酸カルシウムナノ粒子の製造、特性評価および細胞毒性
- 銀ナノ構造の合成方法と応用における最近の進歩
- 金および銀ナノ粒子のグリーン合成のためのPlatycodiRadix(Platycodon grandiflorum)からのPlatycodonサポニン
- 丸い形の金ナノ粒子:シロイヌナズナの根の成長に対する粒子サイズと濃度の影響



