PDMAEMAベースの銀含有共重合体ミセルの容易なinsitu調製およびinvitro抗菌活性
要約
コアシェル構造を備えた明確に定義されたポリマーミセルは、疾患を標的とする抗菌剤の分野で銀ナノ粒子(AgNP)を安定化するための優れたデリバリープラットフォームです。ポリマー構造の合理的な構築、効率的で簡単なグリーン調製アプローチ、およびサイズ、粒子安定性、抗菌活性、その他の特性など、派生したAgNPの包括的な調査が必要です。ここでは、異なる共重合体トポロジーを持つAgNPsで装飾された共重合体ミセルのinvitro抗菌活性を設計および評価しました。最初に、同様の分子量および重合度を有する線状または4アームのスタートリブロックコポリマーが得られ、これは、外部還元剤なしで銀イオンをその場で還元してAgNPを形成するためのDMAEMAから構成された。ミセルシェルのHEMAとPEGMAは、血液循環中のAgNPの安定性を高めました。計算モデリングと実験結果の組み合わせは、両方のタイプのミセルが単分散で球状の形態を持つAgNPを製造できることを示しました。星型共重合体ミセルで安定化されたAgNPは、線形構造を持つものよりも平均サイズが小さく、安定性が高く、抗菌活性が高く、これは星型共重合体からのミセルの安定性が高いためと考えられます。さらに、細胞毒性評価試験は、達成された線状または星型共重合体ミセル安定化AgNPが良好な生体適合性を有することを示した。この作業は、広範囲の細菌感染症と戦うための適切なトポロジーを備えたミセル安定化AgNPの合理的な設計における簡単で普遍的なアプローチを提供します。
はじめに
過去数十年の間に、伝統的な抗菌剤のスレートが感染症の治療に広く使用されてきました。世界保健機関によると、多剤耐性微生物の急速な出現はますます深刻な世界的な問題となっており、人間の健康に対する主要な脅威のリストでトップ3にランクされています[1,2,3,4,5]。したがって、細菌耐性を生じることなく、安全性が高く、効果的な抗菌能力を備えた新しい抗菌剤を開発する必要があります。銀ナノ粒子(AgNPs)は、古くから最高の抗菌剤の1つとして、さまざまな細菌や真菌の病原体に対する優れた性能、哺乳類細胞に対する比較的低い毒性、および限られた細菌耐性のために、消費財に広く使用されていました[6,7、 8,9,10]。 AgNPは、細菌の膜透過性を改善し、細胞質に浸透し、細菌タンパク質を変性させ、細菌の複製を妨害して、細菌を死に至らしめることができます[11、12、13]。 AgNPの抗菌活性を解明するために多数の銀製剤が使用されてきました[14、15、16、17]。たとえば、双性イオン性ポリカルボキシベタインヒドロゲルを介した創傷被覆材と、Zhangらによって提案されたコア成分としての抗菌AgNP。 i>。 [18]、Moreno-Couranjouらによって提案されたAgNPを共固定化するための多成分コーティングによって得られた多機能表面。[19] 。
ただし、大きな比表面積と高い表面エネルギーにより、AgNPが凝集し、アプリケーションの大きなボトルネックになっています。したがって、AgNPを安定化させるには、ポリマーマトリックスまたは外部安定剤が必要です。知られているように、ポリマーマトリックスは、凝集の問題を解決するための最も一般的な方法です。現在、AgNPをポリマーマトリックスで安定化するために、化学的還元法、電気化学的方法、光化学的方法、マイクロ波法などのいくつかの方法が使用されています。それらの中で、化学的還元は一般的で効果的な方法です。硝酸銀は、ヒドラジン水和物(N 2 )などの還元剤を添加することによってAgNPに還元されます。 H 4 )、水素化ホウ素ナトリウム(NaBH 4 )、クエン酸ナトリウム、および溶液中のアスコルビン酸[20,21,22,23]。たとえば、Hoda etal。製造されたポリスチレン-ブロック-ポリアクリル酸(PS- b -PAA)還元剤N 2 の影響下で20nmAgNPをロードした逆ミセル H 4 、およびPSブロックはトルエン中で外層を再生しました[24]。 Liuのグループは、自己組織化ミセルナノテンプレートがポリ(ε-カプロラクトン)-ブロック-ポリ(アスパラギン酸)(PCL- b -PAsp)。十分に分散したAgNPは、AgNO 3 を使用して調製しました。 前駆体およびNaBH 4 として レデューサーとして[25]。しかし、上記の方法は環境にやさしくなく、過剰な還元剤を加えると副産物が生成されるため、AgNPの精製が困難になり、感染症を標的とする抗菌剤の使用が制限されます。
一方、アミン基を含むポリマーは、AgNPをその場で調製するための還元剤と安定剤の両方として使用できることが報告されています。たとえば、Lang etal。 PCL、2-(ジメチルアミノ)エチルメタクリレート(DMAEMA)、およびポリ(エチレングリコール)メチルエーテルメタクリレート(PEGMA)からなる合成6アームスターポリマー。このシステムは、水相に他の還元剤を添加することなく、硝酸銀を直接AgNPに還元しました[26]。上記のAgNPは、金ナノ粒子と比較して、追加の還元剤なしで容易な表面修飾を示しますが[27、28]、ミセルベースの抗菌活性への適用とともに、銀ナノ粒子の還元と安定性に対するポリマートポロジーの影響は少なくなります。勉強しました。
この作業では、ナノプラットフォームと同様の分子量と重合度を持つ線形または4アームのスタートリブロックコポリマーから自己組織化された高分子ミセルを利用して、細菌感染と戦うための穏やかで簡単で環境に優しいアプローチが設計されましたAgNPを装飾する(スキーム1)。このアプローチでは、DMAEMA、2-ヒドロキシエチルメタクリレート(HEMA)、およびPEGMAで構成されるトリブロック共重合体は、水性条件で自己組織化ミセルを生成できます。これは、AgNPの調製と安定化に適したテンプレートです。第三級アミン基を持つPDMAEMAブロックは、Ag + を簡単に吸収できます。 配位相互作用によってイオンを生成し、その場で還元剤なしでAgNPを生成します。親水性の高いHEMAおよびPEGMAブロックを水相の安定剤として使用して、AgNPの安定性をさらに向上させることができます。したがって、硝酸銀は、自己組織化共重合体ミセルの核上で自発的に配位および脱酸して、AgNPを形成する可能性があります。それらはミセルコアに埋め込まれ、細菌の膜を破壊する可能性があります。ここでは、線形または4アームスターコポリマートポロジーが最大吸収波長、形態、粒子サイズ、ゼータ電位、安定性、およびAgNPの抗菌効率にどのように影響するかを十分に調査しました。したがって、構造と特性の関係に関する研究は、細菌感染症の治療のための銀ハイブリッドナノ粒子の詳細な説明を理解するかもしれません。さらに、より安定した構造と制御可能な粒子サイズを備えたAgNPを調製するための設計アイデアと技術的基盤を提供します。
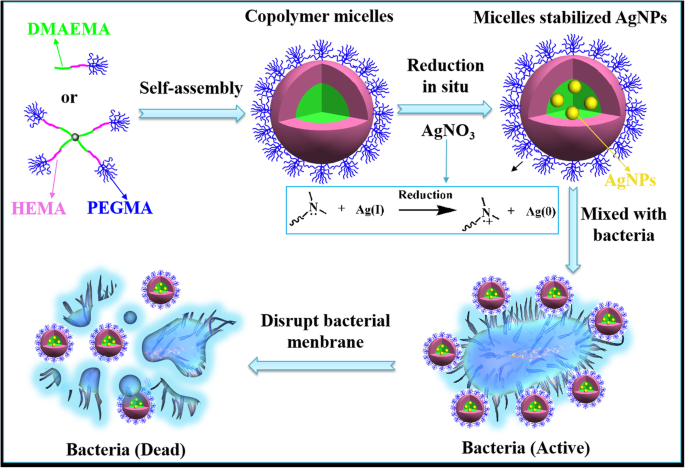
優れた抗菌活性のために線形/星型共重合体ミセル安定化AgNPの形成の概略図
材料と方法
資料
ペンタエリスリトール( J&K Scientific Ltd.)を使用前に、減圧により24時間乾燥させました。 2-(ジメチルアミノ)エチルメタクリレート(DMAEMA、> 98%)、2-ヒドロキシエチルメタクリレート(HEMA、99%)、およびポリ(エチレングリコール)メチルエーテルメタクリレート(PEGMA、 M n =300 Da、99%)、すべてAldrich製で、中性アルミナ含有カラムを通過させて阻害剤を除去することにより精製しました。水素化カルシウム(CaH 2 )、Aldrichのテトラヒドロフラン(THF)およびトルエンを乾燥させた後、減圧下で蒸留して使用しました。 2-ブロモイソ酪酸エチル(EBiB、98%、Alfa Aesar)、臭化2-ブロモイソブチリル(BIBB、98%、Alfa Aesar)、1,1,4,7,10,10-ヘキサメチルトリエチレンテトラミン(HMTETA、99%)、硝酸銀(AgNO 3 、99.9%)、臭化第二銅(CuBr 2 )、メタノール、トリエチルアミン(TEA)、ジクロロメタン(DCM)、アセトン、 n -ヘキサン、ジメチルスルホキシド(DMSO)、オクタン酸第一スズ(Sn(Oct) 2 )、炭酸ナトリウム(Na 2 CO 3 )、重曹(NaHCO 3 )、塩化ナトリウム(NaCl)、硫酸ナトリウム(Na 2 SO 4 )、および J&K から入手した他のすべての試薬 化学会社は受け取ったままの状態で使用されました。
一般的な特性評価と計測
プロトン核磁気共鳴( 1 H NMR)線形または4アームトリブロックコポリマーのスペクトルがCDCl 3 で検出されました。 、およびD 2 Bruker ADVANCE 400 MHz分光計(米国ウィスコンシン州マディソン)を介して25°CでO。線形コポリマー、スターコポリマー、およびそれらのミセル安定化AgNPのフーリエ変換赤外分光法(FTIR)スペクトル測定は、25°Cの透過モードを備えたFT IR分光光度計(Nicolet Nexus for Euro、USA)を使用して実施しました。臭化カリウム(KBr)で粉砕し、圧縮した後、粒状サンプルを調製しました。スペクトルを取得するために、スペクトル条件は、4000〜400 cm -1 の波長で事前に設定されています。 (32スキャン)および8cm -1 の解像度 。異なるモル比で線形および星型共重合体ミセル安定化AgNPのゼータ電位を、各サンプルを25°Cで3回テストしたMalvern Zetasizer Nano S装置(Malvern、WR、UK)を使用した電気泳動測定を使用して測定しました。 200 kVで動作する透過型電子顕微鏡(TEM、FEI Tecnai-G20)を実施して、さまざまなモル比で線形および星型共重合体ミセル安定化AgNPの形態を観察しました。 TEM用の製品の準備プロセスは次のとおりです。10μLのサンプル溶液を最初にカーボンでコーティングされた銅グリッドに滴下し、次に空気中で乾燥させました。線状および星型コポリマーミセルで安定化されたAgNPのUV-Visスペクトルを、UV-Vis分光光度計(UV-2450、島津、京都、日本)を使用してさまざまなモル比で測定しました。熱重量分析(TGA)は、NETZSCH(STA409PC、ドイツ)装置で実行されました。すべての乾燥粉末サンプル(線状共重合体、星型共重合体、およびそれらのミセル安定化AgNP)は、窒素条件下で10°C /分の速度で25から600°Cに加熱されました。
PDMAEMAの合成- b -PHEMA- b -PPEGMA
DMAEMA、HEMA、およびPEGMAの電子移動原子移動ラジカル重合(AGERT ATRP)によって再生された連続活性剤は、Zhang etal。から変更された手順に従って実行されました。 [29、30]。簡単に言えば、CuBr 2 の添加後 (10 mg、0.045 mmol)、100 mLの乾燥した3つ口フラスコを排気し、アルゴンで3回すすいだ。脱気したシリンジを補助して、無水トルエン(25 mL)、EBiB(88μL、0.24 mmol)、DMAEMA(5.15 mL、30.5 mmol)、およびリガンドHMTETA(62μL、0.24 mmol)を容器に順番に注入しました。 10分間の攪拌。 Sn(Oct) 2 を注入した後 (78μL、0.24 mmol)トルエン(2 mL)を溶液として、70°Cの油浴で8時間反応させた。溶液がはるかに濃くなった後、次の8時間の反応のために連続ブロックHEMA(2.32 mL、18.4ミリモル)を注入しました。最後に、3番目のモノマーであるPEGMA(8.89 g、55.6 mmol)を使用して、フラスコをほぼ室温に冷却する前に、72時間の連続反応を確認しました。 THF(30mL)を容器に注入し、次に反応混合物を中性アルミナカラムに通して触媒を除去した。製品PDMAEMA- b -PHEMA- b -PPEGMAは10倍過剰の冷たい n に沈殿しました -ヘキサン、ろ過し、最後に35°Cで48時間真空乾燥します。
(PDMAEMA- b の合成 -PHEMA- b -PPEGMA) 4
スター型ブロモ末端開始剤(Br) 4 ペンタエリスリトール上に存在する末端ヒドロキシル基を2-ブロモイソブチリルブロミドで溶媒としてTHF、酸結合剤としてTEAを使用してエステル化することにより合成されました。通常、ペンタエリスリトール(2.72 g、2 mmol)を充填した後、100 mLの3つ口フラスコを排気し、アルゴンで3回リンスした後、無水THF(120 mL)とTEA(12.51 mL、90 mmol)を連続して滴下しました。 。氷/水環境下で、臭化2-ブロモイソブチリル(11.12 mL、90 mmol)を激しく攪拌した溶液に滴下し、0°Cで4時間反応させた後、25°Cで20時間反応させました。生成物を精製するために、混合物を最初に中性アルミナカラムに通した。粗生成物を水、10%Na 2 で連続して洗浄した。 CO 3 、飽和NaHCO 3 、および飽和NaCl、次にNa 2 を通して連続的に乾燥させた SO 4 一晩、ろ過し、濃縮してから、10倍過剰の冷たい n に注ぎます。 -ヘキサンで生成物を沈殿させ、最後に真空下で24時間乾燥させて生成物を受け取ります。
(PDMAEMA- b の合成経路と給餌量 -PHEMA- b -PPEGMA) 4 PDMAEMA- b と同じ手順を使用して実行されました -PHEMA- b -PPEGMA。
線形または星型の共重合体ミセルを使用したAgNPの調製
PDMAEMA- b -PHEMA- b -PPEGMAまたは(PDMAEMA- b -PHEMA- b -PPEGMA) 4 最初に水溶液(pH 7.0)を取得し、これにAgNO 3 DMAEMAとAg + の還元反応を引き起こしながら、溶液を添加しました。 ミセルコアのinsituでAgNPを形成します。 DMAEMAとAgNO 3 のモル比をとる 例として9に等しい、最初に、PDMAEMA- b -PHEMA- b -PPEGMAまたは(PDMAEMA- b -PHEMA- b -PPEGMA) 4 同量の[DMAEMA] =4.8 mMをアセトン(5 mL)中で4時間撹拌した後、蒸留水(20 mL)を一晩撹拌しながら添加して、安定したミセルを形成します。次に、AgNO 3 溶液(220μL、48 mM)を上記の溶液に滴下注入し、暗所で25°Cで48時間撹拌しました。最後に、線形または星型高分子ミセルで安定化されたAgNPは、次の実験のために-20°Cで保存する前に収集および凍結乾燥することによって調製されました。
抗菌アッセイ
ポリマーミセルで安定化されたAgNPの抗菌性調査は、 Escherichia coli に対して実施されました。 DH5alpha( E 。 コリ DH5α)株は、キャリアとしてルリア-ベルターニ(LB)培地を使用して、超音波によってさまざまな濃度のポリマーミセル安定化AgNP溶液を調製します。モノクローナル E 。 コリ DH5αは、細菌懸濁液を1×10 5 に希釈する前に、200 rpmのシェーカーで37°CのLB培地(5 mL)で一晩培養しました。 LB培地によるCFU / mL。等量の希釈細菌を異なる濃度の共重合体ミセルまたはミセル安定化AgNPと混合し、37°Cで16時間インキュベートした後、600 nmの波長での光学密度の変化をマイクロプレートリーダー(Multiskan Spectrum、サーモサイエンティフィック、ヴァンター、フィンランド)。各アッセイを6回繰り返しました。
細胞生存率の評価
細胞生存率を評価するために、肝細胞癌(HepG2)細胞を用いた3-(4,5-ジメチルチアゾール-2-イル)-2,5-ジフェニルテトラゾリウムブロミド(MTT)アッセイを実施しました。細胞を播種する前に、HepG2細胞を最初に5%CO 2 の加湿雰囲気でインキュベートしました。 10%ウシ胎児血清(FBS)、ペニシリン(100μL/ mL)、およびストレプトマイシン(0.1 mg / mL)を添加したダルベッコ改変イーグル培地(DMEM)で37°Cで。次に、HepG2細胞を96ウェルプレート上の新しいDMEM培地に1×10 4 の密度で播種しました。 ウェルあたり、1日培養。あらかじめ調製した共重合体ミセルまたはミセル安定化AgNPs溶液(100μL)をさまざまな濃度でDMEM培地に置き換えた後、細胞を次の24時間培養し続けました。 PBSバッファーで3回洗浄した後、20μLのMTT試薬(5 mg / mL)と180μLの新鮮なDMEMを添加し、さらに4時間インキュベートしました。最後に、溶液を200μLのDMSOに交換し、プレートを10分間穏やかに振とうしました。上記のマイクロプレートリーダーを用いて570nmでの吸光度を測定した。 6つの並行実験のデータを平均しました。
散逸粒子動力学シミュレーション
AgNPの成長プロセスを分析するために、粗視化モデルに基づく散逸粒子動力学(DPD)シミュレーションを、Materials Studio 8.0(Accelrys Inc.、San Diego、CA、米国)。追加ファイル1:図S1に示すように、6種類のビーズが共重合体PDMAEMA- b を構成しました。 -PHEMA- b -PPEGMAまたは(PDMAEMA- b -PHEMA- b -PPEGMA) 4 :オレンジは中央を表し、MAA1(エチルアミン側鎖の隣のメタクリレート)は薄緑、DMA(アミノエチル側鎖)は緑、HEMAはピンク、MAA2(PEG側鎖の隣のメタクリレート)は青、 PEG。ユニットセル結晶(格子長:3.87Å)を持つ小さなクラスターは、銀ビーズ(金色)としてマークされた4つの銀原子で構成されていました。同時に、黒色の各水ビーズ(W)には5つの水分子が含まれていました。以前の作業によると、追加ファイル1:表S1は、計算相互作用パラメーターの結果を示しています[31、32]。 30×30×30 r c 3 周期境界条件を備えた3次シミュレーションボックスは、100,000の合計シミュレーションステップと0.05nsの積分時間ステップで全方向に使用されました。
統計分析
統計分析は、2サンプルの学生の t を使用して実行されました。 不等分散でテストします。 p <0.05は統計的に有意であると見なされました。
結果と考察
線形/星型共重合体の合成と特性評価
線状共重合体PDMAEMA- b -PHEMA- b -PPEGMAとスターコポリマー(PDMAEMA- b -PHEMA- b -PPEGMA) 4 DMAEMA、HEMA、およびPEGMAとCuBr 2 のARGETATRP重合によって合成されました。 / HMTETAを触媒として、Sn(Oct) 2 還元剤として、およびトルエン中の開始剤としてBIBBで以前にアシル化されたEBiBまたはペンタエリスリトール(スキーム2)。ターゲットポリマーの構造と組成は、 1 によって検証されました。 HNMR。高分子ミセルはPDMAEMA- b から自己組織化されました -PHEMA- b -PPEGMAまたは(PDMAEMA- b -PHEMA- b -PPEGMA) 4 DMAEMAを機能ブロックとして使用します。Ag + イオンは、余分な還元剤を使用せずに引き付けられ、AgNPに還元されました。共重合体のトポロジー構造がAgNPに及ぼす影響について、物理化学的特性、抗菌、および抗癌活性から議論および評価しました。
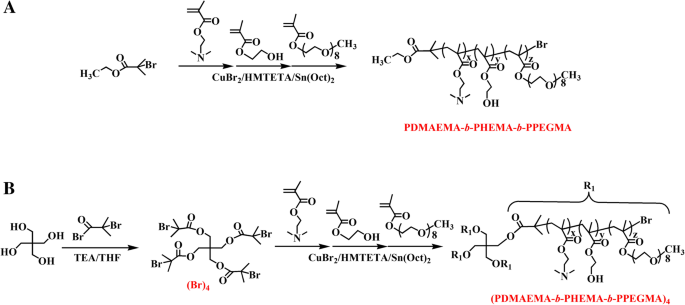
a の合成ルート PDMAEMA- b -PHEMA- b -PPEGMAおよび b (PDMAEMA- b -PHEMA- b -PPEGMA) 4
線状/星型共重合体の化学構造は 1 によって確認されました HNMR。まず、ペンタエリスリトールの末端ヒドロキシル基が完全に末端臭素基(Br) 4 に転移しました。 、 1 に示すように H NMRスペクトル(追加ファイル1:図S2)。 4.33 ppmのピークは、-C H に起因していました。 2 O-ペンタエリスリトール中、新しい-(C H 3 ) 2 -1.94ppmの信号が現れました。また、1.94ppmから4.33ppmのピークの積分比の値は約3でした。追加ファイル1:図S3およびS4に示すように、-C(C H 3 ) 2 -1.94ppmで出現しました。 1.83 ppm、1.00 ppmの信号は、-C H に割り当てられました。 2 -および-CC H 3 -それぞれメタクリル酸メチルの主鎖に。 2.58ppmと4.08ppmのピークは、隣接する2つのメチレンプロトン-C H の特徴的な共鳴に属していました。 2 C H 2 -DMAEMAブロックで、2.29ppmのピークがメチルプロトンに割り当てられました-C H 3 -、これは第三級アミン基に結合していました。 -C H の存在 2 C H 2 -HEMAユニットの末端ヒドロキシル基に接続されたメチレンプロトンは、それぞれ4.08ppmと3.57ppmで現れました。 -OC H の特徴的なPEGピーク 2 C H 2 -および端子-C H 3 プロトンはそれぞれ3.67および3.39ppmで現れました。 1 では、5.5〜6.1ppmの二重結合のピークが消失しました。 HNMRスペクトル。信号(f)と(a)の積分比の値から計算( I f / 私 a )、信号(g)から(a)( I g / 私 a )、(h)を(a)に通知します( I h / 私 a )、それぞれ、PDMAEMA 19.3 - b -PHEMA 12.5 - b -PPEGMA 24.6 および(PDMAEMA 5.0 - b -PHEMA 5.6 - b -PPEGMA 5.0 ) 4 取得されました。
線形/スター共重合体ミセルで安定化されたAgNPの調製と特性評価
AgNPの形成プロセスをスキーム1に示しました。PDMAEMA分子鎖の第三級アミン基に属するN原子上の孤立電子対は、配位と還元の能力を持っているため、トラップ剤としても使用できます。と還元剤。まず、Ag + 間の錯化により、銀イオンがPDMAEMAによってトラップされました。 およびN原子、形成(Ag + )-PDMAEMAコンプレックス。続いて、Ag + 核形成段階で銀原子を形成するためにその場で還元された。その後、Agの核形成は、Ag結晶の成長とともに継続し、AgNPの形成をもたらしました[26]。親水性ブロックPPEGMAはミセルシェルとして機能し、安定した保護層を提供し、AgNPの安定性をさらに向上させました。システム内の自己組織化ミセルの立体安定化効果は、AgNPの安定化とAgNP間の凝集に対するミセルの熱力学的平衡によって決定されました。少量のAgNPの場合、コポリマーの立体安定化により、AgNPのさらなる凝集を防ぐことができます。 Agの数が増えると、AgNPに対するミセルの安定性が弱まり、粒子間の衝突の可能性が高まり、AgNPのサイズが大きくなります。ミセルの空間的安定化を利用して、私たちが準備したAgNPは粒子サイズを制御しており、これは抗菌用途に大きな可能性を秘めています。
DPDシミュレーションは、実際の実験と同じ濃度で、AgNPの成長プロセスと分布を調査するために実行されました(PDMAEMA / AgNO 3 モル比=1/1、線状共重合体の体積分率、Agおよび水ビーズはそれぞれ10%、0.23%、および89.77%です)。図1は、PDMAEMA- b のビーズが -PHEMA- b -PPEGMAおよびAgNPは、最初は水溶液中で不規則に分布した状態を示しました。時間が経つにつれて、8つの自己組織化共重合体ミセルが最終的に形成され、均一に分散し、すべてのAgビーズがミセルにロードされました。平衡状態にあるAgNPは、共重合体ミセル内でさらに凝集することなく安定化できることがわかりました。これは、自己組織化ミセルがAgNPのさらなる凝集を防ぎ、粒子サイズと分布を制御する目的を達成したことを示しています。
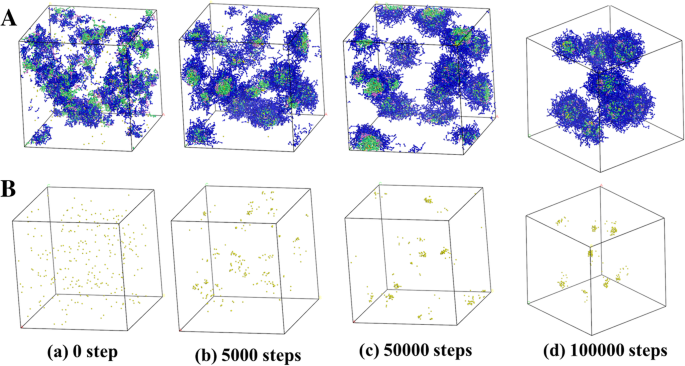
PDMAEMA- b を使用したAgNPの成長プロセスと分布のDPDシミュレーション -PHEMA- b -PDMAEMA / AgNO 3 でのPPEGMA 異なるシミュレーション時間でのモル比=1/1。 a 水分子は明確にするために隠されていました。 b AgNPのみが表示されました
線状/星型共重合体およびそれらのミセル安定化AgNPのFTIR特性は、追加ファイル1:図S5に示されています。明らかに、単純な線形/星型共重合体と比較して、1730 cm -1 での-COOR伸縮振動 1457 cm -1 でのPDMAEMAのC-N結合の曲げ振動 AgNPの形成後に減少し、AgNPが共重合体ミセルに正常にロードされたことを示しています。線状/星型共重合体ミセルで安定化されたAgNPの結晶性は、X線回折スペクトルによって確認されました(追加ファイル1:図S6)。 38.5°、44.8°、64.2°、および78.0°の回折ピーク値は、面心立方(fcc)結晶構造の(111)、(200)、(220)、および(311)結晶面に対応していました。 Ag含有ナノ粒子の分析[33、34]。線形/星型共重合体ミセル安定化AgNPのゼータ電位を測定しました。図2に示すように、これらの共重合体ミセルで安定化されたAgNPのゼータ電位は約15.0〜23.2mVでした。さらに、AgNO 3 の量が増えるにつれて 、より多くのAgNPの装飾により、ミセル安定化AgNPのゼータ電位が著しく増加しました。 AgNPの分散と、AgNPに対するミセルの安定化効果をさらに調査するために、線形/スターコポリマーミセルのDPDシミュレーションにより、さまざまなPDMAEMA / AgNO 3 でAgNPが安定化されました。 モル比を実施した。図2に示すように、結果は、AgNPのサイズが、凝集した小さなAgNPの数が増加し、それらの間の距離が減少した比率に比例し、衝突と凝集の確率が高くなることも示しました。
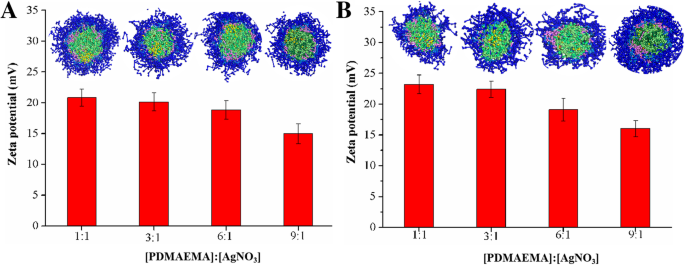
a のゼータ電位と断面図 線形および b スター共重合体ミセルはAgNPを安定化しました。データはさまざまなPDMAEMA / AgNO 3 で収集されました (a)1/1、(b)3/1、(c)6/1、(d)9/1のモル比
4つの線状共重合体ミセル安定化AgNPのスペクトルは、437 nm付近にある最大吸収ピークでわずかな違いがありました。これは、球形/ほぼ球形のAgNPの特徴的な表面プラズモン共鳴(SPR)吸収ピークであり、共鳴励起とバンド間遷移の両方に関連しています。それら(図3a)。結果は、線状共重合体の第三級アミン基が硝酸銀と反応でき、AgNPの形成が線状共重合体ミセルの立体障害にほとんど依存しないことを証明しました。続いて、同じ条件下で同様のブロックおよび重合度を有する星型コポリマーは、PDMAEMA / AgNO 3 の場合、AgNPの粒子サイズが減少した。 モル比が増加しました。これは、UV-Visスペクトルの浅色シフトに反映され、3級アミンでの配位還元によって形成されるAgNPの量が異なるため、最大吸収ピークはそれぞれ429 nm、426 nm、421 nm、および414nmにありました。スターコポリマーミセルの合成(図3b)。言い換えれば、スターコポリマーの立体安定化は、AgNPをよりよく安定させ、少量のAgNPでのさらなる凝集を防ぐことができます。対照的に、AgNPの量の増加は安定化効果を弱め、AgNPの衝突の機会を増やし、最終的にAgNPを大きくしました。図3aと図3bを比較すると、線状共重合体ミセル内のAgNPの437 nmでの吸収ピークはより広い波長分布を持っていましたが、星型共重合体ミセル内のAgNPは約422nmでした。ここでは、線状共重合体のスペクトルに青方偏移は見られませんでした。これは、線状共重合体ミセルのブロックがAgNPの立体障害に及ぼす影響が弱く、その結果、 AgNP。
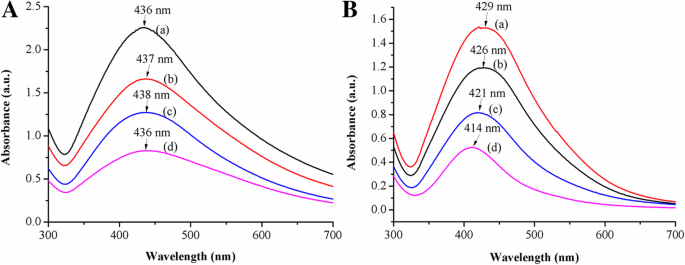
a のUV-Visスペクトル 線形および b スターコポリマーミセルは、異なるPDMAEMA / AgNO 3 でAgNPを安定化しました (a)1/1、(b)3/1、(c)6/1、(d)9/1のモル比
次に、TEM測定を実行して、AgNPのサイズ、サイズ分布、および形態を決定しました。 AgNPのTEM画像はAgNO 3 に依存していました 給餌率を図4に示した。PDMAEMA/ AgNO 3 の場合 モル比は6と1で、ImageJソフトウェアを使用して計算すると、線形共重合体ミセル安定化AgNPの粒子サイズは11.1nmと25.7nmでしたが、星型共重合体ミセル安定化AgNPの直径はそれぞれ3.7nmと6.4nmでした。 AgNO 3 の増加 含有量はミセル中のより多くの銀原子、より高い表面エネルギーをもたらし、凝集したAgNPの数はそれに応じてAgNPのサイズが大きくなるにつれて増加します。ミセルで安定化されたAgNPは単分散で球状であり、線形共重合体ミセルで安定化されたAgNPはやや不均一であることが明らかでした。ミセルで安定化されたAgNPのサイズは、UV-Visの結果をさらに補完しました。

TEM image of a 、 b linear copolymers and c 、 d star copolymers micelles stabilized AgNPs at different PDMAEMA/AgNO3 molar ratios:a 、 c 6/1, b 、 d 1/1
Stability of the Linear/Star Copolymers Micelles Stabilized AgNPs
The stability of the linear/star copolymers micelles stabilized AgNPs is of great influence for the development of biomedical field. Obviously, the SPR peak in UV-Vis spectra (Fig. 5) of star copolymer micelles stabilized AgNPs did not display any significant changes for at least 1 month even after further diluted by one time, three times, and six times, indicating that the prepared AgNPs appeared well long-term colloidal stability within the experimental concentration range. However, the results of linear copolymer micelles stabilized AgNPs showed that the UV absorption wavelength decreased slightly as the increase of dilution ratios. And the micelles concentration of linear copolymer decreased after 1 month of placement may lead to insufficient provision of steric hindrances to stabilize AgNPs.
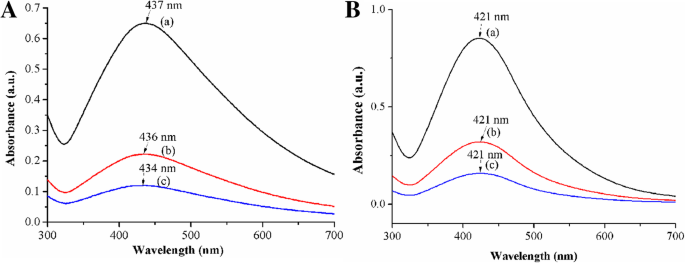
UV-Vis spectra of a linear copolymers and b star copolymers micelles stabilized AgNPs solution at PDMAEMA/AgNO3 molar ratio =6/1 after 1 month at the diluted times of 1 (a), 3 (b), and 6 (c), respectively
From the thermogravimetric analysis curves in Fig. 6, it was shown that the initial decomposition temperature (T onset ) of linear copolymers micelles was 217 °C, which shifted to 172 °C after silver loading, suggesting that the linear copolymer micelles stabilized AgNPs showed lower thermal stability than the pure linear copolymers micelles. It may be due to the fact that the chemical structure of PDMAEMA in the molecular chain changes and the catalytic effect of AgNPs in the thermal degradation process cannot be ignored [35]. As for star copolymers and their stabilized AgNPs, T onset were around 213 °C. The two Tonset of star copolymers micelles and their micelles stabilized AgNPs showed very few gaps, which could be speculated that the more stable star-shaped copolymers have better effect on stabilizing AgNPs than the linear copolymers. Combined the results of UV-Vis, TEM, and TGA measurements, it could be inferred that compared to the linear copolymers, the star copolymers have superior advantages in topology for stabilizing AgNPs, such as better stability, more uniform dispersion, slower nucleation rate during reduction, and the better product with a smaller and more uniform size of AgNPs.
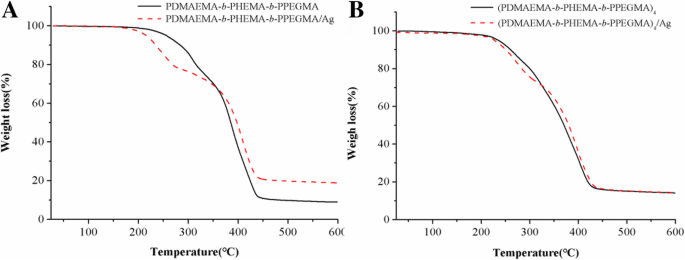
TGA curves of a linear copolymers and b star copolymers micelles and their micelles stabilized AgNPs at PDMAEMA/AgNO3 molar ratio =6/1
Antibacterial Activity and Cell Viability
To evaluate the antibacterial activities of the linear/star copolymers micelles stabilized AgNPs by optical density (OD600 ) measurements, E 。 coli DH5α was selected as the Gram-negative bacterial model. The absorbance at 600 nm after incubation was tested by incubating the bacteria with the eight different concentrations of micelles and micelles stabilized AgNPs at 37 °C. Results shown in Fig. 7a illustrated that the bacterial growth curves were highly correlated with the AgNPs concentration in the LB medium. The inhibition of linear/star copolymers micelles on the growth of bacteria was weak, which was not fatal to bacteria. However, as the concentration of linear/star copolymers micelles stabilized AgNPs increased, the survival rate of E 。 coli DH5α was significantly inhibited, indicating a strong antibacterial efficacy of AgNPs against E 。 coli DH5α. The concentrations of linear copolymers micelles stabilized AgNPs preventing the bacterial growth in the experiments were relatively higher than those of star copolymers micelles stabilized AgNPs, which might due to the fact that bigger size of AgNPs could lead to a lower antibacterial performance because of the inefficient exposure of bacteria to AgNPs and relatively slow release behavior of AgNPs.
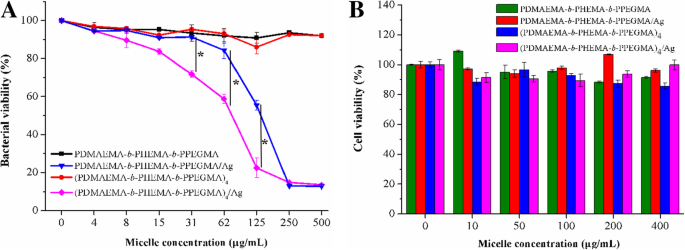
a Antibacterial activity and b cell viability of linear copolymers and star copolymers micelles stabilized AgNPs at PDMAEMA/AgNO3 molar ratio =6/1. *p <0.05, two-tailed Student t テスト
Cancer is an uncontrollable disease of cell growth that can occur in any part of the body. The most common cancers are liver cancer, breast cancer, colorectal cancer, and lung cancer. Among them, the liver cancer has the much higher prevalence in both developed and developing countries. Therefore, the toxicity experiments of the linear/star copolymers micelles stabilized AgNPs on HepG2 cells were carried out, in which HepG2 cells were incubated with linear/star copolymers micelles stabilized AgNPs at different concentrations (10, 50, 100, 200, 400 mg/L, respectively) for 48 h and the cell viability with MTT assay was the most intuitive data to evaluate the biocompatibility of the composite material. As shown in Fig. 7b, the percentage of viable cells for the linear/star copolymers micelles stabilized AgNPs exhibited negligible cytotoxicity, and was about 90% viability even at the highest concentration applied (400 μg/mL) after 48-h incubation, indicating the advantageous cytocompatibility of the micelles stabilized AgNPs within a relatively wide range of concentration.
Conclusion
In conclusion, PDMAEMA-based linear and star copolymer micelles as effective delivery carriers for silver-bearing antimicrobials were developed, and their in vitro antimicrobial efficacy and cell viability were investigated. Being a reducing agent and a stabilizer simultaneously, the micellar PDMAEMA core acted as loading platform for AgNPs in situ translated from the precursor silver nitrate. In silico simulation and experimental results indicated that both types of the copolymer micelles could generate monodisperse and spherical AgNPs. Compared with linear copolymers sliver-bearing micelles, the fabricated star copolymers micelles stabilized AgNPs exhibited smaller average size, better stability against dilution and pyrogenic decomposition, and enhanced antibacterial activities against E 。 coli DH5α due to the serious damage of bacterial membrane caused by loaded AgNPs. Moreover, both types of copolymer micelles stabilized AgNPs possessed great cytocompatibility toward HepG2 cells. Therefore, these studies may provide some guidance for the construction of more effective AgNPs weapon with well-defined and feasible polymer topology for combating the multiple bacteria-induced infections.
データと資料の可用性
現在の研究中に使用および/または分析されたデータセットは、合理的な要求に応じて対応する著者から入手できます。
略語
- AgNPs:
-
銀ナノ粒子
- DMAEMA:
-
2-(dimethylamino) ethyl methacrylate
- HEMA:
-
2-hydroxyethyl methacrylate
- PEGMA:
-
Poly (ethylene glycol) methyl ether methacrylate
- CuBr2 :
-
Cupric bromide
- 1 H NMR:
-
Proton nuclear magnetic resonance
- FTIR:
-
Fourier-transform infrared spectroscopy
- KBr:
-
Potassium bromide
- UV-Vis:
-
Ultraviolet-visible
- MTT:
-
3-(4,5-ジメチルチアゾール-2-イル)-2,5-ジフェニルテトラゾリウムブロミド
- HepG2:
-
Liver hepatocellular carcinoma
- DPD:
-
Dissipative particle dynamics
- SPR:
-
Surface plasmon resonance
- XRD:
-
X線回折
ナノマテリアル
- コバルトをドープしたFeMn2O4スピネルナノ粒子の調製と磁気特性
- TiO2ナノ流体に向けて—パート1:準備と特性
- 小さなセレンナノ結晶とナノロッドの容易な合成と光学的性質
- Sb /パリゴルスキー石(PAL)ナノ粒子の調製と強化された接触水素化活性
- HT29およびSPEV細胞株に対するAuナノ粒子の影響のinvitro研究
- invitroおよびinvivoでのグラフェンおよび酸化グラフェンのバイオセーフティおよび抗菌能力
- 中空構造LiNb3O8光触媒の調製と光触媒性能
- 磁性ポリ(N-イソプロピルアクリルアミド)ナノコンポジット:抗菌特性に及ぼす調製方法の影響
- Cu2ZnSnSe4ナノプレートのワンポット合成とそれらの可視光駆動光触媒活性
- 黄色ブドウ球菌のメチシリン耐性菌株に対するその場で調製されたキトサン/銀ナノ粒子溶液の抗菌活性
- 球状およびサンドイッチ構造のグラフェン/ Sio2サポートによる超高分子量ポリエチレン/グラフェンナノコンポジットのinsitu重合の調製



