一本鎖DNA検出用の磁気グラフェン電界効果トランジスタバイオセンサー
要約
本明細書では、磁気グラフェン電界効果トランジスタバイオセンサーは、化学蒸着グラフェンフィルムをガラス基板上に転写して、感知フィルムおよび導電性チャネルを生成することによって調製された。 1-ピレンブタン酸スクシンイミジルエステルをアンカーとしてグラフェンフィルムに固定することにより、磁気標識された相補的な一本鎖DNAを捕捉するために、プローブアプタマーをグラフェンフィルムに固定化しました。我々の実験は、周期的な磁場内で、バイオセンサーのインピーダンスが周期的な振動を示し、その振幅が相補的DNA濃度と相関していることを示した。この原理に基づいて、磁気グラフェン電界効果トランジスタを使用して、1pMの検出制限で一本鎖DNAを検出しました。結果は、磁力によってDNA鎖が曲がり、それによってグラフェントランジスタの二重導電層の磁性ナノビーズ/ DNA変調が生じるモデルを使用して合理化されました。さらに、周期的な磁場を導入してMGFETの周期的なインピーダンス変化を生成できるため、サンプリング統合を使用して、外部磁場の周期数を増やすことにより、信号対雑音比を効率的に改善できます。そのため、この研究では、高感度のDNA検出用の新しいバイオセンサーを紹介しました。検出原理に基づいて、このシステムは、他の生体分子、細胞などを検出するための潜在的なツールになる可能性もあります。
はじめに
DNAの検出は、分子生物学の研究や遺伝病の診断にとって非常に重要です[1,2,3]。現在までに、蛍光バイオセンサー[4、5]、電気化学バイオセンサー[6、7、8、9]、電界効果トランジスタ(FET)バイオセンサー[10、11、12、13]など、DNA検出用のさまざまなバイオセンサーが開発されています。 ]、後者はその高い感度と特異性のために広く注目されています。 Kaisti etal。 [12]は、ペプチド核酸プローブを使用して非標識一本鎖DNAを検出するためのFETバイオセンサーを開発しました。キムら[13]標準的な相補型金属酸化膜半導体技術に基づいてFETタイプのDNA電荷センサーを製造しました。
その高い比表面積、高い電気伝導率、および優れた電子移動度により、グラフェンは、FETバイオセンサーの製造に理想的な材料であると言われています[14、15、16]。カイら[15]は、ペプチド核酸DNAハイブリダイゼーションを介してDNAを超高感度で検出するためのグラフェンFET(GFET)バイオセンサーを開発しました。私たちのグループはまた、DNAハイブリダイゼーションと単一塩基のミスマッチの結合速度と親和性を決定するためのマルチチャネルGFETバイオセンサーを提案しました[16]。
従来のGFETでは、外部ゲート電極電界により、グラフェン膜と溶液電解質の間の界面に二重導電層が生成されます[17、18、19]。 GFETのキャプティブモデル[16]に基づいて、ゲート電極は電解質を通して二重導電層を充電および放電し、それによってGFETの導電性を変調します。したがって、GFETの導電率は、外部電界の強度と電解質中のイオン濃度に関係しています。
調査中に、GFETの感度に関する調査がfMレベルに達していることがわかりました。たとえば、Ping etal。 [20]およびZhengetal。 [21]は、fMレベルの検出限界を持つ従来のGFETバイオセンサーを報告しています。しかしながら、上記の文献は、半導体分析器の検出によって非常に高い感度を達成しており、これは、高価であり、実際の用途には不便である。さらに、Ag / AgCl電極は一般的に外部ゲート電極として使用されますが、そのサイズと再利用性のために、統合型バイオセンサーの構築には適していません。
ここでは、電場ではなく磁場を利用してGFETの導電率を変調する磁気GFET(MGFET)バイオセンサーが開発されました。導電性チャネルは、2つのインジウムスズ酸化物(ITO)電極を備えたガラス基板上に転写された化学蒸着(CVD)グラフェンフィルムを使用して実現されました。グラフェンフィルムは、1-ピレンブタン酸スクシンイミジルエステル(PBASE)で機能化され、プローブアプタマーの結合を可能にして、相補的な磁気標識された一本鎖DNA(cDNA)を捕捉してハイブリダイズさせました。 MGFETの裏側に周期的な磁場を印加することで、周期的なMGFETの電気インピーダンスが達成されました。さらに、周期的磁場におけるMGFETの電気インピーダンス変動は、cDNAの濃度に関連していた。対応するラボ製の検出デバイスは、MGFETインピーダンスをリアルタイムで検出するために構築されました。磁場はMGFETと直接接触していないため、ここで準備されたMGFETは、従来のGFETバイオセンサーよりも統合および適用が容易です。このホワイトペーパーでは、MGFETの準備、ラボで作成された検出システムの構築、および検出原理についてすべて詳しく説明しました。
メソッド
材料と器具
ITO電極を備えたガラス基板はHuaNan Xiang Cheng Ltd.(中国)から購入しました。プローブアプタマー、cDNA、およびミスマッチDNAは、Sangon Biotech Inc.(上海、中国)から購入しました。プローブアプタマーの配列は(5'-NH 2 -TGG ACC CCC TCA TAA CGC CTC CTT TTC-FAM-3 ')、相補DNAの配列は(5'-NH 2 -GAA AAG GAG GCG TTA TGA GGG GGT CCA-3 ')、完全にミスマッチのDNAの配列は(5'-NH 2 -TCC CCT TCT TAT GGC CTG TTT TTC AAC-3 ')、および一塩基ミスマッチDNAの配列は(5'-NH 2 -GAA AAG GAG TCG TTA TGA GGG GGT CCA-3 ')。 PBASEおよびジメチルスルホキシド(DMSO)は、Sigma-Aldrich(上海、中国)から入手しました。カルボキシル基(10 mg / mL)で修飾された磁性ナノビーズ(MB)は、Xianfeng Nano Material Technology Co.、Ltd。(Nanjing、China)から入手しました。 1-エチル-3-(3-ジメチルアミノプロピル)カルボジイミド塩酸塩、N-ヒドロキシスクシンイミド、ドデシルベンゼンスルホン酸ナトリウム(SDS)、およびドデシル硫酸ナトリウムリン酸緩衝生理食塩水(PBS、P5368-10PAK; pH 7.4)は、Sigma-Aldrich(上海)から購入しました。 、中国)。
ラマン顕微鏡システム(SPEX-1403、SPEX)を使用して、グラフェンの品質を評価し、MGFETの機能化を検証しました。蛍光光度計(LS55、PerkinElmer)を使用して、磁性ナノ粒子のcDNAへの結合を特徴付けました。ラボで作成されたデータ取得システムを使用して、MGFETのインピーダンスをリアルタイムで記録しました。
cDNAをMBに結合する
超音波で20分間均一に分散させた後、カルボキシル基で修飾されたMBの20μL懸濁液を200μLの1-エチル-3-(3-ジメチルアミノプロピル)カルボジイミド塩酸塩(2 mg / mL)および200μLのN-ヒドロキシスクシンイミド(2 mg / mL)を15分間使用して、活性化されたMBを取得します[22、23]。次に、20μLのcDNA溶液をMBs溶液に加え、室温で2時間穏やかに振とうしながらインキュベートしました。次に磁場を導入して、MBを介してcDNAサンプルを濃縮しました。磁性ナノビーズ/ DNA(MB / cDNA)コンジュゲートをPBSで3回洗浄し、将来の使用のためにPBSに分散させました。
MGFETの製造
MGFETの準備については、以下で詳しく説明します。最初に、前述のように[18、19]、CVDグラフェンフィルムを2つのITO電極間の導電性チャネルとしてガラスプレートに転写しました(図1a)。次に、DMSOに溶解したPBASE(10 mM)をMGFETに室温で12時間注入し、π–πスタッキングによってグラフェンと完全に反応させました(図1b)。次に、MGFETをDMSOとPBSで連続して洗浄し、未反応のPBASEをすべて除去しました。第三に、2μMのプローブアプタマーをMGFETに導入し、PBASEと室温で4時間インキュベートして、プローブアプタマーがPBASEと十分に反応できるようにしました(図1c)。次に、MGFETをそれぞれ0.2%SDSで3回洗浄して、結合していないプローブアプタマーをすべて除去しました。
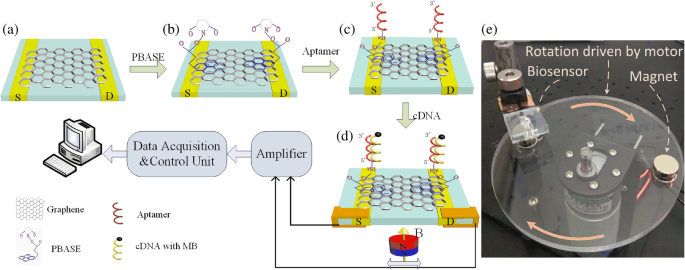
MGFETの機能化と検出原理。 a 化学蒸着によって成長したグラフェン膜。 b PBASEによるグラフェンの機能化。 c PBASEを介したプローブアプタマーの固定化。 d プローブアプタマーとcDNAのハイブリダイゼーション。 e 検出装置の写真
結果と考察
MGFETの特性評価
CVD法で製造されたグラフェン膜は、2つのITO電極間の導電性チャネルとしてガラス基板上に転写されました(図1a)。転写されたグラフェン膜は、ラマンスペクトルで特徴づけられました(図2)。グラフェンの3つの特徴的なピークの出現は、グラフェン膜のガラス基板への転写が成功したことを示しています[24、25]。 2DバンドとGバンドの強度比(I 2D / I G )は、転写されたグラフェンが多層膜であることを示しました[26]。さらに、DバンドとGバンドの強度比(I D / I G )は小さく、欠陥密度が非常に低いことを示しています。
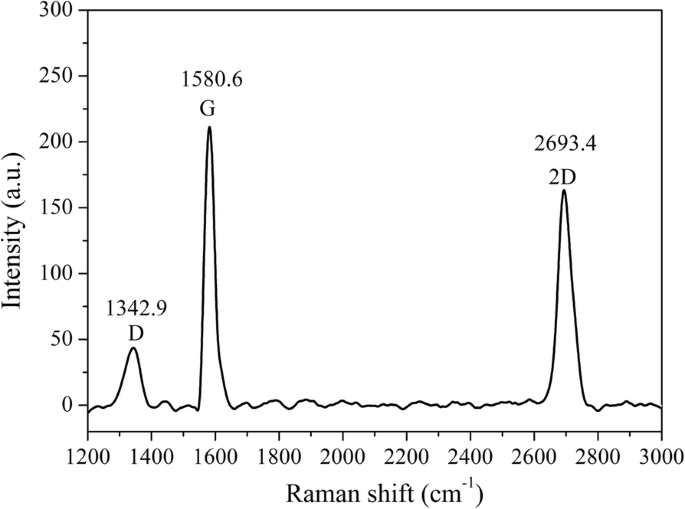
ラマンスペクトル
官能基が不足しているため、CVDグラフェン膜上でアプタマー鎖を修飾することは困難でした。したがって、その芳香族ピレニル基に基づいて、PBASEはリンカーとしてπ–πスタッキングを介してグラフェンフィルム上で修飾されました。 PBASEのもう一方の端では、PBASEのスクシンイミド部分を5'-NH 2 に結合させることができます。 N-ヒドロキシスクシンイミド(NHS)架橋反応に基づく標識プローブアプタマー(図1c)。グラフェンフィルムへのプローブアプタマーの結合を評価するために、プローブアプタマーの3 '末端をFAMフルオロフォアを使用して標識しました(配列:5'-NH 2 -TGG ACC CCC TCA TAA CGC CTC CTT TTC-FAM-3 ')。アプタマーを導入した直後に、蛍光強度が明らかに増強され、グラフェン表面での修飾が成功したことを示しています(図3)。プローブアプタマー濃度を上げると、蛍光強度が増加し、一定値に達するため、MGFETのプローブアプタマーが約2μMで飽和していることを示します。したがって、その後の実験は、2μMのプローブアプタマー濃度で実行されました。
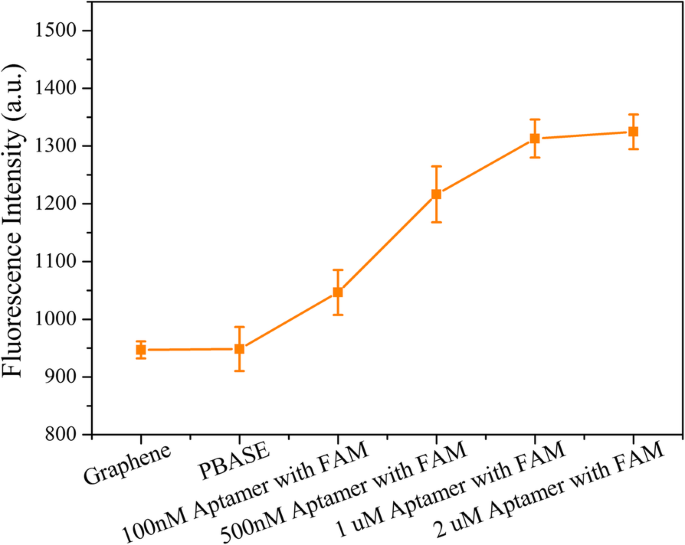
プローブアプタマーによるMGFET修飾の特性評価。エラーバーは、5つの独立した分析の標準偏差を表します
MB / cDNAの特性評価
MBおよびMB / cDNAコンジュゲートの形態は、透過型電子顕微鏡(TEM)によって特徴づけられました(図4a、b)。 MBの粒子サイズ分布は、約7 nmの平均粒子サイズを示しました(図4c)。 cDNAのバイオセンシングの感度と精度を確保するために、cDNAを完全に捕捉するためにMBはcDNAに対して過剰である必要があります。ここで使用するcDNAサンプルへの結合を確実にするために、4 mg / mLの濃度のMBを活性化しました。 FAMによるcDNAの標識により、蛍光強度を利用してカップリング効率を特徴付け、cDNA濃度を最適化しました(図4d)。実際、cDNA溶液にMBを導入すると、上清の蛍光強度が明らかに低下し、cDNAがMBによって捕捉および濃縮されたことを示しています。 MBによるcDNAの捕捉の成功は、10 nMのcDNA濃度で、上清の蛍光強度がPBSの蛍光強度と同等であり、すべてのcDNAがMBによって捕捉され、濃縮されたことを示す観察によって確認されました(図4d 。
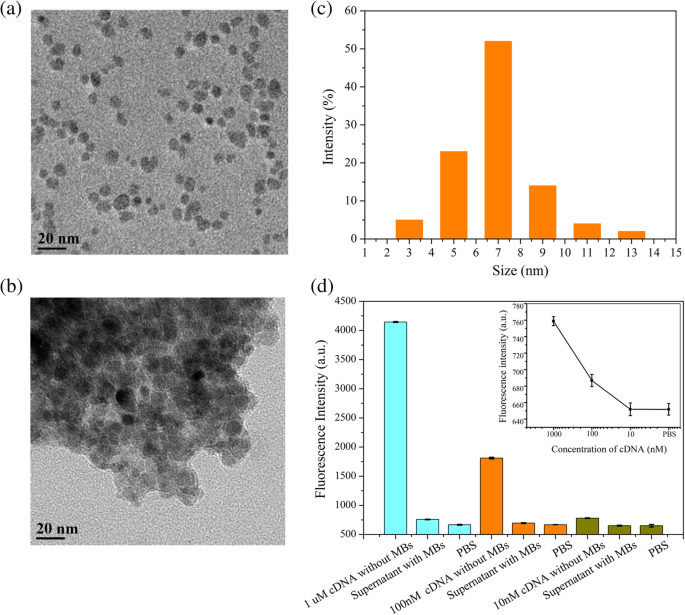
MB / cDNAカップリングの特性。 a MBのTEM。 b MB / cDNAコンジュゲートのTEM。 c MBの粒度分布。 d MB / cDNA(FAM)カップリングの特性評価。エラーバーは、5つの独立した分析の標準偏差を表します
磁場の強さの分析
MB / cDNAコンジュゲートをMGFETに10分間添加して、プローブアプタマーとの完全なcDNAハイブリダイゼーションを可能にしました。プローブアプタマーは修飾アミノ基なしではMBと結合できなかったため、過剰なMBは、MGFETをPBSで3回洗浄することで除去できました。したがって、MB / cDNAコンジュゲートのみがMGFETに残されました(図1d)。永久磁石を回転モーターに取り付けて、MGFETに周期的な磁場を印加しました(図1e)。実験室で作られた検出装置を使用して、MGFETのインピーダンス変動を記録しました。
MGFETのインピーダンスはバックゲートとしての磁場によって変調されるため、磁場強度とMGFETのインピーダンスの相関関係を調査して、磁場強度パラメーターを最適化しました(図5)。グラフェンと電解質の間に形成される二重導電層は、外部電界によって変調され、それによってGFETの導電性が変調されると一般に考えられています[19、27、28]。 MGFETでは、MBと磁場の間の磁力によって、MB / cDNAコンジュゲートとグラフェン膜の間の距離が機械的に制御され、それによってMGFETの二重導電層が変調されました[29、30]。 MGFETバイオセンサーのインピーダンスは、磁場強度の増加に伴って3段階で変化しました。これは、MB / cDNAチェーンを弾性の細いロッドとして使用することで説明できます[31]。この作業では、最初の段階は100mT未満の磁場強度で発生しました。 DNA鎖の弾性細棒モデルに基づくと、磁場力はDNA鎖の半径方向の支持力よりも小さいため、磁場力によってDNA鎖を曲げることは困難です。したがって、MGFETは磁場に敏感ではありません。磁場の強さが100〜200 mTの第2段階では、磁場の強さはDNA弾性細いロッドの半径方向の支持力に打ち勝つのに十分であり、MB / cDNAが急速に曲がり、その後、磁場へのMGFET。最後に、磁場強度が220 mTを超える第3段階では、DNA弾性ロッドの曲げが限界に達します。したがって、MGFETは磁場の変化に応答せず、図5bに示すようにMGFETのインピーダンスが安定します。
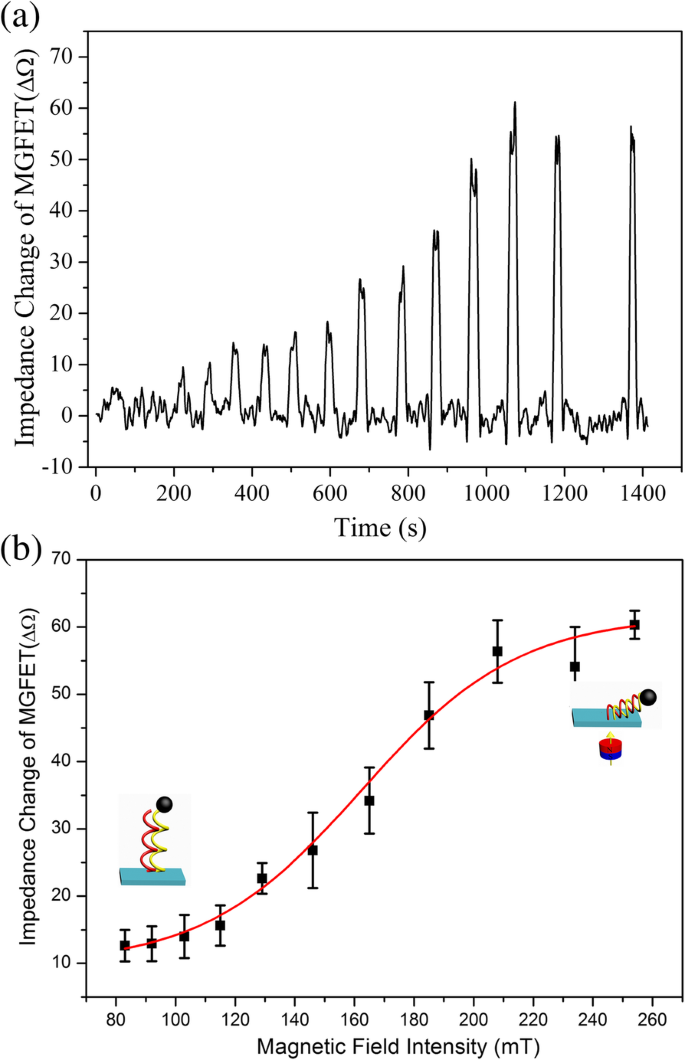
MGFETのインピーダンスに対する磁場強度の影響。 a 時間領域で変化する磁場強度の下でのMGFETのインピーダンス。 b MGFETのインピーダンスと磁場の強さの関係。エラーバーは、5つの独立した分析の標準偏差を表します
cDNAの検出
MB / cDNAコンジュゲート濃度を変化させたときのMGFETインピーダンスの変化を、240 mTの固定磁場強度で測定し、cDNA検出の実現可能性と感度を決定しました。
各cDNA濃度でのMGFETインピーダンスは、リアルタイムで記録されました(図6a)。永久磁石がMGFETの背面にロードされると、インピーダンスが急速に増加しました。逆に、周期的な磁場をかけると、インピーダンスの周期的な変化が観察されました。このインピーダンスの周期性に基づいて、サンプル積分アルゴリズム(SIA)を使用して、MGFETの信号対雑音比を向上させました。磁場をかけない期間を考えると、T 0 磁場をかけた期間はT M (図6a)、SIAは次の手順で記述できます。(1)T 0 中 、ノイズによって生成されたすべてのデータポイントはゼロに正規化されました。(2)各T M の間に取得されたデータポイント 期間は順番にサンプリングされ、平均化されました。 4サイクルにわたるSIA処理の後、図6bに示すように、MGFETの周期的なインピーダンス変化が得られました。理論的には、MGFETの信号対雑音比は、十分に長いサンプリング時間を使用して効果的に改善できます。
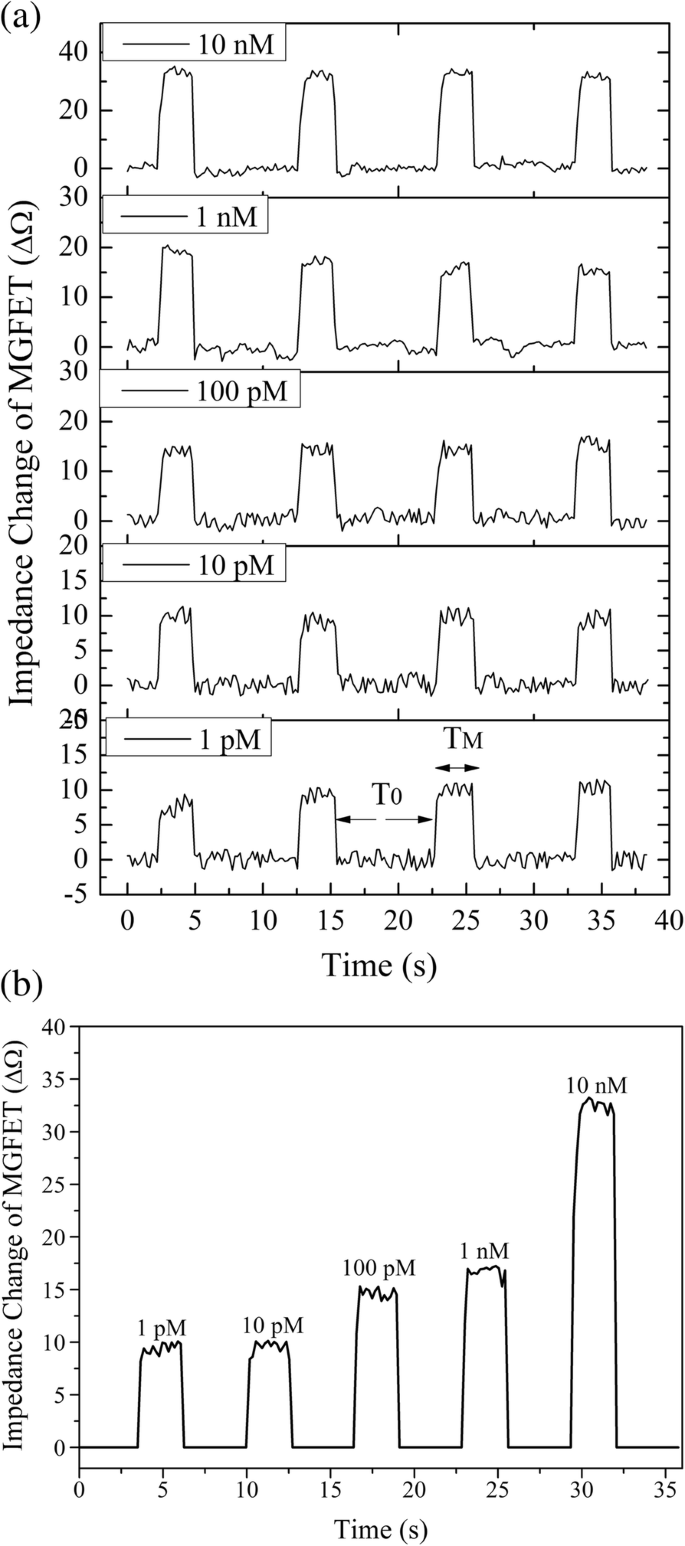
a 異なるcDNA濃度でのインピーダンス変動の時間領域。 b cDNA濃度に応じたMGFETのインピーダンス変化
MGFETのインピーダンス変化は、cDNA濃度と正の相関がありました(図6b)。 MGFETのインピーダンス変化とcDNAの濃度との相関関係を評価しました(図7)。この作業でのMGFETバイオセンサーの高感度は、主に次の2つの側面に基づいています。1つは、MB / cDNAコンジュゲートの機械的な動きが、DNAのみの場合と比較して、二重導電層の変調効果を高める可能性があることです。サンプリング積分の原理に基づいて、周期的な磁場を適用してMGFETの周期的なインピーダンス変化を生成できるため、磁場を伴うMGFETインピーダンスのみをサンプリングして積分し、ノイズを低減しました。したがって、外部磁場の周期数を増やすことで、システムの信号対雑音比を大幅に最適化できます。
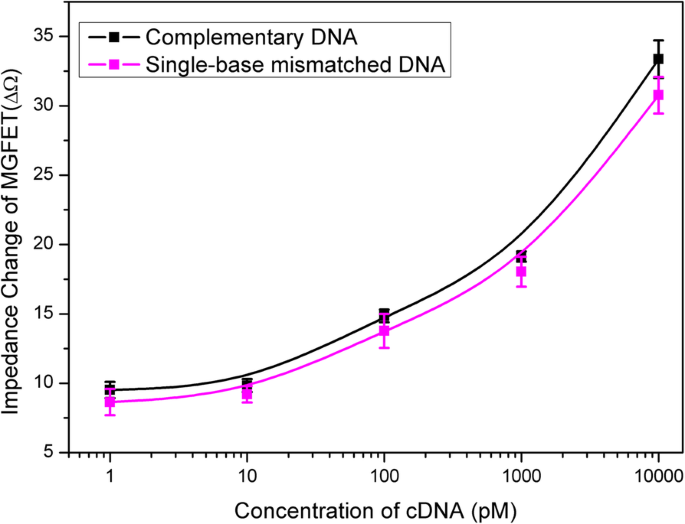
MGFETのインピーダンスとターゲットDNAの濃度の関係。エラーバーは、5つの独立した分析の標準偏差を表します
MGFETの選択性
MGFETの特異性は、完全にミスマッチのDNA鎖と単一塩基のミスマッチのDNA鎖を含む、2つの異なる標的DNA配列を検出することによって評価されました。上記の手順と同様に、完全にミスマッチのDNA(配列:5'-NH 2 -TCC CCT TCT TAT GGC CTG TTT TTC AAC-3 ')および一塩基ミスマッチDNA(配列:5'-NH 2 -GAA AAG GAG TCG TTA TGA GGG GGT CCA-3 ')はそれぞれMBに結合されました。 PBS溶液に溶解したミスマッチのMB / DNAをMGFETバイオセンサーに10分間添加して、アプタマーと十分に反応させました。 MGFETをPBSで3回洗浄して、ミスマッチDNAを除去しました。完全にミスマッチのDNA鎖の場合、MB / DNAのコンジュゲートはアプタマーとハイブリダイズできなかったため、ほとんどすべてのMB / DNAコンジュゲートが除去されました。したがって、図8に示すように、完全に不一致のMB / DNAを追加しても、グラフェンの導電率にはほとんど影響がありません。これは、バイオセンサーの選択性が高いことを示しています。さらに、図7に示すように、単一塩基のミスマッチDNA鎖を介したバイオセンサーの選択性も調査しました。単一塩基のミスマッチ鎖によるMGFETインピーダンスの変化は、相補鎖よりもわずかに低く、各特定の濃度の非相補的なターゲットストランド。したがって、この作業では、単一塩基のミスマッチ鎖を検出できる可能性があります。アプタマーと相補DNA鎖はすべて、主にバイオセンサーの選択性を決定する市販製品ですが、MGFETとその検出システムも、DNA検出の高感度に貢献しています。
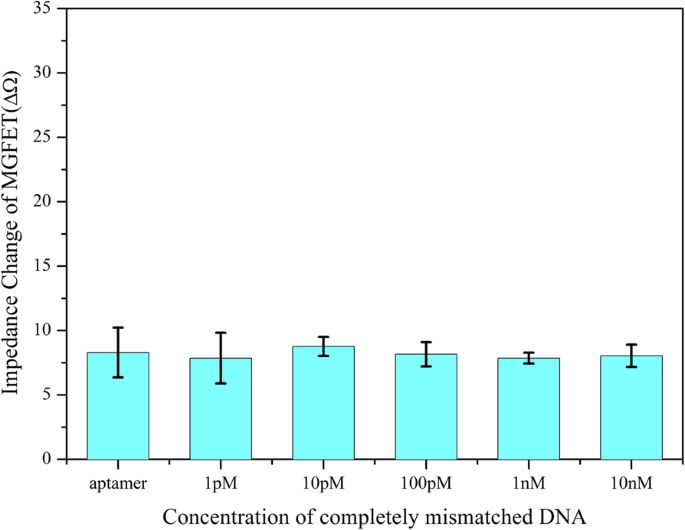
MGFETのインピーダンスと完全にミスマッチのDNAの濃度との関係。エラーバーは、5つの独立した分析の標準偏差を表します
結論
ここでは、cDNAを検出するためにグラフェンと磁性ナノ粒子に基づくMGFETバイオセンサーを紹介しました。 MGFETでは、磁性ナノ粒子がcDNA配列の最後に修飾されていました。 MBと磁場の間の磁力によって、MB / cDNAコンジュゲートとグラフェンフィルムの間の距離が機械的に制御され、それによってMGFETの二重導電層が変調されました。さらに、特定のDNA鎖の場合、MGFETのインピーダンスはDNA鎖の応力を反映し、それがDNA鎖の曲がりを反映すると結論付けることもできます(挿入図、図5b)。したがって、現在のMGFETは、DNA鎖の機械的パラメータの研究に使用される可能性があります。したがって、MGFETはcDNA検出用のバイオセンサーとして機能するだけでなく、DNA鎖の機械的パラメーターを検出する可能性もあります。
データと資料の可用性
この調査中に生成または分析されたすべてのデータは、記事に含まれています。
略語
- cDNA:
-
相補的な磁気標識された一本鎖DNA
- CVD:
-
化学蒸着
- DMSO:
-
ジメチルスルホキシド
- FET:
-
電界効果トランジスタ
- GFET:
-
グラフェン電界効果トランジスタ
- MB:
-
磁性ナノビーズ
- MGFET:
-
磁気グラフェン電界効果トランジスタ
- NHS:
-
N-ヒドロキシスクシンイミド
- PBASE:
-
1-ピレンブタン酸スクシンイミジルエステル
- PBS:
-
ドデシル硫酸ナトリウムリン酸緩衝生理食塩水
- SDS:
-
ドデシルベンゼンスルホン酸ナトリウム
- SIA:
-
サンプル統合アルゴリズム
- TEM:
-
透過型電子顕微鏡
- ITO:
-
インジウムスズ酸化物
ナノマテリアル
- ブログ:マイクロアレイによる遺伝子の検出
- 磁気センサー用ナノダイヤモンド
- 卵巣癌細胞の高感度かつ迅速な検出のための柔軟なグラフェンベースのバイオセンサーのデモンストレーション
- スーパーキャパシター用途向けのグラフェンおよびポリマー複合材料:レビュー
- 過酸化水素の選択的検出のためのデュアルモードナノセンサーとしてのカーボンナノドット
- アロワナの魚の性別を測定するためのアクリルゴールドナノコンポジットからの高感度電気化学DNAバイオセンサー
- 電気触媒作用のためのグラフェンナノシート上のMoS2ナノフレークの温度依存性結晶化
- ポリスチレン-co-アクリル酸複合ナノスフェアを用いたコレラ菌DNAの検出のための超高感度バイオセンサー
- ポリ(4-スチレンスルホン酸-co-マレイン酸)による金磁性ナノ粒子の安定性の向上:タンパク質検出用に調整された光学特性
- トランジスタの欠陥を検出するための高感度な方法
- 電界の検出と特性評価のためのソリッドステートセンサー



