誘電体変調デュアルソーストレンチゲートTFETバイオセンサーのシミュレーションと性能分析
要約
本論文では、生体分子の検出のために、バイオセンサーに基づく誘電体変調ダブルソーストレンチゲートトンネルFET(DM-DSTGTFET)を提案した。 DM-DSTGTFETは、オン状態電流を強化し、双方向電流を生成するために、ダブルソースおよびトレンチゲートを採用しています。提案された構造では、生体分子を充填するために2つの空洞が1nmのゲート酸化物上にエッチングされています。感度研究の分析には、Technology Computer-Aided Design(TCAD)の2Dシミュレーションが採用されています。結果は、低い供給電圧下で、DM-DSTGTFETの電流感度が1.38×10 5 と高いことを示しています。 、およびしきい値電圧感度は1.2 Vに達する可能性があります。したがって、DM-DSTGTFETバイオセンサーは、消費電力が低く、感度が高いため、アプリケーションの見通しが良好です。
はじめに
最近では、高感度、最小遅延、スケーリングされた寸法、および低コストという有望な特性により、シリコンベースの電界効果トランジスタ(FET)バイオセンサーに大きな研究関心が集まっています[1,2,3,4,5、 6]。 FETベースのバイオセンサーには熱電子放出の制限があり、サブスレッショルドスロープ(SS)は60 mV / decadeを超える可能性があります。バンド間トンネリング(BTBT)伝導メカニズムにより、TFETは制限を克服し、短チャネル効果を低下させます[7、8、9、10]。したがって、TFETベースのバイオセンサーは、FETベースのバイオセンサーよりも優れた感度と応答時間の適切な候補として浮上しています[11、12、13、14]。
分子検出に適用されるTFETの最も一般的な方法は、誘電変調に基づいています。ゲート誘電体材料の一部がエッチングされてキャビティが形成されます。生体分子が空洞に充填されると、空洞の誘電率が変化し、その変化がドレイン電流と伝達特性に反映されます[15、16、17]。同時に、誘電変調は、帯電した分子と中性分子の両方を検出するのに役立ちます。現在、誘電変調の概念は最近TFETで利用されており、誘電変調TFET(DMTFET)ベースのバイオセンサーは非常に価値のある研究者を魅了しています。ラベルフリー生体分子検出用のバイオセンサーとして機能するp-n-p-nTFETは、デバイスシミュレーションで研究されています。結果は、TFETベースのバイオセンサーが生体分子の非存在下で低いオフ状態電流を持ち、誘電率と電荷の両方に対して高い感度を持っていることを明らかにしています[18]。トンネル接合は効果的な結合につながる可能性があり、これにより高感度が得られ、DM-TFETは低次元での感度低下に耐えることができます。さまざまな構造のTFETベースのバイオセンサーが研究されています。従来のDGTFETと比較して、ショートゲート(SG)アーキテクチャをDMTFET構造に組み込むことで、感度を大幅に向上させ、コストを削減できます[20]。電荷プラズマベースのゲートアンダーラップ誘電体変調接合のないトンネル電界効果トランジスタ(CPB DM-JLTFET)は、適切なバイアスの下でトンネル接合の近くの空洞の長さと厚さを適切に選択することにより、最大の感度(中性および帯電生体分子)を得ることができます[21]。バイオセンサーの感度を向上させるために、高濃度にドープされたフロントゲートn +ポケットとゲートからソースへのオーバーラップが、垂直誘電変調トンネル電界効果トランジスタ(V-DMTFET)に導入されています[22]。円形ゲートヘテロ接合トンネル電界効果トランジスタは、ゲート構造が不均一であるため、均一ゲートHJTFETよりも高い感度を示します[23]。ダブルチャネルトレンチゲートTFETは、高い電流感度と法外な電圧感度を示します[24]。ダブルゲートおよびダブルメタル材料のTFETバイオセンサーは、感度の変化をより明白にすることができます[25]。
ただし、ほとんどのバイオセンサーはダブルゲートTFETに基づいており、生体分子は両端のゲートの側面から追加する必要があります。提案された構造では、生体分子はデバイスの上部から垂直に追加されます。これは、より簡単な操作です。さらに、ゲートとソースのオーバーラップ領域が大きいため、つまり、ソースと生体分子の相互作用が明らかな領域であるため、DM-DSTGTFETバイオセンサーの感度は、表1に示すように、他のデバイスよりも高くなります。この研究と他の参考文献の研究結果との間の異なる感度の比較。
<図>本論文では、DM-DSTGTFETバイオセンサーの感度を研究し、具体的な内容は以下の通りである。セクション2と3では、基本的なデバイス構造、製造プロセス、シミュレーションモデル、および方法について説明します。セクション4は、DM-DSTGTFETバイオセンサーの感度に対するさまざまな要因の影響を特徴づけます。具体的には、さまざまな誘電率、キャビティの厚さ、および帯電した生体分子が伝達特性、 I に及ぼす影響 on / 私 オフ 感度と△ V th 提案されたデバイスの感度。セクション5は、実施された調査からの調査結果をまとめています。
デバイス構造
図1は、DM-DSTGTFETベースのバイオセンサーの断面画像を示しています。 DM-DSTGTFETのゲート電極の仕事関数は4.2です。 TFETのオン状態電流を増加させるために、デュアルソース構造が利用されます。ドーピング濃度が1×10 20 の2つのソース領域 cm -3 ゲートの両側に対称的に配置されます。高さのあるpチャネル(H c )37 nm、ドーピング濃度1×10 15 cm -3 ソースとゲートの下にあります。ドーピング濃度が1×10 17 のnドレイン cm -3 と高さ( H d )18nmはチャネルの下にあります。ソース領域の2つの酸化物はHfO 2 です。 厚さ2nm。厚さの2つのポケット領域( T p )5 nmは、1×10 19 のドナードーピング濃度でゲートの両側に対称的に配置されます。 cm -3 。さらに、提案されたバイオセンサーについては、 T ox (1 nm)、 T c (5 nm)はHfO 2 の厚さです それぞれ、ゲート酸化物とナノギャップキャビティの幅。感度パラメータの適切な変更を容易にするために、選択されたゲート金属の仕事関数の値は、生体分子が空洞に蓄積したときにのみトンネリングが発生するようにする必要があります。そのため、金属の仕事関数Φ MS =4.2eV(HfO 2 以上 ゲート酸化物)が選択されます。ここで、異なる誘電率(1、2.5、5、11、23)と5つの異なる厚さのナノギャップキャビティ(5 nm、7 nm、9 nm、11 nm、13 nm)を持つ5つの異なるタイプの小さな生体分子が分析されます。提案されたバイオセンサー。
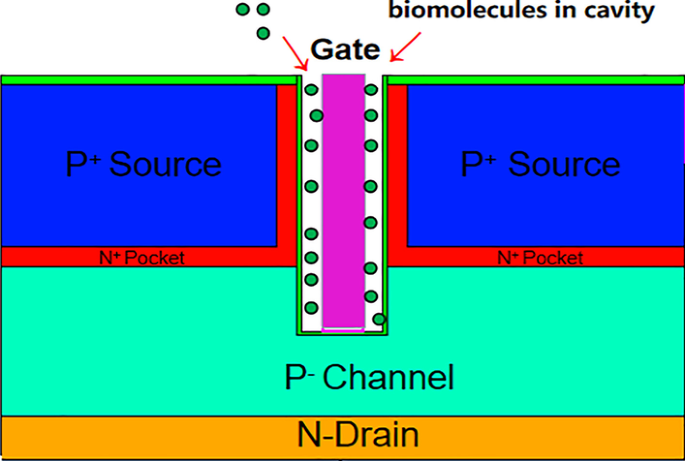
DM-DSTGTFETバイオセンサーの概略断面図
DM-DSTGTFETの製造方法は、公開されている[24]と同様です。図2は、提案されたDM-DSTGTFETの製造ステップを示しています。最初のステップでは、図2aに示すように、マスク、露光、エッチング、イオン注入、および低濃度にドープされたシリコン基板へのアニーリングにより、デバイスの下部にドレイン領域が形成されます。形成されたドレイン領域のドーピング濃度は10 17 / cm 3 、およびドーピングイオンはヒ素です。次に、本質的なシリコンがドレイン領域の上にエピタキシャル成長して、デバイスのチャネル領域を形成します。図2bに示すように、チャネルの上の2つのコーナーがエッチングで除去されます。同時に、N + ドーピングは、DM-DSTGTFETのポケット領域を形成するために、図2cで説明されているように化学蒸着(CVD)技術によって堆積されます。ソース領域では、化学蒸着(CVD)によってSiベースのデュアルソース領域が成長し、ソース領域でのP型高ドーピングに対して、ドーピングを使用して、マスキング、露光、エッチング、イオン注入、およびアニーリングが実行されます。 10 20 の濃度 / cm 3 、図2dに示すように。次のステップでは、チャネル層とSiO 2 にトレンチを作成します。 図2eに示すように、トレンチ内に堆積します。次に、図2fに示すようにトレンチが形成されます。図2gに示すように、金属化とパターニングを行ってゲート接点を取得します。さらに、空洞はSiO 2 に刻まれています 図2hに示すように、ゲートの両側にあります。最後のステップでは、1 nm HfO 2 図2iに示すように提案された構造を得るために空洞の側壁に成長します。
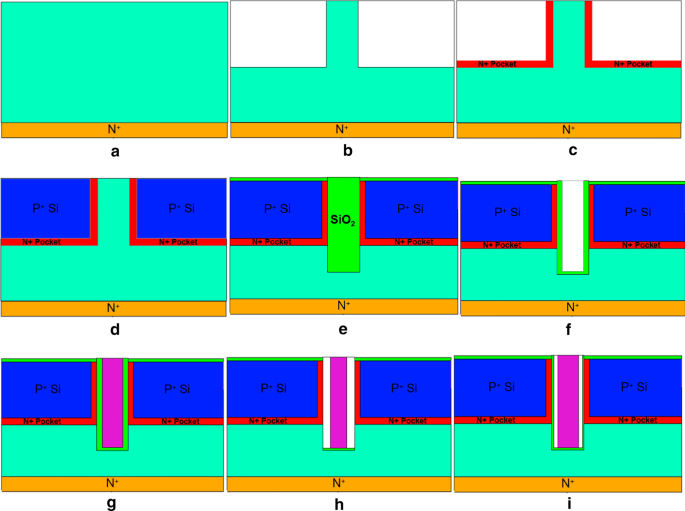
バイオセンサーとしてのDM-DSTGTFETの製造フロー
シミュレーションの方法とモデル
DM-DSTGTFETバイオセンサーの性能をより明確に研究する目的で、この論文はTCADツール(sentaurus)を利用してTFETセンサーの感度を研究します。正確なシミュレーションのために適切なモデルが採用されています。
非局所BTBTモデルは、トンネリングパスの各ポイントでの電界を変数と見なします。つまり、BTBTトンネリングの確率は、トンネリング接合部でのバンドの曲がりに依存します。非局所トンネリングモデルは、TFETシミュレーションの実際の状況とより一致しています[29]。したがって、この論文では非局所的BTBTモデルを採用している。ケインモデルは、sentaurusの動的な非ローカルBTBTトンネリングモデルに使用されます。ケインモデルでは、BTBTトンネリングの速度は[30]:
として表されます。 $$ G _ {{{\ text {BTBT}}}} =A \ left({\ frac {E} {{E_ {0}}}} \ right)^ {P} \ exp \ left({-\ frac {B} {{E_ {0}}}} \ right)$$(1)ここで、定数 E 0 =1V / cm、直接バンドギャップトンネリングの場合はP =2、 P フォノン支援の間接バンドギャップトンネリングの場合は=2.5。このホワイトペーパーのデバイスは主にシリコンであるため、 P 2.5を選択します。パラメータ A =4×10 14 / cm 3 s、 E は電界と指数因子 B =9.9×10 6 V / cm。
Shockley–Read–Hall(SRH)は、キャリアの再結合を含むように選択されています。バンドギャップ狭小化モデルは、バンドギャップの高濃度効果を活性化するために採用されています。フェルミ-ディラック統計は、高濃度にドープされた領域の特性の変化を含めるために呼び出されます。 Si材料の移動度モデルでは、イオン化不純物( µ )の散乱モデルを考慮する必要があります。 dop )、界面散乱モデル( µ InterSc )および高磁場飽和モデル( µ F )[31]であり、最終的な実効モビリティモデルは次のように表すことができます。
$$ \ frac {{1}} {\ mu} =\ frac {{1}} {{\ mu _ {{{\ text {dop}}}}}} + \ frac {1} {{\ mu _ {{ {\ text {InterSc}}}}}} + \ frac {1} {{\ mu _ {{\ text {F}}}}} $$(2)プール-フレンケル移動度モデルは、空洞を埋める材料に導入され、電界の関数としての移動度は次の式で与えられます。
$$ \ mu =\ mu_ {{0}} \ exp \ left({-\ frac {{E_ {0}}} {KT}} \ right)\ exp \ left({\ sqrt E \ left({\ frac {\ beta} {T}-\ gamma} \ right)} \ right)$$(3)ここで、 µ 0 低磁場移動度、β およびγ はフィッティングパラメータです、 E 0 は有効な活性化エネルギー、Eは駆動力(電界)です。 K はボルツマン定数であり、 T は温度です。 E のデフォルト値 0 γは0、β=0.1です。
上記の較正された物理モデルに基づいて、DM-DSTGTFETバイオセンサーの電気的特性が分析されます。
シミュレーション中、4つの異なる誘電率の生体分子( k =2.5、5、11、23)、5つのキャビティの厚さ( T c =5、7、9、11、13 nm)および異なる密度の荷電生体分子がシミュレーションと議論で考慮されます。一般に、センサーの感度を調べる場合は、基準が採用されます。標的物質に対するセンサーの応答を明らかにすることができるリファレンスが提案されています。したがって、空洞が空気で満たされている場合、または単に生体分子が空洞に満たされていない状態で参照が取られる。したがって、DM-DSTGTFETのしきい値電圧感度、ドレイン電流感度、およびサブスレッショルドスロープ感度の測定値は、[22] [28] [32]:
として定義されます。 $$ \ Delta V _ {{{\ text {th}}}} =V _ {{\ text {th(air)}}}-V _ {{\ text {th(bio)}}} $$(4)$ $ S _ {{{\ text {drain}}}} =\ frac {{I _ {{\ text {ds(bio)}}}-I _ {{\ text {ds(air)}}}}} {{I_ {{\ text {ds(air)}}}}} $$(5)$$ S _ {{{\ text {SS}}}} =\ frac {{SS _ {{{\ text {air}}}} --SS _ {{{\ text {bio}}}}}} {{SS _ {{{\ text {air}}}}}} $$(6)ここで、 V th(air) は、空洞が空気で満たされているときのバイオセンサーのしきい値電圧であり、 V th(bio) 空洞が生体分子で満たされているときのしきい値電圧です。同様に、 I ds(air) およびSS air は、空洞が空気で満たされているときのバイオセンサーのオン状態のドレイン電流とサブスレッショルドスイングであり、 I ds(bio) およびSS bio は、空洞が生体分子で満たされているときの、それぞれオン状態のドレイン電流とサブスレッショルドスイングです。
DM-DSTGTFETの電気的特性の分析を通じて、しきい値電圧、オン状態のドレイン電流、およびサブスレッショルドスイングが抽出され、バイオセンサーの感度が分析されます。
結果と考察
DM-DSTGTFETにおけるさまざまな生体分子の影響
図3は、生体分子の異なる誘電率がキャビティを満たす場合のオン状態でのDM-DSTGTFETの伝達特性、エネルギーバンド変動、しきい値電圧感度、および電流感度を示しています。下部ゲート金属の仕事関数(Φ MS =4.2)、ドレイン電流の感度は、異なるkを調整することで調べることができます。
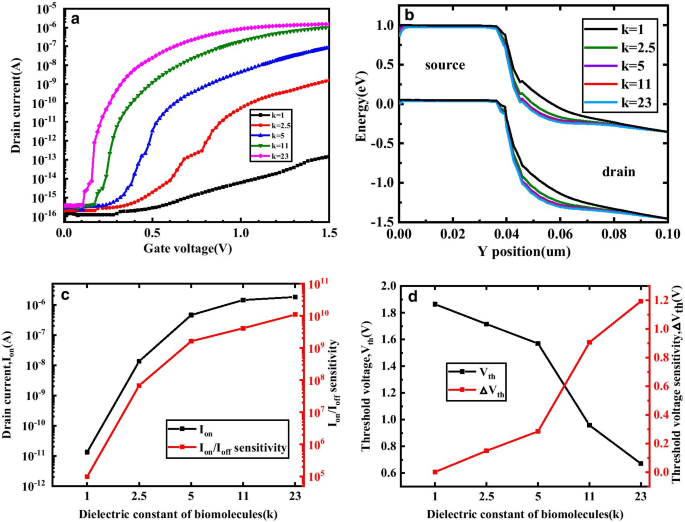
a 伝達特性、 b y軸に対するエネルギーバンドの変動 c 私 on / 私 オフ 感度と d V d でのkのさまざまな値に対するDM-DSTGTFETバイオセンサーのしきい値電圧感度 =0.5Vおよび T c =5 nm
図3aに見られるように、ゲート誘電体のkが増加すると、ゲート制御能力が強くなり、オン状態電流も増加します。図3bは、生体分子のさまざまなkでのエネルギーバンド図を示しています。 k の場合 =1、それは空洞に生体分子が充填されていないことを意味します。この場合、エネルギーバンドのねじれは最小限に抑えられます。さらに、空洞内で一定の生体分子の誘電体が増加し始めると、エネルギーバンドはますます激しく曲がります。これは、より高い k でより多くのエネルギーバンドの整列が行われることを意味します 、したがって、接合部全体のバリア幅が減少します。図3cは、 I に対する生体分子の誘電率の影響を示しています。 on および私 on / 私 オフ DM-DSTGTFETの感度。 k の増加に伴い 、 I on および私 on / 私 オフ 感度も向上します。これは、kが大きくなると、エネルギーバンドの曲がりが激しくなるほど、ソースチャネル接合部のバリア幅が狭くなり、トンネルの可能性が高くなるためです。トンネリング確率が増加すると、電子BTBTトンネリング生成が増加します。これは、図4で明確に確認できます。提案されたデバイスは、最高の I を提供します。 on / 私 オフ 1.1×10 10 の感度 k で =23、これは公開されているTFETベースのバイオセンサーよりも明らかに高いです。図3dは、 V の変化を示しています th および△ V th 生体分子のkに対するDM-DSTGTFETの感度。明らかに、 k として 増加するほど、 I は速くなります on 提案されたデバイスの増加、しきい値電圧の低下。一方、△ V th k の上昇とともに増加傾向を示しています 。その理由は、 V の違いです th さまざまな生体分子が充填され、 V th 生体分子が満たされていないときは大きくなっています。一般的に、 V th 空気で満たされている場合、他のk値よりも大きくなります。提案されたDM-DSTGTFETは最大△ V を実行します th k で1.2Vの感度 =23.したがって、DM-DSTGTFETは、生体分子に高い電流感度としきい値電圧感度を提供します。
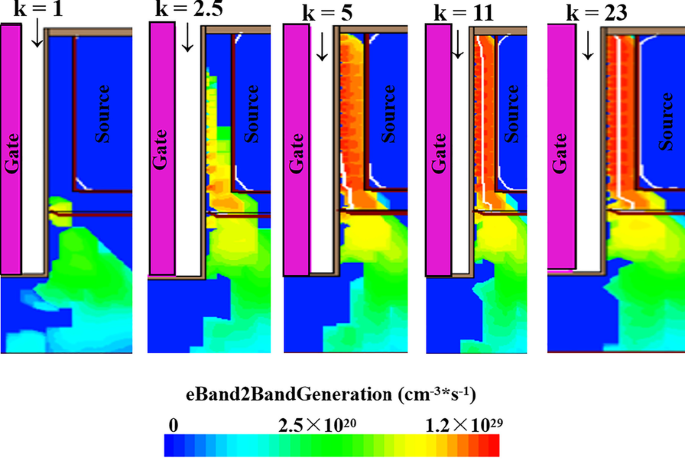
Vd =0.5 V、 T の場合の、さまざまな生体分子のDM-DSTGTFETバイオセンサーでの電子BTBT生成 c =5nmおよびVg =1.5V
図5aは、キャビティが異なる生体分子で満たされている場合のDM-DSTGTFETのSSおよびSS感度を示しています。ここで、誘電率の増加により、SSが減少し、S SS が改善されることがわかります。 。 SSが小さいほど、TFETの消費電力は小さくなり、TFETのパフォーマンスは向上します。したがって、kの値が増加すると、SSは減少し、S SS 増加し、ゲート制御能力が向上します。
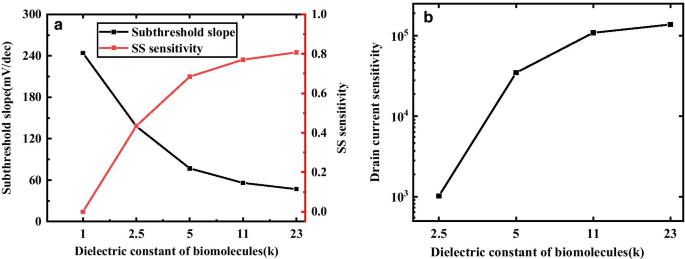
a サブスレッショルドスロープ、サブスレッショルドスロープ感度および b V d の場合、さまざまな生体分子で電流感度をドレインします。 =0.5V、 T c =5nmおよびV g =1.5V
ドレイン電流感度は、図5bで提案されているDM-DSTGTFETのkの関数として変化します。感度はkの増加とともに増加します。これは、kが増加するとトンネル接合部の電界が増強され、トンネル幅が減少し、 S が増加するためです。 ドレイン。
DM-DSTGTFETのキャビティの厚さが異なる場合の影響
k のとき =23、 S ドレイン 、△ V th 感度とS SS DM-DSTGTFETバイオセンサーの中で最大のものです(前のセクションから導き出された結論)。したがって、提案されたバイオセンサーの感度に対する空洞の厚さの影響をより明確に研究するために、このセクションは、 k の条件下で実施される。 =23。
図6は、さまざまなキャビティ厚( T )でのDM-DSTGTFETバイオセンサーの伝達特性を示しています。 c )。 T として c 増加すると、オン状態の電流が小さくなります。さまざまな T の効果 c I on および私 on / 私 オフ DM-DSTGTFETの感度を図7aにプロットします。 T の場合 c が増加すると、ゲートとチャネル間の静電容量が減少し、ソースチャネル接合部のトンネル幅が大きくなり、ドレイン電流が低下します。 k の場合 =23、 I on および私 on / 私 オフ T が増加すると、感度が低下します c T を高くするために、ゲートとチャネル間の容量結合が改善されたため c 。一方、提案されたデバイスは、 V で増加傾向を示します。 th したがって、△ V th T の増加に伴う感度 c 図7bに示すように。これは、 T の増加によるものです。 c I を減らします on したがって、 V が増加します th 。言い換えると、チャネル上のゲートの制御は、キャビティが広くなると減少し、 V が高くなります。 th 。したがって、DM-DSTGTFETは、より狭い空洞用のより優れた電圧バイオセンサーとして機能します。
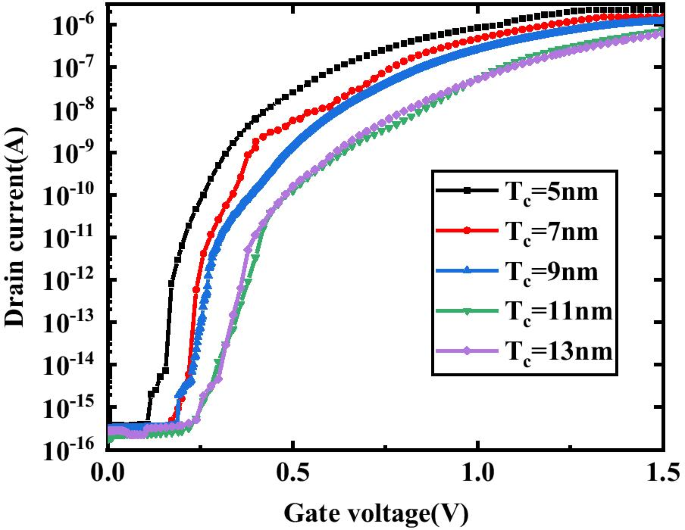
キャビティの厚さ( T )のさまざまな値に対するDM-DSTGTFETバイオセンサーの伝達特性 c )V d で =0.5V、V g =1.5Vおよび k =23
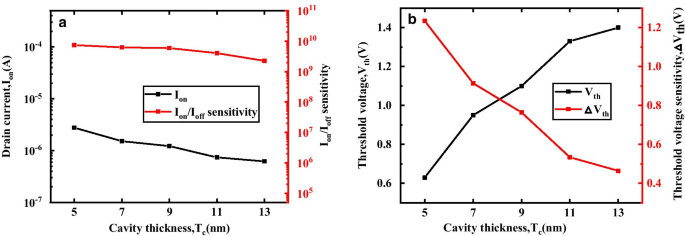
a キャビティの厚さのさまざまな値の影響( T c )on I on 、私 on / 私 オフ 感度、 b V th および△ V th V g でのDM-DSTGTFETの =1.5V、V d =0.5Vおよび k =23
DM-DSTGTFETに対する帯電生体分子の影響
提案されたセンサーの感度に対する生体分子の異なる電荷の影響を調査するために、ダイナミックレンジと検出限界が最初に研究されました。この論文では、DM-DSTGTFETは、10 10 の範囲の電荷密度でセンシング材料を検出できます。 cm −2 〜10 13 cm −2 、他のセンサーと比較してより広い検出範囲[32]。したがって、次のシミュレーションでは、動的限界範囲内の電荷密度が感度研究に使用されます。
図8は、さまざまな k でのDM-DSTGTFETの伝達特性に対する、さまざまな正電荷と負電荷を持つ生体分子で空洞を埋める効果を示しています。 。ご覧のとおり、 k で =2.5、正および負に帯電した生体分子の下では、伝達曲線の変化範囲が大きくなります。したがって、以下の説明では、 k の場合のDM-DSTGTFETバイオセンサーの感度に対するさまざまな正電荷と負電荷の影響に焦点を当てています。 =2.5。
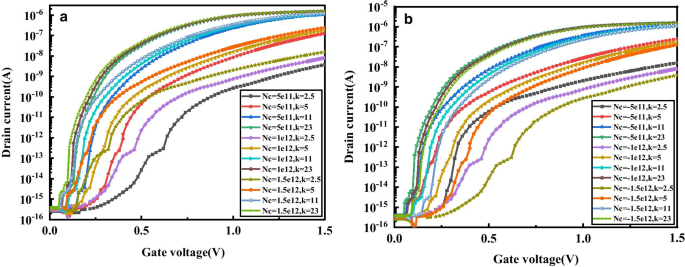
生体分子の誘電率に対するDM-DSTGTFETバイオセンサーの伝達特性 a V d での生体分子の異なる正電荷とb異なる負電荷 =0.5V、V g =1.5Vおよび T c =5 nm
図9aは、イオンと I のバリエーションを示しています。 on / 私 オフ 正電荷の関数としてのDM-DSTGTFETの感度。生体分子の正電荷の増加は、イオンと I の改善につながります on / 私 オフ 提案されたデバイスの感度。キャビティ内の正電荷により、有効なゲート酸化物誘電体が増加し、ゲート制御能力が向上します。このゲート制御能力の向上により、ソース-チャネル接合のトンネリング幅が減少し、 I が改善されます。 on および私 on / 私 オフ 感度。図9bは、 V に対する生体分子の正電荷の影響を示しています。 th および△ V th DM-DSTGTFETの感度。 V が観察されます th 減少し、△ V th 正電荷が増加すると感度が向上します。これは、分子の正電荷が I を増加させるという事実によるものです。 on V を減らします th 。 V の減少 th 空気に対する生体分子の閾値電圧の差を大きくし、△ V の改善につながる th 。
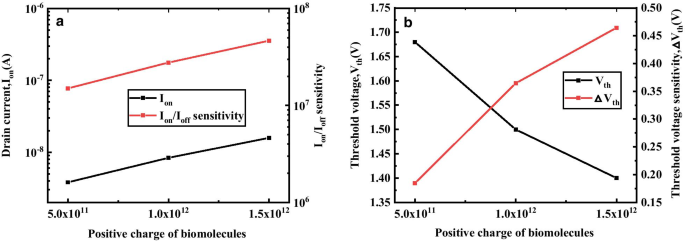
a I に対する生体分子の異なる正電荷の影響 on 、私 on / 私 オフ 感度、 b V th および△ V th V g でのDM-DSTGTFETの =1.5V、V d =0.5V、 k =2.5および T c =5 nm
図10aは、 I のバリエーションを示しています。 on および私 on / 私 オフ k の正電荷の関数としてのDM-DSTGTFETの感度 =2.5。生体分子の負電荷の増加は、イオンと I の減少につながります on / 私 オフ 提案されたデバイスの感度。キャビティ内の負電荷により、有効なゲート酸化物誘電体が減少し、ゲート制御能力が向上します。このゲート制御能力の低下により、ソースチャネルジャンクションのトンネル幅が増加し、イオンと I が減少します。 on / 私 オフ 感度。
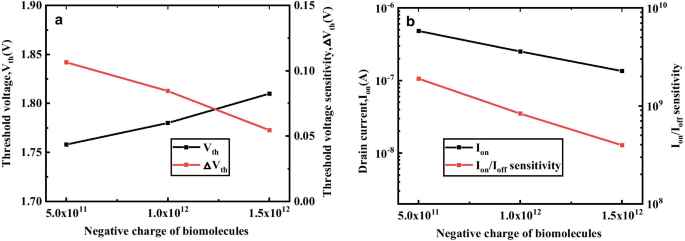
a I に対する生体分子の異なる負電荷の影響 on 、私 on / 私 オフ 感度、 b V th および△ V th V g でのDM-DSTGTFETの =1.5V、V d =0.5V、 k =2.5および T c =5 nm
図10bは、 V に対する生体分子の負電荷の影響を示しています。 th および△ V th DM-DSTGTFETの感度。図から、 k =2.5、 V th 改善し、△ V th 負電荷が増加すると感度が低下します。これは、分子の負電荷が I を減少させるという事実によるものです。 on V を増やします th 。 V の増加 th 空気に対する生体分子の閾値電圧の差を大きくし、△ V を低下させます。 th 。
結論
結論として、DM-DSTGTFETは、バイオセンサーアプリケーションで生体分子を検出するための高感度を備えています。ただし、DM-DSTGTFET構造の検出能力は、比誘電率、空洞の厚さ、帯電した生体分子、 I によってもたらされる影響を調べることによって評価されます。 on / 私 オフ 感度、SSおよびS SS 。結果は、誘電率が大きいほど、キャビティの厚さが薄くなり、正に帯電し、提案されたデバイスの感度が高くなることを示しています。シミュレーション結果は、提案された構造が超高感度で低消費のバイオセンサーデバイスに適用できることを示しています。
略語
- DM-DSTGTFETS:
-
誘電体変調デュアルソーストレンチゲートトンネル電界効果トランジスタ
- TCAD:
-
テクノロジーコンピュータ支援設計
- BTBT:
-
バンド間トンネリング
- DGTFET:
-
デュアルゲートトンネル電界効果トランジスタ
- SS:
-
サブスレッショルドスロープ
ナノマテリアル
- 回路とネットリストの例
- 卵巣癌細胞の高感度かつ迅速な検出のための柔軟なグラフェンベースのバイオセンサーのデモンストレーション
- ポリマーナノ構造上のU2OS細胞におけるアクチンと接着斑組織の分析
- グラフェン-誘電体プラズモン導波路におけるモードと分散特性の二重非線形性制御
- スリーステートエレクトロクロミックデバイスのディップコーティングプロセスエンジニアリングと性能最適化
- セリウムのダイヤモンドカッティングの分子動力学モデリングとシミュレーション
- アルミノシリケートミネラルおよび優れた水分解性能のための代替ドーピング
- Li-Nb-O化合物の調製と光触媒性能に及ぼすLi / Nb比の影響
- 微結晶およびナノセルロースの構造と誘電特性に及ぼす水の影響
- 中空構造LiNb3O8光触媒の調製と光触媒性能
- 抵抗変化型メモリのモデリングとシミュレーションに関する集合的研究



