バッテリー
背景
雷雨の中で凧を飛ばして電気を引き付けるというベンジャミン・フランクリンの有名な実験は、電気について学ぶために行われた18世紀後半から19世紀初頭の多くの実験の1つにすぎませんでした。最初のバッテリーは、1800年にイタリアのアレッサンドロボルタによって建設されました。いわゆるボルタ電池 塩水、灰汁、またはアルカリ性溶液に浸した革または厚紙で分離された銀と亜鉛の交互のディスクで構成されていました。パイルの両端にある金属片は、水銀で満たされた小さなカップに接続されていました。ボルタが両方の水銀カップに指で触れたとき、彼は電気ショックを受けました。彼が組み立てたディスクが多ければ多いほど、彼が受けた衝撃は大きくなりました。
ボルタの発見はさらなる実験につながりました。 1813年、ハンフリーデービー卿は、ロンドン王立研究所の地下に2,000組のディスクを備えた山を建設しました。他のアプリケーションの中でも、デイビーは電気分解のために生成した電気を使用しました。つまり、物質に電流を流すことで化学反応を触媒しました(デイビーはナトリウムとカリウムを化合物から分離しました)。ほんの数年後、マイケル・ファラデーは、磁石を使用してコイル状のワイヤーに電気を誘導する電磁誘導の原理を発見しました。この技術は、今日の発電所で電力を生産するために使用されるダイナモの中心にあります。 (ダイナモは電気の流れが規則的に方向を変える交流(AC)を生成しますが、バッテリーは一方向にのみ流れる直流(DC)を生成します。)非常に大量の電流を生成できる鉛蓄電池、今日の自動車の先駆者 バッテリーは、1859年にフランス人ガストンプランテによって考案されました。
米国では、トーマス・エジソンが電池とダイナモの両方からの電気を実験して電球に電力を供給していました。電球は1880年代初頭に米国で普及し始めました。 1860年代に、ジョルジュルクランシェは湿電池を発明しました。湿電池は、液体成分のために重いものの、商業的に販売および使用することができました。 1870年代と1880年代までに、ルクランシェ電池は乾燥した材料を使用して製造され、アレクサンダーグラハムベルの電話や新しく発明された懐中電灯に電力を供給するなど、さまざまな作業に使用されていました。その後、バッテリーは、第一次世界大戦後の数年間に非常に人気が高まったラジオなど、他の多くの発明に電力を供給するよう求められました。今日、世界中で毎年200億個以上のパワーセルが販売されており、各アメリカ人は年間約27個のバッテリー。
デザイン
すべてのバッテリーは、同様の手順を使用して電気を生成します。ただし、材料や構造の違いにより、さまざまな種類の電池が製造されています。厳密に言えば、一般的にバッテリーと呼ばれるものは、実際にはリンクされたセルのグループです。以下は、バッテリーがどのように機能するかを簡単に説明したものです。
セルの2つの重要な部分は、アノードとカソードです。陰極は、自然にまたは実験室で酸素と結合する金属であり、その結合は酸化物と呼ばれます。 酸化鉄(錆)は、バッテリーで使用するには壊れやすいものの、おそらく最もよく知られている酸化物です。他のいくつかの酸化物は、実際には、加工(切断、曲げ、成形、成形など)してセルで使用するのに十分な強度があります。アノードは、許可された場合に酸化する金属であり、他の条件が同じであれば、カソードの一部を形成する金属よりも酸化する可能性が高くなります。
セルは、陰極の一端と陽極の一端が電気を通すことができる第3の物質に配置され、他端が接続されている場合に電気を生成します。アノードはそれに向かって酸素原子を引き寄せ、それによって電気の流れを作り出します。回路にスイッチがある場合(壁やランプのスイッチと同様)、回路は完全ではなく、スイッチが閉じた位置にないと電気が流れません。スイッチに加えて、電球などの回路内に何かがある場合、電球は、それを通過する電子の摩擦から点灯します。
アノードとカソードが配置される3番目の物質は電解質と呼ばれます。 多くの場合、この材料はアルカリ性であるという特性を持つ化学的組み合わせです。したがって、アルカリ電池はアルカリ電解質を利用した電池です。セルは、単純なスイッチ、またはバッテリーを使用するアプライアンス内の他のスイッチング接続によって完全にされた回路に配置されない限り、それ自体では電気を生成しません。
セルを設計すると、タイプと構造に多くのバリエーションが生じる可能性があります。たとえば、すべての電解質がアルカリ性であるわけではありません。さらに、電解質用の容器は、容器としても、カソードまたはアノードのいずれかとしても機能することができます。一部のセルは、カソードからではなく、空気から直接酸素を引き出します。アノードとカソードの組成を変えると、多かれ少なかれ電気が供給されます。セルで使用されるすべての材料を正確に調整すると、生成できる電気の量、生成速度、セルの寿命を通じて電気が供給される電圧、およびさまざまな温度で機能するセルの能力に影響を与える可能性があります。 。
実際、これらの可能性はすべて存在し、それらのさまざまな用途により、今日利用可能なさまざまな種類の電池(リチウム、水銀など)が製造されています。しかし、何年もの間、最も一般的なセルは1.5ボルトのアルカリ電池でした。
さまざまなバッテリーは、さまざまな状況でより適切に機能します。アルカリ性の1.5ボルトのセルは、写真機器、ハンドヘルドコンピューターと計算機、おもちゃ、テープレコーダー、およびその他の「高ドレイン」用途に最適です。低温でも良いです。このセルは傾斜した放電特性を備えており、突然電力を生成しなくなるのではなく、徐々に電力を失います。棚に未使用のままにしておくと、年間でおそらく電力の4%が失われます。
他のタイプのバッテリーには、フラット放電特性を備えたリチウム/二酸化マンガンバッテリーが含まれます。これは、寿命の初めと終わりにほぼ同じ量の電力を供給し、小型の必要がある場合に使用できます。高出力バッテリー(煙探知器、カメラ、コンピューターのメモリーバックアップなど)。補聴器、ページャー、およびその他の種類の医療機器では、空気亜鉛電池を頻繁に使用します。これにより、連続放電で高いエネルギー密度が得られます。水銀電池は、安定した出力電圧を提供するため、空気亜鉛電池と同じアプリケーションの多くで頻繁に使用されます。
原材料
このセクションと次のセクションでは、アルカリ電池に焦点を当てます。アルカリ電池では、セルを含むシリンダーはニッケルメッキ鋼で作られています。それは、陰極を陽極から分割するセパレーターで裏打ちされており、層状の紙または多孔質の合成材料のいずれかでできています。キャニスターの一端は、鋼板の下にあるアスファルトまたはエポキシシーラントで密封され、もう一端は、シリンダーに打ち込まれた真ちゅう製の釘で密封されています。この釘は金属製のエンドキャップに溶接され、外部のプラスチックシールを通過します。シリンダー内のカソードは、二酸化マンガン、グラファイト、および水酸化カリウム溶液の混合物で構成されています。アノードは亜鉛粉末と水酸化カリウム電解質で構成されています。
製造
プロセス
カソード
- 1アルカリ電池では、陰極は実際には容器の一部としても機能します。二酸化マンガン、カーボンブラック(グラファイト)、電解質(溶液中の水酸化カリウム)などの構成成分が大量に含まれています。
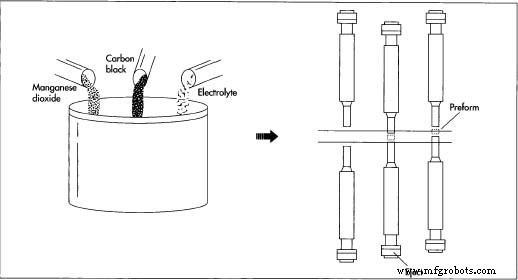 構成成分の混合は、電池製造の最初のステップです。造粒後、混合物はプレスまたは圧縮されてプリフォーム(中空シリンダー)になります。圧縮の原理は単純です。鋼製のパンチがキャビティ内に降下し、混合物を圧縮します。収縮すると、下からパンチが上がり、圧縮されたプリフォームが排出されます。列車で配達され、生産現場で非常に大きなバッチで混合されます。次に、混合物は造粒され、プレスまたは圧縮されて、プリフォームと呼ばれる中空のシリンダーになります。 製造されるバッテリーのサイズに応じて、いくつかのプリフォームがバッテリー内で積み重ねられる場合があります。あるいは、一連のプリフォームを同じ材料の押し出しリングに置き換えることができます。
構成成分の混合は、電池製造の最初のステップです。造粒後、混合物はプレスまたは圧縮されてプリフォーム(中空シリンダー)になります。圧縮の原理は単純です。鋼製のパンチがキャビティ内に降下し、混合物を圧縮します。収縮すると、下からパンチが上がり、圧縮されたプリフォームが排出されます。列車で配達され、生産現場で非常に大きなバッチで混合されます。次に、混合物は造粒され、プレスまたは圧縮されて、プリフォームと呼ばれる中空のシリンダーになります。 製造されるバッテリーのサイズに応じて、いくつかのプリフォームがバッテリー内で積み重ねられる場合があります。あるいは、一連のプリフォームを同じ材料の押し出しリングに置き換えることができます。 - 2次に、プリフォームをニッケルメッキ鋼缶に挿入します。プリフォームとスチールの組み合わせで、バッテリーのカソードを構成できます。大規模な操作では、缶は標準的な切断および成形技術を使用して電池工場で製造されます。缶の上部近くにくぼみを作り、漏れを防ぐためにくぼみの上にアスファルトまたはエポキシシーラントを配置します。
セパレーター
- 3次に、電解液に浸した紙セパレーターをプリフォームに対して缶の内側に挿入します。セパレーターは、(合板のように)互いにクロスグレインで配置された数枚の紙でできています。開いた缶を見下ろすと、缶に紙コップが挿入されているように見えます。セパレータは、カソード材料がアノード材料と接触するのを防ぎます。別の方法として、製造業者は同じ目的で多孔質合成繊維を使用する場合があります。
アノード
- 4アノードは次にバッテリー缶に入ります。これは、主に亜鉛粉末と、水酸化カリウム電解質を含む他の材料で構成されるゲルです。このゲルは非常に濃いペーストの粘稠度を持っています。溶液ではなく、化学的には懸濁液であり、粒子は沈降しません(適切なフィルターで粒子を分離できますが)。バッテリーが使用されると発生する化学反応のためのスペースを確保するために、ゲルは缶の上部まで満たされません。
アザラシ
- 5この時点でバッテリーは発電できますが、オープンセルは実用的ではなく、その電位を急速に使い果たしてしまいます。バッテリーは、3つの接続されたコンポーネントで密閉する必要があります。 1つ目は、真ちゅう製の「釘」または長いスパイクで、ゲル材料を介して缶の中央に挿入され、「集電装置」として機能します。 2つ目はプラスチック製のシールで、3つ目は金属製のエンドキャップです。約3分の2伸びる釘
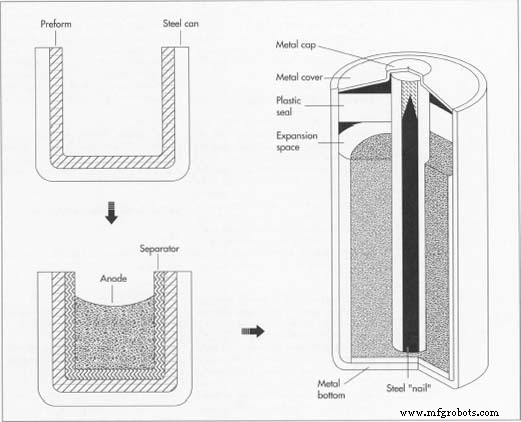 スチール缶に挿入されたプリフォームで構成される典型的なアルカリ電池の容器は、陰極も兼ねています。真ん中の陽極は主に亜鉛粉からなるゲルです。アノードとカソードの間のセパレーターは、電解液に浸した紙または合成繊維のいずれかです。
スチール缶に挿入されたプリフォームで構成される典型的なアルカリ電池の容器は、陰極も兼ねています。真ん中の陽極は主に亜鉛粉からなるゲルです。アノードとカソードの間のセパレーターは、電解液に浸した紙または合成繊維のいずれかです。
完成したバッテリーには、プラスチックシール、スチールネイル、金属製の上下が追加されています。釘は金属の底に溶接されており、陽極を通って缶の中に約3分の2伸びています。缶に入る途中で、金属製のエンドキャップに溶接され、プラスチック製のシールを通過します。 - 6このシールは、場所によっては他の場所よりも大幅に薄いため、缶内にガスが溜まりすぎると、バッテリー全体ではなくシールが破裂します。一部のバッテリー設計では、プラスチックのワックスで満たされた穴を利用しています。過剰なガスは、バッテリーを破裂させるのではなく、ワックスを押し出します。シールアセンブリは、プロセスの開始時に缶に作成されたくぼみに適合し、所定の位置に圧着されます。
- 7次に、缶の反対側の端(バッテリーのプラス側の端)を、所定の位置に溶接するか、エポキシタイプのセメントで接着した鋼板で閉じます。
ラベル
- 8バッテリーが工場から出荷される前に、バッテリーのタイプ、サイズ、およびその他の情報を識別するラベルが追加されます。ラベルは多くの場合、バッテリーに単に接着された紙です。ある大手メーカーは、ラベルのデザインをプラスチックのシュリンクラップに印刷しています。熱に弱いプラスチックのゆるい部分をバッテリー缶に巻き付け、熱を加えると、プラスチックが収縮して缶の周りにぴったりとフィットします。
品質管理
バッテリー技術は特に新しいものでもエキゾチックなものでもないため、品質管理とその結果はブランド競争の基盤として特に重要です。バッテリーが腐食に耐え、さまざまな条件下で適切に動作し、良好な保管寿命と使用寿命を維持する能力、およびその他の要因は、品質管理の直接的な結果です。電池と原料は、製造工程のほぼすべての段階で検査とテストが行われ、完成したバッチは厳格なテストを受けます。
環境問題
バッテリーを作ることはいくつかの環境上の障害を提示しますが、克服できないものはありません。アルカリ電池の主要な化学物質である亜鉛とマンガンは環境に問題を引き起こさず、どちらも食品医薬品局(FDA)によって安全であると見なされています。電池の主な潜在的な汚染物質は水銀です。これは一般に亜鉛に付随し、導電性を高め、腐食を防ぐためにアルカリ電池に長年添加されていました。 1980年代半ば、アルカリ電池には通常5〜7パーセントの水銀が含まれていました。
数年前に水銀が環境に害を及ぼすことが明らかになったとき、製造業者は水銀なしで効率的な電池を製造する方法を模索し始めました。これを行う主な方法は、成分のより良い純度管理に焦点を当てています。今日のアルカリ電池には、約.025パーセントの水銀が含まれている可能性があります。水銀を全く添加していない電池(天然元素であるため、微量でもない製品を保証することは困難です)は一部のメーカーから入手可能であり、最終的には例外ではなく業界全体のルールになります1993年の。
未来
バッテリーは現在、世界中の科学者やエンジニアによる徹底的な調査の焦点となっています。理由は単純です。いくつかの重要な革新は、より優れたバッテリーの作成に依存しています。充電を必要とせずに長期間動作できる実行可能な電気自動車や携帯型電子機器は、より軽量でより強力なバッテリーが開発されるまで待たなければなりません。たとえば、現在自動車で使用されている一般的な鉛蓄電池は、かさばりすぎて、電気自動車で使用するのに十分な電力を蓄えることができません。リチウム電池は軽量で強力ですが、液漏れや発火しやすい傾向があります。
1993年の初めに、アリゾナ州立大学の科学者は、ポリプロピレン酸化物とポリエチレンオキシドをリチウム塩溶液に溶解することにより、新しいクラスの電解質を設計したと発表しました。新しい電解質は、一般的なリチウム電解質よりも導電性が高く、安定しているように見えます。研究者たちは現在、有望な物質を使用したプロトタイプ電池の製造を試みています。
その間、いくつかのメーカーは、ポータブルコンピューターで使用するためのより大きく、より強力なニッケル水素電池を開発しています。これらの新しいバッテリーは1994年後半に登場する予定です。
製造プロセス



