ドラッグリポジショニングのためのファーマコフォアガイドによる仮想スクリーニング
ドラッグリポジショニングは、元の医学的適応の範囲を超えた、承認された、または治験中の治療法の新しいアプリケーションを特定するための長年の戦略です。 1 高血圧と狭心症のために設計された薬物がファイザーの悪名高い「小さな青い錠剤」になるために偶然に再配置されて以来、一般にバイアグラと呼ばれ、薬物の転用が世間の注目を集めてきました。 COVID-19を治療するための治療法の世界的な緊急性により、この薬剤戦略が再び大衆の注目を集めました。
3Dタンパク質モデリングには、ドラッグリポジショニングのためのいくつかの分子モデリングおよびシミュレーション方法が含まれます。このシリーズの以前の投稿では、SARS-CoV-2メインプロテアーゼに結合する可能性のある阻害剤を特定する方法として分子ドッキングについて説明しました。代替の in silico ファーマコフォアモデリングなどの方法は、同等の結果を達成し、ある候補者を別の候補者よりも選択することをサポートする追加の証拠を提供しますか?
代替ルートを利用する
ファーマコフォアモデリングは、タンパク質ターゲットによるリガンドの認識に必要な分子機能の抽象化を提供します。分子の相互作用と結合の表現は、古典的なシミュレーション方法とは対照的な視点を提供します。
Diamond LightSourceからいくつかのSARS-CoV-2主要プロテアーゼタンパク質構造の初期データセットを取得しました。 2 これらの構造を調整し、BIOVIA DiscoveryStudioで利用可能な「InteractionPharmacophoreGeneration」プロトコルを使用して、各受容体-リガンド複合体の非結合相互作用を表すファーマコフォアを生成しました。ファーマコフォアの機能の総数は、5R80および5R7Y結晶構造の2つの機能から、6LU7の9つの機能モデルまでの範囲でした。個々の複合体からのファーマコフォアを単一のモデルにマージし、密接にクラスター化された機能を編集しました。最終モデルには、プロテアーゼと可能な小分子結合剤の間の分子間接触を表す14の機能が含まれていました。
その後、インシリコを実行しました すべての複合体の活性部位残基に対するアラニンスキャニング変異誘発により、変異したときにそのタンパク質-リガンド複合体の結合親和性(ホットスポット)を低下させた残基を特定します。すべての複合体から、8つの残基(HIS41、MET49、ASN142、HIS163、MET165、PRO168、GLN189、およびGLN192)を少なくとも1つの複合体のホットスポットとして識別し、3つの残基を少なくとも4つの複合体のホットスポットとして識別しました。 14機能のファーマコフォアモデルでは、6つの機能が8つのホットスポット残基の1つとの相互作用に対応していました。非共有M PRO の2番目のデータセット ダイヤモンド光源 2 によって放出された配位子錯体 いくつかの異なる結合モードが明らかになり、仮想スクリーニングの次のステップで使用するために、6つの主要なファーマコフォア機能を2つのグループに分離することになりました。
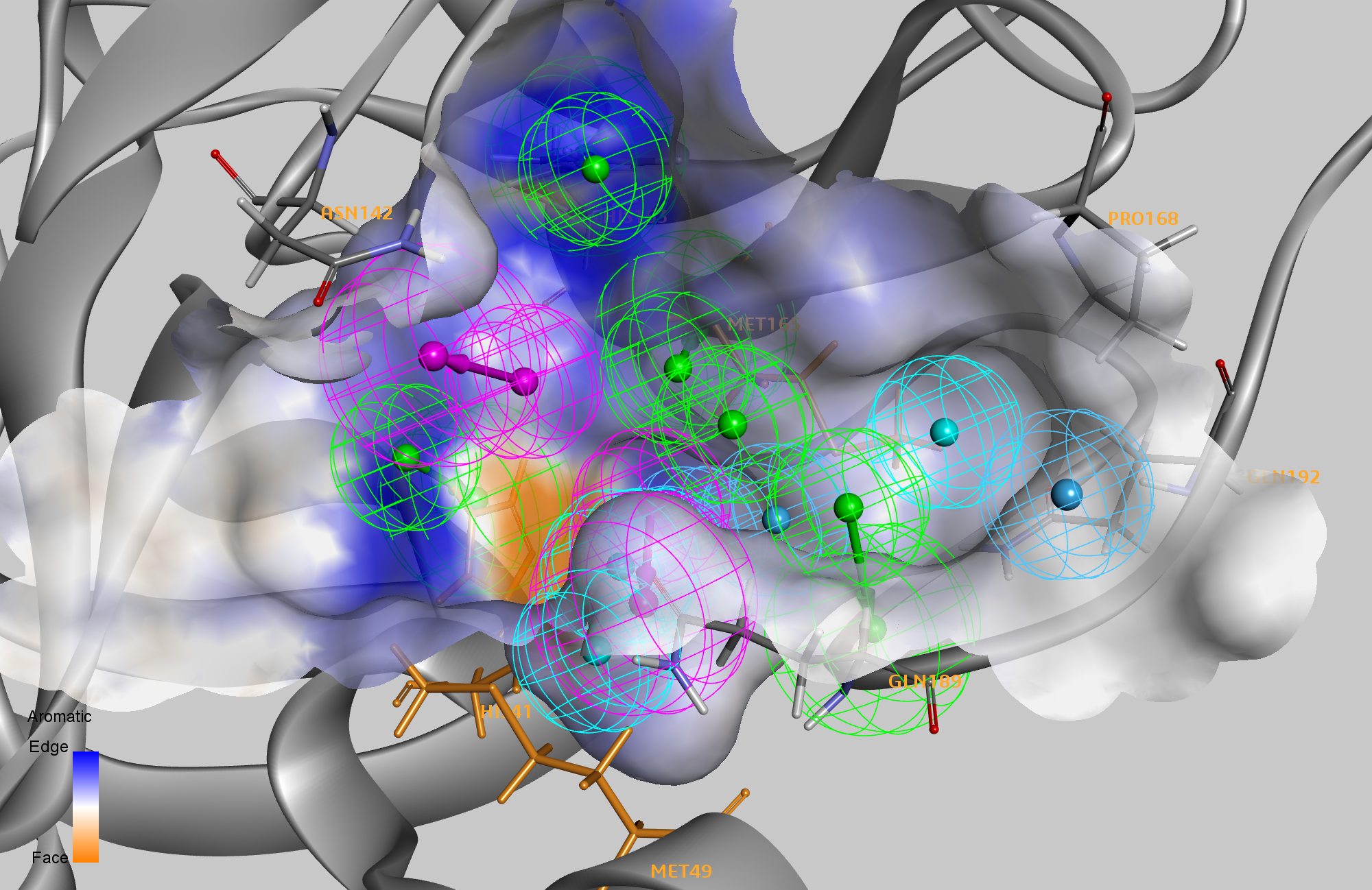
現在、このファーマコフォアモデルを使用して、高速検索用に事前に生成された複数のリガンド確認を備えた2,650のFDA承認薬を含む選択されたライブラリの仮想スクリーニングを実行しました。ヒットを特定するために、2つの必要なグループのそれぞれからの少なくとも1つの機能と、残りの8つの機能からの少なくとも2つの機能を一致させる必要があるという要件で、これらのリガンドを14機能のファーマコフォアに対してスクリーニングしました。これは、リガンドのさまざまな結合モードの多様な探索を可能にすると同時に、アラニンスキャン変異誘発で同定された重要な残基と少なくとも2つの相互作用を形成できるポーズのみが保持されるようにするためです。このアルゴリズムは、基本的に12,000を超えるファーマコフォアの組み合わせを調査します。次に、タンパク質内の各ファーマコフォアの組み合わせに最適なヒットを最小限に抑えました。最後に、CHARMmとGeneralized Born using Molecular Volume(GBMV)陰溶媒モデルを使用して、最適化されたファーマコフォア由来のポーズの結合エネルギーを決定しました。この方法は、事実上、分子ドッキング計算です(以前のブログのように)が、ここでは、最適化されたファーマコフォアモデルを使用して、ドッキングされた結果を抑制およびフィルタリングしました。
各ポーズの非結合相互作用を計算し、4つの主要な残基(HIS41、MET49、CYS145、およびMET165)との相互作用を持つポーズのみに焦点を当てるようにフィルタリングしました。 HIS41、MET49、およびMET165は、以前に特定された少なくとも4つの複合体に共通する3つの残基であり、CYS145は、主要なプロテアーゼホモ二量体の各サブユニットに見られる重要なHIS41 / CYS145触媒ダイアドの2番目の残基です。計算された結合自由エネルギーを使用してヒットをソートし、さらに調査するためのもっともらしい候補のトップ10を特定しました。リトナビルは、ここと以前のブログで特定された唯一の一般的なリガンドでした。リトナビルは7番目に結合自由エネルギーが高く、ドッキング研究でも以前は7位にランクされていました。リトナビルは現在、COVID-19の臨床試験を数多く受けています。 3
動画1 :HIS41、MET49、SER144、CYS145、MET165、GLU166、およびGLN189と相互作用するリトナビルの最高スコアのポーズ。
ここに示した方法で最高のスコアリングリガンドは、システイニルロイコトリエン受容体拮抗薬であるモンテルカストでした。最近発表された論文は、COVID-19感染症の進行を制限するためにその使用を仮定しています。 4
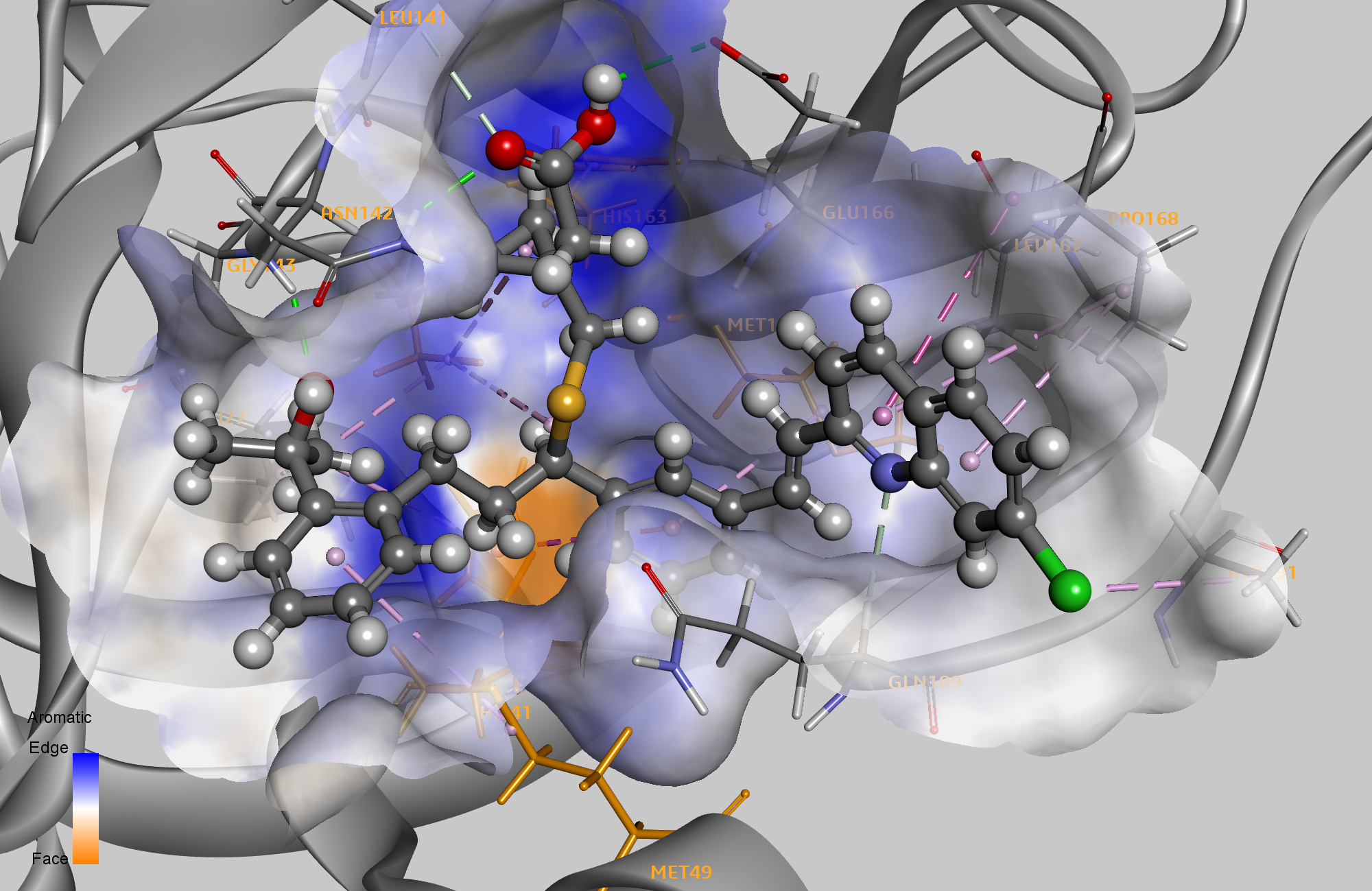
さらに3つの最高得点の化合物には、テルミサルタン、モエキシプリル、ヒドロキシクロロキンという薬が含まれていました。 COVID-19の再利用薬としてのこれらすべての化合物の可能性は、最近精査されています 5 ヒドロキシクロロキンが最も論争を呼んでいます。 2つの方法のトップ10ヒットリストのもう1つの違いは、含まれる創薬ターゲットの多様性です。ドッキング結果の上位10には、7つのHCVまたはHIVプロテアーゼ阻害剤が含まれています。ファーマコフォア優先のヒットリストには、7つの異なるターゲットクラスの薬が含まれています。
私たちのファーマコフォア由来の仮想スクリーニングは、以前のドッキング作業では特定されなかったいくつかの新しい潜在的なCOVID-19薬を含む優先ヒットリストを作成しました。このアプローチでは、 in silico の利用方法を示します。 ファーマコフォアモデルを改良するための有用な技術としてのアラニンスキャニング突然変異誘発。また、スクリーニングプロセス中にフィットするために特定の機能が存在するという要件を課しました。これら2つの調査の結果は、直接比較することはできません。基本的なアルゴリズムの違いによるものではなく、さまざまなサポート戦略の実装によるものです。
2つの方法の結果を簡単に比較すると、焦点を当てるリードの重複はほとんどありませんでした。両方の方法で特定されたリトナビルの共通性は、さらなる研究のためのこの候補者の選択を支持する証拠を提供すると言うことができます。以前の研究では、タンパク質-リガンドドッキングスコアリング関数のコンセンサスを使用すると、推定される薬剤候補の特定が改善されることが示されています。 6 このため、研究者は、各メソッドのユニークな最高スコアの化合物を使用して、実験テスト用の化合物に優先順位を付けることができます。
結論として、ファーマコフォア由来の仮想スクリーニングは、ドッキングのための補足的かつ補完的な方法を提供し、実験的検証のための候補者選択におけるコンセンサスとより大きな信頼に貢献します。転用のための薬剤候補を提供する緊急性を超えて、このファーマコフォア主導の方法は、その後のリード最適化のためにより多様なリガンドを特定する可能性もあります。
生物製剤



