Zn-Al層状複水酸化物による光触媒的に強化されたカチオン染料の除去
要約
煆焼および有機修飾されたZn-Al層状複水酸化物(LDH)は、カチオン染料、すなわちメチレンブルー(MB)を除去するための吸着剤および光触媒として研究されました。 共沈法により、カチオン比2:4のZn-Al LDHが得られた。合成されたままのサンプルをさまざまな温度で焼成し、XRD、TG / DTG、およびUV-vis-DR法によって相変態を調べました。 UV光下での合成されたままのおよび焼成されたZn-Al LDHの活性は、ZnO相の存在に起因した。 LDH中のZnOの量は、Zn / Al比と加熱温度を変えることで調整できます。 LDHの光触媒活性に対するZn / Al比の影響が優勢であることが観察されました。煆焼されたZn-Al LDHは、MBの低い吸着を示した。ドデシル硫酸ナトリウムによるZnAlLDHの修飾は、再構成法を使用して実行されました。有機/ LDHナノハイブリッドはMBへの高い吸着能力を示しました。有機/ Zn-AlLDHを含む溶液からのMBの除去は、MBの光破壊によるUV光の使用によって強化されました。
背景
廃水からの有害な有機染料の除去と地表水中の汚染物質の浄化、地下水は世界の主要な問題です。染料を含む排水の処理には、吸着、凝固、凝集、オゾン処理、膜ろ過、イオン交換、酸化、化学沈殿など、いくつかの従来の方法が知られています[1、2]。吸着は、特別な設定を必要としない安価な技術です。近年、触媒機能を備えた多くの種類の吸着剤が開発され、水から硝酸塩、重金属、および有機汚染物質を除去するために使用されています[3,4,5]。
水性媒体から有機染料を除去するための代替材料としての層状複水酸化物(LDH)の使用が検討されています[6、7、8]。 LDHは、陰イオン性粘土およびハイドロタルサイト様材料として知られています。それらの基本構造は、ブルーサイト、Mg(OH) 2 の構造に似ています。 、分数 x の場合 二価の陽イオンは三価の陽イオンに同形に置き換えられ、正に帯電した層になります。 LDHの化学組成は一般式[M 2+ 1-x M 3+ x (OH) 2 ] [A n- ] x / n ・zH 2 O、ここでM 2+ 一般的かもしれません。 Mg 2+ 、Zn 2+ 、またはNi 2+ 、およびM 3+ 一般的かもしれません。 Al 3+ 、Ga 3+ 、Fe 3+ 、またはMn 3+ 。無機または有機アニオンを補償する非フレームワーク電荷(CO 3 2- 、Cl − 、SO 4 2- 、RCO 2 − )はA n- として署名されています; x 通常は0.2〜0.4です。 LDH層は、M 3+ の同形置換によって正電荷を獲得します。 M 2+ の場合 、これは層間陰イオンと水によって補償されます[9]。
LDHの熱処理により、物理吸着された層間の水分子、OH - が失われます。 層のグループ、および電荷平衡陰イオン。層状構造が崩壊し、混合金属酸化物固溶体が形成されます。混合酸化物は通常、大きな比表面積、熱安定性、および異なる金属成分間の相乗的相互作用を持っていました。したがって、LDHの煆焼製品は、さまざまな触媒プロセスで多くの用途が見出されています[10、11、12]。
LDHは、陰イオン交換容量があるため、陰イオン染料のインターカレーションと収着に適していますが、陽イオン染料には適用できません。 LDHの表面を陰イオン性界面活性剤で修飾することにより、さまざまな種類の有機分子を吸着できる複合材料を得ることができます[13、14]。ドデシル硫酸ナトリウム(DS)で修飾されたLDHは、サフラニン[15]、メチレンブルー[16]、ベーシックブルー[17]などのカチオン染料の非常に高い収着を示しました。
最近、LDHは、その固有の光応答特性、低コスト、および容易な調製と修飾のために、有望な異種光触媒として集中的に研究されています[18]。光触媒としてのLDHは、層状マトリックス内の活性種の高い分散の結果として大きなエネルギー変換効率を示し、これにより電荷の分離が容易になります。半導体特性を備えた混合酸化物は、適切な遷移金属含有LDHの煆焼によって得られます。 Zn 2+ などの多種多様な金属カチオン およびTi 4+ 、レイヤーに導入することができます[19、20]。それらの相対的な比率は広範囲で変化する可能性があり、調整可能な特性を備えた半導体酸化物の調製の可能性を提供します。 LDHの光触媒アプリケーションは興味深い新興分野です。 Zn-Al [20]、Zn-Ce、ZnFe、Zn-Cr [21]、Mg-Zn-Al [22]、およびZn-Ga [23]など、LDHに由来するいくつかの半導体混合酸化物が研究されています。汚染物質の光触媒分解用。
望ましくない色に加えて、染料の分解生成物はまた、人間に対して変異原性または発癌性の影響を示し、それらの摂取は生物に深刻な損傷を引き起こす可能性があります。分解中に生成される塩素と次亜塩素酸は、強力な有毒な酸化剤です。それらは有機物を酸化し、同時に塩化物に還元されます[24]。キャラコの印刷、綿や皮革の染色に使用される重要な基本染料として、MBは目のやけど、胃腸管や皮膚への刺激などのさまざまな有害な影響を引き起こす可能性があります[25]。
メチレンブルー(MB)用のDSで修飾されたZn-Al中間層の高い吸着容量が実証されました[26]。吸着剤中の光活性成分の存在は、UV照射を使用することによってカチオン染料を除去するためのZn-AlLDHベースの材料の効率を高めることができます。したがって、吸着や光破壊によるMBなどのカチオン染料の除去のためのZn-Al LDHの調製に最適な条件が、本研究で決定されました。
メソッド
Zn-AlLDHの合成
すべての化学物質は分析グレードであり、さらに精製することなく使用されました。 [Zn]:[Al] =1:2の[Zn]:[Al] =1:2の炭酸塩を層間アニオンとするZn-Al LDHは、[9]と同様の一定pHで共沈法により合成されました。 Na 2 を含む最初のソリューション CO 3 (0.5M)およびNaOH(1.5M)が得られた。 Zn(NO 3 の金属硝酸塩の混合物を含む2番目の溶液 ) 2 ∙6H 2 OとAl(NO 3 ) 3 ∙9H 2 O(総金属濃度は0.6 M、Zn / Al 2:1、3:1、4:1のモル比)を調製し、攪拌しながら最初の溶液に滴下しました。 NaOHの添加によりpHを10に調整した。添加が完了すると、温度は85 o まで上昇しました。 Cおよびスラリーは、連続的に攪拌しながらこの温度で6時間保持されていた。その後、スラリーを数時間以内に室温まで冷却した。生成物を濾過により単離し、pH7になるまで脱イオン水で数回洗浄した。その後、固体を100℃で乾燥させた。サンプルはZnAl 21 とラベル付けされました LDH、ZnAl 31 LDH、およびZnAl 41 LDH。
上記で合成されたZn-AlLDHは、450°Cで2時間、600°Cで1、2、5時間空気中で煆焼されました。サンプルはZnAl 21 とラベル付けされました -450、ZnAl 31 -450、ZnAl 41 -450、ZnAl 21 -600-1、ZnAl 31 -600-1、ZnAl 41 -600-1、ZnAl 21 -600-2、ZnAl 31 -600-2、ZnAl 41 -600-2、ZnAl 21 -600-5、ZnAl 31 -600-5、ZnAl 41 -600-5。
Zn-Al LDHは、ドデシル硫酸ナトリウムCH 3 で修飾されています。 (CH 2 ) 11 SO 4 再構成法によるNa。 1gの煆焼LDHと50mlの0.05MDS水溶液の懸濁液を室温で24時間撹拌しました。得られた複合材料は、ZnAl 21 とラベル付けされました。 -450 / DS、ZnAl 31 -450 / DS、ZnAl 41 -450 / DS、ZnAl 21 -600-1 / DS ZnAl 31 -600-1 / DS ZnAl 41 -600-1 / DS。
特性評価
サンプルのXRDパターンは、DRON-4-07回折計(Burevestnik Inc.、ロシア、サンクトペテルブルク)、(CuK α 放射線)。熱重量分析(TGA)および示差熱分析(DTA)は、10°min -1 の加熱速度で流れる空気中で動作するDerivatographQ-1500 D装置(MOM、ハンガリー)を使用して実行されました。 。拡散反射スペクトルは、波長200〜1000nmの範囲の統合LabsphereRSA-PR-20を備えたLambda35 UV-Vis(Perkin Elmer、ドイツ)分光計で取得しました。溶液のUV-可視スペクトルは、Lambda 35 UV-Vis分光計(Perkin Elmer、ドイツ)を使用して記録されました。
光触媒実験
0.020gのZn-AlLDHを40mLの9×10 -5 に分散させました。 M(煆焼LDH用)および10 -4 M(DS修飾LDHの場合)石英反応器内のMB水溶液。照射前に、光触媒とMB分子の間の吸着-脱着平衡に到達するために、懸濁液を暗所で1時間(焼成LDH)および24時間(DS修飾LDH)撹拌しました。次に、溶液に水銀灯(λ max )を3時間照射しました。 =365 nm)マグネチックスターラーで攪拌します。所定の時間間隔で、UV-Vis分光法を使用して吸収スペクトルを測定することにより、溶液を分析しました。
結果と考察
特性評価
異なるZn 2+ を持つ合成されたままのZn–AlLDHのXRDパターン / Al 3+ カチオン比を図1aに示します。ハイドロタルサイトのような構造は、すべてのカチオン比で形成されました。 XRDパターンは、層状複水酸化物に関連する特徴的な反射を示します。追加のZnO相がZnAl 41 に存在しました XRDパターンで示されるLDH。 31.9°、34°、および36.2°の2θピークは、ブルーサイト様シート表面に形成されたZnO相に属します。すべての反射は鋭く、結晶性の高い材料を示しています。
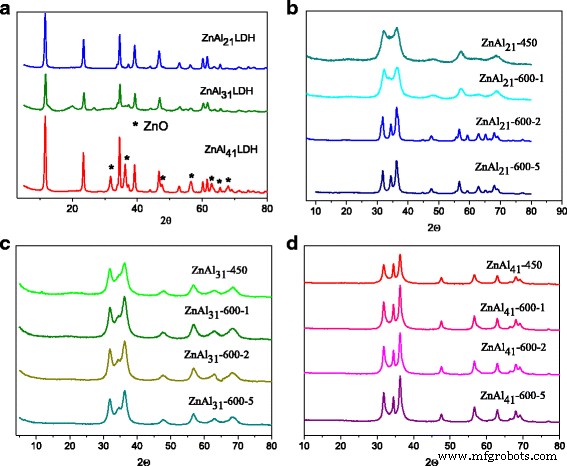
合成されたままのZn-AlLDHのX線回折パターン( a )および煆焼:ZnAl 21 LDH( b )、ZnAl 31 LDH( c )、ZnAl 41 LDH( d )
煆焼誘導体のXRDパターンの分析は、元のLDHの層状構造が完全に破壊されたことを示し、元のLDHがほぼ完全に分解され、ほとんどの層間炭酸陰イオンと水が除去されたことを示しています(図1b–d)。すべての反射は、六角形のウルツ鉱型構造ZnOとして完全にインデックス化できます。 Al 2 に対応する特徴的な反射はありません O 3 XRDパターンで相が観察されました。 Zn 2+ の増加に伴い、ZnOの結晶化度が向上したことに注意する必要があります。 / Al 3+ カチオン比。
水性懸濁液中の煆焼されたZn-AlLDHの水和が、ハイドロタルサイト相の再構築を引き起こしたことが知られています[9]。 DSの水溶液中で煆焼したZn-AlLDHを水和すると、層状構造が回復したことがわかります(図2)。小さな角度での回折パターンの出現は、DSが挿入されたLDHの存在について証明されました。再構築されたすべてのDS修飾Zn-AlLDHには、炭酸塩が挿入された相も含まれていました。層状構造の完全な再構築は、ZnAl 21 でのみ観察されたことは注目に値します。 -450 / DS LDH(図2a)。 ZnAlのXRDパターン 31 -450 / DSおよびZnAl 41 -450 / DS LDHにはZnO反射が含まれていました(図2a)。 [27]によると、Zn / Al比が1:5のZn-Al混合酸化物の水和により、初期のZn / Al比に関係なく、Zn / Al =2のハイドロタルサイト構造が形成されました。したがって、ZnAl 31 -450 / DS、ZnAl 41 -450 / DS LDHには、DSが挿入された相の量が少なかった。 600°Cで焼成されたZn-Al混合酸化物から得られたすべてのDS修飾LDHのXRDパターンには、ZnO相の反射が含まれていました(図2b)。明らかに、Zn 2+ の連続放出 アモルファス酸化物相からの生成により、煆焼温度の上昇に伴い、より多くのZnOナノ粒子が形成されました。
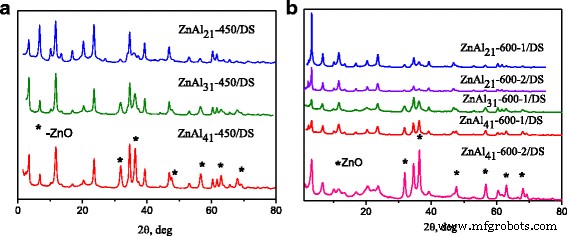
450°Cで焼成されたLDHの再構築によって得られたDS修飾Zn-AlLDHのX線回折パターン( a )および600°C( b )
Zn-Al LDHについて記録された熱重量分析トレースは、すべてのZn / Al比で非常に類似していた。 Zn / Al =4:1のサンプルのTG、DTA、およびDTG曲線を図3に示します。LDH-炭酸塩のTGAプロット(図3a)は、60〜190の温度範囲で質量の損失を示しました。 190〜300、および300〜500°C。最初のステップでの質量損失は、物理吸着された層間水の放出に関連するハイドロタルサイトの一般的な特性です。 2番目の質量損失は、脱ヒドロキシル化の最初のステップと、中間層からの炭酸イオンの除去に起因していました。この温度範囲で、ハイドロタルサイトは脱炭酸および脱ヒドロキシル化反応を起こし、金属酸化物が形成されました。 500°Cを超える温度で発生した質量損失の3番目のステップでは、質量損失は完全な脱ヒドロキシル化と、残っている層間アニオンの除去による構造の崩壊として認識されました[28]。 500〜1000°Cで観察されたわずかな質量損失は、混合酸化物微結晶に強く吸着されたいくつかの炭酸塩アニオンの損失に起因する可能性があります[29]。
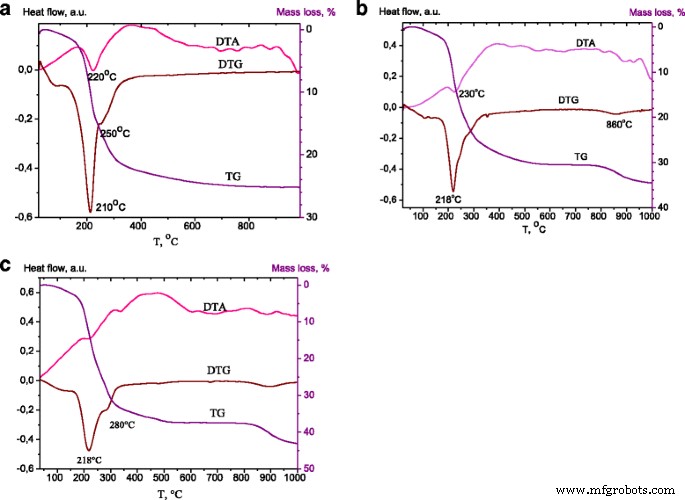
ZnAl 41 のTG、DTA、およびDTG曲線 LDH( a )、ZnAl 41 -450 / DS( b )、ZnAl 41 -600-1 / DS( c )
調査したすべてのZn-AlLDHの熱分解段階を表1に示します。電荷密度の低い材料には炭酸塩アニオンが少ないため、ZnAlLDHのZn / Al比が増加すると、総質量損失は減少します。さらに、ZnAl 31 として LDHとZnAl 41 LDHにはZnOの相が含まれており、サンプルに存在する金属水酸化物と層間炭酸イオンの量は少なかった。したがって、ZnAl 31 の脱ヒドロキシル化と脱炭酸化のプロセス LDHとZnAl 41 LDHはZnAl 21 ほど集中的ではありませんでした LDH。
<図>ZnAl 41 について記録された熱重量トレース -図3bに示されている450 / DS。熱分解の最初のステップは、層間水の損失に起因していました。分解の第2段階であるブルーサイト様シートの脱ヒドロキシル化には、DSの破壊が伴いました。 DSイオンの分解は210〜250°Cの範囲で発生したため[30、31]、200°C未満ではより大きな損失が観察されました。 300〜500°CでのDS修飾LDHの質量損失は、完全な脱ヒドロキシル化と層状構造の崩壊によるものでした。この段階での質量損失の増加は、DSの負荷に起因し、その分解は400〜900°Cでの質量損失に反映されていました。 800〜900°Cでの質量損失は、SO 3 として認識できます。 第二の質量損失段階でのDSの分解によって形成された(Zn、Al)硫酸塩の分解による進化[32]。
ZnAl 31 の総質量損失 -450 / DSおよびZnAl 41 -450 / DSは、ZnAl 21 と比較して少なかった -450 / DSは、Zn / Al比が3:1および4:1のサンプルのDS挿入相の含有量が少ないことを示しています。これらのLDHのパターンにZnO反射が存在することは、DSの水溶液中の混合二重酸化物の再水和下でのLDHの不完全な再構築を示しています(図2a)。 [33]によると、LDHには余分な相が共存しています。合成および再水和されたままのZn-AlLDH(Zn:Al =2:1)には、約25および23 wt。%のアモルファス相が含まれていました[33]。著者らは、再水和されたサンプルにさらに約3wt。 ZnO相(ジンサイト)の%は、ブルーサイト様層からのZnの偏析に起因していました。おそらくZnAl 21 の変更 DSを伴うLDHは、アモルファス水酸化亜鉛相の追加の形成を引き起こしました。 [27]で示唆されているように、アモルファス水酸化亜鉛相の再構築の初期段階で再水和の予備反応があり、その後、再構築プロセス中にZn-Al酸化物の再水和が行われました。おそらく、アモルファス相の再水和は、炭酸塩挿入相の形成をもたらした。 DS溶液中のZn-Al酸化物の再水和により、DS挿入相が形成されました。 ZnAl 21 の質量損失 -600-1 / DS、ZnAl 31 -600-1 / DS、ZnAl 41 -600-1 / DSは著しく異なっていました。明らかに、600°Cで焼成されたZn-Al LDHには、アモルファス相が少なく含まれていました。
光活性ZnOの存在は、LDHおよびLDHベースの複合材料、特に光触媒、UVフィルター、色素増感太陽電池などの用途の範囲を拡大します。紫外線を吸収するZn-AlLDHの能力に対する相変態の影響を調べた。合成されたままのZn-AlLDH、焼成されたZn-Al LDH、およびZn:Al =2:1のサンプルのDS修飾Zn-Al LDHの吸光度スペクトルを図4a、bに示します。 450°Cおよび600°Cで1時間焼成した混合酸化物の再構築により、追加量の結晶性ZnOの形成が促進され、ZnAl 21 の吸収帯の赤方偏移が生じました。 -450 / DSおよびZnAl 21 -600-1 / DS(図4a、b)。 ZnAl 21 の吸収帯 -600-2は約35nmだけ可視光にシフトしました。 LDHを5時間煆焼した結果、Zn:Al =2:1の混合酸化物の吸光度に変化はありませんでした(図4b)。
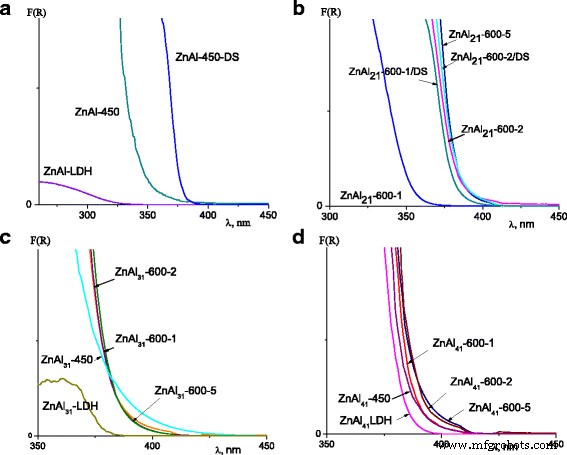
Zn / Al比が2:1( a )のZn-AlLDHのUV-Visスペクトル 、 b )、3:1( c )、4:1( d )
Zn:Al =3:1の混合酸化物の吸収帯の位置は、450°Cと600°Cで処理されたサンプルでほぼ同じであり、熱処理時間に依存しませんでした(図4c)。 Zn-Al LDHおよびZn:Al =4:1の混合酸化物の場合、吸収帯は382〜390 nmに位置していました(図4d)。
Al 2 以降 O 3 はワイドバンドギャップ(5.55 eV)材料であり、サンプルに含まれるZnOによって引き起こされるUV範囲の光の吸収であり、そのバンドギャップは3.37eVです[34]。バンドギャップエネルギーの値(E g )のサンプルは、次の式を使用してUV-visスペクトルの切片から計算されました:E g =1240 /λ[35](表3)。焼成されたZn-AlLDHの中で、バンドギャップエネルギーの値が最も低いのは、Znの含有量が最も多いサンプルでした(表3)。
光触媒研究
Zn-Al LDHの光触媒性能を評価するために、2 * 10 -5 水溶液の分解 UV光下でのMMB溶液を実施した。 Zn / Al比が2:1および3:1のLDHの光吸収能力が低いため、照射下での活性が低くなりました(表2)。
<図>ZnOを含むZnAl 41 他のLDHの中でもLDHは、MBの破壊においてより高い光触媒活性を示しました。形成されるZnO相の量が多いため、サンプルを450および600°Cで焼成すると、光触媒活性が大幅に向上しました。 600°Cで焼成したZn-AlLDHのMB光分解曲線を図5aに示します。焼成されたZn-AlLDHの光触媒性能の違いは、ZnO相によって引き起こされたため、Zn / Al比が4:1のLDHは、MB光破壊で最良の結果を示しました。
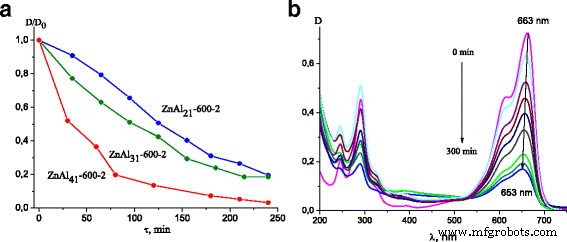
UV光照射下での焼成Zn-AlLDH上でのMBの分解曲線( a ); 2 * 10 -5 の吸収変化 ZnAl 31 での光分解プロセス中のMMB溶液 -600-1( b )
ZnAl 31 の存在下での異なる照射時間にわたるMB溶液の吸光度スペクトルの変化 -600-1は図5bで見ることができます。 610および663nmのピークは共役π系の吸収に割り当てられ、300nmに近いピークは芳香環の吸収に割り当てられました[36]。照射時間の増加に伴い、元のピークの強度が低下していることがわかりました。さらに、強度の平行した減少と663nmに位置するバンドのわずかな青方偏移も観察できました。これは、フェノチアジンのN-脱メチル化とそれに伴う分解によって引き起こされました[37]。 MBの吸光度スペクトルの同様の変化が、すべてのLDHを備えた光触媒システムで観察されました。
Zn-Al LDHのDS修飾は、界面活性剤と色素分子間の疎水性相互作用により、MBに対する親和性を高めました[26]。 ZnAl 41 -600-1 / DSは、MB吸着で最良の結果を示しました(表3)。有機/ Zn-Al LDHの光触媒活性は、煆焼されたZn-Al LDHと同等でした(表3)。 ZnAl 41 では、より高いレベルのMB劣化が観察されました。 -450 / DS。吸着によるDS修飾Zn-AlLDHによるMBの除去の値は、光破壊によるものよりも高かった。 したがって、有機/ Zn-Al LDHによるMBの吸着除去は、光照射を適用することで強化できます。
<図>おそらく、色素の光破壊は、実験条件下で固定されなかったDS修飾Zn-AlLDHの表面で発生しました。平衡に達した後、MBが吸着されたDS修飾Zn-AlLDHは強い青色を示しました。
結論
この作業では、さまざまなカチオン比の合成および焼成されたZn–AlLDHを準備しました。得られた材料を特性評価し、水溶液からカチオン染料MBを除去するために使用しました。 LDHと焼成LDHの両方でのUV光下でのMB光破壊の研究は、次のことを示しています。
Zn–Al LDHの光触媒活性は、ZnO相の存在に起因していました。 LDHでのZnO相の形成は、LDHでのZn / Al比の増加と、LDHの温度処理によって制御できます。
LDHの光触媒活性に対するZn / Al比の影響が支配的でした。合成されたままのZnAl 41 の現在におけるMBの光分解 LDHとZnAl 41 600°CでのLDHはそれぞれ72%と95%でした。 600°Cでの煆焼用ZnAl 31 LDHとZnAl 21 LDH、MBの光分解はそれぞれ76%と74%でした。
有機/ Zn-AlLDHはカチオン染料MBに対して高い吸着能力を示した。彼らはまた、MB破壊における光触媒活性を示しました。したがって、DSで修飾されたZn-Al LDHを含む溶液からのMBの吸着除去は、UV照射を使用することで強化できます。
ナノマテリアル
- MoO3でコーティングされたTiO2ナノチューブ光電極上のAu-プラズモンナノ粒子によって強化された光触媒活性
- 光触媒性能が向上した新規Bi4Ti3O12 / Ag3PO4ヘテロ接合光触媒
- 光触媒活性が強化されたAgナノ粒子/ BiV1-xMoxO4の相乗効果
- 層状複水酸化物(LDH)ベースのナノ材料へのCO2吸着に関する新しい洞察
- Er3 + -Yb3 + -Li +トリドープTiO2のアップコンバージョン材料によるペロブスカイト太陽電池の電力変換効率の向上
- 全炭素3Dナノ濾過膜による水からの抗生物質の除去
- Al / PTFEナノラミネートとの統合に基づく強化されたエネルギー性能
- 高速セレニル化アプローチによるSb2S3平面ヘテロ接合太陽電池の強化された光起電力特性
- 効果的な光吸収が強化されたピン接合ナノコーンアレイ太陽電池の光起電力性能
- 高コンダクタンスのトポロジカル絶縁体ナノシートにおける非常に強化された光電流応答
- メチレンブルーの吸着特性が著しく向上した階層構造カオリナイトナノスフェア



