リチウムイオン電池用のザクロ型Fe2O3 / Cアノードの調製と電気化学的性質
要約
深刻な体積膨張と不十分なサイクル安定性のために、遷移金属酸化物アノードはまだ商業的利用を満たしていません。ここでは、コアシェルザクロ型のFe 2 の合成方法を示します。 O 3 初めてワンステップ水熱プロセスによる/ Cナノコンポジット。電気化学的性能は、リチウムイオン電池のアノード材料として測定されました。 705 mAh g -1 を維持する優れたサイクリングパフォーマンスを発揮します 100 mA g -1 で100サイクル後の可逆容量 。アノードはまた、480 mAh g -1 の放電容量で良好なレート安定性を示しました。 2000 mA g -1 の速度でサイクリングする場合 。優れたLi貯蔵特性は、活性Fe 2 の良好な電気伝導性を保証できるだけでなく、独自のコアシェルザクロ構造に起因する可能性があります。 O 3 、だけでなく、サイクル中の大きな体積変化に対応し、Liイオンの高速拡散を促進します。
背景
リチウムイオン電池(LIB)は、高性能のグリーン化学電源として、エネルギー密度が高く、サイクル寿命が長く、自己放電が少なく、電気自動車がないため、ポータブルモバイルエレクトロニクス市場や電気自動車で広く使用されています。メモリー効果[1]。ただし、時代の発展とともに、グラファイト材料に基づく従来のLIBは、理論容量が低いため(372 mAh g -1 )、高エネルギー密度と電力密度の増大する要件を満たすことができなくなりました。 )グラファイト材料の[2]。遷移金属酸化物(TMO)は、市販のグラファイトよりも優れた比容量を達成することを目的として、過去数十年にわたって繁栄してきました[3、4]。通常、Fe 2 O 3 理論容量が高い(1007 mAh g -1 )ため、最も有望なアノード候補の1つと見なされています。 )、環境にやさしい性質、非毒性、および天然存在比[5、6]。しかし、その大きな可能性にもかかわらず、LIBでの商用アプリケーションは、放電/充電プロセス中の高速容量フェージングやボリューム拡張[7]などのいくつかの重大な欠点によって依然として妨げられています。
上記の問題を克服し、電気化学的性能を改善するために、さまざまな最適化戦略が提案されてきました。広く受け入れられている戦略[8]は、ナノ構造の複合電極の設計です。これは、大きなひずみにうまく対応するだけでなく、リチウムイオンの挿入/抽出のための短い拡散経路も提供します。現在までに、多くのナノ構造のFe 2 O 3 ナノ粒子、ナノロッド、ナノワイヤー、ナノチューブなどの材料は、さまざまな方法で設計および製造されています[9、10、11、12、13、14、15]。ナノ構造の助けを借りて、Fe 2 の体積膨張 O 3 効果的に対応することができます。さらに、TMOベースのLIBパフォーマンスは、最近、導電性マトリックスにナノ構造のTMOを導入することによってさらに改善されました[15、16、17、18、19]。たとえば、Fe 2 へのカーボンコーティング層の導入 O 3 コアは、電気伝導率を効果的に高め、Fe 2 の亀裂や崩壊を抑制する炭素層の能力により、広く研究されてきました。 O 3 サイクリング時のアノード。趙ら[20]準備されたFe 2 O 3 ナノ粒子と酸化グラフェンは、それぞれ水熱法とハマーズ法[21]によるものです。次に、グラフェン-Fe 2 O 3 複合材料は凍結乾燥プロセスによって得られた。一部のFe 2 O 3 カーボンナノチューブ@Fe 2 などの–Cコアシェル複合材料 O 3 @ C、Fe 2 O 3 @C中空球、およびFe 2 O 3 @グラファイトナノ粒子は、熱水反応と高温煆焼プロセスを含む2段階の合成方法によって製造されました[22、23、24]。これらの複合材料は、優れたLi貯蔵特性を示しています。ただし、これらの複合材料の複雑な準備プロセス、長い処理時間、および高コストは、それらのさらなる用途を制限します。したがって、Fe 2 のより単純なアプローチを開発する O 3 –Cコアシェル構造が緊急に必要です。
ここでは、Fe 2 の合成について報告します。 O 3 /カーボンコア-単純なワンステップ水熱プロセスによるシェルナノコンポジット。結果として生じるFe 2 O 3 / Cナノコンポジットは、ザクロのような構造を持ち、Fe 2 O 3 カーボンシェルにカプセル化され、すべてのコアシェルがザクロとして相互に接続されています。このユニークな多孔質ザクロ構造は、活性鉄 2 の良好な導電性を保証するだけではありません。 O 3 、だけでなく、サイクル中の大きな体積変化に対応し、Liイオンの高速拡散を促進します。その結果、アノードをLIBで使用すると、パフォーマンスが大幅に向上しました。
メソッド
硝酸鉄非水和物(Fe 3 (NO 3 ) 3 ・9H 2 O)、無水デキストロース(C 6 H 12 O 6 )、無水エタノール(CH 3 CH 2 OH)、ポリフッ化ビニリデン(PVDF)、および N -メチル-2-ピロリドン(NMP)は、中国のTianjin Fuchen Chemical ReagentsFactoryから購入しました。脱イオン水(H 2 O)河北工業大学から提供されました。
ザクロの形をしたFe 2 O 3 / Cナノコンポジットは水熱法で調製しました。まず、1.212 g Fe 3 (NO 3 ) 3 ・9H 2 Oおよび0.9g C 6 H 12 O 6 C 6 の炭素の比率である30分間のマグネチックスターラーにより、40mLの脱イオン水に溶解しました。 H 12 O 6 Fe 3 でアイロンをかける (NO 3 ) 3 ・9H 2 Oは10:1です。次に、溶液を100 mlのテフロンで裏打ちされたオートクレーブの容量で密封し、190°Cで9時間加熱し、自然に室温まで冷却しました。次に、水熱合成生成物を取り出し、脱イオン水で遠心分離した。最後に、製品を60°Cの恒温乾燥チャンバーで12時間乾燥させました。
サンプルの相組成は、Cu-Kα線(λ)を使用したRigaku D / Max 2500 V / pcX線回折計での粉末XRDによって調査されました。 =1.5406Å)スキャン範囲(2 θ )20〜70°および0.02°のスキャンステップ。ラマンスペクトルは、in ViaReflexラマンイメージング顕微鏡システムを使用して532nmのArイオンレーザーで取得されました。ザクロ型のFe 2 の炭素含有量 O 3 / Cナノコンポジットは、熱重量分析(TGA; TA Instruments、SDTQ600)法[22、24]によって推定され、加熱後の重量変化が示されました。炭素の重量比は45.2wt%と計算されました。サンプルの形態は、走査型電子顕微鏡(SEM)(JEOL JSM-6700F)によって実行されました。微細構造はJEOLJEM-2100F透過型電子顕微鏡(TEM)で特性評価され、サンプルの元素組成はエネルギー分散型X線分光法(EDS)で分析されました。元素とその原子価状態は、X線光電子分光法(XPS; VG ESCALAB MK II、VG Scientific)によって分析されました。
電気化学的性能を調査するために、活物質(80 wt%)、Super-P(10 wt%)、およびポリフッ化ビニリデン(PVDF、10 wt%)を N に混合しました。 -メチル-2-ピロリドン(NMP)でスラリーを形成します。次に、スラリーをCu箔基板にコーティングし、100°Cで6時間乾燥させました。作用電極として活物質を使用し、対電極としてLi金属箔を使用しました。1molL -1 LiPF 6 エチレンカーボネート(EC)とジメチルカーボネート(DMC)(体積比1:1)を電解質として使用し、Celgard 2300をセパレーターとして使用し、CR2025コイン電池をアルゴン雰囲気のグローブボックスに組み立てました。サイクリングテストは、電流密度100 mA g -1 で0.01〜3.00 VのCT-4008バッテリーサイクラーシステムを使用して、25°Cでテストされました。 100サイクル。さまざまな電流密度でのレートテスト(100 mA g -1 でそれぞれ10サイクル 、200 mA g -1 、500 mA g -1 、および2000 mA g -1 )の後に、100 mA g -1 での追加のサイクルテストが続きました。 。サイクリックボルタンメトリー(CV)は、電気化学ワークステーション(Zahner Im6e)で、0.5 mV s -1 のスキャン速度で実行されました。 0.01〜3 Vの電位範囲(vs. Li / Li + ) 室温で。比較のために、Fe 2 の電気化学的性能 O 3 ナノスフェア(25〜50 nm、CAS番号1309-37-1、Shanghai Aladdin Biochemical Technology Co. Ltd.から購入)も同じ測定パラメータを使用してテストされました。
結果と考察
Fe 2 の結晶構造 O 3 / CナノコンポジットはXRDによって確認され、その結果が図1aに示されています。 Fe 2 のXRDパターンがわかります。 O 3 / Cナノコンポジットは、Fe 2 のヘマタイト結晶構造としてインデックス化できます。 O 3 (JPDS番号33-0664)。 Fe 2 の回折ピーク O 3 (012)、(104)、(110)、(006)、(113)、(024)、(116)、(018)、(214)、(300)、および(208)の結晶面は明確になります観察された。炭素の結晶化温度よりも低い熱水反応温度(190°C)のため、炭素の回折ピークは検出されません。
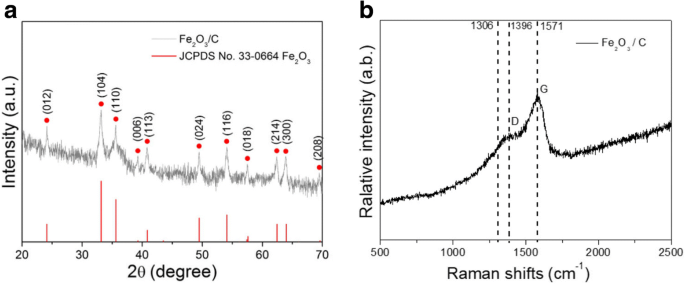
a Fe 2 のXRDパターン O 3 / Cナノコンポジット。 b Fe 2 のラマンスペクトル O 3 / Cナノコンポジット
ラマン測定は、Fe 2 の形成を確認するために使用されます O 3 / Cナノコンポジット。図1bに示すように、ラマンスペクトルは、1306 cm -1 付近にピークを示します。 Fe 2 の特徴であるヘマタイト2マグノン散乱に関連する O 3 。そのため、Fe 2 O 3 Fe 2 のピークであるカーボンでコーティングされていました O 3 明らかではありません[25]。 1396 cm -1 のピーク および1571cm -1 それぞれ特徴的なカーボンDバンドとGバンドのピークです。前者は無秩序な炭素に対応し、後者は2D-グラファイトに割り当てられます。 DバンドとGバンドの強度比(ID / IG)の値が低いということは、グラファイト状炭素の相対量が多く、炭素層の電気伝導率が高いことを意味します。これは、Fe 2 の伝導性に有益です。 O 3 / Cナノコンポジット。
製品の化学組成と原子価状態をさらに評価するために、XPS調査スペクトルを図2に示します。図2aは、Fe 2 のXPS完全スキャンスペクトルを示しています。 O 3 / Cナノコンポジット。 C 1s、O 1s、およびFe 2pコアの光イオン化信号と、FeAugerおよびOAuger信号を明確に見つけることができます。 Fe2pコアレベルのXPS高解像度スキャンを図2bに示します。 711.6および725.2eVのピークがFe2p 3/2 に対応することが示されています。 およびFe2p 1/2 それぞれFe2pスペクトルで。結合エネルギーの差は13.6eVであり、Feの3価の酸化状態と一致しています[26]。 Fe 2 のC1sスペクトル O 3 / C(図3c)は、C–C / C =C(284.2 eV)、C =O(287.3 eV)、およびO–C =O(290.4 eV)グループの3つの炭素含有官能基を示しています。 O 1sスペクトル(図3d)にFe–O–C結合(533.4 eV)が存在することは、Fe 2 間に強い界面相互作用(Fe–O–C結合)が存在することを示しています。 O 3 および炭素ベースのマトリックス。
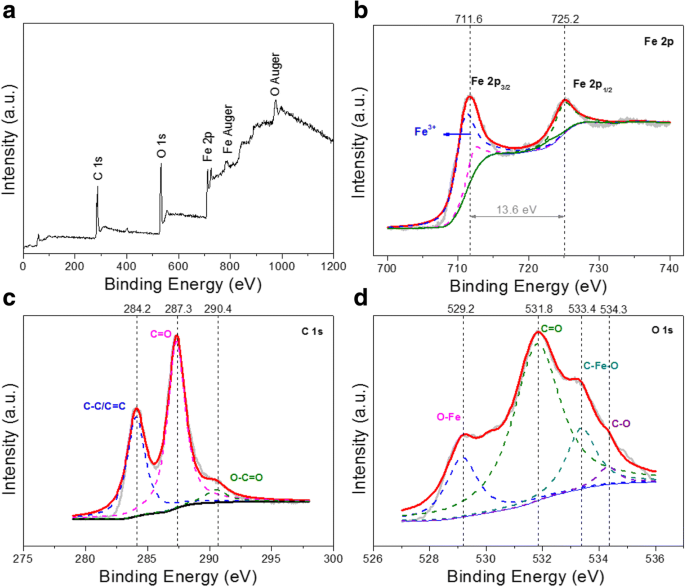
a Fe 2 のXPS調査スペクトル O 3 / C、 b Fe 2p、 c C 1s、および d O1sスペクトル
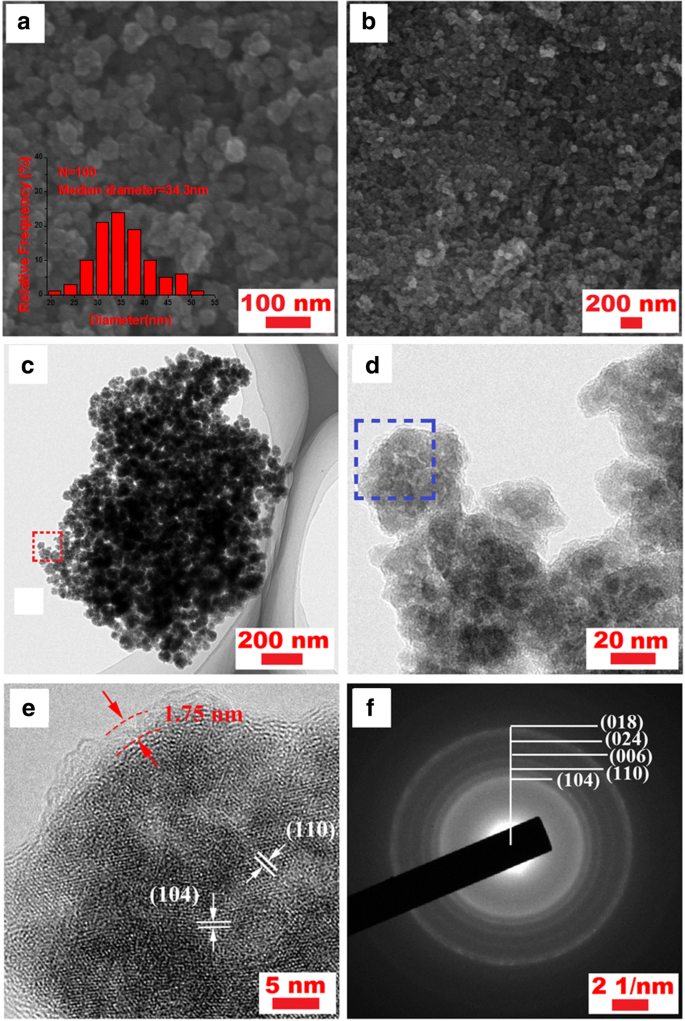
a 、 b Fe 2 のSEM画像 O 3 / Cナノコンポジット;挿入図:Fe 2 の細孔径分布 O 3 / Cコンポジット。 c 、 d Fe 2 のTEM画像 O 3 / Cナノコンポジット。 e 高分解能TEM画像と f Fe 2 の対応するSAEDパターン O 3 / C
Fe 2 のSEM画像 O 3 / Cナノコンポジットを図3a、bに示します。 30〜40nmの均一なサイズの球状ナノ粒子が均一に分散していることは明らかです。粒子間には多くのスペースが残っており、3D導電性構造を形成しています。 Fe 2 の平均直径 O 3 挿入図3aに示すように、/ C粒子は34.3nmであることがわかりました。
Fe 2 に関するより詳細な情報 O 3 / Cナノコンポジットは、TEM画像によってさらに監視されます(図3)。図3c、dに示すように、Fe 2 O 3 ナノ粒子はカーボンシェル内に十分に囲まれており、ザクロのコアシェル構造を意味します。 Fe 2 の高分解能透過型電子顕微鏡(HRTEM)分析によると O 3 / Cコアシェルナノ粒子(図3e)、Fe 2 の結晶面 O 3 (104)、(012)0.33nmと0.27nmの距離間隔で明確に見つけることができます。これは、上記のXRDテスト結果と一致しています。また、Fe 2 O 3 ナノ粒子は、約1.75nmの厚さの炭素層で十分に覆われています。対応する選択領域電子回折(SAED)パターンは、サンプルの多結晶回折リングがFe 2 に対応することを確認します。 O 3 図3fに示すように、平面。
図4aは、0.1 mV s -1 のスキャンレートで0.01〜3.0Vの電圧範囲でのCVプロットを示しています。 。最初のサイクルでは、約0.7Vの陰極ピークがFe 3+ の会話であると考えられていました。 Fe 0 へ 0.1 V付近のブロードなピークは、Li + に関連している可能性がありますが、固体電解質中間相(SEI)膜の形成も同様です。 炭素へのイオン挿入とLiC 6 の形成 [27]。 1.75 Vでの主要な陽極ピークは、Fe 0 の酸化に起因する可能性があります。 からFe 3+ 。関連する反応は、式(1)で表すことができます。 (1)[27]:
$$ {\ mathrm {Fe}} _ 2 {\ mathrm {O}} _ 3 + 6 {\ mathrm {Li}} ^ {+} + 6 {\ mathrm {e}} ^ {\ hbox {-}} \ leftrightarrow 2 \ mathrm {Fe} +3 {\ mathrm {Li}} _ 2 \ mathrm {O} $$(1)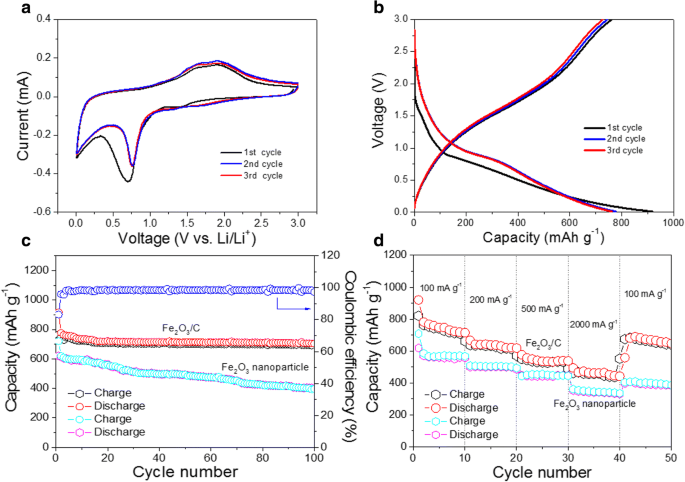
サイクリックボルタモグラム( a )および電圧プロファイル( b )Fe 2 の O 3 / Cは、1番目、2番目、および3番目のサイクルで合成されます。 c Fe 2 のサイクル性能 O 3 / CおよびFe 2 O 3 100 mA g -1 のナノ粒子 。 d Fe 2 のレート機能 O 3 / CおよびFe 2 O 3 電流密度が100〜2000 mA g -1 のナノ粒子
次のサイクルでは、陰極ピークと陽極ピークの両方の位置がより高い電位(それぞれ、0.8Vと1.78V)にシフトしました。これは、Fe 2 の反応速度の改善に起因する可能性があります。 O 3 構造の再調整と電気化学的活性化後の電極。一方、CV曲線の強度はわずかに低下しました。これは、電極と電解質との電気的接触が改善され、安定したSEI膜が形成されたためと考えられます。さらに、次のサイクルでオーバーラップしたCV曲線は、良好な電気化学的可逆性を意味しました。
Fe 2 の最初の3回の充電/放電サイクルの結果 O 3 100 mA g -1 の定電流密度の/ C電極 図4bに示されています。 Fe 2 の最初の放電容量 O 3 / Cは917mAh g -1 たった760mAh g -1 充電中。容量の損失は、固体電解質中間相(SEI)膜の必然的な形成によって引き起こされる可能性があります。 2番目と3番目のサイクルの可逆容量は776と763mAh g -1 それぞれ。優れたサイクル安定性を示します。
100 mA g -1 の電流密度での電極のサイクル性能 図4cに示します。 Fe 2 の2番目の放電容量 O 3 / Cは776mAh g -1 、および100サイクル後、電極は705 mAh g -1 の比容量を保持しました。 、これは2番目の放電容量の約90%であり、良好なサイクリング性能を示しています。また、100サイクル後のクーロン効率はほぼ100%であり、優れた電気化学的性能がさらに確認されています。 Fe 2 のレートパフォーマンス O 3 / C、電流密度が100〜2000 mA g -1 図4dに表示されます。充電容量は710mAh g -1 で、良好なレート能力を示しました。 、620 mAh g -1 、580 mAh g -1 、および480 mAh g -1 100 mA g -1 、200 mA g -1 、500 mA g -1 、および2000 mA g -1 、 それぞれ。レートが100mA g -1 に戻ったとき 、電極の容量は680 mAh g -1 に戻りました。 、優れたレート機能を示しました。優れた電気化学的性能は、主にコアシェルの構造安定性の向上に起因し、カーボンは導電率を向上させます。すべてのコアシェル構造はザクロとして接続され、電子伝達を改善して導電率を改善し、構造の安定性を高めることもできます。
図4c、dは、Fe 2 のサイクリングパフォーマンスも示しています。 O 3 100 mA g -1 のナノ粒子アノード 。 Fe 2 の最初の放電容量 O 3 ナノ粒子は約720.9mAh g -1 、ただし100サイクル後、396.5 mAh g -1 の特定の容量しか保持されませんでした 。そして、Fe 2 のレートパフォーマンス O 3 100〜2000 mA g -1 の範囲の電流速度でのナノ粒子 図4dに示されています。 Fe 2 の容量 O 3 アノードは570mAh g -1 、505 mAh g -1 、450 mAh g -1 、および345 mAh g -1 100 mA g -1 、200 mA g -1 、500 mA g -1 、および2000 mA g -1 、 それぞれ。レートが100mA g -1 に戻ったとき 、電極の容量は395 mAh g -1 に戻りました。 。したがって、Fe 2 の電気化学的速度とサイクリング性能 O 3 ナノ粒子アノードはFe 2 の60%ほど良くありません O 3 / Cアノード。これは主にFe 2 の体積膨張によるものです。 O 3 充電および放電プロセス中のナノ粒子。
理論容量( C theo。 )得られたザクロの形をしたFe 2 O 3 / Cアノードは C theo。 = C Fe2O3、theo。 ×Fe 2 O 3 %+ C カーボン、テオ。 ×カーボン%=1007×54.8%+ 372×45.2%=720 mAh g -1 。 100 mA g -1 での充電/放電サイクル後 100サイクルの間、放電容量は約705 mAh g -1 のままでした。 、理論容量よりわずかに低いです。これらの大容量は、Fe 2 間の相乗的相互作用に起因する可能性があります。 O 3 とカーボン。
図5は、Fe 2 の電気化学的インペンデンス分光法(EIS)を示しています。 O 3 およびFe 2 O 3 100サイクル前後の/ C電極。ナイキスト線図の高周波半円は電極の電荷移動抵抗に関連していますが、低周波の傾斜線は、Liイオンの活物質拡散へのウォーバーグインピーダンスを示しています。半円が小さいほど、電極の電荷移動抵抗が低くなることはよく知られています。明らかに、コアシェルザクロ型のFe 2 の半円の直径 O 3 サイクル前後の/ CコンポジットはFe 2 よりもはるかに小さい O 3 対応する状態の造影剤。コアシェルのザクロ型のFe 2 O 3 / C複合電極は、アノード材料として使用した場合、裸のFe 2 よりも低い接触インピーダンスと電荷移動インピーダンスを持ちます。 O 3 サンプル。この結果は、Fe 2 の多孔質ザクロ型構造に起因する可能性があります。 O 3 / Cアノード。これにより、体積の変化に適応し、Li + を促進するためのスペースを増やすことができます。 リチウム化および脱リチウム化プロセス中のイオン拡散。
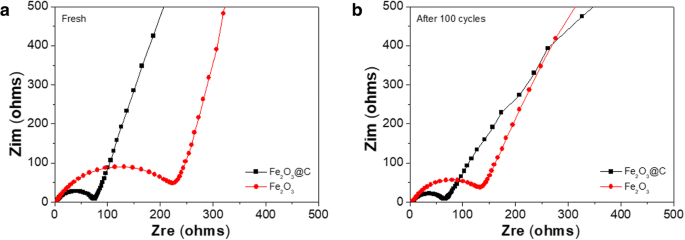
Fe 2 のナイキスト線図 O 3 およびFe 2 O 3 / C電極
得られたままのコアシェルザクロ型Fe 2 のLi貯蔵性能 O 3 / Cアノードおよび関連するFe 2 O 3 以前の文献で報告されている/ C資料は、表1に要約されています[27、28、29、30、31、32、33、34]。表から、ザクロの形をしたFe 2 O 3 / Cアノードは、報告されているほとんどのアノードよりもサイクリング後に高い容量を示します。リチウムイオン貯蔵における材料の優れた性能は、豊富な多孔性を備えた巨視的なザクロの形状の独特の構造と、微視的なコアシェルFe 2 に起因する可能性があります。 O 3 –C構造。これにより、アクティブなFe 2 の良好な電気伝導性を確保できます。 O 3 、サイクル中の大きな体積変化に対応し、Liイオンの高速拡散を促進します。
<図>結論
要約すると、ザクロの形をしたFe 2 の設計と合成に成功しました。 O 3 / C工業化を実現します。 Fe 2 O 3 ナノ粒子はカーボンシェル内に十分に封入されており、すべてのコアシェル構造はザクロとして相互に接続されています。これにより、放電/充電プロセス中のアノードの安定性が向上するだけでなく、リチウム反応速度も向上します。この構造により、体積膨張が大幅に減少し、電解質の拡散が良好になります。したがって、Fe 2 O 3 LIBのアノードとしての/ C複合材料は、優れたリチウムイオン貯蔵性能を示します。
略語
- TMO:
-
遷移金属酸化物
- Fe 2 O 3 / C:
-
Fe 2 O 3 /カーボン
- Fe 3 (NO 3 ) 3 ・9H 2 O:
-
硝酸鉄非水和物
- C 6 H 12 O 6 :
-
無水デキストロース
- CH 3 CH 2 OH:
-
無水エタノール
- PVDF:
-
ポリフッ化ビニリデン
- NMP:
-
N -メチル-2-ピロリドン
- LIB:
-
リチウムイオン電池
- XRD:
-
X線回折
- SEM:
-
走査型電子顕微鏡
- TEM:
-
透過型電子顕微鏡
- HRTEM:
-
高分解能透過型電子顕微鏡
- EDS:
-
エネルギー分散型X線分光法
- XPS:
-
X線光電子分光法
- EC:
-
エチレンカーボネート
- DMC:
-
炭酸ジメチル
- CV:
-
サイクリックボルタンメトリー
- SAED:
-
選択領域電子回折
- SEI:
-
固体電解質中間相
- EIS:
-
電気化学的インペンデンス分光法。
ナノマテリアル
- コバルトをドープしたFeMn2O4スピネルナノ粒子の調製と磁気特性
- TiO2ナノ流体に向けて—パート1:準備と特性
- リチウムイオン電池用のCr3 +およびF-複合ドーピングを用いたLiNi0.5Mn1.5O4カソード材料の合成と電気化学的性質
- In VivoCTイメージングおよび腎クリアランス特性のための新しい生体適合性AuNanostars @PEGナノ粒子
- PPy被覆MnO2ハイブリッドマイクロ材料の調製とリチウムイオン電池のアノードとしてのそれらの改善されたサイクル性能
- Cu / Ti3SiC2 / Cナノコンポジットの微細構造と機械的性質に及ぼすグラフェンとMWCNTの相乗効果
- 着色された低温顔料用のCrドープTiO2の構造的および可視近赤外光学特性
- 水性ナトリウムイオン電池用の高電気化学的性能材料としてのNa4Mn9O18 /カーボンナノチューブ複合材料
- 分子線エピタキシー法を用いたGeBi膜の作製と光学的性質
- コンピュータとバッテリー用の高度な冷却システム
- パンチに使用する鋼材と工具の特性



