アトラジンの高感度検出のための新しい磁気弾性ナノバイオセンサー
要約
ここでは、最初に、競合イムノアッセイを使用してアトラジンを高感度で検出するための、ME材料と金ナノ粒子(AuNP)に基づくワイヤレス磁気弾性(ME)ナノバイオセンサーについて報告します。時変磁場に応答して、ME材料はその共振周波数で縦方向に振動します。これはその質量負荷の影響を受ける可能性があります。 ME材料上のAuNPsコーティングの層は、その生体適合性、安定性、および感度に貢献します。アトラジン抗体は、プロテインAを介してAuNPsでコーティングされたME材料表面に固定化され、ナノバイオセンサーの性能を向上させました。原子間力顕微鏡(AFM)分析は、アトラジン抗体の固定化が成功したことを証明しました。さらに、感度を高めるために、アトラジン-アルブミンコンジュゲート(Atr-BSA)を誘導して、アトラジン抗体との結合についてアトラジンと競合させ、シグナル応答を増幅させました。共振周波数シフトは、1 ng / mLから100μg/ mLの範囲のアトラジン濃度の対数に反比例および線形に比例し、感度は3.43Hz /μgmL -1 検出限界は1ng / mLで、米国環境保護庁(EPA)によって確立された基準よりも大幅に低くなっています。実験結果は、MEナノバイオセンサーがアトラジンに対して強い特異性と安定性を示したことを示した。この研究は、アトラジンを迅速、選択的、高感度で検出するための新しい便利な方法を提供します。これは、水質モニタリングやその他の環境検出分野でのアプリケーションに影響を及ぼします。
はじめに
産業と農業の急速な発展に伴い、ますます多くの環境汚染物質が生態学的環境に放出され[1]、関連する研究についての広範な懸念を引き起こしました[2、3]。近年、除草剤は農業分野の品質と収量を改善するためにますます多く使用されていますが、多くの除草剤は何年もの間水や土壌で活性を維持し、深刻な環境汚染を引き起こします[4]。除草剤の汚染は、水や農産物の生態学的汚染のためにかなりの注目を集めています[5]。除草剤の中で、アトラジン(2-クロロ-4-エチルアミノ-6-イソプロピルアミノ-1,3,5-トリアジン)は、世界中の広葉植物およびイネ科雑草防除に最も広く使用されています[6]。
アトラジンは、一部の多年生雑草に対して一定の抑制効果がありますが、環境汚染物質として非常に毒性が高く[7]、人間や他の動物種に健康上のリスクをもたらす可能性があります[8]。アトラジンを長期間高濃度で摂取すると、癌、先天性欠損症、心臓や肝臓の損傷など、動物や人間の健康を損なう可能性があります[9、10]。米国、欧州連合、および日本はすべて、内分泌かく乱化学物質のリストにアトラジンを含めています[11]。米国では、環境保護庁(EPA)が、飲料水中のアトラジンの許容限度である3μg/ L(生涯健康勧告レベル)を許可しています[12]。したがって、低濃度のアトラジンを正確に定量化する必要があります。
質量分析と組み合わせたLC(LC–MS)[13]、高速液体クロマトグラフィー(HPLC)[14]、質量分析と組み合わせたガスクロマトグラフィー(GC–MS)など、多くの従来の分析技術がアトラジン検出用に開発されました。 )[15]ですが、これらのメソッドには、高コスト、大型機器の必要性、選択性の低さ、時間のかかる[16]などの制限もあります。
ワイヤレスの質量に敏感なプラットフォームとして、ME材料で作られた磁気弾性(ME)センサーは、低コスト、高感度、小型、使いやすさという重要な利点により、さまざまなアプリケーション向けに広く開発されています[17、18]。現在、MEセンサーは通常、Metglas 2826 MB(Fe 40 )などのアモルファス強磁性合金材料でできています。 Ni 38 Mo 4 B 18 )[19]。外部から印加された交流磁場と静磁場の下で、ME材料はその共振周波数で縦方向に振動し[20]、直接の物理的接続なしでピックアップコイルによって無線で検出できる磁束密度を生成します[21]。式によると。 (1)[22]、基本共振周波数 f 0 材料の長さによって異なります L 、密度ρ 、弾性率 E 、およびポアソン比 v 。
$$ {f} _0 =\ frac {1} {2L} \ sqrt {\ frac {E} {\ rho \ left(1- {v} ^ 2 \ right)}} $$(1)小さな追加の質量負荷 ∆m 質量 M のME材料表面に堆積 ( ∆m ≪ M )共振周波数のシフトを引き起こします( ∆f )、これは式で与えられます。 (2)[23]。
$$ \ frac {\ Delta f} {\ Delta m} =-\ frac {f_0} {2M} $$(2)ME材料の上記の固有の特性に基づいて、ME材料の共振周波数は、余分な質量負荷の増加とともに減少します。このように、感知フィルムによる機能化を通じて、ME材料は、応力/圧力[24]、温度/湿度[25]、二酸化炭素[26]の検出など、物理的、化学的、および生物学的分析のために開発されました。エンドトキシン[27]、Salmonella typhimurium / Bacillus anthracis 胞子[28]、および Escherichia coli O157:H7 [29]。しかし、私たちの知る限り、アトラジンの検出にはME材料の適用は適用されていません。
本研究では、その優れた特性と利点を利用して、直接競合イムノアッセイに基づいてppbレベルでアトラジンを検出するために、最初にME材料を基板として、金ナノ粒子(AuNP)をコーティング層として使用するワイヤレスMEナノバイオセンサーを提案しました。手順。共有結合ランダム抗体固定化と比較して、共有結合指向の戦略は、ナノバイオセンサーの感度を改善するためにより有益です。プロテインAは、抗体のFc免疫グロブリン領域と特異的に結合する興味深い代替手段であるため、アトラジン抗体の配向固定化に使用され[30]、最高の固定化密度が得られ、抗原結合効率が向上し、ナノバイオセンサーの性能が向上します。 [31]。アトラジンの直接競合イムノアッセイは、AuNPsでコーティングされたME材料表面で共有修飾されたプロテインAに対するアトラジン抗体の配向固定化と、それに続くアトラジン-アルブミンコンジュゲート(Atr-BSA)およびアトラジンとアトラジン抗体の競合反応によって構築されました。 Atr–BSAは、信号応答を増幅するように誘導され、ナノバイオセンサーの感度を大幅に向上させました。 MEナノバイオセンサーの効率が評価され、微量濃度のアトラジンを検出するための新しいMEナノバイオセンサーの開発に成功したことが実証されました。
材料と方法
資料
アトラジン抗体、アトラジン-アルブミンコンジュゲート抗原(Atr-BSA)、アトラジン、およびプロテインAは、EastCoast Bio(メイン州、米国)から購入しました。シマジン、プロメトリン、およびジクロロジフェニルトリクロロエタン(DDT)は、Chengdu Huaxia Chemical Reagent Co.、Ltd。から入手しました。システアミン、1-エチル-3-(3-ジメチルアミノプロピル)カルボジイミド塩酸塩(EDC)、 N -ヒドロキシスルホスクシンイミド(NHS)、ウシ血清アルブミン(BSA、99%)、およびリン酸緩衝生理食塩水(PBSバッファー、pH =7.4)は、Sigma-Aldrich Corporation(セントルイス、ミズーリ州、米国)から購入しました。
MEナノバイオセンサーの製造
MEナノセンサープラットフォームの準備
Metglas合金2826(Fe 40 )で構成されたME素材のリボン Ni 38 Mo 4 B 18 )はHoneywell Corporation(Morristown、NJ、USA)から購入し、コンピューター制御のレーザー切断機を使用して5mm×1mm×0.028mmに切断しました。有機膜と破片を除去するために、MEリボンをアセトンとエタノールでそれぞれ10分間超音波洗浄し、脱イオン水ですすぎ、窒素流で乾燥させました(図1a)。クロムナノ粒子の約100nmの厚さの層が、AuNPとリボン表面の間の接着を強化するために、MEリボン表面の両側にスパッタされました。続いて、クロムでコーティングされたMEリボン表面の両面にAuNPをスパッタリングして、生体適合性を改善し、リボンを酸化や腐食から保護しました。図1の走査型電子顕微鏡(SEM)画像は、MEリボンにコーティングされたAuNPが球形であることを示しています。 AuNPと-SHは、Au-S結合を簡単に形成できます。低価格、非腐食性、生体適合性、および非毒性という魅力的な利点に加えて[32]、AuNPは化学的または生体認識要素の変更に優れたインターフェースを提供できます[33、34]。その後、MEリボンを200°Cの真空オーブンで2時間アニーリングして、残留内部応力を緩和し、AuNPs層のMEリボンへの接着を促進しました。その後、MEナノセンサープラットフォームが完成し、アトラジン抗体の固定化の準備が整いました(図1b)。
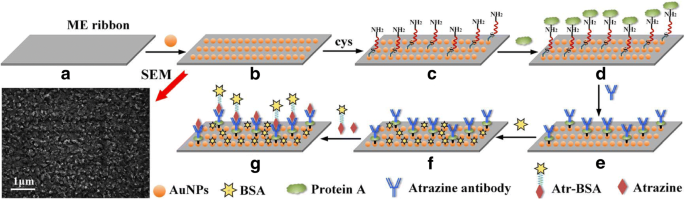
MEナノバイオセンサーの機能化の手順の概略図:( a )裸のMEリボン。 ( b )AuNPsコーティング; ( c )SAMレイヤー。 ( d )プロテインAの固定化; ( e )抗体修飾; ( f )BSAブロッキング; ( g )抗体と競合的に組み合わされたアトラジンおよびAtr–BSA。 AuNPsでコーティングされたナノセンサー表面のSEM画像
アトラジン抗体の固定化
AuNPsでコーティングされたナノセンサープラットフォームを、アセトン、イソプロパノール、脱イオン水、エタノールでそれぞれ5分間超音波洗浄し、窒素気流下で乾燥させました。次に、ナノセンサープラットフォームをシステアミン溶液(10 mM)に室温で12時間浸漬し、自己組織化単分子膜(SAM)を得ました(図1c)。プロテインA(1 mg / mL)は、4 mg / mL EDC-4 mg / mLNHSで室温で30分間活性化されました。その後、活性化プロテインAをSAM修飾ナノセンサー上で37°Cで30分間インキュベートし、PBSバッファーですすいだ(図1d)。次に、ナノセンサープラットフォームをアトラジン抗体と50分間インキュベートし、PBSバッファーで洗浄しました(図1e)。非特異的吸着を防ぐために、アトラジン抗体でコーティングされたナノセンサーをさらに0.5%BSAで30分間処理し、PBSバッファーでリンスして、結合していないBSAをすべて除去し、窒素気流下で乾燥させました。最後に、MEナノバイオセンサーをアトラジン検出用に製造しました(図1f)。
信号測定
MEナノバイオセンサーの共振周波数は、図2に概略的に示されているように、バイアルに巻かれたピックアップコイルとベクトルネットワークアナライザー(AV3620A、第41回CETC研究所、青島、中国)を使用して測定されました。磁場、ピックアップコイルに接続されたネットワークアナライザはS 11 で動作しました コイルに掃引周波数信号を提供するためのモードであり、コイルからの反射信号を監視できます。さらに、棒磁石によって生成された静磁場が、共振挙動を強化するために適用されました。ナノバイオセンサーは、テストする30μLのサンプル溶液を含むバイアルに垂直方向およびワイヤレスで(測定システムとのワイヤー接続なしで)挿入されました。すべての実験は、PBS(0.1 M、pH 7.4)溶媒システムで室温(25±2°C)で実施されました。ナノバイオセンサーの共振周波数は、S 11 の測定によって決定できます。 5分ごとに監視および記録されたパラメータ。
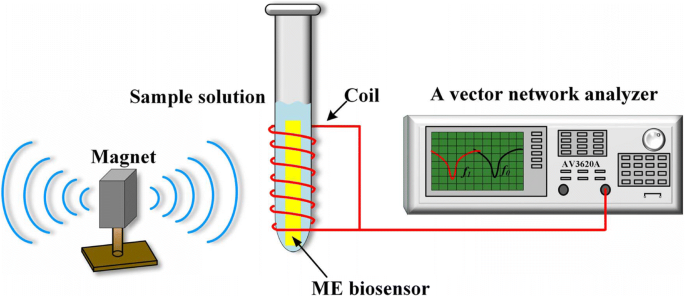
ワイヤレスMEナノバイオセンサー測定システムの概略図
結果と考察
ナノバイオセンサーの表面形態の特性評価
アトラジン抗体の固定化効果を調べるために、原子間力顕微鏡(AFM、ND-100、Park System、韓国)でナノバイオセンサー表面の観察を行いました。 AuNPsでコーティングされたナノバイオセンサーと抗体で修飾されたナノバイオセンサーの表面のAFM画像をそれぞれ図3a、bに示します。表面粗さの増加は、共有結合で固定化されたアトラジン抗体に起因することは明らかです。 AFM断面のトポグラフィーの包括的な分析は、AuNPsでコーティングされたナノバイオセンサーの高さの変動が13.421nmであることを示しています。ただし、抗体修飾後、値は28.425nmに増加しました。抗体分子の直径が約15nmであることはよく知られていますが、アトラジン抗体の固定化は成功していると明らかに結論付けられています。
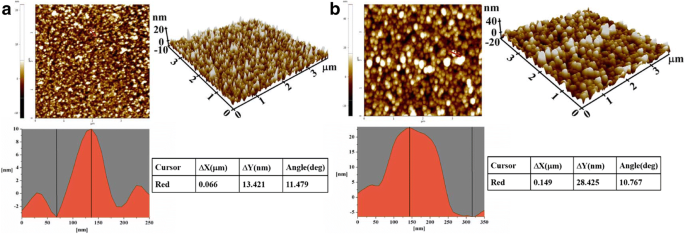
( a のAFM画像 )AuNPsコーティングおよび( b )抗体修飾ナノバイオセンサー表面
アトラジン抗体の濃度の最適化
抗体の固定化濃度は、ナノバイオセンサーの感度に重要な影響を及ぼします。したがって、アトラジン抗体の固定化濃度を変えて(25μg/ mL、50μg/ mL、75μg/ mL、100μg/ mL)、ナノバイオセンサーの共振周波数応答を評価する必要がありました。図4から、共振周波数シフトが50μg/ mLで最大に達したことがわかります。アトラジン抗体の濃度が75μg/ mLに達すると、立体障害と静電反発力により応答が低下し始めました[35]。つまり、50μg/ mLのアトラジン抗体は比較的飽和した固定化を達成できます。したがって、50μg/ mLが固定化に最適なアトラジン抗体の濃度でした。
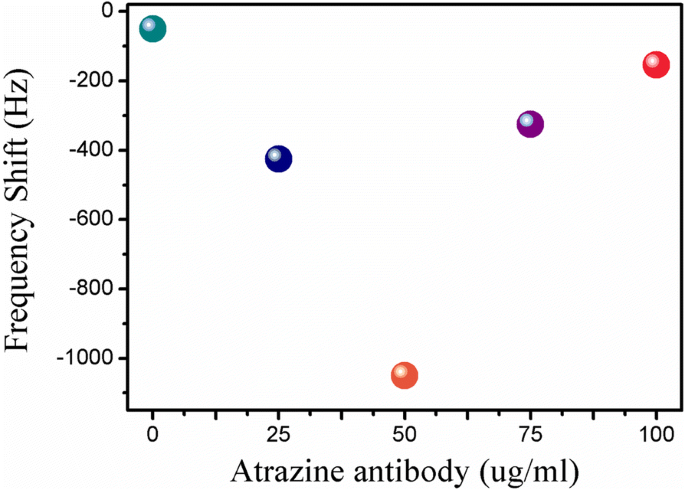
アトラジン抗体の固定化濃度が異なる場合のMEナノバイオセンサーの周波数応答(0μg/ mL、25μg/ mL、50μg/ mL、75μg/ mL、100μg/ mL)
Atr–BSAの濃度の最適化
免疫反応では、アトラジンとAtr–BSAは、ナノバイオセンサー表面の限られた数のアトラジン抗体部位をめぐって競合しました。したがって、固定化に最適なアトラジン抗体の濃度では、重要な要素としてのAtr–BSAの作業濃度が、ナノバイオセンサーの感度に影響を与えます。最適化プロセスは、さまざまな濃度(20μg/ mL、40μg/ mL、60μg/ mL、80μg/ mL)のAtr–BSAに対するMEナノバイオセンサーの共振周波数応答を決定することによって調査されました。図5に示すように、最大応答は40μg/ mLで観察されました。そのため、次の測定では40μg/ mLのAtr–BSAを使用しました。
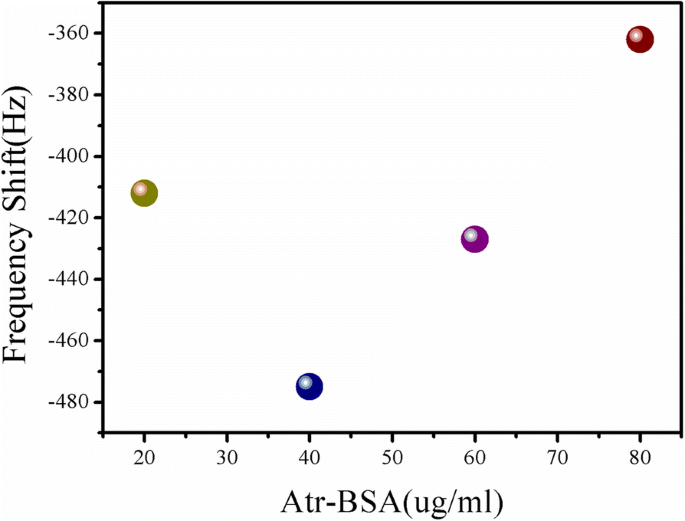
さまざまな濃度(20μg/ mL、40μg/ mL、60μg/ mL、80μg/ mL)のAtr–BSAに対するMEナノバイオセンサーの周波数応答
アトラジン検出
図6は、さまざまな濃度(0 ng / mL、1 ng / mL、10 ng)の15μLAtr–BSA(40μg/ mL)と15μLアトラジンのサンプル混合物で測定されたMEナノバイオセンサーのリアルタイム周波数応答を示しています。 / mL、100 ng / mL、1000 ng / mL、10μg/ mL、50μg/ mL、100μg/ mL)。図1gに示すように、アトラジンとAtr–BSAは、ナノバイオセンサー表面に固定化された抗体と競合的に結合します。これにより、ナノバイオセンサー表面の質量負荷が増加し、その結果、インキュベーションに伴う共振周波数が低下します。時間。図6から明らかなように、定常状態の応答は一般に約50分で達成されます。 Atr–BSA濃度とアトラジン抗体部位の数は固定されていたため、ナノバイオセンサーに結合したAtr–BSAの量は、溶液中のアトラジン濃度に反比例していました。 Atr–BSAの分子量は、アトラジンの分子量よりも大きくなっています。したがって、ナノバイオセンサーの共振周波数は、溶液中のアトラジンの濃度に反比例して変化します。図6に示すように、共鳴周波数シフトの速度と大きさは、アトラジン濃度の増加とともに減少し、アトラジンの濃度が高いほど、共鳴周波数シフトは小さくなります。図6の曲線*は、Atr–BSAに対するブランクコントロールセンサー(アトラジン抗体固定化なし)のバックグラウンド応答を表しています。これは、検出信号よりも約48 Hz低く、非特異的吸着を無視できることを示しています。したがって、アトラジン濃度は、ワイヤレスMEナノバイオセンサーの共振周波数シフトを通じて、反比例の関係で検出できます。
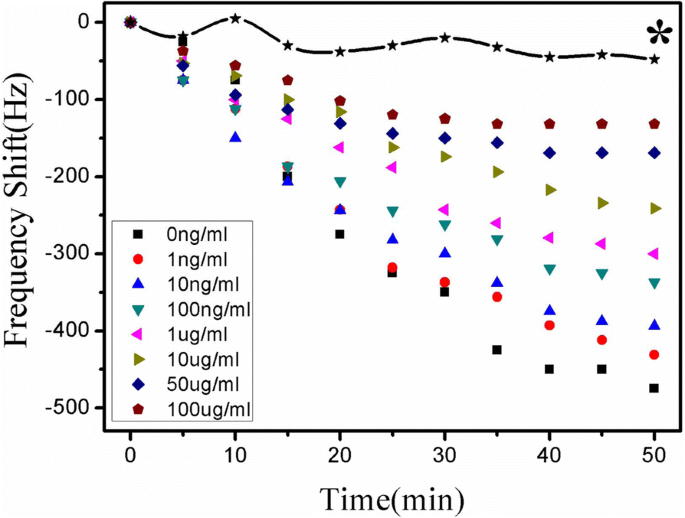
0〜100μg / mLの範囲のさまざまなアトラジン濃度でのリアルタイム周波数応答。 * Atr–BSAに対するブランクコントロール応答(アトラジン抗体固定化なし)
最初の50分間のMEナノバイオセンサーでのアトラジンの検出の標準検量線を図7に示します。各濃度について、ナノバイオセンサーのキャリブレーション実験を同じ条件下で5回実施しました。共振周波数シフトは、1 ng / mLから100μg/ mLの範囲のアトラジン濃度の対数値と線形であることがわかります。これはΔfで表すことができます。 =54.717log C アトラジン − 442.45( R 2 =0.971)。感度は3.43Hz /μgmL -1 と計算されます。 。図7から明らかなように、検出限界(LOD)は1 ng / mLであり、USEPAで規定されているアトラジンの上限である3μg/ Lよりも大幅に低く、現在利用可能な基準を満たしています。さらに、検出限界は以前に報告された方法よりも明らかに低い[36、37]。アトラジンのリアルタイム検出のために、低コスト、ワイヤレス、高感度のナノバイオセンサーが成功裏に確立されたことが実証されています。
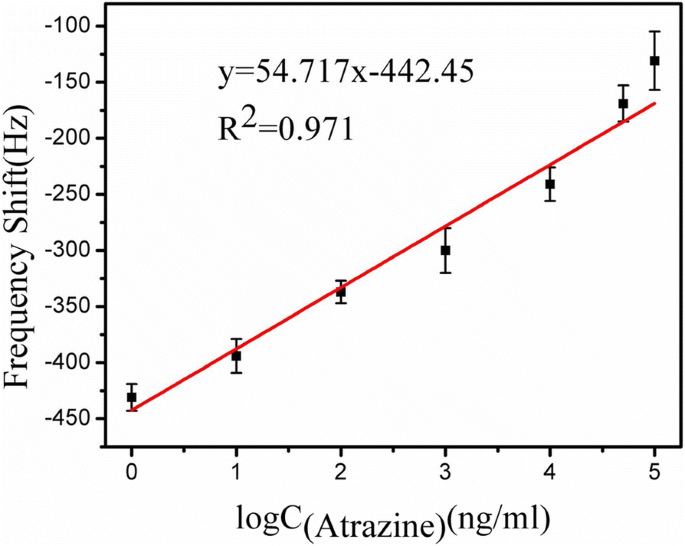
検量線:さまざまなアトラジン濃度の関数としての共鳴周波数の50分のシフト
アトラジンは小分子であるため、MEナノバイオセンサーの感度を向上させるために直接競合イムノアッセイアプローチが採用されました。直接競合イムノアッセイでは、抗体はセンサー表面で修飾され、シグナル応答はAtr–BSA分子の結合に起因します。逆に、間接競合イムノアッセイでは、Atr–BSAはセンサー表面に固定化され、応答は抗体分子の結合に起因します。文献研究[38]と私たちの結果によると、直接競合イムノアッセイは小分子モニタリングに適しています。間接競合イムノアッセイは、微量濃度の分析物サンプルに非常に敏感です[39]。間接競合イムノアッセイは感度が高い[40、41]が、操作が複雑で、信頼性の高い繰り返し使用のために実装するのが難しい場合があります[36]。ただし、直接競合イムノアッセイは非常に高速で、使用が簡単で、自己完結型であり、追加の試薬は必要ありません[36]。したがって、将来の開発のために、直接競合イムノアッセイが最も有望な方法である可能性があります。
MEナノバイオセンサーの特異性
図8に示すように、アトラジンに対するMEナノバイオセンサーの特異性は、プロメトリン、シマジン、DDTなどの他の農薬に対するナノバイオセンサーの応答を測定することによって調査されました。図8から、MEナノバイオセンサーはこれらに対してほとんど応答を示さなかったことが明らかです。非特異的吸収による干渉、およびプロメトリンとシマジンへの応答は、ブランク溶液と同様の応答レベルを持っていたDDTよりもわずかに大きかった。これは、プロメトリンとシマジンの両方が、トリアジン系農薬に属するアトラジンと同様の構造を持っているという事実が原因である可能性があります。ただし、DDTは一種の有機塩素系殺虫剤です。結果は、アトラジンが効果的に認識され、ナノバイオセンサー表面に固定化された抗体と特異的に組み合わされることを示した。したがって、MEナノバイオセンサーはアトラジン検出に対して強い特異性を示しました。
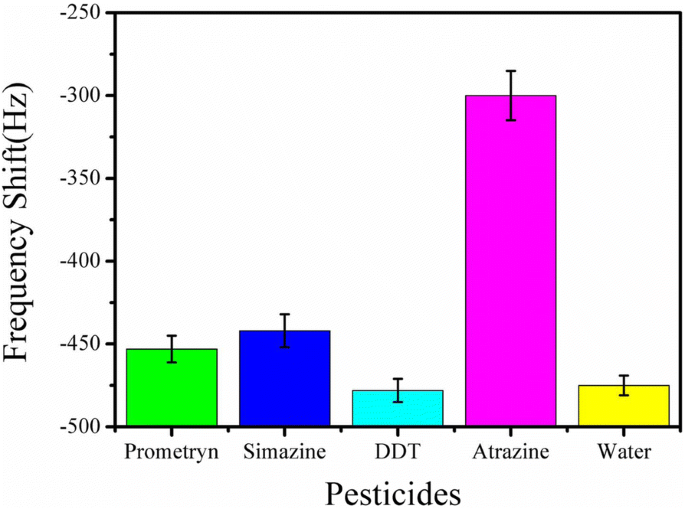
100μg/ mLの濃度の他の干渉物質に対するMEナノバイオセンサーの共振周波数応答
MEナノバイオセンサーの安定性
図9は、アトラジン検出に対するMEナノバイオセンサーの安定性を示しています。同じMEナノバイオセンサーを6つ準備し、4°Cで保存しました。すべてのセンサーを6日まで1日おきに10 ng / mLのアトラジンに対してテストしました。すべての単一の検出サイクルは、50分間だけ1つのナノバイオセンサーをテストしました。ナノバイオセンサーの共振周波数応答はほぼ一定のままであり、相対標準偏差(RSD)は1.8%と計算されていることは明らかです。この結果は、MEナノバイオセンサーがアトラジン検出に対して優れた安定性を示すことを示しています。
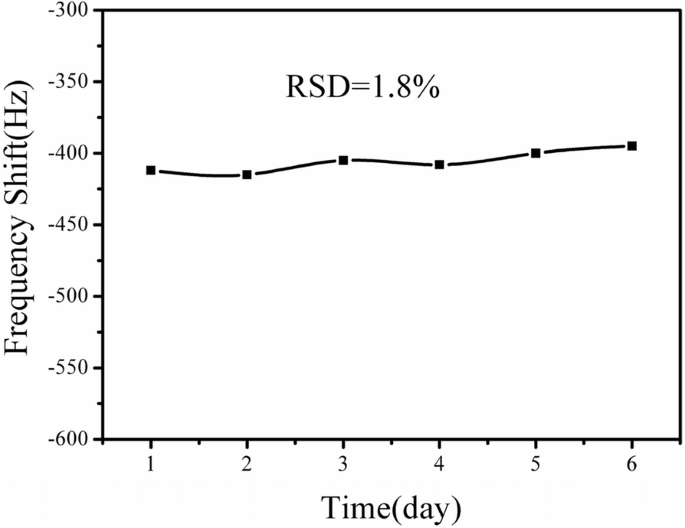
MEナノバイオセンサーでの10ng / mLアトラジンの安定性測定
結論
ME材料とAuNPに基づくワイヤレスMEナノバイオセンサーは、競合イムノアッセイを使用してアトラジンをリアルタイムで高感度に検出するための開発に成功しました。プロテインAを介したアトラジン抗体の配向固定化により、ナノバイオセンサーの性能が向上しました。高分子量のAtr–BSAと、ナノバイオセンサー表面でアトラジン抗体と競合的に結合したアトラジンが信号応答を増幅し、感度が向上しました。主に結合したAtr–BSAによって引き起こされる共鳴周波数シフトは、ターゲットのアトラジン濃度に反比例します。さらに、アトラジン抗体とAtr–BSAの使用濃度は、それぞれ50μg/ mLと40μg/ mLに最適化されました。最適な条件下で、MEナノバイオセンサーは1 ng / mLから100μg/ mLまでのアトラジンの幅広い線形測定範囲を示し、3.43Hz /μgmL -1 の十分な感度を示します。 検出限界は1ng / mLであり、これは立法要件には十分であり、他の報告されている方法よりも低くなっています。 AFM画像は、アトラジン抗体が配向した方法でナノバイオセンサー表面にうまく固定化されたことを確認しました。実験結果は、MEナノバイオセンサーがアトラジンに対して高い特異性と安定性を持っていることを示しています。この研究は、検出限界、シンプルさ、使い捨て特性、ワイヤレスの性質への影響を利用して、アトラジンを高感度で検出するための新しい方法を提案しただけでなく、他の環境汚染物質の検出や水質モニタリングの潜在的な実用性も示しました。
>略語
- AFM:
-
原子間力顕微鏡
- Atr–BSA:
-
アトラジン-アルブミンコンジュゲート抗原
- AuNPs:
-
金ナノ粒子
- BSA:
-
ウシ血清アルブミン
- DDT:
-
ジクロロジフェニルトリクロロエタン
- EDC:
-
1-エチル-3-(3-ジメチルアミノプロピル)カルボジイミド塩酸塩
- ME:
-
磁気弾性
- NHS:
-
N -ヒドロキシスルホスクシンイミド
- PBS:
-
リン酸緩衝生理食塩水
- SAM:
-
自己組織化単分子膜
- SEM:
-
走査型電子顕微鏡
- US EPA:
-
米国の環境保護庁
ナノマテリアル
- 卵巣癌細胞の高感度かつ迅速な検出のための柔軟なグラフェンベースのバイオセンサーのデモンストレーション
- フルアングルマイクロLED用の高反射薄膜最適化
- 過酸化水素の選択的検出のためのデュアルモードナノセンサーとしてのカーボンナノドット
- アロワナの魚の性別を測定するためのアクリルゴールドナノコンポジットからの高感度電気化学DNAバイオセンサー
- 中空多孔質NiOに基づく高感度の非酵素的電気化学的グルコース検出
- 修正されたゾルゲル法によって調製された新しいAgドープメソポーラスα–Fe2O3に基づく高感度エタノール化学センサー
- 癌胎児性抗原を超高感度で検出するための新しい磁気弾性免疫センサー
- CdSe量子ドットとg-C3N4ナノシート間のフェルスター共鳴エネルギー移動に基づくHg2 +の高選択的かつ高感度な検出
- 赤外線ステルス用途向けの伸縮性の高いマイクロ/ナノリンクル構造
- トランジスタの欠陥を検出するための高感度な方法
- 宇宙用の高感度光受信機



