多孔質および中空構造のLiNb3O8アノード材料に向けた熱水支援焼結戦略
要約
多孔質および中空構造のLiNb 3 O 8 アノード材料は、初めて熱水支援焼結戦略によって調製されました。相進化を研究し、多孔質および中空構造の形成メカニズムを提案した。独特の構造の形成は、Li元素の揮発による液相の局所的な存在に起因する可能性があります。アノード材料として、初期放電容量は285.1 mAhg -1 です。 0.1 Cで、LiNb 3 についてこれまでに報告された最大の放電容量 O 8 。 50サイクル後でも、可逆容量は77.6 mAhg -1 を維持できます。 0.1℃で、LiNb 3 の約2.5倍 O 8 従来の固体法で調製されたサンプル。 Liの貯蔵容量の大幅な改善は、Li + の高速インターカレーションのための高密度の活性部位と短い平行チャネルを提供する、特殊な多孔質で中空の構造に起因する可能性があります。 表面を通るイオン。
背景
近年、触媒作用、エネルギー、環境工学、薬物送達、およびセンサーシステムでの広範な用途のために、中空および多孔質構造に多くの注目が集まっています[1,2,3,4]。リチウムイオン電池(LIB)は、他の新エネルギー電池と比較して、携帯用電子機器の主要な電源として商業的に成功を収めており、エネルギー密度が高く、寿命が長く、環境に優しいため、大規模なアプリケーションで大きな可能性を示しています[5 ]。高い電気化学的性能を得るために、LIBの電極は常に開いた構造を持っています。これにより、高密度の活性部位と並列チャネルを提供して、Li + のインターカレーションを高速化できます。 表面を通るイオン[6]。ただし、多孔質および中空の構造を含む開放構造のナノ材料を合成することは困難です。
LIBの性能を向上させるために、人々はアノードおよびカソード材料を含む高性能電極材料を求めてきました。 LiFePO 4 [7]、LiCoO 2 [8]、LiMn 2 O 4 [9]、LiVPO 4 F [10]、およびさまざまなハイブリッド材料[11、12]は、カソード材料の候補として真剣に検討されてきました。アノード材料については、遷移金属酸化物(TMO)[13]、二硫化モリブデン(MoS 2 )など、グラファイトベースのアノード材料の代替として多くの異なる材料が研究されてきました。 )、およびグラフェンベースのハイブリッド[14]。最近の文献では、ニオブは優れた電気化学的性能を持っていることが示されています[15]。 Nb元素をドープしたいくつかの従来の化合物と新しいNbベースの化合物は十分に開発されています[16、17、18、19]。 Nbベースの酸化物は、安全性が向上したLIBの有望なアノード材料と見なされてきました。 Li 4 との比較 Ti 5 O 12 (理論容量は175 mAhg -1 )、Nbベースの酸化物の理論容量は389 mAhg -1 と比較的高くなっています。 。また、2つのNbレドックスカップルNb 5+ が注目に値します。 / Nb 4+ およびNb 4+ / Nb 3+ 、サイクリング中の固体電解質界面(SEI)膜の形成を抑制することができます[19]。 LiNb 3 O 8 、よく知られている材料である、は常にLiNbO 3 の準備プロセスに現れます Liの揮発による不純物相として[20]。 Jian etal。最初に導入されたLiNb 3 O 8 LIBのアノードとして固相反応によって調製された材料。調製されたままのLiNb 3 O 8 アセチレンブラック(LiNb 3 )でボールミル粉砕されたサンプル O 8 -BM)は、初期放電/充電容量を大幅に改善しました(351および212 mAhg -1 )準備されたままのLiNb 3 のものより O 8 サンプル(250および170 mAhg -1 )0.05℃で; 50サイクル後、容量は150 mAhg -1 に達しました。 LiNb 3 の場合 O 8 -BM、0.1 C、わずか30 mAhg -1 LiNb 3 の場合 O 8 サンプル[18]。多孔質LiNb 3 O 8 ナノファイバーは、表面積が大きく、ナノ結晶が小さく、初期放電容量が241.1 mAhg -1 の多孔質構造であるため、容量とサイクル性能の向上も示しました。 0.1℃で[19]。純粋な相を得るのが難しいため、理論容量の高い新しいアノード材料として、LiNb 3 O 8 研究されることはめったにありません。
この論文では、多孔質および中空構造のLiNb 3 O 8 アノード材料は、熱水支援焼結プロセスによって首尾よく調製された。相進化を研究し、多孔質および中空構造の形成メカニズムを提案した。 LiNb 3 の形態学的および電気化学的特性 O 8 アノード材料も詳細に研究されたので。
メソッド
サンプルの準備
LiNb 3 O 8 粉末は、熱水支援焼結プロセスによって調製された。水酸化リチウム一水和物(LiOH・H 2 O、アラジン、ACS、≥98.0%)および五酸化ニオブ(Nb 2 O 5 、アラジン、AR、99.9%)をさらに精製することなく原材料として購入した。まず、3.5ミリモルのNb 2 O 5 35 mlのLiOH・H 2 に分散させました O透明な水溶液(Li:Nbのモル比=8:1)を1時間マグネチックスターラーで攪拌します。次に、懸濁液を50mlのテフロンで裏打ちされた水熱合成オートクレーブ反応器に入れた。その後、反応器を密閉し、260°Cで24時間維持した後、自然に室温まで冷却しました。最後に、調製したままの生成物を遠心分離し、脱イオン水およびエタノールですすいだ。 60°Cのオーブンで12時間乾燥した後、白いLi-Nb-O粉末を収集し、500〜800°Cのさまざまな温度で2時間、5°C /分のランプ速度で焼成しました。
特性評価
Li-Nb-O粉末の熱分解特性は、熱重量分析および示差走査熱量計(TG / DSC、Netzsch STA 409 PC / PG)によって、室温から1200°Cまで、10°C /分のランプ速度で研究されました。 N 2 雰囲気。か焼された粉末の結晶構造は、Cu Kαを用いたX線粉末回折(XRD; Bruker D8 Discover)を使用して分析されました。 放射線。煆焼粉末の形態は、走査型電子顕微鏡(SEM; JSM-6700F)によって特徴づけられました。 X線光電子分光法(XPS)分析は、Thermo-Fisher Escalab250Xi機器で実行されました。
電気化学的測定
LiNb 3 O 8 電極は、LiNb 3 のスラリーを広げることによって準備されました O 8 アルミホイルに8:1:1の重量比の粉末、カーボンブラック、およびポリフッ化ビニリデン(PVDF)。その後、電極を真空オーブン内で120°Cで一晩乾燥させました。アノードは、直径16mmのディスクに打ち抜かれました。電気化学的測定では、CR2025コイン型セルを、対極としてリチウム箔を使用し、セパレータとしてポリプロピレン微孔性膜(Celgard 2320)を使用して、アルゴンを充填したグローブボックス内で組み立て、2つの電極を分離し、次に1.0-M LiPF 6 電解質をエチレンカーボネートとジメチルカーボネートの混合物(体積で1:1)に溶解した。セルの定電流充放電テストは、0〜3 V(vs。Li / Li + )のLand電気テストシステム(Wuhan Land Electronics Co.、Ltd。、中国)を使用して実行されました。 )0.1〜1 Cのさまざまな電流密度(1 C =389 mAhg -1 )。サイクリックボルタンメトリー(CV)曲線は、電気化学ワークステーション(CHI604E、Shanghai Chenhua Instruments Co.、Ltd。、中国)で、1〜3Vの電圧範囲で記録されました。
結果と考察
図1は、さらに煆焼せずに水熱反応後に得られた粉末のTG / DSC曲線をプロットしたものです。温度が1100°Cに達しても、粉末の重量損失は非常に小さく、約5%ですが、この損失は、煆焼プロセス全体を通じて発生しています。これは、溶融温度が低いためにLi元素が蒸発したためと考えられます。これは、焼成プロセス全体にわたる吸熱反応プロセスでのDSCの結果によって確認されています。 330°Cで吸熱ピークが発生します。これは、LiNbO 3 の形成に起因する可能性があります。 。 LiNbO 3 間の反応により、580°Cで発熱反応が発生します。 およびNb 2 O 5 LiNb 3 を形成する O 8 。 DSC曲線に見られるように、1100°Cを超えると、LiNb 3 の分解により発熱反応が強くなります。 O 8 。
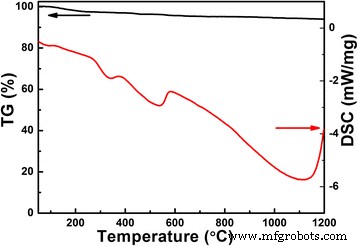
N 2 での10°C /分の加熱速度での室温から1200°CまでのLi-Nb-O粉末のTG / DSC曲線
異なる温度で煆焼されたLi-Nb-O粉末のXRDパターンを図2に示します。主な相はLiNbO 3 であることがわかります。 およびNb 2 O 5 500°Cで。煆焼温度の上昇に伴い、30.26°の回折ピークが現れます。これは、単斜晶系LiNb 3 の(410)面としてインデックスを付けることができます。 O 8 。反応は式(1)で表すことができます。 (1)式ではありません。 (2)[21]:
$$ {\ mathrm {LiNb} \ mathrm {O}} _3 + {Nb} _2 {\ mathrm {O}} _ 5 \ to {\ mathrm {LiNb}} _3 {\ mathrm {O}} _ 8 $$(1) $$ {\ mathrm {LiNb} \ mathrm {O}} _3 \ to {\ mathrm {LiNb}} _ 3 {\ mathrm {O}} _ 8 + {Li} _2 \ mathrm {O} \ uparrow $$(2)<図> <画像>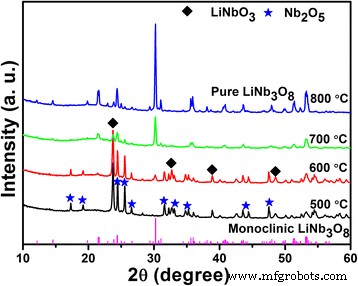
さまざまな温度で2時間焼成したLi-Nb-O粉末のXRDパターン
700°Cでは、単斜晶系LiNb 3 O 8 不純物がほとんどない主な相です。 LiNb 3 の純粋な相 O 8 は800°Cで得られ、すべての回折ピークはP21 / aの空間群である単斜晶相(JCPDSカード番号36–0307)にインデックス付けされています。従来の固体法と比較して、LiNb 3 の純粋な相 O 8 熱水支援焼結プロセスを使用すると、より簡単に得られます。
LiNb 3 のSEM画像 O 8 さまざまな倍率で800°Cで焼成された粉末を図3に示します。ハニカムに似た多孔質で中空の構造は、LiNb 3 によって形成されます。 O 8 数マイクロメートルの長さのナノ粒子。構造は平らではなく、明らかな反りがあり、閉じたタビーのような構造を形成しています。これは、従来の固相反応から生じる粒子の凝集とはまったく異なります。 LiNb 3 のサイズ O 8 図3cに示すように、粒子は約200nmです。小さな粒子サイズと独自の構造は、イオンインターカレーションに有益です[6]。 TG-DSCの結果から明らかなように、独特の構造の形成は、煆焼プロセス中のリチウムの揮発に起因する可能性があります。 Li元素は容易に揮発するため、粉末中に存在する過剰なLi元素は粒子の表面に移動しやすく、液相になります。液相の局所的な存在は、新しいLiNb 3 の形成を助長します。 O 8 サイトに粒子があり、粒子間のネットワークの形成も促進します。

a – c LiNb 3 のSEM画像 O 8 倍率の異なる粉末
元素組成と電子状態をさらに確認するために、多孔質および中空構造のLiNb 3 O 8 図4に示すように、粉末はXPSによって分析されます。XPSデータは、結合エネルギーが284.6eVのC1を参照として使用して較正されました。図4aでは、207.1および209.8eVの2つのピークがNb3d 5/2 に対応しています。 および3d 3/2 、それぞれ、Nb 5+ を示します LiNb 3 の状態 O 8 [22]。図4bのO1のXPSスペクトルは、530.3と532eVの2つのピークにデコンボリューションできます。前者はNb-O結合に割り当てられ、後者は非格子酸素に関連しています[22、23]。
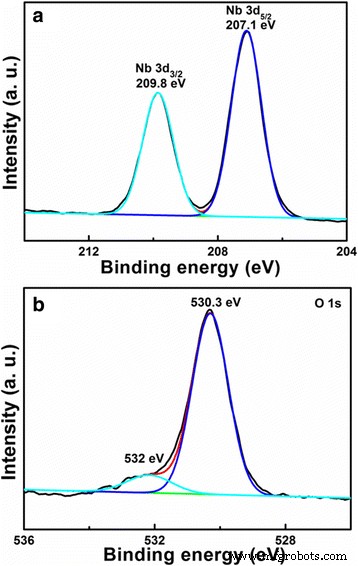
( a のXPSスペクトル )Nb 3dおよび( b )多孔質および中空構造のLiNb3O8のO 1
調製したままのLiNb 3 の電気化学的性能を調査するには O 8 サンプルでは、CVおよび定電流放電-充電サイクルのテストが実行されました。 LiNb 3 の最初の3つのCV曲線 O 8 3〜1Vの範囲で0.1mV / sのスキャン速度の粉末を図5に示します。最初のサイクルでは、1.13Vと1.30Vに2つの顕著なピーク(Li挿入)が観察されます。前者は、Nb 4+ の部分的な還元に起因する可能性があります。 Nb 3+ へ 、後者はNb 5+ の完全な原子価変動に関連している可能性があります Nb 4+ へ [18、19]。図5に示すように、後続のサイクルは最初のサイクルとはかなり異なります。 1.13および1.30Vでのピークの消失は、最初のサイクルでの相転移が不可逆的であることを意味します。 1.71および1.96Vの酸化(Li抽出)ピークのみがサイクリング時に安定したままであり、LiNb 3 の構造変化を意味します。 O 8 後続のサイクルのサンプルは可逆的です。
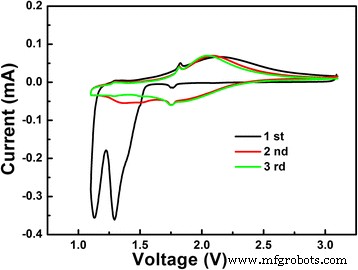
LiNb 3 の最初の3つのCV曲線 O 8 3〜1Vの電圧範囲間で0.05mV / sのスキャン速度で粉末
図6に、LiNb 3 の放電-充電曲線を示します。 O 8 0.1 Cの粉末(ここでは、1 C =389 mAhg -1 )第1、第2、第10、第30、および第50サイクルで3〜1V。最初の放電曲線では、約1.13Vと1.30Vで2つの明らかな潜在的なプラトーが観察されます。これは、2相反応Nb 4+ というCVの結果とよく一致しています。 →nb 3+ およびNb 5+ →nb 4+ 、 行われる。ただし、後続のサイクルでは、最初のサイクルに存在するプラトーが傾斜した曲線に置き換えられ、最初のサイクルと後続のサイクルの間で異なる反応が発生することを意味します。同時に、LiNb 3 の初期放電容量 O 8 サンプルは285.1mAhg -1 0.1 Cで、LiNb 3 についてこれまでに報告された最大の放電容量 O 8 アノード材料[18、19]。 4.4単位式あたりのLiをLiNb 3 に挿入できます O 8 Li 5.4 の組成に対応する材料 Nb 3 O 8 。ただし、最初のサイクルの充電容量は106.4 mAhg -1 、1.6Liのみが可逆的に抽出できることを示します。現在、2.8Liの大きな損失はあいまいです。
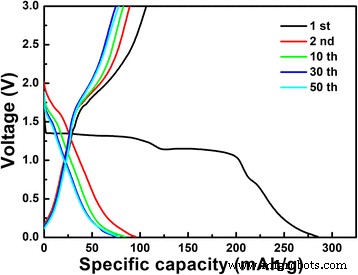
LiNb 3 の定電流充放電プロファイル O 8 0.1 C、3〜1 V
の粉末図7は、LiNb 3 のサイクリングパフォーマンスを示しています。 O 8 最大50サイクルのさまざまな現在のレートでサンプリングします。 LiNb 3 の初期放電容量 O 8 0.1、0.5、および1 Cの割合の粉末は、285.1、250、および228 mAhg -1 、 それぞれ。 0.1 Cの電流レートでも、可逆容量は77.6 mAhg -1 を維持できます。 、LiNb 3 の約2.5倍 O 8 従来の固体法で調製されたサンプル(約30 mAhg -1 0.1℃で、Ref。 [18])。 Li貯蔵容量の大幅な改善は、LiNb 3 の特殊な多孔質および中空構造に起因する可能性があります。 O 8 サンプル。Li + のインターカレーションを高速化するために、高密度の活性部位と短い並列チャネルを提供します。 表面を通るイオン[6]。レートが0.5および1Cに増加すると、50サイクル後の放電容量は39.7および29.4 mAhg -1 のままになります。 、 それぞれ。 LiNb 3 の適切な表面改質により、容量の安定性が向上することが期待されます。 O 8 材料。
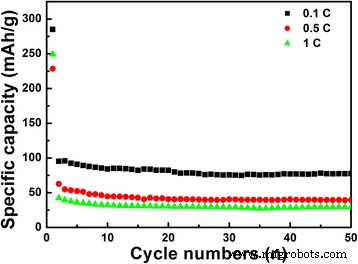
LiNb 3 のサイクリングパフォーマンス O 8 0.1 C、0.5 C、1Cの異なる電流速度での粉末
結論
要約すると、多孔質および中空構造のLiNb 3 O 8 アノード材料は、熱水支援焼結戦略によって首尾よく調製された。相進化を研究し、多孔質および中空構造の形成メカニズムを提案した。独特の構造の形成は、Liの揮発による液相の局所的な存在に起因する可能性があります。アノード材料として、初期放電容量は285.1 mAhg -1 です。 0.1 Cで、LiNb 3 についてこれまでに報告された最大の放電容量 O 8 。 50サイクル後も、可逆容量は77.6 mAhg -1 を維持できます。 、LiNb 3 の約2.5倍 O 8 従来の固体法で調製されたサンプル。 Li貯蔵容量の大幅な改善は、LiNb 3 の特殊な多孔質および中空構造に起因する可能性があります。 O 8 Li + の高速インターカレーションのための高密度の活性部位と短い平行チャネルを提供する粉末 表面を通るイオン。
ナノマテリアル
- 高融点金属粉末とその焼結プロセス
- 無駄のないメンテナンス戦略を構築および測定するためのガイド
- 壊れたメンテナンス戦略の修正:PM最適化とFMEA
- TOTALは保守および検査戦略を開発します
- 7nm以降の材料革新の鍵
- 石油とガスにおけるデジタルトランスフォーメーション戦略の進歩
- Nano and Battery Anode:A Review
- Li-Nb-O化合物の調製と光触媒性能に及ぼすLi / Nb比の影響
- リチウムイオン電池用の効率的なアノード材料としての数層のMoS2 /アセチレンブラック複合材料
- 中空構造LiNb3O8光触媒の調製と光触媒性能
- ゾルゲル法による水熱法による球状銀被覆Li4Ti5O12アノード材料の合成



