堆肥条件下での官能化チタニアナノ粒子(PLA / TiO2)で満たされたポリ(乳酸)の生分解評価
要約
この論文は、官能化アナターゼ-チタニアナノフィラー(PLA / TiO 2 )で満たされたポリ(乳酸)(PLA)の標準化された制御された堆肥化条件下で90日間行われた生分解研究を提示します。 ナノコンポジット)。表面形態、熱特性、生分解の割合、およびさまざまなインキュベーション時間での分子量の変化を、目視検査、走査型電子顕微鏡(SEM)、X線回折(XRD)、示差走査熱量測定(DSC)、およびゲル浸透によって評価しました。標的生分解時間間隔の終わりにコンポストから分解サンプルを採取することによるクロマトグラフィー(GPC)。結晶化度の急激な増加は、PLAおよびPLA / TiO 2 ナノコンポジットは、制御された堆肥化条件下で不均一な分解メカニズムを持っていました。 PLA / TiO 2 の生分解速度 水分子がナノコンポジットに容易に浸透するため、ナノコンポジットは純粋なPLAよりも高かった。 PLA / TiO 2 におけるナノ粒子の分散 ナノコンポジットはPLAの生分解速度に影響を及ぼしました。さらに、PLAの生分解は、分散したTiO 2 の量を追加することによって制御できます。 制御された堆肥化条件下でのナノフィラー。
はじめに
合成生分解性ポリマーであるポリ(乳酸)(PLA)は、石油化学製品からの持続可能な代替品である再生可能材料の必要性が高まっているため、生物医学および消費者向けの用途で世界中で調査されています[1,2,3,4]。 PLAは、炭水化物の微生物発酵によって自然界で最も広く生産されているカルボン酸であるラクチドまたは乳酸の重合から生じる生成物です[5]。しかし、荷重たわみ温度、靭性、劣化速度が不十分なため、PLAの適用範囲は比較的限られています[6、7]。これらの欠点を解決する方法の1つは、典型的なナノクレイ、カーボンナノチューブ、酸化亜鉛、アナターゼ(A-TiO 2 )などの無機ナノ粒子を追加してPLAを修飾することです。 )[8,9,10,11,12,13,14,15]。最近、PLA / TiO 2 ナノコンポジットは、PLAと化学修飾されたTiO 2 を溶融ブレンドすることによって調製されました。 (溶液乳酸グラフト化TiO 2 、以下、g-TiO 2 と呼びます。 )[16]。結果は、TiO 2 ナノ粒子は、PLA / TiO 2 の機械的特性の改善に大きな影響を及ぼしました。 純粋なPLAと比較した、破断時のひずみや弾性などのブレンド。同時に、g-TiO 2 ナノ粒子は、PLAの加水分解と光分解に強い影響を及ぼしました[17、18]。
実験室規模の試験を用いた生分解性材料の生分解性と生分解メカニズムの研究は、これらの材料の耐用年数の理解を提供する産業的および科学的観点から非常に重要な方法です[15]。生分解性材料の生分解性を評価するために現在利用可能ないくつかの方法があり、それらは一般に二酸化炭素生成、バイオガス生成、または酸素消費などの間接測定に基づいています[19、20]。
堆肥中のPLAの生分解特性が研究され、報告されています[21、22、23]。堆肥化は、微生物集団と制御された堆肥化条件の組み合わせの下で、暖かく湿った好気性の環境で有機物の生分解が加速されることです[24、25]。さらに、堆肥化条件でのPLAの生分解、温度および湿度に依存するプロセスには、いくつかのプロセス、すなわち、水分の取り込み、エステルの切断、およびオリゴマーフラグメントの形成と溶解が含まれます[26]。 PLA生分解の最も受け入れられているメカニズムには、2段階の分解プロセスが含まれます。最初に、堆肥の熱と湿気がPLA鎖を攻撃し、それらを分割して、小さなMwポリマーを生成し、最終的には乳酸を生成します。その後、堆肥と土壌中の微生物がオリゴマーの断片と乳酸を無機化して、メタンと二酸化炭素を生成します(CO 2 )それぞれ嫌気性および好気性条件下で[27,28,29]。
最近、PLAの生分解に対するフィラーの影響が大きな注目を集めており、特にナノクレイ、カーボンナノチューブ、ヒドロキシアパタイトなどのナノフィラーに注目が集まっています[23、30、31、32、33、34、35、36、 37,38]。一部の著者[32,33,34]は、ナノ粒子を追加するとPLAの生分解が促進されることを発見しました。これは、ナノ粒子の相対的な親水性が高いため、ポリマーマトリックスへの水の透過が容易になり、加水分解が引き起こされるためです。ただし、他の研究[35,36,37,38]は、ナノコンポジットのバリア特性が強化されているため、生分解が遅延していることを報告しています。
PLA材料の生分解に焦点を当てた文献がいくつかありますが、TiO 2 の役割 PLAの劣化における演劇は物議を醸すままです。 TiO 2 はどうでしたか ナノ粒子がPLAの生分解に影響を与えることは明らかではありませんでした。そこで、TiO 2 によって修飾されたPLAの生分解の研究 堆肥条件下のナノフィラーはまだ必要です。進化するCO 2 の推定に基づく現在の研究 、PLA / TiO 2 の生分解を評価しました 制御された実験室堆肥条件下で広範囲にナノコンポジット、PLA / TiO 2 の分解性を補完する さまざまな劣化条件下でのナノコンポジットは、将来、さまざまな最終用途でのPLAの使用を拡大する可能性があります。
メソッド
資料
PLA(Natureworks @ 製 (4032D))は、19,600 kDaの重量平均分子量(Mw)と、ゲル浸透クロマトグラフィー(GPC)で測定した1.89の多分散度を示しました。 PLAは65°Cで24時間減圧下で乾燥し、使用前に吸湿剤を使用して真空保存しました。乳酸(88%、広水国立化学株式会社)を80℃で蒸留し、使用前に水分を除去しました。アナターゼチタニアナノ粒子、平均一次粒子サイズは約。 20 nmは、Pangang Co.、Ltdから供給されました。トルエンとクロロホルムは、受け取ったままの状態で使用しました。クロマトグラフィーグレードの微結晶性セルロースは、Shanghai Chemical Reagent Co.、Ltdから供給されました。都市固形廃棄物(MSW)の有機画分から得られた堆肥化接種材料は、中国プラスチック加工産業協会( CPPIA)。
サンプル準備
TiO 2 の機能化に関する詳細情報 ナノ粒子とPLA / TiO 2 の準備 ナノコンポジットが報告されています[16]。 G-TiO 2 ナノフィラーは、乳酸オリゴマーをアナターゼ表面にグラフトすることによって調製されました。 PLA / TiO 2 ナノコンポジットは、共回転二軸スクリュー押出機を介した溶融ブレンドによって調製されました。純粋なPLAは、ナノコンポジットと同じ熱履歴を持つように同じ混合処理を受けました。 0、0.5、1.0、2.0、5.0、8.0、および15.0 wt%g-TiO 2 のサンプル PLA、PLA / TiO 2 として準備され、ラベルが付けられました –0.5、PLA / TiO 2 –1、PLA / TiO 2 –2、PLA / TiO 2 –5、PLA / TiO 2 –8、およびPLA / TiO 2 –15ナノコンポジット。
PLAおよびg-TiO 2 の小さなチップ試験片 さまざまな比率で、190°Cで4分間10 MPaでプレスし、続いて室温で5分間5 MPaで冷却することにより、厚さ約0.5mmのシートに変換しました。その後、圧縮成形されたサンプルを5mm×5mmのサイズにカットし、計量しました。
劣化テスト
生分解性試験は、生分解性プラスチック用に設計された標準試験方法(GB / T19277–2003 / ISO 14855-1:2005)に基づく実験室規模の設置で実施されました(制御された堆肥化条件下でのプラスチック材料の最終的な好気性生分解性の決定-方法進化したCO 2 の分析による )。代謝された基質中の炭素のほとんどは、CO 2 への化学変換によってエネルギーを生成します 好気性環境で[39]。したがって、CO 2 の生成の測定 ほとんどの状況で生分解の最も適切な尺度と考えられています。この規格は、発生したCO 2 の量を測定することにより、最終的な好気性生分解性を決定する手順を指定しています。 制御された堆肥化条件下での試験材料の生分解度のパーセンテージ。堆肥化接種材料は、5mm未満のサイズにふるいにかけられたMSWの有機画分から得られました。その後、微細画分を接種材料として使用した。表1は、堆肥化接種物の決定された物理化学的特性を示しています。各テストでは、一連のコンポストリアクター(各サンプルを3回ずつ)に、15 gの参照物質(つまり、標準で提案されている微結晶性セルロース(MCE))またはテスト材料(各フィルムの重量とラベルを前に付けたもの)をロードしました。分解)、85 gの接種材料、および320 gの乾燥海砂(接種材料内の良好な均質条件と改善された好気性環境を提供します)。その後、反応器を光のないインキュベーターに58±2℃で90日間の実験時間かけて置いた。曝気は、水で飽和したCO 2 を使用して開始されました。 -自由空気;各反応器を通る流量は25mL・min -1 に設定されました。 。すべての反応器の湿度、混合、および曝気は、GB / T19277–2003 / ISO14855-12,005要件によって確立されたように制御されました。選択した時間に、各サンプルの3〜4個の標本を選択し、蒸留水で洗浄し、室温で少なくとも24時間乾燥させて恒量にしました。
<図>CO 2 生分解プロセス中に発生したものは、NaOH溶液にトラップされ、滴定法を使用して定期的に測定されました。フェノールフタレインの終点まで、NaOHを標準HCl溶液で滴定しました。合計CO 2 生分解中に発生したものは、対照フラスコを参照して計算された。各サンプルについて報告されたデータは、3つのサンプルから得られた平均値でした。
特性評価
顕微鏡検査
走査型電子顕微鏡(SEM)画像は、5kVで動作するPhilipsFEI INSPECTF装置を使用して取得しました。すべての試験片は、分析前に金でスパッタコーティングされました。
熱分析
サンプルの熱特性は、示差走査熱量測定(DSC)(TA Q20、TA Instruments)によって研究されました。サーモグラムは、窒素フロー(50 mL / min)下で、室温から200°Cおよび200から-50°Cの温度範囲で、それぞれ10°C /分の加熱および冷却速度で取得されました。
XRD研究
X線回折(XRD)分析は、Cu K αを備えたDX-1000X線回折計(Dandong Fanyuan Instrument Co.LTD。China)を使用して実行されました。 (λ =0.154 nm)ソース。発電機は25mAおよび40kVで運転されました。サンプルは、6°/分のスキャン速度でさまざまな角度(つまり、2〜70°)でスキャンされました。
生分解率の決定( D t 、%)
生分解の割合( D t 、%)は、式(1)を使用して計算できます。 1は、式(1)として採用されました。 2 [1、40]。
$$ {D} _t \ left(\%\ right)=\ frac {{\ left({\ mathrm {CO}} _ 2 \ right)} _ T-{\ left({\ mathrm {CO}} _ 2 \ right )} _ B} {{\ mathrm {Th}} _ {\ mathrm {CO} 2}} \ times 100 $$(1)ここで(CO 2 ) T CO 2 の量です (g /フラスコ単位)試験材料から進化した(CO 2 ) B CO 2 の量です (g /フラスコ単位)コントロールフラスコで発生し、Th CO2 は理論上のCO 2 高分子材料によって生成される量。
理論上のCO 2 各フラスコで生成できる量(Th CO2 、g 2 / gサンプル)は、次の式を使用して計算されました。
$$ {\ mathrm {Th}} _ {\ mathrm {CO} 2} ={M} _ {\ mathrm {TOT}} \ times {C} _ {\ mathrm {TOT}} \ times \ frac {44} {12} $$(2)ここで M TOT は、実験の開始時に堆肥化フラスコに追加された乾燥高分子固体材料の総重量(g)、 C TOT はサンプル中の全乾燥高分子固体中の全有機炭素の重量(g)であり、44と12はCO 2 の分子量です。 および C の原子量 それぞれ。
分子量測定
堆肥化前後のPLAナノコンポジットの分子量はGPCによって決定されました。 GPCシステムには、Waters 1515 Isocratic HPLCポンプ、Waters 2414屈折率検出器、およびWaters 717plusオートサンプラーが装備されていました。クロロホルムは、30°Cで0.8 mL / minの流速で溶離液として使用されました。キャリブレーションはポリスチレン標準で行われました。
結果と考察
ポリマーの劣化は、色、表面形態、機械的特性などの特性の変化に関連しています。純粋なPLAおよびPLA / TiO 2 の外観の時間的変化 ナノコンポジットは、実験室の条件下では異なっていました。アモルファス構造と一致して最初は透明であった純粋なPLAマトリックス表面は、2日間の生分解後に比較的白っぽくなりました[41]。この機能は、10日後に完全に不透明になるまで、インキュベーション時間とともに増加しました。水透過と微生物のインキュベーションによって引き起こされる黄褐色から暗褐色のプラークが、30日後にきれいなPLAフィルム表面に観察され始めました。ただし、6日後にPLAナノコンポジットの表面に、大きな領域の暗褐色のプラークが現れました(図は示されていません)。茶色の斑点は微生物のコロニーを意味し、亀裂は生分解効果を表しています。図1は、PLAとそのTiO 2 の表面形態を示しています。 SEM観察下のナノコンポジット。劣化する前に、ニートでPLA / TiO 2 の表面 ナノコンポジットは滑らかでした。ニートPLAは、堆肥条件で5日間の生分解後、表面に有意な変化を示しませんでした。 20日後、ニートPLAの表面粗さが増加しました(図1a、a ')。ただし、PLA / TiO 2 ナノコンポジットは進行性の変化を示し、PLA / TiO 2 のかなりの劣化を明確に示しています。 コンポジットが発生しました。ナノコンポジットの表面に明らかな亀裂とボイド(それぞれ図1b、b '; c、c';およびd、d ';)が観察されました。これは、PLAの加水分解と微生物の活動に起因する可能性があります。インキュベーション時間が長くなると、亀裂とボイドはかなり深く大きくなり(それぞれ図1b '、c'、d ')、時間の経過とともにチェーンの損失と表面の侵食が示唆されます。すべての試験材料のバルク侵食現象は、PLAおよびPLA / TiO 2 の加水分解プロセスと同様でした。 ナノコンポジット[17]。

純粋なPLAの表面のSEM写真( a 0 、 a 、 a ’ )、PLA / TiO 2 –2( b 0 、 b 、 b ’ )、PLA / TiO 2 –5( c 0 、 c 、 c ’ )およびPLA / TiO 2 –8( d 0 、 d 、 d ’ )インキュベーション時間の関数としてのナノコンポジット。 a 0 、 b 0 、 c 0 、 d 0 :0日; a 、 b 、 c 、 d : 5日間; a ’ 、 b ’ 、 c ’ 、 d ’ :20日
PLAおよびPLA / TiO 2 の結晶化度を評価するには 生分解中のナノコンポジット、さまざまなインキュベーション時間で選択されたサンプルの熱特性を分析しました(図2および3)。図2は、ガラス転移温度( T g )分解時間のあるすべてのサンプルでわずかに減少しました。 T の減少 g 明らかに、生分解中のオリゴマーフラグメントと水の加水分解プロセスと可塑化効果の結果として、分子の移動度が向上したためです[33、42]。低温結晶化ピークの消失( T cc )すべてのサンプルについて、2日後にのみ、PLAの加水分解とポリマーマトリックスの結晶化度の急速な増加が原因である可能性があります[43]。 T の減少 m 急速な分子量の減少に起因していました[44、45]。二峰性の融解ピークは徐々に単峰性のピークに変化し、それにより、小さく不完全な結晶が分解時間とともに消失したことを意味します。この結果は、制御された堆肥化条件下での分解の初期段階で、アモルファス領域でPLAの分解が急速に進行することを証明しました。冷却スキャン(図3を参照)は、ニートPLAの結晶化ピークが徐々に増加したことを示しています。ただし、PLA / TiO 2 の結晶化ピーク ナノコンポジットは、最初は大幅に増加し、その後、インキュベーション時間の増加とともにわずかに減少しました。さらに、ナノフィラーの含有量が多いほど、結晶化のピークが早くそのピークに到達しました。結晶化ピークの減少は、アモルファス領域の分解後に結晶領域が分解し始めたことをさらに確認した。 GiulianaとRoberto [42]は、PLAサンプルの場合、短時間で一部のアモルファス領域が結晶に変化し、その後、アモルファス部分の侵食の影響により結晶化度が増加することを報告しました。さらに、結晶領域は長時間加水分解されます。
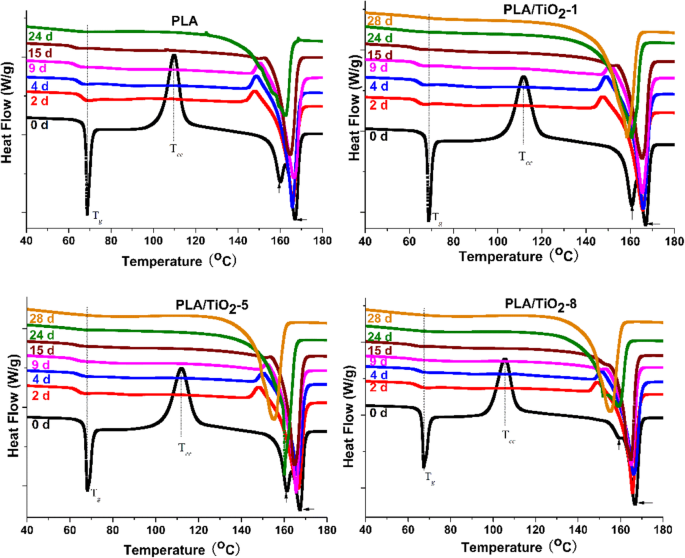
純粋なPLAおよびPLA / TiO 2 の生分解生成物のDSCサーモグラム 異なるインキュベーション時間でのナノコンポジット、最初の加熱スキャン
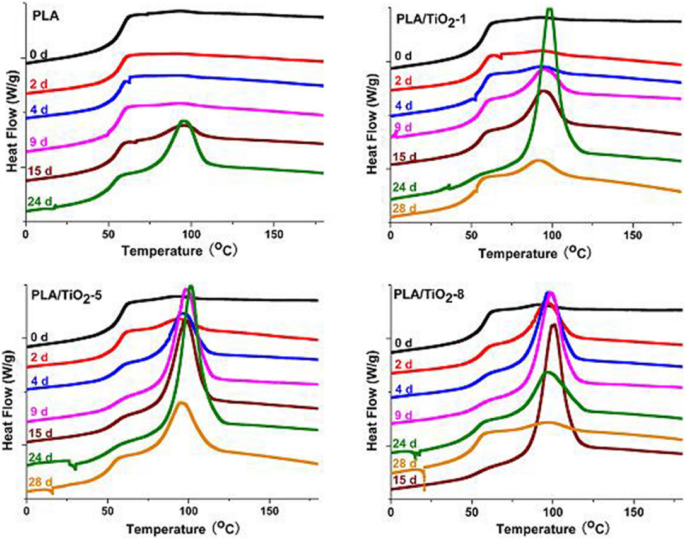
生分解された純粋なPLAおよびPLA / TiO 2 のDSCサーモグラム 異なるインキュベーション時間でのナノコンポジット、冷却スキャン
XRDは、分解中のポリマーの結晶化の変化を監視するための理想的な方法を提供します。 PLAとそのナノコンポジットのXRDパターン(図4)は、ポリマーマトリックスが生分解前にアモルファス構造を維持していることを示しています。 2日後、2 θに2つの強いピークがあります =16.4、18.5°、20.9°、および23.6°がはっきりと現れ、それらの強度はインキュベーション時間とともに増加しました。この結果は、ポリ(L-ラクチド)またはポリ(D-ラクチド)タイプの結晶構造が形成されたことを意味します[46、47]。結晶性ピークの変化は、アモルファス領域が結晶性領域よりも急速に分解し、それが結晶性対アモルファス領域の比率値を増加させたことを示した。この結果は、DSCの結果およびサンプルの透明度の変化と一致していました。
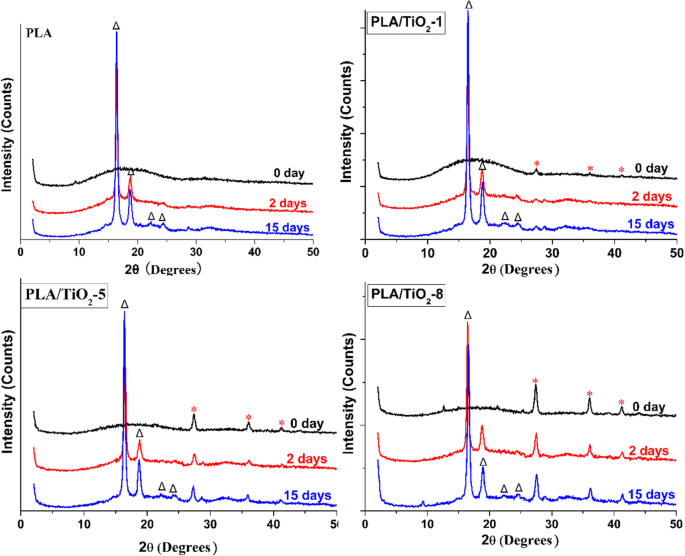
純粋なPLAおよびPLA / TiO 2 のXRDパターン 異なるインキュベーション時間でのナノコンポジット
接種材料の検証の評価は、堆肥化条件下での生分解中に非常に重要です。接種材料の活性は、標準的な方法である D で必要に応じて測定されました。 t 45日間のテストの終了時に、参照資料の70%以上である必要があります。図5の挿入図は、MCEが5日後に生分解を開始し、45日間のインキュベーションの終了時に生分解の割合が最大72%であることを示しています。これらの結果は、実験におけるMCEが参照物質として有効であることを示した。実験では、重複した堆肥化容器は良好な再現性を示しました(標準偏差±1.3%)。図5は、 D を示しています t きちんとしたPLAおよびPLA / TiO 2 の場合 インキュベーション中のナノコンポジット。 PLAとPLA / TiO 2 でも同様の動作が観察されました。 ナノコンポジット、つまり、ラグフェーズが最初に観察され、その後、生分解が急激に直線的に増加し、その後、すべてのサンプルでプラトーフェーズが続きます。増加の急峻さは、劣化の増加を示しているはずです。ただし、曲線は、ナノコンポジットのラグフェーズが純粋なPLAのラグフェーズよりも少し短いことを示しています。この結果は、TiO 2 の存在を示しています。 、ある程度、劣化の初期段階を加速し、CO 2 の割合を増やしました 潜伏期間の終わりに生成されます。制御された堆肥化条件下で80日間培養した後、 D t PLAの場合、PLA / TiO 2 –1、PLA / TiO 2 –2、PLA / TiO 2 –5、PLA / TiO 2 –8、およびPLA / TiO 2 –15は、それぞれ最大78.9、86.9、92.0、97.8、91.3、および85.0%に達しました。国岡ほか[48]は、PLAの最終的な生分解性は80%であると報告しました。私たちの実験の結果は、 D t 商業的に純粋なPLA製品の80%近くも80日の終わりにありました。 D の減少 t PLA / TiO 2 から開始 –8は、TiO 2 の激しい凝集によるものです。 その含有量が8wt%を超えたとき[16]。詳細については、次のセクションで説明します。
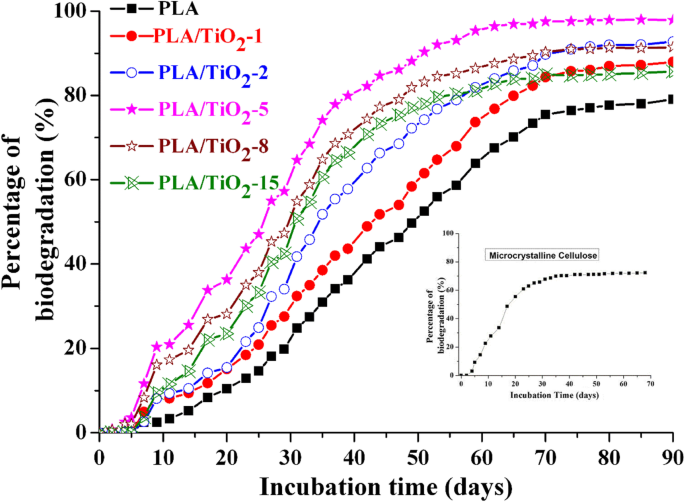
純粋なPLAおよびPLA / TiO 2 のインキュベーション時間の関数としての生分解のパーセンテージ ナノコンポジット。インサートは、微結晶性セルロースの時間の関数としての生分解のパーセンテージです
生分解のさまざまなパーセンテージは、ポリマーマトリックスのさまざまな分子量変化に関連しています。図6は、インキュベーション時間の関数としてのサンプルの分子量変化を示しています。曲線は、PLA / TiO 2 のMnの変化を示しています。 ナノコンポジットは、少なくとも決定されたインキュベーション時間において類似していた(すなわち、Mnの急速な減少とそれに続くほぼ一定のMnのプラトー相)。ナノフィラーの添加によって引き起こされる分解メカニズムを調査するために、生成されたカルボン酸末端基による自己触媒作用を説明するモデルを使用して、参考文献[17、49]に従って触媒分解速度定数を計算しました。
$$ \ ln {M} _ {nt} =\ ln {M} _ {n0} -kt $$(3)ここで k 触媒による加水分解速度定数、 M n0 は分解前の数平均分子量、 M nt は任意の時点での数平均分子量です。
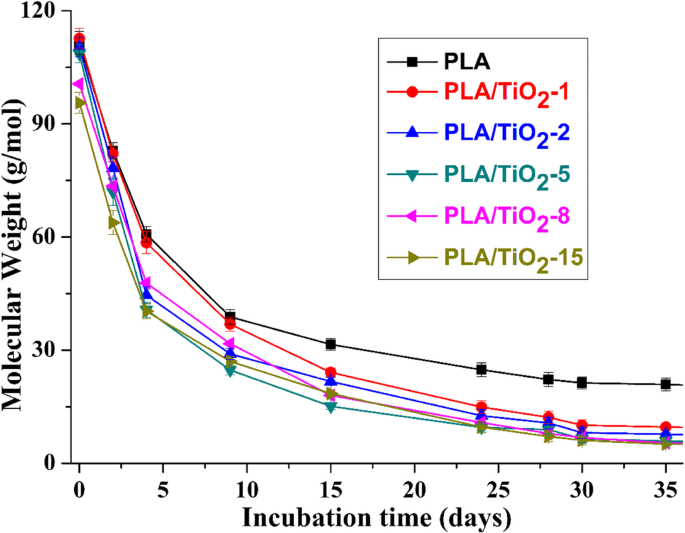
純粋なPLAおよびPLA / TiO 2 の時間の関数としてのMnの変化 ナノコンポジット
k 式によって評価された値。 (3)を図7にプロットします。図7から、PLAおよびPLAナノコンポジットの分解速度をそれぞれ2相および3相に特定することができます。 Mnは、最初の8日間で急速に減少し、その後、ニートPLAではプラトー段階が続きました。 PLA / TiO 2 の場合 ナノコンポジット、 k の最高値 M を意味します n 最初のフェーズで急速に減少しました(つまり、0日から4日)。次の5〜24日は、第2フェーズに起因し、 k の値は 第一段階と比較してわずかに減少しました。いくつかの研究[13、50]は、PLAの結晶部分がアモルファス部分よりも劣化に対して耐性があることを示しました。したがって、 k の減少 この段階では、PLAマトリックスの結晶化度の増加が原因である可能性があります。 24日後(つまり、最後のフェーズ)、 k の値 再び減少した。この段階で、ポリマーは完全にオリゴマーフラグメントまたは乳酸に分解され、微生物は残りの材料を鉱化して、CO 2 を継続的に生成します。 。
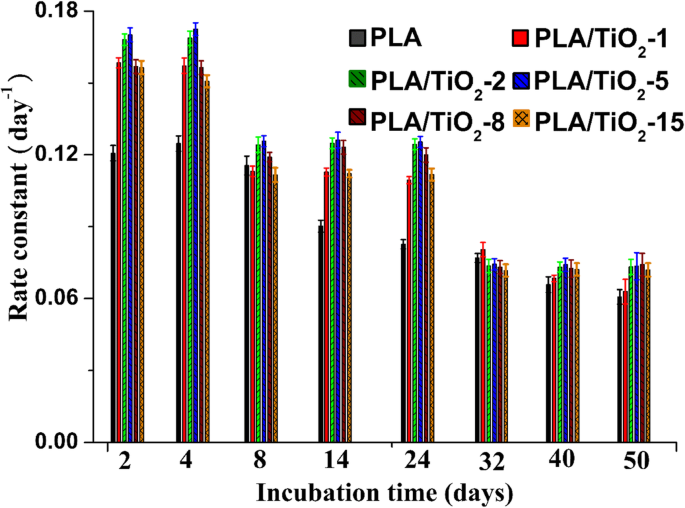
純粋なPLAおよびPLA / TiO 2 の生分解速度とインキュベーション時間の関係 ナノコンポジット
堆肥化条件下では、PLAの生分解傾向に影響を与える要因が、PLA / TiO 2 の分解を制御します。 ナノコンポジット。 g-TiO 2 の量が PLAマトリックスに均一に分散しているため、水分子はサンプル内に容易に浸透し、分解プロセスを引き起こします[17]。その結果、Mnは第1段階で大幅に減少しました。 CO 2 の遅滞期の進化 この期間中のPLAとそのナノコンポジットは、微生物が鉱化するのに適切なポリマー鎖を必要とすることを示しました。インキュベーション時間が長くなると、アモルファス領域のポリマー鎖が劣化し、アモルファス領域の数が減少しました。したがって、アモルファス領域に対する結晶のパーセンテージ(すなわち、χ c )増加[39]、それにより k の減少につながる 第二段階で。しかし、この段階でオリゴマーフラグメントが微生物によって鉱化され始め、それによってPLA鉱化作用の生産段階が起こったことを示しています。残りのオリゴマーフラグメントの減少とχ c の増加に伴い 、 k および D t k は減少し、ほぼ長いプラトー相が観察されました。 および D t 第三段階で。私たちの以前の研究[16]では、各ナノコンポジットの形態が報告され、SEMおよびTEMによって決定されました。結果は、g-TiO 2 の分散が PLA / TiO 2 で5wt%未満 ナノコンポジットは、高濃度のナノフィラーで得られたものよりも優れていました。 TiO 2 の分散と含有量に関して 、PLA / TiO 2 –5の k が最大でした および D t 私たちの実験の他のナノコンポジットと比較しました。
結論
PLA / TiO 2 ナノコンポジットを調製しました(PLAおよび官能化g-TiO 2 に基づく) )そして制御された堆肥化条件下で生分解を受ける。このような標準を使用すると、サンプルの表面のパターンの情報と結晶化度の急激な増加により、PLAとPLA / TiO 2 ナノコンポジットは、不均一な生分解メカニズムを持っていました。堆肥化条件下でのナノコンポジットの分解研究は、官能化チタニアナノ粒子(PLA / TiO 2 )を組み込んだ後も、PLAの固有の分解特性が残っていることを示しました。 )。 TiO 2 の追加 水分子がPLA / TiO 2 に容易に浸透するため、ナノ粒子はPLAマトリックスの分解速度を増加させました。 ナノコンポジット、それによって分解プロセスを活性化します。この現象は、PLA / TiO 2 で特に顕著でした。 TiO 2 が高いため–5 TiO 2 の含有量と良好な分散 他のナノコンポジットと比較したPLAマトリックスのナノフィラー。
略語
- DSC:
-
示差走査熱量測定
- D t :
-
生分解の割合
- GPC:
-
ゲル浸透クロマトグラフィー
- g-TiO 2 :
-
グラフト化されたTiO 2
- MCE:
-
微結晶性セルロース
- Mn:
-
数平均分子量
- Mw:
-
重量平均分子量
- PLA:
-
ポリ(乳酸)
- SEM:
-
走査型電子顕微鏡
- T cc :
-
低温結晶化ピーク
- T g :
-
ガラス転移温度
- XRD:
-
X線回折
ナノマテリアル
- ADMとLG化学が乳酸とPLAの米国生産を調査
- 金ナノ粒子修飾ガラス状炭素電極上の尿酸の強化された光電気化学的検出
- 化学センシング用の貴金属ナノ粒子で装飾されたエレクトロスピニングポリマーナノファイバー
- CuSナノ粒子でコーティングされた着色および導電性CuSCN複合材料の容易な合成
- ラウリル硫酸をドープしたポリアニリンとポリスチレンの新しいナノコンポジット
- 多機能GaN / Feナノ粒子による内皮細胞の標的化
- MoO3でコーティングされたTiO2ナノチューブ光電極上のAu-プラズモンナノ粒子によって強化された光触媒活性
- ポリ(4-スチレンスルホン酸-co-マレイン酸)による金磁性ナノ粒子の安定性の向上:タンパク質検出用に調整された光学特性
- 光触媒活性が強化されたAgナノ粒子/ BiV1-xMoxO4の相乗効果
- クルクミンの処理効果を持つPEGコーティングされたCoFe2O4ナノ粒子の毒性
- 抗菌剤として銀ナノ粒子で装飾された酸化グラフェンベースのナノコンポジット



