水素製鋼
水素製鋼
鉄鋼生産産業は、世界の化石および工業生産の総排出量の点で単一の最大のセクターであり、温室効果ガス(GHG)排出量の約7%から9%を占めています。同時に、鉄鋼は現代の産業社会の主要な材料成分です。インフラの拡張と改善、そして満足のいくレベルに到達するのに十分なペースで世界の生活水準を向上させる必要があるため、鉄鋼の消費量はさらに増加するでしょう。したがって、鋼を材料として社会的に使用することを可能にすると同時に、その製造による環境への悪影響を回避する鋼を製造するプロセスを見つけることが課題である。製鋼のCO2(二酸化炭素)排出量を削減するという観点から、水素(H2)ベースの製鋼ルートは魅力的な選択肢を提供するため、現在大きな注目を集めています。
H2による鉄鉱石の還元は、高炉(BF)での溶銑の製造と、直接還元鉄(DRI)/ホットブリケット鉄(DRI)の製造の両方で行われるため、よく知られています。 HBI)シャフト炉で。 BFでは、H2の製鉄源は、加湿された熱風と注入された微粉炭です。 DR-EAF(直接還元-電気アーク炉)に基づく製鋼ルートの場合、これは常に、天然ガス(NG)から触媒改質装置を介して生成されるH2の使用によって歴史的に特徴づけられてきました。炭化水素源はNGであるため、生成されるH2の濃度はさまざまであり、使用する酸化剤の比率に応じて一酸化炭素(CO)と混合することができます。
鉄鉱石のH2還元は、何十年にもわたって研究されてきました。スウェーデンでは、1950年代にすでにWibergとEdstromによる先駆的な調査が行われ、その後、プロセスの動力学と製造された製品の反応性を説明する多くの調査が行われました。流動床技術に基づく最初の商業規模のH2直接還元鉄鉱石(H2-DRI)プラント、Circoredは、1998年にトリニダードのポイントリサス工業団地にCliffs andAssociatesLtd.によって建設されました。プラントの設計は50万トンでした。 HBIの年間。工場は商業的に成功せず、2016年に閉鎖されました。
現在の世界的なシナリオでは、CO2の排出を完全になくすことはできないにしても、大幅に削減するために、H2による鉄鉱石の削減を利用するプロセスを見つけるためにいくつかの活動が行われています。成功を収める前に克服しなければならない多くの問題があり、製鉄および製鋼に使用されている現在のプロセスに厳しい競争をもたらす可能性があります。克服すべき主な問題のいくつかは、後続の段落で説明されています。
重要な問題の1つは、CO2排出量が少ないプロセスから生成された電力を使用するバルクH2の生産のための費用効果の高い方法を見つけることです。再生可能エネルギーの供給源は、太陽エネルギー、風力エネルギー、水エネルギー、海洋エネルギー、地熱エネルギーです。核エネルギーでは、化石を含まない燃料も使用されます。すべての再生可能エネルギーの中で、最も信頼できる2つの再生可能エネルギー源は、太陽光発電(PV)太陽エネルギーと風力タービンです。しかし、どちらの技術も日射や風の揮発性により電力供給が変動するという特徴があり、電力の供給が怖い時と豊富な時があります。風力と太陽光発電の大部分をエネルギーシステムに統合するには、生産と需要の間の一時的な不均衡を補うための大規模な貯蔵ソリューションが必要です。
2番目の問題は、バルクH2の保管(高圧ガス貯蔵または極低温液化貯蔵)です。 H2ストレージは、電力調達/価格設定の観点からメリットをもたらしますが、プロセスの概念にとってそれほど重要ではありません。今日、H2貯蔵の最も費用効果の高い代替案は、地下の塩層にH2を貯蔵する地下加圧貯蔵です。現在のシナリオでは、これは産業規模でテストされたH2ストレージの唯一のテクノロジーです。現在多くの関心を集めている他の解決策には、天然ガスパイプラインの利用や、中間H2貯蔵としてのアンモニアまたは炭化水素への変換が含まれます。現在スウェーデンで天然ガスに使用されているLinedRockCavern(LRC)技術の初期評価は有望であると考えられています。開発中のH2貯蔵の他の代替方法は、金属水素化物および多孔質材料での貯蔵です。
3番目の問題は、H2による還元によって生成された鉄は、さまざまな割合でCを含む溶銑やDRI / HBIとは異なり、炭素(C)を含まないことです。 Cは、Cボイルの製鋼に必要です。また、鋼はそのC含有量のためにその特性を引き出します。したがって、さまざまなグレードの鋼にさまざまな割合のCが存在します。ただし、EAFにCを追加できるため、この点に関する実際の技術的な問題は予想されません。
第4の問題は、鉄鉱石の採掘、処理、選鉱中、ペレットの製造中、およびこれらの材料の輸送中に発生するCO2排出量です。 H 2還元を利用するプロセスは、好ましくは、供給材料としてペレットを必要とする。この点で、再生可能エネルギー源を使用することで、CO2排出量の一部を削減できる可能性があります。
最初のプロセスはH2の大量生産であり、これは現在メタンの水蒸気改質によって達成されています。このオプションは、通常の99.9%プラス純度ではなく、97%から98%の純度のH2をターゲットにするなど、H2ベースの製鉄用に保持および最適化することもできます。ただし、化石資源に基づいているため、現在追求されている戦略とは異なる戦略を表すCO2回収ユニットが追加されない限り、CO2削減の観点からのパフォーマンスは全体的に平均的なままです。他の好ましいオプションは、水の電気分解によってH2を生成することです。 H2の生産は化石を含まない必要があるため、適切な生産方法は、CO2の少ない電力、つまり再生可能電力または原子力電力を使用した水の電気分解です。課題は、許容できる経済状況でH2の大量生産を達成することです。水の電気分解はよく知られている技術ですが、CO2を削減し、とりわけ製鉄に手頃な価格の大量のH2の目標を達成するには、いくつかの開発が必要です。植物のサイズは、電解槽を増やすことによって達成することができます。プロトン交換膜や高圧または高温電解など、新しく改良された技術も確認されています。
2番目のプロセスは、H2のみで運転されるシャフト炉で鉄鉱石を直接還元することによって鉄を生産することです。それはH2製鉄プロセスの中心です。シャフト炉の上部にはペレットまたは塊鉱石が供給され、重力によって下降し、H2の上昇流に遭遇し、反応器の中央の高さで横方向に供給され、上部から排出されます。還元反応は、還元ガスの出口と入口の間の上部で起こります。鉄への変換は、ガス入口のレベルで完了します。以下では、円錐曲線を使用してDRIを冷却できますが、メタン(CH4)の代わりにH2を使用することが望ましいです。ガス回路の残りの部分は、改良されたNGを使用する従来のDRIプロセスよりもはるかに単純であり、H2-H2Oで構成される上部のガスを冷却して水を凝縮します。分離されたH2はリサイクルされ、電解プラントからの新鮮なH2と混合され、目的の温度(約800℃から900℃)に再加熱されます。
100%で運転されるシャフト炉の還元ゾーンの数学的モデリングから。 H2は、H2による還元速度が速いため、理論的にはH2-CO混合物よりも速く完全な金属化を達成でき、現在のDRシャフトよりも小さい反応器が得られることがわかっています。
3番目のプロセスは、EAFでCフリーのDRIを溶解して鋼を製造することです。 H2ベースの還元プロセスでは、炭素鉄製品がゼロになります。これは、製鋼ステップで必要な化学的性質の鋼製品を製造するには、化石を含まないCソースが必要であることを示しています。
ULCOS(超低CO2製鋼)プロジェクトで研究された最良のH2ベースの製鋼ルート(図1)では、H2は水力または原子力を使用した水の電気分解によって生成されると考えられています。鉄鉱石はシャフト炉でH2によってDRIに還元されると考えられ、CフリーDRIはEAFで処理されて鋼を製造すると考えられます。このルートは、DR(直接還元)炉自体からの排出量がほぼゼロであるCO2電力コストを含め、300 kgCO2/鋼1トン未満のCO2排出量に関して有望なパフォーマンスを示しています。これは、BF-BOF(転炉)ルートの現在の約1,850 kg CO2 /鋼1トンと比較して、85%のCO2排出量削減に相当します。したがって、この新しいルートは、鉄鋼を製造するためのより持続可能な方法です。ただし、その将来の発展は、このガスが大量に、競争力のあるコストで、生産のためのCO2排出量が少ない状態で利用できるようになる、いわゆるH2経済の出現に大きく依存しています。
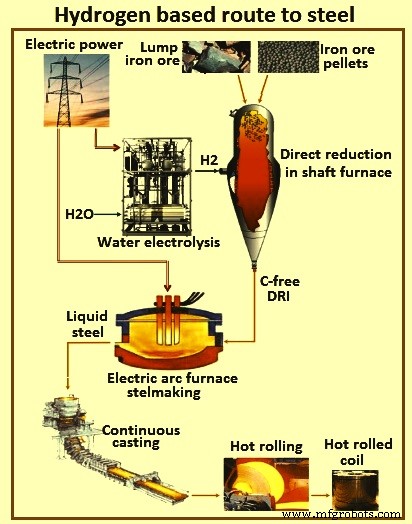
図1水素ベースの製鋼ルート
H2ベースの還元では、DRIルートと同様に、鉄鉱石は気固反応によって還元されます。唯一の差別化要因は、還元剤がCOガス、合成ガス、またはコークスではなく純粋なH2であるということです。 H2による鉄鉱石の還元は2つまたは3つの段階で起こります。 570℃を超える温度では、ヘマタイト(Fe2O3)鉱石は最初にマグネタイト(Fe3O4)に変換され、次にウスタイト(FexO)に変換され、最後に金属鉄に変換されます。熱力学的に安定していません。
H2による鉄鉱石の還元に関与する還元反応は、式(i)3 Fe2O3 + H2 =2 Fe3O4 + H2O、(ii)x Fe3O4 +(4x-3)H2 =3 FexO +(4x-3)で表されます。 )H2O、および(iii)FexO + H2 =x Fe + H2Oここで、xは0.95に等しい。これらの反応によって示されるように、H2による鉄鉱石の還元は、温室効果ガスCO2の代わりに無害な水蒸気(H2O)を放出します。 H2によるヘマタイト鉱石の還元の全体的な反応はFe2O3+3H2 =2Fe + 3H2Oであり、これは反応熱を伴う吸熱反応であり、298℃でのデルタH =95.8 kJ / molであり、プロセスし、注入された還元ガス/ガス混合物でエネルギーの追加を要求します。生産ラインの開発の焦点は、還元温度、反応の動力学、ペレット組成、および還元ガスの予熱技術に基づく最適化です。
ヘマタイト鉱石(Fe2O3)を還元するためのH2の化学量論的消費量は、鉄1トンあたり54kgです。したがって、年間100万トンの鉄鋼プラントには、標準温度および標準圧力(STP)で1時間あたり70,000cumの容量を持つH2プラントが必要です。還元ガスとしてH2を使用する場合、還元ガスとしてH2-CO混合物を使用する反応器と比較して、反応器の挙動の変化を予測することが重要です(図2)。速度論、熱力学、熱伝達、ガス流など、いくつかの要因がさまざまな方法で相互作用する可能性があります。速度論に関して、CO、H2、およびCO–H2混合物による酸化鉄の還元に関する実験室研究は、他のすべてが等しい場合、H2による速度論はCOによるものよりも速い(最大10倍)ことを明確に示しています。反応の特徴はCOによる還元の特徴と非常に似ており、多くのメカニズムが両方に共通しています。ただし、大きな違いもあります。
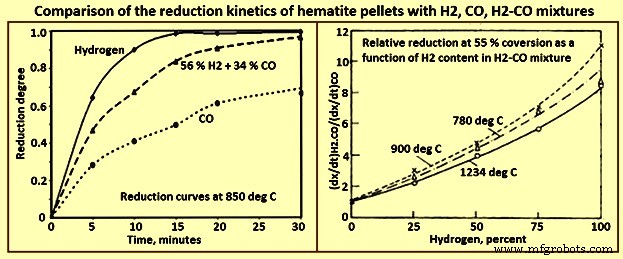
図2ヘマタイトペレットとH2、CO、およびH2-CO混合物の還元速度の比較
最初の主要な要因は熱力学であり、Chaudron図(図3)から明らかなように、低温でCOを優先します。青い縦の矢印は、ウスタイトから鉄への還元の推進力を表しています。これは、H2で温度とともに増加し、COで温度とともに減少します。
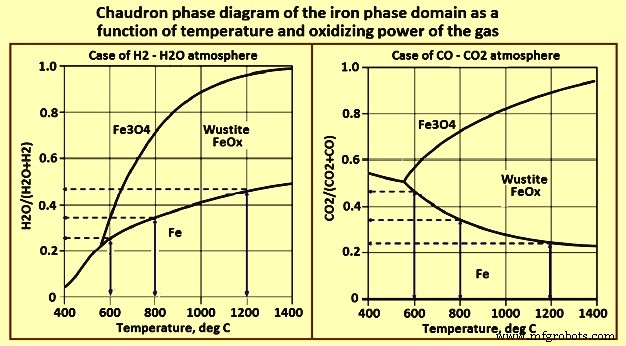
図3温度とガスの酸化力の関数としての鉄相ドメインのショードロン状態図
2番目の要因は、表1に示すように、還元反応の熱です。ヘマタイトからマグネタイトへの反応は、COよりもH2の方が発熱が少なく、マグネタイトからウステイトへの反応は吸熱性が高く、主に、ウスティト-鉄への反応は、H2で吸熱反応し、COで吸熱反応します。全体として、バランスはH2で吸熱還元し、COで発熱還元します。その結果、シャフト内の温度と組成は、入口ガスの組成によって大きく変化します。ガス注入ゾーンを離れるとき、メタン分解により温度は低下しますが、CO含有量が高いと、還元反応の発熱により床は高温に保たれますが、H2が多いほど温度は低くなります。 。
| Tab1還元反応の熱量 | |
| デルタH、800℃ | |
| J / mol | |
| 3Fe2O3 + H2 + 2 Fe3O4 =H2O | – 6,020 |
| 3Fe2O3 + CO =2 Fe3O4 + CO2 | – 40,040 |
| Fe3O4 + H2 =3 FeO + H2O | 46,640 |
| Fe3O4 + CO =3 FeO + CO2 | 18,000 |
| FeO + H2 =Fe + H2O | 16,410 |
| FeO + CO =Fe + CO2 | – 17,610 |
| 注:マイナス記号は発熱反応を示します | |
すべての場合において、COよりも多くのH2が3つの還元(反応速度の結果)に全体的に利用されている場合でも、後者の効果、つまりCOガスの場合は中央ゾーンでのCOによる還元が最終的に決定的です金属化度。また、H2のみを使用する場合(還元ガス入口と下部入口の両方)、より低温の中央ゾーンは存在せず、温度は放射状により均一になり、効率的な反応速度により還元は完了します(100%メタライゼーション)。
上記のように、H2による還元は吸熱性ですが、COによる発熱です。一方、熱力学は、800℃を超えるCOよりもH2の方が有利です。これにより、産業活動が異なります。 H2の場合、供給される高温ガスは、反応が発生するのに十分な高温で固体を加熱および維持するのに十分なカロリーをもたらす必要があります。したがって、化学量論よりも高いガス流量で操作する必要があります。速度論もH2の方が速いと報告されています。これにより、最終製品(鉄)の形態が変化する可能性があります。これは、拡散と化学反応の競合に依存します。特に、ウィスカーの形成は、H2による還元の特徴のようです。ウィスカーは、ウスタイト相から突き出て、粒子の外側に向かって指として成長する鉄の粒子です。ウィスカーは鉄と鉄の接触をより頻繁にし、したがって、高H2含有量で作動する工業用反応器で時々経験される固体粒子の付着の現象を説明することができます。 H2還元で観察される別の厄介な現象は、一部の温度で、反応の最後に速度が低下して変換度の最後のパーセントに達することです。
純粋なH2を備えたシャフト炉では、C源はありません。反応の吸熱性により、大量の熱が吸収され、バルク材料層の内部温度が急速に低下します。その結果、大量の熱を消費する必要のある還元反応は、ガス利用率の低下を引き起こす。望ましい生産性を維持するために、熱媒体としてのH2の量を増やす必要があります。一例として、上部の圧力が0.4 MPaの場合、シャフト炉の還元の熱需要を満たすために、900℃の温度でのH2の量はDRIのトンあたり少なくとも2,600cumである必要があります。 H2の添加量を変更しない場合、DRIの出力は現在の3分の1になり、DRIの製造コストが大幅に増加します。
H2の比重は低く、H2の密度はCOの1/20倍に過ぎません。その結果、入ってくるH2ガス分子は急速に上向きに逃げます。混合還元ガスの経路と方向と比較すると、炉内のH2の経路と方向は非常に速く変化するため、H2はシャフト炉の下部の高温ゾーンに留まらず、鉄鉱石ペレットの還元作業を完了できません。理論的には、DRI製品は、1 MPaを超える圧力と1,000℃を超える温度でH2の流入を維持することにより、設計された指標に到達することもできます。
また、H2は非常に可燃性で爆発性の高い物質であり、シャフト炉は高効率で長期安定した生産が必要です。高温高圧という究極の条件下でシャフト炉システムを長時間稼働させると、安全性が問題になります。つまり、直接還元率と生産効率は、H2比率、温度、圧力、ガス利用率、鉄鉱石の滞留時間、熱伝達、物質移動、シャフト炉の設計など、いくつかの要因の影響を受けます。
HYBRITイニシアチブ
HYBRITは「HYdrogenBReakthroughIronmakingTechnology」の略です。 2016年4月4日、スウェーデンの3社(SSAB、LKAB、Vattenfall AB)は、CO2排出のない電力を一次エネルギー源としてH2ベースのDRI生産プロセスの実現可能性を調査することを目的としたプロジェクトを開始しました。 3社を所有する合弁会社HYBRITDevelopmentABが設立されました。これにより、エネルギー生産、鉱業、鉱石の選鉱およびペレット生産、直接還元、溶解、および粗鋼の生産に至るバリューチェーン全体で最高の能力に完全にアクセスできます。 2017年にH2ベースの直接削減に関する事前実現可能性調査が実施されました。この調査では、提案されたプロセスルートは技術的に実現可能であり、CO2排出量と電力のコストの将来の傾向を考慮すると、スウェーデン北部/フィンランド。
HYBRITプロセスは、EAFと組み合わせて、鉄の直接還元(DR)のために石炭をH2に置き換えます。このプロセスはほぼ完全に化石を含まず、温室効果ガス排出量を大幅に削減します。このプロセスは、H2-DR / EAFセットアップを使用するいくつかのイニシアチブの1つであり、H2を使用した鉄鉱石の直接還元とEAFを組み合わせて、さらに鋼に加工します。 H2-DRプロセスの製品は、DRIまたはスポンジ鉄であり、EAFに供給され、適切な量のスクラップとブレンドされ、さらに鋼に加工されます。
HYBRIT製造プロセスの主なフローシートを図4に示します。このプロセスの主な特徴は、(i)ペレット製造に非化石燃料を使用する、(ii)化石を含まない電気を使用して電気分解でH2を製造する、(iii)特別に設計されたユニットでのH2の貯蔵は、グリッドへのバッファーとして使用されます。(iv)シャフト炉は鉄鉱石の還元に使用され、(v)オーダーメイドのペレットは鉄鉱石の供給に使用されます。(vi)還元ガス/ガス混合物は、シャフトに注入する前に予熱されます。(vii)製品はCを含まないDRIまたはHBIであるか、炭化されます。(viii)DRI / HBIは、EAFでリサイクルスクラップと一緒に溶融されます。
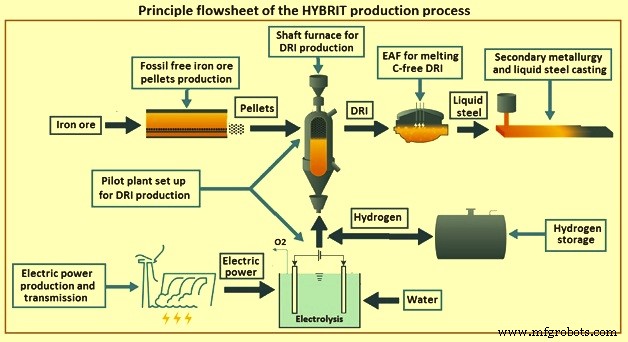
図4HYBRIT製造プロセスの主なフローシート
HYBRITイニシアチブで選択された主な代替案は、化石を含まない電気を使用した水の電気分解によって生成されたH2を使用して、シャフト炉内の鉄鉱石ペレットを削減することです。このイニシアチブの下で、鉱山から完成鋼への化石のないバリューチェーンへの転換には、地域の市場や地理的条件も考慮に入れて開発されるべき多くの問題が含まれます。スウェーデンは、国の北部、鉄鉱石鉱山の近く、バイオマスや製鉄所へのアクセスの良さ、業界、研究機関、大学間の強力なネットワークなど、電力容量が過剰であるという独特の状況にあります。
HYBRITプロセスは、商業展開に実質的に近い技術概念のカテゴリに分類されます。これは、還元剤としてのH2の使用に基づいており、H2は再生可能エネルギーに基づく電気分解によって生成されます。環境の観点から、これの最も重要な利点は、このプロセスからの排気がCO2ではなく水(H2O)であり、その結果、GHG排出量が削減されることです。従来のDRI製鋼と同様に、H2ベースのDRIルートを使用して製造された鉄は、市販のEAF技術を使用してさらに鋼に加工できます。電力とH2がPV(太陽光発電)太陽光/風力/水力電気分解、光化学H2生産、または太陽熱水などの再生可能資源を使用して生産される場合、H2生産とEAF製鋼ステップはCフリーにすることができます分割。
水素を使用したフラッシュ製鉄技術
代替製鉄のための新しい変換技術は、米国のAmerican Iron and Steel Instituteの財政的支援の下で、組織や研究所のコンソーシアムによって開発されています。この技術は、フラッシュ還元プロセスでの酸化鉄濃縮物の直接ガス還元に基づいています。新しい「フラッシュ製鉄技術(FIT)は、現在の平均的なBFベースの操作と比較して、エネルギー消費量を32%から57%削減し、CO2排出量を61%から96%削減する可能性があります。この技術は、フラッシュリアクター内の鉄鉱石濃縮物を、H2や天然ガスなどの適切な還元性ガス、および場合によってはバイオ/石炭ガスまたはそれらの組み合わせで還元します。これは最初のフラッシュ製鉄プロセスです。この技術は、鉄鉱石精鉱(100ミクロン未満)をさらに処理することなく金属に変換する産業活動に適しています。
この革新的な技術は、ペレット化や焼結、およびコークス製造ステップをバイパスしながら鉄を生成します。さらに、濃縮物の微粒子が1,150℃から1,350℃に高速で還元されるという事実のために、このプロセスは集中的である。したがって、このプロセスに必要な滞留時間は、ペレットや鉄鉱石の微粉にさえ必要な分と時間。 1200°C〜1500°Cで2秒〜7秒で90%〜99%の削減が行われます。滞留時間は、温度、供給材料のサイズ、過剰ガスの量/からの距離による反応速度の組み合わせです。平衡線。還元ガスとしてH2を使用するプロセスのエネルギー要件は、5.7 GJ(1,360 Mcal)/溶鉄1トンです。 Fe/FeOの平衡状態図を図5に示します。
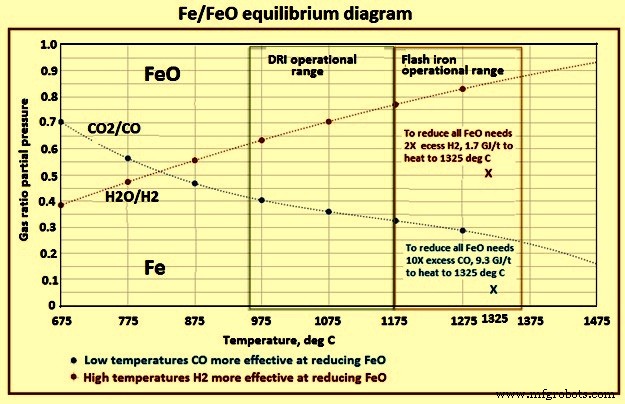
図5Fe/FeO平衡状態図
反応器の加熱部分は、誘導加熱コイルがグラファイトサセプタを加熱する場所です。サセプタは、放射線によって耐火壁を加熱します。サセプタと耐火物の両方が、対流と放射によってガスと粒子を加熱します。温度まで加熱された後、ガスと粒子は反応ゾーンに入ります。反応ゾーンでは、良好な断熱が想定されているため、壁の状態は断熱的に設定されます。反応ゾーンの後に、ガスと粒子を冷却するための冷却パネルを備えた冷却ゾーンがあります。図6にフラッシュ製鉄技術のフローシートを示します。
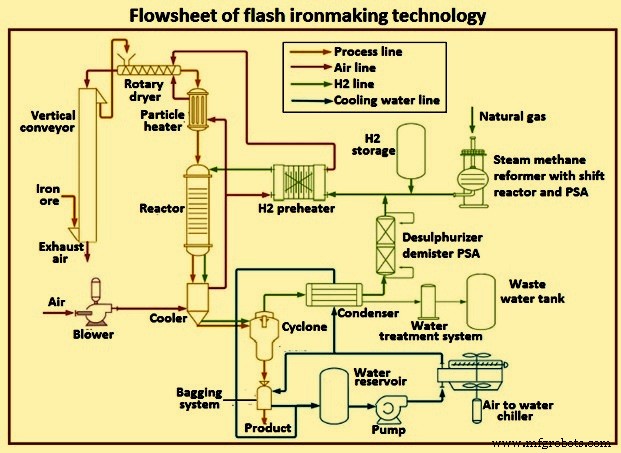
図6フラッシュ製鉄技術のフローシート
還元ガスとしてH2を使用するFITの場合、CO2排出量は溶鉄1トンあたり0.04トンのCO2です。これらの排出量は、製鉄のBFルートの排出量の2.5%です。フラッシュアイアンプロセスは、個々の粒子が酸素除去によって作成された細孔を閉じるのに十分なエネルギーを持つように、十分に高い温度で実行されます。したがって、個々の粒子は、急速な酸化による発火の影響をはるかに受けにくい。ユタ大学は、粉末の少量のサンプルについて調査を行い、それらが自然発火性ではないと判断しました。
このプロセスでは、NG、H2、合成ガス、またはそれらの組み合わせなどのガス状還元剤を使用します。それは製鋼プロセスへの供給として、または連続直接製鋼プロセスの一部として鉄の生産に適用されます。プロジェクトの前の段階で得られた実験データによって正当化されるように、スケールアップ開発作業は現在ユタ大学で進行中です。実験室のフラッシュ炉でのテストにより、幅広い動作条件にわたる反応速度データベースが確立され、より高度なベンチリアクターの完全な設計が実現しました。産業的に実行可能なFITを開発することを目的として、包括的なベンチスケールテストキャンペーンが計画されています。プロジェクトのこのフェーズからの成果物は、プロセスのスケーラビリティ、実質的なプロセスシミュレーションの結果、および産業パイロットプラントの設計と建設につながる基本的なエンジニアリングデータの決定であることが期待されます。
製造プロセス



