アナターゼ-ルチル比とTiO2ナノ粒子の光触媒性能に及ぼす酸性解膠剤の影響
要約
TiO 2 ナノ粒子は、硫酸、硝酸、および酢酸を使用する単純な解膠法によってチタンイソプロポキシドから合成されました。 TiO 2 の物理化学的および光触媒特性に及ぼす解膠酸の影響 粉末が研究された。合成されたTiO 2 の構造特性 粉末は、XRD、TEM、N 2 を使用して分析しました。 -物理吸着、ラマン、DR UV- vis 、FTIR、およびX線光電子分光法。特性評価の結果は、酢酸の解膠が500°Cでの熱処理後の純粋なアナターゼ相の形成を促進することを示しました。対照的に、硝酸の解膠は主要なルチル相の形成をもたらしました(67%)。興味深いことに、硫酸を使用して解膠されたサンプルは、95%のアナターゼと5%のルチル相を生成しました。合成されたTiO 2 の光触媒活性 ナノ粒子は、選択された有機染料(クリスタルバイオレット、メチレンブルー、および p )の分解について評価されました。 -水溶液中のニトロフェノール)。その結果、TiO 2 硝酸を使用して解膠されたサンプル(ルチル相とアナターゼ相が3:1の比率)は、有機色素の分解に対して最高の活性を示しましたが、TiO 2 硫酸と酢酸を使用して解膠したサンプルは、粒子サイズが小さく、バンドギャップエネルギーが高く、表面積が大きくなっています。興味深いことに、TiO 2 硝酸で解膠されたサンプルは、比較的高い理論的光電流密度(0.545 mAcm -2 )を持っていました。 )および細孔径(150Å)。これらは、光化学分解プロセス中の高い電子正孔分離効率と有機反応物の拡散および大量輸送に関与します。 TiO 2 の優れた活性 硝酸でペプチン化されたサンプルは、ルチル相とアナターゼ相の間で光生成された電子が効果的に移動するためです。
背景
二酸化チタン(TiO 2 )は、太陽エネルギー変換、汚染防止、光触媒など、多くの用途で使用されることで広く知られている半導体材料です[1,2,3]。 TiO 2 一般に、アナターゼ、ルチル、ブルッカイトの3つの多形があります。アナターゼとブルッカイトは、高温(<610°C)での熱処理後にルチルに変換できることが報告されています[4、5]。 TiO 2 アナターゼは、有機汚染物質の分解のための活性な光触媒であることが知られています[1、5、6、7、8]。 TiO 2 のサイズ、結晶相、および多孔性が観察されました。 サンプルは、そのアプリケーションに強い影響を及ぼします[9]。多孔質ナノサイズTiO 2 の低温合成 より長い合成時間が必要です[10、11、12]。 Li etal。 [13]アモルファスTiO 2 を熱処理することにより、純粋なアナターゼとルチル相とアナターゼ相の混合物を合成しました 。純粋なアナターゼの形成には、高温(500°C)での熱処理が含まれ[14]、これによりTiO 2 が焼結することがよくあります。 ナノ構造。低温での純粋な結晶アナターゼの合成は、興味深い研究トピックです[15]。ゾルゲル法と水熱合成法[16]を使用して、結晶性の高いTiO 2 を調製しました。 低温および短い反応時間で[17]。王ら。 [12]熱水HNO 3 によって高結晶性アナターゼとルチルナノ粒子を合成 解膠されたTiO 2 ソル。ただし、水熱法では、特別な合成条件と高価な装置が必要であり、高いpHと温度に耐えることができます[18]。
穏やかな温度(<100°C)でチタンアルコキシドをTi前駆体として利用することにより、ゾルゲル合成法を使用し、高度に分散したナノサイズのTiO 2 を生成しました。 サンプル[16]。化学的解膠法は、TiO 2 を含む安定した金属酸化物ナノ構造の合成に適合しました。 [19]、凝固した懸濁液が溶解し、解膠剤を含むナノ粒子の安定した溶液に再結晶します[20]。解膠酸の性質は、結晶子のサイズ、組成、粒子の形態などの物理化学的特性に影響を与えることが報告されています[21]。 Zaban etal。 [22]合成されたTiO 2 HNO 3 のコロイド およびCH 3 熱水条件下でのCOOHは、両方の場合でアナターゼとブルッカイトの混合物の形成を観察しました。 Liu etal。 [23]得られたTiO 2 さまざまな解膠剤下でのメタチタン酸からのヒドロゾルおよび解膠条件がTiO 2 の構造および光触媒特性に及ぼす影響を研究しました ハイドロゾル。 KannaとWongnawa [24]は、ゾルゲル合成法を使用して、HCl、HNO 3 などのさまざまな酸を使用してアモルファスアナターゼルチルを取得しました。 、H 2 SO 4 、H 3 PO 4 、およびCH 3 COOH。著者らは、硫酸基とリン酸基の存在がルチル相の成長の阻害に関与していることを観察しました。その後、Alphonse etal。 [25]合成されたTiO 2 強酸性媒体中でのチタンイソプロポキシドの加水分解によるアナターゼ相とブルッカイト相で構成される凝集体。パラら[26]は、酢酸を用いたアナターゼナノ粒子の合成における反応経路を研究しました。彼らはFTIRおよびNMR技術を使用して、酢酸イオンが2つのTi中心間の二座配位子として機能すると結論付けました。
周ら。 [27] HCl、HNO 3 の効果を研究しました 、およびCH 3 3D TiO 2 を合成するためのソルボサーマル法でのCOOH 異なる形態の構造。著者らは、0.68 M HClで合成されたサンプルは、アナターゼ/ルチル相の両方を持ち、その独特の形態と光学特性により、最高の光触媒活性を提供すると結論付けました。 Tobaldi etal。 [28] HNO 3 によるチタンイソプロポキシドの制御された加水分解/解膠を採用 、HBr、およびHClを使用して、TiO 2 を合成します。 ナノ粒子。ハロゲン化物イオンがアナターゼからルチルへの相転移を促進することが観察され、450°Cでの煆焼後、サンプルには最大77 wt%のルチルと5 wt%のブルッカイトが含まれていました。
以前の出版物[29]では、ナノサイズのTiO 2 の合成 大気湿度条件下でのキセロゲルの酸性解膠による粉末を実施した。超音波振動を伴う酸性解膠がTiO 2 に影響を与えることが観察されました。 構造特性。しかし、ルチル相の形成に対する解膠条件の影響と、その後のTiO 2 の光触媒活性に対する影響を研究するために捧げられた研究は、ほんのわずかでした。 ナノ粒子。この論文では、解膠酸(H 2 )の性質の影響を調べました。 SO 4 、HNO 3 、およびCH 3 COOH)ルチル相の形成とTiO 2 の光触媒効率への影響 3つの異なる有機汚染物質(クリスタルバイオレット(CV)、メチレンブルー(MB)、および p )の分解におけるナノ粒子 -ニトロフェノール( p -NP))。
メソッド
さまざまなペプチド化酸を使用したTiO2ナノ粒子の調製
チタンテトライソプロポキシド[Ti(OPri) 4 ]をTi前駆体として使用し、Ti(OPri) 4 の加水分解を行いました。 標準的な大気条件下で実施された[29]。一般的な合成手順は次のように説明できます:50 mLのTi(OPri) 4 暗いガラス瓶に入れ、ドラフト内に15日間放置しました。ドラフトの温度と湿度は、それぞれ25±5°Cと50±10%と測定されました。 Ti前駆体の加水分解は15日で完了し、得られた溶液をゲルに変換し、次に乾燥させてキセロゲルを得ました。解膠酸(100mLの1N CH 3 COOHまたはHNO 3 またはH 2 SO 4 )をピペットでガラスビーカーに入れ、既知量のアモルファスキセロゲル粉末(2.0 g)を一定の攪拌下でペプチイジング酸にゆっくりと加えました。次に、ビーカーを40°Cに維持された超音波浴に入れ、混合物を10分間超音波処理しました。解膠されたTiO 2 遠心分離後にナノ粒子を収集した。次に、材料を蒸留水で洗浄し、500°Cで3時間煆焼しました。合成されたサンプルは、TiO 2 としてラベル付けされました CH 3 に対応する「ace」、「nit」、および「sul」としての解膠酸の後の頭字語の接頭辞 COOH、HNO 3 、およびH 2 SO 4 それぞれ。
材料の特性評価
粉末X線回折プロファイルは、CuKα放射線を備えたPhilipsPW1700回折計と自動発散スリットを備えたグラファイトモノクロメーターを使用して収集されました。 XRDプロファイルは、標準のJCPDSデータで索引付けされました。 Spurr and Myers [30]式[Eq。 (1)]を使用して、アナターゼ相とルチル相の重量分率を決定しました。
$$ {X} _ {\ mathrm {R}} =1 / \ left [1 + k \ \ left({I} _ {\ mathrm {A}} / {I} _ {\ mathrm {R}} \右)\右] $$(1)ここで私 A および私 R それぞれ、アナターゼの(101)反射とルチルの(110)反射の積分強度です。経験的定数 k この作品では0.80とされました。合成されたサンプルの結晶子サイズは、Scherrerの式[Eq。 (2)]およびアナターゼ(101)とルチル(110)の反射。
$$ D =B \ lambda / {\ beta} _ {1/2} \ cos \ theta $$(2)ここで D は相の平均結晶子サイズ、 B はシェラー定数(0.89)、λ はX線放射の波長(1.54056Å)、β 1/2 は反射の半値全幅であり、θ は回折角です。
サンプルのTEM分析は、200kVのフィールドエミッションガンを備えたPhilipsCM200FEG顕微鏡を使用して実行されました。球面収差係数Cs =1.35mmを適用しました。ピクセルサイズが0.044nmのHRTEM画像は、CCDカメラで撮影されました。サンプルのレーザーラマンスペクトル分析は、FRA106 / SFT-Ramanモジュールと液体N 2 を備えたBrukerEquinox 55FT-IR分光計を使用して実行されました。 -出力レーザー出力が200mWのNd:YAGレーザーの1064nmラインを使用した冷却Ge検出器。
N 2 -物理吸着測定は、ASAP 2010機器、Micromeritics Instrument Corporation、米国を使用して実施されました。比表面積( S ベット )のサンプルは、N 2 を使用して測定されました。 -吸着値とBET方程式。サンプルの細孔幅と細孔容積は、BJH法を適用して決定しました。
拡散反射率UV- vis 合成されたTiO 2 のスペクトル サンプルは、Thermo Scientific Evolution分光光度計を使用して、220〜700nmの波長範囲で記録されました。サンプルのバンドギャップエネルギーは、Kubelka-Munk変換( K )を使用して決定されました。 )式に示されているように。 (3)。
$$ K =\ frac {{\ left(1-R \ right)} ^ 2} {2R} $$(3)ここで R は反射率です。波長(nm)はエネルギー(eV)に変換され、\({\ left(\ mathrm {Kh} \ upnu \ right)} ^ {0.5} \)vsのプロットが表示されます。 hνが描かれました。バンドギャップエネルギー(eV)は、描かれた曲線の2つの勾配の交点として推定されました。
サンプルのX線光電子スペクトルは、Thermo Scientific Escalab 250 Xi XPS装置を使用して、スポットサイズが650mmのAlKαX線で収集されました。電荷補償によるピークシフトは、C 1s の結合エネルギーを使用して補正されました。 ピーク。データは、100 eVの通過エネルギー、0.1 eVのステップサイズ、10〜30回のスキャンで200msの滞留時間を使用して取得されました。
クリスタルバイオレット、メチレンブルー、および p の光触媒分解 -ニトロフェノール
CV、MB、および p の光触媒分解 -NP実験は、合成されたTiO 2 を使用してガラス反応器で実施されました。 さまざまな反応時間のUV照射下での光触媒としてのサンプル。 18 Wの電力と60×2.5cmの寸法の合計6つのブラックUVランプ(F20 T8 BLB)を使用しました。有機染料水溶液の表面でのUV照射の総出力は、Newport 918DUVOD3検出器で測定され、出力計は13 Wm -2 と測定されました。 。 100mLの有機汚染物質(10 ppm)水溶液に100ミリグラムの触媒を添加しました。触媒の光触媒効率を評価する前に、有機染料溶液を45分間撹拌して触媒と平衡化し、触媒表面への有機染料の吸着を安定させました。 CV、MB、および p の光触媒分解 -NPは、Thermo Fisher Scientific Evolution 160 UV- vis を使用して、一定の時間間隔で有機色素の吸光度を測定することによって監視されました。 分光光度計。劣化率は、式を使用して計算されました
$$ \ eta =\ left(1-C / {C} _0 \ right)\ times 100 $$(4)C 0 は照明前の有機染料の濃度であり、 C は特定の反応時間後の濃度です。
光触媒の安定性は、再利用性実験によって分析されました。触媒の再生は、簡単な手順を使用して実行されました。活性測定の最初のサイクルの後、遠心分離によって触媒を光反応器およびアリコートから濾過した。得られた触媒を蒸留水とアセトンで十分に洗浄した。触媒を50°Cで2時間乾燥させた後、次の光触媒測定サイクルに再利用しました。同様に、触媒の安定性を研究するために、実験を数サイクル繰り返しました。
結果と考察
X線粉末回折
煆焼したTiO 2 のX線回折パターン -エース、TiO 2 -nit、およびTiO 2 -sulサンプルを図1に示します。TiO 2 のXRDピーク位置と強度 サンプルに示されているフェーズは、JCPDSデータベースで補完されます。アナターゼ相は2 θに主要な回折ピークを示すことが知られています。 (101)、(004)、(200)、(105)、(211)、および(204)結晶面に一致する24.8°、37.3°、47.6°、53.5°、55.1°、および62.2°の値[JCPDS番号21-1272]。一方、ルチル相は2 θに主要な回折ピークを示します。 (110)、(101)、(200)、(111)、(210)、(の結晶面に対応する27.0°、35.6°、40.8°、54.0°、53.9°、56.1°、および61.0°の値211)、(220)、(002)、および(310)[JCPDS No.21-1276]。サンプルに示されているアナターゼ相とルチル相の結晶子サイズと重量分率は、それぞれシェラー式とスパーおよびマイヤーズ法を使用して決定されました。 TiO 2 の粉末XRDパターン -aceサンプルは、粒子サイズが48 nmの純粋なアナターゼ相(100%)で構成されていることを示しました(表1)。
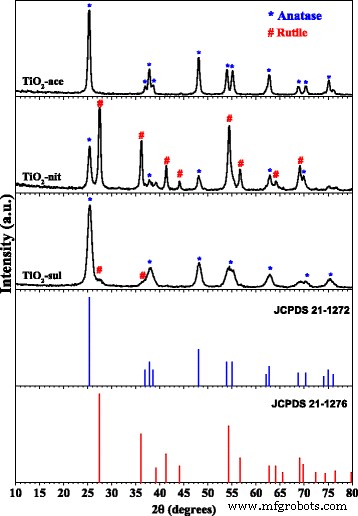
煆焼したTiO 2 の粉末XRDパターン サンプル([29]の許可を得て転載。Copyright@ 2017 Elsevier)
TiO 2 -sulサンプルは主にアナターゼ相(95%)を持ち、粒子サイズは約23nmでした。ただし、このサンプルでは、ルチル相の(110)面に対応する小さな回折ピークを見ることができます。対照的に、TiO 2 -nitサンプルは、アナターゼ相とルチル相の両方でXRD反射を示し、結晶子サイズはそれぞれ41nmと50nmでした。このサンプルでは、ルチルが主要な相(67%)であることが観察されます。これらの結果は、解膠酸の性質がTiO 2 の形成に役割を果たすことを示しています。 フェーズ。
高分解能透過型電子顕微鏡
TEMは、合成されたTiO 2 の粒子のサイズ、結晶化度、および形態を調べるために実行されました。 ナノパウダー。合成されたTiO 2 のTEMおよびHRTEM写真 ナノ粉末が図2に表示されています。TiO 2 -sulサンプルは、推定平均粒径が約7nmの密に詰まったアナターゼ粒子で構成されています。 TiO 2 -nitサンプルは、球形の形態を持つ10〜20 nmのサイズのナノ粒子と、幅20nmの大きなシートを持っていました。対照的に、TiO 2 -aceサンプルはTiO 2 で構成されています ナノ粒子(15〜20 nm)は、ほとんどが定義された球状の形態で構成されていました。 VinogradovとVinogradov [31]も、HNO 3 などの強力な解膠酸を使用した場合に、小さなサイズの凝集体が検出されたのと同様のタイプの結果を観察しました。 およびH 2 SO 4 解膠に使用されました。 Schererの式で測定された結晶子サイズは、TEM分析で測定された粒子サイズと比較してより大きな結晶子サイズをもたらしました。以前に報告されたように、結晶子のサイズは粒子のサイズとは異なります。ただし、結晶子のサイズが粒子のサイズと一致する場合もあります[32]。 TiO 2 のHRTEM画像を観察することができます -sulおよびTiO 2 -aceサンプルは、 d のアナターゼ結晶格子面に対応するフリンジを含む粒子を示しました。 -(101)面の間隔は0.356 nm [33]ですが、TiO 2 のHRTEM画像は -nitサンプルは、 d のルチル結晶格子面(110)の格子縞を持つ粒子を示しました。 -アナターゼ結晶格子(101)面に沿った0.325nmの間隔。

煆焼したTiO 2 のTEMおよびHRTEM画像 サンプル
ラマン分光法
ラマン分光法は、合成されたTiO 2 の相形成を調べるためにも使用されました。 サンプル。図3は、3つのTiO 2 で得られたラマンスペクトルを示しています。 500°Cで煆焼したサンプル。アナターゼ相とルチル相は、それぞれ6つと5つのアクティブなラマンバンドを持っていると報告されています(アナターゼ143、195、395、512、および638 cm -1 ;ルチル145、445、611、および826)[34]。図3から、3つのサンプルすべてが非常に強い鋭いラマンバンド( E )を示したことが明らかです。 g )141〜146 cm -1 の範囲 、アナターゼ相の存在による特徴的なバンドです。挿入図では、アナターゼ相とルチル相の両方に起因する低強度のラマンバンドをはっきりと観察できます。 TiO 2 -nitおよびTiO 2 -sulサンプルは、アナターゼ相とルチル相の両方に起因するラマンバンドを示しました。ただし、TiO 2 の場合、ルチル相の存在によるラマンバンドの強度が高くなります。 -nitサンプル。対照的に、TiO 2 -aceサンプルは、アナターゼ相のみのためにラマンバンドを示しました。
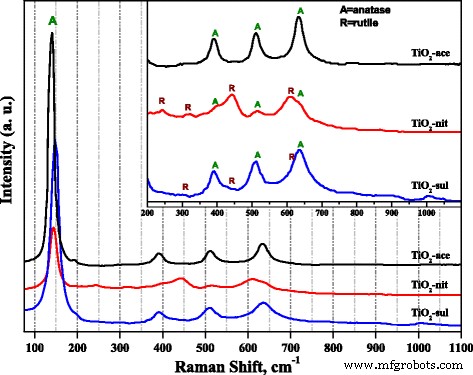
煆焼したTiO 2 のラマンスペクトル サンプル
ラマン分光法の結果を使用して、TiO 2 の粒子サイズを調査できることが報告されました。 ラマンバンドの異常なバンドシフトは、サンプルの粒子サイズの減少と相関している可能性があるため、ナノ粒子[35]。図3では、TiO 2 -aceサンプルは E を展示しました g 141.5 cm -1 のバンド;ただし、バンドは146および150 cm -1 にシフトされました。 TiO 2 の場合 -nitおよびTiO 2 -それぞれsulサンプル。ラマンスペクトルからの観察は、TiO 2 -sulサンプルは、他の2つのサンプルよりも粒子サイズが小さく、XRDおよびTEM観察に準拠しています。
拡散反射UV- vis
DR UV- vis 合成されたTiO 2 のスペクトル 500°Cで熱処理されたサンプルを図4に示しました。DRUV- vis の導関数の最大ピークの位置 図の挿入図には、3つのサンプルのスペクトルが示されています。これは、サンプルがUV領域で強い電子反射率を持っていることを明確に示しています。反射率のピークの最大値は、3つの異なる酸を使用して合成されたサンプルで異なります。 TiO 2 -sulサンプルは372nmで最大ピークを示しましたが、TiO 2 では383nmにシフトしています。 -TiO 2 の場合はaceおよび402nm -それぞれnitサンプル。アナターゼとルチルのバンドギャップエネルギーは、それぞれ3.2 eV(380 nm)と3.0 eV(415 nm)であると報告されています[1]。最大反射率の違いは、サンプルの結晶子サイズと相構造の変化に起因する可能性があります[36]。ルチル相の割合が高いサンプルでは、吸収の最大値がより高い波長にシフトしました。煆焼されたサンプルのバンドギャップエネルギー(eV)は、hνと(αhν)の関係を決定することによって計算されました[2] [追加ファイル1:図S1]。データは、TiO 2 のバンドギャップエネルギーを明らかにしました。 -sul(3.12 eV)は、TiO 2 と比較して高い -ace(2.99 eV)およびTiO 2 -nit(2.97 eV)。 TiO 2 のバンドギャップ サンプルでルチル相が支配的である場合、減少しました。アナターゼ相とルチル相の価電子帯(VB)は、主にO 2p によるものであると報告されています。 州;一方、伝導帯(CB)はTi 3d で構成されています。 状態[37]。 TiO 2 のバンドギャップエネルギー は、主に相組成に影響されるCBおよびVBの位置によって確立されます。したがって、アナターゼ相とルチル相の両方を含むサンプルのバンドギャップエネルギーは、純粋なアナターゼとルチルの値の中間にある必要があります。
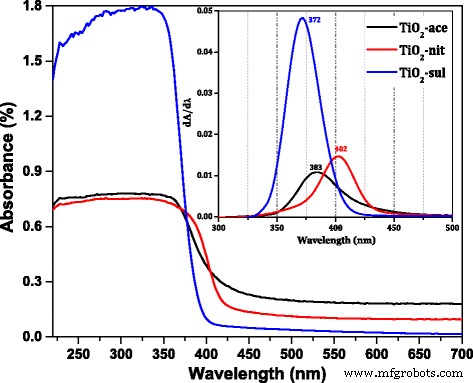
DR UV- vis 煆焼したTiO 2 のスペクトル サンプル(挿入図; DR UV- vis の派生物 スペクトル)
N 2 -物理吸着測定
合成された3つのサンプルの窒素吸脱着等温線を図5aに示します。酢酸(TiO 2 )による解膠によって合成されたサンプルでは、H2タイプのヒステリシスループを持つタイプIV等温線が観察されました。 -エース)および硫酸(TiO 2 -sul)。これは、これら2つのサンプルがTiO 2 の凝集体に起因するメソ細孔を持っていることを示しています。 ナノ粒子。ただし、TiO 2 では、H3タイプのヒステリシスループが狭い典型的なIV型等温線(開いたおよび/またはスリット状の細孔の特性)が観察されました。 -nitサンプル。ヒステリシスループが高い相対圧力( P / P )で閉じられたことも観察できます。 0 = 1)そしてこの観察は大きなサイズの細孔の存在を示しています[38]。
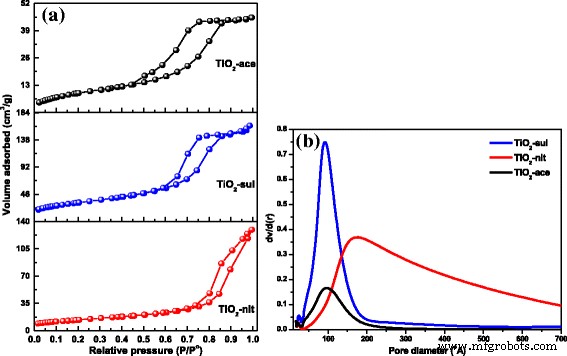
a N 2 吸着-脱着等温線。 b 煆焼したTiO 2 の細孔径分布 サンプル([29]の許可を得て転載。Copyright@ 2017 Elsevier)
合成された材料のBJHモデルの細孔径分布は、等温線の吸着分岐の値から得られました。サンプルのBJH細孔径分布を図5bに示します。 TiO 2 では、狭い単峰性の細孔径分布が観察されました。 -エースとTiO 2 -sulサンプル。しかし、硝酸で調製されたサンプルでは、おそらくより大きな粒子の間にボイドスペースが存在したために、より広い細孔径分布が観察されました。サンプルのテクスチャ特性を表1に示します。結果は、表面積が大きい(115 m 2 )ことを示しています。 g -1 )TiO 2 で観察されました -エースサンプルを500°Cで煆焼。 S の順序 ベット 変化はTiO 2 でした -エース> TiO 2 -sul> TiO 2 -nit。観察された結果は、適応された解膠条件が多孔質テクスチャーを備えたナノ粒子の生成に非常に効果的であることを明確に示しています。
フーリエ変換赤外分光法
TiO 2 の光触媒活性 結晶化度、結晶子サイズ、組成、電子正孔再結合率、表面積、および表面ヒドロキシル基の密度に依存します[39]。 FTIRおよびXPS分光法を使用して、煆焼したTiO 2 に存在する-OH基の性質を調査しました。 サンプル。図6は、3つのTiO 2 のFTIRスペクトルを示しています。 1600〜4000 cm -1 の範囲のサンプル 。 TiO 2 支持体は、さまざまな種類の表面ヒドロキシル基を持つ可能性があります。それらは、孤立したTi-OH、水素結合を介して互いに結合したヒドロキシル基、および化学結合したH 2 として分類できます。 O分子[40]。
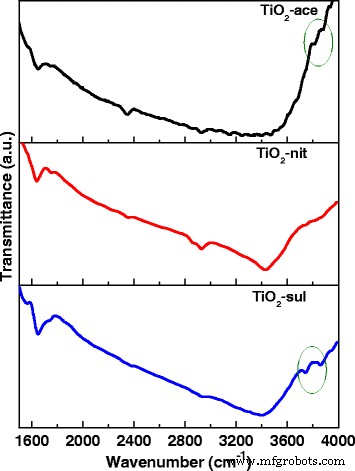
煆焼したTiO 2 のFTIRスペクトル サンプル
3つのサンプルは、3408 cm -1 を中心とする広帯域を示しました。 、これはO-H基(水分子と自由表面–OH基)の伸縮振動に起因します。追加のバンドも2340および1640cm -1 に表示されました 、O-H伸縮振動と分子吸着H 2 に割り当てることができます それぞれO [41]。アナターゼの場合の2つの–OH伸縮振動の存在(3715および3675 cm -1 )および3680 cm -1 の1つの弱いバンド ルチルを含むことは以前に報告されました[42]。合成されたTiO 2 の場合にも、非常によく似た結果が見られます。 サンプル。
X線光電子分光法
図7は、デコンボリューションされたTi 2p を示しています。 およびO 1s 合成されたTiO 2 のXPスペクトル サンプル。 3つのサンプルは、 2p に対応する457.2および463.1eVに2つの主要なピークを示しました。 3/2 および 2p 1/2 Ti 4+ TiO 2 [43]。非常に類似した結合エネルギー値がTi 2p で観察されました。 3つすべてのTiO 2 の領域 これらのサンプルのTi原子が同じ酸化状態で存在したことを示すサンプル。 455.8eVと458.7eVの2つの小さなショルダーピークもすべてのサンプルで観察されました。 455.8 eVのショルダーは、Ti 3+ に割り当てることができます。 状態、TiO 2 の酸素欠乏による [44]一方、458.7 eVのもう一方のショルダーピークは、Ti 4+ から発生します。 Ti-OH種の状態[45]。 Ti 2p から明らかです 酸素欠乏TiO 2 の寄与が示すスペクトル 種はTiO 2 でより高い -TiO 2 よりもニット -sulおよびTiO 2 -エースサンプル。すべてのサンプルはO 1s を示しました XPは、528.4、529.3、531.3eVでピークに達します。 528.4 eVでのXPSピークは、O-Ti 4+ に起因する可能性があります。 TiO 2 の種 結晶格子、529.3および531.3 eVの他の2つのピークは、表面吸着ヒドロキシル基に存在する酸素種に割り当てることができます[46]。
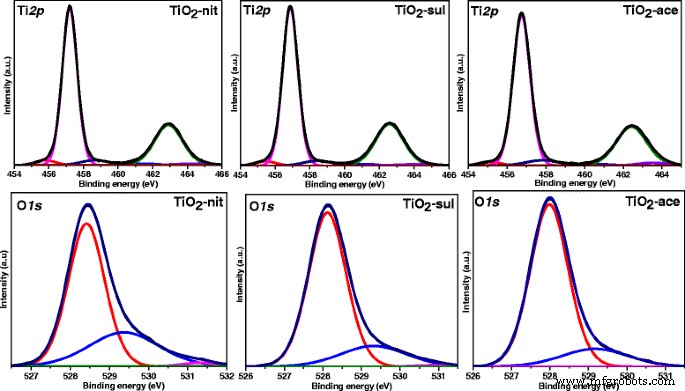
Ti 2p およびO 1s 煆焼したTiO 2 のX線光電子スペクトル サンプル
McCafferty [47]は、O 1s ピークは、高い結合エネルギー値でテールピークを持っていました。これは、Ti-OH基の存在が原因である可能性があります。物理的に吸着された表面であるため、XPS装置の操作に使用される超高真空下でTi-OH基を簡単に除去できます[48]。サンプルに示されているこれらの–OH基は、TiO 2、の表面欠陥に化学的に結合しているTi-OHによるものである必要があります。 ここで、TiO 2 の全酸素種における-OH基の割合 -nitサンプルはTiO 2 のサンプルよりわずかに高い -sulおよびTiO 2 -エース(表2)。
<図>クリスタルバイオレット、メチレンブルー、パラの光触媒分解 -ニトロフェノール染料
煆焼したTiO 2 の光触媒活性 CV、MB、および p の分解用のナノ粒子 -NPが推定されました。光触媒分解反応は、一般的にラングミュア-ヒンシェルウッドの反応速度に従うことが報告されています[1]。したがって、有機色素の光触媒分解は次のように表すことができます
$$-\ mathrm {dc} / \ mathrm {dt} =\ mathrm {kC} $$(5)統合後、式。 (4)導出可能
$$ C ={C} _0 {\ exp} ^ {\ left(-\ mathrm {kt} \ right)} $$(6)ここで C 0 は有機色素の初期濃度(ppm)であり、 k は速度定数であり、反応時間、温度、および溶液のpHに依存します。通常、触媒の光触媒効率は、稼働時間とともに増加します。
光触媒とUV照射の両方の重要性を確認するために、ブランク実験を実施しました。触媒とUV照射を単独で適用した場合、反応は進行しなかった。以前の調査結果でも同様の結果が観察されました[49]。実験セクションで通知されたように、TiO 2 光触媒を有機染料溶液で45分間平衡化して、合成されたTiO 2 への有機染料の吸着を測定しました。 サンプル。 UV- vis CV、MB、および p の吸収スペクトル -NPは、光触媒の平衡化後に記録されました。追加ファイル1:図S2、S3、およびS4は、UV- vis の変化を示しています。 CV、MB、および p の吸光度スペクトル -TiO 2 での反応時間が異なるNP溶液(10 ppm) -エース、TiO 2 -sul、およびTiO 2 -それぞれnitサンプル。 CV、MB、および p に対応する吸収ピークの強度 -NPは反応時間の増加とともに減少しました。 UV- vis 反応生成物のスペクトルは、有機色素が光反応中に分解されたことを示しています。 TiO 2 -nitサンプルはTiO 2 と比較して最も効果的な光触媒であることがわかりました -sulおよびTiO 2 -エースサンプル。 p の50%の劣化 -NPは、TiO 2 で60分以内に観察されました -nitサンプル、50% p の分解には75分と100分が必要でした -TiO 2 のNP -エースとTiO 2 -同様の条件下でサンプルをsulします。 MBおよびCV色素の分解についても、同様の光触媒活性パターンが観察されました。
調査した触媒の分解効率は、式(1)を使用して計算しました。 (4)。図8は、CV、MB、および p の変化率を示しています。 -煆焼したTiO 2 の存在下での室温でのNP水溶液 サンプル。反応のわずか10分後、TiO 2 -nitサンプルは29%のCV分解効率を示しましたが、TiO 2 -エースとTiO 2 -sulサンプルはそれぞれ17%と9%しか示しませんでした。光触媒活性は、3つのサンプルの反応時間の増加とともに急激に増加しました。ただし、120分後、TiO 2 -nitおよびTiO 2 -エースサンプルは99%の効率を示しました。ただし、TiO 2 -sulサンプルは65%の効率しか示しませんでした。
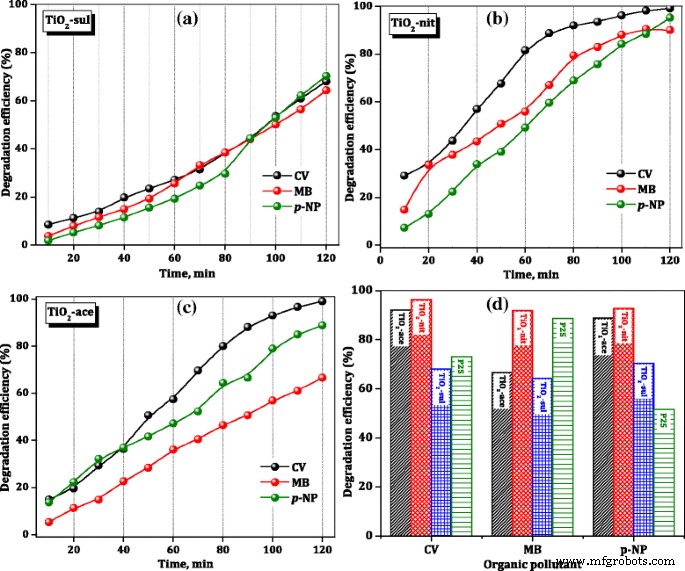
TiO 2 の光触媒分解効率 触媒
合成されたTiO 2 の光触媒性能を比較するには サンプルの場合、120分後の有機染料の市販のP25サンプルの分解効率が図8dに含まれています。 TiO 2 -nitサンプルは、3つの有機染料の分解においてP25サンプルよりも優れた性能を示しました。ただし、TiO 2 -エースとTiO 2 -sulサンプルは、 p の場合にP25触媒よりも低い活性を示しました。 -NPの劣化。これらの結果は、触媒の性能がTiO 2 の物理化学的特性に影響されることを示唆しています。 サンプルと有機染料の性質。
CV、MB、および p の光触媒分解の速度定数 -合成されたTiO 2 上のNP サンプルと市販のP25サンプルは、ln( C の間にプロットされた直線の傾きから決定されました。 0 / C t )および t 、結果を表3に示します。観察された結果は、有機染料の分解の光触媒活性がTiO 2 の組成に大きく影響されたことを示しています。 サンプルと表面ヒドロキシル基の量。実際、この活性は、TiO 2 の粒子サイズ、結晶化度、および表面積の影響を受けません。 この作品で合成。この観察結果は、藤島らによって観察された結果と一致していません。 [8]より小さな粒子サイズを有する触媒が高い光触媒効率を提供したこと。
<図>以前、アナターゼはバンドギャップエネルギーが高く、表面のOH基が多いため、ルチルよりも優れた光触媒であることが報告されていました[50]。 TiO 2 -nitサンプルは、よりルチル相(67%)が存在するため、光触媒活性が低くなります。しかし、正橋ら。 [51]は、ルチルはその優れた結晶性により、アナターゼMB分解よりも高い性能を示したと主張しました。
より多くのルチルを含むサンプルの優れた光触媒性能のより良い洞察の原因となる要因を得るために、光電流値の決定が行われました。光触媒活性は、光電流密度の影響を受ける触媒の電子正孔分離効率に直接関係することが報告されています[52]。 TiO 2 の理論的な光電流密度 サンプルは、TiO 2 の吸収端から計算されました。 サンプル(DR UV- vis から取得 分光測定)および文献[53]に示されている理論式(補足情報)。 TiO 2 の光電流の結果 サンプルは、ルチルおよび光触媒効率の値のパーセンテージとともに表4に示されています。 TiO 2 の光電流密度 -nit(0.545 mA / cm 2 )他の2つの合成されたTiO 2 よりも高い サンプルおよび市販のP25サンプル(0.401 mA / cm 2 )、TiO 2 の光活性の改善におけるルチル相の有益な役割を明らかにする サンプル。
<図>以前は、Melcher etal。 [54]は、市販のP25材料の光触媒能力は、サンプルにルチル相とアナターゼ相の混合物(75%アナターゼと25%ルチル)が存在するために発生することを報告しました。平川ほか[55]は、純粋なルチル自体は強力な光触媒ではないことを示しており、波長380 nmの光は、純粋なアナターゼで電荷キャリアを生成するほど強力ではないことも報告されています[56]。 XPS分光法の結果と理論計算に基づいて、Scanlon etal。 [57]は、電子がルチルからアナターゼに移動し、正孔がアナターゼからルチルに輸送され、電子-正孔の再結合が阻害されたと結論付けました。 Yu etal。 [58]は、TiO 2 と同様の観察結果を報告しました。 混合相のサンプルは、h + の速度を下げるのに有益でした -e − 再結合により、触媒の光触媒効率が向上します。
文献報告では、アナターゼ-ルチル複合サンプルに対して2つの可能な移動メカニズムが提案されています[59]。最初のメカニズムはアナターゼのCBからルチルのCBへの界面電子移動であり[60]、2番目のメカニズムはルチルのCBから低エネルギーアナターゼ活性部位への電子移動です[61]。アナターゼはルチルよりもバンドギャップが大きい(3.12 eV)ため、アナターゼCBはルチルCBよりも負の電位が高いことが知られています。したがって、電子がルチルCBからアナターゼCBに移動することはできません。これは、2つのバンド間のエネルギー障壁を克服する必要があるためです。アナターゼVBのバンドギャップもルチルVBよりもわずかに高いため、生成された正孔をアナターゼVBに移動して、効果的な電荷分離を実現できます。おそらく、電子正孔対は、TiO 2 の場合、ルチルとアナターゼの複合体で形成されます。 -nitおよびTiO 2 -sulサンプル(図9)。このレートはTiO 2 の方がはるかに高くなります。 -主なルチル形成によるサンプルのニット。
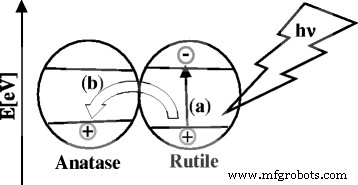
a のもっともらしいモデル 電子正孔対の生成と b 生成された正孔のアナターゼ価電子帯への移動による効果的な電荷キャリアの分離
前駆体溶液中に存在するイオンの移動度を増加させることにより、初期相の結晶成長の増加が可能であることが報告された[62]。何人かの研究者は、解離したイオンの移動度を改善するために少量の鉱酸(塩酸や硫酸など)を追加しました[63]。それらの役割は、溶液中のイオンの拡散速度を上げるだけでなく、表面電荷を変えることでもあります。湿度の高い条件下では、チタンイソプロポキシドはその後ヒドロキシル化および重合してTiO 2 になります。 。
$$ \ mathrm {Ti} {\ left(\ mathrm {OPri} \ right)} _ 4 + 4 {\ mathrm {H}} _ 2 \ mathrm {O} \ to \ mathrm {Ti} {\ left(\ mathrm { OH} \ right)} _ 4 + 4 \ \ mathrm {PriOH} \ kern2.5em \ left(\ mathrm {hydroxylation} \ right)$$(7)$$ \ mathrm {Ti} {\ left(\ mathrm {OH } \ right)} _ {4 \ kern0.5em} \ to {\ mathrm {TiO}} _ {2.} x {\ mathrm {H}} _ 2 \ mathrm {O} + \ left(2 \ hbox {- } x \ right)\ {\ mathrm {H}} _ 2 \ mathrm {O} \ kern5em \ left(\ mathrm {condensation} \ right)$$(8)解膠酸の性質に応じて、TiO 2 の変換 アナターゼまたはルチル相につながります[64]。アモルファスTiO 2 の形成 または準安定アナターゼ相は、Ti前駆体の加水分解の前に凝縮が開始したときに観察されました。高度に酸性の条件下では、凝縮の速度が遅いため、ルチル相の形成が良好です。したがって、硫酸および硝酸を解膠に使用した場合、ルチル相が得られた。解膠剤として弱酸(酢酸)を使用すると、凝縮とオリゴマー化の両方の程度を制御でき、TiO 2 の優先的な結晶化を促進します。 アナターゼ相で。 Zeng etal。 [20]は、解膠剤としてポリカルボン酸を使用し、有機酸のキレート効果に起因するアナターゼのナノ粒子の形成を観察しました。
TiO 6 八面体は、アナターゼ相とルチル相の両方の基本的な構造単位です( D 4h システム)、およびこれら2つの構造の唯一の違いは、八面体鎖のアセンブリです[65]。 TiO 6 の顔共有リンク ユニットはアナターゼ構造をもたらし、エッジ共有リンクはルチル構造をもたらします[66]。 NO 3- 陰イオンは、水溶液中のTi原子に対してCH 3 よりも弱い親和性を持っていました。 COO − およびSO 4 2- 陰イオン。 CH 3 の強い親和性 COO − およびSO 4 2- Ti原子を含む陰イオンは、相転移の抑制に関与します。
以前に報告された研究では、主に光腐食を受けるため、多くの光触媒は再利用についてテストされていません。したがって、それらの光安定性は、さらなる使用のために減少します。煆焼したTiO 2 の再利用性 これらの光触媒の有効性を研究するためにサンプルを調べた。使用した光触媒は、3つの連続したサイクルで90%の効率を提供することが観察されました。触媒の効率は、4番目と5番目のサイクルでそれぞれ80%と75%に低下しました。この減少は、ろ過および再生手順中にある程度の触媒が失われたためです。
結論
簡単な解膠法を採用して、TiO 2 を合成しました。 解膠剤として硫酸、硝酸、酢酸を使用し、Ti前駆体としてチタンイソプロポキシドを使用することによるナノ粒子。 TiO 2 の結晶相、形態、テクスチャ、および表面組成に対する酸種の影響 詳細に研究されました。 TiO 2 酢酸で解膠されたサンプルは純粋なアナターゼ相を持っていましたが、硫酸と硝酸で解膠されたサンプルの場合、ルチル相のマイナー(5%)とメジャー(67%)の形成がそれぞれ観察されました。 TiO 2 硝酸でペプチン化すると、ナノ粒子とともにシート状の構造を示しましたが、TiO 2 硫酸と酢酸で解膠されたサンプルは、ほぼ球状のナノ粒子を持っていました。合成されたTiO 2 の光触媒特性 ナノ構造は、水性CV、MB、および p の光分解について評価されました。 -NPソリューション。 TiO 2 硝酸を使用して解膠されたものは、市販のP25および他の2つの解膠されたサンプルよりも優れた光触媒活性を示し、その光分解効率は p で120分で95%に達しました。 -NPの劣化。 TiO 2 硫酸と酢酸を使用して解膠されたサンプルは、粒子サイズが小さく、バンドギャップエネルギーが高く、表面積が大きいTiO 2 硝酸で解膠されたサンプルは、ルチルおよび光電流密度の割合が高かった。観測された光電流密度は、TiO 2 の光活性によって支配されます。 。結果は、光触媒活性とTiO 2 の光電流密度との間に直接的な相関関係があることを示しています。 サンプル。 TiO 2 の優れた活性 硝酸でペプチン化されたサンプルは、ルチル相とアナターゼ相の間で光生成電子が効果的に移動するためであり、細孔径が大きいと、光化学反応中の反応分子とOHラジカルの拡散と大量輸送が促進される可能性があります。合成されたTiO 2 光触媒は、活動を少し変えるだけでリサイクルできます。
略語
- CV:
-
クリスタルバイオレット
- DR UV- vis :
-
拡散反射紫外可視分光法
- FTIR:
-
フーリエ変換赤外分光法
- HRTEM:
-
高分解能透過型電子顕微鏡
- MB:
-
メチレンブルー
- NMR:
-
核磁気共鳴
- p –NP:
-
パラ –ニトロフェノール
- TEM:
-
透過型電子顕微鏡
- TiO 2 :
-
酸化チタン
- XPS:
-
X線光電子分光法
- XRD:
-
X線粉末回折
ナノマテリアル
- SrTiO3修飾ルチルTiO2ナノファイバーのワンステップエレクトロスピニングルートとその光触媒特性
- 2種類のグラフェン修飾TiO2複合光触媒の高い光触媒性能
- 従来の抗生物質の殺菌効果を活性化するための排出ポンプおよびバイオフィルム阻害剤としてのナノ粒子
- TiO2ナノ流体に向けて—パート2:アプリケーションと課題
- 色素増感太陽電池の光学的および電気的特性に及ぼすTiO2中の金ナノ粒子分布の影響
- Li-Nb-O化合物の調製と光触媒性能に及ぼすLi / Nb比の影響
- MoO3でコーティングされたTiO2ナノチューブ光電極上のAu-プラズモンナノ粒子によって強化された光触媒活性
- 中空構造LiNb3O8光触媒の調製と光触媒性能
- 着色された低温顔料用のCrドープTiO2の構造的および可視近赤外光学特性
- TiO2ナノチューブアレイ:ソフトハードテンプレートで製造され、電界放出性能の粒子サイズ依存性
- 表面分光分析を使用した遷移金属をドープしたTiO2ナノ粒子の触媒活性の決定



