従来の抗生物質の殺菌効果を活性化するための排出ポンプおよびバイオフィルム阻害剤としてのナノ粒子
要約
抗生物質に対する細菌の耐性という普遍的な問題は、医師が感染を制御するという深刻な脅威を反映しています。細菌の進化は、抗生物質の殺菌効果を中和するためのさまざまな複雑な耐性メカニズムの開発をもたらします。たとえば、薬物の改善、標的の修飾、膜透過性の低下、排出ポンプによる薬物の押し出しなどです。排出ポンプは、幅広い基質特異性を獲得し、細菌細胞外への薬物分子の押し出しにも驚異的な効果を発揮します。排出ポンプの機能の障害は、従来の抗生物質の殺菌効果を活性化させる可能性があります。排出ポンプは、細菌細胞でのバイオフィルム形成に関与するクオラムセンシング生体分子の排除または包含においても重要な役割を果たします。細菌細胞の内側または外側のクオラムセンシング生体分子のこの通過運動は、排出ポンプの機能を妨げることによって中断される可能性があります。金属ナノ粒子は、細菌細胞の排出ポンプをブロックする潜在的な候補を表しています。排出ポンプ阻害剤としてのナノ粒子の適用は、従来の抗生物質の殺菌効果を復活させるのに役立つだけでなく、微生物のバイオフィルム形成能力を低下させるのにも役立ちます。このレビューは、排出ポンプ阻害のための従来の抗生物質との相乗効果における金属ナノ粒子の新規で魅力的なアプリケーションに焦点を当てています。
レビュー
バイオフィルムで特定された慢性感染症は、抗生物質と宿主の免疫系の両方に抵抗できるため、根絶するのは困難です[1]。バイオフィルムバリアは、急性感染症から慢性感染症への転換の主な理由の1つです[2]。国立衛生研究所および疾病管理センターの報告に示されているように、約65〜80%の疾病は、主にグラム陰性菌緑膿菌を介して、バイオフィルム誘導菌によって引き起こされます。 および Escherichia coli グラム陽性菌黄色ブドウ球菌 [3]。抗生物質は、バイオフィルムの城壁を通過し、標的となる細菌細胞を駆除する能力が限られているため、バイオフィルムを有する感染症の治療には効果がないように思われます[4]。さらに、バクテリアは、バクテリア細胞の外に有毒物質と老廃物を排出するために独自の排出システムを進化させました[5]。排出ポンプは、幅広い基質特異性と莫大な薬物排除能力を備えた膜結合型輸送体タンパク質です[6]。
バイオフィルムおよび排出ポンプに関連する懸念に関連するこれらすべての疾患は、多剤耐性(MDR)細菌または広範な薬剤耐性(EDR)細菌の出現につながります。このため、従来の抗生物質と組み合わせたナノ粒子は、バイオフィルムを根絶または損傷し、MDRまたはEDR感染症を治療するための代替アプローチとして提案されています。
これらの新しい抗菌剤である金属ナノ粒子は、既存の抗生物質の抗菌活性を高めるだけでなく、それらの殺菌活性を復活させます。抗生物質と金属ナノ粒子の相乗的適用は、それらの個々の適用よりも、それらの潜在的な抗菌効果の多くを示しました[7、8]。抗バイオフィルムまたは排出ポンプ阻害剤としての抗生物質を含むナノ粒子の利用は、十分に調査および調査されてきました[1、9、10、11]。金属ナノ粒子は、細胞毒性が低く(濃度依存性)、表面積が大きく、広域スペクトルの抗菌活性があるため、ヒト細胞株の感染症の治療に広く使用されています[12、13、14]。さらに、金属ナノ粒子と抗生物質を組み合わせて使用すると、薬物投与量としての濃度が低下するため、ヒト細胞株に対する両方の薬剤の毒性が低下します[15]。このレビューは、抗バイオフィルムおよび排出ポンプ阻害剤としての抗生物質とナノ粒子の相乗的応用を強調しており、MDRまたはEDR病原体によって引き起こされる感染症と戦うために広範な研究が行われています。
排出ポンプ阻害剤としてのナノ粒子
殺菌剤としてのナノ粒子の作用機序を決定するために、さまざまな研究が行われてきました。ただし、微生物に対するナノ粒子の抑制作用のメカニズムに関するいくつかのポイントはまだ解決されていない。ナノ粒子の殺菌活性の考えられるメカニズムの1つは、排出ポンプの阻害に起因します。 Banoee etal。 2010年に、 SのNorA排出ポンプに対する酸化亜鉛ナノ粒子の新しい排出ポンプ阻害の役割が追加されました。アウレウス 。彼らは、 Sの酸化亜鉛ナノ粒子の存在下でシプロフロキサシンの阻害ゾーンが27%および22%増加することを発見しました。アウレウス および E。コリ 、それぞれ[16]。その後、Padwal etal。 2014年に、 Mycobacterium smegmatis に対するポリアクリル酸でコーティングされた酸化鉄(マグネタイト)ナノ粒子(PAA-MNP)とリファンピシンの相乗的使用の概念を提唱しました。 PAA-MNPの流出抑制の役割に重点を置いて。彼らは MでPAA-MNPとリファンピシンの融合を使用しました。スメグマ菌 これは、リファンピシン単独とは対照的に、4倍高い成長阻害をもたらしました。これは、一般的な排出ポンプ基質である臭化エチジウムのリアルタイム輸送研究で証明されているように、細菌細胞内の抗生物質の蓄積が3倍に増加することで説明できます[17]。
金属ナノ粒子が排出ポンプの動作を妨げる可能性のあるメカニズムは2つあります。考えられるメカニズムの1つは、金属ナノ粒子が排出ポンプの活性部位に直接結合し、細胞外への抗生物質の放出をブロックすることです。ここで、金属ナノ粒子は、排出ポンプの結合部位に対する抗生物質の競合的阻害剤として作用する可能性があります[18]。別の考えられるメカニズムは、流出速度論の崩壊によるものです。 MDR排出ポンプであるMexAM-OPrMの排出動態を破壊するための銀ナノ粒子の効果は、 Pですでに調べられています。緑膿菌 [19]。金属ナノ粒子は、プロトン勾配の終了に続いて膜電位の破壊またはプロトン原動力(PMF)の喪失を引き起こし、排出ポンプ活性に不可欠な駆動力の低下をもたらす可能性があることが示唆される可能性があります[18、20、21]。ただし、ナノ粒子と排出ポンプの直接結合における主な制約は、サイズと反応性が小さいことです。さらに、ナノ粒子は、単に排出ポンプと相互作用するのではなく、他の膜タンパク質とも結合する可能性があります。そのため、曝露中に毎回、ナノ粒子が特に排出トランスポーターと結合する可能性は制限されます。
Christena etal。部分的には銅ナノ粒子からのCu(II)イオンの生成に起因して、NorA排出ポンプにおける銅ナノ粒子の流出抑制の役割に関する彼らの研究の初期に示した。銅ナノ粒子からの直接のこの部分的効果は、ナノ粒子と排出ポンプとの直接相互作用を意味する可能性があり、最初の仮説を支持します。一方、Cu(II)イオンの放出による部分的効果は、膜電位の破壊と排出ポンプの動作の乱れを示し、支持します。 2番目の仮説[9]。 Chatterjee etal。 Eの膜電位の喪失も明らかにした。コリ それぞれ3.0および7.5μg/ mlの濃度の銅ナノ粒子の存在下で細菌細胞を1時間増殖させた後、-185〜-105および-75mVの細胞[22]。ナノ粒子の流出抑制の役割の明確なメカニズムは依然として不可解であり、さらなる研究が必要です。
抗バイオフィルム剤としてのナノ粒子
バイオフィルムはバクテリアに対する耐性を提供しますが、バイオフィルムが薬剤耐性菌によって生成される場合、この反抗は強まります[23]。数多くの研究により、さまざまな作用機序を通じて厚いバイオフィルムバリアを崩壊させる金属ナノ粒子の驚異的な能力が示されています[24、25、26、27]。金属ナノ粒子の浸透力は、バイオフィルム感染に対してそれらを使用するための有用な機能であり続けます[28、29、30]。ナノ粒子と抗生物質という2つの多様なモダリティのこのユニークな融合は、バイオフィルムを生成するMDRまたはEDR細菌と戦うための新しい方法を切り開きました。
雄弁な研究の1つは、Gurunathan etalによって実施されました。銀ナノ粒子を使用したさまざまな抗生物質の殺菌効果と抗バイオフィルム効果の増強を解明する。アンピシリンと銀ナノ粒子の共生使用は、銀ナノ粒子のみで処理した後の約20%のバイオフィルム阻害とは対照的に、グラム陰性菌とグラム陽性菌のバイオフィルム阻害をそれぞれ70%と55%大幅に強化しました。同様に、銀ナノ粒子とバンコマイシンを組み合わせて使用すると、グラム陰性菌とグラム陽性菌でそれぞれ55%と75%のバイオフィルム阻害が起こります[10]。これらの結果は、抗生物質とナノ粒子を併用してバイオフィルム阻害を誘発し、新しい治療法の臨床的可能性を開くことを示唆しています。
同様の効果は、抗生物質と相乗的に使用した銅ナノ粒子と酸化亜鉛ナノ粒子でも観察されました。この研究によると、銅ナノ粒子と抗生物質の統合は、グラム陽性菌とグラム陰性菌の両方で酸化亜鉛ナノ粒子と抗生物質の組み合わせとは対照的に、より効果的な抗バイオフィルム活性を示しました。銅ナノ粒子によるこの抑制の増加は、ナノ粒子から生成されたCu(II)イオンの押し出しが原因である可能性があります。特定の抗生物質と結合した銅ナノ粒子および酸化亜鉛ナノ粒子は、2%グルコースの存在下で強化された抗バイオフィルム効果を示し、グルコースの存在下での金属ナノ粒子と抗生物質間の結合相互作用の増加を明らかにしました[9]。金属ナノ粒子を炭水化物でコーティングすると、ナノ粒子と細胞の相互作用、細胞への取り込み、細胞毒性が変化する可能性があります[31]。
排出システムとクオラムセンシングの提携
排出ポンプは、生体分子の細胞間シグナル伝達において重要な役割を果たし、バイオフィルムの形成を支援します。薬剤耐性と戦うための1つの考えられるメカニズムは、排出ポンプ阻害剤を使用してクオラムセンシングメカニズムをブロックし、最終的にバイオフィルム形成を妨げることです。クオラムセンシングにおける排出ポンプの役割を示すために、すでにいくつかの研究が行われています[23、32、33、34、35、36、37、38、39]。排出ポンプとバイオフィルム形成の間の明示的なメカニズムの関係はまだ完全に理解されていません。実行可能な正当化の1つは、クオラムセンシングに必要な重要なコンポーネントを押し出す排出ポンプの役割である可能性があります。この機能的側面は、以前の研究ですでに提案されています[40、41、42、43、44、45、46]。排出ポンプ阻害剤の適用によるシグナル伝達分子の押し出しの障害は、クオラムセンシングまたは細胞間シグナル伝達のプロセスに影響を与える可能性があります[47、48](図1)。
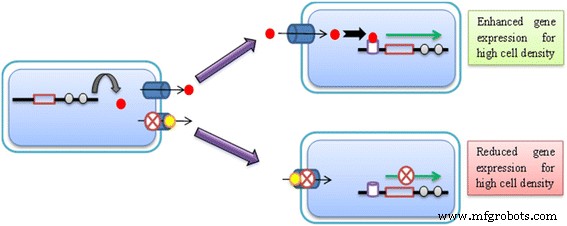
クオラムセンシングシグナル伝達分子の押し出しを妨げるための排出ポンプ阻害剤としての金属ナノ粒子の使用(赤い塗りつぶされた円 )金属ナノ粒子(黄色の塗りつぶされた円)の助けを借りて細菌細胞の外側 )排出ポンプをブロックする(充填シリンダー )シグナル伝達分子の受容体への結合が減少します(空のシリンダー )およびバイオフィルム形成の障害
別の実行可能な正当化は、細胞の外に有毒で廃棄物の副産物を輸出するための排出ポンプの役割である可能性があります。バイオフィルム内の急速に代謝される細胞は、細菌細胞内で起こるさまざまな生化学的活動から生じる有害で無駄な副産物を押し出すために、伝導系に依存している可能性があります[49]。この機能的側面は、Kvistらによって実施された研究でも提案されています。 2008年[50]。この導電性システムを遮断するために排出ポンプ阻害剤を使用すると、細菌細胞内に有毒な副産物がより多く蓄積し、最終的にバイオフィルムの形成が減少する可能性があります(図2)。
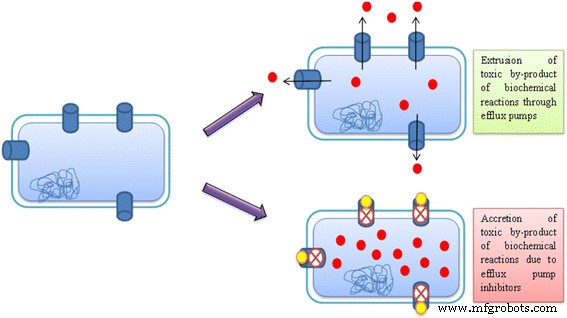
生化学反応の有毒な副産物の押し出しを妨げるための排出ポンプ阻害剤としての金属ナノ粒子の使用(赤い塗りつぶされた円 )金属ナノ粒子(黄色の塗りつぶされた円)の助けを借りて細菌細胞の外側 )排出ポンプをブロックする(充填シリンダー )バイオフィルム形成の妨げになります
いくつかの研究はまた、細胞膜の特性を変化させ、最終的にバイオフィルム形成に影響を与えることにより、細胞凝集に影響を与える排出ポンプの有害性を示唆している[47]。改善された抗菌剤および抗バイオフィルム剤としての抗生物質と組み合わせたナノ粒子の効果を推定するために、すでに多くの研究が行われている。表1には、これらの調査の要約が含まれています。
<図>最近の研究の1つは、Barapatre et al。によって行われ、グラム陽性菌およびグラム陰性菌に対するアミカシン、カナマイシン、オキシテトラサイクリン、およびストレプトマイシン抗生物質と組み合わせた銀ナノ粒子の相乗的な抗菌および抗バイオフィルム活性の増強を推定しています。グリーンケミストリーを中心に、2つのリグニン分解菌、つまり Aspergillus flavus を関与させることにより、硝酸銀を酵素的に還元することにより、銀ナノ粒子を合成しました。 および Emericella nidulans 。病原性微生物に対する抗菌および抗バイオフィルム活性を増強するために、従来の抗生物質を用いたプローブとしてナノ粒子を使用することが提案された[51]。抗生物質と金属ナノ粒子の相乗効果の潜在的なメカニズムの1つとして、排出ポンプ阻害のようなATP依存性機能の破壊が報告されています[52]。
多くの報告は、細菌耐性の2つの多様なメカニズム、すなわち、細菌が従来の抗生物質の作用を回避するMDR排出ポンプとバイオフィルム形成に対するナノ粒子の適用を成功裏に実証しています。このレビューは、抗生物質耐性と戦うために、排出ポンプ阻害剤および抗バイオフィルム剤として抗生物質と相乗的に金属ナノ粒子を採用するための新しい有望なアプローチを表しています。
結論
現在のシナリオでは、MDR感染を制御するための革新的なアプローチが求められています。排出ポンプは2つの役割を果たします。1つは抗生物質を押し出すことであり、もう1つはクオラムセンシングに重要な生体分子を排出することでバイオフィルム形成を支援し、最終的に細菌性病原体の病原性に寄与します。ナノ粒子を介したMDR排出ポンプの遮断は、両方向に役立ちます。それは、細菌細胞の外への抗生物質の流出をブロックし、したがって従来の抗生物質の効果を増加させ、また、クオラムセンシング生体分子の流出をブロックし、したがって細菌細胞のバイオフィルム形成能力を減少させる。このアプローチは、新しい排出ポンプ阻害剤または新しい抗生物質を調査するための新しい研究を実施する必要性を減らしますが、従来の抗生物質との相乗効果で金属ナノ粒子(排出ポンプ阻害剤として使用)の使用を奨励します。また、低濃度の金属ナノ粒子に耐えることができる、ヒト細胞株におけるナノ粒子のコスト、時間、および細胞毒性の問題を軽減するのにも役立ちます。これは、排出ポンプを標的とし、バイオフィルム形成を抑制するためにクオラムセンシング信号を低減するための新しいアプローチです。
将来の展望
細菌の進化は、抗生物質と宿主の免疫系の殺菌効果を元に戻すためのさまざまなメカニズムの採用をもたらしました。それは、MDRまたはXDR感染と戦うための新しいアプローチを発見する緊急の必要性を反映して、多剤耐性感染の生成につながります。抗生物質耐性の出現により、金属ナノ粒子と従来の抗生物質との共生的使用は、抗生物質耐性に対抗するためのより良い代替手段を提供します。排出ポンプ阻害剤としてのナノ粒子の適用は、2つの多様な方向で非常に重要である可能性がありますが、単一の結果、つまり細菌感染と戦うことに終わります。排出ポンプを遮断するナノ粒子の正確な作用機序は、依然として調査する必要があります。 PMFの破壊は、ナノ粒子が流出を阻害する可能性のある間接的なメカニズムである可能性があります。このアプローチの主な課題の1つは、ナノ粒子の反応性に関連しており、ナノ粒子を排出トランスポータータンパク質ではなく他の膜タンパク質と結合させる可能性があります。これは、標的化されたナノ粒子を抗排出モノクローナル抗体またはレクチンと結合させることによってそれらを調製することによって克服することができます。この適切な抑制は、特定のロケールに焦点を合わせるためにそれらを調整します。もう1つの重要な課題は、最終検証の前に最適化する必要がある小さなサイズのナノ粒子の表面積対体積比が大きいため、このアプローチを使用する場合の毒性の問題である可能性があります。
ナノマテリアル
- 癌治療のためのナノ粒子:現在の進歩と課題
- コバルトをドープしたFeMn2O4スピネルナノ粒子の調製と磁気特性
- 小さなセレンナノ結晶とナノロッドの容易な合成と光学的性質
- Sb /パリゴルスキー石(PAL)ナノ粒子の調製と強化された接触水素化活性
- ナノ粒子の跳ね返りに及ぼす弾性剛性と表面接着の影響
- 銀ナノ構造の合成方法と応用における最近の進歩
- クルクミンの処理効果を持つPEGコーティングされたCoFe2O4ナノ粒子の毒性
- アナターゼ-ルチル比とTiO2ナノ粒子の光触媒性能に及ぼす酸性解膠剤の影響
- 丸い形の金ナノ粒子:シロイヌナズナの根の成長に対する粒子サイズと濃度の影響
- 金属および金属酸化物ナノ粒子のグリーン合成と単細胞藻類Chlamydomonasreinhardtiiに対するそれらの効果
- 垂直ポンプと振動



