Fe3 +イオンの高効率検出のためのAgナノ粒子を備えた十分に整列したTiO2ナノチューブアレイ
要約
今日、新しい方法で高感度と選択性を備えた鉄イオンの測定は、健康な体と環境を監視するための緊急の問題になっています。この論文では、初めて、高性能TiO 2 のセットを紹介します。 鉄イオンに非常に敏感なナノチューブアレイ。まず、陽極酸化法を採用して、秩序だったTiO 2 を調製しました。 ナノチューブアレイ、続いて鉄イオン検知の強化能力を備えた機能化されたAgナノ粒子の堆積。その上、TiO 2 のスペクトル Agナノ粒子の有無にかかわらず、ナノチューブをX線光電子分光計で分析しました。これは、Agナノ粒子が電子と正孔の再結合率を効果的に低減し、電極の導電率と電荷移動率を向上させることができることを示しています。さらに、秩序だったTiO 2 上で機能化されたAgナノ粒子の場合 ナノチューブアレイを使用し、陽極ストリッピングボルタンメトリー法で実行される鉄イオン検知を調査して、TiO 2 の大きな可能性を検証しました。 Fe 3+ になる際の感度が約30μA/ ug / Lのナノチューブアレイ センサー。この方法は、Fe 3+ を監視するためのセンサーを開発するための新しい可能性を生み出します サンプル前処理手順なしの生物学的サンプルで。
背景
鉄は人間の健康にとって重要な栄養素であり、通常は酸素とブロック物質の移動と輸送に関与し、人体で最も重要な金属元素の中で2番目にランクされています。ただし、生細胞内の過剰な量の鉄イオンは、フェントン反応を介して活性酸素種(ROS)の生成を触媒し、腎臓病などの病気を引き起こし、細胞の恒常性を乱してアルツハイマー、ウィルソン、およびメンケス病[1、2]。実際のところ、産業や農業で広く使用されているため、汚染された川、湖、または海からの鉄が人間に及ぼす潜在的な毒性の影響は、依然として世界的な課題です[3、4]。したがって、健康な体と環境を監視して、高感度と選択性で鉄イオンを迅速に測定するために使用される実用的で効率的な技術を開発することが特に必要です。
現在、原子吸光分析、誘導結合プラズマ質量分析、誘導結合プラズマ発光分析など、金属イオンを検出する方法は数多くあります。ただし、これらの方法では複雑な装置とサンプル前処理ステップが必要であり、これも大きなコストになります。最近、グラフェン[5,6,7,8,9,10,11,12]、グラフェン量子ドット[13,14,15,16,17,18]などのナノ粒子の研究に多大な努力が払われています。 、カーボンドット[19、20、21]、および金属イオンの検出に必要な寸法の貴金属ナノ粒子またはナノクラスター。これらは、優れた選択性、高感度、および簡単な操作のために大きな注目を集めています。 Vinod Kumar Gupta etal。は、単純な縮合反応によってイミンを合成し、電気化学的および光学的方法によってそれらの金属検出能力を調査する方法を開発しました。 Fe 3+ 低濃度で比色分析(L2)によって検出されると、1.29×10 -6 に達する可能性があります。 M.しかし、この方法は、高い検出限界や強い干渉などの要因により制限されています[22]。 Xiaohui Gao etal。は、水溶液中のFe3 +イオンを検出するためのN-アセチル-L-システイン(NALC)で安定化されたAgナノ粒子(NALC–Ag NP)に基づく簡単な比色センサーを報告しました。この方法は、Fe 3+ の高感度で選択的な検出を実行するために使用できます。 80nMから80mMの線形範囲と80nMの検出限界を持つ水中のイオン[23]。 Kailasa S K etal。は、Fe 3+ を測定するための選択的かつ高感度の比色法を開発しました。 比色プローブとしてp-アミノサリチル酸ジチオカルバメート官能化金ナノ粒子(DTC-PAS-Au NP)を使用することによるイオン[24、25]。このような検出に基づいて、質量分析(MS)または発光分光法(OES)と組み合わせた誘導結合プラズマ(ICP)分析が、鉄イオン分析に採用されることが好ましい[26]。
一方、TiO 2 化学的安定性の高いナノチューブは、その優れた光電気化学、触媒、吸着特性に加えて、ガス/水分センサー[27]、水の水素への光触媒分解[28]などの非毒性により、さまざまな産業で広く使用されています。 、有機汚染物質の光触媒分解[29]、色素増感太陽電池[30]、バイオセンサー[31]、およびスーパーコンデンサー[32]。特に、よく構造化され、高度に秩序化されたTiO 2 ナノチューブは、電荷の方向性と迅速な伝達に適しています[33、34、35、36]。さらに、Ag NPの表面機能化は、TiO 2 の分析適用性を高める上で重要な役割を果たします。 高い選択性と感度で微量分析物をナノチューブで検出します。したがって、TiO 2 の組み合わせを検討します。 微量レベルでのナノチューブと金属イオンの検出が非常に望ましい。私たちの知る限り、機能化されたTiO 2 の使用に関する報告はほとんどありません。 Fe 3+ のベースプローブとしてのナノチューブ 検出。
この論文では、高性能TiO 2 のセット 鉄イオンに非常に敏感なナノチューブアレイが提示されます。まず、陽極酸化法を採用して、秩序だったTiO 2 を調製しました。 ナノチューブアレイ、続いて鉄イオン検知機能を備えた機能化されたAgNP。その上、TiO 2 のスペクトル Ag NPの有無にかかわらず、ナノチューブをX線光電子分光計で分析しました。さらに、秩序だったTiO 2 で官能化されたAgNPを使用した鉄イオンセンシング 陽極ストリッピングボルタンメトリー法によるナノチューブアレイを調査して、TiO 2 の重金属センサーの大きな可能性を検証しました。 ナノチューブアレイ。この方法は、Fe 3+ を監視するためのセンサーを開発するための新しい可能性を生み出します サンプル前処理手順なしの生物学的サンプルで。
メソッド
TiOで鉄イオンを検知する原理 2
電子はバンドギャップを克服し、TiO 2 で十分なエネルギーを吸収すると、価電子帯(VB)からコンダクタンス帯(CB)に移動します。 ナノチューブ。その結果、図1aで説明されているように、VBには占有されていない電子状態(穴)があり、これは正です。このプロセスでは、電子がVBからCBに励起されると、電子が表面に拡散して吸着質への電荷移動を可能にするか、バンドギャップの電子トラップ内にトラップされる可能性があります。ナノチューブの表面が金属ナノ粒子で覆われている場合、吸着質とTiO 2 の間で電荷移動が発生します。 電子遷移のためにナノチューブ。この移動に基づいて、図1bおよび式(1b)に示すように、電荷の量が検出されたときに金属ナノ粒子の量を知ることができます。 (1)–(3)。これらの方程式から、過剰な電荷分布が電子吸引を引き付けるポテンシャルを定義していることがわかります(O 2 )そして電子供与をはじく(H 2 O)分子からO b 金属粒子がTiO 2 に吸着されたときの空孔欠陥 水面。したがって、次の式[37]を使用して電荷移動量を測定することにより、金属ナノ粒子の濃度と種を直接検出できます。
$$ {\ mathrm {Ti}} _ {(6c)} \ \ left [{(4s)} ^ 2 {(3d)} ^ 2 \ \ mathrm {of} \ {\ mathrm {Ti}} _ {( 6c)} \ right] =4 \ times \ left [{\ mathrm {O}} _ {\ left(3 \ mathrm {C} \ right)} \ right] +2 \ times \ left [{\ mathrm {O }} _ {\ mathrm {b} \ left(2 \ mathrm {C} \ right)} \ right] $$(1)$$ \ kern1.5em \ left [{(4s)} ^ 2 {(3d) } ^ 2 \ \ mathrm {of} \ {\ mathrm {Ti}} _ {(6c)} \ right] + \ left [{\ left(1 \ mathrm {s} \ right)} ^ 1 \ \ mathrm { of} \ \ mathrm {H} \ right] =4 \ times \ left [{\ mathrm {O}} _ {\ left(3 \ mathrm {C} \ right)} \ right] +1 \ times \ left [ {\ mathrm {O}} _ {\ mathrm {b} \ left(2 \ mathrm {C} \ right)} \ right] + \ left [\ mathrm {OH} \ right] + {\ mathrm {e}} ^ {-} $$(2)$$ {\ mathrm {Ti}} _ {(5c)} \ \ left [{(4s)} ^ 2 {(3d)} ^ 2 \ \ mathrm {electrons} \ \ mathrm {of} \ {\ mathrm {Ti}} _ {(5c)} \ right] =5 \ times \ left [{\ mathrm {O}} _ {\ left(3 \ mathrm {C} \ right)} \ right] $$(3)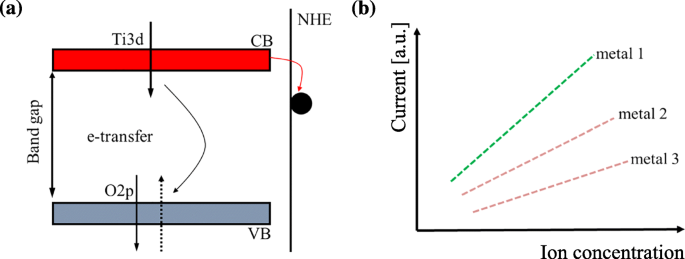
a 金属とTiO 2 間の表面電荷移動の概略図 。 b 電荷移動によって誘導される電流の大きさに基づく金属イオンの濃度と種の決定
ストリッピングボルタンメトリー法を使用して、TiO 2 の表面の金属の濃度と種を特定できます。 ナノチューブアレイ。この方法では、金属の濃度と種に対する電流の依存性を式(1)で示すことができます。 (4)[38]:
$$ \ Delta {i} _p =\ frac {nFA {D} ^ {1/2} \ mathrm {C}} {\ sqrt {\ pi {t} _m}} \ left(\ frac {1- \ sigma } {1+ \ sigma} \ right)$$(4)ここで、σ=exp [( nF / RT )( ∆E / 2)]、および N 金属との反応に関与する電子の数です。 F 、 A 、 D 、 C 、および t m ファラデー定数、電極の面積、拡散係数、金属イオンの濃度、およびパルス幅をそれぞれ表します。この式から、電流は金属濃度に比例することがわかります。
実験の詳細
純チタンシート(20×20×0.1 mm、純度99.9%)を化学研磨して酸化物層を除去し、滑らかな表面を作りました。具体的には、40%の濃度の適切な量のHF酸を比例して(0.5%)イオン水に注ぎました。次に、チタンシートを事前に準備した溶液に10秒間浸し、すぐに取り出してから窒素で乾燥させました。次に、アセトン、無水エチルアルコール、脱イオン水でそれぞれ30℃で12分間超音波洗浄しました。このプロセスでは、アセトンを主に使用して、処理の前後でそれぞれ0.139μmと0.066μmの粗さのTiシートの表面を洗浄しました。より滑らかにするために、実験の前にTiシートの前処理が必要です。実験のセットアップは、参考文献に適用されました。 [39]。島津製作所のAMICUSX線光電子分光計(XPS)を使用して、調製したTiO 2 の定量的組成を定義しました。 ナノチューブアレイ。
さまざまなサイズのAgナノ粒子(NP)がTiO 2 に堆積しました 10 -3 の真空条件下で60Wの電力を持つナノチューブ表面(QPrep400、Mantis) トル。 Agプレートの純度は99.9999%でした。
電気化学ワークステーション(CHI660E、上海陳華)を使用して、Fe 3+ の濃度を検出するためのストリッピングボルタンメトリー実験を実行しました。 イオン。 2つのループで構成される3電極システム(作用電極、参照電極、および補助電極)を使用して、作用電極の電気化学反応プロセスを監視し、化学反応の平衡を維持しました。
実験では、4種類のFe 3+ 10μg/ L、20μg/ L、30μg/ L、40μg/ L、50μg/ Lの濃度でそれぞれ塩化アンモニウムに混合しました。検出されると、中性鉄は最初にTiO 2 に吸着されました。 ナノチューブは、Ti基板との還元反応後、Ag堆積の有無にかかわらず表面化し、逆バイアスが適用されると再酸化されます。スキャンされた電圧は、0.005Vのステップで-1Vから1Vの範囲でした。検出可能な最小電流は10 -5 でした。 A、検出された期間は120秒でした。 Fe 3+ の濃度 イオンは、溶解電流ピークの電圧依存性から評価されました。
結果と考察
TiO 2 の準備と特性評価 ナノチューブアレイ
TiO 2 グリコール、2 vol%の水、0.3 wt%のフッ化アンモニウムで構成された電解質で生成されたナノチューブアレイ。酸化電圧は60 V、酸化時間は2 h、酸化温度は40°C、焼成温度は500°Cです。最適な形態と性能を持っていた[39]。 TiO 2 のトポグラフィーおよび側面走査型電子顕微鏡(SEM)画像 ナノチューブアレイをそれぞれ図2a、bに示します。図2aでは、TiO 2 ナノチューブアレイは、平均直径50nmで適切に配置されています。図2bでは、ナノチューブの長さは約19.2μmで、測定時の基板との相対傾斜角は30°です。これらの結果から、Fe 3+ との接触面積がわかります。 ナノチューブアレイのイオンは、チューブの長さが長くなるにつれて明らかに増加する可能性があり、検出感度を効果的に向上させることができます。

地形( a )および側面図( b )TiO 2 の画像 それぞれナノチューブアレイ
図3a〜dは、TiO 2 のSEM画像を示しています。 それぞれ30秒、35秒、40秒、45秒の持続時間でAgナノ粒子が堆積したナノチューブ。図3aでは、堆積時間が30秒の場合、ナノチューブの壁に吸着されたAgナノ粒子の平均直径と被覆厚はそれぞれ約10nmと5nmでした。これらの結果から、ナノ粒子のサイズ分布が均一であることがわかります。図3b、cでは、堆積時間が35秒と40秒に延長されると、Agナノ粒子の状態は徐々にクラスター状態になり、Ag粒子の直径はそれぞれ20nmと25nmに増加しました。 Agナノ粒子の直径は、TiO 2 の表面を部分的に覆うクラスターになるまでさらに大きくなりました。 堆積時間が45秒に増加したときのナノチューブ。これを図3dに示します。
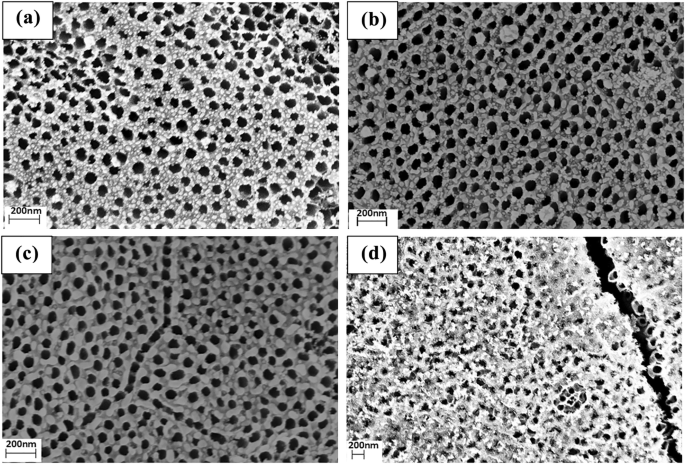
Agナノ粒子をロードしたTiO 2 のSEM画像 ( a に対応する30秒、35秒、40秒、および45秒のスパッタリング持続時間のナノチューブアレイ )-( d )、それぞれ
TiO 2 の組成を確認するため 30秒間のAg粒子吸着の有無にかかわらず、ナノチューブアレイを実行し、XPS実験を実行しました。これを図4a〜dに示します。図4aでは、結合エネルギーの値がそれぞれ368.24eVと374.25eVの場合、Agのスペクトルは3200カウントと2400カウントの強度で示され、AgのFWHM(半値全幅)が約1であることを示しています。 eV。この結果から、Ag 0 の化学状態は1つだけであることがわかります。 Agの堆積後に検出されました。
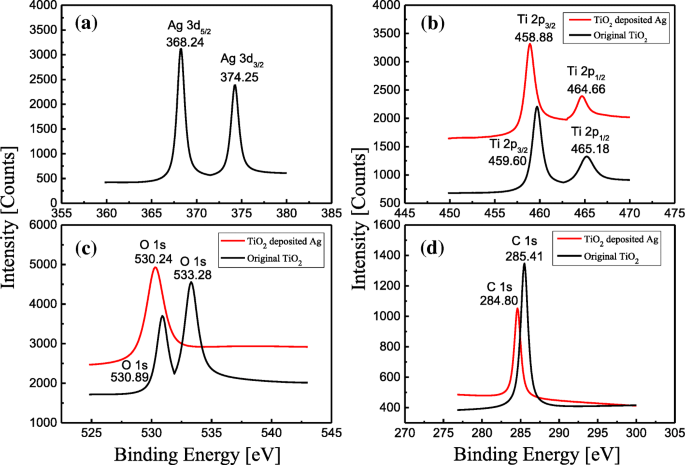
( a のAgのスペクトルの光電子分光法 );およびTiO 2 の分光法 ( b にAgが堆積している/ないナノチューブ )、( c )および( d )それぞれXPSで測定
図4bでは、Agの堆積がある場合とない場合のTiのスペクトルが示され、赤と黒の線でマークされています。 Ag堆積前の、Tiの結合エネルギーの観測値は459.60eVと465.18eVで、強度はそれぞれ2250カウントと1250カウントでした。対照的に、Tiの結合エネルギーの値は458.88eVと464.66eVであり、堆積後の強度の増加はそれぞれ3250カウントと2700カウントでした。 Ag堆積前の結合エネルギーの差は5.58eVでした。対照的に、堆積後の差は5.78 eVに変化し、約0.3eV増加しました。さらに、2つのチタンピークシフトはそれぞれ0.72eVと0.52eVでした。この現象は、AgNPの相互作用によって引き起こされました。
同様の現象が、Agの堆積がある場合とない場合の酸素と炭素のスペクトルで観察されました。これらは、それぞれ図4c、dに示されています。堆積前の酸素の結合エネルギーの値は530.89eVと533.28eVで、強度はそれぞれ3500カウントと4500カウントでした。これらの結果は、酸素が負の2価状態(格子酸素)であり、TiO 2 で構成されていることを示しています。 チタン付き。一方、酸素の結合エネルギーの値は530.24 eVであり、堆積後の強度は4900カウントでした。また、結合エネルギーの酸素ピーク値533.28 eVは堆積後に消失し、酸素ピークシフトは0.67eVでした。これらの結果は、堆積後のAg NPとの反応により、酸素の状態が格子状酸素から吸着酸素に変化したことを示しています。
図4dでは、TiO 2 の炭素汚染のスペクトルを検出しました。 それぞれ赤と黒の線でマークされたAg堆積の有無にかかわらずナノチューブアレイ。炭素汚染の結合エネルギーの値は285.41eVであり、光子数の強度は堆積前に約1350カウントでした。逆に、炭素汚染の結合エネルギーの値は284.80 eVであり、Ag堆積後の光子数の強度は約1050カウントであり、これは結合エネルギーの値と炭素の光子数が0.59 eVと30%減少したことを意味します。それぞれ。これらの結果は、AgNPの堆積後に炭素汚染の量が大幅に減少したことを示しています。言い換えれば、Ag NPの堆積は、電極の汚染を減らすだけでなく、電荷移動の効率を向上させることができます。堆積後に測定された結合エネルギーのシフトは約0.8eVであり、これは主に炭素のシフトによるものであることに注意してください。
したがって、TiO 2 Ag NPで堆積されたナノチューブアレイは、電子と正孔の再結合率を効果的に低減し、TiO 2 と比較して電極の導電率と電荷移動速度を向上させることができます。 AgNPを含まないナノチューブアレイ。
Feの検知 3+ AgNPの堆積がある/ないイオン
実験結果を得るために、電気化学的ストリッピングボルタンメトリーを使用して金属Fe 3+ を検出しました。 TiO 2 を含むイオン AgNPが堆積していないナノチューブアレイ。 Fe 3+ の濃度 イオンは10μg/ Lから50μg/ Lの範囲で設定されます。 Fe 3+ の場合の溶解電流の電圧依存性 検出されたイオンを図5に示します。測定中、印加電圧が-0.3 V未満の場合、溶解電流は一定に保たれ、約0Aのままでした。印加電圧が-0.3Vから-0.16の範囲内の場合V、電流は急速に低下し、ピークは約-1.16×10 -4 から減少しました。 Aから-1.28×10 -4 AとFe 3+ イオン濃度の増分は10μg/ Lから50μg/ Lの範囲内であり、電圧シフトはそれぞれ-0.18Vから-0.16Vの範囲内です。挿入図は、図5に示すように、電流ピークの印加電圧への依存性を示しています。印加電圧V> − 0.16 Vの場合、溶解電流は指数関数的に徐々に増加し、−0.2×10 −の範囲内にとどまりました。 4 Aから−0.4×10 −4 A.この結果から、Fe 3+ の増加に伴い電流のピークが減少していることがわかります。 イオン濃度、およびTiO 2 ナノチューブアレイはFe 3+ として使用できます 検出センサー。
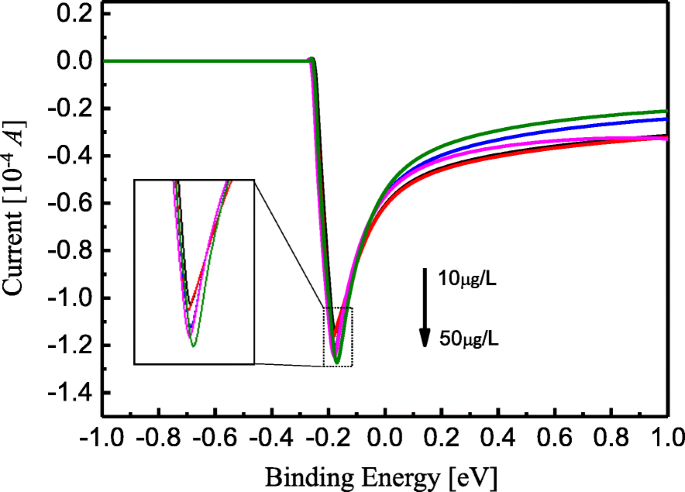
検出されたときの電圧の溶解電流依存性Fe 3+ イオン
図5の電流ピークのFe 3+ への依存性 イオン濃度(10μg/ Lから50μg/ L)も図6にまとめられています。実線はデータフィッティングであり、合理的な方法で直線性と一致しています。近似の結果は、 y で計算できます。 =0.00373 x + 1.1027、ここで y および x それぞれ電流とイオン濃度を表します。このフィッティング結果は、検出可能な最小のFe 3+ を示すのに十分です。 TiO 2 時のイオン濃度 AgNPが堆積していないナノチューブアレイが採用されているのは37.3μA/μg/ Lです。 Fe 3+ の検出限界 (δx =( dy / dx ) -1 ・(1 / dy ))TiO 2 の場合 使用するアレイは、線形範囲を考慮して15.01nMにする必要があります。ここでは、 dy / dx =37.3μA/μg/ L、およびδy =0.01μA、 M Fe =56、それぞれ。この結果は、参考文献[25]の結果に匹敵します。この論文では、消光比A700 nm / A520 nmは、Fe 3+ の濃度に対して線形です。 40mMから80mMの範囲で、Fe 3+ の高感度検出を実行できます。 Fe 3+ のオンサイトおよびリアルタイム検出のためのDTC-PASAuNPベースのUV-可視法の場合、検出限界が14.82nMのイオン 生物学的サンプルで採用されています。
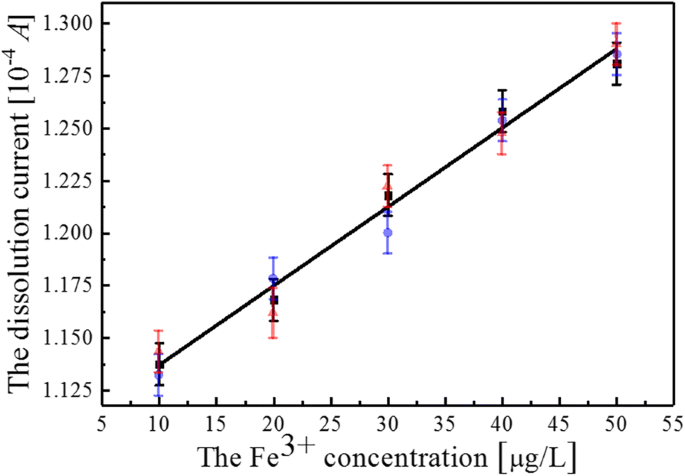
Fe 3+ の電流ピーク依存性 イオン濃度
次に、Fe 3+ の感度向上 TiO 2 の濃度検出 Ag堆積を伴うナノチューブアレイが調査され、堆積期間はそれぞれ30秒、35秒、および40秒でした。 Fe 3+ 濃度を10μg/ Lに設定し、その結果を図7に示します。印加電圧Vが-0.3 V未満の場合、溶解電流はほぼ一定に保たれ、約0Aでした。 − 0.3 Vから− 0.2 Vの範囲で、電流は約-1.35×10 -4 に急速に低下しました。 A、印加電圧が-0.2 Vを超えると、溶解電流は指数関数的に徐々に増加し、-0.08×10 -4 の範囲内にとどまりました。 Aから−0.4×10 −4 A.挿入図は、図7に示すように、電流ピークの印加電圧への依存性を示しています。図7のピークのAg NP堆積への依存性は、持続時間が0秒から40秒の範囲内にあります。図8、実線はデータフィッティングを示しています。電流が最大値(約-1.38×10 -4 )に達したことがわかります。 A)AgNPの堆積時間が30秒の場合。特に、AgがTiO 2 に堆積する前の電流値と比較して ナノチューブアレイでは、電流の値は約-1.15×10 -4 に増加しました A、これはFe 3+ の感度を意味します AgNPの堆積がTiO 2 で発生した場合、検出は20%向上しました。 水面。さらに、30秒の堆積時間における電流の最大値は、TiO 2 上のAgNPの直径と均一な分布に直接関係していると考えられました。 水面。したがって、TiO 2 ナノチューブアレイは、他のFe 3+ と比較して、比較的簡単な製造、高感度、および再現性を特徴としています。 検出方法。さらに、Agコロイド溶液の色の変化は肉眼で識別でき、Fe 3+ かどうかを直接確認するためにも使用できます。 ソリューションに存在し、この調査の強力な基盤として機能します。したがって、秩序だったTiO 2 上の官能化AgNP ナノチューブアレイは、Fe 3+ に対して低コスト、高選択性、および感度のセンシング応答を提供しました 周囲条件下での検出下限があります。特に、Fe 3+ の感度の向上 他のFe 3+ でも検出が可能です。 異なる濃度の溶液。
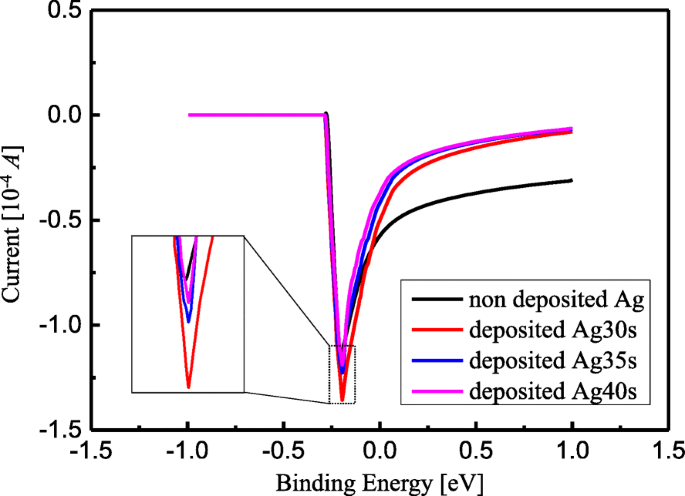
Fe 3+ の検出 AgをロードしたTiO 2 によるイオン さまざまな濃度のナノチューブアレイ
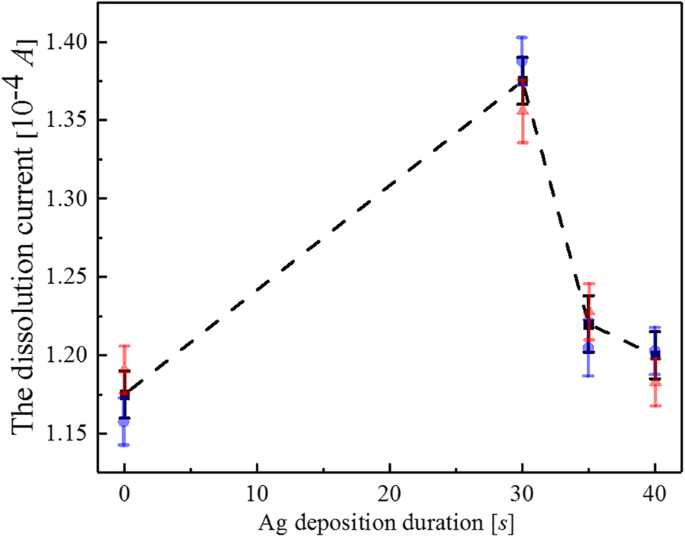
TiO 2 へのAgイオン堆積時間の関係 ナノチューブアレイとFe 3+ の検出濃度 イオン
TiO 2 の選択性を実証するために -Fe 3+ のAgNP イオン、表面プラズモン共鳴(SPR)、UV-可視分光法などを使用した場合、他の金属イオンの存在下で競合実験を実施しました。理論的には、特徴的なピークシフトは、Fe 3+ を含む金属イオンの混合溶液でのみ発生するはずです。 式に示されているイオン。 (1)–(4)。次に、競争実験に焦点を当てます。
結論
TiO 2 は、UV検出器、光触媒、色素増感太陽電池で広く使用されているだけでなく、超高感度センサーの重要な潜在的用途でも使用されている重要な機能材料です。この論文では、よく整列したTiO 2 を利用する方法を紹介します。 Fe 3+ を高効率で検出するためのボルタンメトリーセンサーとしてAgナノ粒子を使用したナノチューブアレイ イオン。当初、陽極酸化法を採用して、秩序だったTiO 2 を調製しました。 ナノチューブアレイ、続いて鉄イオン検知機能を備えた機能化されたAgNP。次に、TiO 2 のスペクトル Ag NPの有無にかかわらずナノチューブをXPSで比較したところ、TiO 2 の格子酸素が証明されました。 Ag NPの相互作用により、ナノチューブアレイは吸着酸素に放出されました。したがって、ナノチューブアレイ上の官能化Ag NPを使用した場合、陽極ストリッピングボルタンメトリー法で実行される鉄イオンセンシングを調査して、重金属センサーになる可能性を検証しました。これにより、秩序だったTiO 2上の官能化AgNPが証明されました。 ナノチューブアレイは、Fe 3+ に対して低コスト、高選択性、および感度のセンシング応答を提供しました 周囲条件下での検出下限があります。この方法は、Fe 3+ を監視するためのセンサーを開発するための新しい可能性を生み出します サンプル前処理手順なしの生物学的サンプルで。
略語
- CB:
-
コンダクタンスバンド
- FWHM:
-
最大値の半分で全波
- NALC:
-
N-アセチル-L-システイン
- NP:
-
ナノ粒子
- ROS:
-
活性酸素種
- SEM:
-
走査型電子顕微鏡
- Ti:
-
チタン
- VB:
-
価電子帯
- XPS:
-
X線光電子分光計
ナノマテリアル
- 効率的な光触媒水素生成のためのS、N共ドープグラフェン量子ドット/ TiO2複合材料
- 化学センシング用の貴金属ナノ粒子で装飾されたエレクトロスピニングポリマーナノファイバー
- グリセロールの電気透析脱塩のための無機イオン交換体のナノ粒子を含む複合膜
- 非常に効果的な標的膵臓腫瘍治療のための、血液循環が延長され、生体適合性が改善されたレスベラトロール負荷アルブミンナノ粒子
- MoO3でコーティングされたTiO2ナノチューブ光電極上のAu-プラズモンナノ粒子によって強化された光触媒活性
- ポリ(4-スチレンスルホン酸-co-マレイン酸)による金磁性ナノ粒子の安定性の向上:タンパク質検出用に調整された光学特性
- 単分散二元FePt-Fe3O4ナノ粒子の合成のための後処理法
- 非常に効率的な光触媒水素発生のためのZnO @ TiO2中空球の階層的ヘテロ構造
- 陽極酸化チタンナノチューブアレイにCeO2ナノ粒子をロードするための簡単な方法
- 可視反射率の低いSiナノワイヤアレイ上にCu2Oナノ粒子を均一に装飾して作られた効率的な光触媒
- リチウムイオン電池アノード用の赤色リンナノ粒子の容易な溶液合成



