AlドープBiFeO3粉末の局所構造のシンクロトロンX線吸収分光法による研究
要約
AlをドープしたBiFeO 3 、つまり、BFA x x のO粉末サンプル =0、0.025、0.05、および0.1は、熱水ルートを介して準備されました。 BFA x の構造的、電気的、および光学的特性に対するAl置換の影響 Oサンプルを調査した。 BiFeO 3 のBサイトでのAlイオンの置換が見出された 構造変化を引き起こさず、 R3c で菱面体晶ペロブスカイト構造を保持しています。 X線回折(XRD)とラマン測定によって確認された対称性。 Fe K の上のX線吸収微細構造(XAFS) -エッジとBi L 3 -BFAのエッジ x O粉末も測定および分析されました。 Feイオンは混合原子価状態を示します(Fe 2+ / Fe 3+ )一方、Biイオンはすべてのサンプルで+3の原子価状態を維持します。 Fe K -エッジXAFSは、Fe 3 d の混成間に競合があったことも示しました。 およびAl3 d O 2 p を使用 軌道とより多くの4 p の発生 Alドーピングの軌道。 Bi L 3 -エッジXAFSは、2 p からの遷移を明らかにしました 3/2 6 d 状態が増加したので、6 d のエネルギーも増加しました 州。さらに、Alイオンドーピングは、Fe原子の最近傍および最近傍の配位シェルとBi原子の最近傍シェルの両方に影響を及ぼしました。紫外可視(UV-Vis)分光法の結果は、BFA x を示しています 水熱法で調製されたOは、適切な可視光光触媒材料である可能性があります。
背景
マルチフェロイクスは、強誘電性、強磁性、強弾性などのフェロイック特性を同時に示す材料です[1]。このような材料は、電気分極などの興味深い挙動を示します。これは、外部電界を印加することで制御でき、その逆も可能です。これらの材料への関心は、化学バイオセンサー、ナノ電子および高密度データストレージデバイスなどでの幅広い用途によるものです[2、3]。ペロブスカイト構造の一般式はABO 3 ここで、Oはイオン(通常は酸素を指します)、AとBはそれぞれ陽イオンです。一般に、Aサイトカチオンは原子価状態が低くなるほど大きくなり、O 2- と結合します。 最密層を形成します(つまり、ユニットセルの隅に)。 Bサイトカチオンは、原子価状態が高いほど小さく、酸素八面体配位環境(つまり、酸素アニオンの八面体の中心)に採用できます[4]。定義上、ほとんどすべてのマルチフェロイックは、転移温度が低い反強磁性(AFM)または弱い強磁性(FM)です。それらは、単相と複合の2つのクラスに分けられます。ただし、単相マルチフェロイック材料は、強誘電性(FE)とFMの特性を同時に示す自然界ではめったに見つかりません[5]。今日知られているすべてのマルチフェロイック材料の中で、ビスマスフェライト(BiFeO 3 ; BFO)は、極空間群 R3c を持つ菱面体晶歪んだペロブスカイト格子型を持つ単相材料の1つです。 。 BFOは、キュリー温度が T の両方のFEを示しています。 C ≈1103kおよびネール温度 T のGタイプAFM注文 N 室温(RT)より約643k高い[6]。この材料は、[111] c に沿ってAFMGタイプのスピン構成を示します。 または[001] h その疑似立方または菱面体構造の方向であり、[110] h に沿って約62Åの周期性を持つ重ねられたスパイラルスピン構造を持っています RTでの軸[7]。それは約90μC/ cm 2 の大きな固有の自発分極を持っています 八面体FeO 6 の歪みによるもの 、6つの s が存在するため 2 孤立電子対[8]。さらに、FEと磁気秩序パラメータの間には磁気電気結合があります。 FE特性は孤立電子対に依存し、FM特性は部分的に満たされた内殻に依存します。つまり、分極はBiサイト(Aサイト)から発生し、磁化はFeサイト(Bサイト)から発生します。
上記とは別に、残念ながら、BFOの主な欠点は、ビスマスや酸素の空孔、不純物相、鉄の原子価変動、界面品質の悪さなどの電荷欠陥による、抵抗率の低さやリーク電流の大きさです[9]。また、Bi 2 のような不純物相があるため、高品質のBFOを得るのは困難です。 Fe 4 O 9 (空間群 Pbam )およびBi 25 FeO 39 (空間群 I23 )。調製過程で不純物が発生することは避けられません。これらの問題と制限に対処するために、いくつかの研究グループは、BFOの欠陥を克服するためにさまざまな方法を使用しています。たとえば、ひずみの修正、二価および希土類イオンのドーピングの置換などです。現在、この研究分野では、AサイトまたはBサイトでの希土類元素または遷移金属イオンのドーピング、またはAサイトとBサイトでの同時ドーピングにより、BFOのマルチフェロイック特性を向上させることができます。たとえば、希土類元素をドープすると、ペロブスカイト構造が安定し、非中心対称性が維持され、Bi 3+ の気化が制御されます。 イオン[10]。遷移金属イオンをドープすると、Fe 3+ の原子価変動を減らすことができます。 イオン。 Aサイト置換の場合はPr、Sm、Eu、Gd、La [11、12]、Bサイト置換の場合はMn、Cr、Ti [13,14,15]などの元素がすでに報告されています。さらに、磁気、誘電、および強誘電特性は、同時ドーピングによって強化することができます。 BFOのAサイトとBサイトの同時ドーピングについては、La-Gd、Ba-Ni、Dy-Cr、Y-Mn、およびTb-Tiが報告されています[16、17、18、19、20]。これまで、ゾルゲル[21]、メカノケミカル[22]、自動燃焼[23]、パルスレーザー堆積[24] 、などのさまざまなルートがあります。 および熱水[25、26]がBFOを調製することが報告されています。水熱法は、その省エネ、微細分散、低コスト、および小さな粒子サイズの特性のために広く適用されてきました[27]。反応温度は、BFOを形成するのに十分な高さである必要があり、サンプル準備中に二次相を除去するためにも使用されます。 BFOのAサイトとBサイトの両方にドープされたAlのこれまでのほとんどの研究は、Azam et al [28]によって構造的、光学的、および輸送特性について調査されています。 Madhu etal。 [29]は、BサイトAlドープBFOの光触媒アプリケーションを報告しています。 Jawadらからの別の報告。 [30]は、ナノ構造のBFOセラミックの誘電挙動を調査しました。王らの仕事。 [31]はAlドープBFOの中空結晶を詳細に研究しました。ただし、材料の局所的な電子構造に対するBサイトのドーピング効果など、いくつかの重要な物理的特性はまだ理解されていません。現段階では、X線吸収微細構造分光法(XAFS)は、原子の局所環境を研究する強力な方法の1つであり、吸収エネルギー、元素の原子価状態、電荷移動などの材料の構造情報を提供します。および結合のタイプ[32]。私たちの知る限り、XAFSによるBFO調査の局所的な電子構造に対するBサイトでのAlドーピングの影響に関する報告は見つかりませんでした。
この作業では、ドープされていないBFOとターゲット組成BiFe 1- x Al x O 3 (BFA x O) x を使用 =0、0.025、0.05、および0.1は、熱水ルートを介して合成されました。主な焦点は、ドープされていないBFOと比較されるBFOの特性に対するBサイトでのAlドーピングの影響の調査にあります。構造特性を詳細に調査しました。
メソッド
水熱法を使用して、ドープされていないBFOおよびBFA x を取得しました。 Oサンプル。この作業で使用した化学試薬は硝酸ビスマス(Bi(NO 3 ) 3 ・5H 2 O)、硝酸鉄(Fe(NO 3 ) 3 ・9H 2 O)、硝酸アルミニウム(Al(NO 3 ) 3 ・6H 2 O)、および水酸化カリウム(KOH)。すべての化学試薬は、さらに精製することなく、受け取ったままの状態で使用しました。 Bi(NO 3 ) 3 ・5H 2 OとFe(NO 3 ) 3 ・9H 2 Oを原料とし、Al(NO 3 ) 3 ・6H 2 OとKOHを添加剤として使用しました。すべての水溶液を作るために脱イオン水が使用されました。 BFO粉末を調製するための一般的な実行は、次のとおりです。各20 mLのBi(NO 3 ) 3 ・5H 2 O、Fe(NO 3 ) 3 ・9H 2 O、およびAl(NO 3 ) 3 ・6H 2 Oを80mLのステンレス鋼オートクレーブに入れ、よく混合しました。その後、適量のKOH溶液を前の混合溶液にゆっくりと滴下し、その体積の65〜80%が満たされるようにしました。次に、強磁気攪拌装置に移して、80°Cで2〜3時間攪拌しました。明確な解決策を得る。方法の手順に従って、得られた暗褐色の溶液をテフロンで裏打ちされたステンレス鋼のオートクレーブに移した。水熱処理は、200℃の温度で10時間、自生圧力下で実施されました。加熱速度は2℃/分でした。水熱反応が完了した後、得られた生成物を自然に室温に冷却した。続いて、得られた粉末を収集し、溶液のpH値が7に達するまでアセトン、脱イオン水、およびエタノールで数回洗浄した。最後に、BFA x O粉末をサーモスタット乾燥オーブンに70°Cで6時間入れ、さらに特性評価のために乾燥させました。 BFA x のサンプルを4セット用意しました Al(NO 3 ) 3 ・6H 2 O 0–0.1Mから。
BFA x の結晶構造 OサンプルはX線回折(XRD、Mac Science M18XHF22-SRA)によって決定されました。 Ar +レーザーからの放射線を用いたラマン分光法(Renishaw InVia Reflex)を使用して、RTでの粉末の構造特性を決定しました。 XAFSデータは、中国の北京シンクロトロン放射光施設(BSRF)のビームライン1W2Bで、さまざまな濃度の透過モードで収集されました。 Fe K -エネルギー分解能がΔ E のエッジスペクトル / E :2×10 −4 およびBi L 3 -エネルギー分解能がΔ E のエッジスペクトル / E :1×10 −4 BFA x について測定されました RTでのOサンプル。最良のXAFSデータを取得するために、BFA x O粉末を瑪瑙乳鉢で粉砕し、次にBNと混合し、最後にプレスしてペレットにしました。吸収スペクトルのバックグラウンド補正、正規化、およびエッジ前とエッジ後の領域は、IFEFFITプログラム内のXAFSデータ処理用ソフトウェアであるATHENAによって適合されました[33]。 E o 値は、エッジ領域の一次導関数の最大値によって決定されました。 χを抽出しました ( k ) k のプロファイル 0–12Å -1 のスペース 。 k 3 ×χ ( k )プロファイルは R にフーリエ変換されました ハニングウィンドウ関数を使用して、0〜8Åのスペース。 Fe 2 O 3 およびBi 2 O 3 参照化合物として測定されました。粉末の光学特性は、紫外可視分光光度計(UV-Vis、UV 3900H)を使用して評価しました。この作業では、調査は0≤ x の低ドーピング濃度に限定されます。 ≤0.1。
結果と考察
ドープされていないBFOのXRDパターン( x =0)およびBFA x 2 θからスキャンしたO粉末 15〜60°の値を図1に示します。図1aのXRDパターンの完全なスペクトルは、すべてのサンプルが、対応する菱面体晶の歪んだペロブスカイト構造の標準回折データとして識別できることを示しています(JCPDSカードファイルNo. 20 -0169、空間群: R3c )。また、すべてのサンプルが少量の二次相を伴うきちんとした回折パターンを示していることもわかります。二次相の痕跡は27.6°と32.8°で見ることができます(Bi 2 の場合は「*」とマークされています) Fe 4 O 9 Bi 25 の場合は「#」 FeO 40 ) x の場合 =0.5および x =0.1サンプル。これは高い焼結温度でのBiの揮発性に起因する可能性があります[34]。これは、さまざまな経路で合成されたBFO粉末でよく見られます[35、36、37]。二次相は、高いドーピング値で連続的に増加することがわかります。したがって、FeのBサイトAl置換は、BFOの純粋な相を促進することはできません。ただし、サンプルの電気的特性は影響を受けません。図1aから、ドープされたサンプルのすべての回折ピークが最初に高い2 θにシフトすることがわかります。 Alドーピングによる値。わかりやすくするために、2 θのXRDパターンの一部 21〜24°の領域が図1bで増幅されています。回折ピークのこの拡大図から、(101)回折ピークが高い2 θに向かって明らかにシフトしていることが観察できます。 ドープされていないBFOに関する値。これは、AlがBFOのBサイトに正常にドープされていることを確認します。ドープされていないBFOと同様に、ドープされたサンプルの(101)回折ピークは、より高い2 θにシフトします。 最初に値、次に下の2 θの小さなシフト x の場合の値 図1cに示すように、=0.1(破線で囲まれています)。図1dに、37〜40°、50〜52°、55〜57°の付近の拡大XRDパターンを示します。 XRDスペクトルには、いくつかのツインピーク、つまり(003)と(021)、(113)と(211)、(104)と(122)があります。 Al含有量の増加に伴い、これらのピークの強度は最初に増加し、次に x のときに減少します。 0.1に達します。ご存知のように、ピークの強度は通常、結晶化度に関連しています。回折ピークの減少は、BFA x の結晶化度を示しています。 Oが減少します。 Al 3+ 以降 (0.51Å)のイオン半径はFe 3+ よりも小さい (0.65Å)、ドーピング量が少ないとBFO格子に容易に取り込まれますが、ドーピングイオンが多すぎるとBFO格子が不安定になります。結晶化度の低下は、Alがより多くの核形成サイトの作成を促進し、それが結晶粒の成長を阻害するという事実に起因する可能性があります。結晶化度の低下は、他のAlドープBFOでも見られます[28、30]。一方、これは、酸素空孔の生成と一部のFe 3+ の変換がある場合に発生する可能性があります。 Fe 2+ へ Al 3+ によってシステム内に作成された電荷の不均衡による 代用。 SrをドープしたBFOでも同様の現象が観察されています[38]。回折ピークのシフトは、Fe 3+ と比較してAlのイオン半径が小さいため、ユニットセルの収縮に起因する可能性があります。 。 XRDの結果は、3価のAl 3+ BFOでの置換は、観察可能な構造変化にはつながりません。
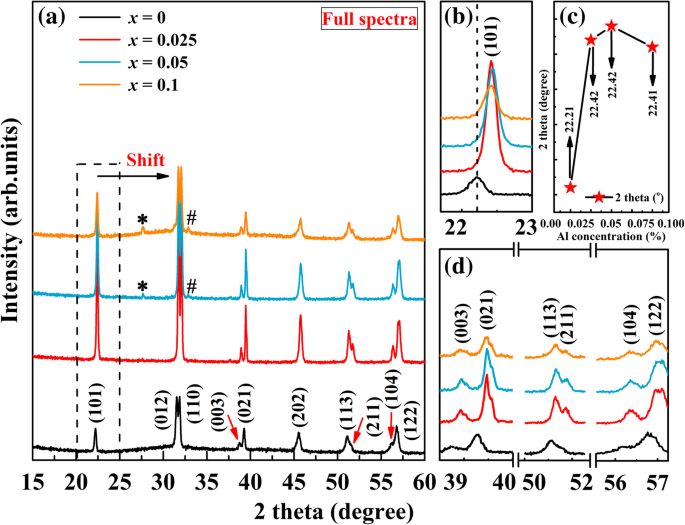
a BFA x のXRDパターン O(0≤ x ≤0.1)。 b 21〜24°の範囲のXRDパターンの拡大図。 c Al濃度の関数としての(101)ピーク位置。 d 37〜40°、50〜52°、55〜57°付近の拡大XRDパターン
XRDによって確認された構造は、ラマンアクティブモードの位置と強度によっても特徴付けることができます。ラマンスペクトルは、原子の変位と分布に敏感です。ドープされていないBFOおよびBFA x のラマン散乱スペクトル O粉末を図2に示します。群論に基づいて、13個の光フォノンラマンアクティブモードと5個の非アクティブモード(つまり、5 A 2 )のBFOは、空間群 R3c の菱面体歪みペロブスカイトに対して予測されます。 [39]。ペロブスカイト R3c の格子振動の理論的解析 構造は次のとおりです。
$$ {\ varGamma} _ {R3c} =4 {A} _1 \ left(z、\ kern0.5em {x} ^ 2、{y} ^ 2、\ kern0.5em {z} ^ 2 \ right)+ 5 {A} _2 \ left(-\ right)+ 9E \ left(x、\ kern0.5em y、\ kern0.5em {x} ^ 2- {y} ^ 2、\ kern0.5em xy、\ kern0。 5em xz、\ kern0.5em y \ right)$$(1)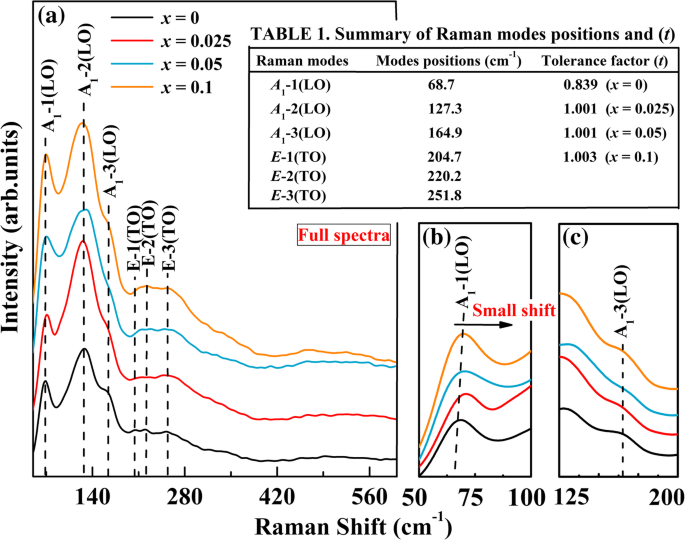
a BFA x のラマンスペクトル O(0≤ x ≤0.1)。 b 50〜100 cm -1 の範囲の拡大ラマンスペクトル および c 125–200 cm -1
ここで A 縦光学(LO)モードで E 横光学モード(TO)です。図2aに示されている完全なスペクトルでは、RTで明確に見られるラマンアクティブモードの数は、予測よりもはるかに少なくなっています。この作業では、6つのラマンアクティブモード(3 A )を観察しました。 1 (LO)+ 3 E (TO))BFA x の場合 Oパウダー。これは、スペクトル内のバンド間の偶発的な縮退と、弱いバンドをバックグラウンドノイズから区別できないこと[40]、またはサンプルの誘電体漏れが原因である可能性があります。ドープされていないBFOの場合、68.7 cm -1 に強くて広いピークがあります。 、127.3 cm -1 、および164.9 cm -1 A に割り当てられました 1 -1(LO)、 A 1 -2(LO)、および A 1 それぞれ-3(LO)モード。 204.7 cm -1 のピーク 、220.2 cm -1 、および251.8 cm -1 E に割り当てられました -1(TO)、 E -2(TO)、および E -3(TO)モード、それぞれ(図2の表1を参照)。スペクトルから、これらの E (TO)モードは表示されません。 A 1 -1(LO)モードは、Bi-O結合に起因しますが、傾斜 A 1 -3(LO)モードはFeO 6 と見なされます 八面体。 E (TO)モードはFe-O振動に割り当てられます[41]。ラマン結果は、準備されたドープされていないBFOが、空間群 R3c を持つ菱面体晶歪んだペロブスカイト構造に属していることを確認します。 。 4つのサンプルすべてが同様のラマンパターンと振動モードを示していることに注意してください。これは、同じ菱面体晶 R3c を示しています 空間群ですが、それらの強度と周波数は多少異なります。 BFA x のラマンパターンの全体像 Oサンプル、 A のピーク位置 1 -1(LO)モードはわずかに高い周波数にシフトし、 A のピーク 1 -3(LO)モードが広がり、ドーパントAlがBFOのBサイトに移動していることを示しています。 E の強度 -1(TO)、 E -2(TO)、および E -3(TO)モードは、ドープされたサンプルでわずかに増加することがわかります。わかりやすくするために、 A 1 -1(LO)および A 1 -50〜100 cm -1 の領域の-3(LO)モード および125〜200 cm -1 図2bおよびcに示します。この拡大されたスペクトルから、 A 1 -1(LO)モードは、Al含有量の増加に伴い、より高い周波数への小さなシフトを示します。ドープされていないBFOのピークと比較すると、 A のピーク 1 -3(LO)モードは、ドープされたサンプルに対して拡張されました。 A の小さなシフト 1 -1(LO)モード、 A のわずかな広がり 1 -3(LO)モード、およびいくつかの E の強度の変化 (TO)モードは、Bi-OおよびFe-O共有結合の変化とAlドープサンプルの圧縮応力に関連している可能性があります[42、36]。一方、上記のすべての変更は、BサイトのFe 3+ が原因である可能性があります。 イオンは部分的にAl 3+ に置換されています イオン。明らかに、これらのラマンの結果はXRDの観察結果と一致しています。ゴールドシュミット許容係数( t )は、結晶構造の幾何学的安定性と歪みを評価するために広く使用されています[43]。ここで、 t は、次のように3種類のイオン半径の比率で定義されます。
$$ t =\ frac {\ left({r} _ {\ mathrm {A}} + {r} _ {\ mathrm {O}} \ right)} {\ sqrt {2} \ \ left({r} _ {\ mathrm {B}} + {r} _ {\ mathrm {O}} \ right)} $$(2)ここで r A はBi 3+ の半径です 、 r B はFe 3+ の平均半径です およびAl、および r O はO 2- の半径です 。ただし、AlとFeの半径 3+ は0.51Åと0.65Åですが、Bi 3+ およびO 2- 半径はそれぞれ1.03Å(参考文献[44]による)と1.38Åです。 t 調査したペロブスカイト複合材料の値BFA x x のOは、0.839、1.001、1.001、および1.003であることがわかります。 =0、0.025、0.05、および0.1、それぞれ(図2の表1を参照)。理想的なABO 3 t の値が大きい場合、化合物は立方最密構造を採用します。 は1ですが、 t の場合 <1または> 1、幾何学的ひずみが発生します[45、46]。 Al濃度が増加すると、平均Bサイトイオン半径が減少し、 t がさらに増加します。 0.839から1.003までの値。これは、BFOの低対称状態の小さな変化が原因である可能性があります。ペロブスカイトのBサイトカチオンは6つの酸素アニオンに囲まれていることはよく知られており、より小さなイオンに置き換えると、配位距離が短くなります。したがって、Al置換の効果を明確に分析するには、BFA x の局所的な電子構造を研究する必要があります。 Oサンプル。
XAFSは、X線吸収端構造(XANES)と拡張X線吸収微細構造(EXAFS)の2つのタイプに分けられます。この測定では、X線が距離 x でスラブを透過するとき 、X線ビームの強度は I に減少します =私 o e - μ x 。 XAFSは、X線エネルギーの関数としてX線の吸収を測定します E 、つまり、X線吸収係数μ( E )=− d ln I / dx X線ビーム強度の減衰から決定されます I 距離 x [47]。 I の比率 / 私 o E の関数としてプロットされます しきい値を超えるFe K -エッジ(7112 eV)およびBi L 3 (13,419 eV)、μ( E の形状に関する重要な情報を提供できます )。電子遷移は、双極子選択規則に従うものとします。 X線吸収μ(ω )は、次のようにフェルミの黄金律によって取得できます。
$$ \ upmu \ left(\ omega \ right)\ propto \ sum \ Limits_f {\ left | \ left \ langle f \ left | D \ right | \ left.i \ right \ rangle \ right。\ right |} ^ 2 \ \ delta \ left \ langle {E} _i- {E} _f + \ omega \ right \ rangle $$(3)ここで| i ⟩は初期状態です| f ⟩は最終状態、 D は双極子演算子、 E i | i のエネルギーです ⟩、 E f | f のエネルギーです ⟩、およびω は光子周波数です。 XANES機能には、吸収体の電子構造と原子構造の局所環境に関連する有用な情報が含まれています。 XANES関数χ ( E )は次のように定義されます:
$$ \ chi(E)=\ kern0.5em \ left [\ frac {\ mu(E)-{\ mu} _ {\ mathrm {o}}(E)} {\ varDelta {\ upmu} _ {\ mathrm {o}}} \ right] $$(4)ここで、μ o ( E )は滑らかな原子のような背景であり、Δμ o は、総原子バックグラウンド吸収エッジの正味の増加から生じる正規化係数です。標準式。 (4)は、XANESデータの処理中のバックグラウンドの減算と除去に使用されました。まず、滑らかな前縁関数を差し引いて、機器から背景を取り除きます。次に、μ( E )が正規化され、滑らかなポストエッジバックグラウンド関数がμ( E )μ o を取得する ( E )。図3aは、Fe K の完全なスペクトルを示しています。 -ドープされていないBFOおよびBFAのエッジXANES x O粉末と参照化合物Fe 2 O 3 図3bは、7100〜7180eVのエネルギー範囲でのXANESスペクトルを報告しています。図3bから、すべてのスペクトルの形状とピーク位置が互いに類似していることがわかります。吸収端は、Al濃度の増加に伴い、より低いエネルギーに向かってわずかにシフトします。これは、化学シフト効果に起因する可能性があります。吸収端のエネルギーは、電荷状態が減少するにつれてより低いエネルギーにシフトし、Bサイトでの複雑な結合構成を示唆しています。エッジシフトを使用して平均酸化状態を取得できることはよく知られています。調査したサンプルの吸収端エネルギーBFA x x の場合、Oは7124.95 eV、7123.87 eV、7123.84 eV、および7123.80eVであることがわかります。 =0、0.025、0.05、0.1。参照化合物Fe 2 の場合 O 3 、吸収端エネルギーは7126.14 eVです(図3の表2を参照)。ドープされたサンプルの吸収端は、Fe 2 の吸収端よりも低くなっています。 O 3 (Fe 3+ )参照化合物。 x を増やす 値は、吸収端がFeO(Fe 2+ )の吸収端に向かって徐々にシフトすることにつながります。 )[48]。このことから、BFA x Oは混合原子価(Fe 3+ / Fe 2+ ) システム。別の態様では、3つの主要な特徴、エッジ前のピークA1およびエッジ後のピークA2およびA3が、4つのサンプルすべてで観察される。 BFOに典型的なプレエッジピークA1は、O 1 s からの電気四重極禁制遷移に対応します。 Fe 3 d へのレベル Al 3 d の少量の混合物を含むもの 州。 Al濃度が増加すると、エッジ前のピークA1の強度は、ドープされたサンプルでわずかに増加します(図3cを参照)。エッジ後のピークA2は、O 2 p に起因します。 Fe 3 d へのバンド転送 軌道、いわゆる配位子から金属への電荷移動プロセス[49]であるのに対し、ピークA3は1 s によって引き起こされます。 〜4 p 双極子許容遷移[50]。 Al濃度の増加に伴い、これら2つのエッジ後のピークの強度は、ドープされたサンプルで増加することがはっきりとわかります(図3dを参照)。エッジ前とエッジ後のピーク強度の上記のすべての変化は、Fe 3 d の混成間の競合の観点から理解できます。 およびAl3 d O 2 p を使用 軌道。その上、Alイオンドーピング後、より多くの空いている4 p BFA x で発生する軌道 O.これらを除いて、スペクトル全体に大きな変化は見られず、これらの結果は、AlイオンがBFA x のBサイトに部分的にドープされていることを証明しています。 O。
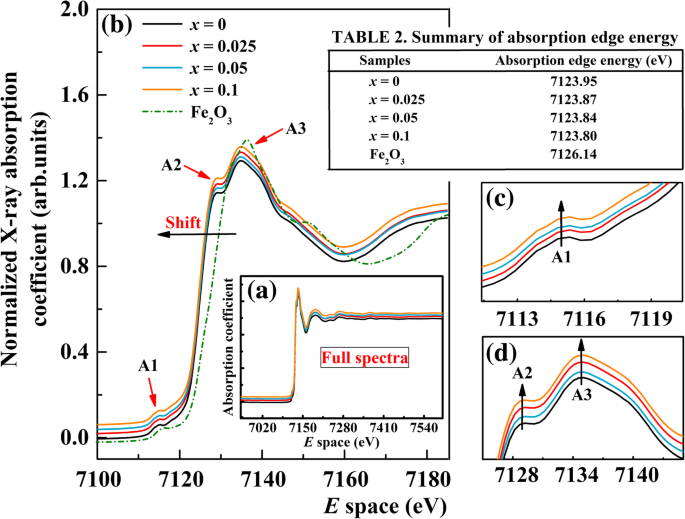
a Fe K -BFA x のエッジXANESスペクトル O(0≤ x ≤0.1)および参照Fe 2 O 3 。 b 7100〜7180eVの範囲のXANESスペクトル。 c ピークAの拡大図。 d ピークBとピークC
k をフィッティングすることにより、Fe-O、Fe-Fe / Al(つまり、Fe-O-Fe / Al)、およびBi-O結合の分布が得られます。 3 -加重( k 3 ×χ ( k ))次のような生データ:
$$ k =\ sqrt {\ frac {2m \ left(E- {E} _ {\ mathrm {o}} \ right)} {\ mathrm {\ hbar}}} $$(5)ここで E o は吸収端エネルギーであり、ħ プランク定数です。次のように、標準のEXAFS方程式を使用して、さらにフィッティング(いくつかの近似と振動)が行われます。
$$ \ chi(k)=\ sum \ Limits_R {S} _ {\ mathrm {o}} ^ 2 {N} _ {\ mathrm {R}} \ frac {\ left | f(k)\ right |} {k {R} ^ 2} \ sin \ left(2 kR + 2 {\ delta} _ {\ mathrm {c}} + \ phi \ right){e} ^ {\ frac {-2R} {\ lambda( k)}} {e} ^ {-2 {\ sigma} ^ 2 {k} ^ 2} $$(6)ここで、\({S} _ {\ mathrm {o}} ^ 2 \)(\(0 <{S} _ {\ mathrm {o}} ^ 2 <1 \))は、削減係数 Nです。 R は距離 R での後方散乱原子の数です 、 f ( k )は後方散乱振幅δです。 c 中央からの位相シフト、 ϕ は後方散乱原子、λ はコアホールの寿命、σ 2 は複数の距離からのデバイ-ワラー因子であり、 k 光電子の平均自由行程です。 EXAFS領域は通常、エッジジャンプの上の20〜30 eVのエネルギー範囲と呼ばれ、短距離秩序タイプ、結合距離、および材料の配位数に敏感です。ただし、式。 (6)は、EXAFS近似と振動に関する情報を提供する可能性がありますが、EXAFSスペクトルの情報コンテンツを視覚化するための特に便利な形式ではありません。したがって、フーリエ変換を使用して k を分解できます。 異なる構成周波数への空間信号[32]。フーリエ変換は、原子間距離 R の複素関数です。 、その振幅はχの実関数で表されます ( R )。この関数では、ピークの位置は結合距離と隣接するイオンに関連しています。式(6)は k から変換できます R へのスペース 次のように、フーリエ変換による空間:
$$ \ chi(R)=\ frac {1} {\ sqrt {2 \ pi}} {\ int} _ {k _ {\ mathrm {min}}} ^ {k _ {\ mathrm {max}}} \ omega (k){k} ^ n \ chi {e} ^ {-2 ikR} dk $$(7)$$ \ left \ {\ begin {array} {c} \ genfrac {} {} {0pt} {} {\ kern2.5em 0 \ kern7.5em k <{k} _ {\ mathrm {min}} \} {\ sin ^ 2 \ left [\ frac {\ pi \ left(k- {k} _ {\ mathrm {min}} \ right)} {2 \ left({k} _2- {k} _ {\ mathrm {min}} \ right)} \ right] \ kern3.25em {k} _ {\ mathrm {min} }ここで k max および k min 変換された k の最大値と最小値です それぞれスペース、χ (R)はハニングウィンドウ関数ωです。 ( k )はガウスウィンドウ関数であり、 k n は重み係数( n =0、1、2、3)。 k 2 および k 3 BFA x の値 Oはそれぞれ2と10であり、 n の値は は2です。Fe K のフーリエ変換 -BFA x のエッジEXAFS 図4aに示すように、Oサンプルが実行されます。 〜1.503Åを中心とする非対称ピーク(最初の破線で囲まれている)は、酸素アニオンからの散乱により、Fe-O結合として識別されます。 〜3.527Å付近の2番目の強いピーク(2番目の破線で囲まれている)は、Fe-Fe / Al結合に対応します。これは、隣接するFe / Al原子からの酸素アニオンの散乱によって説明できます。シェル。 1番目と2番目の配位シェルの距離を図4の表3にまとめました。ピーク位置から、ドープされていないBFOサンプルと比較して、Fe-OおよびFe-Fe / Al結合はわずかに小さいにシフトする傾向があります。 R x の増加に伴う値 。これは、Alイオンによるドーピングが、中央のFe原子の最近傍の局所構造に影響を与えるだけでなく、Fe原子の次に近い配位シェルにも影響を与えることを示しています。一方、Fe-O結合のより小さな R へのシフト 値は、Alイオンの半径がFeイオンの半径よりも小さいことに起因する可能性があります。これはXRDデータと一致しています。 Fe-Fe / Alのより小さな R へのシフト 値は、平均Fe-Fe / Al結合長(2つのFe 3+ イオンは隣接する酸素八面体の中心にあります)は徐々に短くなり、結合角はAlドープサンプルで変更されます。ただし、ドープされたサンプルのFe-O分布のピーク強度はわずかに増加しますが、Fe-Fe / Al分布のピーク強度はほとんど変化しません。これは、Fe-Oの鉄隣接構造がAlドーピングによって変更されていることを示しています。 AlドープサンプルのFe-Fe / Al結合が短いことで、XRDの主要なピーク(101)が2 θにシフトする理由を説明できます。 角度(図1bを参照)。これは、Feの代わりにAlを使用すると、酸素の八面体に影響を与える可能性があることを示しています。これにより、隣接する2つのFe原子間の配位距離がさらに短くなります。図4bは、Fe K を示しています。 -edge EXAFS of the BFAx O samples processed on k 3 × χ ( k ) oscillation with a k space of 0–10 Å −1 。 As can be seen, all the k 3 × χ ( k ) spectra show similar patterns at the smaller k values but different at larger k values with some various noise (surrounded by the dash line). Al-doped samples show a broader k 2 × χ ( k ) spectrum than those of undoped BFO in the k space of 8.2–9.3 Å −1 , implying an enhanced short-range structural disorder in BFAx O samples. The noises are observed in a k space of 10–10.4 Å −1 。 These changes indicated that the local structure of center atoms has changed due to B-site Al doping, similar to what was reported by Li et al. [51].
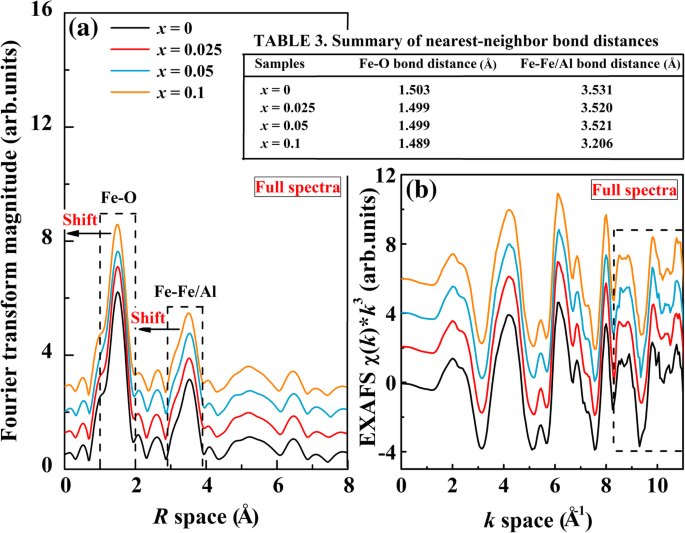
a Fourier transforms of Fe K -edge k 3 -weighted EXAFS data, for the BFAx O (0 ≤ x ≤ 0.1). b EXAFS χ ( k ) × k 3 spectra of BFAx O (0 ≤ x ≤ 0.1). The spectra were aligned along the Y -axis for better comparison
The peak positions, intensities, and shapes of the line in the Bi L 3 -edge XANES spectrum are well known to depend on the local electronic structure of the Bi atoms, which could provide information on the Bi valence. The full spectra of Bi L 3 -edge XANES of undoped BFO and BFAx O samples are also shown in Fig. 5a, while Fig. 5b shows the Bi L 3 -edge XANES spectrum in the energy region of 13,400–13,480 eV. The analysis of these spectra helps to investigate the local electronic structure of Bi ions in the doped system. From Fig. 5b, it can be seen that the shape of all spectra are the same to each other and there is almost no change of absorption edge in the whole series. The absorption edge energies for our study are found to be 13,429.1 eV, 13,429.4 eV, 13,429.3 eV, 13,429.3 eV, and 13,429.8 eV for x =0, 0.025, 0.05, and 0.1 and the reference compound Bi2 O 3 , respectively (see Table 4 in Fig. 5). The absorption edges slightly shift toward higher energies with increasing Al concentration. The absorption edge in the Bi L 3 -edge of the BFAx O samples matches well with that of the reference compound Bi2 O 3 , which indicates that the valence state of Bi ions in all the samples is in + 3 valence state. However, there are two post-edge peaks found in all samples and marked as B1 and B2, respectively. These two post-edge peaks are caused by the electric-forbidden transition from 2p 3/2 level to the 6d ones. Compared with undoped BFO, the intensity of peak B2 can be clearly seen to increase for the doped samples (see Fig. 5c), which means the transition from 2p 3/2 to 6d state increases, so does the energy of 6d 州。 Except these, there is no other significant change in the whole spectrum.
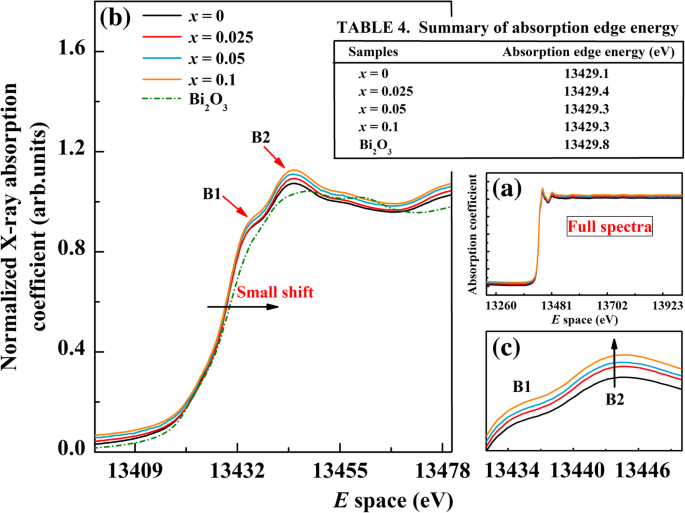
a Bi L 3 -edge XANES spectra of BFAx O (0 ≤ x ≤ 0.1) and reference Bi2 O 3 。 b XANES spectrum in the range of 13,400–13,480 eV. c Enlarged view of the peak D and peak E
Fourier transform of Bi L 3 -edge EXAFS radial distribution functions is performed, as shown in Fig. 6a. A high-intensity peak located at around 1.618 Å corresponds to the nearest Bi-O coordination shell (surrounded by the dash line), which is a result from scattering from the nearest-neighbor atomic shell of Bi, i.e., oxygen anions. However, the position of Bi-O bond shifts toward larger R values for the doped samples (see Table 5 in Fig. 6). This indicates that the substitution of Al for Fe could affect the nearest-neighbor local structure of the central Bi atom. It also indicates the extension of Bi-O bond length. The peak intensity of the Bi-O distribution exhibited a small increase with increasing Al content, which suggests that the iron-neighboring structure of Bi-O has changed. Figure 6b shows the Bi L 3 -edge k 3 × χ ( k ) EXAFS spectra with a k space of 0–14 Å −1 。 From Fig. 6b, it can be seen that all the spectra shape shows similar patterns except some error noises. The error noises are observed in the k space of 12–14 Å −1 (surrounded by the dash line). This result may imply that the k 3 × χ ( k ) EXAFS function of the center Bi atoms has changed with Al doping. This also suggests that the B-site Al substitution influences short-range structural disordering.
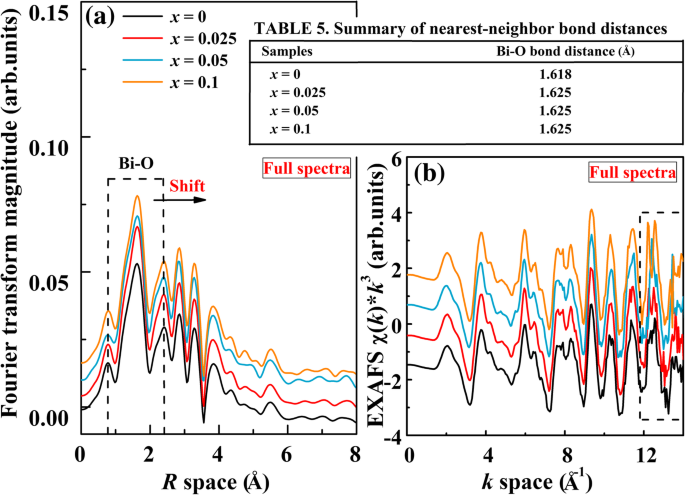
a Fourier transforms of Bi L 3 -edge k 3 -weighted EXAFS data, for the BFAx O (0 ≤ x ≤ 0.1). b EXAFS χ ( k ) × k 3 spectra of BFAx O (0 ≤ x ≤ 0.1). The spectra were aligned along the Y -軸
The optical properties of the samples are studied by using RT UV-Vis, which is used to characterize the optical properties of the materials. The UV-Vis absorption spectra of undoped BFO and BFAx O samples in the wavelength of 300–800 nm are shown in Fig. 7a. As a result, the UV-Vis spectra of the undoped BFO and BFAx O samples show two absorption edges (marked by dashed arrows). One is a band around 650 nm, which is due to the metal-to-metal transition. The other is a band around 760 nm, which is caused by crystal field transition [52]. In addition, the strong absorption band is observed at about 490 nm (marked by dashed arrow), which is attributed to the electronic transition from O 2p to Fe 3d state in the BFO. These strong bands indicate that the BFO prepared by hydrothermal method could be a promising visible-light photocatalytic material. BFO is of direct transition with a value of n as 2. The absorption edge of the doped samples shifted from 659 to 619 nm, suggesting that the BFAx O powders absorb visible light in the wavelength range of 600–659 nm (see Fig. 7a). A similar blue-shift phenomenon was observed earlier in other element-doped BFO [53,54,55]. This blue shift in the absorption spectra of Al-doped samples in comparison with the undoped BFO shows that doping Al causes a change in the local structure for BFO. From Fig. 7a, one can see that the absorption spectra of the Al-doped samples exhibit a sharp increase around 490 nm and it suggests that all samples can absorb remarkable amounts of visible light. For the sample with x =0.025, the absorption spectrum shows a sudden increase. It means that it has a wider absorption range than the other samples in this range of visible light. The optical band gap of the samples has been calculated by Tauc’s formula, as follows:
$$ ahm=A{\left( hm-E\mathrm{g}\right)}^n $$ (9)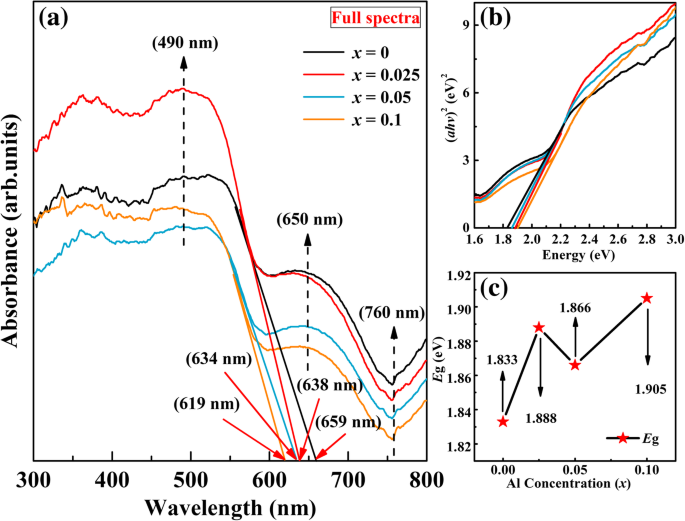
a UV-Vis absorption spectrum of BFAx O (0 ≤ x ≤ 0.1). b Plots of (ahν ) 2 vs. photon energy. c E g values as a function of Al concentration
ここで a is the absorption coefficient, A is the parameter, h is the Planck’s constant, m is the frequency of the incident photon, E g is the optical band gap, and n (for direct n =2, for indirect n =0.5) is a constant associated with different types of electronic transitions, as shown in Fig. 7b. The calculated E g values are found to be 1.833 eV, 1.888 eV, 1.866 eV, and 1.905 eV for x =0, x =0.025, x =0.05, and x =0.1 samples, respectively. It is easy to see that the band gap increases with the substitution ratio, as shown in Fig. 7c. The increase in the band gap is attributed to the doping effect. E g value for the undoped BFO is about 1.833 eV, which is lower than the previous reports [56, 57].
結論
In summary, the BFAx O( x =0, 0.025, 0.05, and 0.1) multiferroic powder samples were successfully synthesized via hydrothermal route. Effects of Al substitution on the structural, electrical, and optical properties of the samples were studied. The structural study reveals that Al-doped BiFeO3 shows the existence of secondary phases and lattice contraction due to lower ionic radii of Al doped into B-site, which still retains its rhombohedral R3c perovskite structure. Raman scattering measurement infers six Raman active phonon modes, which further confirms the result of XRD. XAFS studies on the Fe K -edge and B L 3 -edge of the BFAx O samples and of the reference compounds Fe2 O 3 およびBi 2 O 3 were performed, and the obtained results were compared in order to determine the valance states of Fe and Bi ions in the system. The Fe K -edge XAFS results revealed that BFAx O is a mixed-valent (Fe 3+ /Fe 2+ ) システム。 The results of Fe K -edge XAFS also illustrate a competition between the Fe 3d and Al 3d orbitals on hybridization with the O 2p and occurrence of the more 4p orbitals with Al doping. Besides, Al ion doping affects both the nearest-neighbor and next-nearest coordination shells of the Fe atom. The B L 3 -edge XAFS results indicate that valence states of Bi ions in all the samples are in + 3 and the transition from 2p 3/2 to 6d state and the energy of 6d state increases. Substitution Al for Fe could affect the nearest-neighbor local structure of central Bi atom. The BFAx O prepared by hydrothermal method could be an appropriate visible-light photocatalytic material due to a strong absorption band in the visible region.
略語
- AFM:
-
反強磁性
- BFAx O:
-
BiFe1-x Alx O 3
- BFO:
-
BiFeO3
- EXAFS:
-
X-ray absorption fine structure
- FE:
-
Ferroelectric
- FM:
-
強磁性
- RT:
-
室温
- UV-Vis:
-
紫外可視
- XAFS:
-
X-ray absorption fine structure
- XANES:
-
X-ray absorption near edge structure
- XRD:
-
X線回折
ナノマテリアル
- (p-i-n)接合GaAsナノワイヤ太陽電池におけるプラズモン増強光吸収:FDTDシミュレーション法の研究
- X線シンクロトロン粉末回折によって調べたHoCo0.5Cr0.5O3の異常な熱膨張
- 新規ナノ粒子増強ワーム状ミセルシステムの研究
- 角度分解X線光電子分光法によるAl2O3キャップGaN / AlGaN / GaNヘテロ構造の表面分極に関する調査
- コンドロイチン硫酸-メトトレキサートナノゲルの抗腫瘍研究
- スパイラル型アンテナによるマイクロブリッジ構造のTHzマイクロボロメータの周波数変調と吸収改善
- InSeナノリボンの電子構造とI-V特性
- 赤外領域におけるAlドープZnO膜の光学的性質とそれらの吸収への応用
- GaAs / AlAs超格子の点欠陥の第一原理研究:相安定性とバンド構造およびキャリア移動度への影響
- 黒フォスフォレンへの遷移金属の吸着:第一原理研究
- オゾン検出のための空洞増強吸収分光法(CEAS)



