アプタマー修飾メソポーラスシリカナノ粒子に基づく効率的な細胞標的化ドラッグデリバリーシステム
要約
化学療法薬を腫瘍細胞に効率的かつ選択的に送達して治療効果を改善する方法は、依然として困難な問題です。本明細書では、アプタマーSgc8の腫瘍標的化能力に依存してドキソルビシン(Dox)を標的の白血病細胞に送達する、アプタマー修飾メソポーラスシリカナノ粒子に基づく効率的な細胞標的化ドラッグデリバリーシステム(Sgc8-MSN / Dox)を構築します。方法、それによって治療効果を改善し、毒性を減らします。この研究では、Sgc8-MSN / Doxは持続的なDox放出を示し、CCRF-CEMヒト急性Tリンパ球白血病細胞を標的にして効率的に殺し、癌治療としての可能性を示唆しています。
はじめに
急性リンパ芽球性白血病(ALL)は、人間の健康を深刻に危険にさらす不均一な悪性腫瘍です[1,2,3]。米国では、特に小児および青年において、毎年約6000例の急性リンパ芽球性白血病が診断されています。 ALLは、小児で最も一般的な癌であり、20歳未満の癌による死亡の最も一般的な原因です[4]。
化学放射線療法と骨髄造血幹細胞移植は、ALLの標準的な治療法です。放射線療法は実質的な全身性副作用と関連しており、最適な曝露部位は不明です。骨髄造血幹細胞移植は、費用、患者の年齢、およびドナー骨髄の不足のために、しばしば実行可能ではありません。化学療法は、離れた病巣を排除し、それによって再発を防ぐのに効果的ですが、ほとんどの抗腫瘍薬のごく一部だけが循環を介して腫瘍に到達します。その結果、薬剤のバイオアベイラビリティが低くなり、病気の細胞に対する選択性が正常な細胞よりも低くなり、深刻な副作用や薬剤耐性のリスクが高まります。
ナノドラッグデリバリーシステムは、腫瘍微小環境の特定の条件によって引き起こされる薬物放出を含む、それ自体の薬物よりもはるかに効果的で標的化された抗腫瘍薬の送達を提供することができます[5、6]。そのようなシステムの中で、メソポーラスシリカナノ粒子(MSN)は、その大きな変更可能な表面のために注目を集めています。さまざまな量と種類の薬剤を運ぶことができる、調整可能な細孔容積。そしてそれらの優れた生体適合性[7、8]。機能応答グループによる表面修飾により、特定の条件下で薬物を放出するMSNを作成できます。一方、ターゲティング分子による修飾により、MSNは薬物を目的の組織に選択的に送達できます[9、10]。
MSNと互換性のあるターゲティング分子の1つのタイプは、アプタマーです。アプタマーは、ターゲットに特異的かつ強固に結合する「化学抗体」として機能する一本鎖DNAまたはRNAです。アプタマーは、モノクローナル抗体よりも小さく、調製と修飾が容易であり、組織への浸透性が高く、毒性と免疫原性が低くなっています。したがって、アプタマーは腫瘍の検出と標的化学療法に広く使用されています[11、12、13]。 SELEX法は、CEMヒト急性Tリンパ球白血病細胞に特異的に結合するアプタマーSgc8を同定するために使用されてきました[14、15]。 Sgc8は、CEM細胞膜上のプロテインチロシンキナーゼ-7(PTK-7)を認識します。化学療法薬や特定のナノ材料にSgc8を加えると、白血病細胞の標的化と死滅を改善することができます[16、17]。
白血病細胞を高感度かつ特異的に検出するためのSgc8アプタマー修飾蛍光シリカナノ粒子システム(Sgc8-FSNPs)を設計しました。これは、白血病の診断だけでなく、抗白血病薬の標的送達にも役立つことが証明されています[18 ]。この研究に基づいて、本研究では、Sgc8で装飾したMSNにドキソルビシン(Dox)をカプセル化しました(図1)。得られたSgc8-MSN / Doxは、薬物送達に適した形態とサイズを示し、ナノ粒子は培養中の白血病細胞に選択的に取り込まれ、腫瘍細胞を効果的に死滅させました。この研究の目的は、アプタマー修飾メソポーラスシリカナノ粒子が腫瘍の診断を標的にするだけでなく、薬物をロードすることによって腫瘍を殺し、腫瘍を標的とするセラノスティクスのアイデアを提供できることを明らかにすることです。
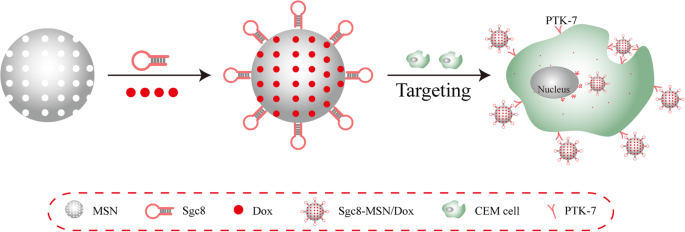
効率的な細胞標的化ドラッグデリバリーシステムのためのSgc8アプタマー修飾メソポーラスシリカナノ粒子の概略図。 CEM細胞、CCRF-CEMヒト急性Tリンパ球白血病細胞;ドックス、ドキソルビシン; MSN、修飾シリカナノ粒子; PTK-7、プロテインチロシンキナーゼ-7
実験資料と方法
試薬と材料
ドキソルビシン塩酸塩(Dox)は、Beijing Huafeng United Technology(北京、中国)から購入しました。分析グレードのテトラエチルオルトシリケート(TEOS)と3-トリエトキシシリルプロピルアミン(APTES)はShanghai Chemical Reagent Factory I(上海、中国)から購入し、セチルトリメチルアンモニウムブロミド(CTAB、純度99%)はShanghai Jizhi Biochemical Technology(上海、中国)から購入しました。 。他のすべての試薬は分析グレードでした。カルボン酸修飾Sgc8アプタマー(5'-ATCTAACTGCCGCCGCGGGAAAATGTACGGTTAG(T) 10 -COOH-3 ')[16]はShanghai Bioengineering(Shanghai、China)によって合成されました。
細胞株
次の細胞株は、中国科学アカデミー(上海、中国)のセルバンクから購入しました:ヒト急性Tリンパ球白血病細胞株CCRF-CEM、ラモスヒトブルキットリンパ腫B細胞株、L02ヒト正常肝細胞株、および293Thuman胚性腎臓細胞株。すべての細胞株は、37°C、5%CO 2 で培養されました。 10%ウシ胎児血清(FBS、Hyclone)およびペニシリン-ストレプトマイシン(Gibco、Grand Island、NY、USA)を添加したDMEMで。
Sgc8-MSN / Doxの準備
MSNは、0.50gのCTABを240mLの超純水に溶解し、1.75mlの2M NaOH溶液を添加し、油浴で80°Cに加熱することにより、[19]に記載されているように調製しました。強く攪拌しながら、2.50 mLのTEOSをゆっくりと滴下し、白色の沈殿物が得られるまで混合物を2時間連続して攪拌した。次に、混合物を10,000rpmで10分間遠心分離し、上澄みを除去し、沈殿物を超純水と無水エタノールで交互に3回洗浄し、次に沈殿物を60℃の真空オーブンで一晩乾燥させてMSNを得た。
Sgc8-MSN / Doxは、3つ口フラスコ内の0.2365gのMSNを23.65mLの無水エタノールと混合し、710μLのAPTESを滴下し、24時間還流することによって得られました。混合物をメタノール-HCl溶液(4:1)および脱イオン水で交互に3回洗浄し、次に乾燥させてMSN-NH 2 を得た。 。室温で、MSNs-NH2材料を10 mLの遠心分離管に入れ、適切な量のリン酸緩衝生理食塩水(PBS)に分散させた後、Dox(5 mg / mL)を滴下し、混合物を24h。最後に、カルボキシル修飾Sgc8アプタマー(100 nM / mL)を加え、混合物を1時間撹拌し、遠心分離し、無色になるまでPBSで洗浄して、Sgc8-MSN / Doxを得た。
Sgc8-MSN / Doxの特性評価
ナノ粒子のX線回折パターン(XRD)は、XRD D4回折計(Bruker Inc.、ドイツ)によって測定された。 N2吸着-脱着等温線は、比表面積および細孔径分析器(TriStar 3000、GA Inc.、USA)によって測定されました。 BET表面積は、BETプロットから計算されました。細孔径分布は、BJH法により等温線の吸着分岐から推定されました。 Nano S動的光散乱分析装置(Malvern Instruments、UK)を使用して、粒子サイズと静電ポテンシャルを測定しました。各サンプルについて3回測定を行い、平均しました。粒子サイズと形態は、100 kVの電子ビーム加速電圧での透過型電子顕微鏡(H-7650、東京、日本)によっても評価されました。一方、MSN表面へのSgc8アプタマーの結合は、FT-IR分光法(Nicolet-5700、USA)によって評価されました。アプタマー修飾MSN / Doxの効率を検出するために、Sgc8-MSN / Doxの調製過程で洗浄上清を収集し、260 nmでの紫外線吸収値を測定し、標準曲線法を使用して量を決定しました。未結合のアプタマーの。したがって、アプタマーの修飾量は、添加された総量から未結合の量を差し引くことによって計算できます。
Sgc8-MSN / DoxからのDoxリリース
Sgc8-MSN / DoxからのDoxの放出を invitro で測定しました 次のように。 Sgc8-MSN / Dox(10 mg)をpH5.0または7.4の10mLのバッファーに37°Cで溶解し、100rpmで振とうしました。所定の時間に、サンプルを取り出し、5000 rpmで10分間遠心分離し、Thermo Scientific Microplate Reader(81 Wyman Street、Waltham、USA)の説明に従って、分光光度法を使用して482nmで上清のDoxをアッセイしました[9]。 P>
Sgc8-MSN / Doxのターゲティング機能
CEMまたはRamosセル(3×10 6 )を含むPBSを15 mLの遠心分離管に加え、Sgc8-MSN / DoxまたはMSN / Dox(アプタマー濃度、200 nM)と混合しました。チューブを37℃で20〜30分間インキュベートした後、遠心分離により細胞を回収し、PBSで3回洗浄し、4%パラホルムアルデヒドで30分間固定し、PBSで3回洗浄しました。細胞を1mg / mlDAPIで5分間インキュベートし、PBSで3回洗浄し、遠心分離しました。細胞ペレットをPBSに再懸濁し、スライド上に置いて蛍光共焦点顕微鏡((Nikon DS-Ri1;東京、日本))で分析しました。
別の実験では、CEMセルとRamosセル(3×10 5 )対数増殖期において、50μLのPBS、45μLの結合バッファー[5 mM MgCl2、4.5 g / Lグルコースおよび1mg / mlウシ血清アルブミン(BSA)を添加したPBS]、および10μLの混合物に再懸濁しました。 200nMのアプタマー濃度で示された材料を含むFBS [1 mg / mlウシ血清アルブミン(BSA)を添加したPBS]の。混合物を暗所で4℃で30分間振とうした。細胞を洗浄バッファーで洗浄し、1000rpmで5分間遠心分離した後、さらに3回洗浄しました。最後に、細胞を500μLの洗浄バッファーに再懸濁し、フローサイトメトリー(Beckman Coulter Epics X L; Beckman Coulter、Inc.、Brea、CA、USA)で分析しました。
MSNの細胞毒性
Doxまたはアプタマーを含まないMSNの細胞毒性は、MTT法を使用して評価されました。対数増殖期のCEM、Ramos、293T、およびL-02細胞を96ウェルプレート(1.5×10 4 )に追加しました。 /良い)。 MSN(100μL)を各ウェルに加え、プレートを5%CO 2 で培養しました。 37°Cで24時間または48時間のインキュベーター。 MTT(20μL)を各ウェルに加え、プレートを37°Cでさらに30分間インキュベートした後、プレートを1500rpmで10分間遠心分離し、培養上清を廃棄しました。 DMSO(200μL)を各ウェルに加え、プレートを暗所で10分間振とうした後、自動マイクロプレートリーダーを使用して570 nmでの光学密度(OD)を測定しました。各サンプルは6回繰り返してテストされ、結果は平均±SDとして表されました。
Sgc8-MSN / Doxによるセルキル
96ウェルプレートのCEM、Ramos、293T、およびL-02細胞(1×10 5 ウェルあたりの細胞数)を、遊離のDox、MSN / Dox、またはSgc8-MSN / DoxとともにDox濃度1、5、10、15、または20μg/ mLで24時間インキュベートしました。 Sgc8-MSN / Doxが実際にアプタマー受容体を介してCEM細胞を殺す標的にされたことをさらに確認するために、まず十分なSgc8アプタマーをCEM細胞と2時間インキュベートし、次にsgc8-MSN / DoxとDox濃度20μg/でインキュベートします。 24時間ml。 「MSNの細胞毒性」のセクションで説明されているように、MTTアッセイを使用して生存率を比較しました。
統計分析
結果は、Studentの t を使用して統計的に分析されました。 最小有意差検定による検定および一元配置分散分析。すべての分析は、GraphPad Prism 6.02(GraphPad Software、米国カリフォルニア州サンディエゴ)を使用して実行されました。
結果と考察
Sgc8-MSN / Doxの特性評価
X線回折データは、合成されたナノ粒子がX範囲に六角形のメソ細孔の典型的な回折ピークを持っていることを示し(図2a)、MSNの構造を確認しました。 MSNの比表面積、細孔径分布、およびメソポーラスパラメータをさらに調査するために、MSNで窒素吸脱着試験を実施しました。 MSNのN2吸着-脱着等温線(図2b)は、タイプIVの等温線特性を示し、メソポーラス特性を示します。 BETモデルで計算された表面積は1389m 2 / g。 BJH曲線は、粒子の細孔径分布が狭いことを示しています(図2b、挿入図)。細孔径は5.23nm、細孔容積は2.51 cm 3 です。 / g。大きな比表面積と細孔容積、および豊富なメソ細孔により、より強力な薬物負荷容量を実現し、優れた薬物担体になる可能性があります。電子顕微鏡は、Sgc8-MSN / Doxが球形または楕円形で、良好な分散性と均一なサイズを持っていることを示しました(図3a)。 PBS中のMSN / Doxの平均ゼータ電位は− 26.53 mVでしたが、Sgc8-MSN / Doxでは− 33.87 mVに減少し(図3b)、Sgc8アプタマーの負電荷を反映しています[20]。メソポーラスシリコンの表面に細孔チャネルが観察された。 PBSでは、MSN / Doxは98.35nmの平均水和粒子サイズを示しましたが、Sgc8アプタマーを結合してSgc8-MSN / Doxを作成した後、103.24 nmに増加しました(図3c、d)。 Sgc8-MSN / Doxの結合が成功したことをさらに確認するために、FT-IR分光分析を実施しました。赤外スペクトルを図3eに示します。 3400 cm -1 のピーク 、1100 cm -1 、および500 cm -1 シリカの特徴的なピークです。ピークは約2400cm -1 CTABテンプレートエージェントのピークです。ピークは約1600cm -1 NH 2 です ピーク。 1700 cm -1 付近に現れるピーク MSNにロードされたDoxのクラスターベースのC =0結合伸縮特性ピークと見なされます。 1650 cm -1 の新しいピーク これは、Sgc8とNH2-MSN / Doxの反応によって生成されるシッフ塩基(–C =N–)によるものです。これらの証拠は、Sgc8-MSN / Doxドラッグデリバリーシステムが正常に準備されたことを証明しています。アプタマー修飾Sgc8-MSN / Doxの効率を検出するために、紫外分光光度計を使用して260 nmでのアプタマーの吸光度密度(OD)を測定し、OD値の変化に基づいてナノ粒子効率に対するアプタマー修飾を計算しました。ナノ粒子の表面へのアプタマー修飾の前後。アプタマー溶液と上澄みの紫外線吸収(UV-Vis)スペクトルを図3eに示します。計算によると、Sgc8-MSN / Doxに対するSgc8アプタマーの修飾量は約6.87nmol mg –1 でした。 Sgc8-MSN / Dox。
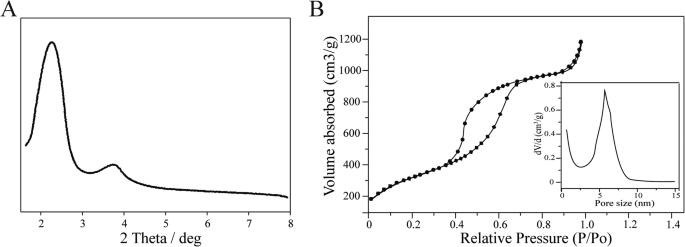
a XRDおよび b MSNの窒素収着等温線; (挿入図)MSNの細孔容積と細孔径分布のプロット
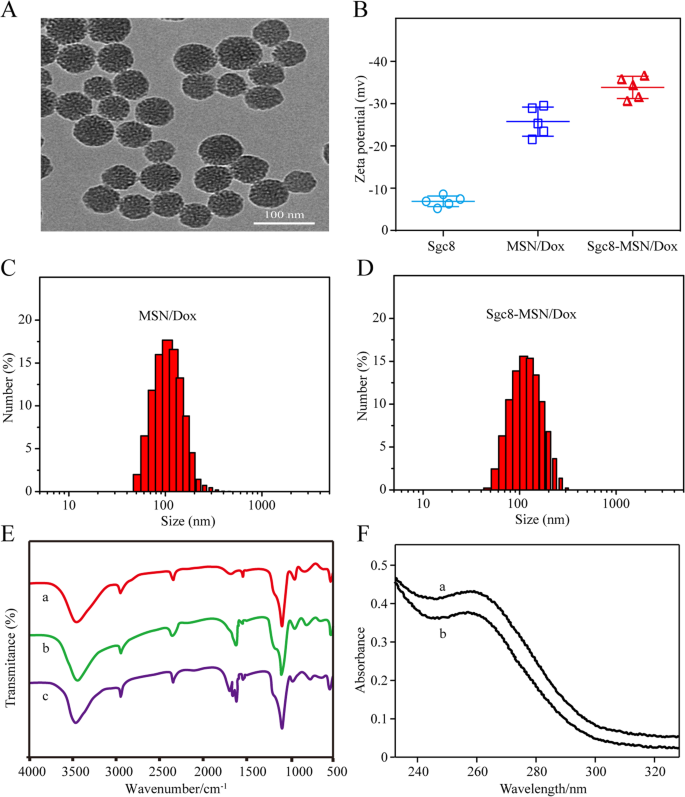
ナノマテリアルの特性評価。 a Sgc8-MSN / Doxの電子顕微鏡写真。 b ナノ粒子のポテンシャル図。 c の粒度分布 MSN / Doxおよび d Sgc8-MSN / Dox。 e ナノマテリアルのFT-IRスペクトル: a MSN、 b MSN / Dox、および c Sgc8-MSN / Dox。 f a のUV-Visスペクトル Sgc8アプタマー溶液、 b 調製過程での上清の洗浄Sgc8-MSN / Dox
Sgc8-MSN / Dox InVitroからのDoxリリース
MSN / DoxおよびSgc8-MSN / Doxは、pH 7.4でゆっくりと薬剤カーゴを放出しました。96時間以内に放出された薬剤は50%以下でした(図4)。これは、MSNが96時間続くゆっくりとした薬物放出をサポートできることを示しています。これはおそらく、薬物がメソポーラスシリコンの内部チャネル全体に広がるためです。放出はpH5.0ではるかに速く、放出率は48時間で60%、96時間で> 80%に達しました。 Dox放出曲線はSgc8-MSN / DoxとMSN / Doxでほぼ同じであり、アプタマーライゲーションがナノ粒子構造に影響を与えないことを示唆しています。腫瘍細胞は弱酸性環境にあり、Sgc8でコーティングされたナノ粒子はエンドソームに内在化されるため、酸性pHでの放出量が多いと便利です[15]。私たちの結果は、メソポーラスシリコンが酸性環境での薬物放出を加速できるという考えを支持しています[21、22]。
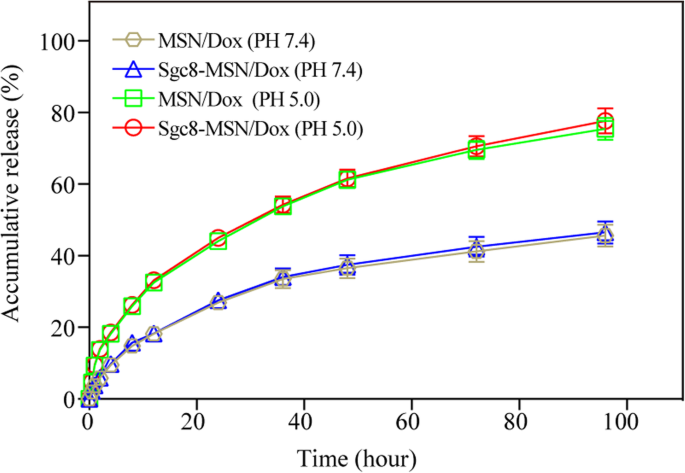
pH5.0または7.4でのinvitroでのSgc8-MSN / DoxおよびMSN / Doxからのドキソルビシンの放出
Sgc8-MSN / Dox InVitroによる白血病細胞のターゲティング
標的細胞としてのCEMTリンパ球白血病細胞および非標的細胞としてのRamosBリンパ腫細胞によるナノ粒子の取り込みを調べた。フローサイトメトリーに基づくと、非標的細胞はSgc8-MSN / Doxと同程度にMSN / Doxを内在化しましたが、標的細胞はMSN / Doxよりもはるかに大きな程度でアプタマー被覆ナノ粒子を内在化しました(図5a)。これらの結果と一致して、蛍光共焦点顕微鏡は、Sgc8-MSN / Doxに曝露されたCEM細胞内で強いDox蛍光(赤)を示しましたが、同じ方法で処理されたRamos細胞内では示されませんでした(図5b)。これらの結果は、白血病細胞を標的とするSgc8アプタマーの確立された能力を反映しています[20]。 Sgc8はCEM細胞の表面にあるPTK-7を認識し[18]、ナノ粒子を表面に動員し、それによってそれらの取り込みをより効率的にします[23]。我々の結果は、Sgc8-MSN / DoxがPTK-7を発現する癌細胞を一次および二次部位または循環系で標的とし、転移の制御に役立つ可能性があることを示唆しています。 MSNアプローチを、他のターゲティング特異性を持つ他のアプタマーに拡張できる可能性があります[24、25]。
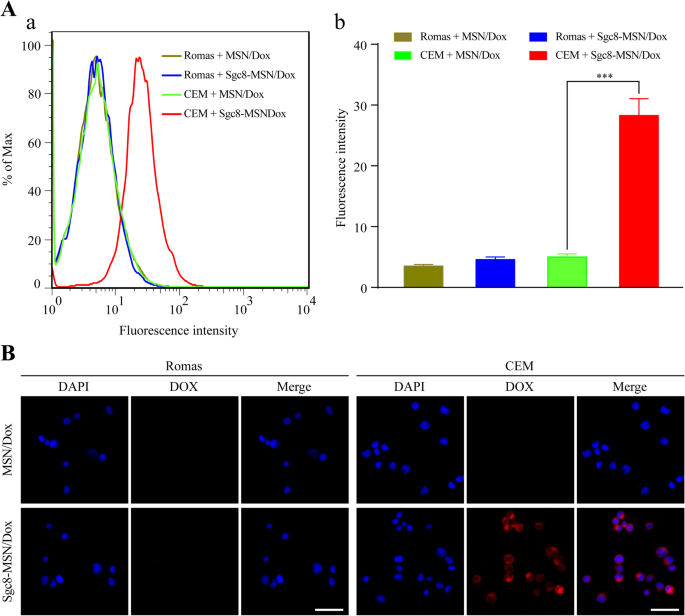
a を使用して分析されたSgc8-MSN / Doxによる白血病細胞のinvitroターゲティング フローサイトメトリーと b 蛍光顕微鏡。 CCRF-CEMおよびRomas細胞をMSN / DoxまたはSgc8-MSN / Doxとインキュベートし、DAPI(青)で染色しました。ドックスは赤く見えた。スケールバー、100μm
MSNの細胞毒性
ナノドラッグデリバリーシステムのバイオセーフティの重要性を考慮して[25]、最初にCEM、Ramos、293T、およびL-02細胞に対するブランクMSNの毒性を調べました。最大100μg/ mLのMSNとの48時間のインキュベーション後でも、すべての細胞株の生存率は90%を超えたままでした(図6)。これは、MSNがほとんど無視できる細胞毒性を示すことを示唆しています。
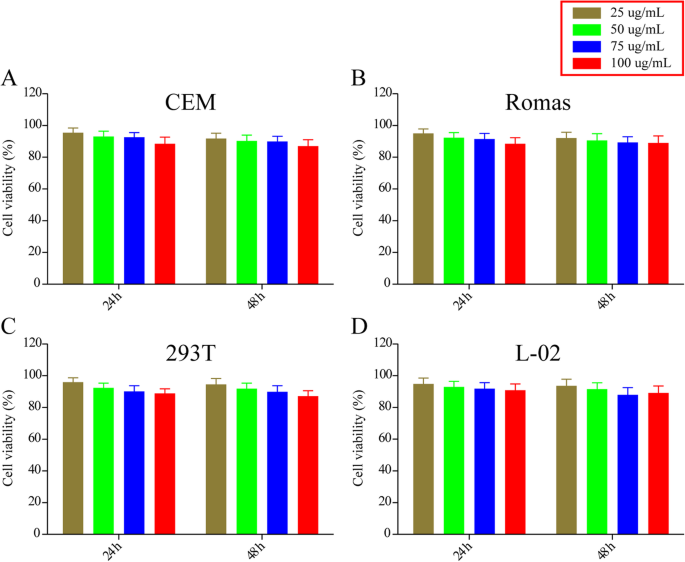
MSNのinvitro細胞毒性。 a CEM、 b ラモス、 c 293T、および d L-02細胞を指示された濃度のMSNで処理し、細胞生存率を測定しました
次に、Sgc8-MSN / Doxが標的腫瘍細胞(CEM細胞)と非標的細胞(Ramos、293T、およびL-02細胞)を殺す能力を調査しました。細胞をさまざまな濃度の遊離Dox、MSN / Dox、またはSgc8-MSN / Doxとともに24時間インキュベートし、MTTアッセイを使用して生存率を評価しました。標的CEM細胞に対して、遊離Doxは2つのMSN製剤よりもわずかに高い毒性を示しましたが、Sgc8-MSN / Doxは同じ薬物濃度でMSN / Doxよりも有意に毒性が高かった(図7)。 Ramos、293T、およびL-02細胞に対して、遊離Doxは、Sgc8の有無にかかわらず同様の毒性を示したMSN製剤よりも有意に高い毒性を示しました。 Sgc8-MSN / Doxが実際にアプタマー受容体PTK-7を介してCEM細胞を殺す標的にされたことをさらに確認するために、最初に十分なSgc8アプタマーをCEM細胞と2時間インキュベートして結合部位をブロックし、次にSgc8と共インキュベートします。 -MSN / Dox。 MTTアッセイは、遊離アプタマーがCEM細胞に対して毒性を持たないことを示し、十分なSgc8アプタマーが結合部位をブロックした後、Sgc8-MSN / Doxは遊離Sgc8-MSN / Doxグループよりも有意に低い毒性を示しました(図7e)。これらの結果は、薬物送達を標的とし、標的細胞の死滅を促進するアプタマーの能力を強調しています。このような標的化は、非標的細胞による薬物の取り込みを減らすのに役立つだけでなく、より低い用量の使用を可能にすることができます。どちらの効果も有毒な副作用のリスクを減らすことができます[26]。
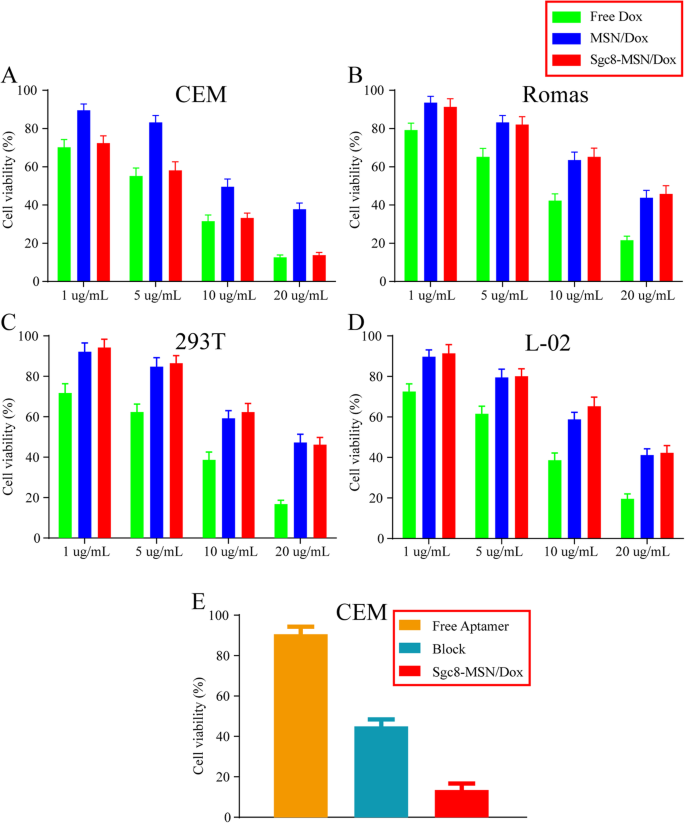
無料のDOX、MSN / Dox、およびSgc8-MSN / Doxが a を殺す能力 CEMセル、 b ラモス細胞、 c 293T細胞、および d L-02セル。 e 遊離アプタマーのCEM細胞殺傷能力、ブロック(CEM細胞は最初に十分なSgc8を2時間インキュベートし、次にsgc8-MSN / Doxとインキュベートします)、およびSgc8-MSN / Dox
アプタマーは、薬物やさまざまな高分子またはナノキャリアを腫瘍細胞に送達するためのガイド分子として使用できます。アプタマーは治療薬としても機能する場合があります。たとえば、AS1411アプタマーはヌクレオリンに特異的に結合することができ、ヌクレオリンは細胞分化、生存、炎症、血管新生、および腫瘍発生に関与する腫瘍細胞内およびその表面に発現します。 AS1411アプタマーは、ヌクレオリンと結合することにより、異種移植モデル(腎がん、肺がん、MX1乳がん、および膵臓がん)の増殖阻害を誘発する可能性があります[27]。さらに、AS1411アプタマーで機能化されたドキソルビシンをロードしたリポソーム(Apt-Dox-Lip)が乳がんでテストされ、その結果は大きな応用の可能性を示しました[28]。アプタマーは、その優れた特性により、幅広い臨床試験で成功を収めています。最初のアプタマーは2005年にFDAによって承認され[29]、それ以来、ますます多くのアプタマーが臨床試験に到達しています。アプタマーは、前立腺癌[30]、肺癌[31]、急性骨髄性白血病[32]などを含む抗腫瘍臨床試験に適用されました。これらのアプタマー関連の臨床試験が、従来の治療スタイルを変える新たな希望を与えることは間違いありません。
近年、腫瘍の標的療法のために、アプタマーがさまざまなナノ材料と組み合わされています。アプタマーは並外れた分子認識およびターゲティング能力を持っていることがわかります。しかし、ヌクレアーゼがインビボでのアプタマーの安定性に影響を与えるかどうか、小分子物質のアプタマーが体内に入り、腎系、および生体内での実際のターゲティング性能が実現可能かどうか。アプタマーベースの標的ナノ材料の可能性を最大限に活用するために、より多くのインビボ試験および臨床的に関連する実験が現在の研究の焦点のままである。同時に、腫瘍のセラノスティクスは将来の開発にとって重要な方向性であり、より多機能な生物学的機能材料の設計と準備は間違いなく開発の傾向です。
結論
白血病細胞を効率的に標的とし、Doxの取り込みを促進できるアプタマー修飾MSNデリバリーシステムを構築しました。このターゲティングは、酸性条件下で薬物カーゴをゆっくりと優先的に放出するMSNの能力と相まって、デリバリーシステムが腫瘍部位に蓄積し、細胞を継続的に殺すのに役立つ可能性があります。適切なアプタマーを選択することにより、このMSNアプローチでほぼすべてのタイプの腫瘍細胞を標的にすることが可能かもしれません。しかし、Sgc8-MSN / Doxにも上記の問題がある可能性があることを無視することはできず、そのinvivoでの安定性とターゲティングにはさらに研究が必要です。次は、これまでの研究を組み合わせて、ドラッグデリバリーシステムに診断試薬と薬剤の両方をロードし、対象を絞った診断と対象を絞った治療のセラノスティック機能を提供します。
略語
- MSN:
-
メソポーラスシリコンナノ粒子
- Dox:
-
ドキソルビシン
- Sgc8-MSN / Dox:
-
アプタマー修飾メソポーラスシリカドラッグデリバリーシステム
- PTK-7:
-
プロテインチロシンキナーゼ-7
- TEOS:
-
テトラエチルオルトシリケート
- APTES:
-
3-トリエトキシシリルプロピルアミン
- CTAB:
-
セチルトリメチルアンモニウムブロミド
- CEM:
-
CCRF-CEMcells
- PBS:
-
リン酸緩衝生理食塩水
ナノマテリアル
- ドラッグデリバリーを強化するためのナノファイバーとフィラメント
- 生体適合性FePO4ナノ粒子:ドラッグデリバリー、RNA安定化、および機能的活性
- 腫瘍治療のためのドラッグデリバリーシステムとしての環境応答性金属有機フレームワーク
- 癌用途のための細胞ベースのドラッグデリバリー
- ゼブラフィッシュ:ナノテクノロジーを介した神経特異的ドラッグデリバリーのための有望なリアルタイムモデルシステム
- 黒色腫の標的化学療法治療のための薬物送達担体としての131I追跡PLGA-脂質ナノ粒子
- ナノテクノロジー:invivoイメージングシステムから制御されたドラッグデリバリーまで
- 多機能GaN / Feナノ粒子による内皮細胞の標的化
- 細胞内タンパク質送達のためのシリカナノ粒子:緑色蛍光タンパク質を使用した新しい合成アプローチ
- 二重ドラッグデリバリーのためのナノリポソームベースのシステムの物理化学的特性に関する調査
- トランスフェリン受容体による細胞内在化が増強されたパクリタキセルベースの標的脂質ナノ粒子の抗増殖およびアポトーシス誘発能—白血病細胞での研究



