黒色腫の標的化学療法治療のための薬物送達担体としての131I追跡PLGA-脂質ナノ粒子
要約
本明細書において、葉酸(FA)結合ポリ(d、l-ラクチド-コ-グリコリド)(PLGA)-脂質複合体(FA-PL)は、不溶性抗癌剤パクリタキセル(PTX)の標的化送達のためのナノ担体として開発された。結果として生じるFA-PLPナノ粒子。さらに、 131 放射性トレーサーとしてのIを使用して、FA-PLPナノ粒子(FA-PLP- 131 )を標識しました。 I)それらの細胞取り込み活性、in vivo血液循環、および生体内分布を評価する。 FA-PLP- 131 Iナノ粒子は、安定性が高く、サイズ分布が狭く(165.6および181.2 nm)、平均ゼータ電位が-22.1mVの球状の形態を持っていました。共焦点レーザー走査顕微鏡は、標的分子FAがPLP- 131 を促進することを示しました 私はメラノーマB16F10細胞に取り込みます。これは、 131 を介した細胞取り込み率によってさらに確認されました。 ガンマカウンターで測定した活動検出。 FA-PLP- 131 PTXなしのI(FA-PL- 131 I)細胞毒性はわずかで、生体適合性は良好ですが、FA-PLP- 131 遊離PTXおよびPLPと比較して効率的な細胞生存率抑制があることが実証されました- 131 I.静脈内注射後、遊離PTXの血液循環半減期( t 1/2 =5.4±0.23h)はFA-PLP- 131 によって18.5±0.5hに延長されました I. FAターゲティングを通じて、FA-PLP- 131 の腫瘍への取り込み 私はPLP- 131 と比較して約4.41倍と12.8倍高かった 私と無料のPTX- 131 それぞれ私。さらに、40日間の治療後、FA-PLP- 131 遊離PTXおよびPLPと比較して改善された腫瘍抑制効果を示しました- 131 私は、再発も、顕著な全身性の生体内毒性もありません。結果は、 131 I標識PLGA-脂質ナノ粒子は、標的化された薬物送達と生体内での薬物の信頼性の高い追跡に同時に適用できます。
背景
最も攻撃的な皮膚がんの1つである黒色腫は、メラノサイトの悪性形質転換に起因します[1、2]。再発が容易で転移の可能性が高いことを考えると、転移した黒色腫患者の5年生存率はわずか10%です。現在まで、黒色腫患者の最も一般的な治療法は化学療法であり、これは望ましくない重篤な副作用、低いバイオアベイラビリティ、低い腫瘍選択性、および用量制限全身毒性を伴い、腫瘍化学療法に大きな課題をもたらします[3、4]。
針葉樹の一種であるイチイの乾燥した根、枝、葉、樹皮に由来する天然植物抽出物であるパクリタキセル(PTX)[5、6]は、卵巣癌や肺を含むいくつかの種類の腫瘍に対して効果的な抗腫瘍活性を示します。がん[7,8,9]。さらに、PTXはヒト黒色腫に対しても有効であると報告されています[10、11]。それにもかかわらず、化学療法薬の上記の欠点に加えて、Cremophor ELおよび脱水アルコール(1:1、 v / v )混合物は、現在の臨床診療でPTXの希釈媒体として使用されており、過敏症などの深刻な副作用を引き起こす可能性があります[12、13]。したがって、化学療法剤の水溶性と腫瘍蓄積を増強して、それらの末梢曝露を低減し、それらのインビボ毒性を最小化するための新規戦略の開発が最も重要である。生体適合性薬物ナノキャリアの最近の開発は、PTXの生理学的安定性を高める可能性を提供します[14、15、16]。さらに、これらのナノキャリアへの標的分子の結合は、腫瘍細胞表面受容体を介した標的効果を介して末梢曝露を低減しながら、腫瘍部位への化学療法剤の選択的送達を可能にする[17、18、19]。
ここでは、葉酸(FA:腫瘍標的分子)を共有結合させ、メラノーマ治療用の化学療法薬としてPTXをカプセル化するポリ(d、l-ラクチド-co-グリコリド)(PLGA)-脂質複合体を調製しました。さらに、 131 放射性マーカーであるIを使用して、PLGA-脂質ナノ粒子を放射性標識し、invivoでの挙動を明確に評価しました。負のベータ放出、物理的半減期、および広範囲の崩壊特性のため、 131 私は一般的にクリニックで放射性標識として使用されています[20、21、22]。 131 の形態、安定性、分散度 I標識PLGA-脂質ナノ粒子(FA-PLP- 131 I)invitroで評価した。さらに、FA-PLP- 131 の細胞取り込み、血液循環、および生体内分布 131 の放射能を測定して調べました I.さらに、FA-PLPの標的となる抗がん効果- 131 私はinvitroとinvivoで研究されました。結果は、FA-PLP- 131 私は、化学療法薬の潜在的な腫瘍ドラッグデリバリーナノキャリアとして使用するための用途の広いナノプラットフォームかもしれません。
メソッド
資料
ポリ(d、l-ラクチド-co-グリコリド)(PLGA、MW:5000–15,000、ラクチド:グリコリド(50:50))およびクロラミン-TはSigma Aldrich(セントルイス、ミズーリ州、米国)から購入しました。 Na 131 私はAtomicHitech(北京、中国)から入手しました。 PTX(99%)および4 '、6-ジアミジノ-2-フェニルインドール(DAPI)は、Aladdin Chemical Reagent Co.、Ltd。(Shanghai、China)から購入しました。 90〜95%のホスファチジルコリン、1,2-ジステアロイル-sn-グリセロール-3-ホスホエタノールアミン- N からなる大豆レシチン -[葉酸(ポリエチレングリコール)-2000](DSPE-PEG 2000 -FA)、および1,2-ジステアロイル-sn-グリセロ-3-ホスホエタノールアミン- N -[カルボキシ(ポリエチレングリコール)-2000](DSPE-PEG 2000 -COOH)は、Avanti(Alabaster、AL、USA)から入手しました。すべての細胞培養試薬はSigmaAldrichから購入しました。
FA-PLPナノ粒子の調製
FA-PLPナノ粒子は、自己組織化ナノ沈殿法によって合成されました[23]。詳細には、10mgのPTXを1mLのエタノールに溶解し、2mgのPLGAを1mLのジクロロメタンに溶解しました。それらを混合した後、レシチン/ DSPE-PEG 2000 -FA(4:1)エタノール水溶液(4 wt%)を混合溶液に滴下し、25°Cで4時間穏やかに攪拌しました。混合物を濾過し、ミリポア限外濾過遠心分離管を使用して脱イオン水で3回洗浄して、カプセル化されていない薬物および有機溶媒を除去した。対照として、FA分子グラフト化のないナノ粒子を同じ方法で調製し、DSPE-PEG 2000 を置き換えました。 -FAとDSPE-PEG 2000 -COOH。精製されたFA-PLPナノ粒子は、さらに使用するまで4°Cで保存されました。
131 の準備 I標識FA-PLPナノ粒子
放射性FA-PLP(FA-PLP- 131 I)ナノ粒子はクロラミン-T酸化法[24]によって調製されました。 1 mL FA-PLP(1 mg / mL)、500μCiNa 131 の混合物 I(FA-PLPに移植できる最大放射能)と100μLの5 mg / mLクロラミン-Tを、pH7.5のリン酸緩衝液中で室温で10分間反応させました。次に、200μLのメタ重亜硫酸ナトリウム(5 mg / mL)を加えることにより、反応を停止させました。 131 I標識PLPおよびPTXは、同じ手順に従って調製しました。遠心分離管(ミリポア)を使用して精製し、残っている遊離Na 131 を除去しました。 ろ液にガンマ活性が検出されなくなるまで。標識されたナノ粒子の放射性標識の収率と純度は、ガンマカウンター(LKBガンマ1261; LKBインスツルメンツ)を使用して分析されました。
特性評価
UV-vis吸収スペクトルは、UV-vis分光光度計(UV7502、Shanghai Advanced Photoelectric Technology Co.、Ltd。、上海、中国)を使用して記録しました。透過型電子顕微鏡(TEM)画像は、Zeiss LIBRA 120TEMで収集されました。ナノ粒子のサイズ、ゼータ電位、および多分散度指数(PDI)は、Zetasizer Nano ZS(Malvern Instruments)を使用した動的光散乱(DLS)分析によって検出されました。光学写真はNikonD3200デジタルカメラで撮影されました。
細胞培養
マウスメラノーマ細胞株B16F10は、中国科学院(上海、中国)のタイプカルチャーコレクションのセルバンクから入手し、10%ウシ胎児血清と100 U / mLのペニシリン/ストレプトマイシンを含むDMEMで加湿培養しました。 5%CO 2 37°Cの雰囲気。
インビトロ取り込みアッセイ
131 の最適な細胞結合効率時間を決定するために、時間依存のinvitro取り込みアッセイを実施しました。 I標識化合物[25]。 B16F10細胞を24ウェルプレートに1×10 5 で播種しました。 ウェルあたりの細胞数とコンフルエンスまで培養。放射性ヨウ素化サンプル( 131 私、PL- 131 私、FA-PL- 131 私、PLP- 131 私、FA-PLP- 131 I)DMEM培地で調製し、細胞培養ウェルに個別に添加しました。 0.5、1、2、4、および6時間のインキュベーション後、細胞をPBSで3回洗浄し、ガンマカウンター(中国科学技術研究所、Jia Branch Innovation Co.、Ltd。)で放射能を測定しました。取り込み値(%)は、以前の文献[25]に記載されているように計算されました。さらに、ナノ粒子を蛍光色素フルオレセインイソチオシアネート(FITC、Sigma)で標識し、B16F10細胞とインキュベートしました。細胞の蛍光画像は、市販の共焦点レーザー走査顕微鏡(FV1200、オリンパス、東京、日本)を使用してキャプチャされました。
インビトロ細胞毒性アッセイ
MTT細胞生存率アッセイを使用して、PL- 131 の細胞毒性を研究しました。 IとFA-PL- 131 私、および無料のPTX、PLP- 131 私とFA-PLP- 131 私は、B16F10細胞に対して。簡単に説明すると、B16F10細胞を96ウェルプレートに24時間播種し、PL- 131 に曝露しました。 IとFA-PL- 131 I(0〜100μg / mLPLGA-脂質)、または遊離PTX、PLP- 131 私とFA-PLP- 131 I(0〜40μg / mLのさまざまな濃度で)24時間。実験は3回行った。すべてのデータは平均±SDとして表されました。
動物モデル
3〜5週齢のBalb / cマウスは、Shanghai Slack Laboratory Animal Co.、Ltd。(Shanghai、China)から購入しました。すべての動物実験は、復旦大学の動物管理使用委員会によって承認されました。この委員会は、国立衛生研究所の実験動物の管理と使用に関するガイドに準拠しています。
B16F10セル(1×10 6 )PBS中をマウスの右脇腹に皮下注射した。成長する腫瘍の体積はキャリパーを使用して測定され、腫瘍の体積は次の式を使用して計算されました:体積=(長さ×幅 2 )/ 2。腫瘍の体積が約80mmに達したとき 3 、マウスは実験グループにランダム化されました。
血液循環と生体内分布の研究
健康なBalb / cマウスにPTX- 131 を静脈内注射しました IとFA-PLP- 131 I(マウスあたり10μCiの100μL、5 mg / kg)。血液循環は、マウスの尾から約10μLの血液を採取することによって測定されました。血液中の放射能は、ガンマカウンターを使用して測定されました。ナノ粒子の生体内分布を検出するために、B16F10腫瘍を有するマウスにPTX- 131 を注射しました。 私、FA-PL- 131 私、PLP- 131 私とFA-PLP- 131 私は同じ用量で、注射の24時間後に犠牲にしました。主要臓器の重さを量り、ガンマカウントのために収集しました。
InVivo腫瘍化学療法
B16F10腫瘍を有するBalb / cマウスに、150μLの生理食塩水、遊離PTX、PLP- 131 を注射しました。 私とFA-PLP- 131 I(同じPTX濃度、5 mg / kg)。腫瘍のサイズと体重は、4日ごとにノギスで測定されました。相対腫瘍体積は V として計算されました / V 0 ( V 0 治療開始時の腫瘍体積でした)。約40日間の治療後、マウスを犠牲にして主要臓器を採取し、4%ホルマリンで固定し、パラフィン包埋してスライスし、ヘマトキシリンとエオシンで染色し、デジタル顕微鏡で検査しました。
結果と考察
131 の準備と特性評価 I標識FA-PLPナノ粒子
FA-PLPの合成スキーム- 131 Iナノ粒子を図1に示します。簡単に説明すると、FA-PLPナノ粒子は、自己組織化ナノ沈殿法と放射性FA-PLP(FA-PLP- 131 )によって合成されました。 I)クロラミンT酸化法[23、24]を使用して調製した。 PTXはPLGA-脂質複合体によってカプセル化され、次にPEG化によってシェルの表面に共有結合したFAがグラフトされました。最後に、 131 ナノ粒子の外側の表面にグラフトしました。 TEM画像は、FA-PLP- 131 Iナノ粒子は、狭いサイズ分布(165.6〜181.2 nm)の球状の形態を持っていました。これは、動的光散乱によって確認されました(図2a、b)。ゼータ電位は-39.1〜-3.2 mVの範囲でした(図2c)。遊離PTXおよびFA-PLPのUV-visスペクトル- 131 I(同じ濃度のPTX)は、233 nmで同じ特徴ピークを示し(図2d)、PTXがFA-PLP- 131 内にカプセル化されたことを示しています。 私とそのカプセル化は、PTXの吸光度に影響を与えませんでした。計算後、FA-PLP- 131 でのPTXのカプセル化効率 私は56.35±1.6%であることが示されました。 PTXの放射性標識収量- 131 私、PL- 131 私、FA-PL- 131 私、PLP- 131 私とFA-PLP- 131 私はそれぞれ45.6±2.3、52.1±4.1、48.9±1.9、56.3±2.5、54.8±2.7でした。
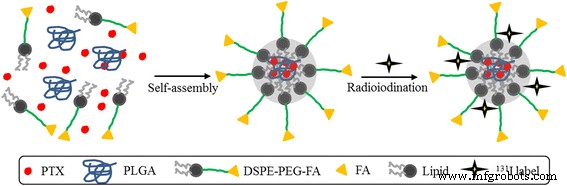
FA-PLPの合成- 131 ナノ粒子
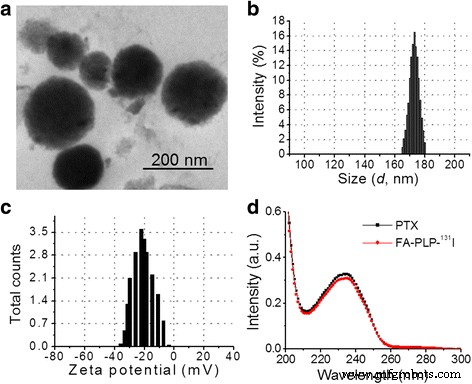
a FA-PLPのTEM画像- 131 I. b 粒子サイズと c FA-PLPのゼータ電位- 131 動的光散乱法で分析しました。 d 遊離PTXおよびFA-PLPの吸光度スペクトル- 131 私
安定性は、ナノ粒子の生物医学的応用に不可欠です[26]。 4週間の保管後、FA-PLP- 131 水、細胞培地、ウシ胎児血清に溶解しましたが、PBSは平均サイズ、ゼータ電位、PDI指数に変化を示さず(図3a–c)、優れた安定性と分散性を示しています。さらに、FA-PLP- 131 の放射性標識の安定性 私は37°Cのマウス血漿で検出され(図3d)、7日以内に15%未満の脱ヨウ素化を示しました。
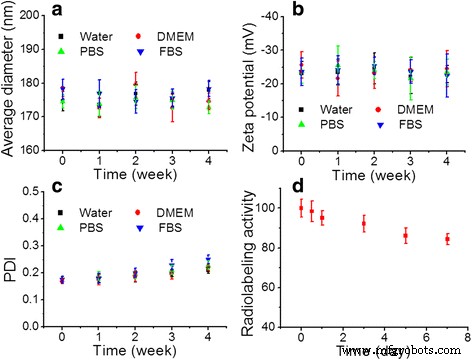
a 、 b コロイドの安定性と c FA-PLPのPDIテスト- 131 私は、水、DMEM、PBS、ウシ胎児血清(FBS)などのさまざまな培地に入れています。 d FA-PLPの放射性標識安定性曲線- 131 保存から2週間以内に37°Cでマウス血漿中の私
インビトロ細胞取り込み
図4は、 131 のinvitroでの時間依存的な取り込みを示しています 私、PL- 131 私、FA-PL- 131 私、PLP- 131 私とFA-PLP- 131 ガンマカウンターで測定されたB16F10細胞のI。 FA-PLP- 131 私とFA-PL- 131 私は、テストされたすべての時点よりも高い取り込み値を示し、時間とともに増加しました。 FA-PLPの組み込み値- 131 6時間のIは、 131 の3.12倍と23.4倍でした。 IとPLP- 131 私は、フルオレセインイソチオシアネート標識FA-PLP- 131 とインキュベートしたB16F10細胞の共焦点レーザー走査顕微鏡画像の結果と一致しています。 IとPLP- 131 Iナノ粒子(追加ファイル1:図S1)。これらの結果は、FA-PLP- 131 の細胞への高い取り込みを示しています。 私は、おそらくB16F10細胞に対するFAを介したターゲティング効果によるものです。
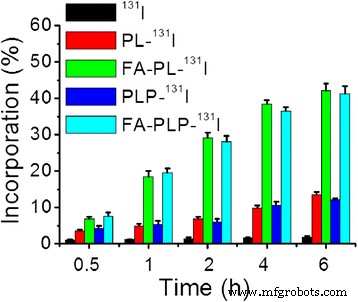
131 の時間依存の組み込み 私、PL- 131 私、FA-PL- 131 私、PLP- 131 私とFA-PLP- 131 私はB16F10セルにいます
インビトロ細胞毒性
コントロールナノキャリア、PL- 131 の細胞毒性 私とFA-PL- 131 私はMTTアッセイでテストされました。 PLで処理された細胞- 131 IとFA-PL- 131 私は24時間、コントロールと同様の生存率を示し(図5a)、生体適合性が良好であることを示しています。さらに、FA-PLP- 131 私は、遊離のPTXやPLPよりもB16F10細胞の増殖を抑制するのにはるかに効果的でした- 131 Iは同じ濃度のPTXであり(図5b)、優れた細胞標的化学療法を示しています。結果は、FA-PLP- 131 私は化学療法効果が高く、放射線毒性や細胞毒性はありません。
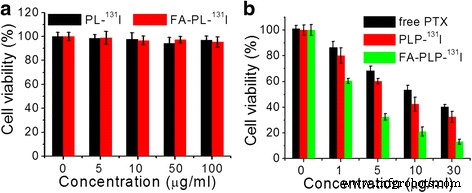
a PL- 131 で処理した後のB16F10細胞の細胞生存率 IとFA-PL- 131 私は24時間です。 b さまざまな濃度の遊離PTX、PLPとのインキュベーション後のB16F10細胞の細胞生存率- 131 私とFA-PLP- 131 私は24時間
血液循環と生体内分布の研究
ナノ粒子の定量的かつ正確なinvivo追跡のために、放射性標識は蛍光イメージングよりも信頼性が高いことが報告されています[27、28]。 131 I標識FA-PLPナノ粒子は、ガンマカウンターで測定した、血液循環や生体内分布などの生体内挙動を調査するために準備されました。無料のPTXの血液循環半減期( t 1/2 =5.4±0.23h)はFA-PLP- 131 によって18.5±0.5hに延長されました I(図6a)は、腫瘍を標的とした蓄積に有利なナノ粒子のカプセル化によるものです[29、30、31]。次に、無料のPTXの生体内分布- 131 私、PLP- 131 私とFA-PLP- 131 注射後1日目のB16F10担癌マウスのIを調査しました(図6b)。 FA-PLP- 131 私とFA-PL- 131 私は、腫瘍取り込みの明らかな増強を示しました。これは、PLP- 131 の4.41倍および12.8倍でした。 私と無料のPTX- 131 私はそれぞれ、FA-PLP- 131 の血液循環が長引いたことが原因である可能性があります 私、FA-PL- 131 私とそのFAターゲティング効果。さらに、肝臓と脾臓も、正常な代謝器官であるナノ粒子代謝のために比較的高い取り込みを示しました[32、33]。
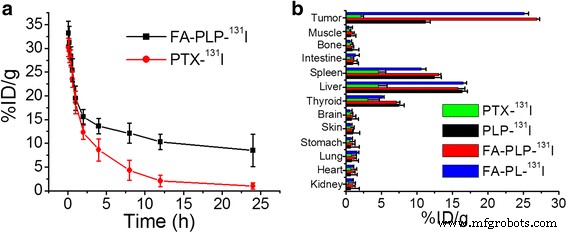
a FA-PLPの血液循環曲線- 131 点滴後です。 b PTXの生体内分布- 131 私、FA-PL- 131 私、FA-PLP- 131 私とPLP- 131 私はB16F10担癌マウスにいます
InVivo腫瘍化学療法
無料のPTX-、PLP- 131 I-、およびFA-PLP- 131 I治療マウスは、生理食塩水対照群と比較して腫瘍増殖の抑制を示しました(図7a)。全体として、FA-PLP- 131 私は、約40日間の治療後、すべての治療群と比較して、再発のない腫瘍増殖抑制に最も効果的でした。これらの結果は、FA-PLP- 131 の血液循環が大幅に延長されていることを考慮すると、予想どおりです。 私、したがって、FAを介した腫瘍標的蓄積を促進するその能力。さらに、腫瘍を標的とした蓄積は、PTXの末梢曝露の減少にもつながり、それによって全身毒性を最小限に抑えました。予想通り、完全な治療プロセスを通じて、体重の目立った減少はなく(図7b)、心臓、肝臓、脾臓、肺、腎臓などの主要な臓器は、どのグループでも明らかな組織学的病変を示しませんでした(図7b)。図7c)。
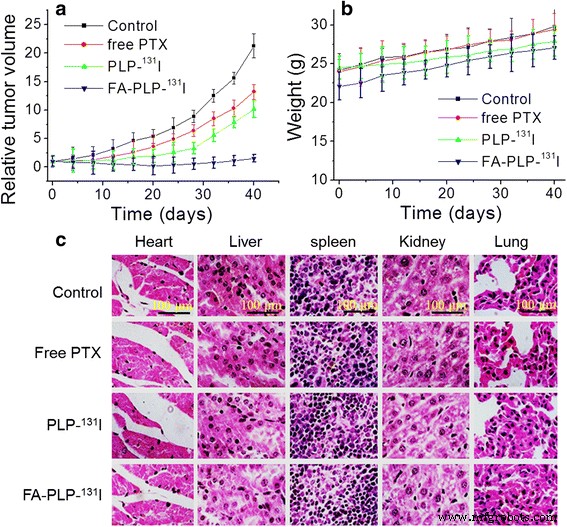
a 相対的な腫瘍体積と b 生理食塩水(対照)、遊離PTX、PLPを尾静脈注射した後の担癌マウスの体重- 131 私、およびFA- PLP- 131 I. b 生理食塩水(対照)、遊離PTX、PLPを尾静脈注射した後の担癌マウスの体重- 131 私、およびFA- PLP- 131 I. c 心臓、肝臓、脾臓、肺、腎臓などの主要臓器の代表的なヘマトキシリンおよびエオシン染色画像。 スケールバー =100μm
結論
要約すると、 131 を合成しました 黒色腫を標的とした化学療法のための薬物送達担体としてのI標識PLGA-脂質ナノ粒子。 131 の放射能を測定する I、FA-PLPのinvitroおよびinvivoでの挙動- 131 Iナノ粒子が研究されました。得られたFA-PLP- 131 優れた分散性とコロイドおよび放射性標識の安定性を示しました。コントロールナノキャリア、PL- 131 私とFA-PL- 131 また、良好な生体適合性を示しました。 PTXのカプセル化に続いて、FA-PLP- 131 私は、FAターゲティング効果に起因する、細胞毒性なしでB16F10細胞増殖を抑制するのに最も効果的でした。さらに、FA-PLP- 131 私は、PTXの血液循環を大幅に延長し、標的となる腫瘍領域内に効果的に蓄積することが実証されました。したがって、FA-PLP- 131 私は優れた腫瘍増殖阻害と優れたinvivo生体適合性を持っていました。結果は、これらの用途の広いFA-PLP- 131 の有望な可能性を浮き彫りにします。 信頼性の高い薬物追跡剤としてのIナノキャリア、および腫瘍標的療法への応用。
ナノマテリアル
- ドラッグデリバリーを強化するためのナノファイバーとフィラメント
- 生体適合性FePO4ナノ粒子:ドラッグデリバリー、RNA安定化、および機能的活性
- 腫瘍治療のためのドラッグデリバリーシステムとしての環境応答性金属有機フレームワーク
- 癌用途のための細胞ベースのドラッグデリバリー
- ゼブラフィッシュ:ナノテクノロジーを介した神経特異的ドラッグデリバリーのための有望なリアルタイムモデルシステム
- ナノテクノロジー:invivoイメージングシステムから制御されたドラッグデリバリーまで
- 単分散二元FePt-Fe3O4ナノ粒子の合成のための後処理法
- 二重ドラッグデリバリーのためのナノリポソームベースのシステムの物理化学的特性に関する調査
- 髄外多発性骨髄腫治療のためのスマートドラッグデリバリーシステムとしてのドキソルビシン負荷PEG-CdTe量子ドット
- ドキソルビシンの超音波を介した標的化送達のための生体適合性キトサンナノバブル
- 非接触型決済の未来



