生物医学分野における活性酸素種に関連するナノ粒子の毒性
要約
ナノ粒子のユニークな物理化学的特性は、最近、さまざまなアプリケーションのセット、特に生物医学分野でますます注目を集めています。ただし、ナノ粒子は過剰な量の活性酸素種(ROS)を生成する傾向が高いため、ナノ粒子の潜在的な毒物学的影響に関する懸念が残っています。強い酸化の可能性があるため、ナノ粒子によって誘発される過剰なROSは、生体分子と細胞小器官の構造に損傷を与え、タンパク質の酸化的カルボニル化、脂質過酸化、DNA / RNAの破壊、膜構造の破壊を引き起こし、さらに壊死、アポトーシスを引き起こします。または突然変異誘発さえ。このレビューは、メカニズムの概要を示し、細胞レベルでのナノ粒子によるROS生成の原因であり、ROSを介した生物毒性のメカニズムへの洞察を提供することを目的としています。ナノ粒子の毒性に関する文献を要約し、生物医学的応用のためにナノ粒子を最適化するための戦略を提案します。
はじめに
ナノ粒子(NP)は、寸法が100nm未満の新しい合成粒子のクラスです。それらの形状とサイズに応じて、明確な物理的および化学的特性がNPに異なる機能を与えます。 NPは、繊維、化粧品、浄水、食品包装など、多くの消費者製品で広く使用されています[1、2]。また、光触媒、エネルギー、オプトエレクトロニクスのエンジニアリングにも使用されています[3,4,5,6]。
特に、NPは生物医学材料で好まれる材料になり、バイオセンサー、siRNA送達、標的遺伝子ノックダウン、薬物送達、および生物充填医療材料で広く使用されています[7、8、9、10、11]。 NPのさらなる使用法はまだ発見されています。たとえば、Duan etal。 [12]は、Fe 3 O 4 -ポリエチレングリコール-ポリアミド-アミン-マトリックスメタロプロテイナーゼ2 @クロリンe6(Fe 3 O 4 -PEG-G5-MMP2 @ Ce6)ナノプローブは、胃の腫瘍増殖を有意に抑制しました。別のケースでは、pDNA-ポリエチレンイミンCeOナノ粒子(pDNA-PEI-CeO NP)は、より多くの線維肉腫細胞のアポトーシスを誘発する可能性があります[13]。さらに、中空シリカ-Fe-ポリエチレングリコール-ヒト表皮成長因子受容体2ナノ粒子(HS-Fe-PEG-HER2 NP)は腫瘍細胞に選択的に結合でき、正常組織と癌細胞を区別するための造影剤として使用されました[14]。最後に、銀ナノ粒子(Ag NP)は、耐性菌のバイオフィルム関連感染症と効率的に戦うナノ抗生物質として機能します[15]。
さまざまな分野でのNPの積極的な応用の可能性にもかかわらず、ますます多くの研究が、NP曝露後の生物[16、17]および細胞[18、19]への悪影響を示しています。 NPの毒性の可能性は、そのサイズと形状に依存します。これにより、活性酸素種(ROS)の生成を誘発する傾向が決まります[20、21]。過剰世代のROSは、遺伝子毒性、アポトーシス、壊死、炎症、線維症、化生、肥大、発がんなど、一連の生理病理学的転帰を引き起こす可能性があります[18、22、23]。 NPの毒性は、炎症誘発性サイトカインの発現を増強し、マクロファージなどの炎症細胞を活性化することも示されています。これにより、ROSの生成がさらに増加します[23、24]。 NPへの曝露後のROSの生成の増加は、細胞機能の調節を誘発することも示されており、場合によっては致命的な結果をもたらします[17、23、25]。このレビューでは、NPによって誘発されるROSバーストの根底にある主なメカニズムについて説明し、NPの細胞毒性の主な理由を分析し、NPの潜在的な病原性効果を要約します。私たちの現在のレビューは、ROSの過剰産生がNPの生物毒性の主な原因であるという圧倒的な証拠を提供します。したがって、新しい研究は、低ROS産生を誘発するNPを設計することにより、NPの細胞毒性を低減することを目的とすべきです。
生物医学分野でのNPの適用
NPはさまざまな医療用途で使用されており、いくつかの新規NPは、新規生物医学材料での使用に有望な特性を示します。表1に要約されているように、Nano-C60は、invivoおよびinvitroの両方で癌細胞の増殖を阻害する抗癌剤として使用できます[26]。 ZnO NPは、整形外科および歯科インプラントのフィラーとして使用されてきました[38]。 TiO 2 抗菌剤として、空気や水の浄化、そして歯科補綴物に使用できます[52,53,54]。 Davaeifar etal。フィコシアニン-ZnOナノロッドが内因性ROS生成を減少させることによって細胞を保護できることを報告しました[68]。 Pacurari etal。 SWCNTは、臨床診断薬および生物工学材料として適用できる可能性があることを指摘しました[88]。それ以外にも、ROSバーストを誘発することで細菌を殺す抗菌剤として多数のNPを使用できます(表1)。
<図>細胞内のNPによって誘発されるROSの増加のメカニズム
ROSは、過酸化水素(H 2 )を含む酸素を含む化学反応性粒子です。 O 2 )、反応性スーパーオキシドアニオンラジカル(O 2- )、およびヒドロキシルラジカル(•OH)[92、93]。 ROSは主に、小胞体(ER)などの細胞小器官、ペルオキシソーム、そして最も顕著なのはミトコンドリアで生成されます[94]。酸化的リン酸化の間、酸素はミトコンドリアの電子伝達系(ETC)を介して電子を追加することによって水の合成に使用されます。これらの電子の一部は、分子状酸素によって受け入れられ、O 2- を形成します。 、H 2 をさらに変換できます O 2 および•OH [93]。
生理学的状況では、ROSは酸素の正常な代謝に対する自然な応答として生成され[95]、さまざまな細胞シグナル伝達経路で重要な役割を果たします[96、97]。 DrögeとHolmstrometal。 ROSは、表皮成長因子(EGF)受容体、マイトジェン活性化プロテインキナーゼ(MAPK)カスケード、転写因子活性化因子タンパク質-1(AP-1)、核因子-KB( NF-κB)、さらに哺乳類の成長、増殖、分化の過程に関与しました[98、99]。さらなる研究により、ROSは創傷修復[100]、低酸素後の生存[101]、細胞内pH恒常性[102]、および自然免疫[103]も調節することが示されました。
それにもかかわらず、NPへの曝露後、ROSの細胞内生成は細胞内でROSバーストを誘発することによって急激に増加する可能性があります[20](表1)。 ROSバーストの主なメカニズムの説明は、NPによって放出された金属イオンがミトコンドリアの呼吸を損なうことによってROSの過剰発現を促進することです[30、104]。
NPによって放出された金属イオンは、フェントン反応を介してレドックスサイクリングおよび化学触媒作用に混合することが示されています[H 2 O 2 + Fe 2+ →Fe 3+ + HO − +•OH]またはフェントンのような反応[Ag + H 2 O 2 + H + =Ag + +•OH + H 2 O] [23、105、106]。解離した金属イオン(すなわち、Ag + )はまた、細胞酵素の不活性化、膜構造の破壊[31、107]、電子遮断プロセスの妨害[108]、酸化還元電位レベルの低下、ミトコンドリア膜電位(MMP)の低下[109]を引き起こし、細胞内ROSの蓄積をさらに高めます。 NPは、電子伝達プロセスを妨害し[32、110]、NADP + を増加させることにより、細胞内ROS蓄積を促進することも報告されています。 / NADPH比[30]、およびミトコンドリア機能の妨害[18]。 NPは、 soxS などの酸化ストレス関連遺伝子の発現をさらに妨害します。 、 soxR 、 oxyR 、および ahpC [58]; sod1 などの抗酸化遺伝子 および gpx 1 [111、112];およびNADPH産生関連遺伝子 met9 [30]。 NPによって引き起こされる酸化および抗酸化遺伝子の発現の不安定性は細胞内ROS蓄積を加速します。
興味深いことに、ROS産生の増加は、NPの特定のサイズと形状と強く関連しています[113、114]。たとえば、TiO 2 NPは細胞内ROS生成に寄与し、それが核酸とタンパク質の損傷を引き起こしました[10]。遼ら10 nm TiO 2 NPは、テストされた他のサイズよりも遺伝子毒性が高いため、より多くのROS生成を誘発する可能性があります[115]。別のケースでは、Se NPは細胞内でのROSの生成を促進し、細胞内ROSの収量はSeNPの直径と高度に関連していました。この場合、直径81 nmは、テストされた他のサイズよりも多くのROS生成を誘発しました[113]。 Cho etal。さらに、NPの形状がROS産生を誘導する能力に強く影響することを示しました。日中の花を模倣する金属ナノ粒子(D-NP)は、夜の花を模倣する金属ナノ粒子(N-NP)よりもROSの生成が大幅に高くなり、細胞殺傷効果が向上します[114](図1)。 P>
周囲の溶液および細胞においてNPによって誘導されるROSの産生[32]。 NPから生成された電子は細胞に入り、呼吸鎖の機能を妨害し、細胞内のROS産生を増強する可能性があります。電子はO 2 とも反応する可能性があります 直接および細胞外ROSの生成を増加させた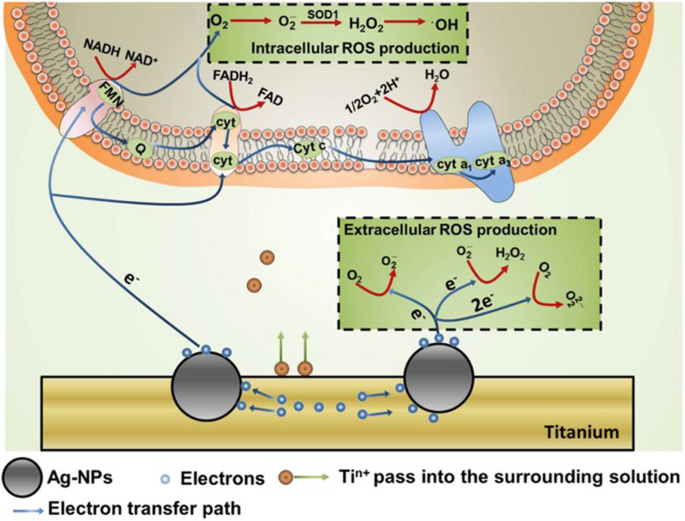
NPは非常に低濃度で細胞内ROSバーストを誘発する可能性があり(表1に示す)、たとえば、1μg/ mLのNano-C60は、酸化ストレスを誘発することによって細胞アポトーシスを大幅に増加させることができます[26、27]。特に、VO 2 で報告されているように、ほとんどのNPには用量依存的な効果があります。 NP [60、61]およびCuO NP [74、75]。
ROS生成の増加による細胞上のNPの壊滅的な結果
細胞に入るNPはしばしば細胞に悪影響を及ぼします。 NPの細胞毒性について最も支持されている説明は、酸化ストレスがROSバーストによって誘発されるということです。 NPによって引き起こされるROSバーストは、生体高分子の酸化的修飾、細胞構造の損傷、薬剤耐性の発生、遺伝子変異、および発がんを引き起こしました[116、117]。さらに、ROSバーストは、トリガー炎症の場合のように、細胞の正常な生理学的機能を変化させ、最終的に細胞機能をブロックし、生物に損傷を与えます[23、118、119]。一般に、NPは最初に細胞表面に吸着され、次に膜を通過して細胞に入り、そこでROSの生成を誘導します[36]。 ROSはその強力な酸化能により、細胞に非常にストレスを与え[46]、炭水化物、核酸、不飽和脂肪酸、タンパク質、アミノ酸、ビタミンなど、細胞内のほぼすべての種類の生体分子を攻撃します[36、120、121 ](図2)。
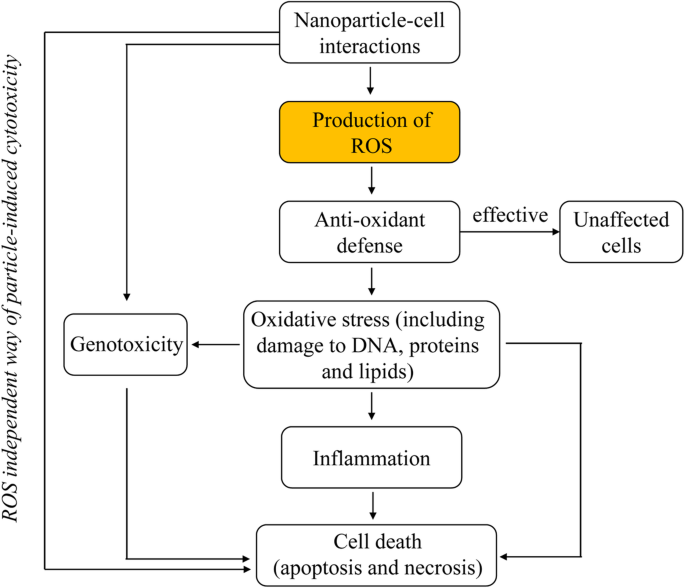
NPによって誘発される細胞毒性におけるROSの重要な役割[33]。 NPが細胞内システムと相互作用した後に発生する可能性のある細胞イベント
ROSは脂質過酸化と膜構造の損傷をもたらします
脂質、特に不飽和脂肪酸は重要な細胞内高分子であり、細胞膜の構造と機能に重要な役割を果たします。 NPは細胞膜に強く引き付けられ、そこでROSを生成し、外膜脂質過酸化を引き起こす可能性があります。細胞膜の脂肪酸含有量が変化すると、細胞透過性が増加し、細胞外環境から細胞質へのNPの制御されない輸送が起こり、細胞損傷がさらに進行する可能性があります[76、122]。
細胞内NPは、次のラウンドのROSバーストを誘発します。過負荷のROSは、細胞小器官の膜の破裂、細胞小器官の内容物の漏出[52、123]、細胞受容体の不活性化[124]、乳酸デヒドロゲナーゼ(LDH)の放出、さらに不可逆的な細胞損傷を引き起こします[125 ]。
ROSはタンパク質を攻撃し、機能を不活性化します
ROSはアミノ酸の疎水性残基を攻撃し、ペプチド結合の切断に寄与し、これらのタンパク質の機能を妨害します[126,127,128]。カルボニル化は、酸化的損傷を受けるタンパク質のもう1つの特徴です[129]。カルボニル化タンパク質は、化学的に不可逆的でプロテアソームを介して分解できない凝集体を形成し、これらのタンパク質の機能を永久に失います[130、131]。グルナサンら。 [132]は、PtNPがROSの生成を促進し、カルボニル化タンパク質レベルを増加させ、骨肉腫の増殖を抑制し、アポトーシスに寄与することを示しました。あるケースでは、燃焼および摩擦由来のナノ粒子(CFDNP)がアルツハイマー病の若年成人の脳に蓄積し、ROSの生成を促進し、タンパク質の誤った折り畳み、凝集、および細動を引き起こした可能性があります[133]。さらに、Pelgrift etal。は、MgNPが遺伝子の転写を阻害したりタンパク質に直接損傷を与えたりする可能性があることを示しました[10]。
ROSによる遺伝子変異
DNAやRNAを含む核酸は、細胞の機能、成長、発達に不可欠であり、それらの構成要素であるヌクレオチドはROSの脆弱な標的です[134,135,136]。酸化還元電位が低いため、ROSは核酸塩基と直接反応して修飾することができます[137]。たとえば、ROSはグアニンを8-オキソ-7,8ジヒドログアニン(8-oxoG)[138]に酸化し、アデニンを1,2-ジヒドロ-2-オキソアデニン(2-oxoA)[139]に酸化することができます。これらの塩基修飾はDNA損傷を引き起こします[140]。遺伝子毒性の可能性とROS形成を誘発する能力[141]のため、NPは一本鎖および二本鎖DNA切断[142、143]、染色体損傷、および異数性遺伝子イベント[144]を有意に誘発します。
ROSの産生の増加は、遺伝子のミスコーディング、異数性、倍数性、およびNPに曝露された細胞における突然変異誘発の活性化の主な原因です[145,146,147,148]。ヌクレオチドプールの中で、グアニンは最も脆弱であり、ROSによって8-oxoGに容易に酸化されます[149]。 DNA中の8-oxo-dGのレベルが上がると、DNA塩基のミスマッチが生じます[150]。同様に、A:8-oxoGを組み込むと、G:C> T:Aの有害な電気的除細動変異の割合が増加します[151、152]。 G:C> T:AトランスバージョンとG:C> A:Tトランジション変異の比率も、酸化的DNA損傷を定量化するための指標として使用されています[153]。
NPによって誘発されるROSの生成は、DNA損傷の蓄積をもたらし、それが変異原性[154]、発癌[155]、多剤耐性[156、157]、老化、および免疫回避[158]の発生を促進します。ジンらROSの過剰産生は、DNA結合転写調節遺伝子の突然変異誘発を劇的に増加させ、その結果、抗生物質の流出が促進され[159]、細菌の複数の抗生物質耐性が促進されることを示しました[34]。 Giannoni etal。ミトコンドリアDNA変異は、細胞内ROSの増加に伴って発生し、ETC複合体Iの活性をさらに損傷し、ミトコンドリア機能障害を引き起こしたと報告しました[160、161]。
NPによって誘発されるDNA損傷は、アミノ酸合成、複製[162]を阻害し、p53 [163]およびRab51タンパク質[82、142]の異常な蓄積を引き起こすことが示されています。 DNA損傷はまた、細胞を遅らせるか完全に停止させる可能性があります[164]。 DNAが損傷した細胞は、成長と増殖の能力を失い[165]、最終的には細胞死を引き起こす可能性があります[166](図3)。
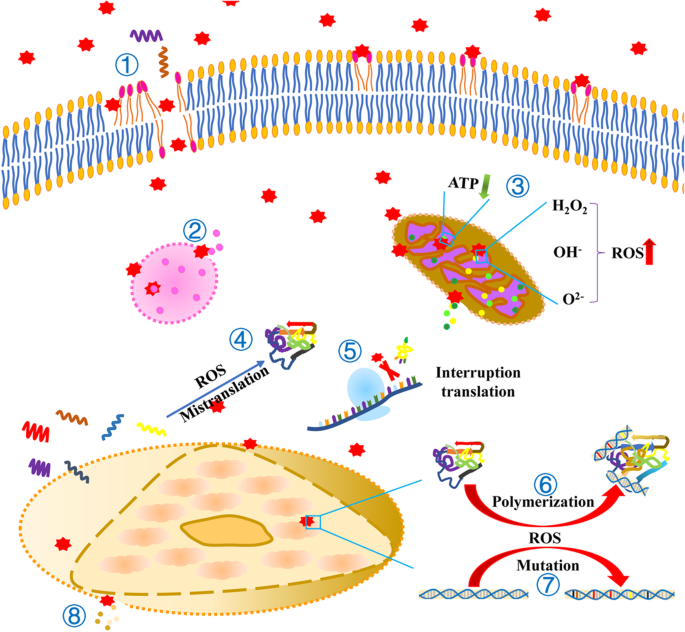
NPによって誘発される細胞イベント。 ①NPは細胞膜の破壊と脂質過酸化に寄与します。 ②リソソーム膜はNPによって破壊され、その内容物が放出されます。 ③ミトコンドリア膜はNPによって損傷を受け、内容物が放出されます。 NPはATPの生成を減らし、ROSの生成を増やします。 ④NPによって誘導されるROSはRNAの誤翻訳を引き起こします。 ⑤NPはtRNAのリボソームへの結合を防ぎます。 ✧NPによって誘導されるROSは、タンパク質とDNAの重合を引き起こします。 ✧NPによって誘発されたROSはDNA変異を引き起こします⑧核膜はNPによって破壊され、その内容物が放出されます
ROSの生成が増加すると、細胞の損傷と病気の発生が誘発されます
NPの細胞毒性は、酸化ストレス、内因性ROS産生、および細胞内抗酸化プールの枯渇に関連しています。酸化ストレスの増加は、生体高分子への酸化的損傷を引き起こし、それが細胞の正常な機能にさらに影響を及ぼし、さまざまな病気の発生と発症に寄与します[167]。
NPは膜損傷を誘発し、細胞質へのNPの輸送を促進します。 NPはリソソーム、ミトコンドリア、および核に集中し、細胞に壊滅的な結果をもたらします[168、169]。 NPは、アデノシン三リン酸(ATP)の生成を減らし[89]、グルタチオンを枯渇させ、タンパク質の誤翻訳を誘発し[170]、リソソームを破裂させ[171]、リボソームサブユニットが転移RNA(tRNA)に結合するのを阻害することが報告されています。これらの細胞イベントは、細胞内の基本的な生物学的プロセスの崩壊を示し、細胞生存率の大幅な低下につながります[47]。 Singh and Scherz-Shouval etal。 NPは、ROSの生成を誘導し、細胞のオートファジーとアポトーシスのプロセスを活性化することにより、細胞骨格機能を妨害する可能性があると報告しました[89]。
NPは、皮膚、肺、腸管などのさまざまな経路を介して体内に入り(図4a)、さまざまな毒物学的影響を及ぼし、炎症や免疫応答などの生物学的応答を誘発する可能性があります[172,173,174]。あるケースでは、細胞をシリカNPに曝露すると、マクロファージが大量のインターロイキン-1β(IL-1β)を分泌し、最終的に細胞死を引き起こしました[175]。 Gaoらは、カーボンナノチューブへの曝露後、肺の炎症がマウスでかなり高く、肺胞マクロファージを活性化し、強い炎症反応を誘発する可能性があると報告しました[176]。別の研究では、ZnO NPに曝露されたモルモットが肺損傷を被り、それが総肺活量と肺活量の低下につながりました[177,178,179]。
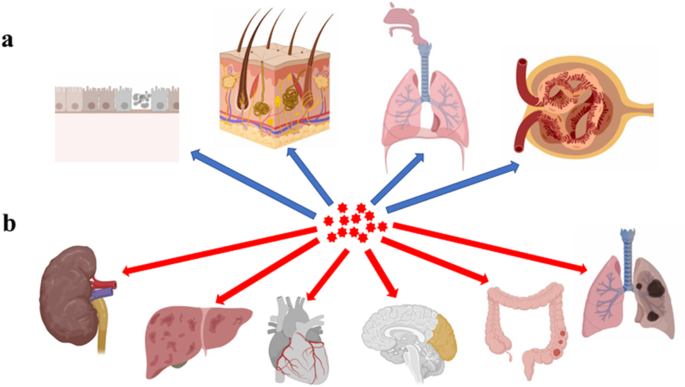
臓器へのNPの侵入と損傷。 a NPは、口腔、鼻腔、気道、腎臓、および腸管を通って生物に侵入する可能性があります。 b NPは体循環によって広がり、腎臓、肝臓、心臓、脳、腸管、肺に蓄積し、臓器機能障害を引き起こす可能性があります(この図はBioRender.comで作成されました)。
ZnO NPはまた、肺胞上皮バリアに重傷を引き起こし、ヒトの肺に炎症を引き起こしました[180]。別のケースでは、腸に吸収されたNPが腸粘膜の炎症と劣化を引き起こしました[181]。 Shubayev etal。 Mg NPは、MMP依存的に血液脳関門と血液神経関門を分解することにより、マクロファージの神経系への移動を促進することに注目した[182]。さらに、カーボンナノチューブを吸入したマウスは、ナイーブな脾臓細胞で免疫抑制と抗体反応の抑制を示しました[183]。最後に、Cd NPは血中単球の生存率を大幅に低下させ、最終的に免疫不全を引き起こしました[184]。
上記の病状に加えて、非常に変動性の高いレベルのROSが、多くのヒトの疾患の発症の主な原因として特定されています。 TretyakovaおよびLiouetal。酸化されたDNAは、心臓や脳に蓄積し、癌、老化関連疾患、慢性炎症の発生に寄与するDNA-タンパク質複合体を形成する傾向があることを示しました[185、186]。 Andersen [187]は、糖尿病、ならびに心血管疾患および神経変性疾患は、ROSの不均衡と非常に関連していると結論付けました。さらに、Pérez-Rosésetal。 ROSの増加がアルツハイマー病とパーキンソン病の発症を促進することを示しました[188]。
さらに、NPは乳がん細胞のアポトーシスを促進し[35]、ROSの生成を促進することによって悪性組織と病原体を破壊することが報告されています[189、190]。しかし、ROSは、正常細胞と癌細胞の両方の増殖を誘発し、突然変異を刺激し、正常細胞で発癌を開始し、癌細胞で多剤耐性を開始することもわかっています[191、192]。ハンディら。カーボンナノチューブに曝露された魚は、曝露時間が長くなると、肺に肉芽腫、肝臓に腫瘍を示すことがわかった[193]。一部のNPは、主に心臓、肺、腎臓、肝臓に影響を与える多臓器不全を引き起こしています。 TiO 2 NPは、体重の減少、脾臓病変、呼吸器系の血液凝固、肝細胞の壊死と線維症、および肺胞中隔の増大を促進することが示されています[194、195]。ある研究では、NPは幹細胞の分化も防ぎ、臓器の損傷を悪化させました[196]。さらなる研究では、NPが精子の質を低下させ[197]、精子を炭素NPに曝露すると、卵子を受精する能力に影響を及ぼし、紫色のウニの胚の発達を損なうことが報告されています[198]。増大する証拠は、微生物、藻類、線虫、植物、動物、およびヒトに対するNPの毒性学的影響を具体的に示しています[22、199、200](図4b)。
細胞毒性が少ないかまったくない新しいタイプのNP
NPは、それらを価値あるものにするさまざまな生物医学的特性を備えています(たとえば、抗菌剤および抗癌剤として[26,27,28])。それらの主な作用機序は、細胞内のROSの産生を増加させる能力です。しかし、この特性はまた、遺伝子突然変異、アポトーシス、さらには発癌を引き起こすことにより、これらの粒子を毒性にします[45、49、58]。したがって、過剰なROS生成を引き起こすことなく、必要な特性を保持する新しいNPを開発する緊急の必要性があります。最近の研究では、細胞内ROSを除去できる新しいタイプのNPが報告されています。これらのタイプは、(1)ROSを除去できるNP [77]と(2)細胞毒性を低下させるために追加の材料でコーティングされたNP [87]の2つのクラスに分類されます。
Panikkanvalappilらは、PtNPがROSを分解することによってDNAの二本鎖切断を阻害することを示しました[201]。別のケースでは、Mn 3 O 4 NPは細胞の酸化還元を調節し、酸化ストレスから生体高分子を保護します[77]。さらに、CeO 2 NPは、フリーラジカル消去能を備えた酸化的損傷から細胞や組織を保護する新しい薬剤です[79、202]。
H 2 O 2 NP-細胞相互作用の主な副産物です。 H 2 O 2 タンパク質、脂質、核酸などの重要な生体分子を破壊します。ただし、細胞をメルカプトプロピオン酸(MPA-NP)またはアミノ化シリカ(SiO 2 )でコーティングされた特殊なMNPで処理した場合 -MNP)、そのような損傷は観察されませんでした[203、204]。同様に、ポリビニルピロリドン(PVP)でコーティングされたGOは、このコーティングがない場合よりも樹状細胞(DC)、Tリンパ球、およびマクロファージに対する毒性作用が少なくなります。 PVP-GOは、Tリンパ球のアポトーシスを減少させ、マクロファージの活性を増加させることさえ示されています[205]。 PtコーティングされたAuNR(PtAuNR)は、従来の金ナノロッド(AuNR)の有効性を維持し、ROSを除去しながら目的の細胞の細胞死を引き起こすことができるため、ROSの生成によって引き起こされる間接的な死から健康な未処理の細胞を保護します[87]。 P>
結論と展望
独自の物理化学的特性(超小型、大きな表面積対質量比、高い反応性など)を備えたNPは、さまざまな用途で非常に望ましいものになっています。商業目的の設計されたNPは急速に増加しています。そのため、NPのバイオセーフティは一般の人々の注目を集めています。このレビューでは、細胞レベルでのNPによるROS形成のメカニズムと責任、および生物医学分野におけるROS関連のNP毒性の最近の進歩を要約し、細胞に優しいNPの新たな分野を強調しました。サイズ、形態、表面積、および成分に関連するNPによって誘発されるROSの生成。さらに、ROSは、細胞生物学および生物医学において生物多機能であるだけでなく、細胞アポトーシス、生存率、および分化を含む細胞シグナル伝達の主要なメディエーターを持っています。
ただし、NPのバイオセーフティを改善し、生物医学分野での使用を加速するには、いくつかのボトルネックを克服する必要があり、多くの作業が依然として必要です。まず、ハイスループット法(HTM)は、invitroおよびinvivoでNPの生物毒性を効率的に検出するように設計されていることが期待されます。 HTMは、時間とリソースを節約し、単一のシステムで複数のパラメーターを組み合わせ、方法論的または体系的なエラーを最小限に抑えることができます。また、NPの特性と細胞応答の関係を深く理解することができ、最適な状態を特定するのに役立ちます。
第二に、NPによって誘発されるROSの生物毒性に関連する分子および細胞のメカニズムはまだ不明です。 NPによるROSの形成に関連するメカニズムをさらに調査することが求められており、これは、ROS生成を制御するためにNPの化学的物理的特徴を改変するためのより多くの情報を提供するであろう。これは、研究者が生物医学分野での臨床的および商業的翻訳を加速するための工学的NPの危険性を減らすための新しい戦略を開発するのに役立つ可能性があります。
最後に、それらの構造的特徴により、NPは複数の経路を介して自由に体内に入る可能性があり、体内にNPが蓄積すると炎症や免疫応答を誘発し、細胞の損傷や死、臓器機能障害を引き起こし、最終的にはアルツハイマー病、パーキンソン病、肝臓の炎症、および異形成症などの多くの疾患。これらの問題は、NPの普及に伴いより差し迫ったものになっています。
データと資料の可用性
この調査中に生成または分析されたすべてのデータは、この公開された記事[およびその補足情報ファイル]に含まれています。
略語
- •OH:
-
ヒドロキシルラジカル
- 2-oxoA:
-
1,2-ジヒドロ-2-オキソアデニン
- 8-oxoG:
-
8-オキソ-7,8ジヒドログアニン
- Ag NP:
-
銀ナノ粒子
- AP-1:
-
転写因子アクチベータータンパク質-1
- ATP:
-
アデノシン三リン酸
- AuNR:
-
金ナノロッド
- CFDNP:
-
燃焼および摩擦由来のナノ粒子
- DC:
-
樹状細胞
- D-NP:
-
日の花を模倣した金属ナノ粒子
- EGF:
-
表皮成長因子
- ER:
-
小胞体
- ETC:
-
ミトコンドリアの電子伝達系
- Fe 3 O 4 -PEG-G5-MMP2 @ Ce6:
-
Fe 3 O 4 -ポリエチレングリコール-ポリアミド-アミン-マトリックスメタロプロテイナーゼ2 @クロリンe6
- H 2 O 2 :
-
過酸化水素
- HS-Fe-PEG-HER2 NP:
-
中空シリカ-Fe-ポリエチレングリコール-ヒト上皮成長因子受容体2ナノ粒子
- LDH:
-
乳酸デヒドロゲナーゼ
- MMP:
-
ミトコンドリア膜電位
- MPA-NP:
-
メルカプトプロピオン酸でコーティングされたMNP
- NADP + / NADPH:
-
ニコチンアミドアデニンジヌクレオチドリン酸酸化/還元
- NF-κB:
-
核因子-κB
- N-NP:
-
夜の花を模倣した金属ナノ粒子
- NP:
-
ナノ粒子
- O 2- :
-
反応性スーパーオキシドアニオンラジカル
- pDNA-PEI-CeO NP:
-
pDNA-ポリエチレンイミンCeOナノ粒子
- PtAuNRs:
-
PtコーティングされたAuNR
- PVP:
-
ポリビニルピロリドン
- ROS:
-
活性酸素種
- SiO 2 -MNP:
-
アミノ化シリカを含むMNP
- tRNA:
-
RNAを転送する
ナノマテリアル



