リポソームナノメディシン:癌治療におけるドラッグデリバリーへの応用
要約
急速で制御不能な細胞増殖が合併症や組織機能障害を引き起こす疾患である癌の蔓延の増加は、科学者や医師の深刻で緊張した懸念の1つです。今日、癌の診断、特にその効果的な治療は、前世紀の健康と医学における最大の課題の1つと見なされてきました。創薬とデリバリーの大幅な進歩にもかかわらず、それらの多くの悪影響と不十分な特異性と感度は、通常、健康な組織や臓器に損傷を与えるものであり、それらを使用する上での大きな障壁となっています。これらの治療薬の投与期間と量の制限も困難です。一方、化学療法や放射線療法などの典型的な癌治療法に耐性のある腫瘍細胞の発生率は、抗腫瘍薬の特性の革新、改善、開発の強い必要性を浮き彫りにしています。リポソームは、異なる物理的および化学的特性を備えた薬物を保存する能力があるため、ナノメディシンにおける薬物送達および癌治療の適切な候補として提案されてきた。さらに、様々なポリマー、リガンド、および分子を結合することによる化学修飾のためのリポソーム構造の高い柔軟性および可能性は、それらの薬理学的メリットを高めるだけでなく、抗癌剤の有効性を改善するためのリポソームにとって重要な利点である。リポソームは、体内のこれらの抗悪性細胞剤の感度、特異性、および耐久性を高め、ナノメディシンに適用される顕著な利点を提供することができます。さまざまな種類の癌や疾患を治療するための臨床応用に焦点を当てて、リポソームの発見と開発をレビューしました。リポソーム薬の特性をどのように改善できるか、そしてそれらの癌治療の機会と課題も検討され、議論されました。
グラフィックの要約
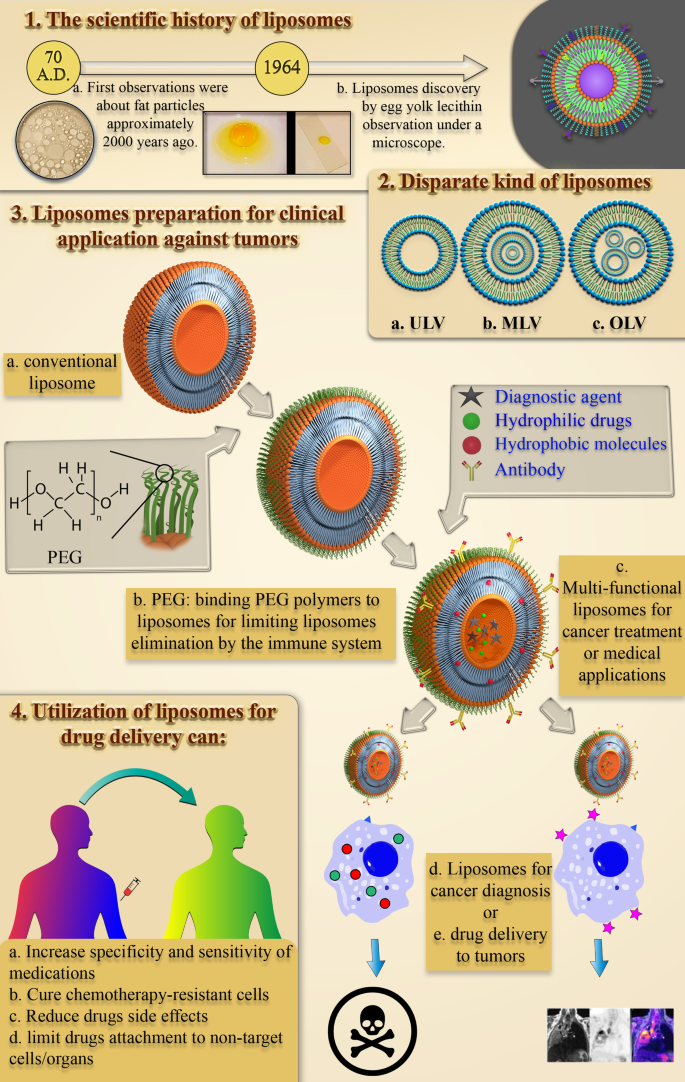
はじめに
健康な体の細胞が正常な状態から抜け出し、制御不能に分裂する病気である癌は、今世紀において大きな医学的課題として認識されています。この合併症は、環境発がん物質または遺伝子変異の蓄積によって引き起こされ[1]、今世紀の大きな医学的課題として認識されています。毎年何百万人もの人々が癌のために亡くなり、新しい患者の数と死亡率は継続的に増加しています[2]。世界保健機関(WHO)の報告によると、2018年の死亡原因は癌が2番目に多く、その年に約960万人がさまざまな癌で死亡したと推定されています。 2018年には、6人に1人の死亡がほぼ癌によって引き起こされました。癌による死亡の約70%は、発展途上国と低所得国で発生しています。ただし、先進国におけるがんの発生率と致死率も考慮する必要があります[3]。
抗腫瘍剤による化学療法は、癌の重要な治療法であることが知られています[4]。適切な感度と特異性が欠如しているため、遊離薬物による化学療法は制限されています。結果として、この制限は副作用による正確な治療を妨げ、十分な抗腫瘍効果の発揮を阻害しました[5]。併用療法である化学免疫療法も、従来の薬剤に耐性のある腫瘍細胞を明示的に治療する、癌治療の効果的で有望な方法として提案されています。近年、さまざまな従来の高度な治療法が発見され、癌の治療に適用されています。一例として、従来の抗がん剤、特に化学療法剤の副作用を軽減するために、ウイルスナノ粒子(VNP)[7、8]、量子ドット[9]、ポリマーナノ材料[10]、およびリポソームを含むさまざまなナノ医薬品[6] [11]が適用されました。
さまざまなナノメディシンの中で、球状ナノ粒子(NP)としてのリポソームは特定の構造を持っています。リポソーム成分中に2つの水相および有機相が存在することにより、両方の種類の親水性および疎水性薬剤の捕捉が可能になり、多くのナノキャリアよりもリポソームに顕著な利点がもたらされる。抗腫瘍薬の特異性、バイオアベイラビリティ、および生体適合性を高める方法の1つは、抗腫瘍薬をさまざまな種類のリポソームに閉じ込めることです[5]。過去20年間にわたって、治療目的でリポソームを利用するために多大な努力が払われてきました。 DaunoXome®やCaelyx®などのこれらの薬剤の中には、一般的および臨床的用途で承認されているものもあれば、最終的な製造および承認段階にあるものもあります[12]。
一般に、免疫リポソームやpH感受性リポソームなど、さまざまな種類の治療用リポソームがあります。免疫リポソームは、標的化ドラッグデリバリーシステム(DDS)としても知られるナノ医療デバイスの大きなグループであり、研究や研究で重要な抗悪性効果を示しています[13]。 pH感受性リポソームは、多形性リポソームのグループとしても知られており、pHの変化によって構造と構成分子が変化し、薬物含有量が放出されます[14]。さらに、リポソームは、他のナノメディシンと同様に、ドラッグデリバリーシステムに加えて、組織の修復と再生、イメージング、および診断に利用できる可能性があります。さまざまな側面でリポソームを使用すると、病気や癌の特定、管理、治療が簡単になります[15]。
この記事では、リポソームの発見と構造、リポソームのさまざまな特性、および市場に出回っている癌治療用のリポソーム薬とその開発に関する調査結果の要約を示します。最終的には、リポソームナノメディシン利用の機会と課題に関するレポートが締めくくられます。これは、科学者の将来の研究で注目すべき重要な問題として強調され、制限の除去とプラスのポイントの強化につながります。
本文
リポソームの科学的歴史:発見と定義
水性環境における小さな脂質粒子の構造と挙動に関する初期の研究から、米国FDAが承認した最初の脂質ベースのドラッグデリバリーナノ粒子まで、約1950年かかりました。アクアでの脂質と脂肪粒子の挙動を研究するプロセスは、ほぼ2000年前のプリニウス長老による最初の観察から始まりました[16]。 17世紀後半、Anthonie Van Hookによる細胞の発見により、細胞の構造について多くの疑問が生じました[17]。次に、GorterとGrendelは、細胞膜にリン脂質二重層が存在することを発見しました[18]。続いて、シンガーとニコルソンは、細胞膜リン脂質の挙動を説明するために、後に二分子膜モザイク膜モデルについて説明しました[19]。これらの科学的観察と仮説は、他の科学者の注目を脂肪由来のNPに引き付けました。 1960年代に、バブラハム研究所で血液凝固プロセスに対する脂質、特にリン脂質の影響を研究したAlec D. Bangham [20、21]は、最初のリポソームを偶然に観察し、自発的な球状粒子が形成されるのを見て驚いた。水[22]。その後、バンガムの研究結果を知っていたアレック・バンガムの研究室の訪問者であるジェラルド・ワイスマンは、アレックが観察したスメクティック・メソフェーズを「バンガム」ではなく「リポソーム」と呼び、ノーベル賞を受賞した[22]。リポソーム発見の科学的歴史は図1に要約されています。
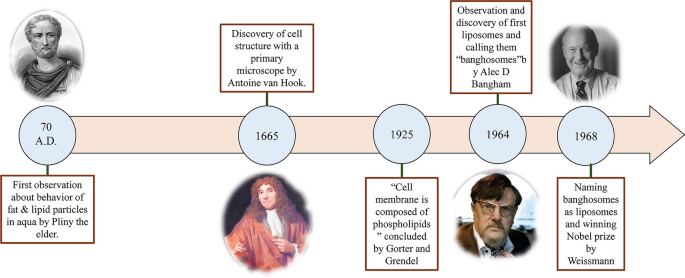
リポソームの発見につながった観察の図。水中の脂質と脂肪粒子の挙動を研究する歴史的および科学的傾向と、リポソームの発見につながる観察、およびイベントに関与した科学者の画像、プリニー・ザ・エルダー[23]、アントニー・ヴァン・フック[24]、アレックD.バンガム[25]とジェラルドワイスマン[26]、それぞれ左から右へ
現在、リポソームナノ粒子として知られている構造は何ですか?
リポソームNPを定義し、それらの特性を合理的に発見するための熱心な努力があります。現在、リポソームは、脂質二重膜と親水性コアからなる、自発的に形成される球状の断片として定義されています。
リポソームのサイズは、約10nmから2500nm(または2.5 µm)の範囲で異なります[15]。ただし、ドラッグデリバリー用に投与されるほとんどのリポソームは、通常、サイズが約50〜450nmです。確かに、はるかに大きな寸法のリポソームは、医療用途にも利用できます[27]。さらに、リポソームは主にリン脂質で構成されています。リン脂質は脂質の一種であり、興味深いことにトリグリセリドに似ています。リン脂質の構造には、親水性の極と2つの疎水性の鎖があります。したがって、リン脂質は両親媒性分子と見なされます。
リン脂質のリポソーム膜には、主にホスファチジルコリン(PC)、スフィンゴミエリン(SM)、ホスファチジルセリン(PS)、ホスファチジルエタノールアミン(PE)が含まれ、両親媒性で水中で特定の構造を形成する傾向が強い[28]。この現象の物理的な理由は、リン脂質に親水性のヘッド(リン酸分子)と2つの疎水性のテール(脂肪酸)が共存していることです。リン酸基はH 2 と相互作用します O極性分子、疎水性テールは水分子から逃げ出し、相互作用します[29]。この場合、非極性鎖は互いに反対側に配置されて二重層を形成し、それらの間に親油性の空間を作り出します。したがって、リポソームのこの親油性部分構造は、疎水性薬剤および材料を貯蔵するために適用することができる。さらに、リン脂質の親水性セクションは、水素結合、ファンデルワールスなどの分子間力を介して水分子に向けられます。これらは、リポソーム内に親水性領域を形成することにつながる。卵黄に豊富に含まれ、水中やリポソームのさまざまな領域でリポソームを形成できる天然リン脂質としてのレシチン分子の構造を図2に示します。
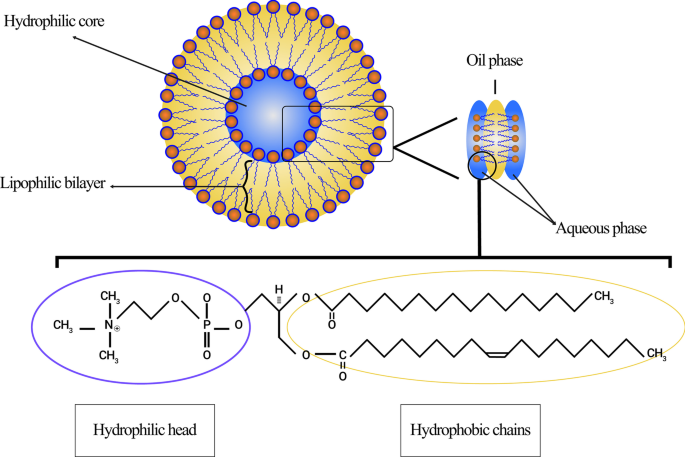
レシチンに由来するリポソームの概略図。親水性コアと疎水性二重層を含むリポソームのさまざまな領域が示されています。レシチン分子の構造、その親水性極、および疎水性鎖が指定されています
同様に、分子の種類、水性媒体の温度、モル濃度、およびイオンなどの他の物質の存在に応じて、水に溶解した後のリポソームの球状構造がその最終的な形状を決定します[30]。リポソームの主な物理的および化学的属性は、その構成脂質、特にリン脂質およびそれを構成する他の分子の正味の特性です。これらの特性には、透磁率、表面電荷密度、および全体のサイズが含まれます[31]。
異なるタイプのリポソーム分類
リポソームの発見以来、これらの構造は、生物学的、生物物理学的、生化学的、または製薬研究の重要な部分として常に利用されてきました。
今日、リポソームは、そのサイズ、リン脂質二重層の数、合成手順、および調製メカニズムに基づいて分類することができます。サイズに関して、リポソームは、小、中、大の3つのグループに分けることができます。膜層の数を考慮すると、それらは単層ベシクル(ULV)、オリゴラメラベシクル(OLV)、および多層ベシクル(MLV)である可能性があります。この点で、ULVは約50〜250 nmの1つのリン脂質二重層で構成されるリポソームですが、MLVははるかに大きく約0.5〜1.5 µmであり、いくつかのリン脂質二重膜が含まれています[32]。合成方法が異なると、これら2つのグループ間にマージンが生じます。アプリケーションの観点から、ULVは内部にも大きな親水性環境を持っているため、親水性薬物の捕捉に適しています。 ULVのような小さな単層ベシクル(SUV)は、1つのリン脂質二重層で構成されていますが、寸法の点では、サイズが100 nm未満です[33、34]。形態学的観点から、OLVは、同一または異なるサイズの2〜5個の小胞で構成されるリポソームです。 OLVの構造では、小胞はすべて、互いに内部に存在することなく、1つの大きなリン脂質二重層に囲まれています。 OLVは通常、約0.1〜1 µmです[33,34,35]。 ULVとは対照的に、MLVは親水性物質の送達には理想的ではありません。 MLVは主に疎水性物質の送達に利用されます[36]。さまざまな種類のリポソームを図3に示します。
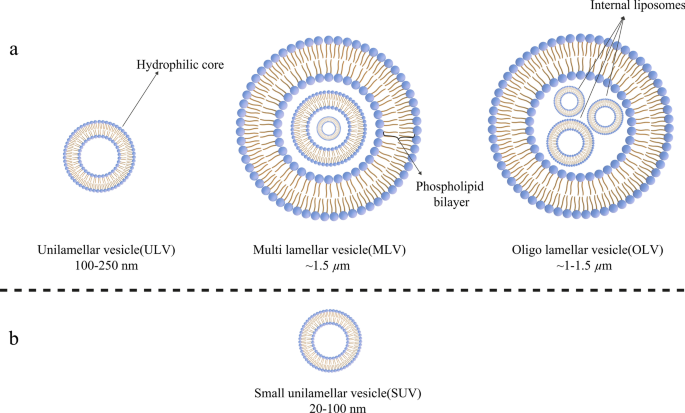
さまざまな基準によるリポソームの分類: a リポソームはサイズの点で3つのカテゴリーに分けられます。 b 目立った小さなサイズの単層ベシクル(ULV)のメンバーとしての小さな単層ベシクル(SUV)構造
リポソームの調製方法と新世代の開発
ハードNPとしての金ナノ粒子とは対照的に、リポソームはソフトNPであり[37]、さまざまな方法で合成できます。たとえば、MLVとULVには、異なる準備メカニズムがあります。これらの方法のほとんどでは、特定の溶媒(クロロホルムやメタノールなど)を使用して、丸底フラスコ(RBF)でリポソーム膜(目的のモル比)を形成することを目的とした脂質を溶解します。たとえば、ハンドシェイクはMLVを合成するための主要な手順です[38]。脂質膜の水和としても認識されるこの手順の間に、脂質が有機溶媒に添加されます。次に、回転装置により溶媒を蒸発させ、固体生成物を脂肪分解する。最終的に、リポソームは水和および押し出し法[39]に従って合成されます。リポソーム合成の他の方法には、超音波処理、逆相蒸発、フレンチプレッシャーセル、凍結乾燥、および膜押し出しが含まれます[38、40]。
さらに、リポソームは、経時的な発見と開発に基づいて、さまざまなカテゴリーで注文することもできます。第一世代のリポソームは、一般的に従来型または古典的なリポソームと呼ばれています。従来のリポソームを治療用NPとして使用した場合に観察された問題は、invivoで非常に迅速に特定されました。初期に検討された問題の1つは、リポソームへの薬物の捕捉の制限でした。言い換えれば、多くの薬剤は第1世代のリポソーム内に保存することができませんでした[41]。安定性、治療効果、臨床応用の可能性など、リポソームの構造と特性を調査したいという大きな願望に加えて、これらの課題は、構成脂質、表面電荷、正味重量を変更することにより、第2世代リポソームの開発につながりました。および総量[42]。正確には、第2世代のリポソームは、主に従来のリポソームに親水性ポリマーを添加して体液中での貯蔵寿命を延ばし、ドラッグデリバリーシステムの適切な候補にすることで合成されます。この種のリポソームは、非特異的長期循環リポソームまたはリガンド標的化長期循環リポソームの2つのグループに分けることができます[43]。
新世代のリポソームとしての古細菌は、古細菌の膜脂質と合成リン脂質類似体で構成されています。過去10年間で、薬物およびワクチンの送達に使用されるアーキオソームの可能性を調査するために、広範囲にわたるかなりの努力がなされてきました。古細菌型脂質の構造核は、約20〜40個の炭素を含む飽和フィタニル鎖を持つジエーテルまたはテトラエーテル分子です。これらの炭素鎖は、アーキオールまたはカルドアーキオールに見られる骨格グリセロールのsn-2,3炭素のエーテル結合に結合します。上記のように、これらの粒子は、腫瘍性合併症、アレルギー、感染症、およびワクチン接種のためのドラッグデリバリーにも非常に使用できます[44]。
リポソームの生体材料特性と物理化学的特性の評価
先に述べたように、医学の進歩にもかかわらず、いくつかの病気、特に癌の治療は、非効率的な治療薬と方法のために、依然として手ごわい課題に直面しています。腫瘍に影響を与えるために注射された薬剤の投与量を調整することは、抗癌剤の治療ウィンドウが狭いため、緊張した問題です。言い換えれば、治療用量と毒性用量の間のわずかな距離、および不適切な感度と特異性により、高度な治療手順に対する大きな需要が生まれました[42]。
さらに、組織への薬物送達のためのナノ材料の利用が最近注目を集めている。生体適合性と生分解性は、デリバリーシステムでナノマテリアルを利用するための生体材料特性からの2つの重要な特徴です。生体適合性は、治療用NPが体の組織やシステムに損傷を与えるのを防ぐために必要であり、生分解性はNPを非毒性化合物に分解し、臓器から簡単に取り除くために急務です[15]。リポソームの検出後、科学者はそれらをドラッグデリバリー用のナノ材料として適用し始めました。言及されているように、リポソームは、治療目的のために2つの必要な生体材料特性を持っています:生体適合性と生分解性[36]。また、リポソームNPには、この目的に適した他の特性があります。例えば、リポソームの特定の構造のために、親水性(水溶性)および疎水性(脂溶性)薬物の両方のグループをそれらにカプセル化することができます。さらに、リポソーム中のリン脂質二重層膜の存在は、酵素分解、免疫学的構造による生物学的不活性化、およびインビボでの化学変化などの様々な現象および損傷からリポソームに保存された薬剤を保護する。この点には2つの重要な長所があります。1つは、リポソームに閉じ込められた分子の構造が標的組織に到達する前に保存され、修飾が行われないこと、2つ目は、他の健康な非標的組織が曝露から保護されることです。リポソーム膜による薬物であり、これらの薬剤の影響を受けることはありません[42]。リポソームは、DNA、RNAなどの遺伝物質の送達や遺伝子治療の目的にも適用できます。この目的で使用されるリポソームは、カチオン性、アニオン性、中性脂質、およびリン脂質またはそれらの混合物で構成することができます[45]。カーボンドットなどのいくつかの診断薬および造影剤は、リポソームの組み合わせまたは単独での癌の検出および画像化に利用することができます[46]。カーボンドットは臨床応用のために部分的に承認されており、調査で利用されていますが、細胞毒性はそれらの幅広い応用にとって依然として挑戦的な障壁です[47]。リポソーム薬物NPの一般的な構造を図4に示します。
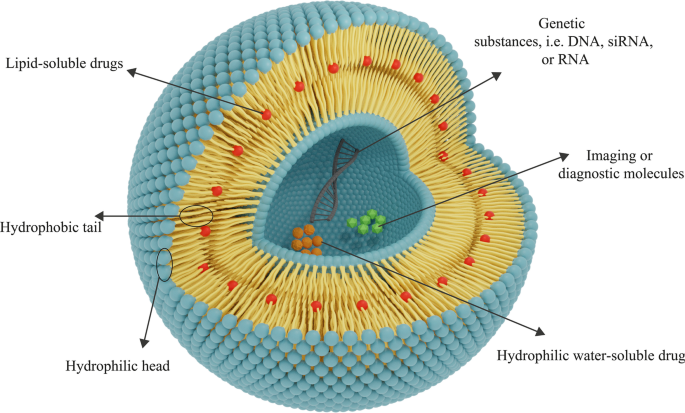
リポソームの一般的な構造は、リン脂質層で構成されています。薬物の親水性-疎水性に応じて、その送達に適切な種類のリポソームが決定されます。親水性薬物は中央の親水性核に閉じ込められ、疎水性薬物は親油性領域に配置されます。リポソームは遺伝子の送達にも利用できます
リポソームに存在する膜形成リン脂質は非毒性の化合物であり、広範囲のサイズで合成することができます。リポソームの物理化学的属性は、それらの成分に依存しています。したがって、コレステロール、ポリエチレングリコール(PEG)などの特定の化合物を添加することにより、目的の特性を持つリポソームを合成できます。さらに、リポソームの膜は巨大分子に対して不浸透性であり、リポソーム内の物質をよりよく保持するのに役立ちます[48 ]。リポソームの言及されたすべての特徴は、様々な疾患、特に癌を治療するための治療薬の送達における利用のための適切なナノ材料としてそれを導入します。
グレゴリー・グレゴリアディスは、この分野の先駆的な研究者の1人として、薬物送達システムにリポソームを使用するという仮説を提案し、薬物化合物がリポソームに閉じ込められる可能性があると述べました[49]。リポソームの適切な生体材料および物理化学的特性が報告されています。一例として、動物モデルで使用される抗腫瘍薬シトシンアラビノシドを含むリポソームに関する調査は、L1210白血病によるマウスの寿命の有意な増加を示しました[50]。リポソームを適用することにより、十分な量の活性型の薬物を保護された方法で標的部位に送達することができます[42]。
治療用途におけるリポソームNPの特異性と感度の向上
前述のように、さまざまな分子やポリマーを使用することで、リポソームの構造や膜を変化させることができ、これにより、リポソームに新しい機能を追加したり、その特性を変更したりすることができます[51]。血液中のリポソームの循環を延長することと、EPR効果を介して特定の腫瘍組織または病理学的部位に蓄積する能力を高めることの両方が、リポソームのクリアランス率が高いために考慮すべき最初の重要な特徴です。化学的コンジュゲーションによるリポソーム膜へのPEG分子のコンジュゲーションは、この機能をリポソームに追加するために順次使用されてきました[52]。リポソームの半減期の延長におけるエチレングリコールポリマーの重要性と役割、特に血液などの体液中のリポソーム治療用NPは、約20年前に表明されました[53]。
AbuchowskiとMcCoyは、PEGをそれらの構造に結合させることにより、血流中のリポソームの半減期を延長する最初の試みを行いました。その結果、彼らの努力は一般的にリポソームの循環時間と血流中のそれらの半減期を増加させました[54]。数ヶ月後、他の研究者は、単核貪食細胞(MPS)によるリポソームの高速クリアランスを低下させる可能性を調査しました。リポソームの表層分子にPEGを付着させることにより[53]、血液中のリポソーム循環の改善が期待されます。この分野には多数の記事があります。さらに、従来のリポソームとは異なり、PEGでコーティングされたリポソームは用量に依存しない薬力学特性を示しました[55]。さまざまなポリマーの中で、PEG分子はリポソーム表面に付着してinvivoでの貯蔵寿命を延ばすことができるポリマーの1つです。他のポリマーもこの目的に使用できます[56]。図5は、PEGポリマー分子がリポソームを抗体から保護し、血流中での寿命を延ばす方法を示しています。
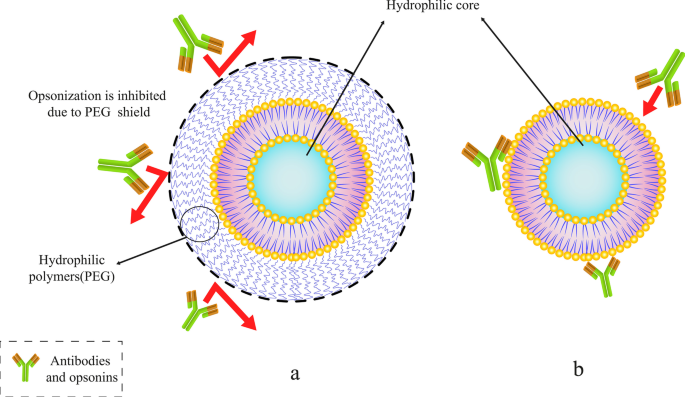
ポリエチレングリコール(PEG)などの特定のポリマーをリポソームに結合させます。 a PEGポリマー分子を含むPEG化リポソームはシールドします。 b 抗体とオプソニンによってトラップされた従来のリポソーム
前述のように、PEGに加えて、他の分子を利用してリポソームの循環を延長できることは注目に値します。さらに、ポリオキサゾリンポリマーは、リポソーム膜を修飾してそれらの半減期を延長するために使用される物質の中にある。この点で、Woodle etal。ステルスリポソームを合成するためにポリ[2-エチル-2-オキサゾリン](PEOZ)を適用した最初のグループでした。彼らの結果は、肝脾細胞によってラットに注射されたポリ[2-エチル-2-オキサゾリル化] PETOX化リポソームの除去と取り込みの減少を証明しました[57]。彼らの結果は、ポリ[2-エチル-2-オキサゾリン]やポリ[2-メチル-2-オキサゾリン](PMOZ)などの他のポリマーの結合が、半減期の延長とインビボでのリポソームの循環。彼らはまた、さまざまな臓器やシステムにおけるPEG、PEOZ、およびPMOZ結合リポソームの生体内分布を比較しました。結果はまた、血液と脾臓におけるこれらすべてのリポソームの生体内分布がほぼ同じであることを示しましたが、肝臓では、PMOZの分布は他のものよりはるかに低かった[57]。
痛み等。デキストラン分子をULVの表面に結合させた。彼らの結果は、デキストラン結合リポソームが、従来のリポソームと比較して、より拡張された循環を有し、肝臓および脾臓によるより低い吸収および取り込みを有することを示した。この結果は、体内のリポソームの貯蔵寿命を延ばすだけでなく、デキストラン分子が安定性を高め、リポソームからの薬物放出速度を調節するためにも適用できることを証明しました[58]。
注意すべき2番目の問題は、リポソームの流動性と安定性です。コレステロールを含む他の脂質は、リポソームの枠内で使用することができます。コレステロールは、リポソームのいくつかの特性を強化するために、リン脂質二重層のいくつかの化合物の代わりに使用される場合があります。それにもかかわらず、リポソーム二重層の含有量を変更し、リン脂質分子の一部を特定の化合物、特にコレステロールで置き換えると、リポソームの流動性が低下する可能性があることが証明されています[59]。さらに、リポソームの膜にコレステロールが存在すると、それらの構造の安定性が向上します(invivoおよびinvitro実験の両方)。また、透過性が低下し、閉じ込められた物質が漏れる可能性が低くなります。コレステロールは、リン脂質二重層間の疎水性鎖と相互作用して、リポソームの膜に存在するときにその構造を安定化させる疎水性ステロイドです。コレステロールのこの作用は、リポソームが体内で高密度リポタンパク質(HDL)および低密度リポタンパク質(LDL)に変換されるのを防ぐため、invivoでリポソームを臨床的に利用する場合に重要です。さらに、血液および細胞内液に存在する脂質構造は、リポソームに印象を与える可能性があります。 LDLやHDLなどのリポタンパク質は、注入されたリポソームに影響を与え、脂質の移動と膜の再配列を引き起こします。それらはまた、薬物含有リポソームNPの安定性を劇的に低下させます[12]。 DNAや治療用途のリポソーム膜で利用される他の分子などの他の材料は、膜内のコレステロールに固定されなければならないことに注意してください。リポソーム膜にさまざまな物質を加えることは、リポソームにポジティブな特徴を作り出す1つの方法です[42]。
考慮すべき3番目の重要な特徴は、正確な同定と標的細胞への特異的結合のためのリポソームの感度と特異性です。モノクローナル抗体などの化合物を結合することにより、F ab フラグメントおよびトランスフェリンや葉酸などの他の結合分子は、リポソームの特異性を高めることが可能であり、腫瘍細胞への特異的結合をもたらします[60]。さらに、薬物ナノキャリア、特にリポソームの特異性と感度の向上が以前に調査されました。たとえば、Mohammad J. Akbar etal。小細胞肺癌(SCLC)を治療するためにペプチド-PEG-脂質結合リポソームを研究しました。彼らの結果は、ガストリン放出ペプチド受容体(GRPR)アンタゴニストペプチドをリポソームに結合させると、GRPR発現細胞におけるこれらのリポソームの特異性と蓄積が増加する可能性があることを示した。彼らはまた、ペプチドに付着したこれらのリポソームは、それらのGRPR発現遺伝子のアップレギュレーションのために肺癌細胞を治療するために適用できると主張しました[61]。
最終的に、適切な特性のために、薬物および薬物がPEG化リポソームに追加され、現在、これらのリポソーム構造は、産業臨床利用のために確立されています[62]。抗体はまた、標的細胞に結合するリポソームの能力を高めるために初期の研究で使用されました[63]。この場合、受容体を介したエンドサイトーシスはリポソームによって行われ、細胞に侵入しました[64]。一方、抗体をリポソームに結合させるための様々な方法が開発されてきた[65]。抗体結合リポソームに関する研究は、培養腫瘍細胞に対する抗癌剤の毒性が、リポソーム表面への抗体の結合とともに増加することを証明した[66]。抗体がPEGリポソームの表面に適用された場合、特にPEGに付着した側鎖が長い場合、それらの標的受容体に付着する抗体の遺物はPEGポリマーによって覆い隠されました[67]。したがって、リポソーム薬用のPEGと抗体の同時使用とその欠点は、科学者が検討する必要があります。
リポソームの治療への応用における4番目の重要な要素は、リポソームに閉じ込められた薬物の放出のエチュードです。損傷した組織の異常な状態によって影響を受けるそれらの内部の薬物の脱出のためのリポソームの調整は、リポソームを臨床的に投与する際の重要な問題の1つです。さらに、標的細胞の組織および膜表面に結合することができるリポソームの表面における温度感受性化合物、pH、または特定の代謝産物の使用は、これらの薬物を正確に放出する方法である。この方法を利用すると、標的細胞の膜表面にリポソームの特定の効果をもたらし、それらの内部の薬物含有量を放出することもできます[68]。
リポソームNPに捕捉された化合物の放出速度は、標的部位で利用可能な薬物の用量を調整するための5番目の実質的な基準です。リポソームを含むあらゆる種類のドラッグデリバリーシステムを適切に使用するために考慮すべき重要な目的の1つは、薬物の放出速度と規制です。リポソームドラッグデリバリーシステムおよびNPに関しては、リポソームにカプセル化された物質は生物学的に利用可能ではなく、初期状態から放出されている間のみ生物学的に利用可能であることに言及する価値があります。したがって、薬物含有リポソームは、癌性組織に生物学的に利用可能な薬物の濃度を高め、治療の質を改善する能力を提供することができ、リポソームからの薬物放出の速度が調整されるという条件で治療効果を達成することができる[69]。さらに、リポソーム二重層の含有量を変更し、一部のリン脂質を特定の化合物、特にコレステロールなどのステロイド分子に置き換えると、それらに保存されている化合物の透過性と意図しない漏出が減少する可能性があることが証明されています[70]。したがって、この利点を利用して、カプセル化された化合物の放出速度を調整することができます。放出されると、薬物は細胞に十分に浸透し、それらの影響を与えるために必要な生理学的生化学的変化を起こさなければなりません。
先に述べたように、アプタマーを含む様々な化合物をリポソームに結合させることができる。この点で、Mohammad Mashreghi etal。 Caelyx®リポソームを機能化するためのアプタマーとして抗上皮細胞接着分子(抗EpCAM)を適用しました。彼らの実験結果は、このアプタマーによるCaelyx®の機能化がこのリポソーム薬のメリットを高め、癌治療の実行可能な選択肢にする可能性があることを決定しました[71]。図6は、invitroまたは臨床科学目的で使用されるさまざまなタイプのリポソームの構造を概略的に示しています。
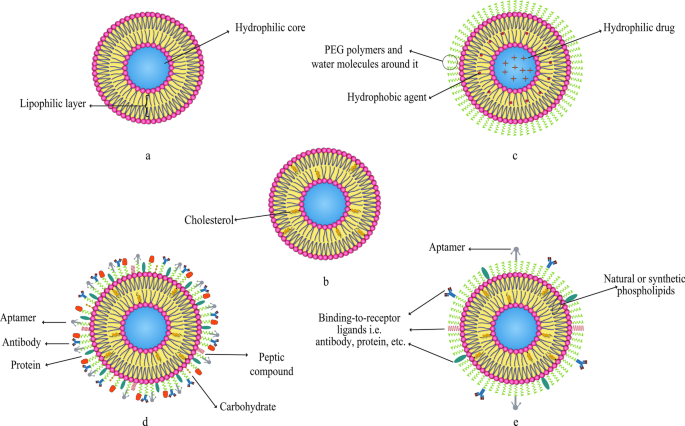
各種リポソーム。 a 従来のリポソーム; b コレステロール結合リポソーム; c PEG化またはステルスリポソーム; d リガンド標的化リポソーム; e 多機能リポソーム
リソソームを通過して細胞(低pHで多くの分解酵素を含む)に入る薬物の通過は、リポソームへの共役薬の実用化にとって6番目に重要な要素です。細胞外および細胞内空間での望ましくない変換から治療薬を保護するために、細胞透過性ペプチドがリポソーム表面に付着します[72]。
リポソーム薬物薬理学について:薬物動態学と薬力学
医学および製薬科学の本質的な部分としての薬理学的属性の評価は、薬物担体としてのリポソームの長所と短所をよりよく理解するためだけでなく、臨床試験でそれらを確認および評価するためにも必要です。リポソーム薬物の薬理学的特性およびそれらの身体との相互作用は、薬物動態(治療化合物に対する身体の効果)および薬力学(薬物がどのように作用し、身体および細胞経路に影響を与えるか)の2つのさまざまな側面で調べることができます[73]。一般に、癌治療または他の障害における薬物送達のためのリポソームの利用は、一方ではこれらの薬剤の有効性を高め、他方では正常組織に対するそれらの毒性を低減することを必要とする。 NPベースの薬物の適切な投与経路、血流および半減期におけるそれらの循環、組織におけるそれらの生物学的分布、およびそれらの細胞代謝、ならびにそれらの排除、代謝およびクリアランスなどの主題が、この分野で研究されてきた。薬物動態学[74]。リポソームの薬物動態は、主に、さまざまな体液および組織におけるリポソーム結合薬のバイオアベイラビリティを研究します。確かに、化学分解と生物学的排泄、およびリポソームの取り込みと精製の研究も薬物動態学で考慮されています。遊離薬物の代わりにリポソーム薬物を使用することの薬理学的利点に関する研究の結果(DDSに適用されるリポソームのタイプに関係なく)は、次のことを示しました:
主に、リポソームは薬物放出プロファイルを持続放出に変更することができ、その結果、一定の注射の必要性を減らすことができます。第二に、それは血流および体液中の薬物の存在を延長し、その結果、その半減期を増加させる可能性があります。第三に、健康な毛細血管の内皮を通過する粒子サイズが限られているため、健康な組織への薬物の影響を減らしながら、癌性組織でのより良い生体内分布につながる可能性があります。最終的には、薬物代謝物のクリアランスに対するプラスの効果に加えて、標的組織に到達する前に血漿中の薬物代謝と不活化を低減します[75、76]。
ただし、リポソームの溶解性、特異性、および感度を高めるには、リポソームの薬物動態にいくつかの変更が必要です。これらの変更により、化学療法抵抗性細胞を克服し、有効性と半減期を高めることができます。さらに、それらの代謝の結果としてのそれらの毒性または意図しない代謝化合物生成物は、これらの修飾によって減少するはずです[77]。
リポソーム薬の投与を消費した後、それらは体内に入り、特定の半減期で血流を循環します。それらのサイズと形成的組成は、リポソーム薬の半減期を決定します。さらに、リポソーム薬物の体内からの迅速なクリアランスは、それらの作用期間および治療指数を低下させる可能性があります。前述のように、リポソームにPEGなどの親水性ポリマーを添加すると、それらのクリアランス速度を低下させ、この課題を解決することができます[78]。また、コレステロール分子を添加することにより、リポソーム膜の流動性と薬物放出速度を調整することが可能です。
薬物送達のためのリポソームの適用は、薬物の薬物動態にいくつかの変化をもたらす可能性があります[79]。リポソームがさまざまな薬物および薬物の薬物動態特性を変化させる能力は、薬物送達システムにおけるそれらの重要な利点の1つです[80]。リポソームのクリアランスと除去のプロセスに関しては、リポソーム構造が投与後に血漿タンパク質の影響を受けることは明らかです。例えば、リポソームナノ粒子の注入後、オプソニンはリポソームの表面に吸着されます。オプソニンは血漿タンパク質であり、主に免疫グロブリンとフィブロネクチンが含まれています[42]。リポソームの表面にオプソニンが存在すると、血液や体液からのさまざまな薬物の重要な除去セクションの1つとして、MPSによるオプソニンの除去が行われます。それらはまた、オプソニン-リポソーム複合体への補体C3bおよびFcなどのいくつかの受容体の付着を介してリポソームを除去します[81]。肝臓のクッパー細胞、脾臓、骨髄、リンパ節に存在するマクロファージなどのさまざまな組織や細胞が、リポソームNPのクリアランスに関与しています[82]。
国際純正応用化学連合(IUPAC)の定義によると、薬力学とは、化合物が生体系に及ぼす薬理学的影響と、これらの影響の生化学的および生理学的影響の研究を指します[83]。リポソームにカプセル化されたときに治療薬を特定するための溶出の増加は、リポソーム利用の薬力学的利点の1つとして認識されています[84]。
さらに、物理化学的特性は、リポソーム薬の薬理学に大きな影響を及ぼします。粒子サイズ、膜の電荷、および膜脂質の組成は、薬剤の薬物動態および薬力学に影響を与える可能性のあるこれらの物理化学的特性の一部です。第一に、リポソームを含むナノ粒子の粒子サイズとそれらのクリアランス速度の間には直接的な関係があります。 NPのサイズを大きくすることにより、免疫系とMPS細胞によるそれらの除去率も向上します[85]。第二に、リポソーム膜の正味電荷は、リン脂質およびそれらを構成する他の構成粒子の電荷の結果であることに言及する価値があります。結果として、膜電荷の上昇は、これらの薬剤のクリアランス速度の向上に関連しています[86]。膜脂質の組成やその他の構造的特徴(親水性のコア半径など)も、リポソーム薬の薬物動態に著しく影響します[87]。
さらに重要なことに、異なるタイプのリポソームは、それらの様々な構造に応じて、異なる薬物動態/動力学を示すという仮説が立てられています。薬物放出速度は、リン脂質二重層の数とロードされた薬物化合物の含有量にも依存します。また、流体力学的直径、総体積、およびその他の薬物動態特性にも依存します[88]。
リポソーム薬の投与経路
多くの異なる薬と同様に、NPベースのリポソーム薬はさまざまな経路から投与できます。言い換えれば、経口摂取[89]と、静脈内(I.V.)投与やさまざまな局所注射などの別個の注射方法が、リポソーム薬の一般的な投与経路の1つです[90]。ナノ粒子は薬物のバイオアベイラビリティを高め、細胞との相互作用を改善し、酵素による薬物の分子構造の変化を防ぐため、経口投与による薬物送達のためのリポソームを含むナノ粒子の使用は、効果的な戦略として強調されています。胃腸管の胃液。さらに、それらは、粘膜および表皮層への修復分子の放出を増強するだけでなく、初回通過効果の間の望ましくない変化から薬物を保護する能力を有する[89]。静脈内注射は、FDAまたは他の当局によって承認された多くのリポソーム薬の主要な投与経路として使用されています[42]。一方、局所注射のタイトルで分類される皮下(SC)、皮内(ID)、腹腔内(IP)、および筋肉内(IM)も、リポソーム薬の投与に利用されます[90,91,92]。 。
リポソーム薬のinvivoでの運命とその作用機序
リポソーム薬の投与後、血流を介して標的部位の病理学的病変に到達し、そこに蓄積します。腫瘍に対するリポソーム薬物の作用機序は、標的部位でのそれらの蓄積、腫瘍細胞によるそれらの取り込み、および遊離薬物の放出から始まります[93]。体内に入った後、リポソーム薬はさまざまな標的作用メカニズムを介して腫瘍に到達し、さまざまな方法で細胞と相互作用します[94]。一般に、腫瘍標的化メカニズムは、受動的標的化と能動的標的化の2つのカテゴリーに分けられます。受動的標的化とは、リポソームが腫瘍部位に自発的に蓄積され、特定のリガンドの存在なしに標的細胞と相互作用するメカニズムを指します[95]。強化された透過性と保持(EPR)の効果は、最も重要なパッシブターゲティングメカニズムとして提案されています。正確には、腫瘍部位での治療用NPおよびリポソーム薬の自発的蓄積はEPR効果と呼ばれます[96]。この現象は、通常の組織毛細血管とは異なり、腫瘍組織血管の漏出性に起因する可能性があり、分子やNPに対して透過性があります。その結果、これは最終的にこれらの組織における薬物化合物の蓄積とEPRの効果につながります[97]。腫瘍細胞の細胞内液および細胞質における薬物の最終的な運命は、放出メカニズム、ナノキャリア成分、および分子構造などのいくつかの要因に依存します[98]。健康な組織では、毛細血管の数と形状はそれぞれ比例して正常です。しかし、癌性臓器では、健康な組織とは異なり、血管新生プロセスのために、毛細血管の数と構造がそれぞれ高くなり、変形します。さらに、腫瘍の毛細血管構造が破壊され、内皮の指節細胞が減少します。その結果、細胞間空間に漏れる血漿液の量が増加します。しかし、健康な組織では、毛細血管の指節細胞は細胞の緊密な癒着を保持し、NP、小分子、およびリポソーム薬物が細胞間空間に浸透するのを防ぎます[99]。癌性毛細血管におけるEPR効果と、正常および健康な組織血管との違いを図7に示します。
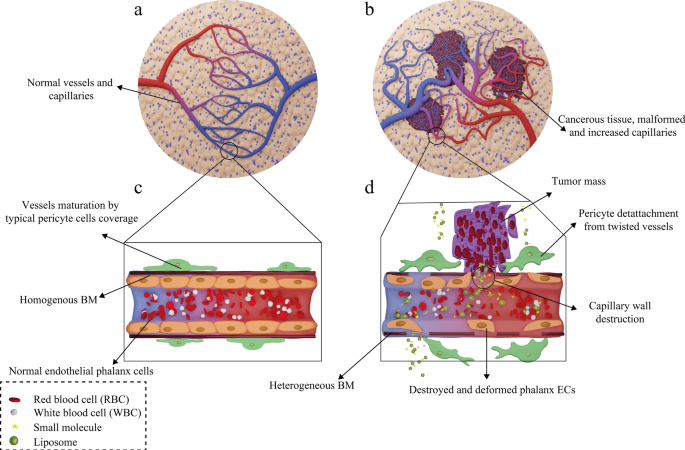
EPR効果を介した腫瘍細胞に対する薬物含有リポソームの作用機序。 a 健康な組織とその正常な毛細血管; b 変形した血管が増加した癌性組織; c 正常で健康な血管の構造; d 腫瘍組織の破壊と変形した毛細血管
一方、能動的ターゲティングは、その適切な有効性と高い特異性により、作用のターゲティングメカニズムの1つとしてかなりの注目を集めています。アクティブターゲティングにはさまざまなタイプが含まれ、一般に、健康な細胞や非標的組織に対するリポソームNPのオフターゲットの影響を減らすことも目的としています[95]。この方法では、モノクローナル抗体、小分子、シグナルペプチド、ビタミン、特定の炭水化物、糖脂質、またはアプタマーなどの分子が、リポソームの表面修飾に一般的に利用されます[100、101]。さらに、アクティブターゲティングは、さまざまな機能に応じてさまざまなサブタイプに分割できます。たとえば、次の2つの一般的なカテゴリに分類できます。
- 1。
腫瘍細胞および癌組織受容体の標的化:この方法は、特定の分子をリポソームの膜表面に結合させ、癌細胞上の特殊な受容体または過剰発現した受容体に結合できるようにすることに依存しています[102]。癌細胞では、さまざまな遺伝子のアップレギュレーションにより、急速な細胞増殖に対する代謝要求の強化に応じて、特定の細胞表面受容体の発現が増加します[103]。アクティブターゲティングでは、特定の分子修飾を適用して、葉酸受容体(FR)、トランスフェリン受容体(TfR)、上皮成長因子受容体(EGFR)などの癌細胞の過剰発現表面受容体を特異的にターゲティングできます[95]。この点で、癌細胞における葉酸受容体の役割は葉酸の取り込みを増加させることです[104]が、トランスフェリン受容体はトランスフェリンに結合し(血清中の重量が80 kDaの遊離分子として)、この単量体糖タンパク質のエンドサイトーシスを引き起こします[104]。 105]。さらに、EGFR受容体は、組織の分化や修復などの細胞プロセスに関与するチロシンキナーゼのクラスです。癌細胞におけるこの受容体の発現は、血管新生、細胞増殖、転移などのプロセスに関与しているため、大幅に増加しています[106]。
- 2。
腫瘍微小環境を標的として利用する:この方法では、リポソームの表面の変化を利用して、癌細胞の微小環境内のシグナルペプチドまたは他の受容体を標的にすることができます。言い換えれば、このアクティブなターゲティングメカニズムは、腫瘍細胞の増殖と転移を抑制し、新生血管内皮細胞の遺伝子型と表現型の変化を防ぎ、薬剤耐性を制御することができます[107]。さらに、血管内皮増殖因子(VEGF)、血管細胞接着タンパク質(VCAM)、マトリックスメタロプロテアーゼ、インテグリンなど、腫瘍微小環境の一部の受容体がこのメカニズムの標的になっています[95]。
治療用NPの細胞取り込みと標的細胞に対するリポソーム薬の効果:作用と相互作用
先に述べたように、リポソームは受動的または能動的に腫瘍細胞を標的にすることができます。リポソームは、ターゲティングメカニズムを介して癌細胞および腫瘍環境に到達した後、その治療内容を放出し、さまざまなメカニズムによってその効果を発揮することができます。その結果、脂質組成、膜の表面電荷、癌の種類、標的細胞の種類、およびリポソーム膜上の特定のリガンドの存在が、細胞とリポソームの相互作用に影響を与える可能性があります[108]。
図8は、さまざまな種類のリポソームと標的細胞との相互作用を示しています。薬物を含むリポソームは、体内に注入された後、血管を通ってさまざまな組織に移動し、最終的には表面のリガンドに基づいて標的細胞に到達します。これらのリポソームは、これらのリガンドを介して細胞受容体に結合することができ、これは比吸収と呼ばれます[42]。とはいえ、受容体を含まないリポソームは、分子引力、静電力、および非特異的吸収と呼ばれる分子相互作用を介して標的細胞表面に付着することもあります。リポソームが細胞に結合した後、治療薬は細胞質に放出され、その効果はさまざまな方法で生み出される可能性があります。リポソームナノキャリアは、細胞の原形質膜に完全に融合し、薬物を放出することができます。薬物化合物はまた、リポソームから細胞に放出され、融合を起こさずにマイクロピノサイトーシスまたは受動拡散を介して細胞に入ることができる。リポソームは、細胞と直接相互作用するか、タンパク質を介したプロセスを通じて脂質断片を細胞膜と交換する可能性があります。同時に、薬は細胞に作用し、リポソーム薬の治療効果を発揮する可能性があります。ただし、一部のリポソームはエンドサイトーシス(特異的または非特異的)を介して入ることができます。特に、この継代を介して細胞に浸透するリポソームは、様々な運命を有する可能性がある。それらがリソソームと結合することは可能です。このような場合、リソソーム酵素はファゴリソソーム嚢のpHを下げることによって薬物の構造に影響を与えます。最終的に、リポソームはそれを細胞膜またはエンドサイトーシスに融合させることによって薬物を放出し、その後、薬物療法はそれらの治療効果を発揮します[42、62]。リポソームが細胞に浸透してその効果を発揮するためのすべての可能な方法が図8に示され、比較されています。
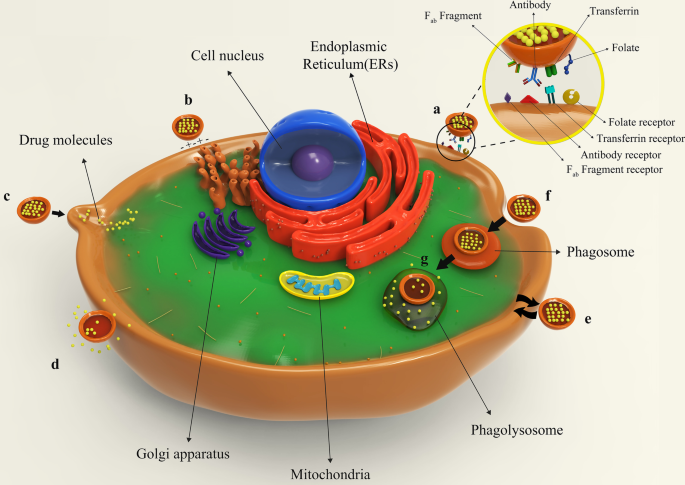
リポソームの標的細胞への結合。 a リガンド-受容体相互作用を介した特異的付着; b 分子内静電力によるリポソームの非特異的吸収; c リポソームの細胞膜への付着および融合および薬物放出; d 標的細胞へのリポソームの到着および融合を伴わない薬物放出; e タンパク質を介したプロセスを通じて、細胞膜とリポソームの間で脂質断片を交換します。 f 標的細胞によるリポソームのエンドサイトーシス; g 細胞質におけるリポソームのリソソーム消化
一方、NPベースの薬剤は、標的細胞によるエンドサイトーシス、飲作用、または食作用を受ける可能性があります。エンドサイトーシスは、細胞空間の外側の化合物が細胞膜に近づき、小胞として細胞に入るプロセスとして知られています[109]。飲作用は、流体エンドサイトーシスとしても認識され、小分子または懸濁液が細胞膜に陥入を引き起こすことによって小胞を介して細胞に導入されたときに発生します。さらに、飲作用は脂肪滴を吸収するためにヒト細胞で広範に発生します。免疫学的研究において、田中百合子等。リポソーム結合抗原の飲作用は、抗原処理細胞(APC)によって実行できると報告されています。この報告は、リポソームが飲作用メカニズムを受けることができることを証明しました[110]。食作用では、0.5 µmを超える粒子が免疫細胞に飲み込まれます。これは、リポソーム(特に、MLVや500 nmを超えるリポソーム)でも発生する可能性があります。たとえば、Jitendra N. Verma etal。マクロファージによるマラリア抗原を伴うリポソームの食作用に関する研究により、リポソームでの食作用の発生を確認した[111]。
カポジ肉腫、リポソーム薬のアプリケーションの成功例の1つ
カポジ肉腫は、主に子宮内膜間質肉腫として知られる進行性多巣性抗増殖性癌です。この癌は、免疫系が弱まっているHIV患者によく見られます。さらに、それは皮膚組織で一般的に見られ、他の組織も含む可能性があります。したがって、この障害は一般に皮膚粘膜肉腫と呼ばれます[112]。この病気を治療するために、改変された長期循環リポソームが役立つ可能性があります。この点で、リポソームは受動的に腫瘍細胞を標的とします。さらに、EPRと特異的結合の効果により、癌組織における治療薬の濃度が正常な皮膚の5〜11倍に増加します[113]。この目的のために、ドキソルビシンはこの病気の治療に使用されます。同様に、ドキソルビシンをリポソーム(半減期を延長するためにPEG化された)に閉じ込めると、正常組織が薬物にさらされるのを防ぎます。また、心臓などのこれらの健康なドキソルビシン感受性組織による薬物摂取を減らします[114]。
さらに、ドキソルビシンのリポソーム型であるドキシルは、US-FDAによって臨床投与が承認されているアントラサイクリン薬の一種です。エイズ関連のカポジ肉腫や多発性骨髄腫の治療に使用されます[115]。ドキソルビシンは、腫瘍を間接的に標的とする能力に起因する可能性がある遊離ドキソルビシンよりも優れた治療効果と毒性がありません。また、腫瘍血管の漏出とEPR効果による受動的ターゲティングでもあります[116]。さらに、ドキシル単層リポソームのサイズは<100 nmであり、さまざまな種類のがんの治療に使用されています[42]。分析はまた、遊離ドキソルビシン濃度が標的組織部位でのドキソルビシンの濃度よりも低いことを証明しました[117]。この点で、小河原ら。雄マウスの癌細胞に対するドキソルビシン(ドキソルビシンをPEGリポソームに結合することによって形成される)の効果を調査し、PEGリポソームドキソルビシンまたはドキソルビシンがドキソルビシン耐性およびドキソルビシン感受性C26細胞群の両方に有効であったことを示した[118]。これは、リポソームNPの利用の重要性を浮き彫りにすることができます。それらは、新しい臨床治療化合物を発見するための時間のかかる研究作業なしに、低コストで一般的な化学療法剤に対する癌細胞の耐性を克服するために消費できるためです[119]。ドキソルビシンを腫瘍組織に送達するためのリポソームなどのナノ粒子の適用が広く研究されてきた。 ATP結合カセットトランスポータースーパーファミリーBメンバー1(ABCB1)基質ドキソルビシンのリポソームへの捕捉は、薬物取り込みを増加させ、癌細胞、特にABCB1発現癌細胞内での細胞内分布を増強する可能性があります[120]。 Doxilの単純な構造を図9に示します。
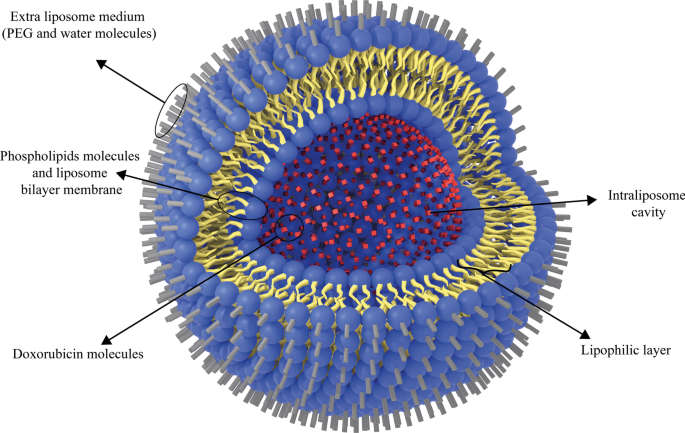
ドキシル薬の概略構造。ドキソルビシン薬物分子は、単層のPEG化リポソームの親水性空洞に閉じ込められています
さらに、リポソームナノ材料は、感染症の治療に利用することができます。全身性真菌感染症は、腎臓細胞に対して非常に毒性の高いアムホテリシンBで通常治療される最も困難な状態の1つです。この目的のために、リポソームに捕捉されたアンホテリシンBの使用は、その遊離型と比較してこの薬物の毒性を減らすことができます[48]。単層リポソームは、この薬剤を捕捉するために使用されてきました。リポソーム型アムホテリシンBは遊離剤形よりも効果的であることが証明されています[121]。製剤に基づいて、これらのリポソームは、抗がん剤などのアムホテリシンBの生体内分布も変化させ、作用機序を整えるだけでなく、標的組織での有効投与濃度を高めます[122]。リポソーム型アムホテリシンBであるAmbiSomeは、行政にも承認されています。抗真菌薬から癌治療薬まで、他の承認されたリポソーム薬を表1にまとめています。
<図>癌を治療するためのリポソームNPの適用は、薬物送達および腫瘍細胞に影響を与えるための実行可能な解決策として宣伝されてきたが、中枢神経系(CNS)の癌性組織への薬物送達は依然として重要な課題である。さらに、中枢神経系細胞への薬物送達は、血液脳関門(BBB)のために多くの混乱に直面しています。ただし、この問題は、新しい方法を開発し、脂質ベースの化合物を使用することで部分的に解決できます[136]。
治療目的の調査段階にあるリポソームナノ粒子
リポソームsiRNA
RNAは、翻訳や転写の過程など、さまざまな機能を備えた遺伝子分子の一種です。低分子干渉RNA(siRNA)の発見は、過去10年間の生物学における重要な進歩です[137]。合成siRNAは、癌遺伝子とそのmRNAを標的とするために利用できます。さらに、siRNAは、腫瘍細胞の発癌、増殖、転移、または標準的な化学療法や放射線に対する耐性に寄与する遺伝子を標的とするために適用できます[138]。したがって、それは癌治療のための現代的な方法と考えられてきました。一方、siRNAの送達に使用されるナノ粒子は、生分解性、優れた生体内分布、低毒性などの特性を備えている必要があります。これらの機能はすべてリポソームによって提供できるため、この人気のあるドラッグデリバリーシステムはこの目的の有望な候補になります[ 28]。中性脂質ベースのNPに結合したsiRNAは、これらのリポソームから十分に分離されています。それらはまた、エフリンA型受容体2(EphA2)、焦点接着キナーゼ(FAK)、ニューロピリン-2、インターロイキン8(IL-8)、およびTROJANモバイルリモート受信システム/赤芽球形質転換特異的(TMRRS / ERG)、伸長に影響を与えますファクター2キナーゼ(EF2K)またはBcl-2経路。このメカニズムの発生に続いて、卵巣癌、結腸癌、および乳癌細胞などに対して適切な抗腫瘍効果が観察されています[139、140]。リポソームによるsiRNA送達について多くの研究が行われており、それらのほとんどにおいて、カチオン性脂質ジオレオイル-3-トリメチルアンモニウムプロパン(DOTAP)がリポソームの構造に広く費やされてきた。 DOTAPの高い正電荷により、このカチオン性脂質は細胞に毒性を示す可能性があります。細胞溶血を刺激し、究極の生体適合性を低下させる可能性もあります。これは、siRNA送達に適用されるリポソームの組成におけるこの脂質の適用に挑戦しました[141]。
リポソームクルクミンナノ粒子
クルクミン結合リポソームは、リポソームナノ粒子の使用の別の例です。クルクミンは、クルクマロンガに豊富に含まれる天然のポリフェノールと親水性の化合物です。 植物であり、主にターメリック抽出から調製することができます。今日、クルクミンの抗がん効果は、乳がん、肝臓がん、前立腺がんなどの多くの腫瘍細胞に対してよく示されています[142]。癌細胞に対するクルクミンの作用の主なメカニズムは、Bcl-xlなどのタンパク質の翻訳を妨害し、それらのプロセスに影響を与え、反応性酸素種(ROS)とチトクロームの放出を制御し、サイクリンなどの分子因子を調節することによってアポトーシスを調節することです。細胞周期に影響を与えます。一方、クルクミンは肝臓癌細胞の核およびミトコンドリアDNA構造に損傷を与え、それによってそれらの機能を破壊する可能性があります[143]。遊離クルクミンと比較して、リポソームクルクミンの適用は、腫瘍を標的とするために必要な投与量を減らしながら、薬物動態および薬力学を改善します。 Matheus Andrade Chave etal。クルクミン分子をMLVリポソームに挿入することにより、クルクミン含有リポソームを探索しました[144]。リポソームクルクミンの合成とクルクミン構造を図10に示します。
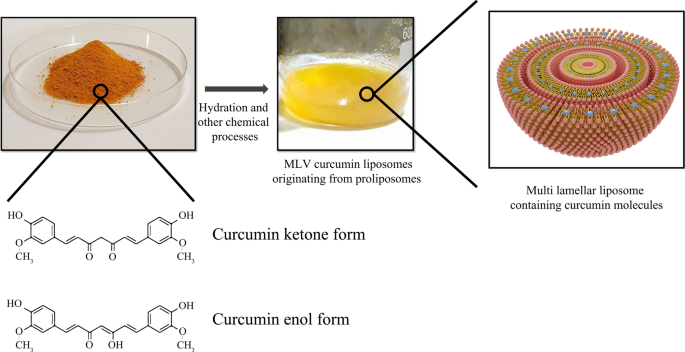
クルクミン粉末とリポソームクルクミン合成の概要。リポソームのクルクミン生成およびさまざまな形態のクルクミン分子構造に対して実行される化学反応が簡単に示されます
さらに、治療研究用途のために調製されたリポソームは、様々な方法を使用することによって合成することができる。たとえば、Qiao Wang etal。超音波処理と脂質膜水和法を利用して、ダイゼイン長期循環リポソーム(DLCL)を合成しました[145]。 Xiaoyuan Ding et al. also used the film hydration method for the synthesis of aptamer and Au-NPs (Apt-Au)-modified Morin pH-sensitive liposome. Their outcomes showed high biocompatibility and insignificant toxicity of these liposomal structures and highlighted these liposomes as a viable option for selective targeting of tumors [146].
Other Liposomal NPs in the Investigational Phase
Several liposomal drugs have been synthesized and utilized in various medications at the investigational phase. For instance, CPX-1 was produced by entrapping the antitumor agents, Irinotecan and floxuridine (1:1 molar ratio) in liposomes, and was designed to treat advanced colorectal cancer. This therapeutic nanoparticle is in phase II research status [128]. Lipovaxin-MM is another momentous liposomal nanoparticle in phase I research prepared by placing melanoma antigens in liposomes and mainly administrated for immunotherapy of malignant melanoma. This agent is also under investigation [128].
結論
As spherical structures in liquids, liposomes can be applied as a promising option for cancer therapy and drug delivery, as well as imaging, and disease management. By reviewing liposomes pros and cons, scientists will be able to improve them in future research works.
Some opportunities and challenges in liposomes utilization are described in the following. One of the convenient features of liposomes is their morphological similarity to cells (presence of phospholipids), as well as increasing the effectiveness of the drugs. As a negative point, liposomal phospholipids may sometimes undergo hydrolysis or oxidation reactions which may be problematic. Other pros of liposomes include increased stability of the encapsulated drug in it, reduced contact of sensitive tissues with therapeutic molecules, decreased drug toxicity, improved pharmacokinetic and pharmacodynamics properties, the ability to regulate the rate of drug release, and the potential of their structure to accept the desired chemical modification. In contrast to these opportunities, there are some challenges such as leakage or unintended entrapment of drugs, low liposome bioactivity, decreased-solubility, rapid clearance of conventional liposomes from the blood by the reticuloendothelial system (RES), and problems caused by continuous intravenous administration or local injection.
Besides examining the advantages and disadvantages of liposomes, we should take their proper targeting mechanism of action into account. Passive targeting is considered a beneficial mechanism due to the abundant clinical evidence and experience. It also increases the circulation time of liposomal drugs. The problem of this mechanism lies in its non-specific drug delivery and its physiological barriers. In contrast, beneficial features of active targeting include increased specificity in drug delivery, the possibility of overcoming chemotherapy-resistant tumor cells, and reduced off-target effects. However, the difficulty in identifying accurate binding sites on cancer cells and the lack of adequate evidence of its former utilization have led to some ups and downs in its application.
Liposomes are reasonable candidates for elevating the effectiveness of current anticancer agents and preventing the incidence of drug resistance. Future research in this area should be focused on further investigation into the properties of liposomal structures. To probe about drug entrapment in therapeutic nanoparticles, including liposomes, much more detailed examinations will be required.
略語
- WHO:
-
World Health Organization
- VNPs:
-
Viral nanoparticles
- NP:
-
ナノ粒子
- US FDA:
-
United States Food and Drug Administration
- DDSs:
-
Drug delivery systems
- PC:
-
Phosphatidylcholine
- SM:
-
Sphingomyelin
- PS:
-
Phosphatidylserine
- PE:
-
Phosphatidylethanolamine
- ULVs:
-
Unilamellar vesicles
- OLVs:
-
Oligo lamellar vesicles
- MLVs:
-
Multilamellar vesicles
- SUVs:
-
Small unilamellar vesicles
- RBF:
-
Round-bottom flask
- LNs:
-
Liposomal nanoparticles
- MPS:
-
Mononuclear phagocytosis system
- PEG:
-
ポリエチレングリコール
- PEOZ:
-
Poly [2-ethyl 2-oxazoline]
- PETOXylated:
-
Poly [2-ethyl-2-oxazolylated
- PMOZ:
-
Poly [2-methyloxazoline]
- HDL:
-
High-density lipoprotein
- LDL:
-
Low-density lipoprotein
- SCLC:
-
Small cell lung cancer
- GRPR:
-
Gastrin-releasing peptide receptor
- Anti-EpCAM:
-
Anti-epithelial cell adhesion molecule
- IUPAC:
-
国際純正応用化学連合
- I.V.:
-
Intravenous
- S.C.:
-
Subcutaneous
- I.D.:
-
Intradermal
- I.P.:
-
Intraperitoneal
- I.M.:
-
Intramuscular
- EPR:
-
強化された透過性と保持力
- fR:
-
Folate receptor
- TfR:
-
Transferrin receptor
- EGFR:
-
上皮成長因子受容体
- VEGF:
-
血管内皮増殖因子
- VCAM:
-
Vascular cell adhesion protein
- APC:
-
Antigen-presenting cells
- ABCB1:
-
ATP-binding cassette transporter superfamily B member 1
- HSPC:
-
Hydro soy phosphatidylcholine
- DSPG:
-
1,2-Distearoyl-sn-glycero-3-PG
- DOPC:
-
Dioleoylphosphatidylcholine
- DPPG:
-
1,2-Dipalmitoyl-sn-glycero-3-phosphoglycerol
- DSPC:
-
1,2-Distearoyl-sn-glycero-3-phosphocholine
- AML:
-
Acute myeloid leukemia
- ALL:
-
Acute lymphocytic leukemia
- DSPE:
-
1,2-Distearoyl-sn-glycero-3-phosphoethanolamine
- DOPE:
-
Dioleoylphosphatidylethanolamine;
- EPG:
-
Esterified propoxylated glycerols;
- DMPC:
-
1,2-Dimyristoyl-sn-glycero-3-phosphocholine
- DOPS:
-
1,2-Dioleoyl-sn-glycero-3-phospho-L-serine
- POPC:
-
1-Palmitoyl-2-oleoyl-sn-glycero-3-phosphocholine
- DMPG:
-
1,2-Dimyristoyl-sn-glycero-3-phosphoglycerol
- MPEG:
-
Methoxypolyethylene glycols.
- CNS:
-
中枢神経系
- BBB:
-
血液脳関門
- siRNA:
-
Small-interfering RNA
- EphA2:
-
Ephrin type-A receptor 2
- FAK:
-
Focal adhesion kinase
- IL-8:
-
Interleukin-8
- TMRRS/ERG:
-
TMRRS/ERG TROJAN Mobile Remote Receiving System/erythroblast transformation-specific
- EF2K:
-
Elongation factor 2 kinase
- DOTAP:
-
Dioleoyl-3-trimethylammonium propane
- ROS:
-
活性酸素種
- DLDC:
-
Daidzein long-circulating liposomes
- RES:
-
細網内皮系
ナノマテリアル
- シード処理アプリケーションに不可欠な正しいポンプ選択
- ドラッグデリバリーを強化するためのナノファイバーとフィラメント
- 癌治療のためのナノ粒子:現在の進歩と課題
- 腫瘍治療のためのドラッグデリバリーシステムとしての環境応答性金属有機フレームワーク
- 癌用途のための細胞ベースのドラッグデリバリー
- ゼブラフィッシュ:ナノテクノロジーを介した神経特異的ドラッグデリバリーのための有望なリアルタイムモデルシステム
- 黒色腫の標的化学療法治療のための薬物送達担体としての131I追跡PLGA-脂質ナノ粒子
- 透明導体用途向けの柔軟な銅ナノワイヤメッシュフィルムのUV処理
- ソラフェニブ送達のためのヌクレオシド-脂質ベースのナノキャリア
- 腫瘍の光検出および治療のための5-アミノレブリン酸-スクアレンナノアセンブリ:invitro研究
- 3Dプリントされたマイクロロボットはドラッグデリバリーの約束を保持します



