転移性乳がんの治療のための免疫チェックポイント阻害と組み合わせた光熱治療のための標的化単層カーボンナノチューブ
要約
癌による死亡率の最大の原因は、転移とその治療の結果です。ここでは、標的単層カーボンナノチューブ(SWCNT)と光熱療法とチェックポイント阻害剤による免疫刺激を組み合わせた転移性乳がんの新しい治療法を紹介します。アネキシンA5(ANXA5)機能化SWCNTバイオコンジュゲートを使用した同系BALB / cJマウスにおける原発性同所性EMT6乳房腫瘍の選択的近赤外光熱除去が、抗細胞傷害性Tリンパ球関連タンパク質4(抗CTLA- 4)依存性のabscopal応答、腫瘍接種後100日で生存率の増加(55%)をもたらします。比較すると、光熱療法単独または免疫刺激単独のいずれにおいても、100日で生存はありませんでした。光熱療法の前に、SWCNT-ANXA5バイオコンジュゲートは、1.2 mg / kgの比較的低用量で全身投与され、その後、ANXA5依存性結合を介して腫瘍血管系に蓄積しました。光熱治療中、腫瘍の平均最高温度は54°Cに達しました(持続時間175秒)。コンビナトリアル光熱焼灼と免疫刺激から生じる長期生存のメカニズムは、脾臓の抗腫瘍免疫エフェクター細胞のフローサイトメトリーによる定量化と血清サイトカインの定量化によって評価されました。
はじめに
転移とその治療の結果は、癌の唯一の最大の死因です[1]。たとえば、乳がんが転移すると、患者の5年生存率は25%を下回ります。過去60年間で、200を超える新しい抗腫瘍薬が患者の転帰を改善しましたが、転移性疾患の全生存期間は依然として不良です[2]。ここでは、腫瘍を標的とした単層カーボンナノチューブ(SWCNT)バイオコンジュゲートと抗細胞毒性Tリンパ球関連タンパク質4(抗CTLA-4)チェックポイント阻害によって促進される光熱療法の新しい組み合わせが転移性乳がんの治療のために研究されています同所性マウスモデル。
ナノマテリアルとしてのSWCNTのユニークな特性は、癌との闘いにおける潜在的なツールとしてのSWCNTの使用に大きな関心を呼んでいます。 SWCNTはさまざまな生物学的効果を発揮しますが、癌の治療におけるSWCNTの使用は、主に近赤外(NIR)光との相互作用と、結果として生じる光熱効果に焦点を当てています。SWCNTは、光熱療法と呼ばれるプロセスで腫瘍を急速に加熱します。 (PTT)。多数のグループが、SWCNTが乳がんのいくつかのモデルのPTTベースの治療戦略で使用される可能性を調査しました[3,4,5,6,7,8,9,10]。これらの研究は、NIR光の減衰がほぼ完全である数mm以下の深さで原発腫瘍を治療するPTTの能力に主に焦点を合わせています。
以前に、同系マウスの原発性同所性乳房腫瘍は、光熱増強SWCNTバイオコンジュゲートと組み合わせた穏やかなNIRレーザー光を使用してほぼ完全に排除できることを示しました[11]。このバイオコンジュゲートでは、SWCNTはタンパク質アネキシンA5(ANXA5)で機能化されました。これは、腫瘍細胞および腫瘍血管系の内皮細胞に外部から発現する陰イオン性リン脂質ホスファチジルセリンに高い親和性で結合しますが、血管系の正常細胞には結合しません。 12,13,14]。このコンジュゲートは、原子間力顕微鏡(AFM)を使用して視覚化され、コンジュゲートの高さが2.5〜5.0 nmであることが示されました。これは、他のSWCNT-タンパク質コンジュゲートの場合と同様です[11]。この以前の転移モデルでは原発腫瘍を根絶することができますが、光熱療法だけでは生存期間がわずかに延長されました。しかし、シクロホスファミドなどの免疫調節剤との併用治療が生存率を高めることができることを示唆する予備的な証拠を発見しました。
最近、シクロホスファミドなどの免疫調節剤がSWCNTに向けられたPTTを相乗的に増強する可能性が大きな関心の対象となっています。有望な免疫調節剤の1つのカテゴリーは、チェックポイント阻害剤です。チェックポイント阻害剤は、抗CTLA-4、抗PD-1、抗PDL-1などの抗体であり、癌に対する体の反応の調節に関与する重要な細胞タンパク質に結合します。これらの抗体は、体が癌に対する免疫系の反応をダウンレギュレートできる重要な生物学的「チェックポイント」をブロックします。これらのタンパク質は通常、体の免疫応答を制御する上で重要な役割を果たします。チェックポイント阻害剤は、これらのタンパク質の作用をブロックすることにより、免疫系が通常その自然な抗腫瘍反応を抑制するメカニズムを取り除きます。最近、いくつかのグループが、抗CTLA-4チェックポイント阻害とSWCNT強化PTTの組み合わせが、乳がんにおける強力な免疫応答を促進する可能性があることを観察しました[15、16]。
現在の研究では、免疫刺激剤抗細胞毒性Tリンパ球関連タンパク質4(抗CTLA-4)と組み合わせた新規PTTモダリティの組み合わせを評価します。もともと転移性黒色腫の治療に承認されていた[17]、現在、抗CTLA-4は他の免疫刺激剤と組み合わせた臨床試験で乳がんの治療のためにテストされています[18]。抗CTLA-4チェックポイント阻害と組み合わせたPTTにおける抗腫瘍免疫の増強のメカニズム、および標的臓器におけるSWCNTの長期的な運命を評価します。
材料と方法
資料
ANXA5をコードするプラスミド、pET-30 Ek / LIC / ANXは、以前にこの研究室で構築されました[11]。ウシ血清アルブミン(BSA)、Triton X-100、EDTA、β-メルカプトエタノール、フェニルメチルスルホニルフルオリド(PMSF)、およびTris-acetate-EDTAバッファーは、Sigma-Aldrich(セントルイス、ミズーリ州)から入手しました。リン酸ナトリウムとドデシル硫酸ナトリウム(SDS)は、Mallinckrodt Chemicals(Phillipsburg、NJ)から入手しました。 HPLCグレードのエタノールはAcrosOrganics(マサチューセッツ州、ウォルサム)から入手しました。 His-trapカラムは、GE Healthcare(シカゴ、イリノイ州)から入手しました。フローサイトメトリー染色バッファー、固定/透過処理バッファー、透過処理バッファー、発色性エンドトキシン定量キット、およびSlide-A-Lyzer透析カセット(3.5 kDa)は、Thermo Fisher Scientific(マサチューセッツ州、ウォルサム)から入手しました。 2kDaおよび100kDaの透析膜は、Spectrum Laboratories(Rancho Dominguez、CA)から入手しました。ロズウェルパークメモリアルインスティテュートの細胞培地(RPMI-1640)とハンクの平衡塩類溶液はATCC(バージニア州マナッサス)から入手しました。ウシ胎児血清(FBS)は、Atlanta Biologicals(Lawrenceville、GA)から入手しました。トリプトン、酵母エキス、およびカナマイシン一硫酸塩は、Alfa Aesar(マサチューセッツ州、ワードヒル)から入手しました。水酸化ナトリウム、塩化カリウム、および塩化ナトリウムは、VWR Inc(Radnor、PA)から入手しました。 HRV-C3プロテアーゼはSinoBiologics(Portland、OR)から入手しました。抗CTLA-4マウスモノクローナル抗体(クローン:9H10)およびマウスサイトカインELISAキット(TNF-α、IFN-γ、IL-6)は、BioLegend(San Diego、CA)から入手しました。 CoMoCAT SWCNT(平均直径0.8±nm、平均長さ1.5±0.5 µm)は、CHASM(マサチューセッツ州、ボストン)から入手しました。 CoMoCAT法は、少数の( n )のSWCNTを生成することが知られています。 、 m )選択性の高いキラリティー[19]。この研究で使用されたサンプルは、[5、6] SWCNTが高度に濃縮されており、980nmの波長で強いNIR光吸収を示します。この吸収はS 11 に対応します このタイプのナノチューブの、占有されたファンホーベ特異点から対応する占有されていない特異点への遷移。したがって、腫瘍に沈着したSWCNTによる放射線吸収を最大化するために、この研究で使用されたレーザーの波長は980 nmであり、S 11 の波長と正確に一致していました。 光学遷移[20]。追加ファイル1の図S1は、蛍光スペクトルを示しており、S 11 を明確に示しています。 可視光でS22遷移を励起した後のNIR放射。
細胞培養
ATCC(バージニア州マナッサス)のEMT6乳がん細胞は、15%FBSを添加した2 mML-グルタミンを含むWaymouthのMB752 / 1培地で培養しました。すべての細胞は、37°C、湿度100%、5%CO 2 で培養しました。 。すべての細胞は、0.53 mM EDTA中の0.25%(w / v)トリプシンを使用して継代されました。細胞系統とマイコプラズマのない状態は、STRテスト(Charles River)によって確認され、リムルスアッセイによってエンドトキシンフリーであるとアッセイされました。
ANXA5およびSWCNT-ANXA5の本番
SWCNT-ANXA5コンジュゲートは、2.5 mg ANXA5 / mgSWCNTを与える以前に開発した手順を使用して調製されました[11]。簡単に言うと、 E。コリ ANXA5をコードするプラスミドpET-30Ek / LIC / ANXをトランスフェクトし、固定化Ni 2+ を使用した固定化金属アフィニティークロマトグラフィーを使用して増殖および精製しました。 (His) 6 を除去するための酵素的切断を伴うANXA5を単離する 鬼ごっこ。凍結乾燥したCoMoCATSWCNTを、20 Wでのプローブ超音波処理と29,600 gでの遠心分離をそれぞれ30分間使用して、1%ドデシル硫酸ナトリウム(SDS)に分散させました。懸濁したSWCNTは、NIR蛍光(追加ファイル1:図S1)によって特徴付けられ、1,2-ジステアロイル-sn-グリセロ-3-ホスホエタノールアミン-ポリエチレングリコール-マレイミド(DSPE-PEG-マレイミド)リンカーに30分間結合しました。 SWCNTとDSPE官能基間の疎水性相互作用を可能にするために室温で。その後、蒸留水で8時間透析して、余分なリンカーとSDSを除去しました。次に、透析したコンジュゲートを1つのシステイン基を含むANXA5と2時間反応させ、1.5 mg ml -1 でブロックしました。 L-システイン。最終生成物であるSWCNT-ANXA5を、20 mMリン酸ナトリウム緩衝液に対して8時間透析し、過剰なANXA5とL-システインを除去しました。タンパク質の重量と純度はSDS-PAGEで特徴づけられました。バイオコンジュゲートのSWCNTおよびANXA5含有量は、UV-Vis-NIR蛍光分光法、フーリエ変換赤外分光法(FT-IR)ラマン分析、およびブラッドフォードアッセイによって特徴づけられました(追加ファイル1:図S2)。
In Vivo Studies
すべての手順は、オクラホマ大学の施設内動物管理使用委員会(IACUC)によって承認されたプロトコルに準拠していました。 6週齢の雌のBALB / cJ雌マウスを使用しました(Jackson Laboratory、メイン州バーハーバー)。マウスには標準的な固形飼料を与えた。 NIRレーザー光による腫瘍の光熱照射中に、ノーズコーンを使用してマウスを2%イソフルランと98%酸素で麻酔しました。
腫瘍は10 6 の同所注射によって誘発されました 100 µLのPBS中のEMT6マウス乳がん細胞をIV乳腺脂肪パッドに入れます。腫瘍は12日間成長させ、体積が60 mm 3 に達したときに成長させました。 (直径〜5 mm)、マウスは全身静脈内投与を受けました。外側尾静脈を介した1.2mg / kgのSWCNT-ANXA5(mg SWCNT / kg体重)バイオコンジュゲートの注射。 3時間後、腫瘍境界を5 mm超えた領域に、175 J / cm 2 のエネルギーおよび電力レベルでNIR光(980 nm)を照射しました。 および1W / cm 2 、それぞれ(175秒の時間、Diodevet-50 NIRレーザー、B&W Tek Inc.、デラウェア州ニューアーク)。チェックポイントの抑制は、シリアルIPによって達成されました。腫瘍接種後8、11、16日目に100 µlのPBSに200 µgの抗CTLA-4抗体を投与。腫瘍体積は、修正された楕円体式\(V =\ frac {1} {2} \ times {\ text {length}} \ times {\ text {width}} ^ {2} \)を使用して、ノギス測定値を使用して計算されました。最長寸法と垂直幅。腫瘍温度は、検出された最大温度を自動スキャンするように設定されたハンドヘルドFLIR TG165スポットサーマルカメラ(Raymarine ITC、英国フェアラム)によって監視されました。毒性評価のために標的臓器を採取し、10%中性緩衝ホルマリンで固定し、染色したホルマリン固定パラフィン包埋(FFPE)スライドを準備し、毒性分析のためにヘマトキシリンとエオシンで染色しました。
Ex VivoSWCNT検出
マウスは、1.2 mg / kgのSWCNT-ANXA5(mg SWCNT / kg体重)を尾静脈から全身注射されました。選択した時点で、マウス( n =3)安楽死させ、壊死させ、分析のために標的臓器を取り出した。組織サンプルは以前に記載されたように調製された[21]。次に、ex vivo組織サンプル中のSWCNTの存在を、NS3 NanoSpectralyzer(Applied NanoFluorescence、テキサス州ヒューストン)を使用した相対NIR蛍光分光法によって決定しました。
フローサイトメトリー
治療の14日後にマウスを安楽死させ、脾臓の抗腫瘍免疫エフェクター細胞を以前に記載されたように定量化した[21]。
サイトカインの検出
上記の治療後、マウス( n =4–5)採血のための光熱療法の7日後に安楽死させました。希釈血清サンプル中の腫瘍壊死因子アルファ(TNF-α)、インターフェロンガンマ(IFN-γ)、およびインターロイキン6(IL-6)の濃度は、サプライヤーのプロトコルに従ってELISAによって定量化されました。
統計分析
GraphpadPrismソフトウェアを使用してデータを分析しました。統計的有意性は、一元配置分散分析とテューキー-クラマー多重比較検定を使用して評価されました。生存曲線の統計的有意性は、マンテルヘンツェルログランク検定によって決定されました。サイトカイン血清濃度の統計的有意性は、一元配置分散分析とダネットの多重比較検定によって分析されました。多重比較は、ボンフェローニしきい値によって修正されました。誤差は、プロットされた平均点記号のサイズを超えない限り、平均の標準誤差としてグラフで表されます。この場合、明確にするためにバーは除外されています。
結果
熱動力学
図1に示すように、1.2 mg / kgのSWCNT-ANXA5の線量を使用して、NIR光による治療の過程で腫瘍の最高温度を記録しました。照射前にSWCNT-ANXA5を投与されたマウスは、生理食塩水を投与されたマウスと比較した全NIR光治療。 SWCNT-ANXA5を投与されたマウスの腫瘍の平均温度は、生理食塩水を投与されたマウスの場合とは有意に異なっていました(54°C対37°C、 p <0.05)。この強化された光熱療法の結果として、SWCNT-ANXA5グループでのみ目に見える腫瘍切除が発生しました。腫瘍切除は、急速な変色、それに続く皮膚拘縮およびしわの出現を特徴とした。 48時間以内に、光熱焼灼の部位にかなりの痂皮が形成されました。完全な皮膚の再生には数週間かかりました。
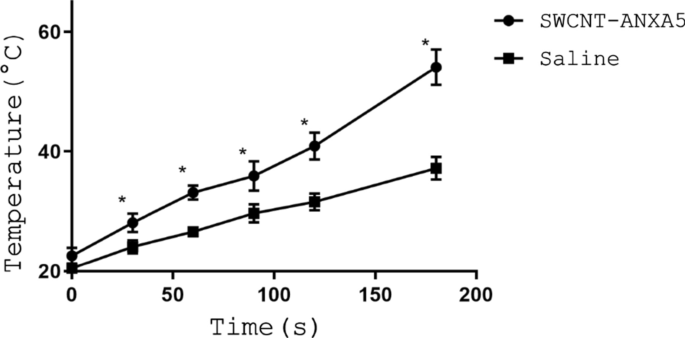
980nmのNIR光による腫瘍の放射から生じる熱動態。 EMT6腫瘍を有するBALB / cJマウスに静脈内注射した。尾静脈に1.2mg / kgSWCNT-ANXA5を投与。 SWCNTが循環から排除されるまで3時間待った後、175 J / cm 2 のエネルギーと出力密度でNIRレーザーを腫瘍に照射しました。 および1W / cm 2 、それぞれ( t =175秒)。腫瘍の最高温度を時間の関数として記録した。 SWCNTを投与されたマウスの腫瘍の温度は、 t で生理食塩水を投与されたマウスよりも有意に高かった。 =175秒( p <0.05)。データは平均±SE( n )として表されます =3)
光熱療法とチェックポイント阻害
抗CTLA-4モノクローナル抗体を使用したチェックポイント阻害と光熱療法を組み合わせた結果を図2に示します。光熱療法だけで原発性乳がん新生物を容易に根絶できましたが、NIRレーザー光が数mmを超えて透過できないため、乳がん転移の治療。局所的なNIR光熱抗腫瘍治療の不足を克服するために、この独自の治療治療法と全身チェックポイント阻害の組み合わせを検討しました(図2)。光熱療法は原発性EMT6腫瘍の破壊に優れていましたが(図2a)、この治療は転移を根絶することができず、EMT6同所性腫瘍を有するマウスの生存率をわずかに増加させました(図2b)。対照的に、抗CTLA-4によるチェックポイント阻害は全生存期間を延長しましたが、原発腫瘍の成長を一時的に遅らせるだけでした。どちらの治療法だけでも全生存期間は延長されませんでしたが、SWCNT-ANXA5の強化された光熱療法と抗CTLA-4チェックポイント阻害の両方の組み合わせにより、全生存期間が改善され、腫瘍接種後100日で55%の生存率が得られました。
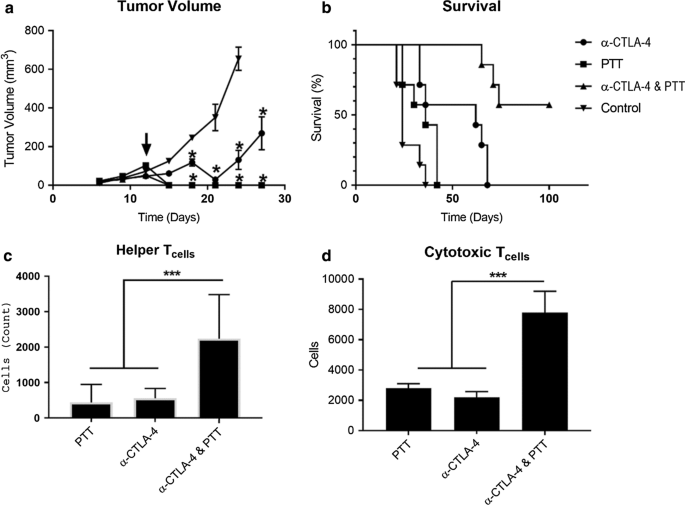
EMT6腫瘍におけるコンビナトリアル光熱療法(PTT)とチェックポイント阻害(抗CTLA-4)の結果。よく発達した同所性同系腫瘍を有するマウス( d ≥5mm)を静脈内投与しました。全身投与量1.2mg / kgSWCNT-ANXA5。 a 次に、1 W / cm 2 の出力密度で175秒間、NIRレーザー光を照射(矢印)した後、腫瘍の体積をモニターしました。 接種後12日目。 PTTに加えて、選択したグループは8、11、および16日目に抗CTLA-4(100 µg)を投与されました。コントロールグループのマウスは静脈内注射されました。生理食塩水で。平均±SE( n )として示される腫瘍体積 =7)。コントロールと比較した重要性は*( p )で示されます <0.05)。 b 光熱療法と免疫チェックポイント阻害の組み合わせは、対照と比較して生存率を有意に増加させました( p <0.05、 n =7)。 c 、 d マウスが抗CTLA-4チェックポイント阻害と組み合わせて光熱療法を受けた場合にのみ、CD4 + の相対数が有意に増加しました。 およびCD8 + PTTの2週間後に脾細胞が観察されました。平均±SE( n )として示される脾細胞 =3)。重要性は***( p )で示されます <0.005)
治療後の脾臓エフェクター細胞のサイトメトリー分析により、コンビナトリアル光熱療法およびチェックポイント阻害を受けたマウスの生存率が改善されたと推定されるメカニズムが明らかになりました。マウスにEMT6を接種し、前述のように処理しました。治療の2週間後、マウスを犠牲にし、複数の免疫エフェクタータイプのパーセンテージと相対数の両方を定量化しました。ヘルパーT細胞、細胞傷害性T細胞、好中球、骨髄由来抑制細胞(MDSC)単球、FoxP3制御性T細胞、およびマクロファージの集団を評価しました(追加ファイル1:図S3)。これらの集団の分析は、光熱療法と抗CTLA-4チェックポイント阻害の両方の組み合わせを受けたマウスでのみ、治療集団と対照との間に有意差を明らかにしました。この組み合わせを受けた動物では、ヘルパーT細胞(CD4 + )の相対数の増加が観察されました。 )および細胞傷害性T細胞(CD8 + )、(図2c、d)。 CD4 + の増加 およびCD8 + 細胞数は、剖検後に観察された脾臓サイズの全体的な増加と相関していました。
脾臓エフェクター細胞のサイトメトリー分析に加えて、PTTの7日後に血清サイトカイン濃度を測定し、抗腫瘍免疫のメカニズムを解明しました。炎症誘発性サイトカインIL-6、IFN-γ、およびTNF-αのレベルを図3に示します。SWCNTまたは抗CTLA-4治療のみでは、未治療の対照群と比較してサイトカインのレベルを有意に増加させませんでした。しかし、PTT治療だけでTNF-αを有意に増加させることができました。 PTT治療に抗CTLA-4をさらに追加すると、TNF-α、IL-6、およびIFN-γのレベルが大幅に増加しました。
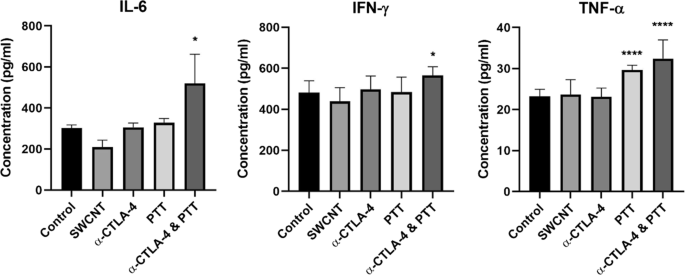
血清サイトカイン濃度。 PTTの7日後のマウス血清中の血清サイトカインレベルの定量化は、チェックポイント阻害(抗CTLA-4)と組み合わせたPTT後のマウスのIL-6、IFN-γ、およびTNF-αレベルの有意な増加を示しました。結果は、未処理のコントロール、SWCNT処理のみ、抗CTLA-4処理のみ、PTT処理、およびPTT +抗CTLA-4処理について示されています。データは平均±SE( n )として表されます =4–5)。ダネットの多重比較検定を使用した一元配置分散分析により、未処理の対照群と比較した処理群の統計的有意性を分析しました。統計的有意性は*( p )で示されます <0.05)および****( p <0.0001)
SWCNT-ANXA5の生体内分布と毒性
さまざまな臓器での光熱治療強化のための投与後のSWCNT-ANXA5の生体内分布は、標準と比較した生息域外組織溶解物中のSWCNTの蛍光定量化で監視されました(追加ファイル1:図S4)。標的臓器の生体内分布は、静脈内投与後4か月間追跡されました。健康なマウスに1.2mg / kgのSWCNT-ANXA5を注射します(図4a、b)。対照的に、前述の注射プロトコルに従って、投与後のEMT6担癌マウスにおけるSWCNT-ANXA5の蓄積は、投与後3時間で測定されました。 (治療研究で光熱療法が行われた時間。)臓器採取前の4か月間、マウスの身体的副作用と異常行動をモニターしました。この期間中にSWCNT-ANXA5を注射したマウスでは副作用は観察されませんでした。研究の終わりに、標的臓器からのヘマトキシリンおよびエオシン染色されたFFPE切片の検査中に、組織病理学的毒性は観察されませんでした(追加ファイル1:図S5)。
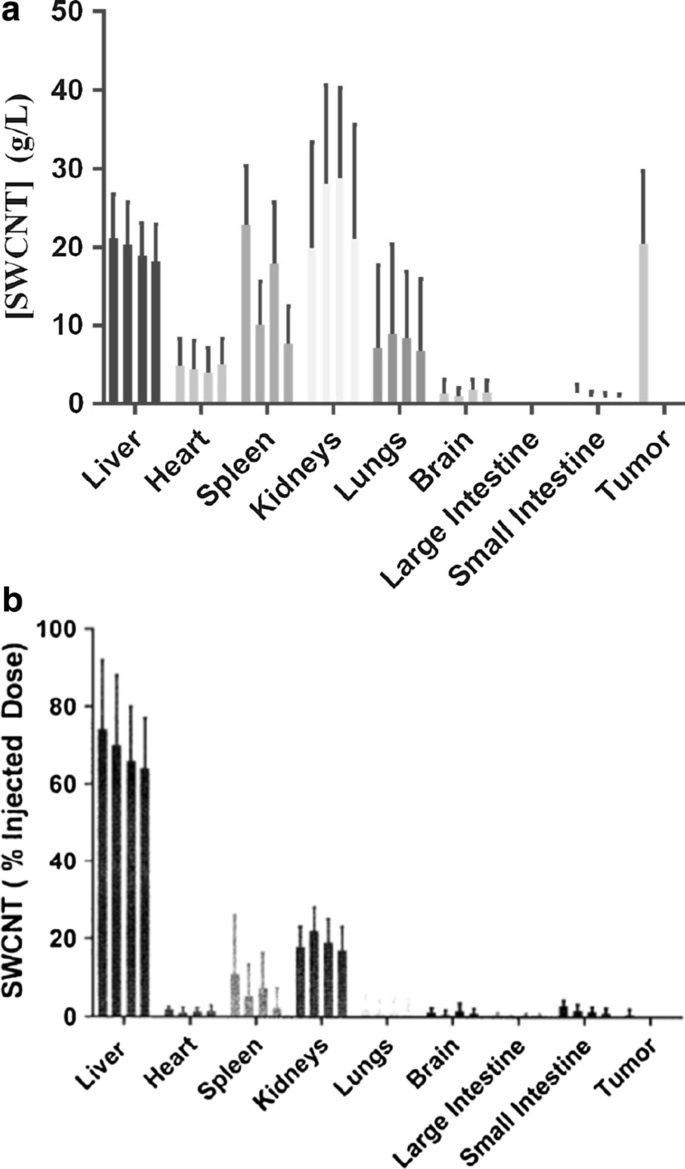
注射された用量の%として測定されたSWCNT-ANXA5の生体内分布( a )およびg / L単位の組織濃度( b )。 SWCNT-ANXA5コンジュゲートは静脈内投与されました。 Balb / cJマウスに1.2mg / kgの用量で注射しました。 SWCNT濃度は、1、2、3、および4か月後(左から右)に腫瘍のないマウスのさまざまな臓器で測定されました。腫瘍のあるマウスの場合、SWCNTの濃度は、光熱療法治療の直前と同じように測定されました。データは平均±SE( n )として示されています =3)
ディスカッション
ここに提示されたデータは、転移性乳がんの治療のための標的光熱療法と免疫チェックポイント阻害を組み合わせる効果のサポートを提供します。この現象は「アブスコパル効果」として知られており、局所放射線が一次標的から離れた腫瘍の成長を抑制する抗腫瘍反応を開始する能力を表しています。 1950年代には早くも、研究者らは局所的な腫瘍照射が遠隔腫瘍に有意な影響を与えることを観察しました[22]。研究によると、アブスコパル効果の全身的な性質は、宿主の免疫応答によるものであることがわかっています[23、24、25]。 γ線照射はほとんどのアブスコパル研究の主な焦点でしたが、研究の増加は、光熱療法がアブスコパル効果も誘発できることを示しています。多くの研究は、チェックポイント阻害剤である抗CTLA-4と組み合わせた熱焼灼が免疫応答の亢進をもたらすことを示しています[16、26、27、28、29]。乳がんのEMT6モデルで、標的を定めた光熱焼灼と抗CTLA-4遮断に続いて、同様の腹膜反応が観察されます。
アブスコパル効果は、図2a、bのデータで示されています。同所性EMT6腫瘍は急速に成長し、光熱療法で治療されるまでに転移します。これが、原発腫瘍が完全に切除されたにもかかわらず、光熱療法のみで治療された腫瘍を有するマウスが、未治療のマウス対照と比較して生存率がわずかに増加しただけである理由です。抗CTLA-4の単独投与は、対照と比較して腫瘍の成長を遅らせ、生存期間を68日に延長しましたが、治癒には至りませんでした。 EMT6腫瘍増殖の遅延の同様の結果がJure-Kunkelらによって観察されました。抗CTLA-4が投与されたとき[30]。光熱療法と抗CTLA-4の組み合わせでは、治療を受けたマウスの55%が、腫瘍接種後100日で生存し、治癒する可能性があります。
脾臓の免疫エフェクター細胞の集団を定量化するためにフローサイトメトリーを使用することにより、抗腫瘍免疫のメカニズムへの洞察を評価した。光熱療法または抗CTLA-4単独のいずれかと比較して、併用療法はヘルパーCD4 + の7倍の増加をもたらしました。 T細胞と細胞溶解性CD8の3倍の増加 + T細胞。これらの結果は両方とも統計的に非常に有意です( p <0.005)。これらの結果は、光線療法と免疫チェックポイント阻害を伴うT細胞共刺激療法の組み合わせによる潜在的なabscopal応答のさらなる証拠を提供します。
CD4 + の増加 およびCD8 + 細胞数は、剖検中に観察された脾臓サイズの増加と相関していました。脾臓のサイズが大きくなると、免疫応答が高まることを示します。脾臓は複数の細胞タイプで構成されており、その中で最も一般的なのはCD4 + です。 、CD8 + 、およびB細胞系統[31、32]。この一連の作業では調査されていませんが、CD4 + とともにB細胞数が増加すると予想されます。 およびCD8 + T細胞は数えます[33]。ヘルパーCD4 + T細胞は、サイトカイン刺激と直接的な細胞間相互作用によって他の免疫細胞を促進することにより、体液性免疫を支援します。細胞溶解性CD8 + T細胞は腫瘍細胞を直接殺します。 CD4 + の増加 およびCD8 + 細胞数は、全身性の腹筋免疫応答を示しています。
併用療法後の全身性腹膜免疫応答の存在は、マウス血清炎症性サイトカインレベルの増加によってさらに裏付けられます(図3)。 TNF-αは腫瘍関連マクロファージを活性化して抗腫瘍効果を示します[34、35]。 IFN-γは腫瘍の監視において重要な役割を果たします[36、37]。 IL-6はマクロファージとリンパ球の増殖を促進します[38]。抗CTLA-4と組み合わせたPTT治療の7日後のマウス血清中のこれらのエフェクター分子の有意な増加は、抗腫瘍免疫応答の存在をさらにサポートします。
SWCNTを投与されたマウスの照射の終わりに、平均最大腫瘍温度は54°Cでした。この温度は、腫瘍を完全に切除するのに十分でした(図1)。これは、酵素の不活性化とミトコンドリアの損傷が発生する45〜60°Cの範囲内です[39]。生理食塩水対照群の腫瘍の温度は40°C未満のままでした。これは最小限の治療効果しか得られない温度です[39,40,41]。
濃度に基づくSWCNT-ANXA5の蓄積の大部分は、主に肝臓、心臓、脾臓、腎臓、肺、および腫瘍にあることが観察されました(図4a)。 EMT6腫瘍のあるマウスでは、SWCNT-ANXA5の濃度が肝臓と腎臓の濃度と類似していることが観察されました(図4a、b)。微量のSWCNT-ANXA5が脳、大腸、小腸で検出されました。注入された線量(ID)の%に基づくSWCNTの生体内分布は、標的組織内のSWCNTの絶対濃度とはあまり相関しないことに注意することが重要です。これは主に臓器重量の違いによるものです。たとえば、臓器内の特定の%IDは、小さな臓器内のより高い濃度、およびより大きな臓器内のより小さな濃度に対応します。 SWCNT濃度に基づいてサンプルを比較すると、最も高い濃度が腎臓内にあり、次に肝臓と脾臓が続くことがわかります(図4a)。
生体内分布研究の期間中、さまざまな臓器でSWCNTが分解したという証拠がいくつかあります(図4a、b)。臓器内のSWCNTの分解は、多層カーボンナノチューブがマクロファージで分解されるという以前の発見に基づいて予想されます[42]。この調査で使用したSWCNTの平均直径は0.8nm、平均長さは1500 µmです。 Zhuらの研究に基づくと、このサイズは細胞毒性があるとは予測されていません。 [43]、長さと直径に基づいてカーボンナノチューブの毒性による脂質二重層の損傷の可能性を分類した。この分類によると、使用したSWCNTは「生物学的に柔らかい」カテゴリーに属し、細胞毒性を最小限に抑えています。これは、SWCNTの投与の結果として副作用や組織病理学的毒性が観察されなかったマウスでの研究での観察と一致しています。 -ANXA5コンジュゲート。
結論
ここでは、抗CTLA-4ベースのチェックポイント阻害と組み合わせたSWCNT-ANXA5バイオコンジュゲートによる光熱療法を使用して、進行性転移性乳がんのマウスで比較的高い生存率を得る新しい組み合わせ治療法を示します。腫瘍血管標的タンパク質ANXA5の使用により、低用量で原発腫瘍を根絶するために必要な全身送達されたSWCNTの量が最小限に抑えられました。興味深いことに、原発腫瘍のみが照射されたにもかかわらず、コンビナトリアル療法で治療された転移性癌のマウスの生存率の増加に注目しました。重要な脾臓抗腫瘍エフェクター細胞の数を定量化する機構的研究により、両方の治療法の組み合わせのみがCD4 + の数を増加させることが明らかになりました。 ヘルパーとCD8 + 細胞傷害性T細胞。 T細胞のこの増加は、抗腫瘍エフェクター細胞が腫瘍転移を抑制した腹膜反応を反映していると仮定します。 SWCNTは、投与後4か月でも臓器に存在することがわかりましたが、実験の過程で副作用や明らかな組織毒性は観察されませんでした。
データと資料の可用性
すべてのデータは制限なしで完全に利用可能です。
略語
- SWCNT:
-
単層カーボンナノチューブ
- ANXA5:
-
アネキシンA5
- anti-CTLA-4:
-
抗細胞毒性Tリンパ球関連タンパク質4
- EDTA:
-
エチレンジアミン四酢酸
- SDS-PAGE:
-
ドデシル硫酸ナトリウム-ポリアクリルアミドゲル電気泳動
- DSPE:
-
1,2-ジステアロイル-sn-グリセロ-3-ホスホエタノールアミン
- PTT:
-
光熱療法
ナノマテリアル
- カーボンナノチューブはフレキシブルエレクトロニクスの限界を押し上げる
- 癌治療のためのナノ粒子:現在の進歩と課題
- NIR-II光熱治療用のBSAコーティングされた金ナノロッド
- グラファイトナノプレートレットを備えた多層カーボンナノチューブに基づくハイブリッド複合材料の電気的性質
- リチウムイオン電池の電気化学的性能が向上したLiNi0.8Co0.15Al0.05O2 /カーボンナノチューブの機械的複合材料
- 黒色腫の標的化学療法治療のための薬物送達担体としての131I追跡PLGA-脂質ナノ粒子
- 非常に効果的な標的膵臓腫瘍治療のための、血液循環が延長され、生体適合性が改善されたレスベラトロール負荷アルブミンナノ粒子
- ヒドロキシル基を介したカーボンナノチューブのスライドロール運動モードの調整
- 光熱治療のためのポリドーパミンカーボンドットの簡単なワンポット合成
- 効率的な光線力学癌治療のためのセラノスティックナノエージェントとしてのカーボンドット@プラチナポルフィリンコンポジット
- 膀胱癌細胞を阻害するための疎水性修飾プルランナノ粒子を用いたミトキサントロンの新規送達および阻害効率に対するナノ薬物サイズの影響



