貴金属ナノ粒子合成の現在の戦略
要約
貴金属は何世紀にもわたって人類の歴史に不可欠な役割を果たしてきました。しかし、ナノテクノロジーと材料科学の最近の進歩との統合は、学界と産業界の両方で新しい研究の機会を提供し、医療を含む新しい一連の高度なアプリケーションをもたらしました。貴金属ナノ粒子(NMNP)は、個別化医療および診断における重要性のため、過去数十年にわたって生物医学の分野で非常に重要でした。特に、プラチナ、金、銀のナノ粒子は、抗菌剤や抗ウイルス剤、診断薬、薬物担体、イメージングプローブなどの生物医学的用途を含む、非常に多様な産業用途のおかげで、リストの中で最も支配的なスポットを達成しています。特に、極端な腐食条件や酸化に対する優れた耐性が高く評価されています。特に、過去20年間で、高度に調整可能な物理化学的、光学的、熱的特性、および生化学的機能を材料に提供する、より費用効果が高く堅牢なNMNP合成法の新しい戦略の開発に大きな進歩がありました。その結果、ポリマー、グラフェン、カーボンナノチューブ、量子ドット、コアシェルシステムを備えた新しい高度なハイブリッドNMNPが開発され、物理化学的特性がさらに強化され、優れた診断および治療アプリケーションが実現しました。このレビューでは、NMNP(Au、Ag、Pt)の合成における現在の進歩を要約することを目的としています。
はじめに
貴金属は非常に長い間使用されており、最初のエジプト文明にまでさかのぼり、常に優れた権力と富のしるしと見なされてきました。その結果、それらは高価な芸術作品、コイン、宝石などの形で歴史の中で見ることができます[1]。これらの金属は、地球の地殻で利用できるため、一般的に他の金属よりも高価になる傾向があります[2、3]。それらの堅牢な性質、腐食および酸化の極端な条件に対する耐性のために、それらは航空宇宙、自動車、化学、エネルギー、電気および電子産業、さらに重要なことにヘルスケア(外科用機器からイメージングのコントラストエンハンサーまで)で広く使用されています[4 、5]。
過去20年間で、ナノテクノロジーは最も有望な将来のテクノロジーであることが証明されており、数え切れないほどの可能性を提供しています。学術および産業部門からの学際的なサポートにより、この分野は最も急速に拡大しており、非常に有望な成果が得られています[6、7、8]。現在、ナノスケールレベルでの金属の合成と制御における技術的飛躍は、個別化医療、診断、および治療を進歩させるための計り知れない研究機会を提供しています[9、10、11]。金属ナノ粒子(MNP)は、その印象的な物理化学的特性と、バルク材料(金属)と比較して大きな表面積対体積比のために、最も一般的かつ広く研究されていることが判明しています。生物医学的用途に関しては、NMNPは、過酷な環境への耐性のために自然な選択となりました。それらは、高感度の診断アッセイ、放射線療法の熱焼灼促進剤、および薬物および遺伝子送達媒体として適用されてきました[3、12、13]。
最近のナノテクノロジーと材料科学の融合により、個々のコンポーネントと比較して、熱的、触媒的、電気的、光学的、機械的特性が大幅に向上した新しいナノコンポジット材料が開発されました。特に、NMNPで作られた複合材料は、ナノスケールのビルディングブロックの変更に重要な役割を果たし、触媒作用(主に電極触媒作用)、光学系、ナノ医療、環境保護に幅広い用途をもたらす印象的な物理化学的特性により、多くの研究関心を集めています。 14,15,16,17]。コロイド状態の貴金属は、主に治療および診断におけるそれらの有効性のために、集中的な研究の対象となっています[2、18]。同様に、酸化グラフェンや還元型酸化グラフェン[14、19、20]、量子ドット[21、22、23]、カーボンナノチューブ[24、25、26]などの材料の合成の改善は、より実現可能で効果的なものに貢献しています。 NMNCの形成方法。
Au、PtNP、およびNMNPのサイズが小さく、表面積対体積比が大きく、高電子移動プロセスを支援できるため、電気化学センサーとしてのアプリケーションに最適です[27、28、29]。 NMNPの光学特性は、多くの研究、特にAgとAuNPのトピックとして役立ってきました。これらのNPは、さまざまな波長の光(Auによる可視領域から近赤外領域への広範な散乱)に対して異なる応答をすることができるため、表面増強ラマン分光法(SERS)、局在表面プラズモン共鳴の信号増強剤として適用されます。および他の共鳴散乱分光法[30、31、32、33]。 AuNPの広範囲に調整可能な光学特性と生体適合性により、腫瘍の光熱治療とin vivoイメージング(光音響イメージング)に適用されています[34、35、36]。最近、AgNPは光熱療法でもその可能性を示しており、一般にAgコアシェルシステムまたは複合材料(酸化グラフェン/カーボンナノチューブが還元されたもの)として適用されています[37、38、39]。 NMNPと細胞および組織との生体適合性により、診断における幅広い適用性が開かれました[14]。 NMNPおよびNMNC(特にグラフェン)のバイオセンサーは、既存の生体分子診断法よりも優れた精度と特異性の向上に重要な役割を果たしてきました[40、41]。一般に、AuおよびPtNPは、生体分子に吸着する能力とその最高の導電性および安定性により、新しいバイオセンサーおよびプローブの開発に使用されます[42、43、44、45]。その結果、NMNP自体またはNMNCの形式で、免疫センサー[46]、検出用の生体分子[47]、およびナノプローブ(in vivo細胞イメージング、疾患進行の病因の追跡および研究用)[2、6、48 ]。 NMNPとNMNCのこれらすべての利点にもかかわらず、人体におけるそれらの安全性プロファイルに関しては、依然として多くの質問と議論があります[49,50,51]。
このレビューでは、NMNP(Ag、Au、Pt)とNMNC(Ag、Au、Ptを含む)の合成方法論と、NMNCが示す相乗効果を含む治療および診断としての生物医学アプリケーションの現在の開発に関する調査を提供します。材料研究で現在注目されているトピックである、パフォーマンスの向上という観点からNMNPを使用します。
NMNP合成の現在の傾向
NMNPの合成方法
NPの準備は、基本的に2つの異なるアプローチ、(1)トップダウン(破壊的方法)と(2)ボトムアップ(建設的方法)に従います(図1)。
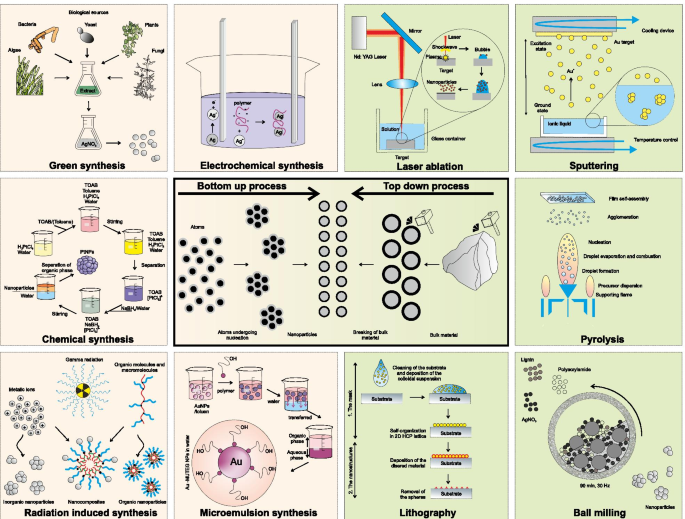
ナノ粒子合成のトップダウン(背景が緑色の画像)およびボトムアップ(背景が淡黄色の画像)アプローチの概略図。画像は[52,53,54,55,56,57、 58,59,60]
トップダウンプロセスでは、さまざまな物理的および化学的方法を使用して、バルク材料をナノ寸法の小さな粒子に分解します。対照的に、ボトムアップアプローチでは、NPは、原子、分子、またはクラスターの自己組織化によって生成されます。トップダウンアプローチには、材料を希望の順序と形状に切断、フライス盤、成形する外部制御プロセスが含まれます。熱分解[61、62]、ナノリソグラフィー[63、64]、熱分解[65]、放射線誘発法[66,67,68]などのいくつかの物理的方法がこのカテゴリーに属します。ただし、このアプローチには大きな制限があります。これは、結果として得られるMNPの不完全な表面構造であり、物理的および化学的特性に大きく影響します[1]。さらに、この方法は、合成手順中に高圧および高温条件を維持するために膨大な量のエネルギーを必要とし、プロセスを高価にします。
ボトムアップ方式では、NPは、化学的および生物学的手順を使用して、対応する原子、クラスター、および分子から組み立てられます。ボトムアップアプローチは、より均一なサイズ、形状(物理的パラメーター)、および化学組成で最終生成物の形成をはるかによく制御できるため、有利であることが判明しています。さらに、このアプローチは一般的に安価です。ボトムアップアプローチは、一般に、化学[69、70]、電気化学[71,72,73]、音響化学[74、75]、グリーン合成[76、77]などの湿式化学合成手順です。ボトムアップアプローチでは、反応混合物(有毒化学物質、有機溶媒、試薬)から合成粒子を精製することは、グリーン合成法を除いて、生物医学的応用に疑問を投げかける大きな課題です。
トップダウンアプローチ
スパッタリング
スパッタリングは、最も一般的に使用される合成プロトコルの1つであり、基板上でのイオンの衝突とそれに続くアニーリングによって生成される薄層としてのNPの堆積が含まれます。この方法は、物理蒸着(PVD)法とも呼ばれます[78、79]。この方法の効率は、主に層の厚さ、基板の種類、アニーリング時間、温度などの要因に依存します。これらの要因は、NPのサイズと形状に直接影響します[55、80、81]。
マイクロパターニング
バイオセンサー、マイクロアレイ、組織工学、細胞研究[82]で採用されている一般的な手法であるマイクロパターニングは、MNPの合成にも使用されます。一般に、この手法は、適切な前駆体からナノ構造アレイを合成するために、光ビームまたは電子ビームのいずれかを使用して、材料を必要な形状とサイズに切断または成形する印刷プロセスと同等です。これは、MNPインクのレーザー焼結を使用してMNPを合成するためにフォトリソグラフィーを使用する低温の非真空法です[83、84]。フォトリソグラフィーとは別に、スキャン、ソフトナノインプリント、コロイド、ナノスフェア、電子ビームリソグラフィーなどの多くのリソグラフィー技術が開発されています[2、57、85、86]。
フライス盤
フライス盤は、バルク材料をマイクロ/ナノ構造に直接分解することを伴うため、一般にトップダウンプロセスの公の顔として表されます。機械的フライス盤では、ローラー/ボールの運動エネルギーがバルク材料に伝達され、その結果、粒子サイズが小さくなります[87]。ミルのタイプ、ミリング雰囲気、ミリング媒体、強度、時間、温度などのパラメーターは、NPの形状とサイズを制御する上で重要な役割を果たします[88、89]。これらの制約を克服するために、シェーカーミル、タンブラーミル、振動ミル、摩耗ミル、遊星ミルなど、さまざまな技術が開発されています。
レーザーアブレーション
レーザーアブレーションは、処理時間が速く、粒子のサイズと形状をより適切に制御し、長期安定性を高めて高収率を実現するため、従来の化学的方法の適切な代替と見なされる方法の1つです[78、90 、91,92]。レーザーアブレーションプロセスでは、固体表面(通常は純金属のプレート)にレーザービームが照射され、低フラックスのプラズマプルームが生成されます。このプルームは最終的に蒸発または昇華してNPを形成します[93]。より高いフラックスでは、材料はプラズマに変換されます。過剰な試薬を除去する必要がないこと、および水性溶媒と有機溶媒の両方での金属ナノ粒子合成の可能性により、生体分子とMNPのinsitu結合などの生物医学的用途でのレーザーアブレーション法の実装が可能になりました。標準的な手法よりも効果的である[54、94、95]。
熱分解
熱分解は、MNP合成のために個別にまたは他の物理的方法と組み合わせて一般的に使用されるもう1つの重要な手法です[78]。これは吸熱化学分解プロセスであり、熱を使用して化合物の化学結合を切断し、前駆体を分解して化学反応させ、他の副生成物とともに灰の形でNPを生成します。得られた固形灰をさらに処理することにより、NPが回収されます。熱分解は、高貴なMNPの調製に頻繁に使用されます[56、96、97]。過度のエネルギー消費は、この方法の最も重要な欠点の1つです。
化学蒸着
この方法は、真空堆積法としても知られており、ガス状の反応物が、基板の過熱を促進する他のガス分子の組み合わせとともに、薄膜として基板上に堆積されます。反応中、基質は結合したガスと接触し、イオンの還元につながります[78]。この反応の生成物は通常、NPを削り取る必要のあるフィルムの形をしています。この方法では、高純度で均一な非多孔質ナノ粒子が生成されます。その結果、この方法は電子機器および半導体業界で非常に重要になっています。これらの大きな利点にもかかわらず、この方法にはいくつかの大きな欠点があります。反応用のフィルムとチャンバーを作るための特別な装置の必要性、およびこの反応のガス状副生成物が非常に有毒であるという事実[98]。
>ボトムアップアプローチ
溶液中の金属イオンの還元
このアプローチは、好ましい反応パラメータ(pH、温度など)の下で安定剤の存在下で様々な化学還元剤を使用することにより、それらのイオン性塩から金属イオンを還元することを含む。この手順は、その非常に単純なため、すべてのボトムアップアプローチの中で最も一般的で信頼性の高い方法です[2、99]。このプロセスでは、一般的に使用されるクエン酸ナトリウム[10、100]、タンニン酸[99]、ボロ水和物ナトリウム[101]、ヒドラジン、水素、水素化アルミニウムリチウム、およびアルコールを含む多数の還元剤の広範なリストを利用できます。使用する[2、60]。同様に、安定剤に関しては多くの選択肢があり、それらは一般に(1)低分子量(例えば、クエン酸塩、SDS、キトサンなど)と(2)高分子量のものの2つのカテゴリーに分類されます。 (例えば、でんぷん、トゥイーン、PVP、PEG、DISPERBYKなど)。低分子量安定剤(一般的に帯電した洗剤)は、合成された粒子の表面電荷を変化させ、粒子間の反発力を維持して凝集を防ぐ傾向があります。このタイプの安定剤は、一般に、環境ストレス要因(特に保管温度と露光量の変化)から十分に保護しません。高分子量安定剤は一般に粒子を飲み込み、環境ストレスから粒子を保護します。それらは、低分子量安定剤よりも効率的であることが示されています。それらの利点にもかかわらず、それらの生物学的用途および触媒特性は、それらの溶解を妨げる粒子上の安定剤の厚い層のために疑わしい[102、103]。粒子サイズと形状の均一性に関して、明確な勝者は化学物質ベースの還元です。これは、反応パラメータ(pH、還元剤と安定剤の比率)を変えることで還元を容易に調整できるためです。 Tyagiと彼のチームは、室温、pH 3、クエン酸塩とAuCl 3 のモル比が2:1および5:1で、クエン酸塩還元法を使用してAuNPs [104]を生成しました。 の、平均サイズがそれぞれ28nmと25nmの粒子を生成します。このpHでは、反応は他のpH値よりもはるかに速かった。彼らはまた、プリズム、ロッド、球などのさまざまな形状のAuNPが、3〜6の範囲のpH値で形成されることを示しました(クエン酸塩とAuCl 3 のモル比は2:1です。 )。 AgNPの合成に同様のクエン酸還元法を適用したAgnihotriと共同研究者による別の研究[105]では、クエン酸ナトリウムの最高濃度(4.28×10 –3 <)で平均サイズ5nmの粒子が得られました。 / sup> mol dm -3 )。それらのサイズは、クエン酸塩の濃度が高くなると増加しました(1.77×10 –2 で100nmに mol dm -3 )。 Houらによる別の研究。 [106]は、電極触媒用途向けのヒドロゾルの形での非常に安定した単分散のPtナノ粒子の合成について説明しました。
マイクロエマルジョン
マイクロエマルジョンに基づく金属NPの製造は、非常に興味深いトピックになりつつあり、サイズや形状など、合成されたナノ粒子の物理的側面をより適切に制御できる効果的な方法としても浮上しています。一般に、マイクロエマルジョンは、界面活性剤の存在下での2つの非混和性液体の単なる混合物です。これらのシステムは一般に、超低界面張力、大きな界面面積、および熱力学的安定性を備えています[107]。 NMNPの最初のマイクロエマルジョンベースの合成は、Muñoz-Floresらのチームによって説明されました。 [58、108、109]プラチナ、パラジウム、ロジウムのNPを合成した人。マイクロエマルジョンベースのNP合成では、2つの別々のマイクロエマルジョンが調製されます。1つはイオン性塩を含み、もう1つは両親媒性環境で生成された還元剤を含みます。エマルジョン間の衝突により、反応物が混合され、イオンが塩から中性原子に還元され、ナノ粒子が形成されます[2]。油中水系は一般に金属ナノ粒子の合成に使用され、この方法で生成されるナノ粒子はエマルジョンの形で得られるため、一般に熱力学的に安定しています。必要に応じて、このプロセスは、界面活性剤と油の比率を変えることにより、特定のタイプのナノ粒子を合成するように調整することもできます。これにより、粒子のサイズと形状を制御できるようになります[110]。
電気化学的方法
電気化学的プロセスは、NMNPおよびナノコンポジットの合成に一般的に使用されます。これらは主にそれらの触媒特性に使用され、最近ではバイオセンサーとして生物医学アプリケーションで使用されています[111]。電気化学法は、1994年にReetzとHelbigによって最初に導入されました。彼らは、アノードから純粋な金属シートを溶解して、電解質の存在下で電気化学セルのカソードに金属塩を堆積させ、ナノ粒子を生成しました[2、112]。 。この方法の有効性は、還元剤の性質、金属と安定剤の純度、電解質の選択、濃度比、温度などのさまざまなパラメーターに依存し、NPの物理的パラメーターに直接影響します[53]。現在、電気化学的方法を使用したナノコンポジット(特にグラフェンを使用したもの)の合成は、NPの合成よりも好ましい[113]。
放射線誘発合成法
この方法では、金属ナノ粒子の合成に電離放射線(特にガンマ線とX線とUV光を含む)を使用します。完全に還元された高純度(副産物を含まない)金属ナノ粒子を提供するため、従来のNP合成方法と比較して非常に効率的であることが証明されています。このトピックは、いくつかのレビュー[59、66、114、115]でうまくカバーされています。このプロセスでは、還元剤と安定剤の水溶液が放射線を介した放射線分解にさらされ、NPが形成されます。放射線被曝中に、水分子は分解し、強力な酸化剤または還元剤として作用し、金属イオンを中性金属原子に還元する一時的な生成物を生成し、さらに核を形成してNPを形成します。シンクロトロンX線技術により、コロイド状NPの成長軌道をリアルタイムで監視することができました[116]。 NPの合成に重要な物理的パラメータには、放射線量、システムのpH、および合成に使用される溶媒の種類が含まれます[117]。最近、放射線誘発合成が、抗菌用途のトゥイーン80安定化AgNPの生成に使用されました[118]。
マイクロ波によるグリーン合成法
一般に、マイクロ波支援合成はワンポット合成としても知られており、塩および界面活性剤溶液からのNPの合成が含まれます。これは、合成されたNPの形態の制御をサポートする信頼性が高く、高速で簡単な方法です[2]。この方法は、双極子相互作用(分子はマイクロ波の振動電場と歩調を合わせて整列し、振動する傾向があり、それらの間の衝突と摩擦が熱を引き起こす)とイオン伝導(分子が試みるときに電場がイオン運動を生成する)の原理に基づいて機能します急速に変化する電場に向きを変え、瞬間的な過熱を引き起こします)加熱効果を生み出し、その結果、金属イオンがNPに還元されます[119、120]。マイクロ波照射時間と反応物の濃度は、主にNPの形態学的パラメーターを決定します。最近、マイクロ波支援合成によって調製された超常磁性マグネタイトNPの単分散性や粒子サイズなどの物理的特性は、合成のさまざまな段階でのフメート-ポリアニオンの注入によって制御されました[121]。マイクロ波誘起放電は、溶媒や界面活性剤の非存在下での金属粒子からのCu、Ni、およびZnナノ粒子の合成にも使用されました[122]。
グリーン合成メソッド
化学合成における化学物質の過度の使用は、NMNPの生物学的応用の将来をほぼ危うくしています。これにより、化学物質の使用を最小限に抑えた他の生態学的手法の探求がもたらされました。植物抽出物、微生物、生体高分子を使用するグリーン合成法は、NP合成の化学的方法に代わる有力な候補であることが証明されています(図2)[123]。よりシンプルで環境に優しい方法論のおかげで、過去20年間で出版物が指数関数的に増加しました[52、124、125]。
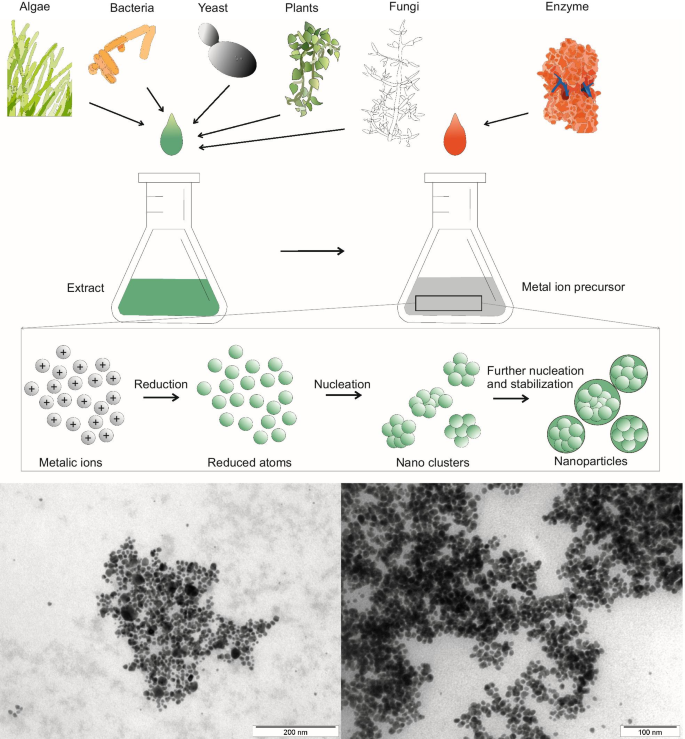
グリーン合成法の概略図
NMNPSのバイオシステム合成
経済的および環境的に有益な方法の開発の探求は、ナノ粒子の合成の潜在的な候補としての微生物の探索につながりました[126、127]。生物学的システムは、原子と分子の階層的組織の優れた例であり、ナノマテリアルの準備のための潜在的な細胞工場として微生物を使用するように研究者を引き付けます。原核生物(細菌)と真核生物(藻類、真菌、植物)の両方の種が、NPのグリーン合成に使用されます[123]。
バクテリアベースのナノ粒子合成
金属が豊富な環境に繰り返しさらされてきたバクテリアは、これらの極端な条件に対する耐性を発達させることがよくあります[128]。したがって、原核生物はナノ材料を生産するための自然な選択となっています。 シュードモナススタッツェリ 銀山から分離された金属蓄積細菌であるAG259は、クラウスらによって利用されました。 [129]最大200nmのサイズの金属銀の細胞内ナノ結晶を作成します。 NPの細胞外合成は、Shahverdiとその同僚によって最初に報告されました[130]。ここで、AgNPは水性Ag + の還元によって生成されました。 グラム陰性菌、すなわちエンテロバクタークロアカエのさまざまな培養上清を介したイオン 、 Escherichia coli およびクレブシエラ肺炎 。合成速度は細胞内合成よりもはるかに速かったため、細胞ろ液に遭遇したAg +イオンから5分以内にAg-NPが合成されました。微生物、すなわち Bacillus licheniformis によって産生される細胞外レダクターゼ酵素 および Bacillus clausii 、銀イオンを中性銀に還元し、ナノサイズの粒子を生成します。これらの微生物のタンパク質アッセイにより、NADH依存性レダクターゼ酵素が銀イオンの銀ナノ粒子への生体内還元に重要な役割を果たしていることが明らかになりました。レダクターゼ酵素は、NADH酸化からNAD +への電子を取得します。酸化中、酵素も同時に酸化され、銀イオンがAgNPに還元されます。場合によっては、硝酸塩依存性レダクターゼも生体内還元に関与する可能性があることが観察されています[131,132,133]。さらに、いくつかの細菌株(グラム陰性菌およびグラム陽性菌)、すなわち A。カルコアセチカス、B。アミロリケファシエンス、B。フレクサス、B。メガテリウム および S。アウレウス 、AgNPの細胞外生合成と細胞内生合成の両方にも使用されています[123]。同様に、AuNPとPtNPも、バクテリアによる金と白金の塩の蓄積と還元によって調製されます。 B。 licheniformis、B。メガテリウム 、 Delftia sp KCM-006。、 Shewanella sp 。、ステノトロホモナスマルトフィリア および Lactobacillus sp 。金ナノ材料を生産するために使用されてきたバクテリアのいくつかの例です[134、135]。さらに、バクテリア Shewanella sp 。およびアシネトバクター・カルコアセチカス PUCM 1011はPtNPの調製に利用されました[136、137]。バクテリアを介した合成は、その緑色の性質と粒子の形状とサイズの制御(主に細胞外合成)の点で有望ですが、取り扱いの難しさや低収量などの欠点があります。
真菌ベースの合成
近年、真核微生物を用いたNMNP合成は、高い細胞内金属取り込み能力、異なる化学組成のNPを合成する能力、単位バイオマスあたりの大量の酵素を生成する能力、および容易なバイオマス処理により、原核生物のより良い代替物として浮上しています。実験室規模で[131]。
一般に、真菌は、金属の生体内蓄積能力、耐性、高い結合能力、および細菌のような細胞内取り込みにより、金属NPを合成する可能性があります[127]。真菌はNPの合成に細胞内法と細胞外法の両方を使用します。細胞外合成は、Ag + を変換する大量の細胞外酵素を生成する能力があるため、最も一般的に報告されている合成メカニズムです。 イオンからナノスケールの銀粒子[138,139,140]。細胞内合成では、Ag + イオンは、酵素の負に帯電したカルボン酸基と正に帯電したAg + の間の静電相互作用によって細胞表面に吸着されます。 イオン。 Ag + イオンは後に細胞壁に存在する酵素によって還元されてAgNPを形成します。このプロセスでは、NPは溶液ではなく菌糸体の表面に形成されます。 2001年、 Verticillium sp を使用したAuNPの細胞内調製 Mukherjeeらによって最初に報告されました。 [141]、ここでAu 3+ テトラクロロ金酸からのイオンは真菌細胞内で還元され、20nmのサイズ範囲内の粒子が形成されました。ワッハーブ派と同僚[142]は Trichodermareesei を採用しました AgNPs合成の場合、バイオマスを含む培地にAgNO 3 を接種しました。 そして72時間にわたってインキュベートすると、5〜50nmのサイズ範囲のAgNPが形成されます。同様に、Vigneshwaranらのチームによる別の研究。 [138]は、 Aspergillus flavus からのAgNPの細胞内合成を実証しました そして、細胞壁の酵素が主に還元に関与し、タンパク質が安定化に関与していることを報告しました。より速い合成、および合成された粒子のサイズと形状のより良い制御などのこれらすべての利点にもかかわらず、細胞内プロセスは、NPが細胞に結合するため、プロセスを困難かつ高価にする製品回収の点で大きな欠点に悩まされます。結果として、細胞外合成が好ましい。細胞外合成では、無細胞培養液/懸濁液が合成プロセスで使用され、より環境に優しく、費用効果が高いことがわかります。 2016年、バラクマーランらのチーム。 [143] Aspergillus terreus の無細胞懸濁液を使用しました AuとAgNPの両方を合成するために、AgとAuNPでそれぞれ8〜20 nmと10〜50nmのサイズ範囲の球状ナノ粒子が生成されます。粒子のFTIR評価により、タンパク質とNPの結合が確認されました。
藻類ベースの合成
藻類を介したNPの合成には、次の4つの方法があります。(1)藻類細胞全体を、遠心分離を使用して特定の成長段階で培地から回収し、金属塩の水溶液に直接分散させます。 (2)新たに採取または凍結乾燥した細胞から作られた無細胞水性抽出物。 (3)粉砕された、新鮮な、または乾燥した藻類の水性抽出物濾液または上澄み。 (4)藻類ブロスの水性濾液。抽出物を介した合成は、最も一般的に報告されている藻類ベースの合成メカニズムです[131、144]。 Chlorella vulgaris の乾燥細胞懸濁液では、AuNP(9〜20 nm)の形で金元素が蓄積していることがわかりました。 Hosea et al。によると、時間の経過とともに金の濃度が増加することも報告されており、テトラクロロ金酸から金イオンを取り込み、還元する藻類細胞の能力が証明されています[145]。 Velgosovaと共同研究者[146]は、 Parachlorella kessleri からの非常に安定したAgNPの合成について報告しました。 、緑藻の水性抽出物で、合成された粒子のサイズ範囲は約20 nmで、1年間にわたって優れた安定性を示しました。 Pithophora oedogonia などの他の藻類sp 、ホンダワラ および Plectonema boryanum 、Ag、Au、PtNPをそれぞれ構築するために使用されています[147,148,149]。
植物ベースの合成
植物および植物抽出物を介した合成は、最も一般的に報告されている合成方法論です[123、135、150]。このタイプの合成は、植物合成と呼ばれます。この合成法の主な利点は、製品の回収が容易なことです。 2003年、Gardea-Torresdey他のチーム。アルファルファもやし( Medicago sativa )を備えた生きた植物システムを使用した金属ナノ粒子(AgNP)の合成を最初に説明したのは )寒天培地で。根は、媒体からAgを吸収し、同じ酸化状態でシステムのシュートに沿って輸送する傾向があります。シュートでは、Ag原子がさらに配置されてAgNPを形成します。同様に、別の研究では、アルファルファ植物のセクレトームを使用して、Au + を減らしました。 Au 0 へ 、これも同様の手順に従ってAuNPを生成しました[151]。植物抽出物を介した合成では、NPの合成に植物成分(葉、茎、根、新芽、花、樹皮、種子)抽出物を使用します。この方法の主な利点は、抽出物が還元剤として機能する能力です。および安定剤[152]。この方法は、長期安定性を備えたナノ粒子を製造するための最も費用効果が高く、ユーザーフレンドリーな方法であることが証明されています。 2016年、Balashanmugam他のチーム。 Cassia roxburghii からのAgNPの植物性合成を実証しました 水性葉抽出物。合成されたAgNPは約35nmのサイズ範囲であり、1年間にわたって優れた安定性を示しました。この方法はまた、個々の粒子とバイメタル粒子の両方の合成を容易にしました。ニーム(アザディラクタインディカ )葉の抽出物はShankarらによって首尾よく使用されました。 [153]銀、金、バイメタルのAu / AgコアシェルNPを準備します。同様の植物抽出物(樹皮、葉、果実、ガム)は、さまざまなNMNPを生成するために数人の研究者によって使用されてきました[153,154,155]。現在、光誘起ナノ粒子が脚光を浴びています。これは、この手順により、混合物を太陽光にさらす際の合成が速くなるためです。クマール等。 [156]使用 Erigeron Bonariensis 13 nm(TEMサイズ)のサイズ範囲の球状および楕円形のAgNPを生成する銀ナノ粒子を合成するための水性葉抽出物。この合成で考慮すべき重要なパラメーターは、露光時間と反応系の植物抽出物の濃度です。
結論
NPの合成のために、いくつかの物理的、化学的、および生物学的方法が開発されてきました。これらのプロセスはすべて、ナノ製品の有用性と適用性に基づいて広く使用されています。ただし、既存の各プロトコルには特定の欠点があり、これらのプロセスのほとんどは大規模な生産のためにスケールアップすることはできません。したがって、制御された調整可能な特性を備えたNPを製造するための代替プロセスの開発は、依然として未解決の課題です。
データと資料の可用性
該当なし。
略語
- NM:
-
貴金属
- NP:
-
ナノ粒子
- NMNP:
-
貴金属ナノ粒子
- AuNPs:
-
金ナノ粒子
- AgNPs:
-
銀ナノ粒子
- PtNPs:
-
白金ナノ粒子
- NMNC:
-
貴金属複合材料
- PVD:
-
物理蒸着
- SDS:
-
ドデシル硫酸ナトリウム
- PVP:
-
ポリビニルピロリドン
- PEG:
-
ポリエチレングリコール
- AuCl 3 :
-
塩化金
- NADH:
-
ニコチンアミドアデニンジヌクレオチド
- TEM:
-
透過型電子顕微鏡
ナノマテリアル



