再吸収抑制タイプII /タイプIZnSe / CdS / ZnSコア/シェル量子ドットの合成と免疫吸着アッセイへのそれらの応用
要約
複合タイプII /タイプI構造とその結果としての再吸収抑制特性を備えたZnSe / CdS / ZnSコアシェル量子ドット(QD)を合成するためのホスフィンフリーワンポット法を報告します。合成されたままのQDは、高効率の赤色発光(量子収率82%)と高い光学安定性を備えています。タイプIのQDと比較して、ZnSe / CdS / ZnSのQDは、ストークスシフトが大きく、再吸収が少ないため、発光損失を減らし、蛍光出力のレベルを向上させることができます。 ZnSe / CdS / ZnS QDは、蛍光標識として使用され、検出限界(LOD)が0.85のC反応性タンパク質(CRP)の検出において、蛍光結合免疫吸着アッセイ(FLISA)でのアプリケーションを初めて活用します。 ng / mL。これは、CdSe / ZnSタイプIQDベースのFLISA(1.00 ng / mL)よりも感度が高くなります。この結果は、ZnSe / CdS / ZnSタイプII /タイプIQDが、生物医学情報検出のアプリケーションに適している可能性があることを示しています。
背景
蛍光コア/シェル半導体量子ドット(QD)は、従来の有機色素よりも広い発光範囲、高いフォトルミネッセンス(PL)量子収率(QY)、高い光学的および化学的安定性などの優れた光学特性を特徴としています。これらの利点は、生物医学診断、分子イメージング、および光電フィールド用の蛍光標識の革新的な進歩の機会を開きます[1,2,3,4,5,6,7]。コアとシェルの材料間のバンドアラインメントに従って、コア/シェルのQDは、タイプI、逆タイプI、およびタイプIIの構造に分類できます。電子と正孔の両方をコア領域に閉じ込めて放射再結合を強化し、光学活性コアの表面を周囲の媒体から物理的に分離してPL強度を向上させる、「ネストされた」バンドアライメント構造を特徴とするタイプI量子ドットおよび光学安定性[6,7,8,9]。これらの好ましい特性にもかかわらず、吸収スペクトルとPLスペクトルの差と呼ばれる小さなストークスシフト(わずか数十ナノメートル)が深刻な再吸収を引き起こし、全体的な発光損失を引き起こし、定量測定への適用を制限します[10、 11]。対照的に、バンドギャップアラインメントがずらされたタイプII QDは、コア/シェル構造の異なる領域への電子と正孔の空間的分離を促進します。後続のバンドエッジe–h再結合遷移エネルギーは、構成材料コンポーネントのいずれかのバンドギャップよりも小さく、どちらの単一コンポーネント材料でも利用できない、大幅な赤方偏移発光につながります。タイプII量子ドットの最初の励起子吸収機能の振動子強度は、コア量子ドットの振動子強度と比較して劇的に減少します[12、13]。主に赤方偏移した発光と平坦化された最初の励起子吸収ピークは両方とも、吸収スペクトルと発光スペクトルのオーバーラップを低下させ、再吸収を抑制し、生物学的定量的検出に役立ちます。典型的なタイプIIZnSe / CdS QDは、青みがかった紫から赤の範囲まで調整可能な発光を示し、再吸収が抑制されています[13]。ただし、CdSシェルで非局在化された電子は、表面欠陥または周囲の媒体からのトラップに対して脆弱であり、蛍光量子収率が低くなります。実行可能な解決策は、量子収率と光学的安定性を高めるために表面を不動態化するだけでなく、有毒なCd元素の漏れを制限し、生物毒性を減らすために、ZnSe / CdSQDをZnS最外殻でコーティングすることです。これまでのところ、研究の大部分はタイプI QDに焦点を当てており、ZnSe / CdS / ZnSタイプII /タイプIQDについてはごくわずかしか実施されていません[12、13、14、15]。さらに、ZnSe / CdS / ZnS QDの合成プロセスに関するすべての研究では、粗ZnSeコアQDを前精製することによる2段階の調製を使用し、有毒で高価なホスフィンを使用しました。さらに、生物学的検出におけるZnSe / CdS / ZnSQDの適用を伴うものはありませんでした。
ここでは、再吸収抑制とQDの最初の使用の機能を備えた高品質の赤色発光ZnSe / CdS / ZnSタイプII /タイプIコア/シェルQDを合成するためのホスフィンフリーワンポット法を報告します。蛍光結合免疫吸着測定法(FLISA)を作成します。反応性が高く毒性の低いSe前駆体(ODE-Se)とオレイン酸亜鉛を使用して高品質のZnSeコアQDを合成し、コア量子ドットを精製することなくマルチシェル成長を実現しました。これは、コア/シェル量子ドットの大規模合成に大きな期待を示しています。調製されたままの赤色発光ZnSe / CdS / ZnSタイプII /タイプIQDの量子収率は、生物医学分野での生物毒性を低減するために特に重要な低毒性カドミウム含有量で82%に達する可能性があります。さらに、QDには大きなストークスシフトと平坦な最初の吸収ピークがあり、PLと吸収スペクトルのオーバーラップが低くなり、再吸収効果が抑制されます。
肝細胞からの急性期タンパク質としてのC反応性タンパク質(CRP)は、感染症および自己免疫疾患の初期の指標と見なされてきました。そのような病気はしばしば非常に低いCRPレベルで始まります。したがって、生物学的サンプル中のCRPレベルの高感度の定量的イムノアッセイ分析は、疾患の進行を診断および監視するために非常に重要です[16]。従来の酵素結合免疫吸着測定法(ELISA)と比較して、FLISAは酵素反応なしで時間を節約し、蛍光QDの光学的品質に由来する環境条件に対する感度が低くなります[17]。したがって、FLISAは定量的イムノアッセイの新しい研究ホットスポットになりました[2、18、19、20、21]。ここでは、最初に、水溶性ZnSe / CdS / ZnSタイプII /タイプIコア/シェルQDを蛍光プローブとして使用するFLISA定量的イムノアッセイを実証しました。 CRPタンパク質の定量検出の検出限界(LOD)は0.85 ng / mLに達し、対照実験ではCdSe / ZnSタイプIQDベースのFLISAよりも15%感度が高かった。高いQY、優れた光学安定性、および低い再吸収効果により、生物医学および光電分野でのZnSe / CdS / ZnSタイプII /タイプIQDの適用が促進される可能性があります。
メソッド
化学薬品
酸化カドミウム(CdO、99.99%)、酸化亜鉛(ZnO、99.9%、粉末)、セレン(Se、99.9%、粉末)、1-オクタデセン(ODE、90%)、1-オクタンチオール(OT、98%)、オレイン酸(OA、90%)ポリ(無水マレイン酸-alt-1-オクタデセン)(PMAO)、および2-(N-モルホリノ)エタンスルホン酸(MES)はAldrichから購入しました。パラフィンオイル(分析グレード)、アセトン(分析グレード)、ヘキサン(分析グレード)、およびメタノール(分析グレード)は、中国の北京化学試薬株式会社から入手しました。 NaOH、HCl、Na 2 CO 3 、NaHCO 3 、KH 2 PO 4 、Na 2 HPO 4 、H 3 BO 3 、Na 2 B 4 O 7 ・10H 2 OおよびTween-20は、中国のShanghai Sangon Co.、Ltdから購入しました。ウシ血清アルブミン(BSA)と子牛血清はSigmaから購入しました。 1-エチル-3-(3-(ジメチルアミノ)プロピル)カルボジイミド(EDC)、N-ヒドロキシスルホスクシンイミド(スルホ-NHS)およびマイクロプレートはThermo Fisher Scientific(USA)から購入しました。マウス抗C反応性タンパク質モノクローナル抗体およびCRP抗原は、Abcam(USA)から入手しました。すべての化学薬品と溶媒は、さらに精製することなく、受け取ったままの状態で使用しました。
Se前駆体のストックソリューション(0.1 M)
Se(6 mmol)とODE(60 mL)を100 mLの3つ口フラスコに入れ、窒素下で220°Cに180分間加熱して、黄色の透明な溶液を得ました。
Zn前駆体(0.4 M)およびCd前駆体(0.2 M)のストックソリューション
ZnO(30 mmol)、オレイン酸(30 mL)、および45 mLODEを100mLの3つ口フラスコに入れ、窒素下で310°Cに加熱して透明な溶液を得ました。得られた溶液を注入のために140°Cまで冷却しました。 Cd前駆体の調製プロセスは、濃度を0.2 Mに調整し、反応温度を240°Cに設定したことを除いて、Zn前駆体と同じでした。
ZnSe / CdS / ZnS Type-II / Type-IQDの一般的な合成
典型的な合成手順として、4 mLのSe前駆体とODE(15 mL)を100mLの丸底フラスコに入れました。混合物を310℃に加熱した。この温度で、2mLのZn前駆体を反応フラスコにすばやく注入しました。 QDの粒子サイズと協調するPL位置の変化を監視するために、さまざまな時間間隔でアリコートを抽出しました。コアナノ結晶が目的の寸法に達したとき、CdSシェルの成長のために反応温度を230°Cに下げました。精製ステップなしで、Cd前駆体と1-オクタンチオールの混合物(OTとカチオンのモル放射は1:1.2)が、シリンジポンプを使用して3 mL / hの速度で滴下し始めたため、温度は310°Cに上昇しました。同じプロセスがZnSのシェル成長に適用されました。 ZnSe / CdS / ZnSコア/シェルQDの発達を分析するために、反応中にQDのアリコートを採取した。調製したままのコア/シェルQDは、アセトンを添加して精製した後、クロロホルムに再分散させました。
CdSe / ZnSタイプI量子ドットの一般的な合成
CdSe / ZnS QDは、以前のレポート[7]に記載されているように合成されました。その後、相間移動、QD-抗体検出プローブ、およびFLISAの調製のプロセスは、以下に説明するZnSe / CdS / ZnSQDのプロセスと同じでした。
バイオアプリケーション用のZnSe / CdS / ZnSQDの相間移動
ポリ(無水マレイン酸-alt-1-オクタデセン)(PMAO)-疎水性末端がQDの有機コーティングとインターリーブし、親水性末端基が周囲のバッファーと自由に相互作用する両親媒性オリゴマー-疎水性QDを純粋なものに転写するために使用されています水。 ZnSe / CdS / ZnS QDとPMAOを混合し、超音波処理しながらクロロホルムに溶解しました(QD / PMAOのモル比は1:7でした)。その後、45°Cでの回転蒸発によりクロロホルムを除去しました。次に、等量の0.1 M NaHCO 3 水溶液(pH =8.5)を加えてQD-PMAOを溶解しました。 PMAOでカプセル化されたZnSe / CdS / ZnSタイプII /タイプIQDは、蛍光損失がなく、幅広いpH環境で水溶液中で高い安定性を示します。
QDの準備-抗体検出プローブ
この手順は以前の文献で広く報告されています[1,2,3]。 QD-PMAOは、EDCおよびスルホ-NHSによるこれらの-COOH基の活性化を通じて、最初にモノクローナルCRP抗体と結合しました。次に、一定量のモノクローナルCRP抗体をQDに添加し、BSバッファーに溶解した後、BSAでブロックしました。最後に、遠心分離下で生成物を5 mM BSバッファー(pH =8.0)で洗浄しました。 QDs-mAbは50μLのBSバッファー(5 mM、pH =8.0)に保存されました。
抗体でコーティングされた蛍光マイクロプレートの準備
マイクロプレートの各ウェルで一次抗体(CRPモノクローナル抗体の濃度は1.8 mg / mL)を炭酸塩-重炭酸塩バッファー(50 mM pH =9.6、CBバッファー)で希釈しました。続いて、マイクロプレートをシーリングフィルムで覆い、4°Cで24時間インキュベートしました。余分なコーティング抗体を除去するために、マイクロプレートを洗浄バッファー(10 mM PBS中の0.05%Tween-20、pH =7.4)で3回洗浄しました。次に、過剰な結合部位を10 mM PBS(pH =7.4)中の0.5%(w / v)BSAでブロックし、4°Cで一晩インキュベートしました。このプロセスにより、マイクロプレートウェルの利用可能な残りの結合側がすべて確実にカバーされました。マイクロプレートを一定の温度と湿度のチャンバー内で24時間乾燥させた後、将来の使用のために4°Cで保存しました。
蛍光結合イムノアッセイによるCRPの定量的検出
96ウェルマイクロプレートの各ウェルに、含まれているコーティング抗体を100μLの標準抗原を加え、サンプルバッファーで一連の濃度に希釈しました。プレートを37°Cで30分間インキュベートした後、洗浄バッファーで5回洗浄しました。次に、100μLのQD-mAbプローブをプローブバッファー(0.1 M PBS中の10%子牛血清(v / v))で希釈し、上記のプロセスと同じようにインキュベートして洗浄しました。
特性評価
室温のUV-vis吸収およびPLスペクトルは、Ocean Optics分光光度計(モードPC2000-ISA)で測定しました。 PL量子収率(QY)は、溶液中のQDサンプルの積分蛍光強度を既知のQYの標準(ローダミン101(R101)エタノール溶液(標準として0.01%HCl、QY =100%))の蛍光強度と比較することによって決定されました。 。透過型電子顕微鏡(TEM)の研究は、200kVで動作するJEOLJEM-2010電子顕微鏡を使用して実施されました。製品の位相測定は、Cu-Ka放射線(波長=1.54Å)を使用してX線回折計(D8-ADVANCE)で実行されました。 QDおよびQD抗体プローブのサイズは、動的光散乱法(Nano-ZS 90、Malvern Instruments、英国)を使用して記録されました。
結果と考察
シェル成長プロセスのUV-vis吸収およびPLスペクトルを図1に示します。ZnSeコアのストークスシフトはわずか8nmで、最初の吸収ピークは420 nm、発光ピークは428 nm、半値全幅は半分です。最大(FWHM)は17nmです。ただし、CdSシェルの単分子層(ML)が1つだけZnSeコア上で成長した場合、ストークスシフトは54 nmに大幅に増加し、最初の吸収ピークは497 nm、発光ピークは551 nmで、半値全幅(FWHM)が発光します。 38nmの電子波動関数の非局在化により、ZnSe / CdS QD(629 nm)のPL発光はZnSeコアQD(428 nm)に対して赤方偏移し、FWHMはCdSシェルの堆積によって52nmに広がります。拡大されたPLFWHMは、強化されたFrölichのような励起子-フォノン相互作用に由来します[22、23]。さらに、最初の吸収ピークの振動子強度は、ZnSeの価電子帯からCdSの伝導帯への空間的に間接的なタイプII遷移のために急速に弱まりました。この現象は、タイプIIの量子ドットで一般的です[24、25、26]。一方、青色のスペクトル領域(<500 nm)での吸収の劇的な増加は、バルクCdS材料のバンドギャップ(2.42 eV)に割り当てられました。その結果、ZnSe / CdSタイプIIQDの赤色発光、平坦化された最初の励起子吸収ピーク、および短波長領域(<500 nm)での強い吸収により、大きなストークスシフトが発生し、再吸収が抑制されました。 ZnSシェルの連続的な成長に伴い、PLは短波長にシフトし、FWHMは52nmから43nmに狭まりました。この現象は、Zn原子がCdに富む領域に拡散して、高温で勾配シェルを形成し、シェルのバンドオフセットが増加するという事実に起因していました。 QYは、CdSおよびZnSのZnSeコアへのシェル成長プロセス中に20%から82%に増加する可能性があります。
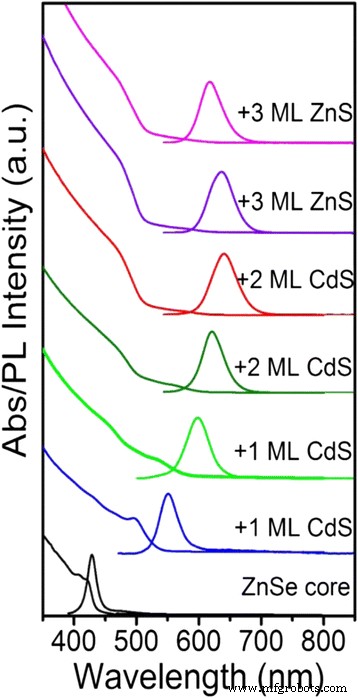
ZnSe / CdS / ZnSコア/シェルQDの連続成長によるUV-vis吸収およびPLスペクトルの変化
高品質で単分散のZnSeコアQDを得るには、コア溶液中のSe前駆体に比べて過剰なZn-OA前駆体が必要であったことは注目に値します。その結果、高温(> 200°C)がZn 2+ > およびCd 2+ 、およびCd-OT前駆体中の豊富なオクタンチオールも過剰なZn-OAと反応する可能性があります[7、12、27、28]。合金シェルは、界面張力と欠陥を減らしてQYを上げるだけでなく、正孔のエネルギー障壁を生成することもできます。 ZnCdSeS合金シェル材料の伝導帯端はZnSeとCdSの伝導帯端の間にあり、価電子帯端はCdSよりも深かった。これにより、正孔の追加のブロッキング層として、価電子帯の端に大きな潜在的な谷が形成されました(スキーム1)[12]。このエネルギーバンド構造により、電子と正孔の重なりをさらに減らして、最初の励起子吸収ピークの強度を下げ、再吸収を抑えることができます。
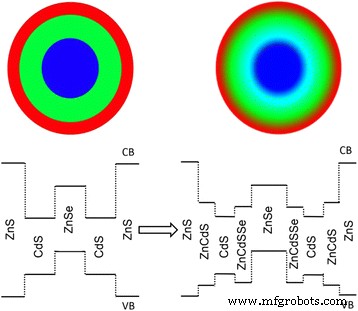
概略構造( up )とバンドの位置合わせ(下 )対応する急激な界面と合金化された界面にそれぞれ基づくZnSe / CdS / ZnSタイプII /タイプIQDの場合
コア/シェルバンド構造およびシェル成長中のPLと吸光度の変化に関する情報は、コアとコア/シェルナノ結晶のXRD、TEM、およびHRTEMの比較によってさらに検証できます。 ZnSeコア、ZnSe / CdS、およびZnSe / CdS / ZnSコア/シェルの粉末XRDパターン(図2の左側の写真)は、回折ピークが鋭くなり、バルクウルツ鉱(WZ)CdSに対応する位置にシフトすることを示しています。またはZnS結晶構造。この結果は、最終的なコア/シェルQDのZnSeコアと比較して大量のCdSまたはZnSシェルの予測値と一致しており、マルチシェルの成長を証明しています。さらに、閃亜鉛鉱(ZB)タイプのZnSeコアからWZタイプのコア/シェルへの変換がCdSおよびZnSコーティングで発生しました。この現象は、CdSe / CdSコア/シェルQDシステムで報告されています[29、30]。コアQDといくつかのコア/シェルQDのTEM画像を図2a− 2 Fに示します。すべてのTEM画像は、元のZnSeコア(3.90 nm)からZnSe / 6CdSタイプまで平均直径が徐々に増加するほぼ単分散の球状QDを示しています。 II QD(7.98 nm)およびZnSe / 6CdS / 6ZnSタイプII /タイプIQD(11.92 nm)。 ZnSeコアQDのHRTEM画像(図2aの挿入図)に示されているように、(111)面の格子間隔は0.32 nmであり、QDは良好な結晶化度と単分散性を備えています。シェルの成長に伴い、XRDデータに従って、格子定数は対応する変化(CdSの場合は0.35 nm、ZnSの場合は0.31 nm)を示しました。この結果は、CdSとそれに続くZnSシェル材料の制御可能な成長を明確に示唆しています。
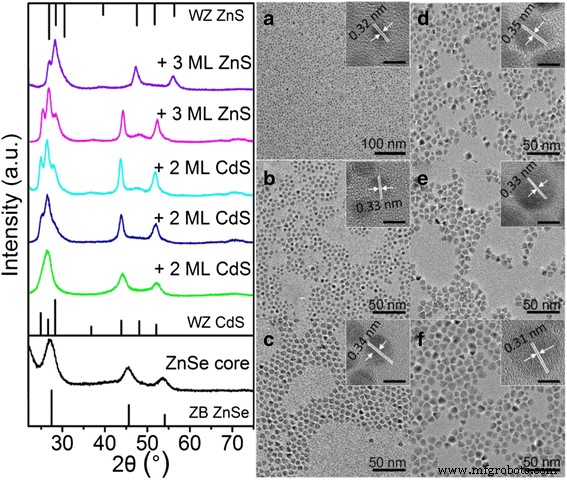
左 :シェル成長段階が異なるZnSe / CdS / ZnSタイプII /タイプI量子ドットのXRDパターン。閃亜鉛鉱(ZB)ZnSe(下)、WZ CdS(中央)の回折線 )、およびWZ ZnS( top )インデックスが付けられます。 そうです :対応するTEMおよびHRTEM(挿入図 、5 nmのバー)ZnSeコアの画像( a )、2MLのZnSe / CdSタイプIIQD( b )、4 ML( c )および6 ML( d )それぞれCdSシェル、およびそれぞれ3 ML(E)と6 ML(F)のZnSe / CdS / ZnSタイプII /タイプIQD
一方、マルチシェルの成長中の組成の変化を確認するために、追加ファイル1:表S1に示すように、コア/シェル成長のさまざまな段階でエネルギー分散型X線分光法(EDS)分析が行われました。 EDSデータは、Cd、Se、Zn、およびSの含有量の対応する変化がシェルの成長段階に応じていることを示しています。ただし、結果として得られるZnSe / CdSQDのCd /(Zn + Cd)モル比は、Zn 2+ > およびCd 2+ 200°C以上でCdSシェルをZnSeコアにコーティングするプロセス中。典型的なタイプIのCdSe / CdS / ZnS QD(Cdモル比〜40%)[31]に関する発行済みの文献と比較すると、タイプII /タイプIのZnSe / CdS / ZnS QDにははるかに少ないCd元素が含まれています(〜 13%)。
クロロホルム中の疎水性QDと、太陽光およびUV光下の水中のPMAOキャップQDの視覚的比較を、追加ファイル1:図S1(A)に示します。どちらのQDソリューションも邪魔されず、ナノ粒子の凝集がないようです。両方のQDは、ハンドヘルドUVランプ(365 nm)で照らされたときに、同じ赤色光を発しました。追加ファイル1:図S1(B)は、相間移動前後のQDのUV-可視吸収およびPLスペクトルを示しています。クロロホルム中の疎水性QDと比較して、PMAOでキャップされたQDのPLスペクトルの変化はごくわずかであり、粒子サイズとPL特性に明らかな変化がないことを示しています。追加ファイル1:図S1(C)および(D)は、相間移動前後のQDのTEM画像を示しており、PMAOでキャップされたQDの形態と状態をさらに決定します。 PMAOでキャップされたQDは十分に分離されており、集合体として観察されることはめったにないようです。
相間移動プロセス中のPMAOカプセル化QDの形成を確認するために、FTIR分光法を使用してQDの表面の官能基を特性評価しました(追加ファイル1:図S2に示されています)。 1777 cm -1 でのピークの減少 (PMAOとQD-PMAOの比較)および1715 cm -1 でのピークの増加 (3つのサンプルと比較して)無水物の分解と-COOHの形成に起因していました。 FTIRの結果は、PMAO両親媒性ポリマーがZnSe / CdS / ZnSQDの表面にうまくコーティングされたことを示しています。
調製されたままのQDの安定性は、その後の治療にとって非常に重要です。図3aは、精製ステップでの疎水性ZnSe / CdS / ZnSQDの相対的なPL安定性の変化を示しています。 ZnSe / CdS / ZnSコア/シェルQDのPL強度は、ヘキサンでの精製の多くのサイクルで85%を維持できます。図3bに示すように、BSバッファー(pH =7.2)中のQDs-PMAOのコロイド安定性は、25°Cでの時間の関数として推定されました。 PL強度はほぼ一定に保たれ、400時間後でも溶液は透明でした。これは、QD-PMAOがBSソリューションで損傷することなく安定していることを示しています。図3cは、酸性から塩基性のpH(pH =1-14、HClまたはNaOHで調整)溶液に30分間浸漬したQD-PMAOのPL強度の変化を示しています。親水性QDのPL強度は、PH =14の場合を除いて85%以上保持できます。図3dは、QD-PMAOの相対蛍光強度に対する温度パラメーターの影響を示しています。蛍光強度は温度の上昇とともに徐々に減少しましたが、90°Cでは76%を維持しましたが、PLピークは、熱膨張と電子-フォノン結合効果により、徐々に長波長にシフトしました。すべての安定性評価は、ZnSe / CdS / ZnSタイプII /タイプIQDおよびQD-PMAOが非常に安定しており、生物学的用途に適していることを示しています。
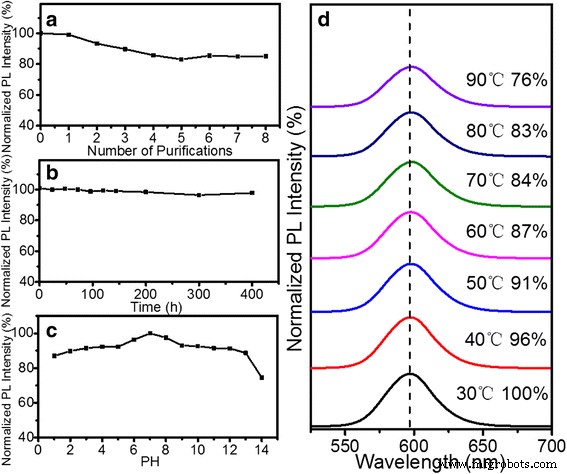
( a での疎水性QDの安定性テスト )繰り返される精製プロセスステップ。 QDの安定性テスト-PMAO( b )BSバッファ、( c )PH、および( d )温度
CRPは肝細胞からの急性期タンパク質であり、そのレベルは感染症や自己免疫疾患の初期の指標と見なされています。ここでは、合成されたままのPMAOでキャップされたZnSe / CdS / ZnS QDをCRPと組み合わせて、定量的イムノアッセイへの応用の可能性を示しています。水性ZnSe / CdS / ZnSQDとQDs-mAbの蛍光スペクトルの比較図を図4aに示します。明らかに、両方のサンプルのPLピーク形状は、遠心分離分離プロセス中の不可避のサンプル損失のためにカップリング反応後に蛍光強度が60%に低下することを除いて、ほぼ同じです。抗体タンパク質カップリングプロセス後でも、ZnSe / CdS / ZnSタイプII /タイプIQDの優れた光学的安定性を証明します。
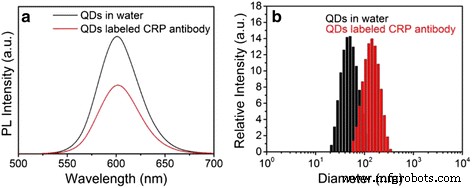
蛍光スペクトル( a )および動的光散乱( b )バッファ内のQD-PMAOおよびQD-mAbの
QDのサイズに対する共役の影響をさらに調査するために、水性QDおよびQD-mAbは動的光散乱(DLS)によって特徴付けられます。 DLSの結果(図4b)は、両方のサンプルのサイズ分布が狭く、単分散性が良好で、凝集することなく離散的な形状を維持しているのに対し、流体力学的サイズはカップリングプロセス後に46nmから120nmに増加することを明確に示しています。これは、CRP抗体との結合の成功を示しています。
さらに、蛍光プローブとしてCdSe / ZnSタイプI量子ドットの代わりにZnSe / CdS / ZnSタイプII /タイプI複合量子ドットを使用して、CRPの定量的検出のためのFLISAを確立しました。アセンブルプロセスは、追加ファイル1:スキームS1に示されています。図5aは、さまざまな濃度のCRP抗原の検出におけるイムノアッセイ用のQD蛍光ラベルの相対蛍光強度を示しています(標準のCRP抗原は0、1、5、10、50、100、200、400 ng / mLに希釈されています)。明らかに、PL強度はCRPの濃度の増加とともに徐々に増加します。図5bは、蛍光強度とターゲットCRP濃度の相関関係が、 y の2次回帰曲線方程式に従っていることを示しています。 =44230 + 8121.1x-10.3x 2 相関係数は0.9991で、1に近いほど良いです。使用濃度の範囲は0〜400 ng / mLです。 LODは、FLISAのイムノアッセイの重要なパラメーターの1つです。 ZnSe / CdS / ZnS複合タイプII /タイプIQDを蛍光プローブとして使用することにより、CRPの定量的検出の感度は0.85 ng / mLであり、CdSe / ZnSタイプに基づくFLISAの感度よりも15%高くなります。 -I QD(1.00 ng / ml)(追加ファイル1:図S3)
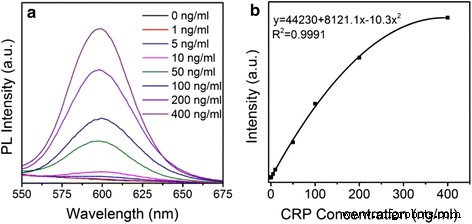
さまざまな濃度のCRP抗原を測定するためのFLISAのフォトルミネッセンススペクトル( a )および検量線( b )
さらに、回収実験を使用して、分析用の一連の既知の標準CRP抗原を使用したFLISAのマトリックス効果を評価し、最終濃度は低、中、高リスクレベルをカバーしました。表1に示すように、すべての回復率は83.61〜105.9%の範囲内です。これらの結果は、再吸収抑制特性を備えたZnSe / CdS / ZnSタイプII /タイプIQDに基づくFLISAが高精度であり、定量的イムノアッセイ検出に大きな利点があることを示しています。
<図>結論
大きなストークスシフトとフラットな最初の吸収ピークを持つ再吸収抑制ZnSe / CdS / ZnSタイプII /タイプIコア/シェルQDを合成するためのホスフィンフリーワンポット法を報告します。これらの特性により、再吸収が減少し、蛍光出力のレベルが向上します。合成されたままのQDは、QYが高く(82%)、さまざまなテスト条件に対して高い安定性を備えています。次に、最初にZnSe / CdS / ZnS QDをFLISAの蛍光プローブとして使用して、CRPタンパク質を高感度(LOD 0.85 ng / mL)で定量的に検出します。これは、再吸収が抑制されたZnSe / CdS / ZnSタイプII /タイプIコア/シェルQDが、生物医学および光電分野での応用に有望な可能性を秘めていることを示しています。
略語
- BSA:
-
ウシ血清アルブミン
- CRP:
-
C反応性タンパク質
- DLS:
-
動的光散乱
- EDC:
-
1-エチル-3-(3-(ジメチルアミノ)プロピル)カルボジイミド
- EDS:
-
エネルギー分散型X線分光法
- ELISA:
-
酵素免疫測定法
- FLISA:
-
蛍光結合免疫吸着測定法
- FWHM:
-
半値全幅
- LOD:
-
検出限界
- MES:
-
2-(N-モルホリノ)エタンスルホン酸
- OT:
-
1-オクタンチオール
- PMAO:
-
ポリ(無水マレイン酸-alt-1-オクタデセン)
- QD:
-
量子ドット
- QY:
-
量子収率
- sulfo-NHS:
-
N-ヒドロキシスルホスクシンイミド
ナノマテリアル
- 合成および生物医学的応用のための蛍光ナノ材料の進歩と挑戦
- 効果的な酵素模倣物としてのピリジニックリッチN、S共ドープ炭素量子ドットの合成
- 重金属を含まない発光ダイオードに適用するためのInP / ZnSコア/シェル量子ドットのグリーン合成
- ZnOナノ結晶の合成と逆ポリマー太陽電池への応用
- ポリ(3,4-エチレンジオキシチオフェン)/金/グラフェン複合材料の固体加熱合成とその亜硝酸塩およびヨウ素酸塩のアンペロメトリー定量への応用
- 水溶性硫化アンチモン量子ドットの合成とそれらの光電特性
- コア/シェルCdSe / ZnS量子ドットフィルムの光励起発光に対する可逆的電気化学的制御
- Co3O4ナノワイヤの環境にやさしく簡単な合成とリチウムイオン電池でのグラフェンによるそれらの有望な応用
- グラフェン/ Ag3PO4量子ドット複合材料の簡単なワンステップソノケミカル合成と光触媒特性
- 修飾BiOClの合成と特性評価および水溶液からの低濃度染料の吸着におけるそれらの応用
- ユウロピウムをドープしたコアシェルZnSe / ZnSe量子ドットにおける粒子間エネルギー移動のシェル厚依存性



