超微細チタニア核形成に対する硫酸陰イオンの効果
要約
四塩化チタンの加水分解中のナノ分散チタニア合成に対する硫酸陰イオン効果の現象論的モデルを研究した。硫酸塩アニオンと八面体配位[Ti(OH) h (OH 2 ) 6-h ] (4-h)+ モノナーはアナターゼ相の核形成の決定要因です。
背景
超微細なTiO 2 有害有機化合物の分解[1]、廃水洗浄[2]、NO x 、SO x センサー材料[4]や太陽電池[5]などの新しい産業分野への空気浄化[3]。相組成、粒子サイズ、表面状態は、TiO 2 の触媒反応性、感光性、吸着特性を決定する最も重要な特性です。 。たとえば、チタニアの粒子サイズの減少は、触媒活性の急速な増加につながります[6]。同時に、チタニアの光触媒特性は、TiO 2 の相組成に非常に敏感です。 アナターゼ、ブルッカイト、ルチルなどの多形[7]。
物理的および化学的パラメータを制御するチタニア合成法の選択は、結果として得られる組成の決定要因として非常に重要です。ナノサイズのTiO 2 の調製 ゾルゲル法[8]、化学沈殿法[9]、マイクロエマルジョン法[8]および熱水法[10]によって可能です。ゾルゲル法は、ナノサイズの酸化物を調製するための最も柔軟な手法です。一次前駆体の種類、加水分解条件、温度、反応媒体のpHの変化により、ナノ粒子の核形成と成長を制御できます。得られたチタニアのゾルゲル法は、通常、チタンアルコキシドTi(OR) n の反応に基づいています。 加水分解。これらの高価な化学物質のTiCl 4 などのより安価な前駆体への変更 ナノサイズのTiO 2 の大規模製造に非常に有望です 。 TiCl 4 の有望な利点 アプリケーションは、チタニアの特定の相の予測された核形成を使用して、付加イオンによって制御される重縮合反応の可能性です。
このホワイトペーパーの目的は、SO 4 の効果を調査することでした。 2- TiCl 4 に基づくゾル-ゲルプロセスのチタニア核形成中のオリゴマー重縮合および酸化物ネットワーク形成上の陰イオン 加水分解。
メソッド
四塩化チタンTiCl 4 (メルク、99.9%、比重1.73 g / cm 3 20°Cで)を0°Cに冷却し、塩酸(36.0%水溶液)を加えてさらに塩化水素を蒸発させました。 TiCl 4 塩酸に対する比率は2:1でした。炭酸ナトリウムの水溶液をオキシ塩化チタンTiOCl 2 のゾルに滴下した。 激しく攪拌しながらpHを5.0〜5.5にします。すべてのpH上昇プロセス中にゲル形成が観察されました。ナノ粒子の懸濁液を80°Cで3時間保持し、さらに蒸留水で洗浄してNa + を除去しました。 およびCl − イオン。沈殿したTiO 2 150°Cで乾燥させ、得られたキセロゲルをS1とマークしました。 S2材料合成プロセスも同様に実行されましたが、結晶乾燥したNa 2 SO 4 TiCl 4 の段階で四塩化チタンに直接添加されました 加水分解。
回折パターンは、X線管BSV28(CuK α)を備えた回折計DRON-4-07で得られました。 放射線、40 kV、30 mA)、Bragg-BrentanoジオメトリタイプおよびNiK β -フィルター。 ICSD構造モデルを使用して定性分析を実施しました。アナターゼとルチルの構造モデルは、それぞれICSD#92363とICSD#24780に基づいています。平均粒径が約50μmの真空(850〜900°Cで4時間)でアニールされた銅粉末を参照サンプルとして使用して、機器のピークの広がりを決定しました。 2θ=43.38°でのこの参照サンプルの回折ピークの半値全幅(FWHM)は0.129°でした。したがって、アナターゼ相とブルッカイト相を区別することが可能になりました。コヒーレント散乱ドメインのサイズは、シェラーの式によって計算されました:\(D =\ frac {K \ lambda} {\ beta cos \ theta} \)、 K はシェラー定数( K =0.9)、λ は波長(0.154 nm)、β FWHM(ラジアン)、およびθ はピーク角度位置です。ガウス関数とコーシー(支配的)関数の組み合わせをプロファイル形状として使用しました。
赤外線スペクトルは、Thermo-Nicolet Nexus 670FTIR分光計を使用して4000〜400 cm -1 で記録されました。 領域。 TiO 2 振動粉砕後の/ KBr混合物をペレットにプレスし、透過モードで測定しました。
サンプル粉末の形態は、100 kV顕微鏡JEOLJEM-100CX IIを使用した透過型電子顕微鏡(TEM)によって研究されました。薄い透明なカーボンフィルムで覆われた微細な銅グリッドは、TEM研究の試料サポートとして使用されました。
結果と考察
反応媒体中の硫酸ナトリウムの存在は、得られた材料の相組成に大きく影響しました(図1)。 Na 2 の非存在下で合成された材料 SO 4 添加剤(S1)は、アナターゼとルチルの混合物であり、相対相含有量はそれぞれ65±4および35±5 wt%でした。コヒーレント散乱ドメイン(CSD)の平均サイズはアナターゼで約14 nm、ルチルで9 nmであったため、どちらの相も良好に結晶化しています。一方、2θ=16–32 o のXRDパターンにハローが存在するため、材料の一部はアモルファス状態に近くなります。 明らかです。合成条件によれば、非チタニア相の形成は起こりそうにない。結果として、材料は異なる結晶化度を持つ分離された領域で構成されます。 S1サンプルの比表面積は約152m 2 でした。 g -1 。材料S2は、アナターゼの明確な構造的特徴を備えたアモルファス超微細チタニアに近かった。この場合、XRDパターンのハローも観察されますが、比較的狭くなり、より大きな2θ値にシフトします。 CSDの平均サイズは約4〜5 nmでした(材料の結晶化度が低いため、分析は複雑です)。 S2サンプルの比表面積は328m 2 に増加しました g -1 。
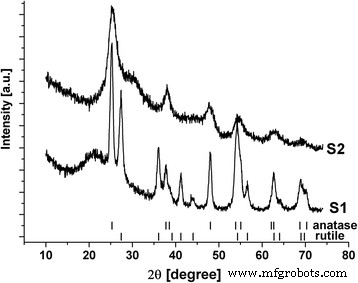
S1およびS2材料のXRDパターン
S1サンプルのTEM画像(図2a)では、その形態について明確な結論を出すことはできませんが、観察された凝集体は、10〜15nmのサイズの層状の一次粒子で構成されていました。さらに、結晶領域の境界の証拠はありません(図2b)。 S2サンプルは、凝集体の泡のような形態を持っていました(図2c、d)。 HR TEMは、この材料の一部の粒子の高い結晶化度を示し(図3)、面間距離は0.34〜0.37nmでした。得られた面間隔は、アナターゼの(101)面(0.352 nm)に対応します。これは、CSD(微結晶)の好ましい成長方向が[010]結晶学軸であることを示しています。この結果は、酸素化された表面を持つアナターゼナノ結晶が〈010〉方向にファセットを発達させたという結論に至りました[11]。

サンプルS1のTEM画像( a 、 b )およびS2( c 、 d )

{101}面からのフリンジを含むS2材料のHRTEM画像
合成された材料に関するより多くの情報は、FTIR分光法によって得られました。 3400 cm -1 付近の広い吸収領域 チタニア粒子の表面に化学吸着されたOH基が存在することを示します(ν-OHモード)(図4)[12]。通常の3700〜3600から約3400 cm -1 へのν-OHバンドのシフト 水素結合の存在によって引き起こされる可能性があります[13]。約1600cm -1 のバンド 分子吸着水の存在を示します(δ-H 2 Oモード)[14]。 S1サンプルの結晶化度が高いと、チタニアの特徴的な領域(400〜700 cm -1 )に比較的明確な吸収帯が形成されます。 )[15]。
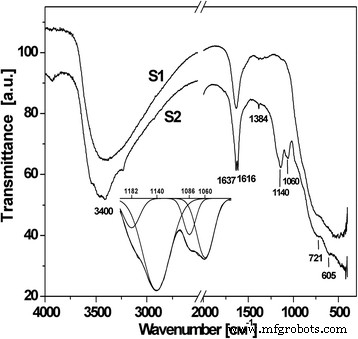
S1およびS2材料のFTIRスペクトル
1139および1060cm -1 でのS2材料のFTIRパターンの追加の吸収帯 化学吸着されたSO 4 に対応 2- イオン[16]。鋭い低強度バンド1384cm -1 硫酸イオンバンドによって修飾され、S =O伸縮周波数に割り当てられた金属酸化物に典型的です。一方、吸収帯は1325 cm -1 までの低周波領域でシフトするため、S =O–H調整は起こりそうにありません。 この場合。 SO 4 には2つの異なるバリエーションがあります 2- チタニア表面への固定化—2つの酸素を介した1つの金属イオンへの配位を伴うキレート二座錯体形成または2つの金属イオンを介した結合を使用した架橋二座錯体形成。両方の複合体はC2vポイントグループに属しています。ブリッジ二座SO 4 2- Ti 4+ に配位した陰イオン 930〜1200 cm -1 の特徴的なストレッチ周波数があります 範囲、および1148 cm -1 での主要な吸収ピーク 非対称伸縮振動に起因します[17]。 1300〜900 cm -1 のバンド SO 4 の領域が観測されました 2- / TiO 2 システム、および1217、1134、1044、および980 cm -1 のピーク [18]で、二座橋SO 4 の特徴的な周波数として識別されました。 2- 金属にコーディネート。 [19]によると、架橋二座錯体には、1195〜1160、1110〜1105、1035〜1030、および990〜960 cm -1 に4つの吸収帯があります。 、S =OおよびS–O結合の非対称および対称伸縮周波数に割り当てられます。
SO 4 でのキレート錯体形成のエネルギー的好感度に関する結論 2- 陰イオンは、DFT計算を使用した硫酸化チタニアの調査に基づいて作成された2つの酸素を介してTi原子に配位します[20]。キレート硫酸塩複合体の形成は、1201 cm -1 の骨格FTIRバンドに対応します。 [21]キレート二座錯体は、1240〜1230、1125〜1090、1035〜995、および960〜940 cm -1 に4つのバンドを持っているため これらは、S =OおよびS–Oバンドの非対称および対称伸縮周波数に割り当てられます[19]。
1200〜1000 cm -1 のデコンボリューション S2材料のFTIRスペクトルの領域では、1182、1140、1086、および1060 cm -1 に4つのバンドが存在することが明らかになりました。 。 1086 cm -1 の吸収帯 キレート二座複合体のそれに非常に近いです。キレートおよび架橋二座錯体の2つのバンドが互いに重なり合うため、1182 cm -1 でバンドします。 両方のタイプの複合体に対応できます。 1060および1140cm -1 のバンド S2サンプルの表面に架橋二座錯体が形成されていることを意味します。
SO 4 の次のモデルを提案できます 2- [22]に示されている結果を考慮に入れると、一次水素化複合体間のオレーション相互作用の段階でのチタニア核形成への影響。 TiCl 4 の加水分解 [Ti(OH 2 ) 6 ] 4+ Ti 4+ の形成 イオンは、[Ti(OH) h への次の変換で八面体配位にあります (OH 2 ) 6-h ] (4-h)+ 脱プロトン化の結果としてのモノマー。加水分解比 h はpHの関数であり、部分電荷理論によって決定されます[23]。これらのモノマーでは、OH - グループには、八面体の赤道面内の位置、およびH 2 の熱力学的利点があります。 O分子は主に「頂点」の位置を占めます[24]。加水分解生成物は[Ti(OH)(OH 2 ) 5 ] 3+ および[Ti(OH) 2 (OH 2 ) 4 ] 2+ 反応媒体のpHが1に近い場合のモノマー。pH=3では、[Ti(OH) 2 (OH 2 ) 4 ] 2+ および[Ti(OH) 3 (OH 2 ) 3 ] + 複合体は溶液中に共存します。 pH =4では、加水分解により[Ti(OH) 3 が形成されます。 (OH 2 ) 3 ] + 錯体、およびpH =6–8の範囲では、[Ti(OH) 4 (OH 2 ) 2 ] 0 モノマーが形成されます。チタン多形形成の可能性は、[Ti(OH) h の空間構成によって定義されます。 (OH 2 ) 6-h ] (4-h)+ 一次モノマー。 [Ti(OH) 4 (OH 2 ) 2 ] 0 モノマー(OH基が八面体赤道面とH 2 を占める O分子は頂点にあります)中性またはアルカリ性媒体で形成されます[20、25]。二量体は、八面体配位が八面体赤道面の外側に共通のエッジを有する2つの一次モノマー間の脱離反応の結果として形成されます。さらに重縮合した後、[Ti n のジグザグ状またはらせん状の鎖 (OH) 4n (OH 2 ) 2 ] 0 多面体が形成され、アナターゼ相の核形成の条件が作成されます。 [Ti mn O mn (OH) 2分 (OH 2 ) 2m ] 0 ポリマーは m から形成されます [Ti n の線形構造 (OH) 4n (OH 2 ) 2 ] 0 オレーションの相互作用。アナターゼ相の核形成は、面の側面による八面体の融合の結果です[26]。同時に、反応媒体のヒドロニウムイオンは八面体赤道面のヒドロキシル基と相互作用します。反応媒体中のヒドロニウムイオン濃度が上昇すると、[Ti(OH) h (OH 2 ) 6-h ] (4-h)+ モノマーは h の下で形成されます <2条件。それらの間のオレーション相互作用は、モノマーが八面体赤道面の接合エッジによって結合されるポリマー鎖形成につながり、したがって、ルチル相核形成の前提条件を定義します[25]。
SO 4 の存在 2- pH約5.5の反応媒体中のイオンは両方のTi(SO 4 )(OH) 2 (H 2 O) 2 キレート化とTi 2 (SO 4 )(OH) 6 (OH 2 ) 2 二座複合体の形成を橋渡しします(図5)。これらの複合体間のオレーション相互作用には2つの異なる経路があります。 2つのモノマーは、互いに接続するか、水分子の脱水と頂端(キレート錯体の影響)または赤道面(架橋二座錯体の影響)を共有することによって接続します。どちらの場合も次の段階で、2つの水分子の脱水を伴う歪んだジグザグ状の四核チタン錯体の形成が起こり、アナターゼ構造の核形成が始まります。
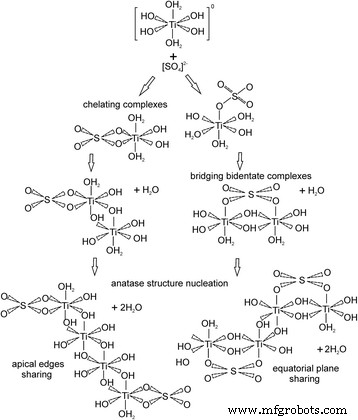
キレート化および架橋二座SO 4 の形成を伴うアナターゼ相核形成の提案されたメカニズム 2- 複合体
結論
SO 4 の効果 2- 四塩化チタンの加水分解中のチタニア核形成上の陰イオンを研究した。核形成プロセスは主に反応媒体のpHとSO 4 によって制御されると結論付けました。 2- 陰イオンの存在。硫酸陰イオンは両方のキレートTi(SO 4 )(OH) 2 (H 2 O) 2 二座Ti 2 をブリッジします (SO 4 )(OH) 6 (OH 2 ) 2 四塩化チタンの加水分解の段階での錯体。 SO 4 の場合、チタノ硫酸錯体間のオレーション相互作用の2つの経路を持つモデルを提案しました。 2- 配位子は、スクリューポリマー鎖の形成とTiO 2 の核形成を刺激します アナターゼ相。
ナノマテリアル



