ナノテクノロジー:invivoイメージングシステムから制御されたドラッグデリバリーまで
要約
科学技術は常に人間の闘争のバイタルであり、マイクロサイズからナノサイズまでの新しいツールや製品の開発にのみ利用されてきました。ナノテクノロジーは、特にバイオイメージングとドラッグデリバリーに関連する生物医学への広範な応用により、大きな注目を集めています。さまざまな病気の診断と治療のために、さまざまなナノデバイスとナノ材料が開発されてきました。ここでは、ナノメディシンの2つの主要な側面、つまりin vivoイメージングとドラッグデリバリーについて説明し、最近の進歩と将来の探求に焦点を当てています。特に癌細胞のイメージングのためのナノテクノロジーツールの途方もない進歩が最近観察されました。ナノ粒子は、部位特異的なイメージングやターゲティングを含む分子レベルの変更を実行するための適切な媒体を提供します。放射性核種、量子ドット、磁性ナノ粒子、カーボンナノチューブの発明、およびバイオセンサーでの金ナノ粒子の使用は、イメージングの分野に革命をもたらし、疾患の病態生理学の理解を容易にし、診断能力を向上させ、治療の提供を強化しました。ナノメディシンのこの高い特異性と選択性は重要であり、したがって、この分野における最近の進歩は、より良い今日とより豊かな未来のために理解される必要があります。
レビュー
はじめに
実際のところ、ナノテクノロジーは工学と科学のすべての不可欠な分野で進歩しており、科学者は原子ごとに最小のスケール長で動作できるものを設計することによって、すべての産業と人間の生活に革命をもたらしています[1]。ナノテクノロジーには、非常に小さな構造の研究が含まれます。ナノテクノロジーは、ナノメートルスケールで1〜100 nmのサイズ範囲内の物質を制御することにより、機能性材料、システム、およびデバイスの研究、作成、設計、合成、および実装として包括的に定義できます。さらに、分子ナノテクノロジーとも呼ばれるこのナノメートルスケールでの革新的な現象の操作と物質の改善された特性は、最小の人工器具が宇宙の分子と原子に遭遇するスケール長の魔法のポイントです[2,3,4 ]。
ナノテクノロジーとナノメディシンの概念の初期の始まりは、小さなナノロボットと関連デバイスを開発し、製造し、分子レベルで細胞を修復するために人体に導入できるというファインマンの目の肥えたアイデアから生まれました。 1980年代と1990年代の後半に、この革新的な概念はDrexlerの有名な著作[5、6]で提唱され、1990年代と2000年代にはFreitasの人気のある著作[7、8]で提唱されました。ファインマンは、心臓病を治療するためのナノ医療手順に関する最初の既知の提案を提供しました。一般に、医療ツールの小型化は、人間の生活の質を向上させるための、より正確で、制御可能で、信頼性が高く、用途が広く、費用効果が高く、迅速なアプローチを提供します[9]。 2000年に、初めてNational NanotechnologyInitiativeが発足しました。その後、新しい材料の電子機器と分子構造のモデリング、ナノスケールのフォトニックおよび電子デバイスの確立[10、11]、3Dネットワーキングの開発、ナノロボティクス[12]、および多周波力顕微鏡の出現[13]が始まりました。分子ナノテクノロジーの出現への道。
ナノ粒子は、ナノテクノロジーの重要な構成要素と見なされています。強力な化学結合の存在、サイズによって変化する価電子の広範な非局在化、およびナノ粒子の構造変化により、融点、光学特性、磁気特性、比熱、表面反応性など、さまざまな物理的および化学的特性がもたらされます。これらの超微細ナノ粒子は、サイズ、分布、粒子のサイズなどの特定の特性の変化により、バルクの対応物と比較して完全に新しく改善された特性を示し、表面積対体積比が大きくなります[14、15、16]。ナノ構造材料の分野が進化するにつれて、3Dナノ粒子、ナノ結晶、ナノフィルム、ナノチューブ、ナノワイヤー、および無限の数の特性の有望な可能性を備えた量子ドットを含む多くの異なるラベルと用語が使用されています[17]。さまざまな潜在的なアプリケーション(産業および軍事を含む)のために、政府はナノテクノロジー研究に数十億ドルを投資してきました。米国は国家ナノテクノロジーイニシアチブを通じて37億ドルを投資し、欧州連合も12億ドルを助成し、7億5000万ドルが日本によって投資されました[18]。
今日、ナノテクノロジーは科学研究の最も革新的で先駆的な分野の1つであり、驚異的な速度で進歩し続けています[19]。ナノテクノロジーの進歩により、多くの最先端技術がドラッグデリバリーに利用できるようになりました。研究者は、癌[20、21]、ワクチン接種[22]などのさまざまな生物医学的用途において、薬物、タンパク質、モノクローナル抗体、DNA(デオキシリボ核酸)などのさまざまな微小分子および高分子の標的特異的かつ制御された送達のためのナノデバイスの可能性を広範囲に調査しました。 、歯科[23]、炎症性[24]、およびその他の健康障害。したがって、生体内イメージングシステムから制御された薬物送達に至るまでのナノテクノロジーアプリケーションの効率的な使用を実証し、現在の進歩を示し、医療分野での差し迫った研究の方向性を得ることが必要です。
製薬ナノシステム
製薬ナノテクノロジーは、ナノツールの2つの主要なカテゴリ、つまりナノマテリアルとナノデバイスに分類できます。ナノマテリアルは、構造、寸法、相組成などの3つの基本的なパラメーターに基づいてさらに分類できます。ナノ構造はさらに、ナノ粒子、ミセル、デンドリマー、薬物複合体、金属ナノ粒子、量子ドットなどの高分子構造と非高分子構造に分類されます[25]。それらの寸法に基づいて、ナノ材料は4つのグループ、すなわち、ゼロ、1、2、および3つのナノ寸法材料に分類されます。相組成に応じて、これらのナノ材料は3つのグループに分類できます。ナノデバイスは、微小電気機械システム/ナノ電気機械システム(MEMS / NEMS)、マイクロアレイ、および呼吸細胞を含む3つのグループに細分されます。これらの構造とデバイスは、分子レベルで細胞と相互作用する医学で使用するための高度な機能特性を備えて製造できるため、生物学的システムとこれまで達成できなかった最新技術との統合が可能になります[26]。医薬品ナノツールの詳細な分類は、表1の例で説明されています。
<図>製造アプローチ
ナノサイジング技術は、難水溶性薬物の処方にとって非常に重要になっています。 Noyes-Whitneyの式[27]によれば、粒子サイズをナノスケールの範囲に縮小することにより、表面積が増加するため、溶解速度とバイオアベイラビリティが向上します。材料の製造に使用されるアプローチは、ボトムアップ手法、トップダウン手法、およびボトムアップ手法とトップダウン手法の組み合わせに分類されます。ボトムアップ手法には、分子の構築が含まれます。ナノスケール材料を製造するためのボトムアップアプローチに従う技術のいくつかには、逆ミセル、化学蒸着(CVD)、ゾルゲル処理、および分子自己組織化に基づく液相技術が含まれます。ボトムアップによって生成されるコンポーネントは、それらを一緒に保持する共有結合力のために、マクロスケールコンポーネントよりも大幅に強力です。トップダウン技術では、材料はナノ材料の製造のために切断、彫刻、成形によって微粉化されます。例としては、ミリング、物理蒸着、ハイドロダーマティック技術の電気めっき、ナノリソグラフィーなどがあります[28]。表2に、それぞれのタイプのさまざまな製造アプローチを示します。
<図>高度なナノテクノロジーの生物医学的応用
イメージング
特に癌細胞を対象とした研究では、イメージングと治療にナノテクノロジーツールを使用して、過去10年間に驚異的な進歩が報告されました。サイズが10〜100 nmのナノ粒子は、癌細胞での部位特異的イメージングやターゲティングなどの分子レベルの変更を実行するのに非常に適した媒体を提供します[29]。次のセクションでは、イメージング技術の最近の進歩をまとめています。
放射性核種イメージング
小分子を非侵襲的手法で見ることができないため、部位標的造影剤を使用して、正常な周囲組織から分離することが不可能な選択されたバイオマーカーを特定します[30]。放射性核種イメージングは、発現されたタンパク質が放射性医薬品または同位体標識された薬剤または細胞でプローブされ、invivoでさらに追跡されるという概念で開発されました[31]。ポジトロン放出断層撮影(PET)イメージングは、P糖タンパク質の放射性標識基質として99 mのテトロフォスミンとセスタミビを使用したP糖タンパク質輸送による多剤耐性のイメージングに成功しています[32、33]。イメージングのメカニズムは、リポソーム[34]、デンドリマー[35]、バッキーボール[36]、および多数のポリマーとコポリマー[37]を含むナノキャリアなどのイメージングに使用されるモダリティのタイプによって決定されます。それらは、イメージング機器での検出のために、光学活性化合物や放射性核種などの多数のイメージング粒子で満たすことができます。 BODIPY(ホウ素ジピロメタン)標識ジャスプラキノリド類似体は、生細胞内の長寿命アクチンフィラメントを視覚化するために使用されています[38、39]。
ナノテクノロジーの巨大な成長は、多くの造影剤を用いた分子イメージングの研究をリードしています。適切な画像を取得するには、選択した造影剤の半減期が長く、バックグラウンドシグナルが低く、特異的なエピトープ結合があり、ノイズ増強に対するコントラストが増強されている必要があります。多数のキャリアの利用可能性は、疾患の分子および細胞メカニズムに特に焦点を当てたイメージングのさらなる進歩を定義することができます。これにより、イメージングおよびドラッグデリバリーシステムの合理的な開発の機会が増えます[30]。
量子ドット
半導体量子ドットは現在、新しいクラスの蛍光標識として使用されています。これらの半導体ナノ結晶は、表面化学が容易であるため、生体細胞の可視化に有望なツールであり、生体適合性と蛍光時間の延長との結合を可能にします[29、40]。量子ドットの可視化特性(蛍光波長)は、サイズに強く依存します。量子ドットの光学特性は、外殻と金属コアで構成されているため、その構造に依存します。たとえば、緑色蛍光カーボンナノ材料の一種であるグラフェン量子ドット(GQD)は、酸化グラフェンをソルボサーマルで切断することによって作られ、可視化特性を支配していることがわかっています[41]。
量子ドットコアは通常、セレン化カドミウム、硫化カドミウム、またはテルル化カドミウムで構成されています。量子ドットの蛍光特性を維持した電気絶縁を提供するために、外殻は高いバンドギャップエネルギーでコア上に製造されています。特定の波長の可視化特性を備えたさまざまなサイズと組成の微調整されたコアとシェルは、多数のバイオマーカーを提供します[40]。量子ドットは、生物学的受容体への特異的結合を得るために、さまざまなリガンドと結合しています。腫瘍標的リガンドは両親媒性ポリマー量子ドットと結合しており、マウスの前立腺癌の画像検査を実施するために使用されます[42]。同様に、量子ドットは、狭帯域幅の発光、より高い光安定性、単一励起源の拡張吸収スペクトルなど、従来の色素に比べて大きな利点を提供します。さらに、量子ドットの疎水性の課題は、それらを水溶性にすることによって克服されました。体液中での保持時間が長い水性量子ドットの例は、チオール含有荷電基で製造された高蛍光金属硫化物(MS)量子ドットの開発です[43]。さらに、量子ドットのユニークな蛍光特性により、量子ドットは癌細胞に適したイメージングツールになりました[42]。ドキソルビシンと結合したA10RNAアプタマー(QD-Apt-Dox)と結合した量子ドットは、標的癌細胞イメージングの例です[44]。しかし、重金属の取り込みにより量子ドットの毒性の増加が観察されており、その結果、生体内イメージングでの使用が制限されています。それにもかかわらず、最近のアプローチは、毒性の低減と、体細胞に対する量子ドットの生体適合性の強化に焦点を合わせています。また、直径が5.5 nm未満の量子ドットは、尿から迅速かつ効率的に排泄され、毒性が低下することにも言及しておく価値があります。この現象は、カドミウムを含まないCulnS 2 の合成によって示されました。 量子ドットのコアおよびシェルとしての/ ZnS(硫化銅インジウム/硫化亜鉛)。これにより、リンパ節イメージングの生細胞の安定性が向上し、急性局所毒性が明らかに減少しました[45、46]。
>バイオセンサー
ここ数年以来のナノマテリアルの最大の成果の1つは、バイオセンサーの開発です。バイオセンサーは、トランスデューサーに接続または統合された生物学的感知要素を含むデバイスです。バイオセンサーは、抗体抗原、酵素基質、受容体ホルモンなどの構造に基づいて、体内の特定の分子を認識することで作用を発揮します。それらの特異性と選択性を含むバイオセンサーの2つの主要な特性は、この認識システムに依存しています。バイオセンサーのこれらの基本的な特性は、信号に比例する濃度に最も重要に使用されます[47、48、49]。
高効率でバイオセンサーを製造するためには、センシング材料の分散のために選択された基板が前提条件です。量子ドット[50]、磁性ナノ粒子[51]、カーボンナノチューブ(CNT)[52]、および金ナノ粒子(GNP)[53]を含むさまざまな種類のナノ材料がバイオセンサーに適用されます。ナノマテリアルの特徴的な化学的、物理的、磁気的、光学的、および機械的特性により、検出の特異性と感度が向上します。 GNPを含むバイオセンサーは、電極の表面に固定化された生体分子の濃度を増加させた生体分子のための適合性のある環境を提供した。その結果、バイオセンサーの感度が向上しました[54、55]。バイオセンサー内で最も広く使用されている電極表面は、GNPから修飾されたグラッシーカーボン電極(GCE)です。さらに、それらは最高の感度と電気化学的安定性を示しています。この点で、メチレンブルー(MB)とGNPは、ヒト絨毛性ゴナドトロピン(HCG)の濃度を検出するために、GCE上のフィルムの形でレイヤーバイレイヤー(LBL)技術を介して簡単に組み立ておよび変更できます[56]。抗HCGをロードするためにナノ粒子に含まれる表面積が大きいため、これらの免疫センサーは、ヒトの血液または尿サンプル中のHCGの濃度を検出するために使用できる可能性があります。同様に、CNTは、生物医学工学、生物分析、バイオセンシング、およびナノエレクトロニクスで優れた用途を見出しています[57、58、59]。さらに、ポリマーのバイオナノコンポジット層の形をした多層カーボンナノチューブ(MWNT)は、DNA検出に使用できる可能性があります[60]。さらに、磁性ナノ粒子は、磁気共鳴画像法(MRI)造影剤[61]、温熱療法[62]、免疫測定法[63]、組織修復[64]、細胞分離[65]、 GMRセンサー[66]、および薬物または遺伝子送達[67]。
同様に、新しいタイプの磁性キトサンミクロスフェア(MCMS)も、キトサンとカーボンコーティングされた磁性ナノ粒子を使用するだけで製造されています[68]。この研究では、架橋剤としてグルタルアルデヒドを使用することにより、ヘモグロビンもMCMS修飾GCE表面にうまく固定化されました。バイオセンサーのもう1つの重要な用途は、バイオセンサーとしてSsDNA-CNTプローブを使用することによるさまざまな種類のDNAオリゴヌクレオチドの検出を含む光学技術です[69]。同様に、リポソームベースのバイオセンサーも、パラオキソンやジクロルボスなどの有機リン系農薬の最小レベルのモニタリングに使用されているため、かなりの注目を集めています[70]。
磁性ナノ粒子
磁性ナノ粒子(MNP)は、生物学的相互作用の分子レベルまたは細胞レベルで機能する能力を備えているため、排他的な磁気特性を提供します。これにより、MRIの造影剤として、またドラッグデリバリーの担体として最適な化合物になります。ナノテクノロジーの最近の進歩は、生物医学的応用のためのMNPの特性と特徴の変更に役立ったため注目を集めています。この点で、RESを介した超常磁性酸化鉄(SPIO)の取り込みを介した肝腫瘍および転移のイメージングは、わずか2〜3 mmの病変を区別できることが示されています[70、71]。さらに、これらの超小型の超磁性酸化鉄(USPIO)は、直径がわずか5〜10mmのリンパ節の転移の画像化にも非常に効果的です[72]。さらに、この非侵襲的アプローチの重要性は、リンパ管播種の検出においても示されています。これは、ステージングおよび乳がんおよび前立腺がんの治療アプローチの特定において重要な部分と見なされているためです[73]。
>ドラッグデリバリー
ナノテクノロジーは、物理的、光学的、および電子的特性が異なるため、材料科学から生物医学に至るまでの分野にとって魅力的なツールです。ナノテクノロジーの最も効果的な研究分野は、病気の治療、予防、診断にナノテクノロジーの原理を適用するナノメディシンです。さらに、過去数十年の間に世界中でナノメディシン研究が急増したため、ナノメディシンの多くの製品が販売されてきました。現在、ナノメディシンはドラッグデリバリーシステムの影響を受けており、総売上高の75%以上を占めています[74]。この点で、ナノ粒子ベースのドラッグデリバリープラットフォームは、従来の製剤に関連する薬物動態の欠点に対処する上で最も適切な媒体であるという科学者の信頼を得ています[75]。したがって、薬物の治療効果を高めるために、リポソーム、固体脂質ナノ粒子、デンドリマー、および固体金属含有NPなどの薬物送達システムとしてさまざまなナノフォームが試みられてきた[76、77]。関心のある主要な分野のいくつかを以下で説明します。
眼科
眼科経路を介した薬物送達は、製薬科学者にとって非常に魅力的でありながら挑戦的です。目は、複数のコンパートメントを持つ小さな複雑な器官です。その生化学、生理学、および解剖学により、生体異物に対して最も不浸透性になっています。眼の投与を必要とする一般的な状態には、緑内障などの角膜障害に加えて、結膜炎などの眼の感染症が含まれます。眼球送達で使用される最も一般的な薬物クラスには、mydriaticsまたはcycloplegics miotics、抗感染性、抗炎症性、診断、および外科的アジュバントが含まれます。小さな眼の不規則性については、遺伝子治療も必要であり、この領域内で多くの作業が行われています。ナノキャリアがサポートするアプローチは、その適合性と特異性について科学者の注目を集めています。ミクロスフェアやナノ粒子などの粒子送達システム、およびリポソーム、ニオソーム、ファーマコソーム、ディスカムなどの小胞担体が、さまざまなタイプの薬物分子の薬物動態および薬力学特性を改善したことが報告されています[76]。ヒドロゲル、粘膜付着性ポリマー、マイクロエマルジョン、デンドリマー、イオントフォレーシス薬物送達、siRNAベースのアプローチ、幹細胞技術、非ウイルス遺伝子治療、および強膜プラグを用いたレーザー治療を含む、多くの新しい制御された薬物送達システムが出現した[78]。 。薬物送達のための異なるシステムは、眼の経路を介した薬物の送達のために装備されている。すべてのドラッグデリバリーシステムの主な目標は、滞留期間を改善し、角膜透過性を高め、後眼房で薬物を解放し、バイオアベイラビリティを高め、患者のコンプライアンスを改善することです[79]。
Abrego etal。ヒドロゲルの形で眼科送達用にプラノプロフェンのPLGA(ポリ乳酸コグリコール酸)ナノ粒子を調製しました。このヒドロゲル製剤は、プラノプロフェンの眼への送達に適したレオロジー的および物理化学的特性を備えており、薬物のバイオ医薬品の概要が改善されています。さらに、それは薬の局所的な抗炎症および鎮痛の結果を強化し、患者のコンプライアンスを改善しました[80]。別の研究では、キトサンのセフロキシムをロードしたナノ粒子が、二重エマルジョン技術での二重架橋を使用して開発されました。推論は、キトサン-ゼラチン粒子が眼内レベルでのDDの強力に実用的な候補であることを指摘しています[81]。さらに、ジクロフェナクをロードしたN-トリメチルキトサンナノ粒子(DC-TMCN)は、薬剤の眼のバイオアベイラビリティを改善するために眼科用に開発されました[82]。さらに、キトサンベースのリン酸デキサメタゾンのナノサイズの超分子集合体は、その粘膜接着特性により、角膜前の薬物滞留時間を改善するために開発されました。これらのナノ粒子は、眼球表面と薬物の両方と強力に相互作用し、薬物を代謝分解から保護して、角膜前の滞留を延長します[83]。眼科疾患である緑内障は、固体脂質としてモノステアリン酸グリセリルを使用して、ブリモニジンベースの負荷持続放出固体脂質ナノ粒子で治療されました[84、85]。同様に、ダプトマイシンをロードしたキトサンでコーティングされたアルギン酸塩(CS-ALG)ナノ粒子は、眼の用途に適したサイズと高いカプセル化効率(最大92%)で開発されました。この研究により、ダプトマイシンナノキャリアシステムは、細菌性眼内炎に対する前向き治療として、またキトサンナノ粒子の効率的な代替として機能するために、この抗生物質を直接眼に送達するために将来使用できることが明らかになりました[86]。
角膜移植における移植片の短期的および長期的な失敗の主な原因の1つは、免疫学的移植片拒絶反応です。この目的のために、デキサメタゾンリン酸ナトリウム(DSP)のPLGAベースの生分解性ナノ粒子システムが調製され、角膜移植片の拒絶を防ぐためにコルチコステロイドの持続放出がもたらされました[87]。さらに、クルクミンのMePEG-PCL(ポリエチレングリコール-ポリカプロラクトン)ナノ粒子が報告され、それらは、遊離クルクミンよりも効率の向上、角膜でのクルクミンの保持の強化、および角膜血管新生の予防の有意な改善を示しました[88]。同様に、銀ナノ粒子を注入した組織接着剤(2-オクチルシアノアクリレート)は、機械的強度と抗菌効果を高めて開発されました。これらのドープされた接着剤(銀ナノ粒子)は、実行可能なサプリメントまたは縫合糸の代替としての組織接着剤の使用をサポートしました[89]。
呼吸器学
肺疾患はおそらく喘息、慢性閉塞性肺疾患(COPD)、および肺がんの発生率が高く、生命を脅かすことがよくあります。たとえば、COPDは4番目の主要な死因であり、肺癌は世界で最も一般的な癌による死因であると説明されています。ナノ粒子は、これらの重篤な疾患の治療を改善するための選択肢として精査されています[90]。さまざまな薬物を含むナノ粒子が、肺疾患の治療における局所的および全身的効果のために利用されてきました。肺疾患の作用部位への治療薬の送達は、慢性肺感染症、肺癌、結核、および他の呼吸器疾患の効果的な治療を可能にする可能性があります[91]。この目的で使用されるナノキャリアには、リポソーム、脂質またはポリマーベースのミセル、デンドリマー、およびポリマーNPが含まれます[92]。ポリマーは、共重合、表面修飾、またはバイオコンジュゲートして、カプセル化された薬剤の標的化能力および分布を改善することができるため、ポリマーNPは名目上重要です。肺のドラッグデリバリーで一般的に使用されるナノキャリアには、ゼラチン、キトサン、アルギン酸塩などの天然高分子と、ポロキサマー、PLGA、PEGなどの合成高分子が含まれています[93]。
PLGA NPは、肺タンパク質/ DNA送達の担体として最も便利な一連の特性を示すのに対し、ゼラチンNPは好ましい相互選択であることが観察されました[94]。同様に、ドキソルビシンとクルクミンの異方性またはヤヌス粒子は、吸入による肺癌の治療のために抗癌剤を輸送するために処方されました。粒子は、生体適合性および生分解性材料の二成分混合物を使用して配合された。これらの粒子は、遺伝子および細胞毒性の結果を示さなかった。癌細胞はこれらのヤヌス粒子を内在化し、核と細胞質にそれらを集中させ、長期の保持をもたらします。さらに、ポリアミドアミン(PAMAM)デンドリマーは、G3、G4、およびG4 [12]デンドリマーを使用して、モデルの弱溶性抗喘息医薬品ベクロメタゾンジプロピオン酸(BDP)の肺送達用のナノキャリアとして評価されました。この研究は、BDPデンドリマーがエアジェットおよび振動メッシュネブライザーを使用した肺吸入の可能性があることを示しました。さらに、エアロゾルの特性は、デンドリマーの生成ではなくネブライザーの設計によって影響を受けることが観察されました[95]。さらに、無機金属、金属酸化物、メタロイド、有機生分解性、および無機生体適合性ポリマーで構成される人工ナノ粒子(ENP)は、ワクチンやドラッグデリバリー、およびさまざまな肺疾患の管理のための担体として効率的に使用されました。肺に対するENPの特性と有効な効果を図1に示します。無機ENP(銀、金、および炭素ENP)、金属酸化物ENP(酸化鉄、酸化亜鉛、および二酸化チタン)、および有機ENP(脂質ベース、多糖類ベース、ポリマーマトリックスベース)が開発され、肺免疫止血について評価されました。比較的安全なキャリアであるだけでなく、現代の研究では、抗炎症特性(銀やポリスチレンなど)と免疫恒常性の維持を示す肺の刷り込み(ポリスチレンなど)を備えた有益な結果を克服するENPケーブルが示されました。メカニズムをさらに知ることは、肺の免疫恒常性および/または炎症性肺疾患の管理に対するENPの有用な効果をよりよく理解するのに役立つ可能性があります[96]。
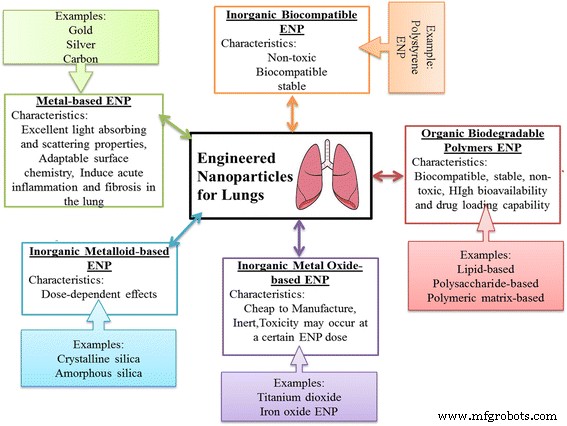
肺に対するENPの特性と有効効果
機能化されたカチオン性リポポリアミン(Star:Star-mPEG-550)が、肺血管細胞へのin vivo送達用のsiRNA(短鎖干渉RNA)用に最近開発されたことを述べることが重要です。このバランスの取れた脂質製剤は、マウスの肺におけるsiRNAの保持を強化し、標的遺伝子の有意な分解を達成しました。結果は有用であり、機能化カチオン性リポポリアミンナノ粒子を使用して肺動脈症を動員し、激しい肺動脈性肺高血圧症(PAH)のラット内の心臓の機能を矯正することにより、肺へのmiRNA-145阻害剤送達の毒性が低下することがわかりました[97]。 / P>
心臓血管系
心血管疾患は、心血管系、脳と腎臓の血管疾患、および末梢動脈障害に影響を与える病気です。薬理学的および臨床的管理のすべての進歩にもかかわらず、心不全は世界中の罹患率の最大の理由です。心不全を治療するために、細胞移植、遺伝子送達または治療、およびサイトカインまたは他の小分子を具体化する多くの新しい治療戦略が研究されてきた[98]。発展途上国では不十分な数の人々が影響を受けています。心血管障害による死亡の80%以上は発展途上国で発生し、男性と女性でほぼ均等に発生します[99]。マザーズら。 2008年には、毎年940万人が死亡していると推定されています[100]。これは、冠状動脈性心臓病による死亡の45%、心臓発作による死亡の51%を結論付けています[101]。高分子ミセル、リポソーム、デンドリマー、リポタンパク質に支持された医薬品担体、ナノ粒子薬物担体など、多くの異なるタイプの薬物送達媒体があります。
捕捉効率が83%以上のシロリムスのキトサンベースのリポソームは、再狭窄の治療のために開発され、効率的な標的化送達のための新しいプラットフォームであることが証明されています[102]。同様に、85%の捕捉効率を有するカルベジロールの胆汁酸塩に富むニオソームは、薬物の生物学的利用能の増強をもたらし、したがって、より良い治療効果が得られた[103]。バルーン損傷頸動脈の再狭窄の抑制は、血小板由来成長因子(PDGF)受容体の選択的遮断薬であるAGL2043およびAG1295をカプセル化するPLGAベースのナノ粒子を開発することによってラットで達成されます[104]。血管内皮増殖因子(VEGF)による心筋虚血の血管新生療法は、低酸素症とその続発効果を克服するための好ましいアプローチです。 VEGFを負荷した高分子粒子は、ラット心筋虚血モデルへのサイトカインの送達のための有望なシステムであることが証明されている。このアプローチは、臨床研究のためにさらに探求することができます[105]。コエンザイムQ10(CoQ10)は、ミトコンドリアの電子伝達系における役割のため、心筋虚血(MI)を治療するための信頼できる候補であるように見えますが、その貧弱なバイオ医薬品特性は、有望なデリバリーアプローチを開発することによって対処する必要がありました。高分子ナノ粒子は、CoQ10をカプセル化してその貧弱な医薬品特性を克服するために開発され、MI誘発ラットに投与されました。心臓機能は、3か月の治療の前後の駆出率を決定することによって分析されました。結果は、3か月後に駆出率の有意な改善を示しました[106]。
腫瘍学
癌は世界中の死亡の主な原因です。世界保健機関は、2005年から2015年の間に8400万人が癌で死亡すると決定しています。癌治療の最終的な目標は、化学療法の全身毒性を最小限に抑えることによって患者の寿命と生活の質を高めることです[107]。化学療法剤は過去25年間腫瘍学で広く研究されてきましたが、それらの腫瘍特異性は不十分であり、したがって用量依存的な毒性を示します。この制限を克服するために、最近の関心は、癌細胞を直接標的とし、制御された速度で薬物を送達し、治療効果を最適化することができるナノスケール送達担体の開発に集中している[108、109]。受動的および能動的ターゲティングは、腫瘍部位に薬剤を送達するために使用されます。松村と前田によって発見された「強化された透過性と保持(EPR)効果」と呼ばれる受動的な現象は、化学療法に使用される主要な経路です[110、111]。アクティブターゲティングは、受容体または刺激ベースのキャリアに結合するナノキャリアの表面にリガンドをグラフトすることによって達成されます。たとえば、デュアルリバース感熱[112]、光応答[113]、磁性ナノ粒子[114]、および酵素的に活性化されたプロドラッグ[115]。ナノ粒子(NP)は、高分子ナノ粒子[116]、ミセル[117]、リポソーム[118]、固体脂質ナノ粒子(SLN)[119]、タンパク質ナノ粒子[120]、ウイルスナノ粒子[121]などのさまざまなスマート治療担体と結合させることができます。 、金属ナノ粒子[122]、アプタマー[123]、デンドリマー[124]、およびモノクローナル抗体[125]は、それらの有効性を改善し、全身毒性を低減します。表3は、治療効果を最大化し、毒性を最小化して腫瘍を標的とするために広く研究されている、薬物送達のさまざまなアプローチをまとめたものです。
<図>タモキシフェンをロードした生分解性ポリ(o-カプロラクトン)ナノキャリアは、エストロゲン受容体特異的乳がんの管理のために開発されました[126]。この研究は、選択的エストロゲン受容体モジュレーターのナノ粒子調製物が特定のエストロゲン受容体ゾーンに薬物を送達し、治療効果を高めることを示唆しました。同様に、ドキソルビシンとシスプラチンのナノコンジュゲーションは、Chohenらによって開発されました。 [127]は、限局性進行性乳がんの治療において、負荷された薬剤の効率の向上と副作用の軽減を示しています。同様に、化学療法薬であるオキサリプラチンをロードしたナノ粒子ミセルは、Cabralらによって調製されました。 [128]は、腫瘍微小環境での負荷された薬物の持続放出により、抗腫瘍効果の増強をもたらしました[128]。さらに、SLNをロードした-5-FUは、バイオアベイラビリティの向上とカプセル化された抗がん剤の持続放出をもたらし、抗腫瘍効果の向上につながりました[129]。
結論
ナノテクノロジーは、特にヘルスケアの革新を行うために、さまざまな面で途方もない進歩を遂げています。標的選択的ドラッグデリバリーと分子イメージングのアプローチは、ナノテクノロジーが進歩的な役割を果たしている研究にとって最も重要な分野です。このレビューは、治療薬のイメージングと配信のためのさまざまなナノテクノロジーベースのアプローチの新しい進行中の可能性に関する幅広いビジョンを読者に提供します。効果的なドラッグデリバリーを得るために、ナノテクノロジーベースのイメージングにより、ナノマテリアルと生物学的環境との相互作用を把握し、受容体、疾患の病態生理学に関与する分子メカニズムを標的とし、治療反応のリアルタイムモニタリングが可能になりました。ナノメートル範囲の粒子のサイズを測定する分析技術の開発、およびナノ材料の最新の製造アプローチの出現により、眼科、肺、心血管疾患、さらに重要なことに癌の治療のための治療薬を送達するためのより効果的な方法が確立されました。治療。これらの新薬療法は、従来の療法よりも副作用が少なく、より効果的であることがすでに示されています。さらに、イメージング技術は、人体の腫瘍位置の決定とそれらの選択的ターゲティングを強化しました。全体として、この比較的新しく繁栄しているデータは、「概念実証」段階でさらに追加の臨床および毒性研究が必要であることを示唆しています。ナノメディシンのコストと大規模な製造も、対処する必要のある懸念事項です。それにもかかわらず、ナノメディシンの未来は前向きです。
略語
- AIE:
-
凝集による放出
- BDP:
-
ジプロピオン酸ベクロメタゾン
- BODIPY:
-
ホウ素ジピロメタン
- CNT:
-
カーボンナノチューブ
- COPD:
-
慢性閉塞性肺疾患
- CulnS 2 / ZnS:
-
銅インジウム硫化物/硫化亜鉛量子ドット
- CVD:
-
化学蒸着
- DNA:
-
デオキシリボ核酸
- ENP:
-
人工ナノ粒子
- EPR:
-
強化された透過性と保持力
- GCE:
-
ガラス状炭素電極
- GNP:
-
金ナノ粒子
- GQD:
-
書記素量子ドット
- HCG:
-
ヒト絨毛性ゴナドトロピン
- MEMS:
-
微小電気機械システム
- MI:
-
心筋虚血
- MNP:
-
磁性ナノ粒子
- MSN:
-
メソポーラスシリカナノ粒子
- MWNT:
-
多層カーボンナノチューブ
- NEMS:
-
ナノ電気機械システム
- PAH:
-
肺動脈性高血圧症
- PCL:
-
ポリカプロラクトン
- PDGF:
-
血小板由来成長因子
- PEG:
-
ポリエチレングリコール
- PET:
-
陽電子放出断層撮影
- PLGA:
-
ポリ乳酸-co-グリコール酸
- ROS:
-
活性酸素種
- SiRNA:
-
短鎖干渉RNA
- SLNS:
-
固体脂質ナノ粒子
- SPIO:
-
超常磁性酸化鉄
- VEGF:
-
血管内皮増殖因子
ナノマテリアル
- ラズベリーパイ制御アクアポニックス
- ドラッグデリバリーを強化するためのナノファイバーとフィラメント
- 生体適合性FePO4ナノ粒子:ドラッグデリバリー、RNA安定化、および機能的活性
- 腫瘍治療のためのドラッグデリバリーシステムとしての環境応答性金属有機フレームワーク
- 癌用途のための細胞ベースのドラッグデリバリー
- ゼブラフィッシュ:ナノテクノロジーを介した神経特異的ドラッグデリバリーのための有望なリアルタイムモデルシステム
- 黒色腫の標的化学療法治療のための薬物送達担体としての131I追跡PLGA-脂質ナノ粒子
- In VivoCTイメージングおよび腎クリアランス特性のための新しい生体適合性AuNanostars @PEGナノ粒子
- 二重ドラッグデリバリーのためのナノリポソームベースのシステムの物理化学的特性に関する調査
- ナノ粒子と超音波によって制御される水の過冷却
- コンパクトな3DLiDARイメージングシステム



