PPy被覆MnO2ハイブリッドマイクロ材料の調製とリチウムイオン電池のアノードとしてのそれらの改善されたサイクル性能
要約
MnO 2 @PPyコアシェルマイクロマテリアルは、MnO 2 上でのピロールの化学重合によって調製されます。 水面。ポリピロール(PPy)は、MnO 2 上に均質な有機シェルとして形成されます。 水面。 PPyシェルの厚さは、ピロールの使用によって調整できます。 SEM、FT-IR、X線光電子分光法(XPS)、熱重量分析(TGA)、およびXRDの分析を使用して、PPyシェルの形成を確認します。定電流セルサイクリングおよび電気化学的インピーダンス分光法(EIS)は、リチウムイオン電池のアノードとしての電気化学的性能を評価するために使用されます。結果は、MnO 2 の形成後 @PPyコアシェルマイクロマテリアルにより、リチウムイオン電池のアノードとしてのサイクル性能が向上します。 50マイクロリットルのPPyコーティングされたキャディークルーのようなMnO 2 620 mAh g -1 と同様に、最高のサイクリックパフォーマンスを発揮します。 300サイクル後に特定の容量を放電します。比較として、裸のMnO 2 の放電比容量 材料が200mAh g -1 を下回った 10サイクル後。 MnO 2 の改善されたリチウム貯蔵サイクル安定性 @PPyは、MnO 2 の構造の膨張と収縮を緩衝できるコアシェルハイブリッド構造に属性をサンプリングします。 Liイオンの埋め込みと解放の繰り返しによって引き起こされ、MnO 2 の粉砕を防ぐことができます 。この実験は、(リチウムイオン電池)LIBのアノード材料としての遷移金属酸化物材料の容量低下の問題を軽減する効果的な方法を提供します。
背景
3d遷移金属酸化物(MO; MはFe、Co、Ni、およびCu)が、Tarascon etal。によってリチウムイオン電池の高理論容量アノードとして機能することが提案されたためです。 [1]、さまざまな形態のマイクロ/ナノ金属酸化物を調製し、リチウムイオン電池のアノードとしての電気化学的性能を研究するために多くの努力が払われてきました[2、3、4、5、6]。たとえば、朱の研究グループは単分散のFe 3 を作成しました O 4 およびγ-Fe 2 O 3 界面活性剤を含まないソルボサーマル法によるミクロスフェア[3]。それらは、1307および1453 mAh g -1 の高い初期放電容量を持っていました。 、 それぞれ。 110サイクル後、放電容量は450 mAh g -1 のままでした。 Fe 3 の場合 O 4 および697mAh g -1 γ-Fe 2 の場合 O 3 。 Hongjing Wu etal。は、単純なシェルごとの自己組織化熱熱処理によって、均一なマルチシェル、特に5シェルのNiO中空球を準備していました。この研究のメリットは、マルチシェル中空構造の合成方法論に大きく貢献しました。しかし、NiO中空球のリチウム貯蔵性能はあまり優れていませんでした[4]。 MnO 2 理論的に重量分析で約1230mAh g -1 の高いリチウム貯蔵容量を備えています。;したがって、MnO 2 の設計、合成、および応用について多くの研究が行われています。 リチウムイオン電池用アノード[7,8,9,10]。たとえば、Chenの研究グループはγ-MnO 2 を作成しました 中空の微小球形状とナノ立方形状[11]。 20サイクル後、ナノキューブとミクロスフェアの放電容量は656.5と602.1 mAh g -1 でした。 。さらに、彼らはMnO 2 について多くの研究を行ってきました。 2000年から現在までのリチウムイオン電池の材料[12、13]。また、MnO 2 のアプリケーションについても調査しました。 リチウムイオン電池用のアノードですが、裸のMnO 2 の放電比容量 材料は200mAh g -1 を下回るまで急速に低下しました 10サイクル後[14]。
遷移金属酸化物材料は理論的に大きな比容量を持っていますが、MnO 2 を含むこれらすべての材料は アノードは一般に急速な容量低下に悩まされています。サイクル安定性が低い理由は次のとおりです。(1)遷移金属酸化物材料の電子伝導性は通常低く、電子またはイオンは拡散プロセスが困難であるため、不可逆的な電極反応と急速な容量低下が発生します。 (2)充電/放電サイクル後、遷移金属酸化物は大きな機械的応力を受けて粉砕され、活性粒子と集電体の間の電気的接触損失につながります。電気的接触のない遷移金属酸化物粒子は、充電/放電サイクルに参加できなくなり、容量が低下します[15、16]。
シェルコーティングは、サイクリングの安定性を向上させるための効果的な戦略です。この構造では、シェルは、Liイオンの繰り返しの埋め込みと解放によって引き起こされる金属酸化物材料の構造的な膨張と収縮をある程度緩衝することができます。現在のところ、カーボンコーティング、有機導電性ポリマーコーティング、グラフェンハイブリッド、およびその他の無機化合物コーティングが使用されています[17、18]。たとえば、Yin etal。準備されたポリピロール(PPy)でコーティングされたCuOナノコンポジット。コアシェルサンプルは、760 mAh g -1 という高い可逆容量を持っていました。 これは、裸のCuOサンプルよりもはるかに優れていました[19]。 Li etal。準備されたグラフェンで包まれたMnO 2 ナノリボン。可逆比放電容量は890mAh g -1 に達しました 0.1 A g -1 180サイクル後。したがって、MnO 2 にPPyシェルコーティングを施すことが必要かつ緊急です。 リチウムイオン電池のアノードとしてのサイクル安定性を向上させる材料[20]。
本研究では、MnO 2 の周期的性能を改善する リチウムイオン電池のアノードとしての材料であるポリピロール(有機導電性ポリマー)コーティングは、化学重合によって調製されていました。その結果、MnO 2 の形成後、サイクル性能が向上しました。 @PPyコアシェルマイクロマテリアル。この実験は、(リチウムイオン電池)LIBのアノード材料としての遷移金属酸化物材料の容量低下の問題を軽減する効果的な方法を提供します。
メソッド
サンプルの準備
すべての試薬は分析グレードであり、Shanghai ChemicalCompanyから購入しました。ピロールは、使用前に減圧蒸留によって精製し、0〜5°Cで保存し、残留重合を防ぐために光にさらされないように保護しました。他の試薬はさらに精製することなく使用されました。
MnO 2 マイクロマテリアルは、Yuらによって説明された同様の方法を使用して準備されました。 [14、21]いくつかの変更として。キャディークルーのようなMnO 2 を準備するには マイクロマテリアル、1.70 g MnSO 4 ・h 2 Oを15mLの蒸留水に激しく攪拌しながら溶解しました。溶液が透明になったら、2.72 g K 2 を含む20mL水溶液 S 2 O 8 連続的に攪拌しながら上記の溶液に加えた。次に、得られた透明な溶液を、総量の80%の容量のテフロンで裏打ちされたステンレス鋼のオートクレーブ(50 mL)に移しました。オートクレーブを密閉し、110°Cで6時間維持しました。反応が完了した後、オートクレーブを自然に室温まで冷却させた。固体の黒い沈殿物をろ過し、蒸留水で数回洗浄して不純物を除去した後、空気中80°Cで3時間乾燥させました。得られたキャディークルーのようなMnO 2 PPyコーティングされたMnO 2 の製造のためにマイクロマテリアルが収集されました 材料。ウニのようなMnO 2 マイクロマテリアルは同様の方法で調製されました。 1.70gのMnSO 4 を追加した後 ・h 2 Oおよび2.72g K 2 S 2 O 8 35 mLの蒸留水、2mLのH 2 SO 4 その後、追加されました。
MnO 2 @PPyハイブリッドマイクロマテリアルは、MnO 2 上でのピロールの化学重合によって調製されました。 界面活性剤としてベンゼンスルホン酸ナトリウム(BSNa)とFeCl 3 を使用した表面 酸化剤として。 BSNaに対するモノマーピロールのモル比は3:1でした。まず、0.2 g MnO 2 0.01 mol L -1 を50mL入れたビーカーに分散させました。 BSNa水溶液で、0.5時間攪拌します。混合物を攪拌しながら氷/水浴(0〜5°C)に入れました。次に、一定量のピロールを混合物に加えた。 0.5時間攪拌した後、少量のFeCl 3 溶液を水溶液に滴下して加え、重合プロセスを開始した。淡い黒から濃い黒への色の漸進的な変化は、PPyの形成を示した。混合物を0〜5°Cで12時間撹拌しながら維持し、MnO 2 を形成しました。 @PPyコアシェルマイクロマテリアル。 PPyの厚さは、ピロールの使用量によって制御されました。最後に、得られた複合材料をろ過し、水とエタノールで洗浄した後、60°Cで4時間真空乾燥しました。
サンプルの特性評価
SEM画像とエネルギー分散型分光法(EDS)の形態学的調査は、走査型電子顕微鏡(QUANTA-200 America FEI Company)で行われました。製品の結晶構造は、XRDを使用して決定されました。XRDは、Cuターゲットを備えたRigaku D / max-2200 / PCで、7°/分のスキャン速度で2θが10°から70°の範囲で記録されました。 MnO 2 のフーリエ変換赤外(FT-IR)スペクトル KBrでパレット化された@PPyハイブリッドマイクロマテリアルは、NicoletIS10分光計で実行されました。熱重量分析(TGA)も、MnO 2 の重量損失を決定するために使用されました。 @PPyハイブリッドマイクロマテリアル、空気中25〜800°Cで10°C /分(MELER / 1600H熱重量分析装置)。 X線光電子分光法(XPS)の測定値は、励起源としてAlKαX線を使用して、Ulvac-PHI、PHI5000 Versaprobe-IIX線光電子分光器で記録されました。 XPS分析で得られた結合エネルギーは、284.8eVのC1sピークに対して較正されました。
細胞の組み立てと電気化学的研究
合成された製品の電気化学的リチウム貯蔵特性は、乾燥したアルゴンが充填されたグローブボックス内に組み立てられたCR2025コイン型テストセルを使用して測定されました。作用電極を製造するために、 N に溶解した60wt。%の活物質、10 wt。%のアセチレンブラック、および30 wt。%のポリフッ化ビニリデン(PVDF)からなるスラリー -メチルピロリドンを銅箔にキャストし、80°Cで真空下で5時間乾燥させました。リチウムシートを対極および参照電極として使用し、Celgard2320メンブレンをセパレーターとして使用しました。電解質は1M LiPF 6 の溶液でした エチレンカーボネート(EC)-1,2-ジメチルカーボネート(DMC)(体積で1:1)。定電流充放電実験は、Land電気試験システムCT2001A(Wuhan Land Electronics Co.、Ltd。)によって、電流密度0.2 C、0.01〜3.00 V(Li / Li + に対して)で実行されました。 )。 MnO 2 の比容量を計算する場合 @PPyコアシェルマイクロマテリアル、PPyの質量が含まれています。電気化学インピーダンス分光法(EIS)の測定は、電気化学ワークステーション(CHI604D、Chenhua、Shanghai)で実行され、周波数は0.1Hzから100KHzの範囲で、AC信号の振幅は5mVでした。
結果と考察
サンプルの形態的特徴
純粋なPPyサンプル、ウニのようなMnO 2 の形態 サンプル、およびMnO 2 ピロールの重合量が異なる@PPyハイブリッドマイクロマテリアルは、SEM測定によって特徴付けられます。図1に示すように、純粋なPPyサンプルは、直径が約800 nmの球形であり、層状の岩として一緒に凝集する傾向があります。ウニのようなMnO 2 サンプルを図1aに示します。 MnO 2 マイクロマテリアルは、直径が約3μmの均一なウニのような形状であり、約1μmの均一な長さのいくつかの真っ直ぐで放射状に成長したナノロッドで構成されています。 MnO 2 の形態の進化 @PPyハイブリッドマイクロマテリアルを図1b–eに示します。ピロールの量が少ない場合、PPyは最初に核を形成し、次にMnO 2 の針状ナノロッドのギャップに埋め込まれます。 サンプル。図1bの針状のナノロッドは、図1aに示されているものよりも明らかに幅が広い。ピロールの量が20μLに増加しても、ナノロッド構造はまだ存在しますが、明らかではありません。ピロールの量が30μLに増加すると、MnO 2 の針状のナノロッド構造 マイクロマテリアルは完全に消え、球形になります。ピロールの量がさらに増えると(図1e)、PPyシェルは非常に厚くなります。スキーム1は、MnO 2 の可能な形成プロセスを示しています。 @PPyハイブリッドマイクロマテリアル。最初の段階では、PPyの小さな結晶核が、FeCl 3 の酸化によってモノマーピロールから生成されます。 。次に、結晶核が「ウニ」の表面のとげの間の隙間に沈着します。 PPyの連続重合により、とげの間の隙間が徐々に埋められていきます。最後に、「ウニ」全体がPPyで均一にコーティングされます。 MnO 2 の低倍率SEM画像 追加ファイル1の@PPyハイブリッドマイクロマテリアルは、PPyシェルがMnO 2 上で均一に形成されていることを確認します @PPyサンプル。

PPyでコーティングされたウニのようなMnO 2 のSEM画像 サンプル。左上隅には純粋なPPy、 a があります ウニのようなMnO 2 サンプル、 b 10μL、 c 20μL、 d 30μL、および e 50μLのピロールでコーティングされたウニのようなMnO 2 サンプル。スケールバーは1μm
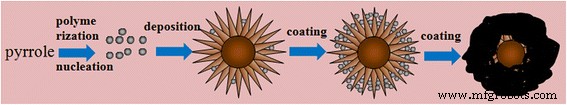
MnO 2 に提案された形成メカニズムの概略図 @PPyマテリアル
この作品では、キャディークルーのようなMnO 2 マイクロマテリアルも同様の方法でPPyでコーティングされています。 SEMの形態は、追加ファイル1に示されています。サポート情報1.キャディークルーのようなMnO 2 マイクロマテリアルはナノワイヤーの形をしており、直径2〜4μmの球体に凝集して、キャディスクリューのように見えます。ピロールの量が少ない場合、PPyは最初に小さな粒子として形成され、MnO 2 の表面に付着します。 サンプル。ピロールの量が増えると、PPyは徐々にキャディークルーのようなMnO 2 を覆います。 完全に岩のように見える大きなブロック構造を形成します。
PPyの均一なコーティングは、エネルギー分散型X線(EDX)分光分析によってさらに検証されます(表1を参照)。純粋なMnO 2 では、炭素と窒素の信号は検出されません。 サンプル。 PPyおよびMnO 2 で、かなりの量の炭素および窒素信号が検出されます。 PPyシェルの形成による@PPyサンプル。ピロールの使用量が増えると、炭素と窒素の含有量も増えます。 caddice-clewのようなMnO 2 のEDXデータ @PPyサンプルは、追加ファイル1:サポート情報4に示されています。
<図>サンプルのFT-IR分析
合成されたPPyとMnO 2 の構造の特徴と組成 @PPyサンプルは、FT-IR分光法によってさらに特徴づけられます(図2を参照)。すべてのMnO 2 @ PPyサンプルとPPyサンプル、1550、1448、1283、および1130 cm -1 のバンド PPyリングの特徴的なピークです。その中で、約1550 cm -1 のピーク これは、C-CおよびC =Cの伸縮によるもので、約1448 cm -1 にピークがあります。 PPyのC-Nストレッチからです。約1130cm -1 のピーク これは、BSNaに属するS =O伸縮振動ピークによるものです。これは、スルホン酸イオンがピロール環にドープされていることを示しています。 I 1550 の比率 とI 1448 通常、PPyの共役とドーピング度に起因します[22]。 I 1550 が高いほど / I 1448 はより高い共役であり、PPyのドーピング度はです。つまり、I 1550 / I 1448 が高い場合、PPyの導電率はより良いはずです。 1550、917、および778 cm -1 のバンド 30μLのPPyでコーティングされたウニのようなMnO 2 サンプルは、50μLのPPyでコーティングされたキャディークルーのようなMnO 2 のサンプルよりも弱いです。 サンプル。したがって、PPyでコーティングされたキャディークルーのようなMnO 2 の導電率 サンプルの方が優れているはずです。50μLのPPyでコーティングされたキャディークルーのようなMnO 2 サンプルは、より優れたリチウム貯蔵性能を備えている必要があります。 1040および778cm -1 のバンド C βのC-H変形の面内および面外振動です。 -H吸収帯。 C αなし -H吸収帯がスペクトルで観察されます。これは、ピロール環が主にPPyのα-αによって結合されていることを示しています。 1657 cm -1 の吸収帯 製品に水分子が含まれているためです。したがって、FT-IRの結果は、PPyシェルがMnO 2 上に形成されていることを証明しています。 @PPyサンプル。
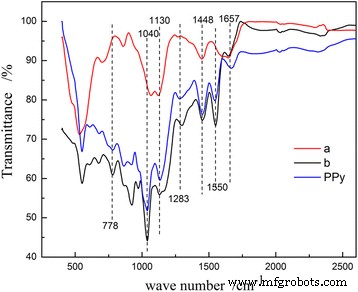
(a)30μLのPPyでコーティングされたウニのようなMnO 2 のFT-IRスペクトル サンプルおよび(b)50μLのPPyコーティングされたキャディークルーのようなMnO 2 サンプルと純粋なPPy
XPSの結果
通常、コアシェル構造はTEMで検証する必要があります。ただし、純粋なMnO 2 ここのサンプルは厚すぎて、良好なTEM画像を撮ることができません。そこで、コアシェル構造を検証するために、XPSテストとEDSテストを実行して、表面とサンプル全体のさまざまなコンポーネントを検証しました。わかりやすくするために、30μLのPPyでコーティングされたウニのようなMnO 2 の分光法のみ サンプルと50μLのPPyコーティングされたキャディークルーのようなMnO 2 サンプルを図3に示します。その他は追加ファイル1:サポート情報5にあります。最終結果を表2に示します。O1、N1、C1、およびMn(2p1 / 2、 2p3 / 2)は、それぞれ531.2、398.9、284.8、651.4、640.3eVと決定されます。 973と901.6、および848.9 eVのピークは、O KLLピーク(酸素原子からのオーガーピーク)とMn LMMピーク(Mn原子からのオーガーピーク)です。図3に示すように、XPSによって検出されたFeまたはClがいくつかあります。ここで、FeまたはCl信号の出現は、FeCl 3 の使用によるものです。 PPyシェルを調製する際の重合酸化剤として。表2に示されているように、EDS分析とXPS分析の違いは明確です。 XPS分析では、O、N、およびCの含有量ははるかに高くなります。 Mnの含有量は少ないです。 XPSの最大分析深度は約5〜10nmです。強いO、N、およびCピークは、MnO 2 サンプルはPPy有機フィルムで覆われています(SEM段落で説明されています)。
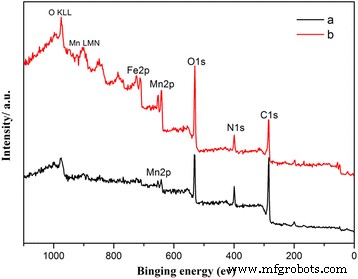
(a)30μLのPPyでコーティングされたウニのようなMnO 2 のXPSスペクトル サンプルおよび(b)50μLのPPyコーティングされたキャディークルーのようなMnO 2 サンプル
TGAの結果
合成されたMnO 2 でPPyシェルを証明する @PPyサンプル、裸のMnO 2 のTGA サンプル、ベアPPy、およびMnO 2 @PPyサンプルは空気中で実行されます。図4はTGAの結果です。図4からわかるように、裸のPPy粉末は2つの減量領域を示しています。 60〜260°Cの温度範囲での最初の約12%の重量減少は、以前の文献[19、23、24]で述べられているように、物理吸着水の脱着と表面吸収溶媒の除去に起因する可能性があります。一方、260〜600°Cの範囲で約88%の2回目の重量減少は、PPyの酸化によるものです。その結果、裸のPPy粉末は600°Cで完全に燃焼します。 TGAテスト後、裸のウニのようなMnO 2 サンプルとキャディークルーのようなMnO 2 サンプルは800°Cで88.7wt。%と91.6%のままです。最も重量が減少するのは60〜300°Cの温度範囲であるため、両方のサンプルが非常に乾燥しているように見えますが、表面に吸収された溶媒が除去されたことが原因である可能性があります。 30μLのPPyコーティングされたウニのようなMnO 2 サンプルでは、60〜260°Cの範囲での重量損失は10%であり、0〜800°Cの範囲での全体の重量損失は32.3%です。 PPyの酸化前後の重量の変化は、MnO 2 のPPyの量に直接変換できます。 @PPyサンプル[25]。この方法を使用すると、30μLのPPyでコーティングされたウニのようなMnO 2 のPPyの量 サンプルは約22%です。この値は、PPyの理論量に近い値です。 50μLのPPyコーティングされたキャディークルーのようなMnO 2 サンプルでは、0〜800°Cの範囲での全体の重量損失は43.9%であり、60〜260°Cの範囲での重量損失は14%です。したがって、50μLのPPyでコーティングされたキャディークルーのようなMnO 2 のPPyの実際の量 サンプルは約30%で、理論値に非常に近い値です。したがって、結果はMnO 2 粒子はPPy有機フィルムで覆われています。
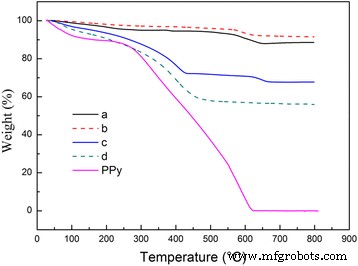
PPyおよびMnO 2 のTGA曲線 サンプル。 ( a )ウニのようなMnO 2 サンプル、( b )caddice-clew-like MnO 2 サンプル、( c )30μLのPPyコーティングされたウニのようなMnO 2 サンプル、および( d )50μLのPPyコーティングされたキャディークルーのようなMnO 2 サンプル
サンプルのXRD特性評価
MnO 2 の結晶構造 @PPyサンプルはXRDによって検査されます(図5)。示されているように、PPyはアモルファス構造です。 PPyでコーティングすると、ウニのようなMnO 2 @PPyサンプルはα-MnO 2 を保持します 構造。回折ピークは2θ=12.7°、18.1°、28.8°、37.5°、42.1°、49.9°、56.2°、および60.3°に現れ、(110)、(200)、(310)の回折ピークとよく一致します。 (211)、(301)、(411)、(600)、および(521)α-MnO 2 の結晶面 標準データ(JCPDSカードPDFファイルNo.44-0141)。 PPyの量が増えると、アモルファスPPyの形成により、XRDピークの強度が徐々に低下します。 PPyでコーティングされたキャディークルーのようなMnO 2 に示されているように サンプルでは、75および100uLのサンプルに15°から30°の明らかなアモルファスピークがあります。 PPyでコーティングすると、キャディークルーのようなMnO 2 @PPyサンプルはα-MnO 2 を保持します 構造も。 PPyの量が増えると、材料は明らかに結晶からアモルファスに変化します。これらの結果は、PPy有機膜がMnO 2 にうまくコーティングされたことをさらに証明しています。 粒子。
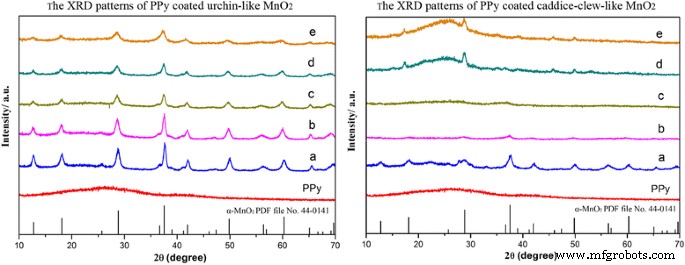
PPyコーティングされたMnO 2 のXRDパターン サンプル。左は( a )ウニのようなMnO 2 サンプルと( b )10μL、( c )20μL、( d )30μL、および( e )50μLのPPyコーティング。右は( a )caddice-clew-like MnO 2 サンプルと( b )30μL、(c)50μL、( d )75μL( e )、および100μLのPPyコーティング
電気化学的性能
これらのMnO 2 の電気化学的性能 LIBのアノード材料としての@PPyサンプルが調査されます。図6a、bは、裸のMnO 2 から構築されたアノードの典型的な充放電曲線(フルバッテリーと比較)を示しています。 サンプルとMnO 2 @PPyは、0.01〜3.00Vの電圧範囲で0.2Cのレートでサンプリングします(vs. Li / Li + )。わかりやすくするために、裸のMnO 2 のみ サンプルとMnO 2 最高の充放電性能を持つ@PPyが表示されます。ご覧のとおり、MnO 2 の放電-電荷プロファイル @PPyサンプルは、ベアMnO 2 のサンプルと類似しています。 、これは、有機PPyシェルでコーティングされたハイブリッド製品がMnO 2 の電気化学的性質を変化させないことを示しています。 LIBアノード。ただし、PPyコーティングされたMnO 2 のリチウム貯蔵性能 サンプルが大幅に改善されました。むき出しのウニのようなMnO 2 サンプルとPPyでコーティングされたウニのようなMnO 2 サンプルは両方とも、約1200〜1400 mAh g -1 の高い初期放電比容量を持っています 、理論上の放電比容量は1232 mAh g -1 です。 。余分な放電固有の容量は、SEI層の形成に起因する可能性があります[14]。 10サイクル後、裸のウニのようなMnO 2 の排出比容量 サンプルが200mAh g -1 未満に減少します 。比較として、PPyでコーティングされたウニのようなMnO 2 の放電比容量 サンプルは約500mAh g -1 のままです 300サイクル後でも。キャディークルーのようなMnO 2 そしてPPyでコーティングされたキャディークルーのようなMnO 2 よく似ています。 10サイクル後、裸のキャディークルーのようなMnO 2 の放電比容量 200 mAh g -1 未満に減少します 。 PPyでコーティングされたキャディークルーのようなMnO 2 サンプルは500〜600 mAh g -1 に維持されます 300サイクル後。
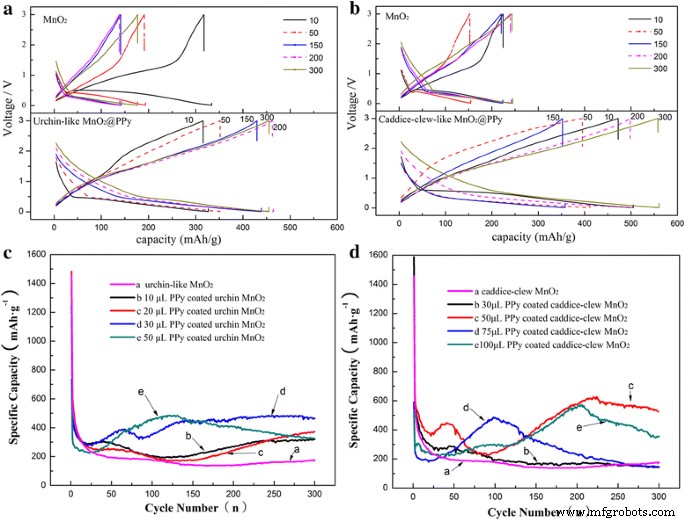
a 、 b 30μLのPPyでコーティングされたMnO2サンプルと50μLのPPyでコーティングされたキャディークルーのようなMnO2サンプルの選択されたサイクルの放電曲線。 c 、 d MnO2サンプルとPPyコーティングされたMnO2サンプルのサイクリング性能
リチウム貯蔵サイクルの安定性を評価するために、放電/充電の測定がMnO 2 で300サイクル実行されます。 さまざまなピロールがコーティングされた@PPyサンプル。 PPyの厚さは、ピロールの量によって制御されます。図6c、dに示すように、ピロールの量が少ない場合(たとえば、キャディークルーのようなMnO 2 の場合は30uL ウニのようなMnO 2 の場合は10uL )、このハイブリッドMnO 2 のリチウム貯蔵容量 @PPyサンプルは明確に改善されていません。これは、PPyフィルムが薄すぎて、MnO 2 を防ぐことができないことを示しています。 粉砕に苦しむ材料。ただし、ピロールの量が増えると、ハイブリッドMnO 2 の放電比容量 @PPyサンプルは著しく強化されています。キャディスクルーのようなMnO 2 の場合 、ピロールの量が50 uLに増加すると、ハイブリッドMnO 2 @PPyサンプルは、最大の放電固有容量が620 mAh g -1 です。 300サイクル後。ウニのようなMnO 2 、最大の放電比容量は、30uLのピロールを使用した場合に表示されます。 300サイクルでの放電比容量は480mAh g -1 。さらに、図6c、dからわかるように、すべてのハイブリッドMnO 2 @PPyサンプルでは、周期的安定性が向上しています。ハイブリッドMnO 2 の改善されたリチウム貯蔵循環安定性 @PPyサンプルは、金属酸化物/導電性ポリマーのコアシェルハイブリッド製品の独自の構造に起因する可能性があります。この構造では、柔軟なPPyシェルにより、MnO 2 の構造的な膨張と収縮を効果的に緩衝できます。 Liイオンの繰り返しの埋め込みと解放によって引き起こされます。さらに、PPyシェルはMnO 2 の粉砕を防ぐことができます 、およびMnO 2 間の電気的接触の喪失を保護します 材料と集電体(銅箔)。一方、裸のMnO 2 の低容量と高速容量のフェージング MnO 2 の粒子間接触の粉砕と喪失に起因する可能性があります またはMnO 2 の連絡先 繰り返しの充放電プロセス中の大容量の膨張/収縮による銅箔コレクターを使用。したがって、このPPyコーティングの実験は、LIBのアノード材料としてのすべての遷移金属酸化物材料の容量低下の問題を軽減する効果的な方法を提供します。
MnO 2 のレートパフォーマンス @PPyサンプルを図7に示します。レート能力をテストするために、充電/放電サイクルは0.01〜3.0 Vの電圧範囲で実行され、放電レートは0.2C→0.5C→1.0C→2.0C→5.0Cです。 →2.0C→1.0C→0.5C→0.2C。図7aは、5.0〜0.2 Cの段階でのレート能力です。示されているように、すべてのMnO 2 の放電比容量 5.0〜0.2 Cの段階のサンプルは、0.2〜5 Cの段階のサンプルと非常によく似ており、MnO 2 サンプルは比較的高い可逆性を持っています。ただし、すべてのMnO 2 の放電固有の容量 サンプルは1Cレートを超えると不十分です。ハイブリッドMnO 2 のメリット レートパフォーマンスの@PPyサンプルは、低レート(0.2、0.5、および1 C)で確認できます。 5°Cでの放電後、PPyでコーティングされたキャディークルーのようなMnO 2 の放電容量 サンプルは508mAh g -1 0.2 Cで、わずか160 mAh g -1 として、はるかに小さい放電容量が得られます。 裸のキャディークルーのようなMnO 2 の0.2Cで サンプル。したがって、PPyでコーティングされたキャディークルーのようなMnO 2 サンプルのレートパフォーマンスが向上しました。 PPyでコーティングされたウニのようなMnO 2 の状況 サンプルは非常に似ています。それにもかかわらず、放電容量は、PPyでコーティングされたキャディークルーのようなMnO 2 の放電容量よりも少し低くなっています。 サンプル。
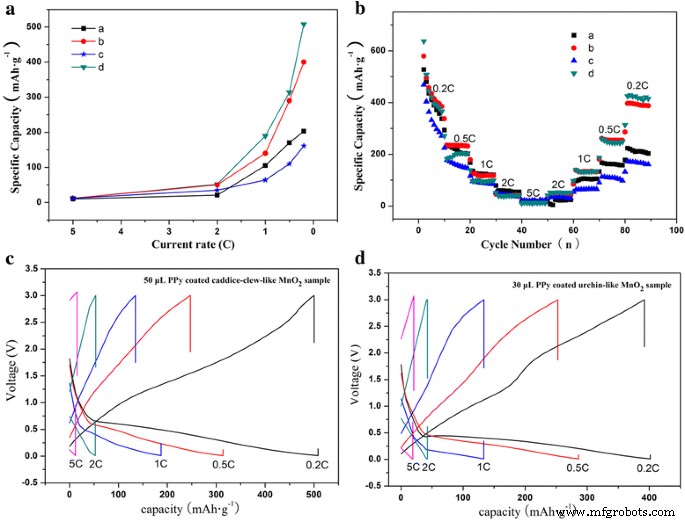
a レート機能、 b パフォーマンスを評価し、 c 、 d MnO 2 の充放電曲線 @PPyサンプル。 ( a 、 b )ウニのようなMnO 2 サンプルと30μLのPPyコーティングされたサンプル。 ( c 、 d )Caddice-clew-like MnO 2 サンプルと50μLのPPyコーティングされたサンプル
レートパフォーマンスに示されているように、ウニのようなMnO 2 マイクロマテリアルは、キャディークルーのようなMnO 2 よりも比較的高い放電比容量を持っています 以前の報告[14]と一致するマイクロマテリアル。ただし、PPyコーティング後、キャディークルーのようなMnO 2 @PPyサンプルは、リチウム貯蔵の周期的安定性が優れています。ここで、PPyの共役次数が1つの理由である可能性があります。 FT-IR分析は、キャディーズクルーのようなMnO 2 のPPy共役度を示しています。 @PPyサンプルの方が高くなっています。つまり、キャディークルーのようなMnO 2 @PPyサンプルは、より優れた導電性とより優れた電気化学的性能を備えている必要があります。それを確認するために、EISテストが実行されます。
図8は、動作電圧での5サイクル後のリチウム電池のEIS結果を示しています。図8aに示すように、キャディスクリューのようなMnO 2 のインピーダンススペクトル 明らかに、高周波数領域から中周波数領域の2つの扁平な半円と、低周波数領域の傾斜した線で構成されています。ただし、他の3つのサンプルの2つの半円は、簡単には区別できません。 Z での切片 本物 高周波領域の軸は、オーム電解質抵抗( R )に対応します。 s )。高周波の最初の半円は、リチウムイオンの移動抵抗( R )に起因します。 sf )SEIフィルムを介して。高から中周波数の2番目の半円は、電荷移動抵抗( R )に起因します。 ct )。低周波数領域の傾斜線は、ウォーバーグインピーダンス( W )を表します。 s )、これは活物質中のリチウムイオン拡散に関連しています。両方のハイブリッドMnO 2 の半円形部分 @PPyサンプルは、コーティングされていないMnO 2 のサンプルよりもはるかに小さいです。 サンプル。これは、ハイブリッドMnO 2 の導電率を示しています。 @PPyサンプルの方が優れており、PPyコーティング後のLiイオンの電荷移動抵抗は減少します。キャディスクルーのようなMnO 2 の半円抵抗 @PPyサンプルはわずか77Ωです。ウニのようなMnO 2 の半円抵抗 @PPyサンプルはわずか95Ωです。ここでは、PPyコーティング後、キャディークルーのようなMnO 2 の抵抗が低くなります。 マイクロマテリアルは、リチウム貯蔵のサイクル安定性の向上を説明できます。
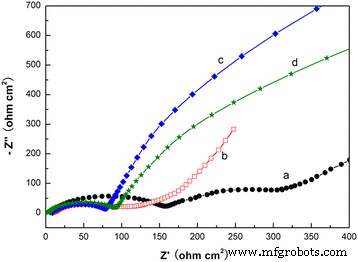
Li / MnO 2 のナイキスト線図 開回路電圧のセル。 ( a )caddice-clew-like MnO 2 サンプル。 ( b )ウニのようなMnO 2 サンプル。 ( c )50μLのPPyコーティングされたキャディークルーのようなMnO 2 サンプル。 ( d )30μLのPPyコーティングされたウニのようなMnO 2 サンプル
結論
要約すると、MnO 2 @PPyコアシェルマイクロマテリアルは、MnO 2 でのピロールの化学重合によって正常に調製されます。 水面。 PPyシェルの厚さは、ピロールの使用によって調整できます。 MnO 2 の形成後 @PPyコアシェルマイクロマテリアル、リチウムイオン電池のアノードとしてのサイクル性能が向上しています。 50マイクロリットルのPPyコーティングされたキャディークルーのようなMnO 2 最高のサイクリックパフォーマンスを持ち、620 mAh g -1 300サイクル後に特定の容量を放電します。比較として、裸のMnO 2 の放電比容量 材料が200mAh g -1 を下回っている 10サイクル後。 MnO 2 の改善されたリチウム貯蔵サイクル安定性 @PPyサンプルは、コアシェルハイブリッド構造に起因する可能性があります。この構造では、柔軟なPPyシェルにより、MnO 2 の構造的な膨張と収縮を効果的に緩衝できます。 Liイオンの埋め込みと解放の繰り返しによって引き起こされ、MnO 2 の粉砕を防ぐことができます 。したがって、このPPyコーティングの実験は、LIBのアノード材料としての遷移金属酸化物材料の容量低下の問題を軽減する効果的な方法を提供します。
ナノマテリアル
- 改善された診断および治療用途のための多機能金ナノ粒子:レビュー
- リチウムイオン電池の電気化学的性能が向上したLiNi0.8Co0.15Al0.05O2 /カーボンナノチューブの機械的複合材料
- リチウムイオン電池用のCr3 +およびF-複合ドーピングを用いたLiNi0.5Mn1.5O4カソード材料の合成と電気化学的性質
- リチウムイオン電池用の効率的なアノード材料としての数層のMoS2 /アセチレンブラック複合材料
- 中空構造LiNb3O8光触媒の調製と光触媒性能
- リチウムイオン電池用の金属酸化物アノードの電気化学的性能に及ぼす異なるバインダーの影響
- リチウムイオン電池のアノード材料としてのマグネシウム-熱還元によって製造された埋め込みSi /グラフェン複合材料
- Co3O4ナノワイヤの環境にやさしく簡単な合成とリチウムイオン電池でのグラフェンによるそれらの有望な応用
- リチウムイオン電池用のパルスレーザー堆積によって調製されたナノ結晶Fe2O3膜アノード
- 階層的多孔質シリカライト-1カプセル化AgNPの調製と4-ニトロフェノール還元のためのその触媒性能
- リチウムイオン電池の高性能アノードの前駆体としての酸素内方拡散によるスラッジSiのナノSi / SiOx構造への変換



