卵殻膜テンプレートMnO2ナノ粒子:容易な合成とテトラサイクリン塩酸塩除染
要約
MnO 2 を合成するために、表面の網状タンパク質と還元基を利用して、卵殻膜(ESM)が選択されました。 ESMがテンプレートと還元剤の両方として機能する非常に簡単な方法による過マンガン酸カリウムからのナノ粒子。このプロセスは、過酷な反応条件や複雑な後処理を回避し、グリーン合成、便利な操作、低コスト、および容易な精製のメリットを備えていました。 ESMテンプレートのMnO 2 ナノ粒子(MnO 2 NPs / ESM)の特性を明らかにし、テンプレート上のナノマテリアルの含有量をテストしました。 MnO 2 NPs / ESMは、テトラサイクリン塩酸塩(TCH)の除染に優れた能力を示しました。遠心分離やろ過の代わりに、膜を取り出して分解を止めることにより、巨視的な材料を簡単に分離することができます。 TCHの72.27%(50 mg / L)が20分で0.1920 g / L MnO 2 によって除染されたことが調査されました。 ナノ粒子、および除去効率は、緩衝条件下で60分後に83.10%に達する可能性があります。動力学は緩衝液の有無にかかわらず研究され、分解プロセスは疑似二次モデルに従ったと結論付けられた。材料の容易な合成と効果的な分解は、ナノMnO 2 を促進します ベースの除染アプリケーション。
背景
医薬品とパーソナルケア製品(PPCP)は一種の新たな水質汚染であり、生態学と人間の健康を考慮して研究者によって密接に懸念されています[1,2,3,4,5]。細菌感染症を治療および予防するための薬としての抗生物質は世界中で使用されており、それに伴って環境への動揺のリスクが徐々に現れています[6]。代表として、テトラサイクリン(TC)薬は、獣医学および水産養殖で何年にもわたって使用されてきました[7]。しかし、TCは環境中でほとんど分解されないため、長期間持続し[8、9]、生態系や人間の健康にさまざまな悪影響を及ぼします[10、11、12、13]。したがって、TCで汚染された水を除染するための簡単で効果的な方法をスクリーニングすることは、研究のホットスポットになっています。有望な技術の1つは、二酸化マンガンナノ材料の支援かもしれません。
二酸化マンガンナノ材料は、高表面積、調整可能な構造、触媒酸化活性、および環境に無害であるという独自のメリットにより、広く研究されてきました[14、15]。したがって、nano-MnO 2 ベースのアプリケーションは、触媒作用[16、17]、センサー[18、19]、コンデンサー[20、21]からドラッグデリバリー[22、23]、癌治療[24、25]に至るまでさまざまな分野をカバーしています。同様に、MnO 2 吸着および酸化特性を備えたナノ材料が廃水処理に適用されています。 MnO 2 で処理された重イオン[26]、有機染料[27]、フェノール[28]などの水質汚染物質 ナノマテリアルが報告された。一方、レボフロキサシン[29]、シプロフロキサシン[30]、ノルフロキサシン[31]、スルファメトキサゾール[32]、スルファジアジン[33]、セファゾリン[34]、リンコサミド[35]、TC [36、37]などの抗生物質は成功しています。 MnO 2 による除染 処理。 TC抗生物質に特異的で、多孔性の高いMnO 2 ナノシートを利用してテトラサイクリンを分解し、pH、温度、および用量ベースの動態を調査しました[38]。 MnO 2 テトラサイクリン塩酸塩(TCH)とAs(III)を同時に除去するためにベースのスキームが適用され、MnO 2 中のヒ素と抗生物質に対する相互作用効果 治療が研究された[39]。 MnO 2 によるテトラサイクリン抗生物質の分解 が実行され、変換の速度論と経路が報告されました[40]。上記の作業でTCの高い除去効率が得られましたが、通常、抗生物質溶液から材料を分離するための遠心分離またはろ過に伴う分解操作は、処理時間の多くを要し、プロセスを複雑にしました。
並外れた特性を持つユニークな生体材料としての卵殻膜(ESM)は、材料科学で広く利用されています[41]。 ESMの繊維の主な組成は、ESMに金属を結合する能力を与えるタンパク質です。 AgNPやAuNPなどの貴金属ナノ材料は、ESMをテンプレートとして使用して正常に合成されました[42、43、44]。さらに、ZnO [45]、Co 3 などの金属酸化物ナノ材料 O 4 [45]、PbO [45]、Mn 3 O 4 [46]、およびTiO 2 [47]は、ESMテンプレートによっても作成されました。これにより、合成が容易になり、制御できるようになり、金属または金属酸化物ナノ粒子を合成するための新しいパスが提供されました。
この作業では、卵殻膜テンプレートMnO 2 ナノ粒子(MnO 2 NPs / ESM)は、バイオテンプレート法によって簡単かつ迅速に合成されました。卵殻膜は、ナノ粒子を巨視的膜上に均一に分散させるテンプレートと還元剤としての二重の役割を果たしました。酸化性MnO 2 を組み合わせる 操作が簡単な膜、MnO 2 を備えたナノ粒子 NPs / ESMはさらにテトラサイクリン塩酸塩除染に適用され、溶液を取り出すだけでナノマテリアルを簡単に分離できました。
メソッド
材料と装置
導電率が18.2MΩcm -1 の脱イオン水 この実験では、浄水システム(ULUPURE、成都、中国)から使用されました。過マンガン酸カリウム(KMnO 4 、 M w =158.03)、MnO 2 粉末およびその他の試薬は、少なくとも分析グレードであり、Kemiou Chemical Co. Ltd.(Tianjin、China)から購入しました。テトラサイクリン塩酸塩(TCH、USPグレード)およびグルタチオン(GSH、98%)は、Aladdin Reagents Company(上海、中国)から購入しました。太原工業学院のHongye学生食堂から入手した新鮮な卵殻から卵殻膜(ESM)を注意深く剥がしました。 PBS緩衝液(0.2 M、pH =7.0)は、39mLのNaH 2 を混合して調製しました。 PO 4 溶液(0.2 M)および61 mL Na 2 HPO 4 溶液(0.2 M)、および異なるpH値のPBS溶液は、上記の溶液を水酸化ナトリウムまたは塩酸溶液(両方の濃度は0.2 M)で必要なpH値に滴定することによって調製しました。
MnO 2 の走査型電子顕微鏡(SEM) NPs / ESMは、形態観察のためにQuanta 200FEG走査型電子顕微鏡で実施しました。 MnO 2 の透過型電子顕微鏡(TEM)および高分解能透過型電子顕微鏡(HRTEM) NPはTecnai-G20透過型電子顕微鏡で実施されました。調製したままのMnO 2 のサイズ分布 NPはレーザー粒子サイザー(Malvern Nano-ZS90)で得られました。 X線光電子分光法(XPS)は、製品の表面組成と化学状態テストのために、単色AlKα放射線を使用してAXIS ULTRA DLD電子分光計(Kratos)で収集されました。 ESMおよびMnO 2 の熱重量分析(TG)分析 NPs / ESMは、Rigaku TG熱分析装置(Rigaku Co. Japan)を使用して、空気中で10°C /分の加熱速度で測定されました。 4000〜400 cm -1 のフーリエ変換赤外分光法(FTIR) ESMとMnO 2 の NPs / ESMは、Tensor II FTIR分光計(Bruker、ドイツ)のKBrディスクに記録され、スペクトルはデコンボリューションによって処理されました。 TCHの紫外可視(UV-vis)吸収スペクトルは、TU-1901 UV-vis分光光度計(中国、蒲渓)で記録されました。
ESMテンプレートMnOの合成 2 ナノ粒子
卵殻膜テンプレートMnO 2 ナノ粒子(MnO 2 NPs / ESM)は、簡単で簡単な方法で合成されました。典型的なプロセスでは、最初に卵殻膜を新鮮な卵殻から手作業で剥がし、脱イオン水で10回洗浄して、不要な卵白を除去しました。室温で乾燥させた後、きれいなESMをそれぞれ5mgの重さのスライスにカットしました。合成時に、ESMの10スライスを20 mL KMnO 4 に浸しました。 溶液(1 mmol / L)とオープンシステムを室温で攪拌し続けました。 35分後、ESMスライスを取り出し、脱イオン水で10回洗浄して、余分な溶液を除去しました。最後に、得られたメンブレンを乾燥させ、室温で保存して、さらに特性評価と使用を行いました。
TCHの除染
TCHの除染は、MnO 2 を追加することによって実行されました。 NPs / ESMをTCH溶液に入れ、室温で攪拌します。 MnO 2 の20スライス NP / ESMを15mLのTCH溶液(50 mg / L)に入れ、PBS緩衝液で希釈し、60分間攪拌し続けました。処理後のTCH溶液のUV-visスペクトルは、室温ですぐに記録されました。 TCH測定のすべての吸収強度は、358nmの波長に設定されました。除去効率( R 、%)は、次の式を使用して計算されました:
$$ R =\ frac {C_0-C} {C_0} \ times 100 \%$$ここで C 0 および C (mg / L)は、それぞれ処理液中のTCHの初期濃度と最終濃度を表します。
結果と考察
MnOのメカニズムとモニタリング 2 NPs / ESM合成
MnO 2 の合成 NPs / ESMは、バイオテンプレートとしてESMを使用したオープンシステムで実行されました。卵殻膜は多くの繊維状タンパク質で構成されており、その上に–OH、–NH 2 などの多くの還元基があります。 、–SHなどが点在していました。 KMnO 4 が発生すると、その場での酸化還元反応が引き起こされました。 が導入されました。 MnO 2 生成され、これらのアクティブなグループの周りで徐々に成長しました。結果として、繊維状タンパク質の表面に均一に分散し、ESMテンプレートのMnO 2 を形成しました。 NP。
図1aは、さまざまな時点での合成システムの写真を示しています。紫色のKMnO 4 溶液は徐々に薄茶色に変わり、その間に白いESMスライスは茶色になりました(図1b、c)。合成プロセスを監視するために、KMnO 4 の吸収強度 525 nmで、このシステムのpHを図1dで調べました。示されているように、KMnO 4 の吸収強度 時間の経過とともに低下し、逆にpHは徐々に改善しました。 2セットのデータは両方とも35分後にプラットフォームを示したため、合成時間を選択しました。 pHの上昇は、反応中の–OHの形成に起因し、反応過程は以下のように推測されました。
ESM(赤)+ KMnO 4 + H 2 O→MnO 2 / ESM(Ox)+OH¯+ K +
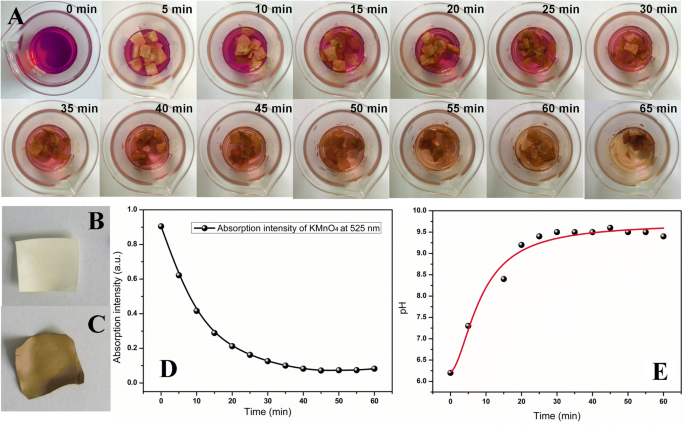
a さまざまな時点での合成システムの写真。 b レドックス反応前のESMスライスの画像。 c MnO 2 の画像 NP / ESM。 d KMnO 4 の吸収強度 525nmで。 e さまざまな時点での合成システムのpH
MnO 2 の特性評価 NP / ESM
得られたMnO 2 の形態 NPs / ESMは、図2の走査型電子顕微鏡(SEM)によって調査されました。多層で交差するフィブリンネットワークが図2a、bで観察されました。さらに増幅した後、繊維状タンパク質の表面に均一にコーティングされた多くの粒子が見つかりました。したがって、ESMは還元剤としてだけでなく、合成中にテンプレートとしても機能したと結論付けられました。 MnO 2 のサイズをさらに調査するには 粒子、レーザー粒子サイザー試験を実施した。 4.8 nmの粒子が分解されたタンパク質である可能性を排除するために、MnO 2 NP / ESMと等量のブランクESM(コントロール)を最初にNaOH溶液(0.1 M)に入れ、30分間煮沸した後、ろ過して溶液を形成し、試験条件を満たすようにしました。追加ファイル1:図S1で、MnO 2 の平均サイズが見つかりました。 NPは4.8nmでした。 MnO 2 の写真 NaOH処理前後のNP / ESMは、追加ファイル2:図S2Aに表示されています。膜の茶色は明らかに色あせたが、NaOH処理後も膜は変化しなかったことが明らかであり、MnO 2 NPはテンプレートから解放されました。卵殻からのタンパク質のサイズが結果を妨げる可能性があるという問題を考える際に、NaOH処理後のろ過溶液はブランクESMとMnO 2 の両方から得られました。 (追加ファイル2:図S2B)は、それぞれ無色と茶色になります。さらに、NaOH処理後のESMのサイズ分布データは、追加ファイル2で平均1.7nmのサイズを示しました。図S2C。したがって、4.8nmの粒子がESM自体から分解されたタンパク質である可能性は除外されました。これに基づいて、前述のろ液を透析した後、TEMを取得しました。図2cに示すように、球状のナノ粒子が観察され、サイズは追加ファイル1のサイズと一致していました:図S1。図2dのHRTEM画像は、2.5Åの格子間隔を示しています。これは、α-MnO 2 の(400)格子面とよく一致しています。 [48]。

MnO 2 のSEM画像 異なるスケールバーを備えたNP / ESM(2μm( a )および200 nm( b ))。 TEM( c )およびHRTEM( d )MnO 2 の画像 NP、スケールバーはそれぞれ10nmと5nmでした
また、得られたMnO 2 の表面組成と元素分析のためにX線光電子分光法(XPS)技術を実施しました。 NP / ESM。フルスキャンスペクトル(図3a)は、合成された材料が元素Mn 2p、O 1s、N 1s、およびC1sで構成されていることを示しています。要素C1、N 1、および部分O 1は、テンプレートESMから取得されました。詳細を研究するために、Mn2pおよびO1sの部分XPSスペクトルを測定しました。図3bに示すように、653.8および642.0eVの2つのピークをMn2p 1/2 に割り当てることができます。 およびMn2p 3/2 、 それぞれ。 O 1sスペクトル(図3c)は、結合エネルギーが532.6、531.4、および530.5 eVの3つの成分ピークに分割できます。これらは、H–O–H、Mn–O–H、およびMn–O–Mnに起因します。 、 それぞれ。上記のデータは、準備されたままの材料がESMテンプレートのMnO 2 であることを示しています。 NP。
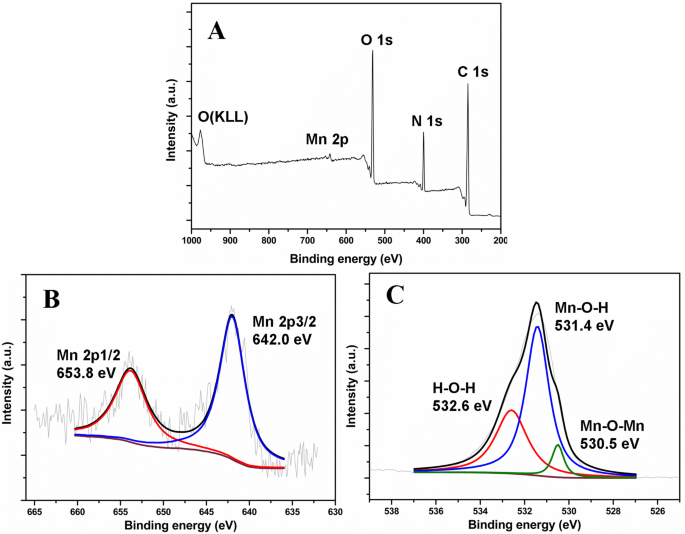
XPS( a )フルスキャン、( b )Mn 2p、( c )調製されたままのMnO 2 のO1sスペクトル NP / ESM
この結果をさらに検証するために、GSHとMnO 2 の間の特別な反応に触発されて得られた材料を、GSH溶液をテストに適用しました。 [49、50]。追加ファイル3:図S3に示すように、MnO 2 の茶色 GSH溶液に1分間浸した後、消えました。これは、ESMにコーティングされた材料がMnO 2 であることを示しています。 。さらに、熱重量分析(TG)分析を実施して、MnO 2 の質量含有量を測定しました。 ESMで。追加ファイル4の黒と赤の曲線:図S4は、ESMのみとMnO 2 の質量変化を表しています。 それぞれNP / ESM。 ESMの相対的な品質は600°Cでほぼゼロであり、ESMが完全に燃え尽きていることを示しています。ただし、ESMテンプレートのMnO 2 の相対的な品質 ESMが燃え尽きた後、NPは2.61%のままでした。 MnO 2 500°Cで熱分解され、Mn 2 に変換されました O 3 [51]。さらに、Mn 2 のさらなる熱分解 O 3 Mn 3 へ O 4 1000°C以上で発生しました[52]。したがって、この実験で得られた800°Cでの2.61%の質量含有量は、Mn 2 の含有量を反映しています。 O 3 。 Mnの質量保存の法則によると、元のMnO 2 ESMへのコンテンツの読み込みは2.88%と計算されました。
ESMおよびMnO 2 のFTIRスペクトル(追加ファイル5:図S5) 材料を粉末に粉砕した後、NP / ESMを収集した。タンパク質とナノ粒子間の相互作用には、主に二次構造の変化が含まれます。これは、アミドI〜1650 cm -1 のバンドに反映されます。 (少しずれることがあります)またはアミドII〜1550 cm -1 。ただし、1650または1550 cm -1 付近でピーク位置に明らかな変化はありませんでした。 MnO 2 の前後のESMの タンパク質の構造変化を示すことができた以前に報告された結果とは異なっていた[53]。詳細を調べ、小さな変更を見逃さないようにするために、これらのスペクトルにデコンボリューションが適用されました。 1650または1550cm -1 付近には、観測可能なピークは見られませんでした。 、506 cm -1 の新しいピーク MnO 2 の後に登場 NPの負荷、およびそれはMn–Oの特徴的な振動モードと関連していた[54]。
Mnにはさまざまな酸化状態があるため、Mn 2 などの酸化物にはいくつかの種類があります。 O 3 、MnO、およびMnO 2 。 Mn 2 の結合エネルギー O 3 MnO 2 のそれに近い 。この作業でMnの酸化状態を調べるために、準備されたままの材料のHRTEMを画像化し、図2dに表示しました。検出された2.5Åの格子間隔は、α-MnO 2 の(400)格子面とよく一致しています。 [48]。さらに、私たちのMn材料は、KMnO 4 間の酸化還元反応に基づいて得られました。 MnO 2 の形成に有利な中性条件下でのESM 他の酸化状態の代わりに[55]。重要なのは、調製されたままの材料がGSHとの反応活性を持っていることです(追加ファイル3:図S3)。これは、ナノ粒子がMnO 2 であることの証言でもあります。 [49、50]。 MnO 2 500°Cで熱分解され、Mn 2 に変換される可能性があります O 3 [51]。追加ファイル4の準備されたままの材料のTG曲線:図S4は、500°C付近で明らかな重量減少を示しており、MnO 2 からの変換を示しています。 Mn 2 へ O 3 、これは、Mnの酸化状態がMnO 2 であるという別の証拠です。 。
MnO 2 によるTCH除染 NP / ESM
酸化的MnO 2 を利用する NPと巨視的テンプレート、MnO 2 NPs / ESMは、効果的な除去と簡単な操作により、テトラサイクリン塩酸塩(TCH)の除染に適用されました。図4aは、ESMのみ(黒)とMnO 2 で処理された358nmでのTCHの時間依存吸収強度を示しています。 NP / ESM(赤)。 ESMのみの存在下で吸収強度が変化しないことが示された。ただし、最初は急激に低下し、MnO 2 の下では徐々に平らになりました。 NPs / ESM治療。この明らかなコントラストは、MnO 2 の容量を示しています TCH除染のためのNP / ESM。同様に、ESM処理後のTCHのUV-vis吸収スペクトルはほとんど変化しませんでしたが、358nmの吸収ピークはMnO 2 の後で明らかに減少しました。 NP / ESM除染(図4b)。図4cは、TCHの吸収スペクトルの変動を調査したもので、最初の10分間で270 nmの吸収ピークが低下しましたが、時間の経過とともに358nmの別のピークが低下しました。 MnO 2 による時間依存の除去効率 NP / ESM除染は図4dで計算され、除去効率は20分で72.27%であり、60分で83.10%に達する可能性があることがわかりました。
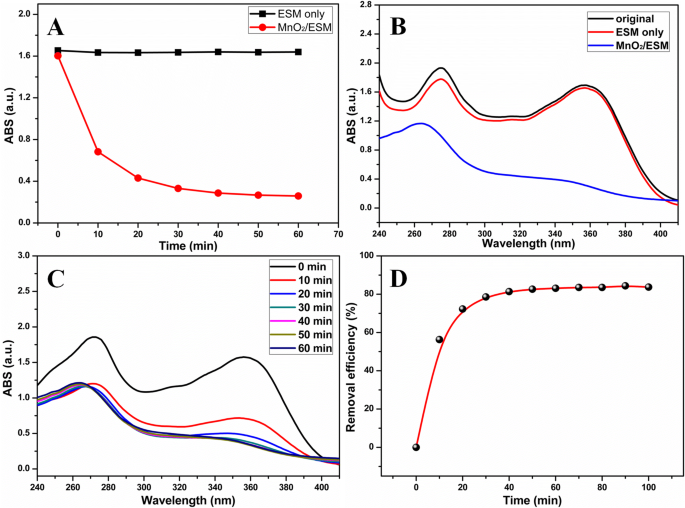
a ESMおよびMnO 2 によるTCHの時間依存吸収強度 NPs / ESM治療。 b ESMまたはMnO 2 の前後のTCHのUV-vis吸収スペクトル NPs / ESM治療。 c TCHおよび( d の時間依存UV-vis吸収スペクトル )MnO 2 で処理された除去効率 NP / ESM。 (条件:MnO 2 の20スライス NPs / ESMまたはESM、TCHの初期濃度は50 mg / L、制御されたpHは3.0)
TCH除染に対するpHとバッファーの影響
pHはMnO 2 で重要な役割を果たしました ベースの酸化分解、およびこの作業でのTCH除染に対するpHの影響を調査しました。図5aは、MnO 2 の前後のTCHの吸収強度を示しています。 さまざまなpHで60分間のNP / ESM処理、および対応する除去効率を図5bで計算しました。 MnO 2 によるTCHの最適な除染が実証されました NPs / ESMは、pH3.0のPBSバッファー下で達成されました。さらに、MnO 2 によるTCH除染 緩衝液なしのNPs / ESMを図5cで調査しました。この図では、TCHの吸収強度が徐々に低下し、分解システムのpHが着実に向上しました。除染プロセス中のpH上昇の同じ現象は、以前の研究でも報告されています[38]。バッファーなしの除去効率は、最初(最初の20分)のバッファー状態の場合よりも急速に増加したことは注目に値します。ただし、時間が経つにつれて、30分後にバッファーありの除去効率がバッファーなしの除去効率を上回りました(60分でバッファーありの場合は83.10%、バッファーなしの場合は78.37%)。除去効率は、線形検量線プロットから計算されたTCHの濃度変動によって監視されました(追加ファイル6:図S6および追加ファイル7:図S7)。緩衝条件下では、PBSからの生理食塩水イオンがTCH分子のMnO 2 の表面への拡散を妨げました。 さらなる反応のためのNP、したがって、反応速度は緩衝液なしの場合よりも低かった。しかし、緩衝されていない条件下での時間とともに反応系のpHが上昇すると、MnO 2 の酸化能力が制限されました。 NP、したがって除去効率は、制御された最適pHの下で得られるものに到達することはできません。
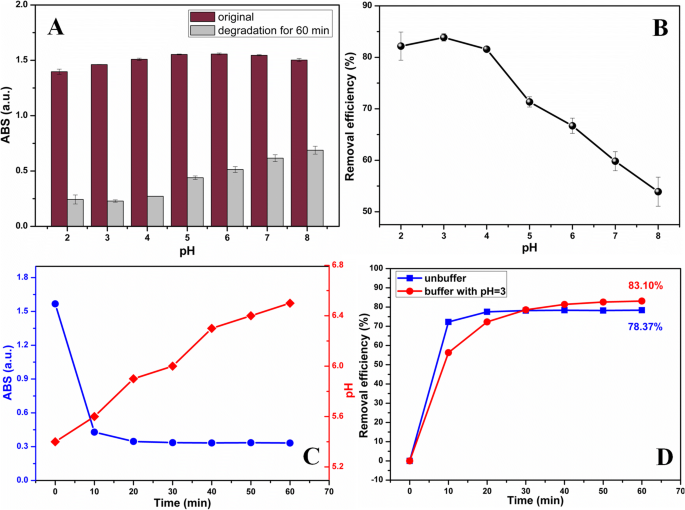
a 分解前後のTCHの吸収強度と( b )異なるpHでの除去効率。 c 緩衝されていない条件下でのTCHの時間依存吸収強度およびpH変動。 d 緩衝条件下と非緩衝条件下でのTCHの除去効率の比較。 (条件:MnO 2 の20スライス NPs / ESM、TCHの初期濃度は50 mg / Lでした。)
TCH除染の速度論的研究
MnO 2 によるTCHの劣化をさらに理解する NPs / ESM、速度論的研究は、MnO 2 のTCH初期濃度または用量を変更することによって実施されました。 。さまざまな量のMnO 2 による分解の速度論を調査しました バッファリングされた条件下で。図6aは、さまざまな用量のMnO 2 によって劣化したTCHの時間依存吸収強度を示しています。 (0.0960、0.1440、および0.1920 g / L)、および対応する除去効率は図6bで計算されました。また、疑似1次と疑似2次による線形速度論プロットを、それぞれ図6c、dに適合させました。さらに、さまざまな時間での吸収強度(図7a)と除去効率(図7b)を監視することにより、バッファーを使用したさまざまな初期濃度のTCH(30、50、および70 mg / L)での分解を調べました。図7c、dは、線形1次/ 2次反応速度プロットをフィッティングして、反応速度を調査しました。同様に、さまざまな量のMnO 2 での分解速度 バッファなしの条件下でのNPとさまざまな初期TCH濃度は、それぞれ追加ファイル8:図S8と追加ファイル9:図S9で調査されました。表1は、さまざまな条件から得られた速度論データを示しています。 MnO 2 によるTCH分解の速度論を実証するために、相関係数を線形適合させて計算しました。 NP / ESM。一般に、疑似2次モデルで計算された相関係数は、疑似1次モデルで計算された相関係数よりも高く、このプロセスが疑似2次モデルとより一貫していることを示しています。詳細には、この疑似2次モデルは、少量のMnO 2 でより高い相関係数を示しました。 またはTCHの高い初期濃度。いずれにせよ、バッファーなしの劣化と比較して、バッファー条件では相関係数は1に近かった。
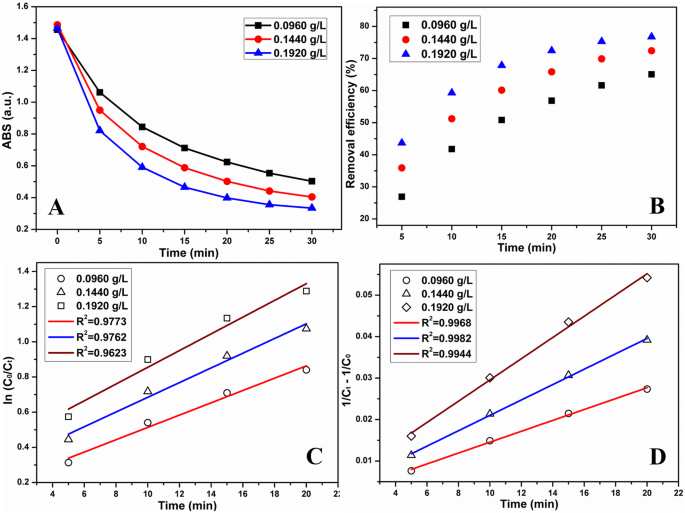
時間依存の a TCHと b の吸収強度 さまざまな量のMnO 2 による除去効率 NPs / ESM治療。 c 線形一次反応速度プロットと d さまざまな量のMnO 2 による線形2次反応速度プロット NPs / ESM治療。 (条件:TCHの初期濃度は50 mg / L、制御されたpHは3.0でした)
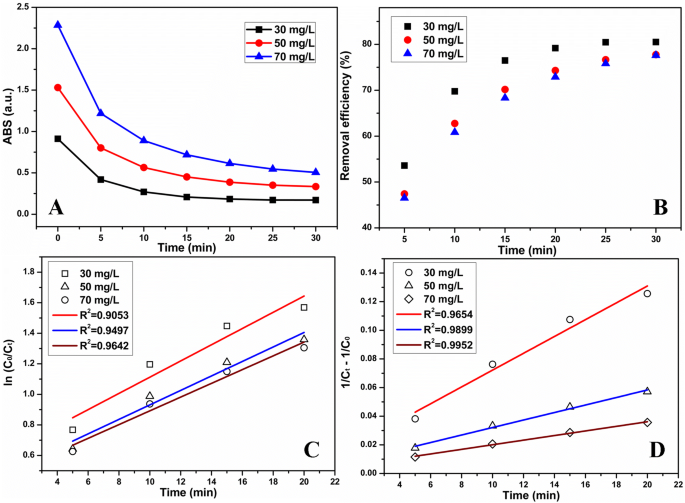
時間依存の a TCHと b の吸収強度 TCHのさまざまな初期濃度の劣化に対する除去効率。 c 線形一次反応速度プロットと d TCHのさまざまな初期濃度の劣化に関する線形2次反応速度プロット。 (条件:MnO 2 の投与量 NPs / ESMは0.1740g / L、制御されたpHは3.0)
商用MnOの比較 2 粉末およびその他の報告された資料
準備されたままのMnO 2 の高度な特性を説明するため NPs / ESM、同量の商用MnO 2 粉末は、同じ条件下でTCH除染について対照的にテストされました。図8は、調製したままのMnO 2 からの除去効率を示しています。 NP / ESMおよび商用MnO 2 緩衝液の有無にかかわらず粉末。 MnO 2 NPs / ESMは、市販のMnO 2 よりも優れた利点を示しました。 両方の条件下で粉末。 MnO 2 による除去効率は約80%ですが 除染は以前の研究[38、39]で得られ、MnO 2 を介してpH =6.5で最大98%に達する可能性があります。 MnO 2 とのZVIカップリングによる複数の効果に起因する、ゼロ価鉄(ZVI)ベースの透過性反応性バリア(PRB)システム[56] 。その上、他の材料もTC除染に適用されました。固定化されたTiO 2 AuおよびCuSナノ粒子で修飾されたナノベルト(Au–CuS–TiO 2 NB)は、その優れた光触媒活性により、オキシテトラサイクリン(OTC)に対して96%の除去効率を示しました[57]。効率的な吸着剤としての酸化グラフェン(GO)は、24時間後にTCの良好な除去を示しました( R =96%)[58]。粉末活性炭/ Fe 3 O 4 磁性ナノ粒子(PAC / Fe 3 O 4 MNPs)はH 2 への触媒として適用されました O 2 支援されたTC分解、および94.5%の除去効率が得られました[59]。処理時間を延長したり、材料の投与量を増やしたりすることで、除去効率を高めることができることに気づきました[39]。それにもかかわらず、すべての作業には複雑な劣化測定とその後の処理が必要であり、これにより労力とテスト時間が増加します。遠心分離やろ過などの便利な操作により、除染手順が容易になります。
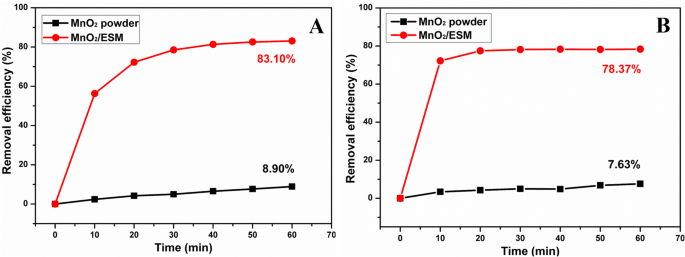
同等の市販のMnO 2 によるTCHの除去効率の比較 粉末とMnO 2 a でのNP / ESM バッファリングされ、 b バッファリングされていない状態
結論
MnO 2 ナノ粒子は、卵殻膜と過マンガン酸カリウム溶液を混合することにより、非常に簡単な手順でこの作業で合成されました。この過酷な反応条件や複雑な後処理の不必要な方法により、合成と精製のプロセスが迅速かつ便利になりました。得られたMnO 2 ナノ粒子は繊維状タンパク質の表面に均一に分散し、微視的/巨視的組み合わせモードを形成します。さらに、卵殻膜テンプレートMnO 2 ナノ粒子はテトラサイクリン塩酸塩除染に適用されました。バッファリングされた条件下で60分後に83.10%の除去効率と、疑似2次モデルの反応速度が得られました。最も注目すべきは、MnO 2 NP / ESMは、溶液から取り出すことで簡単に分離でき、遠心分離やろ過などの複雑な操作を回避できるため、ナノマテリアルベースの廃水除染に有利です。
略語
- ESM:
-
卵殻膜
- GSH:
-
グルタチオン
- HRTEM:
-
高分解能透過型電子顕微鏡
- NP:
-
ナノ粒子
- OTC:
-
オキシテトラサイクリン
- PBS:
-
リン酸緩衝生理食塩水
- PPCP:
-
医薬品およびパーソナルケア製品
- SEM:
-
走査型電子顕微鏡
- TCH:
-
テトラサイクリン塩酸塩
- TC:
-
テトラサイクリン
- TEM:
-
透過型電子顕微鏡
- TG:
-
熱重量分析
- UV-vis:
-
紫外可視
- XPS:
-
X線光電子分光法
ナノマテリアル
- Escherichia coliに対する酸化銅ナノ粒子の生体合成、特性評価、および抗菌力の評価
- 小さなセレンナノ結晶とナノロッドの容易な合成と光学的性質
- リチウムイオン電池用の高性能アノード材料としてMWNTに固定されたSiO2 @ Cナノ粒子の容易な合成
- CuSナノ粒子でコーティングされた着色および導電性CuSCN複合材料の容易な合成
- アスペクト比が異なり、高性能で柔軟な透明電極として使用される銀ナノワイヤーの容易な合成
- フェニルトリメトキシシランで修飾されたアルミナナノ粒子をベースにしたAl2O3:SiOCナノコンポジットの形成と発光特性
- 水溶性α-NaGdF4/β-NaYF4:Yb、Erコアシェルナノ粒子の合成と発光特性
- 光熱治療および光音響イメージングのためのポリピロール被覆鉄-白金ナノ粒子の合成およびinvitro性能
- 蒸発誘起自己組織化と強化されたガス検知特性によるワームホールのようなメソポーラス酸化スズの容易な合成
- 銅ナノ粒子の合成と安定化におけるグリーン熟達度:触媒、抗菌、細胞毒性、および抗酸化活性
- Co3O4ナノワイヤの環境にやさしく簡単な合成とリチウムイオン電池でのグラフェンによるそれらの有望な応用



