空気環境にゼオライト-3AをドープしたEu3 +イオンとその効率的な緑色発光ダイオードから得られたEu2 +活性化緑色発光リン光物質
要約
Eu 2+ 活性化リン光物質は、その優れた光学性能により、照明およびディスプレイ領域に広く適用されています。この論文では、優れた緑色発光ゼオライト-3A:1.3 wt%Euリン光物質が、還元性雰囲気や薬剤を使用せずに、環境に優しい高熱反応法によって調製されています。一方、Eu 3+ からの還元メカニズム Eu 2+ へのイオン イオンが調査されます。実験結果は、形態、結晶構造、および発光特性が焼結温度の影響を受けることを示しています。得られたサンプルは、広い励起バンドが310〜450 nmの範囲にあり、広い発光バンドのピークが523nmにあることを示しています。さらに、ゼオライト-3A:1.3 wt%Euリン光物質は、市販のUV発光チップにカプセル化され、国際照明委員会(CIE)の色座標が(0.295、0.537)の純粋な緑色発光ダイオード(LED)を製造します。 。
背景
発光材料は、照明やディスプレイデバイスなどの多くの分野で広く使用されています[1,2,3,4,5]。希土類(RE)ユーロピウム(Eu)で活性化された発光材料は、高輝度[6、7]、高い化学的安定性[8、9]、優れた特性などの独自の光学特性により、長年にわたって注目を集めています。環境にやさしい[8、10]。特に、Euイオンには2価の2つの酸化状態(Eu 2+ )があります。 )および3価(Eu 3+ )、異なる発光特性を示します。通常、Eu 3+ イオンは主に 5 に由来する赤色発光活性剤として存在します D 0 → 7 F J ( J =1、2、3、4、および5)遷移[11、12、13]。ただし、Eu 2+ イオン、つまり外側の軌道にある5d電子は、周囲の影響を受けやすくなっています。したがって、それらの放出は、紫外線(UV)から赤までの広い領域を持つ結晶場環境の影響を受けやすくなります。 Chen etal。準備されたEu 2+ 活性化フルオロホスフェートBa 3 GdNa(PO 4 ) 3 青と赤の二重発光リン光物質を含むF [14]。佐藤ら報告された赤色発光Ca 2 SiO 4 :Eu 2+ リン光物質[15]。リンら。合成されたEu 2+ 、Mn 2+ -活性化されたCa 9 Mg(PO 4 ) 6 F 2 青から黄色に発光するリン光物質[16]。 Eu 2+ パリティが許可された5d–4f電子遷移によって引き起こされる活性化リン光物質は、強力な広い発光バンドを示します[7]。したがって、Eu 2+ 活性化リン光物質は、近年の発光材料の主な焦点です。
現在、Eu 2+ ドープされた発光材料は、Eu 3+ を還元することによって得られます Eu 2+ へ 、天然のEu 2+ がないため ドープされた材料。通常、H 2 を含む還元性雰囲気で実現できます。 、H 2 / N 2 、またはCO。たとえば、Gao etal。最近入手したEu 2+ Eu 3+ からの活性化リン -交換されたUSY(Na 28 Si 168 Al 28 ・240H 2 O、Si / Al比=6)H 2 での熱処理によるゼオライト / N 2 還元性雰囲気[17]。 Chen etal。 Eu 2+ 増感されたSr 6 Ca 4 (PO 4 ) 6 F 2 :Tb 3+ リン光物質は、H 2 で高温固体法を使用して得ることができます。 / N 2 還元性雰囲気[18]。それにもかかわらず、還元性雰囲気での反応は比較的危険であり、設備の整った作業環境を必要とし、それはリン光物質のより高いコストにつながる。また、CO還元条件下で反応を進めると環境汚染が発生します。そのため、環境に優しく、環境に優しく、低コストの準備方法が注目を集めています。
よく知られているように、Eu 3+ ホウ酸塩[19]、リン酸塩[20]、アルミン酸塩[21]などのいくつかの特殊な化合物ホストの中でも、Eu 2+ に還元することができます。 高温の空気中で。これらの化合物はすべて、剛体の四面体BO 4 を含むことが示唆されています。 、PO 4 、AlO 4 、または八面体AlO 6 生成されたEu 2+ を取り囲み、絶縁するグループフレームワーク 酸素からのイオン[21、22]。アルミノケイ酸塩の一種であるゼオライトは、天然鉱物であるだけでなく、工業的に低コストで合成することもできます[23、24、25、26、27、28]。特に、それらの構造は前述の要件を満たすことができ、Eu 3+ を削減します。 Eu 2+ へのイオン イオンとEu 2+ の作成 イオンは安定しています。また、化学的安定性が高いため[29、30]など、発光材料用途の優れたホスト材料としても広く使用されています。さまざまなゼオライトの中で、ゼオライト-3A(\(\ frac {2} {3} \)K 2 O・\(\ frac {1} {3} \)Na 2 O・Al 2 O 3 ・2SiO 2 ・\(\ frac {9} {2} \)H 2 O、Si / Al比≈1)は、ダウンコンバージョンリンのホスト材料として使用されています。ここでは、Eu 2+ を達成します 還元性雰囲気のない高熱処理法による活性化ゼオライト-3Aリン光剤。得られたEu 2+ 活性化ゼオライト-3Aリン光物質の量子収率は約36.6%です。この準備方法は、安全で環境に優しく、環境にやさしい方法です。得られたサンプルの広い励起バンドは310〜450 nmの範囲にあり、発光バンドのピークは523nmにあります。また、サンプルは安定しており、簡単に再準備できます。緑色発光ゼオライト-3A:1.3 wt%Euリン光物質をUV発光チップにカプセル化することにより、国際照明委員会(CIE)の色座標が(0.295、0.537)、輝度が231.6の優れた緑色LEDを取得します。 cd / m 2 3Vの電圧の下で。これらの結果は、シンプルで環境に優しい準備アプローチを示しているだけでなく、照明やディスプレイの分野で有望なアプリケーションを備えた優れた緑色発光リン光物質を提供します。
メソッド
調査の目的
Eu 2+ の準備を目指しています -安全で環境にやさしい合成方法により、還元性雰囲気なしで明るい緑色の発光を示す活性化リン光物質。
資料
ゼオライト-3A(\(\ frac {2} {3} \)K 2 O・\(\ frac {1} {3} \)Na 2 O・Al 2 O 3 ・2SiO 2 ・\(\ frac {9} {2} \)H 2 O、Si / Al比≈1)Shanghai Tongxing Molecular Sieve Co.、LTDから購入し、酸化ユーロピウム(Eu 2 O 3 )Sinopharm Co.、Ltdから入手したものを、さらに精製することなく使用した。シリコーン樹脂とInGaNブルーチップ(5mm×5mm、λ =375 nm)はShenzhen Looking Long Technology Co.、Ltd。から受け取りました。
サンプルの合成
Eu 2+ -活性ゼオライト-3Aサンプルは、典型的な高温固相反応法を使用して調製しました。まず、異なる化学量論量のゼオライト-3AとEu 2 O 3 よく混合し、瑪瑙乳鉢で40分間完全に粉砕しました。そして、雰囲気を下げることなく、異なる温度で焼結しました。最後に、冷却後にターゲットサンプルが取得されました。
緑色LEDの製造
Eu 2+ 活性ゼオライト-3A粉末とシリコーン樹脂を質量比1:5で混合し、均一に攪拌した。組成物をInGaNチップ上にコーティングし、60°Cで約2時間硬化させました。最後に、複合材料の厚さは約1mmと測定されました。
特性評価
得られた生成物の形態と構造は、電界放出型走査電子顕微鏡(FESEM、FEI Sirion-200)およびCuKα放射線(λを使用したX線回折(XRD、Philips X’Pert)によって特徴づけられました。 =0.15405 nm)。熱重量分析(TG)曲線は、SDT Q600 V20.9 Build 20によって測定されました。これは、窒素雰囲気(流量10 ml / min)で室温から800°Cまで10°C /分の加熱速度で得られたものです。 。フォトルミネッセンス励起(PLE)およびフォトルミネッセンス(PL)スペクトルは、450 WXeランプを備えたEdinburghInstrumentsFLS920時間分解および定常状態蛍光分光計を使用して室温で取得しました。ユーロピウム元素の酸化状態は、X線光電子分光法(XPS、ESCALAB 250)によって調査されました。エレクトロルミネッセンス(EL)スペクトルは、ファイバー積分球(FOIS-1)とKeithley2400電位計を備えたOceanOpticsFLAME-S-VIS-NIR分光計によって調査されました。
結果と考察
図1aは、元のゼオライト-3AのSEM画像を示しています。自然のままのゼオライト-3Aの形態は、一辺の長さが約1.5μmの不規則な立方構造であることが観察できます。ゼオライト-3A:1.3 wt%のEuリン光物質は、還元性雰囲気なしで、高温固相反応法によって得られます。ゼオライト-3Aの形態と構造:1400°Cで3時間得られた1.3 wt%のEuリン光物質は、それぞれ図1b、cに示すように、電界放出型走査電子顕微鏡とX線回折測定によって特徴付けられます。図1bは、粒子が不規則な形態構造を示し、結晶子サイズの分布が均一ではないことを示しています。図1bとaを比較すると、ゼオライトの粒子は、1400°Cで3時間焼結した後に互いに凝集していることがわかります。図1cに見られるように、ゼオライト-3AのXRDパターンのすべての回折ピーク:1.3 wt%Euリン光物質は、純粋なゼオライト-3A相(JCPDS番号00-019-1227)とよく一致しており、他の不純物ピークが観察されます。これは、Eu 2+ を意味します イオンはゼオライトホスト格子と一定量のEu 2+ にうまく導入されます イオンドーピングは明らかに結晶構造を変化させません[10]。図1dは、純粋なゼオライト-3Aとゼオライト-3AのTG曲線を示しています。1400°Cで焼結された1.3 wt%のEuリン光物質です。純粋なゼオライト-3AのTG曲線では、約266°Cまでの加熱中に連続的な質量損失があり、約19.45%の値に達することがわかります。これは、ゼオライト-3Aの空洞とチャネルに局在する物理的に結合した水の放出に対応します[31]。温度が連続的に上昇するため、質量損失の現象は明らかではありません。ゼオライト-3AのTG曲線からわかるように:1400°Cで焼結された1.3 wt%のEuリン光物質は、質量損失がほとんどありません。これらの結果は、ゼオライト-3A:1400°Cで焼結された1.3 wt%Euが非常に安定していることを示しています。
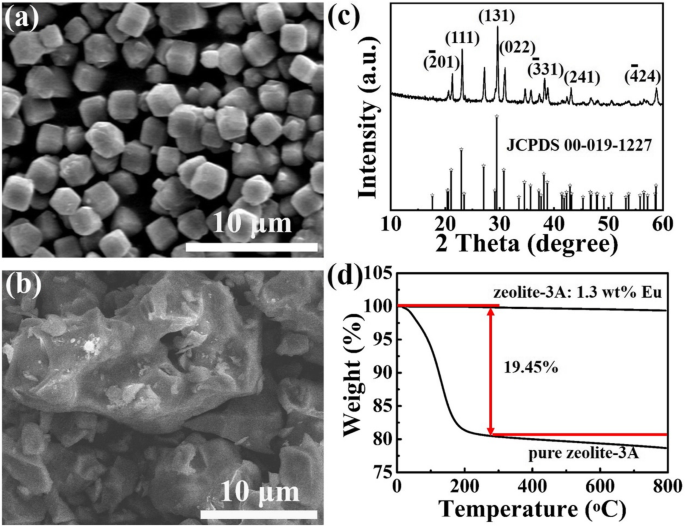
a のSEM画像 純粋なゼオライト-3Aおよび b ゼオライト-3A:1.3 wt%のEuリン光物質を1400°Cで3時間焼結。 c ゼオライト-3AのXRDパターン:1.3 wt%Euリン光物質を1400°Cで3時間焼結。 d 純粋なゼオライト-3Aおよびゼオライト-3AのTG曲線:1400°Cで3時間焼結した1.3 wt%Euリン光物質
図2は、ゼオライト-3AのSEM画像とXRDパターンを示しています。さまざまな温度で焼結された1.3 wt%のEuリン光物質です。 SEM画像(図2a〜d)から、焼結温度の上昇に伴って形態が大幅に変化することがわかります。焼結温度が比較的低い場合(600°Cおよび800°C)でも、サンプルの形態は元のゼオライト-3Aとして維持されます。つまり、平均サイズが1.5μmの立方体の形状になります(図1aを参照)。 。しかし、焼結温度が1000°Cと1200°Cに達すると、粒子が凝集し始めることが観察できます。焼結温度が上昇すると、粒子は凝集し続け、塊状の構造を形成する可能性があります(図1b)。一方、それらのXRDパターンを図2eに示します。 600°Cおよび800°Cで調製されたサンプルの回折ピークは、純粋なゼオライト-3A標準カード(JCPDS番号00-019-1227)に完全にインデックス付けされていないことに注意してください。 2つのサンプルには、12.5°と16.3°に位置する余分な回折ピークがあり、Eu 2 のピークに割り当てられています。 O 3 (JCPDS番号00-012-0384)。これは、煆焼温度が800°C未満の場合、Euイオンをゼオライトホスト格子にうまく組み込むことができないことを意味します[32]。それにもかかわらず、1000°C以上で焼結されたサンプルは、純粋なゼオライト-3A標準カードの主要な特徴的なピークに対応するピークを示しています。
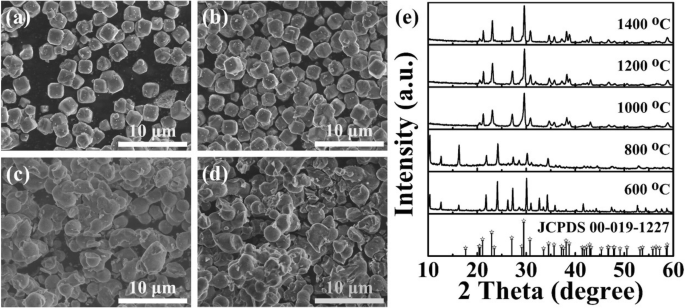
ゼオライト-3AのSEM画像:600°Cで焼結した1.3 wt%のEuリン光物質( a )、800°C( b )、1000°C( c )、および1200°C( d )、 それぞれ。 e ゼオライト-3AのXRDパターン:それぞれ異なる温度で焼結した1.3 wt%Euリン光物質
PL発光に対する焼成温度の影響を調査するために、さまざまな焼成温度でのサンプルのPL発光スペクトルをテストし、図3aに示します。挿入図に見られるように、600°Cと800°Cで焼結されたサンプルは、 5 に起因する617nmを中心とする赤色の発光ピークのみを示しています。 D 0 → 7 F 2 Eu 3+ の電気双極子遷移 イオン[33]。焼結温度が上昇するにつれて、赤色の発光ピークは徐々に弱くなり、緑色の発光ピーク(523 nmを中心とする)が明らかに観察されます。特に、1400°Cで調製されたサンプルは、主に典型的な特徴的なEu 2+ を示します。 4f 6 による523nmを中心とした発光 5d→4f 7 遷移[34]。図3aのさまざまなPL曲線を比較すると、Eu 3+ の量がわかります。 →Eu 2+ 焼結温度の上昇とともに連続的に増加します。この結果は、図2eのXRDパターンの結果と一致しています。つまり、Eu 3+ 煆焼温度が1000℃以下の場合、イオンが主な形態です。 Eu 3+ イオンは徐々にEu 2+ に還元されます 焼結温度が1000°Cより高い場合のイオン。図3bは、1400°Cで焼結したサンプルのPLEおよびPLスペクトルを示しています。 PLEスペクトルは、約310〜450 nmの広い励起帯域を示していることがわかります[7、35]。挿入図は、365nmのUVランプを照射した明るい緑色の発光を示す写真です。図3bのPLスペクトルは、写真で見られる色と一致しています。
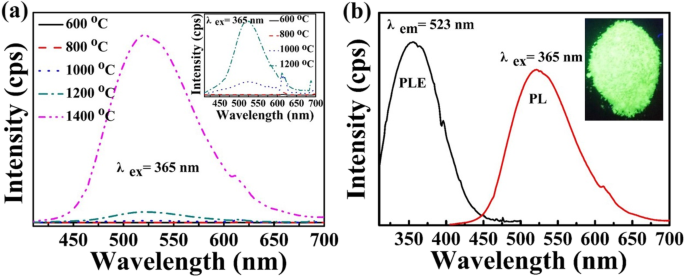
a ゼオライト-3AのPL発光スペクトル:それぞれ異なる温度で焼結した1.3 wt%Euリン光物質。挿入図は倍率スペクトルを示しています。 b ゼオライト-3Aのフォトルミネッセンス励起(PLE)およびフォトルミネッセンス(PL)発光スペクトル:1400°Cで3時間焼結した1.3 wt%Euリン光物質。挿入図は、365 nmUVランプの照明を備えたサンプルの写真です
Eu元素の酸化状態をさらに調査するために、1400°Cで得られたサンプルのEu3dのXPSパターンを監視し、図4に示します。1165eVと1135eVにあるピークはEu に対応しています。 3+ 酸化状態ですが、1155eVおよび1125eV付近のピークはEu 2+ に起因します。 酸化状態[11、36]。この結果は、Eu 3+ の一部が イオンはEu 2+ に還元されます 高熱処理反応下のゼオライトホスト中のイオン。この結果はPLスペクトルと一致しています(図3)。考えられる反応メカニズムは、次の式で示されます。
$$ {\ mathrm {Eu}} _ 2 {\ mathrm {O}} _ 3 \ overset {{\ mathrm {K}} _ 2 \ mathrm {O}} {\ to} \ kern0.5em 2 {\ left [{\ mathrm {Eu}} ^ {3+} \ right]} _ {\ mathrm {K}} ^ {\ ast \ ast} + \ kern0.5em 4 {V} _ {\ mathrm {K}} ^ {\ prime } +3 {\ mathrm {O}} _ {\ mathrm {O}} ^ {\ times} $$(1)$$ {V} _ {\ mathrm {K}} ^ {\ prime} \ to {V } _ {\ mathrm {K}} ^ {\ times} \ kern0.5em + {\ mathrm {e}} ^ {\ prime} $$(2)$$ {\ left [{\ mathrm {Eu}} ^ {3+} \ right]} _ {\ mathrm {K}} ^ {\ ast \ ast} \ kern0.5em + {\ mathrm {e}} ^ {\ prime} \ to {\ left [{\ mathrm { Eu}} ^ {2 +} \ right]} _ {\ mathrm {K}} ^ {\ ast} $$(3)$$ {\ left [{\ mathrm {Eu}} ^ {2+} \ right ]} _ {\ mathrm {K}} ^ {\ ast} + {\ mathrm {e}} ^ {\ prime} \ to {\ left [{\ mathrm {Eu}} ^ {2+} \ right]} _ {\ mathrm {K}} ^ {\ times} $$(4)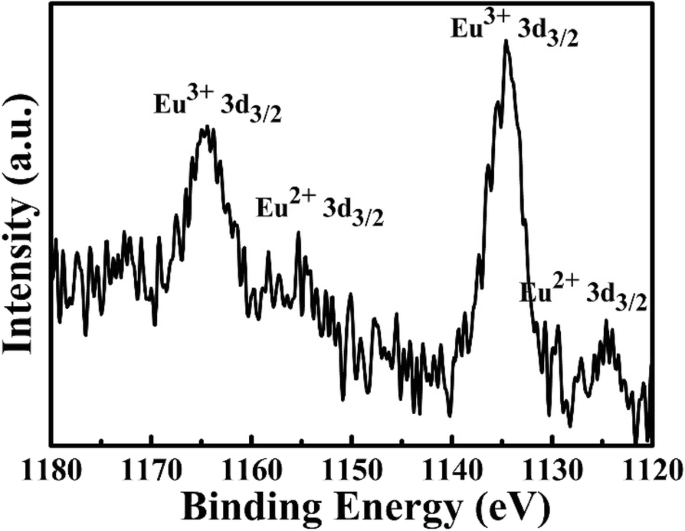
ゼオライト-3AのEu元素のXPSスペクトル:1400°Cで3時間焼結した1.3 wt%Euリン光物質
ここでは、[Eu 3+ ] K および[Eu 2+ ] K Eu 3+ を表す およびEu 2+ K + のイオン置換 それぞれイオンの位置。 O o マトリックス結晶中の酸素に対する酸素の位置を表します。およびV K K + の空室です イオン。上付き文字「*」、「**」、「 '」、および「×」は、それぞれ1つの正電荷、2つの正電荷、1つの負電荷、および電気的中性を示します。焼結中、Eu 3+ イオンがK + に置き換わる ゼオライト中の位置。充電バランスを保つために、1つのEu 3+ イオンは3つのK + の代わりになります イオン。したがって、K + の2つの空孔欠陥 イオン( V K ' )およびEu 3+ の1つの欠陥 イオン([Eu 3+ ] K ** )は、外観上それぞれ1つの負電荷と2つの正電荷を帯びており、ゼオライトホストに生成されます(式(1)からわかる)。次に、欠員 V K ' 電子の供与体(式(2)からわかる)として機能し、[Eu 3+ ] K ** 欠陥は電子の受容体です。高温では、[Eu 3+ ] K ** K + の空孔から1つの電子を捕獲します イオン( V K ' )そしてこの電子はEuイオンの4f軌道に充填されます。したがって、Eu 3+ イオンはEu 2+ に還元されます および[Eu 3+ ] K ** 欠陥は[Eu 2+ になります ] K * 欠陥(式(3)から見られる)。このとき、Eu 2+ の位置 イオンは明らかに1つの正電荷を持っています。 [Eu 2+ ] K * 欠陥は別のK + の負の電子を引き付けます 周囲に空孔があり、明らかに電気的中性になります[Eu 2+ ] K × (式(4)に示されています)[11、21、22、37、38、39、40、41]。
AlO 4 の剛直な3次元正方晶フレームワークが提案されています およびSiO 4 Eu 2+ を囲むことができます イオンとそれらを酸素から絶縁し、次にEu 2+ 私たちの狙いのリン光物質に着実に存在することができます。
ゼオライト-3Aの特性を最適化するには:1.3 wt%Euリン光物質、PLに対するEu元素の影響、さまざまな化学量論量のゼオライト-3AとEu 2 のPL発光スペクトルと相対PL強度を観察します。 O 3 図5に示します。図5aから、Eu 2+ の発光強度がわかります。 Eu 2 のドーピング濃度とともに増加します O 3 0.9から1.3%に増加します。ただし、ドーパント濃度が連続的に増加すると減少します。 Euドーピング濃度が約1.3%のときにPL効果が最も優れていることがはっきりと観察できます。より多くのEu 2+ イオン、より多くの発光中心。 Eu元素の濃度が1.3%を超えると、PL強度の低下は、主にEu 2+ 間のエネルギー移動によって引き起こされる濃度消光に起因する可能性があります。 イオン。 Eu 2+ の濃度が イオンが増加すると、Eu 2+ 間の距離が増加します イオンが短くなり、エネルギー移動が増加します[42、43、44]。相対PL強度とEuドーピング濃度のエラーバー曲線を図5bに示します。これは、各Eu濃度の相対PL強度の変化範囲が小さいことを示しています。これは、これらのサンプルが非常に再現性があることを意味します。
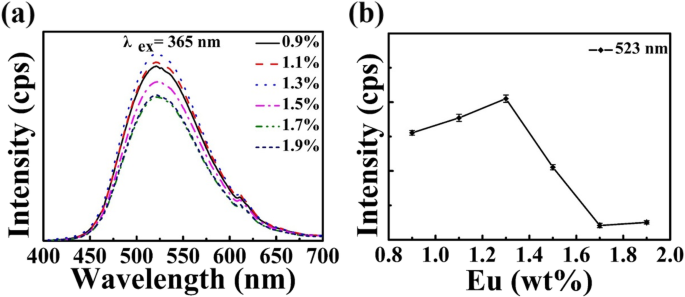
a PL発光スペクトルと b 相対PL強度は、ゼオライト-3AのEu元素の濃度によって異なります:1.3 wt%Euリン光物質( x =0.9〜1.9)1400°Cで3時間焼結
照明用途の証拠として、緑色発光ゼオライト-3A:1.3 wt%Euリン光物質をUV発光チップにカプセル化して緑色LEDを製造します。 3V電圧でのEL発光スペクトルを図6aに示します。 UV発光チップと緑色発光リン光物質の発光ピークは、それぞれ〜375 nmと〜523nmにあることがわかります。挿入図は、3Vの電圧で明るい緑色の光を発する緑色のLEDの動作写真です。結果として得られる緑色LEDの色座標(図6b)は(0.295、0.537)と計算され、優れた緑色の色純度を示します。
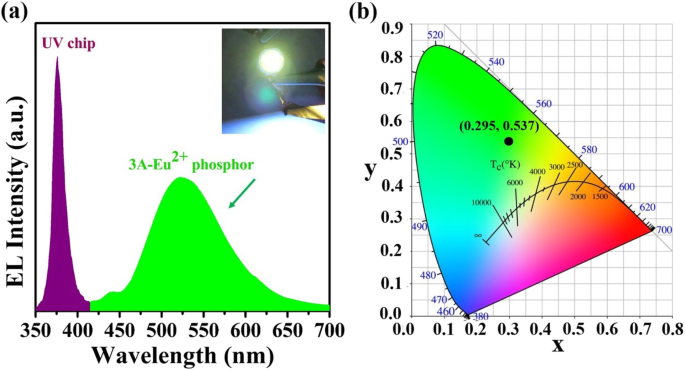
a ゼオライト-3Aの3V電圧でのエレクトロルミネッセンス発光スペクトル:1.3 wt%Euリン光物質を1400°Cで3時間焼結し、挿入図は3V電圧で動作する緑色LEDの写真です。 b CIE1931図の色座標
結論
この作業では、明るい緑色の発光ゼオライト-3A:Eu 2+ を取得しました。 還元性雰囲気のない環境にやさしい高熱反応法により、量子収率が約36.6%、発光ピークが523nmにあるリン光物質。さらに、サンプルには310〜450 nmの範囲の広い励起バンドがあり、これは市販のUVチップ励起(実際にはλ)に対応できます。 =375 nm)。 Eu 2+ 煆焼温度が上昇するにつれて、イオンはゼオライトホスト格子に徐々に組み込まれる可能性があります。私たちの研究によると、最適な焼結温度は1400°Cであり、Euイオンの最適なドーピング濃度は1.3%です。緑色発光ゼオライト-3Aを利用する:Eu 2+ UV発光チップにカプセル化されたリン光物質、国際照明委員会(CIE)の色座標が(0.295、0.537)、明るさが231.6 cd / m 2 の優れた緑色LED が得られます。また、緑色発光ゼオライト-3A:発光特性が向上した1.3 wt%のEuリン光物質は、照明やディスプレイの有望なアプリケーションになります。
データと資料の可用性
この記事の結論を裏付けるデータセットは、記事で入手できます。
略語
- CIE:
-
国際照明委員会
- EL:
-
エレクトロルミネッセンス
- Eu:
-
ユーロピウム
- FESEM:
-
電界放出型走査電子顕微鏡
- LED:
-
発光ダイオード
- PL:
-
フォトルミネッセンス
- PLE:
-
フォトルミネッセンス励起
- RE:
-
希土類
- TG:
-
熱重量分析
- XPS:
-
X線光電子分光法
- XRD:
-
X線回折
ナノマテリアル
- モバイルメンテナンスソフトウェアと効率的なワークフローの構築におけるその役割
- ミルスケール廃棄物からのマグネタイトナノ吸着剤を使用した水溶液からの銅(II)イオンの吸着除去:合成、特性評価、吸着および速度論的モデリング研究
- アルミノシリケートミネラルおよび優れた水分解性能のための代替ドーピング
- Agで装飾されたSnO2ミクロスフェアのワンポットグリーン合成:4-ニトロフェノールの還元のための効率的で再利用可能な触媒
- 重金属を含まない発光ダイオードに適用するためのInP / ZnSコア/シェル量子ドットのグリーン合成
- パラジウム(II)イオンインプリント高分子ナノスフェアの調製と水溶液からのパラジウム(II)の除去
- 金および銀ナノ粒子のグリーン合成のためのPlatycodiRadix(Platycodon grandiflorum)からのPlatycodonサポニン
- 高いMgドーピング効率のために特別に設計された超格子p型電子ブロッキング層を備えたほぼ効率の低いAlGaNベースの紫外線発光ダイオード
- CA / TPUヘリカルナノファイバーの製造とそのメカニズム分析
- PEG-PCCLナノ粒子の毒性評価とパクリタキセル負荷の抗腫瘍効果に関する予備調査
- 強化された光触媒評価と抗菌分析のためのZnOナノ粒子に対するMgドーピングの影響



