酸素レドックス反応に根ざした新しいカソード材料のためにLi2RuO3によって活性化されたリチウムベースのナノコンポジット
要約
リチウムベースの材料は、その大容量と安定したサイクル性能により、リチウムイオン電池のアニオン(酸素)レドックス反応に基づく有望なカソードです。この研究では、Li 2 によって活性化されたリチアベースのカソードの特性 RuO 3 特徴づけられました。 Ruベースの酸化物は、陰イオンの酸化還元反応を安定化させる役割を果たすことができるため、優れた触媒として機能することが期待されます。それらの高い電子伝導性はまた、リチアの低い伝導性を補うことができるので魅力的です。 lithia / Li 2 RuO 3 ナノコンポジットは、500 mAh g -1 の容量制限まで安定したサイクル性能を示します に達しましたが、これは理論上の容量(897 mAh g -1 )を下回っています。 )しかし、他のリチアベースのカソードよりも優れています。 XPS分析では、スペクトルのRu 3dピークはほとんど変化しませんでしたが、ペルオキソ様(O 2 ) n- 種は、サイクリング中に可逆的に形成および解離しました。これにより、lithia / Li 2 の容量が明確に確認されます。 RuO 3 ナノコンポジットは、主にアニオン性(酸素)レドックス反応に起因する可能性があります。
はじめに
私たちの社会は、携帯電話、ラップトップ、電気自動車の使用が増えるにつれて、エネルギー貯蔵システム(ESS)への依存度がますます高まっています。さらに、環境にやさしい発電システムから生成された電力は、大規模なエネルギー貯蔵システム(ESS)に貯蔵する必要があります。これらのESSの例は、主に二次電池システムに基づいており、最先端の二次電池と見なされているリチウムイオン電池(LIB)の市場シェアを急速に拡大しています。ただし、現在のLIBのエネルギー密度は、多くのアプリケーションの要件を満たすのに十分ではありません[1,2,3,4,5,6,7]。したがって、多くの研究がバッテリーシステムのエネルギー密度の改善に焦点を合わせてきました。特に、従来の遷移金属ベースの酸化物よりも高い可逆容量を示す優れたカソード材料の開発は、大きな研究対象です[1,2,3,4,5,6,7]。
陰イオン(酸素)レドックス反応と互換性のあるいくつかの材料は、高エネルギー密度のカソードに有望である可能性があります[8、9、10、11、12、13、14、15、16]。現在使用されているカソード材料の可逆放電容量は、化合物中のカチオン性遷移金属イオンの酸化還元反応に基づいています。しかし、酸素に根ざしたアニオン性レドックス反応の導入は、遷移金属酸化物の容量限界を克服して、潜在的に高い可逆容量を駆動する可能性があります。たとえば、酸素レドックス反応(ORR)は、主に x などのLiに富む材料の高エネルギー密度の原因です。 Li 2 MnO 3 −(1 − x )Li(Ni、Mn)O 2 [17、18]。 Liに富む材料が陽イオン(遷移金属酸化物)レドックス反応領域に帯電すると、可逆ORR(2O 2- ➔O 2 x − )進行します。この反応は、遷移金属イオンのカチオン酸化還元反応と併せて、Liに富む材料の可逆的能力に貢献します。ただし、これらの反応では、ORRをアクティブにするために高い充電電圧(> 4.5 V)が必要であり、有機電解質の劣化を引き起こし、深刻な容量低下を引き起こします[19、20、21、22、23]。
リチア(Li 2 O)ベースの化合物は、ORRに基づくカソード材料として最近提案されています[24、25、26、27、28、29]。 Liに富む化合物の可逆的能力は主に遷移金属イオンの陽イオンレドックス反応に起因しますが、リチアベースの化合物のそれはほぼ純粋にO 2- <間の陰イオン(酸素)レドックス反応に依存します。 / sup> およびO x − (0.5≤ x <2)。この電池の化学的性質は、主にORRを使用するという点で、リチウム空気電池に匹敵します。ただし、リチウム空気電池の基本的な酸化還元反応は、ガス(O 2 )からの相転移に基づいています。 )から固体(Li 2 O 2 );この反応は、組成を変えない「相転移」だけでなく、Liイオンが関与する化学反応です。ただし、この研究分野では、相変化を伴うため、「相転移」プロセスと呼ばれます。ガスと固体の接触が不安定なため、容量の低下とLi-airセルの高い過電圧が発生し、反応速度が遅くなります[30、31、32、33、34、35、36]。対照的に、リチアベースの化合物の酸素イオンは、充電および放電プロセス中に相転移なしで固相を維持します。したがって、リチウムベースの化合物は、リチウム空気電極のサブクラスではなく、LIBの新しいカソード材料として分類できます。
実際、固体リチアの酸素イオンは、充電プロセス中にほとんど活性化されません。したがって、リチアの酸素イオンを活性化し、反応生成物(Li 2 )を安定化するには、触媒(ドーパントと呼ばれることもあります)が不可欠です。 O 2 またはLiO 2 )。 Co、Fe、およびCu酸化物は、リチアを活性化するための触媒として使用されてきました[24、25、26、27、28、29]。これにより、リチアベースの化合物の電気化学的性能は、存在する触媒の組成と量に非常に敏感です。より効率的な触媒であるLi 2 を探索する取り組みの一環として、 RuO 3 この研究では、リチアの活性化のための新しい触媒として紹介されています。 RuイオンはLiリッチ酸化物の陰イオンレドックス反応を安定化する役割を果たし[37,38,39]、RuベースのLiリッチ酸化物はより可逆的な酸素レドックスプロセスを示し、酸素放出に対して構造的に安定していることに注目しました。 Co、Ni、およびMnベースのLiリッチ酸化物と比較して。これは、Ruイオンが、以前に使用された他の遷移金属イオン(Co、Fe、Cuなど)よりも安定してORRを活性化するためのより優れた触媒になる可能性があることを意味します。さらに、Ru酸化物の高い電子伝導率は、リチアの不十分な伝導率を補う可能性があります。この作業では、lithia / Li 2 を準備しました RuO 3 ナノコンポジットを作成し、X線回折法(XRD)、X線光電子分光法(XPS)、および電気化学測定を使用してそれらの特性を調査し、触媒としての酸化Ruの効果を確認しました。スキーム1は、lithia / Li 2 の構造を示しています。 RuO 3 この研究におけるナノコンポジットと本質的な概念。
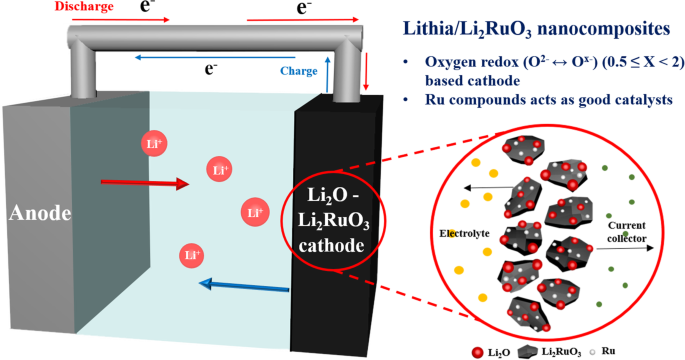
lithia / Li 2 の構造を示す概略図 RuO 3 この研究におけるナノコンポジットと本質的な概念。
メソッド
Li 2 RuO 3 ナノリチアを活性化するための触媒として採用された。 Li 2 を形成するには RuO 3 、RuO 2 (Alfa Aesar、99.9%)およびLi 2 CO 3 (Aldrich、99.99%)を1:1(mol%)の比率でペレット化し、950°Cで24時間空気中で煆焼しました。次に、煆焼されたペレットを粉砕して粉末にした。 Li 2 RuO 3 およびナノリチア(Li 2 O)粉末(Alfa Aesar、99.5%)を組み合わせて、Ru含有量( f Ru =Ru /(Ru + Li))0.09、次にブタノール(Aldrich、無水、99.8%)に分散。混合物を30分間超音波処理し、次に濾過した。得られたLi 2 RuO 3 / Li 2 O粉末を90℃で24時間真空乾燥し、次にプラネタリーモノミル(PULVERISETTE 6、FRITSCH)を使用してボールミル粉砕し、リチア/ Li 2 を得た。 RuO 3 ナノコンポジット。粉砕は600rpmで150時間(1時間の粉砕後30分間休止)行った。直径5mmと10mmのジルコニアボールを1:1(wt%)の比率で使用しました。粉砕プロセスは、グローブボックスと密封されたジルコニア容器を使用して、Ar雰囲気下で実行されました。合成されたリチア/ Li 2 のXRDパターン RuO 3 ナノコンポジット粉末は、単色化されたCu K αを使用して、10〜90°の2θ範囲でRigaku Miniflex IIX線回折計を使用して得られました。 放射線(λ =1.5406Å)。 Li 2 の分散度を観察する RuO 3 lithia / Li 2 のlithia RuO 3 ナノコンポジット、高分解能透過型電子顕微鏡(HR-TEM; JEM-2100F)およびエネルギー分散型X線分光法(EDS)が採用されました。
電気化学的試験では、活物質(lithia / Li 2 )を混合して正極を作成しました。 RuO 3 ナノコンポジット)、カーボンナノチューブ、およびポリフッ化ビニリデン(PVDF)バインダーを60:30:10(wt%)の比率で。参考までに、Li 2 RuO 3 電極も80:12:8(Li 2 のwt%)の比率で調製しました。 RuO 3 /カーボンナノチューブ/ PVDF)。電極部品のボールミル粉砕を90分間行った。その後、lithia / Li 2 RuO 3 ナノコンポジットとLi 2 RuO 3 スラリーをアルミホイルにキャストし、80°Cで24時間真空乾燥しました。
コイン電池(2032タイプ)を使用して、アノードとしてLi金属、1 M LiPF 6 を使用した電気化学的試験を行いました。 電解質として5vol%の炭酸ビニレンを含み、セパレーターとしてポリプロピレン(Celgard 2400)を含むエチレンカーボネートとジメチルカーボネート(1:1 v / v)中。セルはArで満たされたグローブボックスに組み立てられました。 lithia / Li 2 RuO 3 ナノコンポジットセルは、さまざまな電流密度(10、30、100、および200 mA g -1 )で1.8〜4.35Vの電位範囲を循環しました。 )。リチアの質量に基づいて計算されたカソードの容量は、300〜600 mAh g -1 に制限されていました。 。 Li 2 RuO 3 セルはまた、電流密度30 mA g -1 で2.0〜4.6Vの電位範囲で循環されました。 。
結果と考察
lithia / Li 2 の構造特性 RuO 3 ナノコンポジットは、XRDとTEMを使用して調査されました。図1は、lithia / Li 2 のXRDパターンを示しています。 RuO 3 ナノコンポジット、Li 2 RuO 3 、Li 2 O(lithia)、およびRu。 lithia / Li 2 の回折パターン RuO 3 ナノコンポジットは、原材料(Li 2 )のナノコンポジットと一緒に存在していました。 RuO 3 およびlithia)および新しく形成されたRuピーク。シャープで大きなRuピークは、Li 2 の一部を示しています。 RuO 3 粉砕プロセス中にRuに分解されます。ただし、Li 2 の広いが大きな回折ピーク RuO 3 かなりの量のLi 2 RuO 3 結晶性Li 2 のほとんどは残っていますが、まだ残っています RuO 3 粉砕過程でアモルファス相に変化したようです。リチアピークの減少は、結晶性リチアもアモルファス相に変化していることを示しています。アモルファス相の存在は、導電率の低下などの悪影響をもたらす可能性があります。ただし、これにより、過電圧が低下する可能性もあります。これは、アモルファスリチアの相転移が、放電プロセス中に必要なエネルギーが結晶リチアの相転移よりも少ないためです[29]。
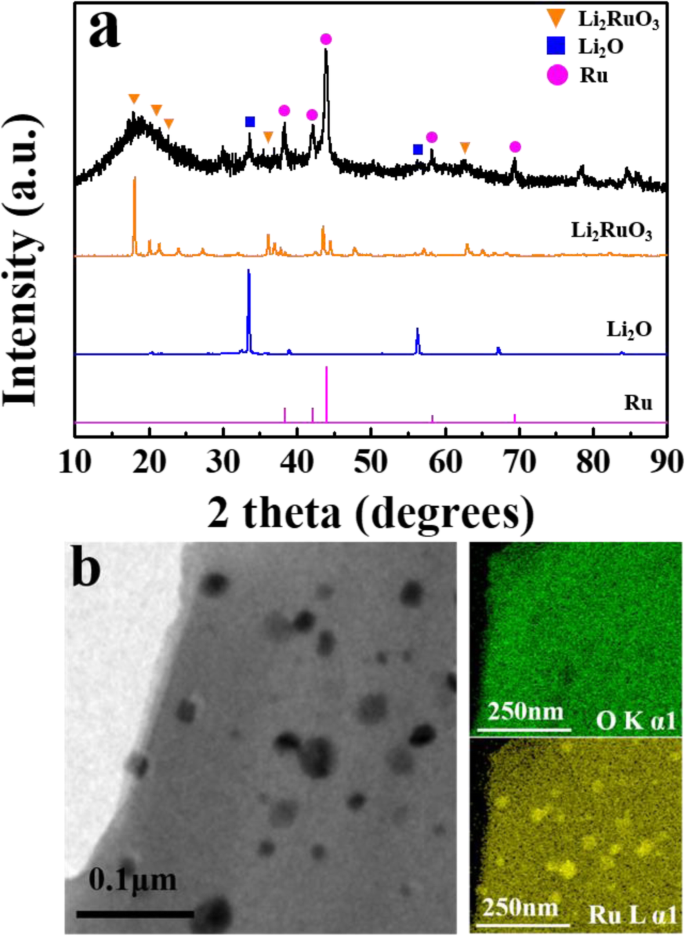
a lithia / Li 2 のXRDパターン RuO 3 Li 2 と比較したナノコンポジット RuO 3 、Li 2 O、Ru。 b lithia / Li 2 のTEM画像とEDS元素マッピング RuO 3 ナノコンポジットパウダー
XRD分析に基づくと、アモルファスLi 2 だけでなく RuO 3 しかし、Ruはリチアを活性化するための触媒としても機能します。触媒の分布とナノコンポジットの形態は、HR-TEMとEDSの元素マッピングによって観察されました。図1bに示すように、ナノコンポジットのHR-TEM画像には、このセクションで大量のRuを示すEDSマッピングによってサポートされているように、Ru粒子である可能性が高いいくつかのダークスポットが含まれています。 Li 2 の分解によってRuが形成されると RuO 3 、金属Ruの延性のため、粉砕プロセスで細かく分散させるのは難しいようです。したがって、Ru粒子の一部は凝集しているように見えます。残りのナノコンポジット材料は、EDSマッピングで示されているように、均一に分布したリチアと触媒で構成されているように見えます。
lithia / Li 2 を含むセルの電気化学的特性 RuO 3 Li 2 の効果を調査するために、ナノコンポジットを調べました。 RuO 3 触媒。図2は、lithia / Li 2 の電圧曲線とサイクル性能を示しています。 RuO 3 電流密度が10mAg -1 の場合のナノコンポジット 。リチアが過充電されると、酸素の酸化状態が-2(Li 2 )から変化する可能性があるため、酸素発生が発生する可能性があります。 O形式)から0(O 2 ガス)[25,26,27]。過充電が発生しない限界容量を確認するために、充放電容量を300、400、500、600 mAh g -1 に制限しました。 、リチアの質量に基づいて計算されます。図2a–dに示すように、lithia / Li 2 の電圧曲線 RuO 3 ナノコンポジットは、2サイクルの間、すべての限られた容量で安定しているように見えます。容量が300mAhに制限された場合g -1 、狭い電圧範囲(3.5〜2.7 V)が発生します。ただし、制限容量が大きくなると、電圧範囲も大きくなります。容量が600mAhに制限された場合g -1 、電圧は充電時に約4.0 Vに上昇し、放電時に約2.0Vに低下しました。図2e–hは、lithia / Li 2 の周期的性能を示しています。 RuO 3 同じ条件下でのナノコンポジット。ナノコンポジットは、300〜500 mAh g -1 の限られた容量で循環させた場合に安定しています。 。ただし、容量を600 mAh g -1 に上げると 、容量は13サイクル後に徐々に減少し始めました。これは、lithia / Li 2 の容量範囲が安定していることを示しています。 RuO 3 ナノコンポジットは600mAh g -1 未満です;過充電は容量の不安定性の原因となる可能性があります。リチアの場合(Li 2 O)は帯電しており、凝縮状態(固体)のままであり、リチアの酸素はO 2- から変化します。 O x へ − (0.5≤ x <2)。しかし、リチアが固体を維持するための限界を超えて帯電した場合、酸素の酸化状態はゼロに近づき、酸素ガスを生成することができます。このプロセスにより、サイクリング中に容量が低下します。ただし、リチアからの酸化還元反応を想定すると(Li 2 O、O 2- )過酸化物(Li 2 O 2、 O 1- )、リチアの理論容量は897mAh g -1 [26、27]。レドックス反応によりO 0.5- が生成される場合 (LiO 2 )、リチアの理論容量は1341 mAh g -1 に増加します [29]。したがって、観測された容量が600 mAh g -1 未満の場合 、lithia / Li 2 におけるlithiaの容量制限 RuO 3 ナノコンポジットに到達していません。
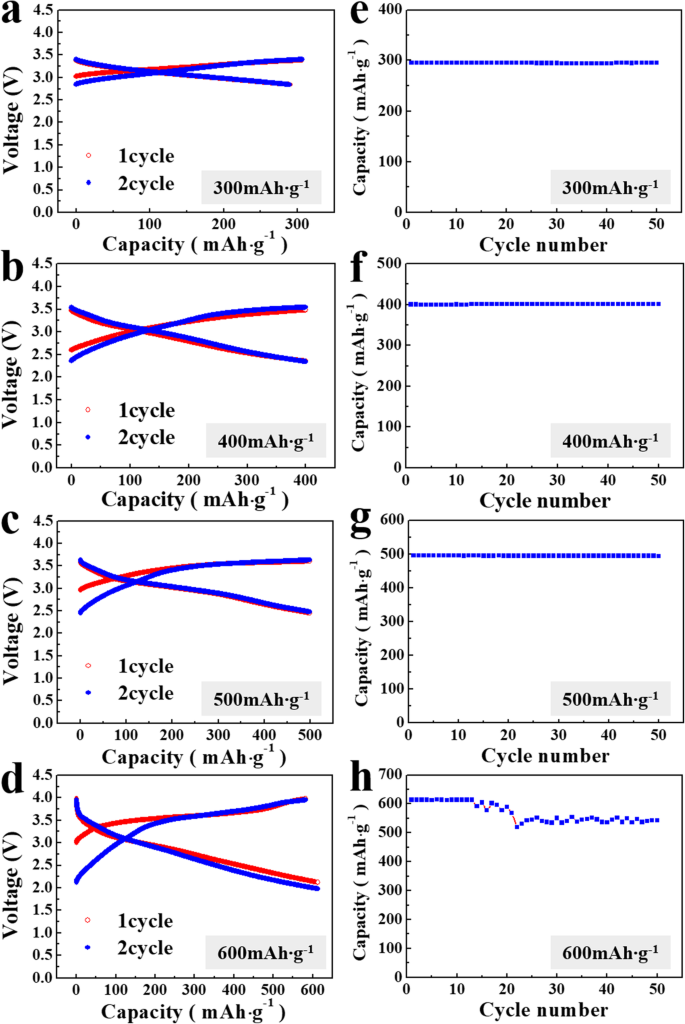
lithia / Li 2 の電圧曲線 RuO 3 容量が a に制限されている場合のナノコンポジット 300、 b 400、 c 500、および d 600 mAh g -1 ;容量制限時のサイクリングは e に対応します 、 f 、 g 、および h 、それぞれ
触媒はリチアを活性化し、不安定な反応生成物(Li 2 など)を安定化させるため、リチアの能力は触媒と密接に関連しています。 O 2 およびLiO 2 )。 lithia / Li 2 の利用可能な容量が少ない RuO 3 リチアの理論的容量と比較したナノコンポジットは、ナノコンポジットの触媒がリチアを十分に活性化して全容量を抽出できないことを意味する場合があります。反応生成物の安定化は、リチアベースのカソードの容量安定性にも大きく影響します。反応生成物(例:Li 2 O 2 およびLiO 2 )リチアの酸化還元反応から形成される反応性が高い。したがって、電解質などの他の物質と反応し、他の物質に変化する可能性があります。これらの副反応を抑制し、反応生成物を安定化することも触媒の機能です。図2hに示すように、特定のサイクル数後の容量の低下は、サイクリング中の反応生成物の不安定性、つまり600 mAh g -1 と関連している可能性があります。 lithia / Li 2 のRuベースの触媒の限界を超えている可能性があります RuO 3 ナノコンポジットは反応生成物を安定させることができます。
lithia / Li 2 の容量ですが RuO 3 ナノコンポジットは、理論上の容量、つまり安定した容量(> 500 mAh g -1 )に達していません。 リチアの質量に基づく)は、ミリングプロセス(<400 mAh g -1 )によって調製された以前に報告されたリチアベースのカソードと比較して優れています。 )[25、26、27、28]。これは、Li 2 RuO 3 そしてその分解相(Ruなど)は、サイクリング中にリチアを効果的に活性化し、反応生成物を安定化します。触媒がリチアでより完全に分散している場合、それらはより良い触媒活性を示す可能性があります。機械的粉砕には限界があるため、(機械的粉砕ではなく)化学的調製などの他の方法を検討する必要があります。
lithia / Li 2 の容量とサイクル性能 RuO 3 ナノコンポジットは、さまざまな電流密度を使用してより詳細に分析されました。図3aは、電流密度10、30、100、および200 mAg -1 でのナノコンポジットの初期電圧プロファイルを比較しています。 500 mAh g -1 の制限された容量 。電流密度が増加しても、電圧プロファイルの形状は大きく変化しません。ナノコンポジットを含むセルの過電圧は、両方のシステムが同様にORRに根ざしているにもかかわらず、一般的なリチウム空気電池の過電圧よりもはるかに低くなっています。リチウム空気システムは、充電および放電中に気相と凝縮相の間でカソードの大きな構造変化を伴いますが、リチウムベースのカソードはレドックス反応を処理し、凝縮相(固体)を保持します。これにより、充電および放電中の電子およびイオンの移動と相変態に起因するエネルギー障壁が減少し、リチアベースのシステムの過電圧が比較的低くなります。
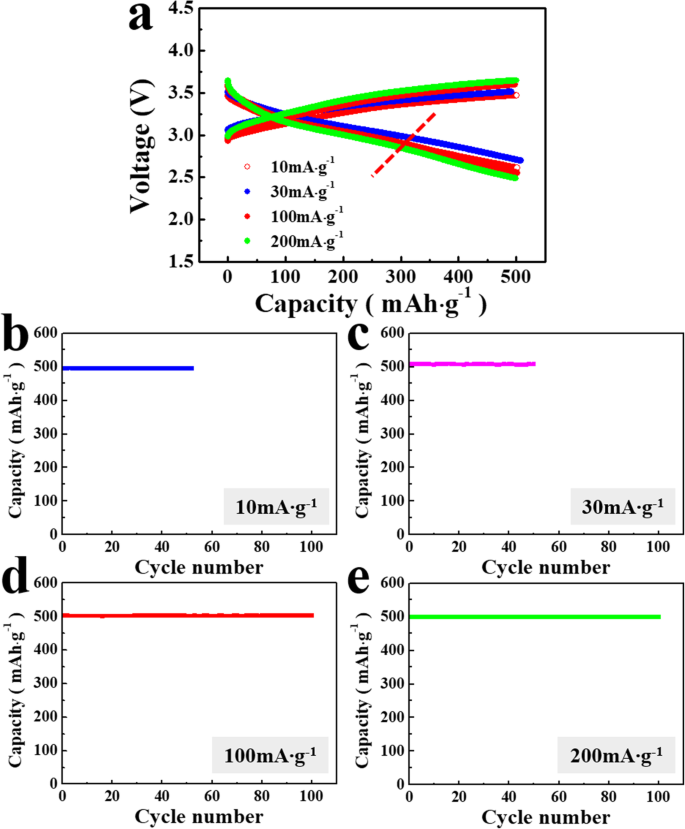
lithia / Li 2 の電圧プロファイルとサイクル性能 RuO 3 10、30、100、および200mAの電流密度でのナノコンポジットg -1 500 mAh g -1 の制限された容量 。 a 電圧プロファイル; b での周期的なパフォーマンス 10 mAg -1 、 c 30 mAg -1 、 d 100 mAg -1 、および e 200 mAg -1
lithia / Li 2 の周期的性能 RuO 3 ナノコンポジットは、500 mAh g -1 の限られた容量で安定しています。 (図3b–e)。サイクリング前および選択したサイクル(つまり、1、50、および100サイクル)後のナノコンポジットを含むセルのナイキスト線図を分析して、サイクリング中のインピーダンス値を決定しました。図4に示すように、ナイキスト線図の半円部分のサイズは、サイクリング前に測定されたものと比較して、1回目のサイクル後にわずかに増加します。これは、一般に電荷移動抵抗と固体電解質界面に起因するインピーダンス値が、初期サイクル中に大幅に変化しないことを示しています。 50サイクル後、セルのインピーダンスは増加しますが、100サイクル後のインピーダンスの増加はそれほど顕著ではなく、セルのインピーダンスは、いくらか増加しますが、サイクリング中は比較的安定していることを示しています。
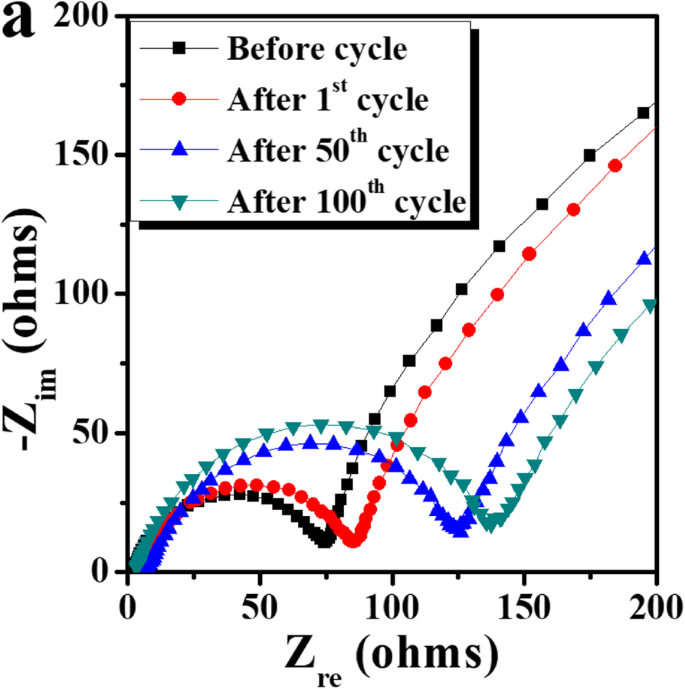
lithia / Li 2 を含むセルのナイキスト線図 RuO 3 サイクリング前および選択したサイクル(1、50、および100サイクル)後のナノコンポジット
ナノコンポジットの放電曲線の分析(図3a)は、2.9〜2.7 V付近の勾配のわずかな変化を示しています(図3a、赤い線でマーク)。これは、電流密度が高い場合により明確に現れます。リチアのORRを考慮すると、赤い線の上の高電圧領域は、ペルオキソ様(O 2 ) n − 充電プロセス中に形成された種であり、低電圧領域はO2pホールの中和に起因します[27]。リチアの純粋なレドックス反応による放電容量が3.1V未満の低電圧範囲で示されているため(図3a)、容量の一部が約3.1 V以上で観察されることは注目に値します[25、26、27、 28,29]。したがって、lithia / Li 2 の容量 RuO 3 〜3.1 Vを超えるナノコンポジットは、リチアではなく他の材料に起因する可能性があります。 Li 2 RuO 3 lithia / Li 2 に含まれています RuO 3 ナノコンポジットはかなりの放電容量を持っているため、総容量に寄与することができます。 Li 2 の充放電特性を観察する RuO 3 、Li 2 を含むセル RuO 3 陰極が準備され、電圧曲線が測定されたので。図5aに示すように、十分な充電には約4.3 Vの高電圧が必要であり、放電容量の大部分は3.1 Vを超えます。図5bは、リチア/ Li 2 の放電プロファイルを比較しています。 RuO 3 ナノコンポジットとLi 2 RuO 3 、2つのカソードの電圧範囲が異なることを示しています。したがって、lithia / Li 2 の放電容量の大部分 RuO 3 ナノコンポジットは、リチウムの酸化還元反応に関連しており、Li 2 の容量には関連していません。 RuO 3 。ただし、lithia / Li 2 の容量の一部が存在する可能性があります。 RuO 3 〜3.1 V以上で観察されたナノコンポジットは、Li 2 の酸化還元反応によるものです。 RuO 3 、ただし、かなりの量のLi 2 があるため、これはありそうにありません。 RuO 3 粉砕プロセス中にRuに分解されます。さらに、残留Li 2 RuO 3 図1aで確認されたように、アモルファス相に変化しました。
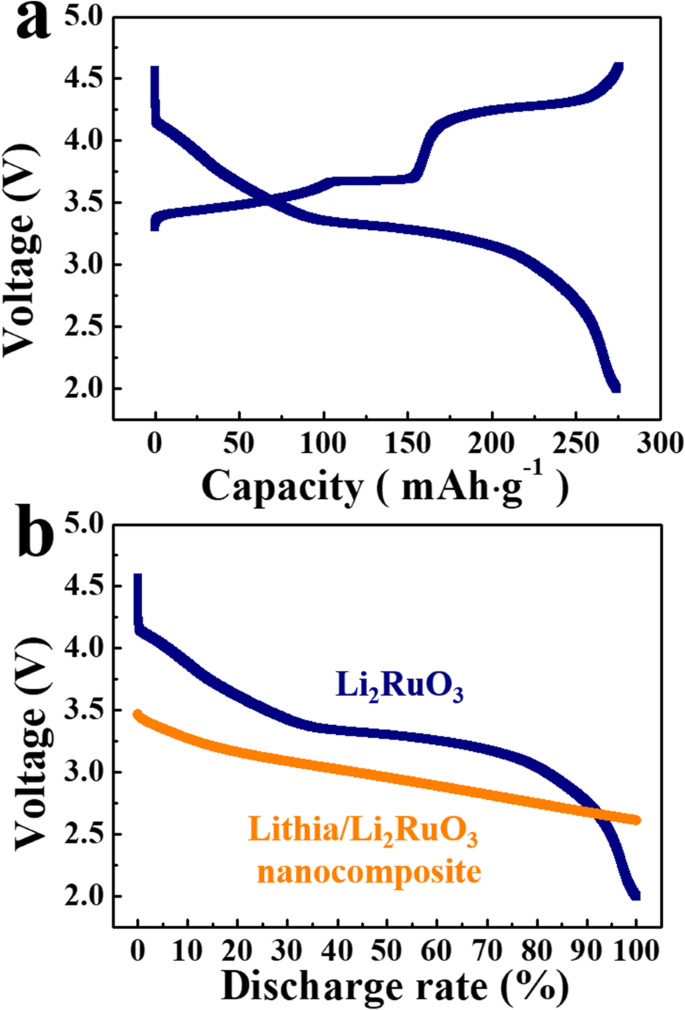
a Li 2 の充放電プロファイル RuO 3 。 b lithia / Li 2 間の放電プロファイルの比較 RuO 3 ナノコンポジットとLi 2 RuO 3
充電/放電プロセス中に発生する酸化還元反応を解明するために、lithia / Li 2 RuO 3 XPSを使用して、さまざまな充電状態と放電状態のナノコンポジットを分析しました。図6は、lithia / Li 2 のO1sおよびRu3dスペクトルを示しています。 RuO 3 サイクル中のナノコンポジット。測定のために、ナノコンポジットを350および500 mAhg -1 に充電しました。 (完全に充電されたものとして割り当てられます)、次に250および500 mAh g -1 に放電されます 、 それぞれ。図6aに示すように、ナノコンポジットのO 1sスペクトルは帯電プロセス中に変化しました。 〜531.5 eVおよび〜533.5 eVの大きなピークは、炭酸溶媒の分解による酸素化された堆積種に起因します[39、40]。サンプルが350mAhに充電されたときg -1 、格子O 2- 〜529.5 eV(スカイブルーでマーク)のピークが減少し、〜531 eV(赤でマーク)の新しいピークが現れました。セルが500mAh g -1 に完全に充電されると、新しいピークが大きくなりました。 、格子O 2- の減少を伴う ピーク。この新しいピークは、ペルオキソ様(O 2 ) n − 格子酸素のORRを介した種(O 2- )。これらの種は不安定で、液体電解質に容易に溶解します。ただし、XPSスペクトルは、それらが固体構造に存在することを示しています。これは、触媒が原因である可能性があります。サンプルが排出されると、ピークはペルオキソ様(O 2 ) n − 種は減少し、ほとんど消えます(500 mAh g -1 に完全に放電された場合 )、これは格子O 2- の増加を伴います ピーク。これは、酸素による陰イオン酸化還元反応がリチア/ Li 2 で可逆的に進行することを確認します。 RuO 3 充電/放電プロセス中のナノコンポジット。図6bは、Ru 3d 5/2 を使用したRu3dスペクトルを示しています。 図6cで拡大された断面。 Ru 3dピークはサイクリング中に著しくシフトせず、Ruの酸化状態が変化しないことを示しています。 Li 2 の容量があるため、これは注目に値します。 RuO 3 カチオン性レドックス反応に起因するものは、アニオン性(酸素)レドックス反応に加えて、Ruの酸化状態の変化を伴う。サイクリング中のRu3dピークシフトに関する以前の報告は、Li 2 のXPS分析によって明確に観察されました。 RuO 3 [40]。しかし、我々の結果に基づくと、Ruによるカチオン性レドックス反応は、リチア/ Li 2 の放電容量にほとんど寄与しません。 RuO 3 ナノコンポジット。前に説明したように、lithia / Li 2 の容量のかなりの部分が疑わしいです。 RuO 3 ナノコンポジットは、Li 2 の容量に由来します RuO 3 Li 2 RuO 3 ナノコンポジットでは、大容量を表示する機能があります。ただし、Li 2 の容量を考慮すると RuO 3 これは主にRuのカチオン酸化還元反応に起因し、リチア/ Li 2 の容量の大部分が明らかです。 RuO 3 ナノコンポジットは、リチアの純粋な酸素レドックスから生成されます。アモルファスLi 2 の酸素はまだ可能です RuO 3 結晶相からアモルファス相への遷移が電気化学的性能を変える可能性があるため、構造もORRに関与する可能性があります。さらに、Li 2 の分解から形成された酸化リチウム種 RuO 3 フライス盤中にも容量を持つことができます。 〜3.1 V以上で観察された容量のごく一部は、これらの追加のレドックス反応に関連している可能性があります。
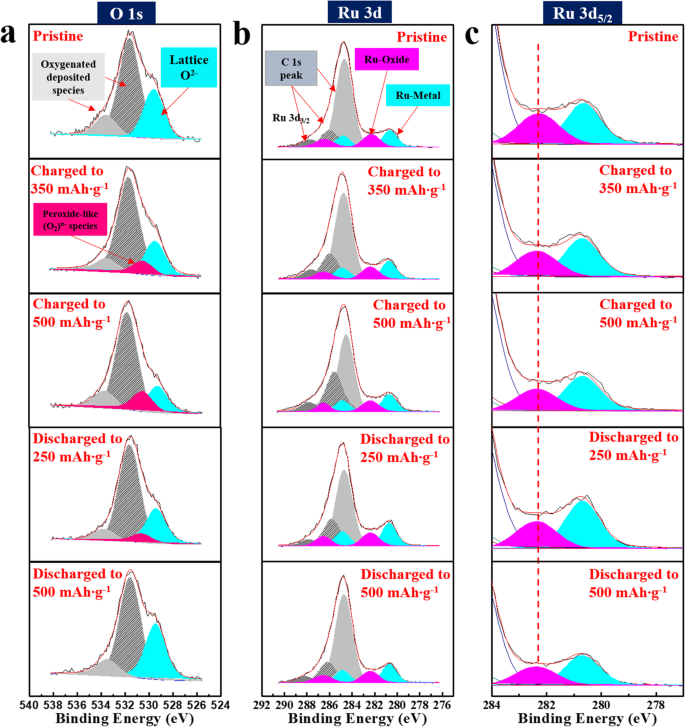
lithia / Li 2 のXPSスペクトル RuO 3 さまざまな充電および放電ポイントで測定されたナノコンポジット。測定のために、ナノコンポジットを350および500 mAh g -1 に充電しました。 (フル充電として割り当てられます)、250および500 mAh g -1 に放電されます フル充電後。 a O 1のスペクトル、 b Ru 3dスペクトル、および c Ru 3d 5/2 スペクトル
結論
リチア/ Li 2 RuO 3 ナノコンポジットは粉砕プロセスによって調製され、構造的および電気化学的性能が特徴づけられました。 Li 2 RuO 3 リチアを活性化し、Li 2 などの不安定な反応生成物を安定化するための新しい触媒として使用されました O 2 およびLiO 2 。粉砕プロセス中、かなりの量のLi 2 RuO 3 Ruに分解され、残ったものはアモルファス相に変換されました。結晶性リチアも、粉砕プロセス中にアモルファス相に変化しました。 lithia / Li 2 RuO 3 ナノコンポジットは、500 mAh g -1 で制限容量に達するまで、安定したサイクル性能を示します。 。ただし、制限容量が600 mAh g -1 に増加した場合 、サイクリングは不安定性をもたらし、セルが安定して充電および放電できる限界を超えて過充電されたことを示しています。 XPS分析から、リチア/ Li 2 の容量が確認されました。 RuO 3 ナノコンポジットは、主にペルオキソ様(O 2 )の可逆的な形成と解離に起因します。 ) n − 種族。対照的に、Ru 3dスペクトルはサイクリング中に目立って変化せず、リチア/ Li 2 の容量に対するカチオン(Ru)レドックス反応の寄与が確認されました。 RuO 3 ナノコンポジットはごくわずかです。したがって、lithia / Li 2 の容量の大部分 RuO 3 ナノコンポジットは、リチアの酸素酸化還元に起因します。ただし、容量の一部、特に〜3.1 Vを超える高電圧領域の容量は、Li 2 の分解から形成される酸化リチウム種など、ナノコンポジットに存在する他の材料に関連している可能性があります。 RuO 3 。 lithia / Li 2 RuO 3 ナノコンポジットは、大容量のリチアベースのカソードを開発するための優れた候補となります。この作品がlithia / Li 2 の理解に貢献できることを願っています。 RuO 3 ナノコンポジットとリチアベースのカソードの研究を刺激します。
データと資料の可用性
著者は、資料、データ、および関連するプロトコルが読者に利用可能であり、分析に使用されるすべてのデータがこの記事に含まれていることを宣言します。
略語
- ORR:
-
酸素レドックス反応
- XRD:
-
X線回折法
- XPS:
-
X線光電子分光法
- EDS:
-
エネルギー分散型X線分光法
- PVDF:
-
ポリフッ化ビニリデン
- TEM:
-
透過型電子顕微鏡
ナノマテリアル



