染料分解のための優れたフェントン様光触媒としてAAO膜に電着によって調製された3次元CuO / TiO2ハイブリッドナノロッドアレイ
要約
三次元(3D)CuO / TiO 2 テンプレート支援の低コストプロセスによって製造された、貴金属を含まない組成のハイブリッドヘテロ構造ナノロッドアレイ(NR)を、色素分解用のフォトフェントン様触媒として使用しました。ここでは、CuO NRは、さまざまな温度でアニールされた電着法によって陽極酸化アルミニウムテンプレートに堆積され、続いてTiO 2 が堆積されました。 Eガン蒸発による薄膜、結果としてCuO / TiO 2 p-nヘテロ接合。 CuO / TiO 2 の元素と組成の分布 p-nヘテロ接合は、EDSマッピングとEELSプロファイルによってそれぞれ分析されました。 H 2 の存在下 O 2 、CuO / TiO 2 ハイブリッド構造は、500W水銀キセノンアークランプの照射下でのローダミンB分解に対してCuONRよりも効率的に機能しました。この研究は、CuONRの長さがCuONRおよびCuO / TiO 2 の光分解性能に及ぼす影響を実証しました。 ヘテロ構造。最適化されたCuO / TiO 2 ハイブリッドNRアレイ構造は最高の光分解活性を示し、染料の光分解における触媒として作用する光フェントンのメカニズムと役割も調査されました。
背景
1760年代の産業革命は、人間の生活を楽にしました。しかし、産業は有毒な化合物を生成し、個人や環境に有害な深刻な汚染物質を排出します。特に開発途上国では、有機性廃棄物を水域に排出する繊維産業や石油化学産業の成長により、環境汚染の問題が悪化しています。したがって、廃水処理は非常に重要になっています[1、2]。廃水処理にはさまざまな方法があり、物理的、化学的、生物学的プロセスに分類できます。高度な化学酸化プロセス(AOP)は、有機分子の破壊または分解を促進する最も安定した強力な方法の1つです[3]。一般に、AOPは、無害で強力な短命の酸化剤である反応性ヒドロキシルラジカル(OH・)の急速な生成により、優れた分解能力を示します。特に、19世紀からよく研究されてきたフェントンシステムは、工業用有機汚染物質の除去に適した候補です[4、5]。フェントン(Fe 2+ / H 2 O 2 )またはフェントンのようなもの(例:Fe 3 O 4 / H 2 O 2 )システムは有機汚染物質の分解に広く使用されています[6、7]。 Feベースの材料などのフェントンのような触媒は、より安定しており、制御可能で、無害であり、フェントン触媒と同じくらい高い効率を示します。場合によっては、不適切なpHや溶液中の反応性物質の存在など、過酷な環境でパフォーマンスが向上し、沈殿や吸収を引き起こして触媒を消費する可能性があります[8、9、10]。 Feベースの材料とは別に、一部のCuベースの材料もフェントンのようなシステムで優れた性能を示します。
さらに、熱、照射、電気、振動力などの余分なエネルギーを使用することで、触媒作用を強化することができます[11]。その中でも、触媒による光分解、すなわち光触媒作用は、その単純さと容易さから大きな注目を集めています。光触媒性能を支配する2つの重要な特性があります。 1つは、電子正孔対を生成する触媒の能力です。これは、水酸化反応物のフリーラジカルを生成する光触媒反応に関連しています[12、13、14、15]。もう1つは、発光によって生成された電子正孔対が十分に分離されているため、再結合が妨げられます。半導体材料は、バンドギャップが狭い光触媒として機能するのに非常に適しています。これにより、最適な熱または光エネルギーを吸収するときに、電子が価電子帯(VB)から伝導帯(CB)に励起されやすくなります。最も広く使用されている光触媒の1つは二酸化チタンです。これはn型金属酸化物半導体であり、その高い活性と低コストのために広く研究されてきました[16、17、18、19]。さらに、酸化銅(CuO)は、フェントンのような狭いバンドギャップのp型金属酸化物半導体光触媒です。
陽極酸化アルミニウム(AAO)は、電気化学エッチング法によって製造された均一で平行な細孔の高密度アレイを備えた、自己組織化され秩序化された六角形のハニカム状ナノポーラス構造です[20、21、22 、23、24、25、26]。細孔の直径は、数ナノメートルから数百ナノメートルまで小さくすることができ、長さは、数ナノメートルから数百マイクロメートルを超えるまで制御することができる。多孔質構造のサイズは、電解質、電圧、電流密度など、さまざまな陽極酸化条件と相関させることができます[27、28、29、30、31、32、33、34、35、36、37、38]。さらに、パルス電流電気めっきは、ステップ電流と周波数を変更することにより、堆積速度や結晶化度など、室温での堆積特性を正確に制御できます[39、40、41、42、43、44]。それにもかかわらず、パルス間の比較的長い緩和は、堆積中に応力を解放します。これは、制御可能な核形成と十分に分離された成長の利点と見なすことができます[45、46、47]。さらに、短いデューティサイクルと高周波の組み合わせにより、表面の亀裂を減らすことができます。
この点に関して、犠牲テンプレートとしてのAAOと、パルス電着プロセスとEガン蒸着堆積法の組み合わせにより、高効率で大量生産された触媒が得られました。ここで、CuOはパルス電着によってプレハブAAOに堆積されました。最終的に、TiO 2 Eガン蒸発によって堆積されました。次に、色素分解に応用するためのNRアレイ構造を備えた非イオン性フェントン様光触媒の改良に焦点を当てました。明らかに、CuOとTiO 2 は、p-nヘテロ接合フォトフェントンのような触媒として動作するように組み合わされ、元素の分布とp-nヘテロ接合の組成は、それぞれEDSマッピングとEELSプロファイルによって分析されました。 CuONRおよびCuO / TiO 2 の性能 500W水銀キセノンアークランプの照射下でのローダミンB分解のハイブリッド構造を比較研究しました。さまざまな長さのCuONR、およびさまざまなCuOとTiO 2 のアニーリング温度への影響 ローダミンBの光分解に関する研究が詳細に研究されました。
メソッドセクション
材料と試薬
アルミニウム箔(99.99%、GUV Team Int)、硫酸銅(II)五水和物(99.99%、Sigma Aldrich)、塩化銅(97%、Alfa Aesar)、過塩素酸(75%、JT Baker)、シュウ酸(99.5% 、JT Baker)、エタノール(99.5%、Sigma Aldrich)、塩酸(30%、FLUKA)、リン酸(99.99%、Sigma Aldrich)、水酸化ナトリウム(98%、Sigma Aldrich)、過酸化水素(30%、Sigma Aldrich)、重クロム酸カリウム(99%、Merck)、エポキシ353ND(EPO-TEK)、および2-ヒドロキシプロパン-1,2,3-トリカルボン酸三ナトリウム(99%、Merck)。
ナノロッド(NR)アレイハイブリッド構造を備えた光触媒の改良に焦点を当て、色素分解に応用しました。高効率の光触媒の製造には、酸化銅ナノロッド/二酸化チタン(CuO / TiO 2 )ハイブリッド構造、テンプレート支援アプローチは、パルス電着プロセスおよびEガン蒸着堆積法と組み合わせて使用されました。 p-nヘテロ接合光触媒を形成するために、酸化銅(CuO)をパルス電着、次に二酸化チタン(TiO 2 )によって陽極酸化アルミニウム(AAO)に堆積させました。 )E-gun蒸発によってその上に堆積されました。さまざまな長さのCuONR、およびさまざまなアニーリング温度のCuONRとCuO / TiO 2 への影響 ローダミンBの光分解に関するハイブリッド構造が詳細に研究されました。
陽極酸化アルミニウム(AAO)の形成
純度99.997%のアルミホイルをGUVチームインターナショナル株式会社から調達しました。アルミホイルを1cm 2 の等形にカットしました。 そして、20 vol。%の過塩素酸と80 vol。%の無水アルコールを含む電解液中で40 Vで5〜10秒間電気化学研磨する前に平らにしました。次に、陽極酸化に使用する前に、基板を脱イオン水ですすいだ。自家製のAAO膜は、非常によく知られている2段階の陽極酸化法によって製造されました。最初のステップの陽極酸化は、0.3Mシュウ酸中で40Vで10分間実施しました。 AAOの規則性比は、最小の欠陥に対応する最大値を示しました[31]。 AAOの安定した成長を制御するために、冷却システムを使用して溶液を10℃に維持しました。次に、2.24 wt。%の重クロム酸カリウムと6 wt。%のリン酸の溶液に60°Cで1時間浸漬しました。 AAOがエッチングされ、基板の表面に凹みが残され、これが陽極処理中の成長のための形成部位となった。 2番目のステップである20分と80分の陽極酸化により、AAOのチャネル長はそれぞれ1.85μmと6.53μmになりました。陽極酸化が完了した後、5分間の電流内で電流を段階的に変化させてバリア層の厚さを薄くすることにより、陽極酸化電圧を5Vに下げました。バリアを薄くするプロセスにより、テンプレートは電着に適したものになりました。次に、5 wt。%リン酸に室温で45分間浸漬して、チャネルの直径を広げました。
酸化銅/二酸化チタン(CuO / TiO 2 )の製造 )ハイブリッド構造
酸化銅(CuO)は、よく知られているパルス電着法によって陽極酸化アルミニウム(AAO)膜に堆積されました。電解液には、0.6 Mの硫酸銅、6 wt。%の2-ヒドロキシプロパン-1,2,3-トリカルボキシレート三ナトリウム、および室温で100 mlの脱イオン(DI)水に溶解した10μlの界面活性剤が含まれていました。従来の3電極電気化学セルの作用電極には、パルスが40 mA / 10msおよび0mA / 40msの非対称の長方形電流が供給されました。パルスは、AAOに対してそれぞれ1.85μmと6.53μmの2つの異なる長さで6000サイクルと20,000サイクルで適用されました。 CuOの堆積後、酸素の存在下、400、500、600°Cのさまざまな温度で管状炉内で12時間アニーリングを行いました。完全に酸化された酸化銅NRを得るために、O 2 フラックスは100sccmに維持されました。 TiO 2 NRの終わりにNRアレイを覆うEガン蒸着によって、100nmの厚さのCuO / AAOの上部に堆積されました。サンプルの2回目のアニーリングは、管状炉内で400、500、600°Cのさまざまな温度で5時間酸素周囲雰囲気で行われました。界面での2つの異なる金属酸化物間の結晶化度と付着力を高めるために、酸素フラックスは100sccmに保たれました。触媒膜をアルミニウム基板からガラスに転写するために、(TiO 2 側面)100°Cで3時間加熱したエポキシ353ND(EPO-TEK®)を使用してサンプルをガラスに接着しました。次に、ガラス上に転写されたサンプルを塩酸、無水塩化第二銅、および脱イオン水からなる溶液に浸し、AlとCu 2+ の間の酸化および還元反応によってアルミニウム基板を除去しました。 。アルミニウムは銅に置き換えられましたが、基板への銅の付着はより悪く、残りのナノ構造はAAOで覆われていました。サンプルを1M水酸化ナトリウム溶液に室温で5時間浸すことにより、残留酸化アルミニウムを除去しました。
酸化銅/二酸化チタン(CuO / TiO 2 )の染料分解 )ハイブリッド構造
酸化チタン薄膜でキャップされたCuO-ナノロッド(NR)アレイは、基板支援の不均一光フェントン触媒として機能します。分解試験用のフォトフェントン様試薬は、500Wの水銀キセノンアークランプの下で、50ppmのローダミンBと88mMの過酸化水素を含む100mLの溶液に適切な量の触媒を加えることによって調製されました。光源と溶液の間の距離は20cmに維持されました。照射前に、溶液と触媒を1時間暗所に置き、吸着/脱着平衡が確立されていることを確認しました。サンプリングは5分間隔で実施しました。毎回、100μLの溶液を収集し、10 mLの脱イオン水で希釈してから紫外可視領域分光法(UV-Vis)測定を行いました。サイズが1cm 2 のCuONRサンプル すべての分解実験で使用されました。最初に、光分解実験は、400、500、および600°Cのさまざまなアニーリング温度の下で、1mgの1.85μm長のCuONRを使用して実行されました。次の一連の実験は、600°Cでアニールされた1.85μmの長さのCuO NRの1、2、3、および5mgを使用して実行されました。さらに、色素劣化測定は、600°Cでアニールされた1mgの1.85μm長のCuONRと100nmの厚さのTiO 2 を組み合わせて実施されました。 400、500、600°Cでアニーリング。次に、光劣化測定を、厚さ100nmのTiO 2 で収集した6.53μm(3 mg)および1.85μm(1 mg)の長さのCuONRを使用して実行しました。 500°Cでアニーリング。さらに、100、200、および300nmの厚さのTiO 2 を使用して一連の測定を実行しました。 長さ1.85μmのCuONRをキャッピングする層。光分解測定の最終セットは、最適化された触媒を使用して実行されました。1mgの1.85μm長のCuO NR(600°Cでアニール)と100nmの厚さのTiO 2 (500°Cでアニーリング)100 mlの50、250、および750ppmローダミンB溶液に添加。
特性評価
表面形態とNRの長さは、電界放出型走査電子顕微鏡(FE-SEM、Hitachi-SU8010)によって確認されました。材料(酸化銅(CuO)と酸化チタン(TiO 2 )の結合の種類と組成 ))532 nmレーザーを備えたラマン分光分析(HORIBA Jobin-Yvon、LabRAM、HR 800)によって検証されました。材料(酸化銅と酸化チタン)の相と結晶化度の結果は、X線回折(D2フェイザー、CuKα、λ)によって収集されました。 =0.154 nm)20°から80°の範囲の2θでスキャンします。 TiO 2 の形態、d間隔、および組成 キャップされたCuONRは、エネルギー分散型X線分光法(EDX)および電子エネルギー損失分光法(EELS)を備えた透過型電子顕微鏡(TEM)によって決定されました。分解効率は、紫外可視近赤外分光光度計(U-4100)で測定したローダミンBの吸光度データから算出しました。 TEM観察の前に、サンプルは集束イオンビーム技術によってナノスケールでスライスにカットされました。 TEM分析には通常、50 nm未満のスライスの厚さが適切です。これにより、鮮明な画像が得られ、EELSスペクトル分析が可能になります。
結果と考察
この研究で製造された不均一光フェントン触媒は、酸化銅NRアレイ上の酸化チタン薄膜層を含む2種類の金属酸化物半導体で構成されています。全体的なプロセスを図1に模式的に示します。1.85μmと6.53μmの2つの異なる長さのAAOを、2段階の陽極酸化プロセスとそれに続くバリア薄化を使用してアルミニウム基板上に製造しました。 CuO NRを形成するために、酸化銅(CuO)を、制御されたサイクル数のパルス電着によってAAO膜に堆積させました。完全に酸化された酸化銅NRを取得するために、サンプルの最初のアニーリングを、O 2 の下でさまざまな温度で12時間実行しました。 アンビエント。 TiO 2 の堆積 次に、Eガン蒸着によって実行され、CuO / AAOの上部に100nmの厚さの薄膜を形成しました。界面での2つの異なる金属酸化物間の結晶化度と密着性を高めるために、サンプルの2回目のアニーリングを、O 2 の下で400、500、および600°Cで5時間実行しました。 アンビエント。次に、さらなるプロセスのために、触媒膜をアルミニウム基板からガラスに転写した。最初にアルミニウム基板を取り外しました。次に、残留酸化アルミニウムを基板から除去した。最終的なガラスサンプルは、特性評価と測定にさらに使用されました。
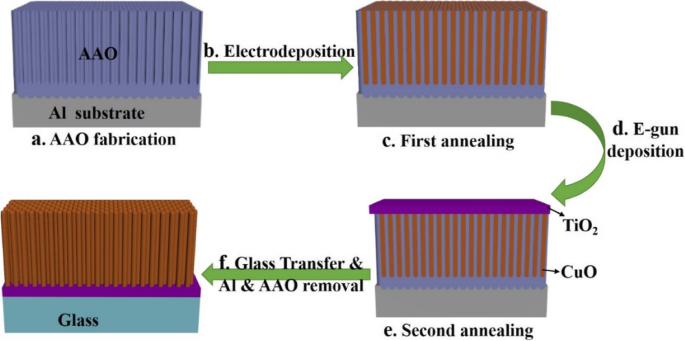
CuO / TiO 2 の製造プロセスフローの概略図 ハイブリッドナノロッド(NR)アレイ
図2に示すように、AAOおよびテンプレート支援CuONRアレイの形態をFE-SEMで観察しました。図2aおよびbは、AAOの上面図および断面図のFE-SEM画像をそれぞれ示しています。平均細孔径が〜76 nm、長さが〜1.85μmであることが確認されました。図2cおよびdは、AAO内のCuONRの上面図および断面図のSEM画像を示しています。ここでCuONRは、チャネル長1.85μmのAAOを使用して作成されています。イチジクから。図2cおよびdにおいて、CuO NRは、電着による高い充填速度でAAOに十分に堆積された。同様に、6.53μmの長さのCuO NRは、追加ファイル1:図S1に示すように、断面図のSEM画像から確認された6.53μmのチャネル長のAAOを使用して作成されました。 AAOテンプレート支援技術は、CuONRの製造の再現性を保証できます。

a 上面図と b 電着前のAAOの断面SEM画像。 c 上面図と d CuO電着後のAAOの断面図SEM画像(スケールバー、1μm)
材料の結晶化度と組成は、材料の品質と相を示すラマンとXRDの結果によって検証されました。ラマンおよびXRD分析では、サンプルをガラス基板に移し、続いてAl基板とAAOを除去しました。上記のプロセスの詳細については、実験のセクションで説明しています。上記のプロセスに続いて、生のCuO NR、さまざまな温度でアニールされたCuO NR、およびCuO NR / TiO 2 を含む、合計7つのサンプルがラマンおよびXRD分析用に準備されました。 異なる温度でアニールされた構造。 CuO 1-x のラマンシフト 400、500、600°Cのさまざまなアニーリング温度で調製されたNRを図3aに示します。 297 cm -1 に2つのピーク および352cm -1 CuO 1-x のラマンスペクトルで見つけることができます アニーリングプロセス後のNRは、黒銅鉱相を含む標準の純粋なCuOとよく一致します。ラマン分析の結果は、XRD分析によって裏付けられました。 XRD分析で観察されたピークは、2θで32.5°、35.5°、38.7°、48.7°、58.3°、および61.5°であり、(110)、(11 \(\ overline {1} \))、(111)に対応します。 、(20 \(\ overline {2} \))、(202)、および(11 \(\ overline {3} \))平面は、それぞれ図3bに示すように黒銅鉱相にあります。 AAOテンプレートのCuONRは完全に酸化され、酸素環境で12時間保持された400°Cを超える高いアニーリング温度で黒銅鉱相に変換されました。さらに、アニーリング温度が高くなると、結晶化度が増加します。これは、黒銅鉱相のメインピークの半値全幅(FWHM)を計算することで証明されました。ガウス関数フィッティングにより、400、500、および600°CでアニールされたCuOサンプルの(11 \(\ overline {1} \))ピークのFWHMは、それぞれ0.284°、0.251°、および0.22°に対応します。 FWHMは、アニーリング温度が上昇するにつれて減少し、結晶化度と粒子成長の改善を示します。さらに、Eガン堆積したTiO 2 の結晶構造 異なるアニーリング温度でCuOを覆う薄膜を図3cに示します。ラマンスペクトルは、純粋なCuOとTiO 2 のアナターゼ相を示しました。 400、500、および600°Cのアニーリング温度の後に達成されます。ラマンピークは145、397 [1]、516、および637 cm -1 TiO 2 のアナターゼ相を表します 一方、ピークは299および397 cm -1 純粋なCuOを描写します。 CuO / TiO 2 のXRD結果 図3dに示すように、2θ=25.3°のピークは、TiO 2 のアナターゼ相の存在を示しています。 (101)面では、他のピークはCuOの存在に起因しています。明確に、アナターゼTiO 2 の結晶化度 アニーリング温度が400から500°Cに上昇するにつれて、相は増加します。ただし、FWHMの結果で確認されているように、温度をさらに500°Cから600°Cに上げると低下します。 (101)面に関連する回折ピークの拡大図に基づいて、2θで0.432、0.411、および0.416°のFWHMが、以下に示すように、それぞれ400、500、および600°Cのアニーリング温度で計算されました。図3e。アナターゼ型TiO 2 の結晶化度の低下 600°Cの相転移温度でのルチル相の核形成に関連していました[48]。ただし、ラマン分析では、通常600°Cで得られるルチル相は示されませんでした。それにもかかわらず、追加ファイル1:図S2は、TiO 2 のXRD分析によってルチル相の存在を示しています。 25〜29°の2θ範囲にわたって。
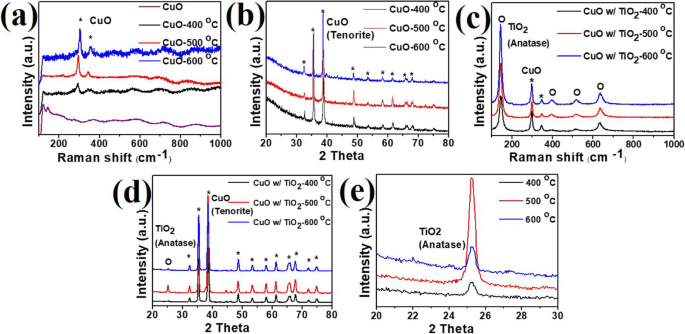
a ラマンと b さまざまな温度でアニールされたCuONRのXRD結果。 c ラマンと d CuO / TiO 2 のXRD結果 さまざまな温度で焼きなました。 e CuO / TiO 2 のXRD結果の拡大図 20〜30°の2θ範囲で
TiO 2 の典型的な低倍率画像 2段階でアニールされた薄膜コーティングされたCuONRアレイでは、最初のアニールプロセスはCuO堆積後600°Cで12時間実行され、2番目のアニールプロセスはTiO <の後に500°Cで5時間実行されました。 sub> 2 図4aに示すような堆積。図4bは、図4aから選択した部品の高分解能TEM(HRTEM)画像を示しています。これを使用すると、TiO 2 薄膜は、CuONRの上部に十分に堆積されています。図4bに見られるように、清澄化されたTiO 2 CuONRの上部にコーティングされた層を確認できます。 FFTによって計算されたd間隔とCuONRのFFT画像を図1と図2に示します。それぞれ4cとd。 CuOは、(111)面で0.232 nm、\(\ Big(\ overline {1} 11 \))で0.249nmのd間隔を示します。格子定数と回折パターンは、CuOの黒銅鉱相(JCPDSカード#05-0661)とよく一致しています。図4eは、TiO 2 のEDSマッピング画像を示しています。 キャップされたCuONR。 EDSの結果からのコンポーネントマッピング画像は、元素の均一な分布を示しており、キノコのような形状のCuONRの上部の局所領域に集中しているチタン信号を見つけることができます。図4fに示すEELSプロファイルは、それぞれチタン、酸素、銅の組成を示しています。チタン信号は片側にのみ存在し、銅と酸素の信号は構造全体に現れますが、覆われた領域と覆われていない領域の間で異なる比率で現れます。 Cu信号とO信号は、CuO NRでほぼ1:1の比率で十分に分散されていますが、カバーされた領域のCu:O:Ti信号は、それぞれ3:6:1の比率を示しています。
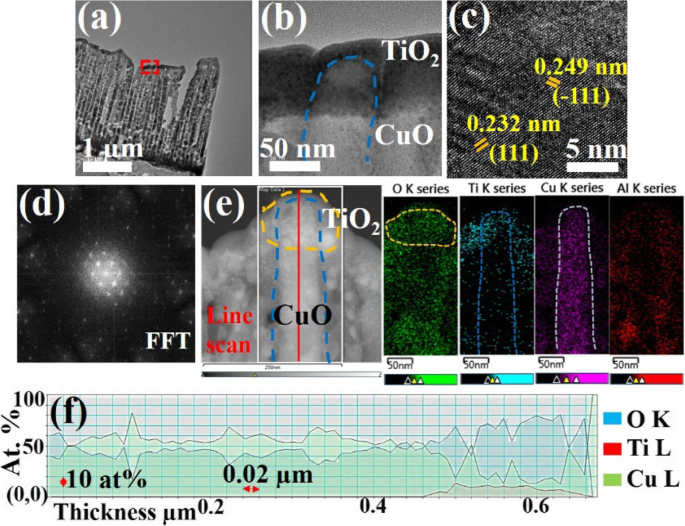
a TiO 2 でキャップされたCuONRアレイの低倍率TEM画像 薄層。 b TiO 2 の対応するHRTEM画像 - a で示される長方形の領域から取得されたキャップ付きCuONR 。 c d-spacingおよび d CuONRのFFT結果。 e EDSマッピング画像と f CuO / TiO 2 のEELSラインスキャン結果
染料廃液の精製と廃水処理のために、ローダミンB(RhB)の光分解が集中的に研究されてきました[49、50]。水溶性と有機溶解性の両方が高く、潜在的に毒性があり発がん性があることがわかっているキサンテンクラスの基本的な赤色染料は、繊維や食品の着色剤として広く使用されています。また、よく知られているウォータートレーサー蛍光色素です[51、52]。脱色によって引き起こされる色の変化に関連する吸光度は、UV-vis結果の測定によって決定できます。吸光度は、赤色光領域で450〜600 nmの範囲の波長で記録され、RhBは554nmでの光吸収の最大結果を示しました。光吸収材料の吸光度は、次の式に従ってその濃度に比例します。
$$ \ mathrm {A} =\ log \ left(\ frac {I} {I_o} \ right)=\ log \ left(\ frac {1} {T} \ right)=\ upalpha \ mathrm {lc} $ $(1)$$ \ frac {\ mathrm {C}} {C_o} =\ frac {\ mathrm {A}} {A_o} $$(2)ここで A o および A は照射前後の色素溶液の吸光度です。 I および私 o 入射光と透過光の強度、 T 光の透過率、α は吸収係数、 l はサンプルのパスの長さであり、 C o および C はそれぞれ照射前後の色素溶液の濃度です。光分解の効率は、適切な波長範囲での濃度と吸光度の関係によって測定できます[53]。ただし、高濃度では、非線形の振る舞いのため、濃度から吸光度への曲線は式に従いません。一方、より低い色素濃度では、ヒドロキシルラジカルとヒドロペルオキシルラジカルのかなりの部分が再結合してH 2 を生成します。 O 2 そして分解はより低い濃度のOHラジカルで行われた。過剰な酸素バブルはフリーラジカルを吸収し、バブルで生成されたOHラジカルの約10%のみが溶液に拡散し、それによって分解速度が遅くなるため、試薬が減少します。染料濃度の増加に伴い、分解速度が上昇し、飽和限界に達すると平衡状態になります。異なる分解時間での吸光度と濃度の比率を計算し、さまざまな操作条件下での分解速度を求めました。さらに、濃度変化に関する情報は、化学反応の順序を示します。通常、色素分解の場合、反応は疑似一次反応です。反応の次数を計算する式を以下に示します。
$$ \ mathrm {C} ={C} _ot + B $$(3)$$ \ ln \ left(\ frac {\ mathrm {C}} {C_o} \ right)=kt + B $$(4) $$ \ frac {1} {\ mathrm {C}} =\ frac {1} {C_o} + kt $$(5)C は濃度、 t 反応時間、 k は平衡定数であり、 B 定数です。光触媒活性は、さまざまな条件下でRhB溶液の分解速度を測定することによって明らかになりました。式(3)はゼロ次反応を表し、式(4)と(5)はそれぞれ1次反応と2次反応を表すことに注意してください。濃度プロファイルは、活性だけでなく反応順序も示します。ここでは、触媒の投与量を変えて反応順序を測定しました。このシステムは、疑似一次反応として分類できます。分解速度は、投与量の増加とともに増加し、触媒/溶液の界面に付着した反応物の飽和により平衡条件を満たします。これは、不均一系触媒の表面積が反応の決定要因の1つであるために発生しました。表面積対質量比が大きくなると、平衡状態に達するために必要な触媒の投与量ははるかに少なくなりました。私たちの場合、平衡状態の場合、約3 mgの投与量が必要であり、次に動的平衡定数 k 0.436 min -1 として計算できます 。
図5aは、酸素環境で12時間、400、500、600°Cのさまざまなアニーリング温度で、長さ1.85μmの1mgのCuONRの光触媒性能を示しています。アニーリング温度を600°Cに上げると、触媒の結晶化度が高くなり、より優れた性能を発揮します。 TiO 2 を使用したRhBの分解速度 酸素環境中で400、500、600°Cのさまざまな温度で5時間アニールされたキャップ付きCuONRを図5bに示します。アナターゼ型TiO 2 キャップされたCuONR、触媒は優れた効率を示します。また、アニーリング処理後の光触媒活性をさらに向上させることができます。興味深いことに、500°Cの温度でアニーリングされたサンプルは最高の光触媒活性を示しますが、600°Cでアニーリングされたサンプルは低下した光触媒性能を示します。その結果、CuO / TiO 2 500°CでアニールされたハイブリッドNRアレイは、最高の触媒性能を示し、速度論的平衡定数 k をもたらしました。 0.921 min -1 。 600°Cでアニールされた触媒が500°Cよりも低い性能を示した理由は、ルチル相の存在に関連しています。 O 2 の下 周囲条件、TiO 2 の相転移 アナターゼからルチル相への移行は、約600°Cの温度で発生します(追加ファイル1:図S2)[48]。アニーリング温度が相変態温度に達すると、TiO 2 の光触媒活性 ルチル相への核形成の形成により減少します。一般的に、TiO 2 アナターゼとルチル相の比率が一定の混合相で構成されている場合、アナターゼとルチル相の両方の単相よりも優れた導電性と光触媒特性を示します。この場合、TiO 2 のアニーリング条件 相変態温度を受けた。ルチル相の核形成によりアナターゼ相の粒子サイズが小さくなるため、TiO 2 の結晶化度が低下します。 ルチル相が減少すると、光触媒活性が低下します。 CuO / TiO 2 における2つの異なる長さのCuONRの影響 光分解性能の概要を図5cに示します。 CuO NRサンプルの場合のみ、NRの長さが長い(6.53μm)と、触媒の投与量が多くなり、長さが短いNRよりも優れた光触媒性能を示しました。 TiO2薄膜と組み合わせたCuONRの場合、光の侵入深さが重要な役割を果たす可能性があります。空乏ゾーンが照射にさらされた場合にのみ、p-nヘテロ接合半導体は優れた光活性を示します。次に、光励起された電子正孔対が急速に分離し、試薬と反応する可能性があります。ここで、侵入深さは次の式で計算できます。 d =1 / α 、ここでα CuOの吸収係数を表します。水銀キセノンアークランプのスペクトルの分布は、3eVを超える光子エネルギーを持つUV光に近いです。 CuOのさまざまな軸によると、シミュレーションから計算された侵入深さは1〜5μmになります[54]。したがって、1.85μmの長さのCuO NRは、ヘテロ構造に対して優れた性能を示しました。さらに、CuONRおよびCuO / TiO 2 のNRの長さへの影響 入射光の侵入深さに関連するものを図5cに示します。ヘテロ構造のNRの長さが長い(6.53μm)と、光が空乏ゾーンに到達するのが制限されることに注意してください。したがって、1.85μmの長さのCuONRはTiO 2 で覆われます。 層は、TiO 2 で覆われた長さ6.53μmのCuONRと比較して、はるかに優れた触媒効果を示します。 層。 RhBの劣化に関する測定は、最も活性の高いサンプル、つまりTiO 2 と組み合わせた後、600°Cでアニールされた長さ1.85μmのCuONRを使用して異なる初期RhB濃度で実施されました。 図5dに示すように、500°Cでアニールされた層。 50、250、および750 ppmの初期RhB投与量の場合、反応はそれぞれ10、25、および75分で完了しました。 CuO / TiO 2 のバンド図 は、図6に示すように、千鳥ギャップ(タイプII)ヘテロ接合半導体です。
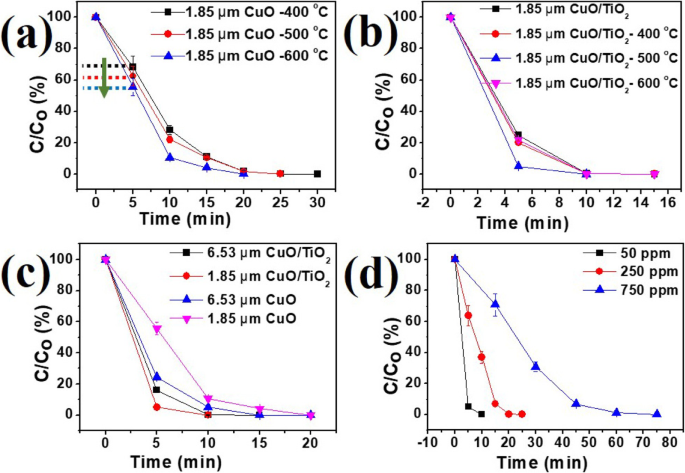
a の分解結果 さまざまな温度でアニールされたCuONRサンプル。 b CuO / TiO 2 異なる温度でアニールされたサンプル。 c TiO 2 のキャッピングがある場合とない場合のさまざまな長さのCuONRのサンプル 層。 d 最も活性の高いサンプルでのRhBのさまざまな初期濃度(600°C1.85μmCuONRs+ 500°CTiO 2 )
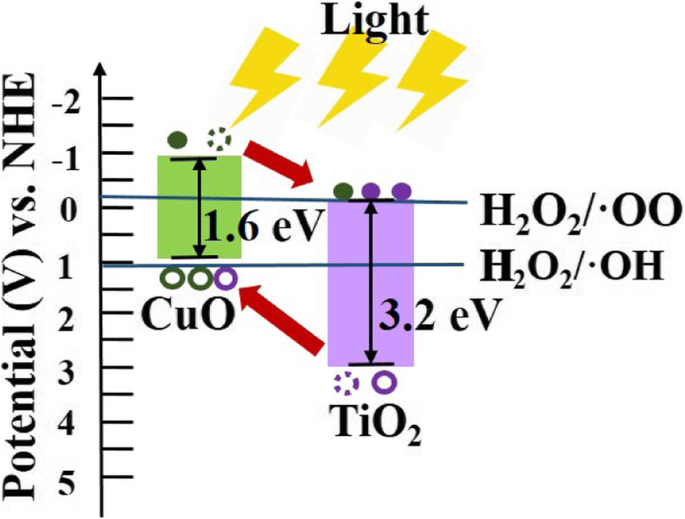
CuOとTiO 2 のバンド図 pH =7で[55、56]
光フェントン触媒作用の基本原理は、H 2 によって生成されるヒドロキシルラジカルとヒドロペルオキシルラジカルによって分解される汚染物質を参照する酸化および還元反応です。 O 2 照射下で励起された電子正孔対を介して触媒の助けを借りて[50、57、58]。なお、不均一系触媒の一般的なタイプである分解速度・投与量プロファイルにより、疑似一次反応の反応が確認されています[59]。触媒のより多くの投与量からもたらされるより大きな表面積は、H 2 のための領域を提供しますが O 2 界面に付着するために、ヒドロキシルラジカルとヒドロペルオキシルラジカルの平衡濃度は、温度、照射、pHなどのさまざまな条件での反応速度に関連している可能性があります。 H 2 が十分に取り付けられている O 2 、反応はほぼ一次のように見えました。これは、化学反応が拡散ではなく律速段階として機能したことを意味します。 H 2 の分解反応 O 2 以下に示します。
$$ \ mathrm {CuO} \ left({\ mathrm {h}} ^ {+}-{\ mathrm {e}} ^ {-} \ right)+ {\ mathrm {H}} _ 2 {\ mathrm {O }} _ 2 =\ mathrm {OH} \ cdotp + {\ mathrm {O} \ mathrm {H}} ^ {-} + \ mathrm {HOO} \ cdotp + {\ mathrm {H}} ^ {+} $$ (6)$$ \ mathrm {CuO} \ left({\ mathrm {h}} ^ {+} \ right)-{\ mathrm {TiO}} _ 2 \ left({\ mathrm {e}} ^ {-} \ right)+ {\ mathrm {H}} _ 2 {\ mathrm {O}} _ 2 =\ mathrm {OH} \ cdotp + {\ mathrm {O} \ mathrm {H}} ^ {-} + \ mathrm {HOO } \ cdotp + {\ mathrm {H}} ^ {+} $$(7)$$ \ mathrm {RhB} + \ mathrm {OH} \ cdotp + \ mathrm {HOO} \ cdotp =\ mathrm {Oxidized} \ \ mathrm {product} $$(8)励起された電子はH 2 と反応します O 2 、電子正孔がH 2 を酸化している間にOH・ラジカルを生成します O 2 、HOO・ラジカルを生成します。方程式から推測されるように、より多くの電子正孔対が生成されるほど、より多くのラジカルがシステムに関与し、最終的には分解速度が上昇します。フォトフェントンのような不均一系触媒の場合、CuO NRアレイは、照射時に生成される電子正孔対によって反応を促進します。 CuOとH 2 のエネルギー準位の架橋領域 O 2 VBがH 2 を引き付けている間、CBの電子正孔対の傾向を示した O 2 それぞれHOO・およびOH・ラジカルを生成します。より低い活性化エネルギーを持つ触媒の関与によって生成される代替反応メカニズムは、より大きな速度定数 k と呼ばれます 、これは化学反応の律速因子になりました。バンドプロファイルの変化により、電子正孔対の分離という現象が強化され、反応の電子正孔対の寿命が長くなります。 TiO 2 のさまざまなフェーズ間 、アナターゼ相の間接バンドギャップは、ルチル相およびブルッカイト相の直接バンドギャップよりも長い光励起電子および正孔の寿命を示すため、アナターゼ相はヘテロ接合に適用するのに非常に適しています。また、光生成された電子と正孔の有効質量が最も軽く、より高い性能でより良い電流輸送に貢献しました[60]。これが、ルチル相が現れると分解速度が低下する理由です。 TiO 2 の厚さの増加 追加ファイル1に示すように、薄膜は光分解性能に影響を与えません。図S3、厚さ100nmのTiO 2 薄膜は、p-nヘテロ接合の十分に発達した空乏ゾーンを形成するのに十分な厚さです。さらに、染料分解のための異なる触媒間の比較を表1に示します。ここで、当社の触媒は、少量のCuO / TiO 2 で優れた光触媒性能を示します。 NRアレイヘテロ構造。
<図>結論
要約すると、高アスペクト比のTiO 2 AAOテンプレートでe-gun蒸着と電着を利用して合成された薄膜キャップCuONRアレイは、優れたフォトフェントンのような触媒特性を示しました。黒銅鉱相を含むCuONRは、400°Cで5時間アニーリングした後に得られました。 TiO 2 のアナターゼ相 400°Cで12時間のアニーリング後の薄膜を形成できますが、600°Cで12時間のアニーリング温度でルチル相が発生します。 CuO NRの場合、6.53μmの長さのNRはより高い効率を示しました。これは、触媒の投与量が多いことに起因する可能性があります。また、アニーリング温度を上げることによって得られるCuO NRの結晶化度が高いほど、光触媒活性が高くなります。ただし、TiO 2 のルチル相の存在 より高いアニーリング温度下では、光触媒性能が低下しました。さらに、CuO / TiO 2 のCuONRの長さが短い(1.85μm) ヘテロ接合は、UV光の侵入深さが短いため、より優れた性能を示しました。 TiO 2 の厚みが増すと CuO / TiO 2 の薄膜 ヘテロ接合では、劣化性能は影響を受けませんでした。
データと資料の可用性
この調査中に生成または分析されたすべてのデータは、この公開された記事とその補足情報ファイルに含まれています。
略語
- 3D:
-
三次元
- AAO:
-
陽極酸化アルミニウム
- AOP:
-
高度な化学酸化プロセス
- CuO / TiO 2 :
-
TiO 2 CuONRについて
- EDS:
-
エネルギー分散型分光法
- EDX:
-
エネルギー分散型X線分光法
- EELS:
-
電子エネルギー損失分光法
- FE-SEM:
-
電界放出型走査電子顕微鏡
- FFT:
-
高速フーリエ変換
- FWHM:
-
半値全幅
- HRTEM:
-
高分解能透過型電子顕微鏡
- NR:
-
ナノロッドアレイ
- RhB:
-
ローダミンB
- SI:
-
補足情報
- UV-Vis NIR:
-
紫外可視近赤外
- XRD:
-
X線回折
ナノマテリアル
- TiO2ナノ流体に向けて—パート2:アプリケーションと課題
- プラズマ化学原子層堆積によって調製されたCo3O4被覆TiO2粉末の光触媒特性
- 水素製造用の効率的な光触媒としてのZr-金属-有機フレームワークの探索
- 効率的な光電気化学水酸化のためのCdSナノ粒子修飾α-Fe2O3/ TiO2ナノロッドアレイ光アノード
- 着色された低温顔料用のCrドープTiO2の構造的および可視近赤外光学特性
- TiO2ナノチューブアレイ:ソフトハードテンプレートで製造され、電界放出性能の粒子サイズ依存性
- SドープSb2O3ナノ結晶:有機分解用の効率的な可視光触媒
- SnO2-TiO2ナノメイスアレイに基づく高性能セルフパワーUV検出器
- 陽極酸化チタンナノチューブアレイにCeO2ナノ粒子をロードするための簡単な方法
- 色素分解のための新規p-Ag3PO4 / n-BiFeO3ヘテロ接合複合材料の容易な合成と強化された可視光光触媒活性
- 可視光下での304ステンレス鋼の光生成陰極保護用のBi2Se3増感TiO2ナノチューブフィルム



