Nec-1は、RIP1を介してSh-Sy5y細胞上の二酸化チタンナノ材料によって誘発される神経毒性を軽減します
要約
二酸化チタンナノ材料は、その優れた物理化学的特性により多くの分野で適用されており、それが人の健康に潜在的な脅威をもたらします。最近、多くのin vivo研究により、二酸化チタンナノ粒子(TNP)は、さまざまな経路で曝露された後、動物の脳に輸送される可能性があることが明らかになりました。吸収されたTNPは脳に蓄積し、神経細胞を乱して脳機能障害を引き起こす可能性があります。インビトロ研究は、TNPの神経毒性を検証しました。 TNPの神経毒性の根底にあるメカニズムは不明なままです。ネクロトーシスがTNPの神経毒性に関与しているかどうかは不明です。したがって、in vitro研究を実施し、TNPがSH-SY5Y細胞に炎症性損傷を用量依存的に誘発することを発見しました。これは、ネクロスタチン-1(Nec-1)前処理によって軽減されました。受容体相互作用プロテインキナーゼ1(RIP1)がNec-1の標的であると報告されているため、siRNAによってサイレンシングしました。変異細胞と野生型細胞をTNPに曝露し、炎症性損傷を評価しました。 RIP1発現のサイレンシングは、TNP曝露によって誘発される炎症性損傷を抑制しました。まとめると、Nec-1はRIP1を介してTNPの神経毒性を改善します。ただし、TNPの神経毒性とRIP1の相関関係を包括的に評価するには、さらに多くの研究を実施する必要があります。
はじめに
その優れた物理化学的性質により、二酸化チタンナノ材料は合成され[1]、化粧品[2]、産業分野[3、4]、医療分野[5]などのさまざまな目的に広く使用されています。しかし、この広範な使用は、人間の健康に大きな脅威をもたらす可能性があります[6]。一度暴露されると、二酸化チタンナノ粒子(TNP)の大部分は、吸入と摂取によって人体に侵入します[6]。呼吸器系[7]、消化器系[8]、および心臓血管系[9]はすべて、吸収されたTNPによって中断される可能性があります。同様に、中枢神経系の最も重要な部分である脳も、循環中のTNPが血液脳関門を通過する可能性があり、吸入されたNPが嗅覚経路を介して脳に輸送される可能性があるため、妨害される可能性があります[10]。 。 TNPが脳に入ると、そこに蓄積して脳に損傷を与え、機能障害を引き起こす可能性があります。脳への損傷は通常不可逆的で深刻であるため、損傷の潜在的な原因を調査する必要があります[11]。
TNP曝露と脳疾患との関連を調査した疫学研究はありませんが、多くのinvivoおよびinvitro研究でTNPの神経毒性が確認されています[12]。さらに、主な焦点は、根底にあるメカニズムを明らかにするための研究にありました。この目的のために、我々は以前にTNPの神経毒性の現在知られている分子メカニズムをレビューし、アポトーシスやオートファジーなどのプログラム細胞死(PCD)プロセスがTNPの神経毒性に関係していることを発見しました[13]。
調節性壊死とも呼ばれるネクロトーシスは、別の種類のPCDです。カスパーゼ依存性であるアポトーシスとは異なり、ネクロトーシスは受容体相互作用プロテインキナーゼ1/3(RIP1 / RIP3)依存性です。活性化されたRIP1はRIP3を動員してネクロトーシスを形成し、ネクロトーシスを開始する混合系統キナーゼドメイン様タンパク質(MLKL)を活性化します[14]。ネクロトーシスは細胞死と神経炎症を調節する可能性があり[15、16]、どちらもTNPの神経毒性に関与しています。したがって、ネクロトーシスはTNPによって引き起こされる神経毒性に関係していると仮定しました。
私たちの仮説をテストするために、TNPの神経毒性におけるネクロトーシスの役割を調査するためにinvitro研究を実施しました。この研究では、TNP曝露後に、細胞生存率、LDH漏出、および炎症性サイトカイン(TNF-α、IL-1β、IL-6、およびIL-8)を測定しました。まず、SH-SY5Y細胞をさまざまな濃度のTNPで培養しました。第二に、細胞は、ネクロトーシスの強力な阻害剤であるNec-1の有無にかかわらずTNPに曝露されました。第三に、Nec-1によって抑制できるRIP1遺伝子発現は、siRNAを使用してサイレンシングされ、その後、変異細胞と野生型細胞がTNPで処理されました。この研究は、TNPの神経毒性の根底にある分子メカニズムの包括的な理解に光を当てます。
結果
TNPは細胞生存率を阻害します
SH-SY5Y細胞に対するTNPの細胞毒性を検証するために、最初にCCK8アッセイを使用して細胞生存率を評価しました。細胞は、5〜160μg / mLの範囲のTNP濃度で、24、48、および72時間培養されました。図1に示すように、細胞生存率は、24時間の曝露後、5、10、20、および40μg/ mLで処理された細胞では変化しませんでした。細胞を48時間および72時間処理した場合、細胞生存率は5μg/ mLグループ( p )でのみ変化しませんでした。 =48時間で0.4507および p =72時間で0.1002)。さらに、細胞生存率は、48( p )後に80μg/ mLのTNPで処理された細胞で劇的に低下しました。 =0.0007)および72時間( p =0.0008)。これらの結果に基づいて、TNPは用量および時間に依存して細胞生存率を低下させたと結論付けました(データは示していません)。これは、長期暴露がより毒性が高いことを示しています。
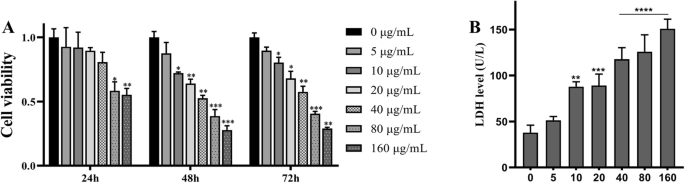
24、48、および72時間でのSH-SY5Y細胞の細胞生存率、および72時間でのLDH漏出に対する、さまざまな濃度のTiO2-NP曝露。 (対照群と比較して、 * p <0.05、 ** p <0.01、 *** p <0.001、 **** p <0.0001)
TNPは膜の完全性を損なう
ネストでは、72時間の曝露後の膜の完全性に対するTNPの毒性効果を分析しました。膜の完全性は、LDH漏出を測定することによって評価されました。図1bに示すように、LDHレベルは、5μg/ mLを超える用量のTNPで処理された細胞で有意に増加しました。 40、80、および160μg/ mL( p )で処理した細胞でLDH産生の増加が観察されました。 <0.0001)。これらの結果は、TNPが用量依存的にLDHレベルを上昇させることを示唆しており、これはCCK8アッセイと同様でした。
TNPの曝露は炎症を促進します
TNP曝露後の炎症反応をELISAを使用して分析した。細胞をさまざまなTNP濃度で72時間処理した後、TNF-α、IL-1β、IL-6、およびIL-8のレベルを測定しました。図2に示すように、IL-8分泌はすべてのTNP処理細胞でアップレギュレーションされました。 TNF-α、IL-1β、IL-6、およびIL-8のレベルは、5μg/ mL( p )を超える用量で処理された細胞で均一に上昇しました。 <0.01)。さらに、炎症は、10μg/ mLグループ( p )より高い用量で処理された細胞で有意に高かった。 <0.0001)。全体として、TNPは用量依存的に炎症を増強しました。
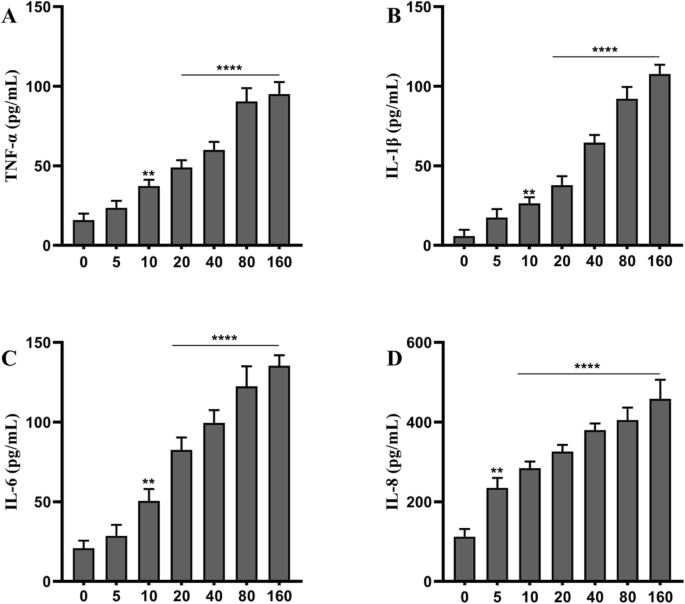
72時間でのSH-SY5Y細胞の炎症に対する異なる濃度のTiO2-NP(μg/ mL)曝露。 (対照群と比較して、 **** p <0.0001)
我々の結果は、TNPが用量依存的に炎症性損傷を誘発したことを示した。以下の実験では、TNPの神経毒性におけるネクロトーシスの役割を調査するために、80μg/ mLのTNP濃度と72時間の曝露期間を採用しました。
Nec-1の併用治療はTNPの神経毒性を阻害します
炎症性損傷におけるネクロトーシスの役割を分析するために、細胞をNec-1(ネクロトーシス阻害剤)とTNPで同時処理しました。図3aに示すように、SH-SY5Y細胞はTNPまたはTNP + Nec-1(1、5、10、15、または20μM)に曝露され、Nec-1がTNPによって誘発される減少を劇的に改善することがわかりました。細胞生存率(10、15、20μM)( p <0.0001)。 15μMおよび20μMで処理したグループの細胞生存率は、10μMで処理したグループの細胞生存率よりも高くなかったため(p =0.6643および p =0.6292)、細胞を10μMのNec-1で共処理して、膜の完全性への影響を分析しました。
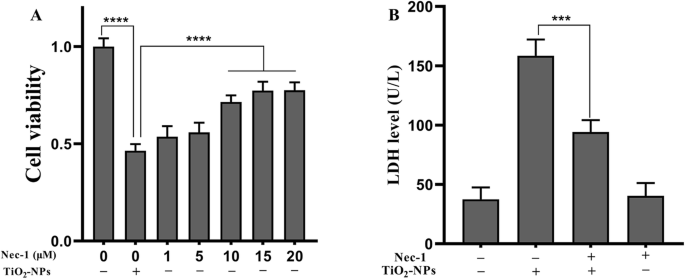
TNP曝露後の細胞生存率とLDHに対するNec-1の効果。 ( *** p <0.001、 **** p <0.0001)
TNPsまたはTNPs + Nec-1で細胞を培養した後、TNPs + Nec-1グループのLDHレベルはTNPs単独グループのLDHレベルよりもはるかに低いことがわかりました( p =0.0005)。さらに、Nec-1単独での治療はLDH漏出を増加させませんでした( p =0.9878)。
結論として、10μMのNec-1はTNPの細胞毒性を効果的に阻害でき、細胞に対して毒性はありませんでした。
Nec-1の抗炎症能力を分析するために、細胞をTNPまたはTNP + Nec-1とともに培養しました。図4に示すように、TNF-αの産生( p =0.003)、IL-1β( p =0.0013)、IL-6( p <0.0001)、およびIL-8( p =0.0004)TNPs + Nec-1グループの方がTNPsグループよりも有意に低かった。
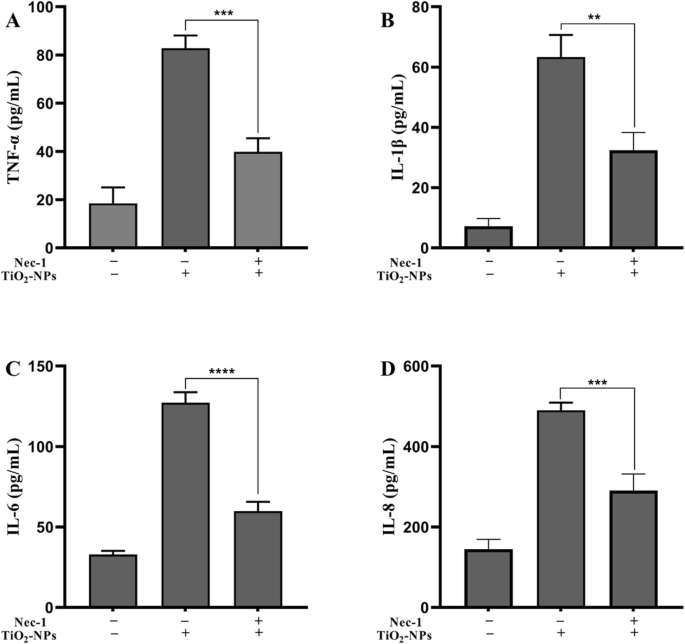
TNP曝露後の炎症に対するNec-1の効果。 ( ** p <0.01、 *** p <0.001、 **** p <0.0001)
これらの結果は、Nec-1がTNP曝露によって誘発される炎症反応を軽減できることを示唆しています。
RIP1をサイレンシングすると、TNPによって引き起こされる炎症性傷害が軽減されます
Nec-1がRIP1を介してTNPによって誘発された炎症性損傷を無効にしたかどうかを判断するために、siRNAを使用して細胞のRIP1発現を効果的に抑制しました(図5、 p <0.0001)。次に、変異型および野生型細胞へのTNP曝露後の炎症性損傷を測定しました。図6aは、TNPs + si-RIP1グループの細胞生存率がTNPs + si-NCグループの細胞生存率よりも著しく高かったことを示しています( p =0.0002)。 LDH産生(図6b、 p <0.0001)およびTNF-αのレベル( p <0.0001)、IL-1β( p =0.0001)、IL-6( p <0.0001)、およびIL-8( p =0.0001)(図7)TNPs + si-RIP1グループでは、TNPs + si-NCグループよりも劇的に低かった。これらの結果は、TNPがRIP1を介して炎症性損傷を促進したことを示しています。
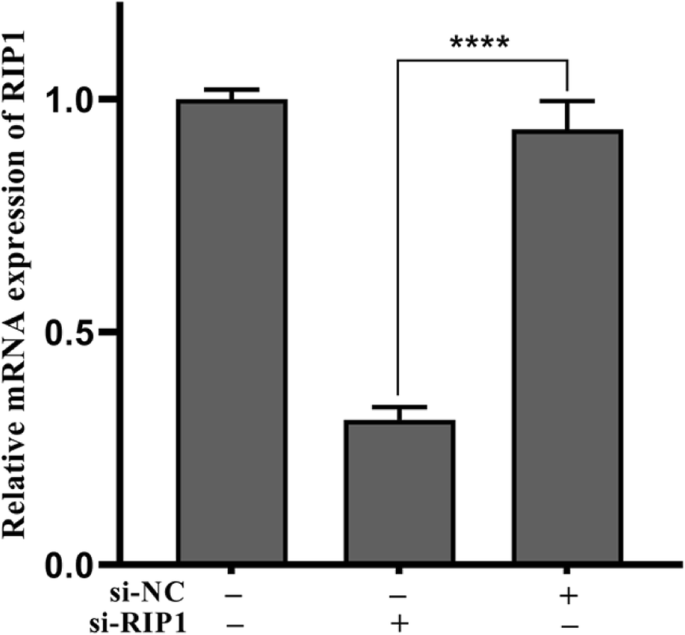
si-RIP1でトランスフェクトされたSH-SY5Y細胞後のmRNA発現。 ( **** p <0.0001)
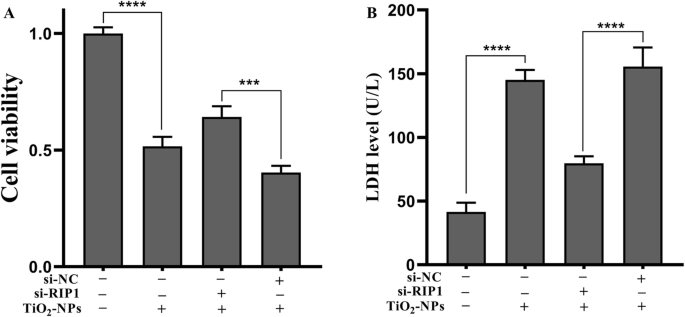
変異体および野生型細胞がTNPに曝露された後の細胞生存率およびLDH漏出。 ( *** p <0.001、 **** p <0.0001)
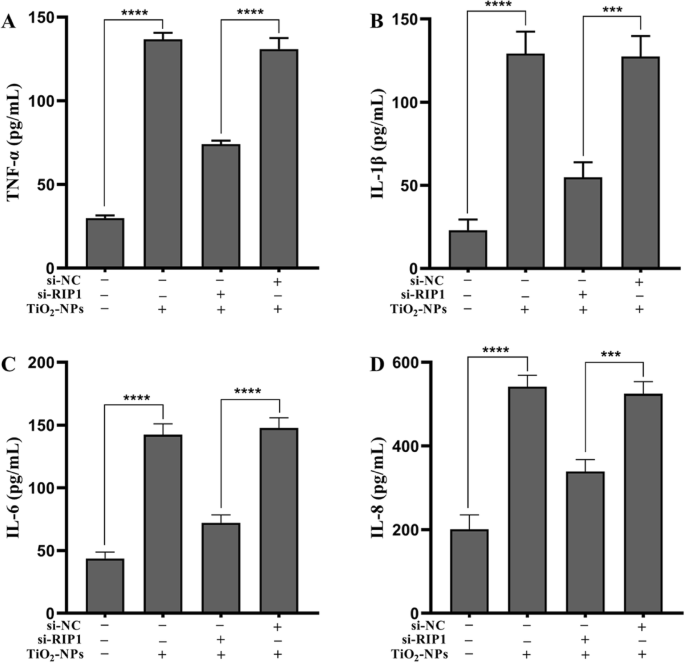
変異細胞および野生型細胞がTNPに曝露された後の炎症。 ( *** p <0.001、 **** p <0.0001)
ディスカッション
この研究では、TNPへの曝露がSH-SY5Y細胞に用量依存的に細胞毒性を誘発し、ネクロトーシスがTNPの神経毒性に関与していることを発見しました。ネクロトーシスの役割を調べるために、Nec-1(強力なネクロトーシス阻害剤)の有無にかかわらずTNPに細胞を曝露し[17、18]、細胞生存率、LDH漏出、および炎症性サイトカインのレベルを測定しました。私たちのデータは、Nec-1の併用治療がTNPによって誘発される炎症性損傷を軽減できることを示唆しています。 Nec-1はRIP1活性を抑制することでその効果を発揮することが研究により示されているため、細胞にsi-RIP1をトランスフェクトして、RIP1がNec-1の保護効果に関与しているかどうかを調べました。変異細胞と野生型細胞をTNPで処理し、炎症性損傷を評価しました。これは、si-RIP1グループの細胞生存率がsi-NCグループよりも高く、LDH漏出および炎症性サイトカインのレベルがTNPへの曝露後のsi-NCグループよりもsi-RIP1グループの方が低かったことを示しています。 。結論として、本研究は、ネクロトーシスがTNPによって誘発される細胞の炎症性損傷に関与していることを初めて明らかにしました。
我々は、invitro研究でTNPの神経毒性を再確認しました。 SH-SY5Y細胞をさまざまな濃度のTNPにさまざまなインキュベーション時間曝露した後、CCK8アッセイを使用して細胞生存率を評価しました。図1aに示すように、TNPへの曝露は用量依存的に細胞生存率を低下させました。 48時間および72時間の曝露後、80および160 TNPsグループの細胞生存率は、コントロールグループと比較して劇的に減少しました( p <0.001)。細胞毒性をさらに確認するために、LDHリークも測定しました。図1bのデータは、72時間の曝露後にLDH産生が用量依存的に増加し、40、80、および160グループのLDHレベルが対照グループよりも著しく高かったことを明らかにしました( p <0.0001)。以前の研究では、神経炎症はTNPへの曝露によって促進されることが示されているため[19]、TNF-α、IL-1β、IL-6、およびIL-8のレベルも測定されました。図2は、これら4つの炎症性サイトカインのレベルが対照群と比較して有意にアップレギュレーションされ、20〜160μg / mL( p )で治療された群で劇的に高かったことを示しています。 <0.0001)。まとめると、我々の結果は、TNPが用量依存的に神経毒性を誘発する可能性があることを示しており、これは以前の研究と一致している。 TNPは神経細胞に吸収され、増殖を阻害する可能性があります[20、21、22]。さらに、TNP曝露は、細胞生存率を低下させ、用量依存的にLDH漏出を促進する可能性があります[23、24、25、26、27]。
ネクロトーシスがTNPによって引き起こされる神経毒性に関与しているかどうかを明らかにするために、細胞をNec-1で同時処理しました。細胞をNec-1の有無にかかわらず示された濃度のTNPで処理した後、細胞生存率、LDH漏出、および炎症を評価しました。図3aは、TNP曝露後の細胞生存率の低下が、10μMのNec-1との同時処理によって有意に抑制されたことを示しています。一方、図3bは、10μMのNec-1で処理してもLDHレベルが上昇せず、TNP + Nec-1グループで処理した細胞のLDHレベルがTNP単独グループよりも劇的に低いことを示しています。次に、TNPによって誘発される炎症に対するNec-1との併用治療の効果を測定しました。図4は、TNF-α、IL-1β、IL-6、およびIL-8のレベルが、TNP + Nec-1で処理された細胞で著しく低かったことを示しています。これらの結果は、Nec-1が細胞を死や炎症過程から保護できることを再確認しました[28、29]。
最後に、RIP1はNec-1のターゲットであるため、RIP1がTNPの神経毒性を調節できるかどうかを評価しました。 RIP1の発現をサイレンシングして変異細胞を構築しました(図5)。図6および図7のデータは、TNP曝露後、細胞生存率が高く、LDH、TNF-α、IL-1β、IL-6、およびIL-8レベルがsi-RIP1グループよりも低いことを明らかにしました。これは、TNPがRIP1を介して細胞毒性を促進することを示唆しているsi-NCのそれです。同様に、いくつかの研究は、RIP1が細胞死と炎症過程の両方を調節できることを明らかにしました[30、31]。
Nec-1がネクロトーシスシグナル伝達経路を抑制することによりTNPの神経毒性を軽減できることを初めて報告しましたが、私たちの研究にはいくつかの制限があります。第一に、ナノサイズの材料の細胞毒性はバルクのものとは異なり、表面特性によって大きく影響を受ける可能性があります[32]。これは、Sebastiánetal。によって発見された細胞生存率の増加の反対の結果を説明する可能性があります。 [33]。したがって、細胞増殖、膜の完全性、酸化ストレス、炎症、ミトコンドリア機能、細胞周期、細胞骨格、エピジェネティクスなどの複数の側面から、被験者のナノ毒性を包括的に評価することが不可欠です。第二に、RIP1はRIP3を動員して、MLKLの重要な活性化因子である機能性ネクロソームを形成し、ネクロトーシスを開始することができます[34]。 RIP3 / MLKLがTNPの神経毒性に関与している可能性があると仮定します。これは、将来の研究で調査する必要があります。さらに、RIP3 / MLKLとTNPの神経毒性との関連も評価する必要があります。第三に、活性酸素種(ROS)は、TNPの神経毒性の根底にある主要なメカニズムとして[35、36]、RIP1の上流シグナルであると報告されています[37]。したがって、ROSがTNPの神経毒性においてRIP1の上流にあるかどうかをさらに議論する必要があります。第4に、慢性細胞毒性を評価するために、細胞を非毒性濃度(TNP <5μg/ mL)に長期間(72時間以上)曝露する必要があります。第5に、より多くの神経細胞株と初代ヒトおよび動物の神経細胞におけるTNPの神経毒性におけるネクロトーシスの役割を評価する必要があります。
結論
私たちの研究は、TNPによって引き起こされる神経毒性に関与する別のプログラム細胞死メカニズムとしてネクロトーシスを明らかにしました。この研究では、TNPがSH-SY5Y細胞に用量依存的に炎症性損傷を誘発する可能性があり、Nec-1(ネクロトーシスの強力な阻害剤)の併用治療がこれらの有害な影響を改善できることを発見しました。 Nec-1の標的であるRIP1は、si-RNAによってサイレンシングされ、TNPへの曝露によって誘発される炎症性損傷を効果的に軽減しました。結論として、Nec-1は、RIP1経路を標的とすることにより、TNP曝露によって誘発されるSH-SY5Y細胞の炎症性損傷を抑制しました。 TNPの神経毒性に関与するRIP1の上流および下流のシグナル伝達経路をさらに評価する必要があります。
材料と方法
TNPの準備と細胞培養
以前にTNPの特性を評価し、以前に公開された手順[38]に従って準備しました。簡単に説明すると、TNPをRPMI 1640に溶解して、5、10、20、40、80、および160μg/ mLのさまざまな濃度にしました。処理前に粒子が凝集しないように、TNP溶液を室温で滅菌および超音波処理(300 W、10分)しました。 TNPに曝露されていない培地中の細胞が対照群として機能した。中国科学アカデミー上海生命科学研究所のセルバンクから購入したSH-SY5Y細胞を、10%ウシ胎児血清(Gibco、製品)を添加したRPMI 1640培地(HyClone、Logan、UT、USA)で培養しました。サーモフィッシャーサイエンティフィックのライン、ウォルサム、マサチューセッツ州、米国)、100 U / mLペニシリン、および100μg/ mLストレプトマイシン、37°C、5%CO 2 の加湿インキュベーター 。
細胞生存率とLDH漏出アッセイ
細胞生存率は、細胞計数キット-8(CCK8。Dojindo、カタログ番号CK04)を使用して測定しました。簡単に言うと、1×10 4 SH-SY5Y細胞を96ウェルプレートに入れ、37°C(5%CO 2 )のインキュベーターで培養しました。 )TNPへの曝露前に24時間。次に、細胞をさまざまな濃度(0、1.25、2.5、5、10、20、40、および80μg/ mL)のTNPとともにさらに24時間インキュベートしました。処理後、細胞をCCK-8とともにさらに2時間インキュベートしました。次に、96ウェルプレートをマイクロプレートリーダー(BioTek、Winooski、VT、USA)に配置することにより、450 nmで光学密度(OD)を測定しました。各グループの細胞生存率は、パーセンテージで表され、(ODtreatment-ODblank)/(ODcontrol-ODblank)×100%として計算されました。
膜の完全性は、市販のキット(Nanjing Jiancheng Bioengineering Institute、中国)によって測定されました。 SH-SY5Y細胞をさまざまな濃度のTNPに72時間曝露した後、LDH分泌を製造元の指示に従って分析しました。
炎症反応
ELISAを適用して、SH-SY5Y細胞によって産生されるTNF-α、IL-1β、IL-6、およびIL-8のレベルを測定しました。簡単に説明すると、SH-SY5Y細胞をTNPに72時間曝露し、製造元の指示(Elabscience Biotechnology Co.、Ltd。)に従って分析のために上清を収集しました。
siRNAトランスフェクション
メーカーのプロトコルに従って、100 nM濃度のsi-RIP1またはネガティブコントロールsiRNA(si-NC)を、Lipofectamine2000を使用して細胞にトランスフェクトしました。siRNAによる遺伝子サイレンシングの効率はリアルタイムPCRで推定されました。
リアルタイムPCR
さまざまな濃度のTNPに曝露された細胞のRNAは、RNAqueousキット(Ambion Inc.、Austin、TX、USA)を使用して、製造元の指示に基づいて分離されました。 RIP1の相対的な発現はリアルタイムPCRによって測定されました。 RIP1の相対的なmRNAレベルはβ-アクチン発現に対して正規化されました。
統計分析
SPSS 11.0ソフトウェア(SPSS Inc.、シカゴ、イリノイ、米国)を使用してデータを分析しました。一元配置分散分析を使用して、グループの平均を比較しました。 p <0.05は統計的に有意であると見なされました。
データと資料の可用性
原稿から入手できます。
略語
- TNP:
-
二酸化チタンナノ粒子
- Nec-1:
-
ネクロスタチン-1
- RIP:
-
受容体相互作用プロテインキナーゼ
- MLKL:
-
混合系統キナーゼドメイン様タンパク質
- ROS:
-
活性酸素種
ナノマテリアル



