ZnOナノロッドへのMgのドーピングにより、分子ドッキング分析による光触媒分解と抗菌力の向上が実証されました
要約
共沈法を使用して、さまざまな濃度のMgドープZnOナノロッド(NR)を調製しました。この研究の目的は、ZnOの光触媒特性を改善することでした。 ZnOの構造、相構成、官能基の存在、光学特性、元素組成、表面形態、および微細構造に対するMgドーピングの影響を、それぞれXRD、FTIR、UV-Vis分光光度計、EDS、およびHR-TEMで評価しました。調製されたサンプルから得られた光吸収スペクトルは、ドーピング時に青方偏移の証拠を示した。 XRDの結果から、Mgを添加すると結晶子サイズが徐々に減少するナノコンポジットの六方晶ウルツ鉱相が明らかになりました。 PL分光法は、トラップ効率と電子正孔再結合挙動を伴う電荷キャリアの移動を示し、HR-TEMは層間のd間隔を推定しました。 ZnOの界面での化学結合、振動モード、および官能基の存在は、FTIRおよびラマンスペクトルによって明らかになりました。この研究では、メチレンブルーとシプロフロキサシン(MBCF)の混合物を分解することにより、調製されたNRの光触媒、超音波触媒、および超音波光触媒の性能を体系的に調査しました。実験結果は、改善された分解性能が、MgをドープしたZnONRによって示されたことを示唆した。この研究で合成された製品は、廃水処理に有益で有望な光触媒であることが証明されると信じています。結論として、MgをドープしたZnOはかなりの量( p <0.05)グラム陽性(G + ve)細菌と比較したグラム陰性(G-ve)に対する有効性。 EのDHFR(結合スコア:− 7.518 kcal / mol)、DHPS(結合スコア:− 6.973 kcal / mol)、およびFabH(− 6.548 kcal / mol)に対するMgドープZnONRのインシリコ分子ドッキング研究。コリ 殺菌活性の背後にある可能性のあるメカニズムとして、与えられた酵素の阻害を予測しました。
はじめに
水中の有機汚染物質排出物と食品中の感染性細菌汚染物質は、私たちの周囲の健康的な環境を維持するために克服する必要のある主要な課題になりつつあります[1、2]。例として、フレキシネル赤痢菌によって引き起こされる感染症 バクテリアは、食べ物や飲み物の汚染により、年間で約150万人が死亡していると主張しています[3]。水生環境に放出された染料に存在する毒性および発がん性物質は、環境と公衆衛生に深刻なリスクをもたらします[4]。これらの染料は、淡水の透明度を低下させる働きをするシアノバクテリアや藻類などの水生生物の光合成活性にも影響を与えます[5]。
物理的、生物学的、化学的方法、および廃水から染料を除去するための新しい技術を開発するために、無数の実験的研究が行われてきました。これまで、限外ろ過膜、吸着と沈殿[6]、生物学的アプローチなどの物理的方法が研究されてきました。さらに、生分解手順は、放電中に存在するバクテリアを根絶するための可溶性有機物分解に使用されてきましたが、化学的方法は、光化学的脱色、塩素化、およびオゾン処理で構成されています[7]。化学的沈殿、吸着、凝固、分離などの従来の廃水処理方法は、ある地点から別の地点への染料の移動を必要とし、二次汚染を引き起こすため、適切な技術ではありません[8]。したがって、研究者は、有機汚染物質を無害な化合物に直接分解する環境に優しい処理技術を探しています[9]。
最近、半導体ナノ粒子(NP)の存在下での光触媒および超音波触媒の高度な酸化プロセス(AOP)が、その化学的安定性、費用効果、および非毒性のために多くの考慮を集めています[10、11、12]。光触媒は、光照射による半導体光触媒の電荷キャリア生成を伴う、改良された酸化方法です。光生成された電荷担体は酸化還元反応に関与し、水から汚染物質を除去します[13、14]。いくつかの研究は、OH ・ ラジカル種は、光化学反応中に光触媒表面に蓄積し、さまざまな有機色素の分解を引き起こします。今日では、OHの生産の増加の結果として ・ イオン、光触媒(PCA)と超音波照射の相乗効果、いわゆるソノフォト触媒(SPCA)は、ナノ触媒の分解効率を高めるようです。実際、SPCAは、毒性、危険性、毒性のある水中の化合物の分解速度に有益な影響を与えることが示されています[15]。現在、汚染された水の処理に金属酸化物NPを使用することは、その費用便益、環境への配慮、安定性、およびリサイクル性のために、研究者の関心を集めています[16、17]。さらに、TiO 2 などのバンドギャップの広い無機半導体 、WO 3、 ZrO 2 とZnOは、色素を分解する光誘起触媒酸化還元プロセスで成功することが証明されています[18、19]。よく知られているワイドバンドギャップ(Eg =3.37eV)半導体であるZnOは、PCAアプリケーションのアクティブな表面欠陥サイト、卓越した物理化学的安定性、高い酸化還元電位、励起子の大きな結合エネルギー(〜60 meV)により、並外れたポテンシャルを示します。安価で無毒であることに加えて[20,21,22,23]。さまざまな金属の中で、マグネシウム(Mg)は、光学Eg工学によるZnOナノ材料を合成するための最も魅力的なドーパントです。 ZnO中のMgの置換は、以下の要因のために好まれます。 (i)格子定数は不変、(ii)イオン半径は非常に近い(Mg +2 =0.72ÅおよびZn +2 =0.74Å)、(iii)ZnOへのMgの高い溶解度、(iv)ドープされたZnOは、EgおよびUV-Vis発光強度の増加をもたらし、オプトエレクトロニクスアプリケーションに役立ちます。さらに、MgをドープしたZnOは、その広い光学バンドギャップの結果として、色素分解の効果的な光触媒として機能し、抗菌剤を促進することができます[23]。
この研究では、共沈法を採用して、触媒および殺菌活性のための効率的なMgドープZnOナノコンポジットを合成しました。準備されたサンプルは、詳細な分析のために、XRD、HR-TEM、EDS、FTIR、UV-Vis、およびラマン分光法によって特性評価されました。調製したサンプルの触媒活性は、メチレンブルーとシプロフロキサシン(MBCF)の混合物の分解について研究され、抗菌活性は、G + veおよびG-ve細菌に対してテストされました。さらに、分子ドッキング研究は、葉酸生合成経路およびβのジヒドロ葉酸レダクターゼ(DHFR)およびジヒドロプテロイン酸シンターゼ(DHPS)に対して実施されました。 -脂肪酸生合成経路のケトアシル-アシルキャリアタンパク質シンターゼIII(FabH)。
メソッド
現在の研究は、MgをドープしたZnOナノロッドの分子ドッキング分析により、光触媒分解と抗菌力を向上させることを目的としていました。
資料
硝酸亜鉛四水和物(Zn(NO 3 ).4H 2 O、99.0%)、塩化マグネシウム六水和物(MgCl 2。 6H 2 O、99.0%)および水酸化ナトリウム(NaOH、99.0%)はSigma-Aldrichから入手しました。
Mgをドープした酸化亜鉛(ZnO)の合成
一定量のZnOナノ材料にドープされた様々な濃度のMgを共沈法で合成した。 0.5 MのZn(NO 3 ).4H 2 O溶液をZn前駆体として使用し、MgCl 2 を注ぐことにより、所望の量(2、4、6、および8 wt%)のドーパントを添加しました。 ソリューションに。調製した溶液を脱イオン水(DI水)中で80°Cで90分間撹拌し、撹拌溶液にNaOH(0.1 M)をゆっくりと加えることでpHを約12に維持しました。得られた沈殿物を4000rpm(20分)で遠心分離し、100℃で24時間乾燥させた後、粉砕して微粉末を得た(図1)。
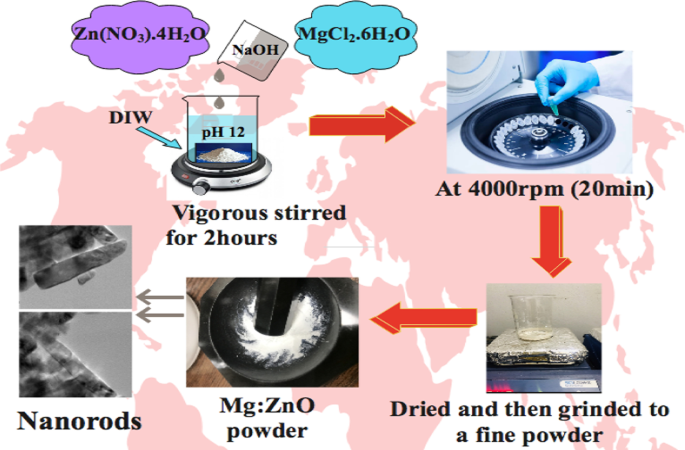
MgをドープしたZnOナノロッドの合成戦略の概略図
マテリアルの特性
製品の相構成と構造を特定するために、CuKアルファ線(λ=1.541874Å)を備えたPANanalytical X-pert PRO X線回折計-XRDを2θ°の範囲(20°–80°)で操作しました。 。 PerkinElmer分光計を使用した官能基の存在は、FTIRを介して検証されました。 UV-Vis分光光度計を使用して、光学特性を観察しました(Genesys 10S分光光度計)。 300〜500 nmバンドのフォトルミネッセンス(PL)発光スペクトルを取得するために、JASCOFP-8200分光蛍光光度計を使用しました。 INCA EDSソフトウェアを使用したエネルギー分散型X線分光法(EDS)により、元素組成が推定されました。走査型電子顕微鏡(SEMモデルJEOL JSM 6460LV)と高分解能透過型電子顕微鏡(HR-TEMモデルJEOL JEM 2100F)を使用して、合成されたサンプルの形態と微細構造を決定しました。
光触媒、超音波触媒、超音波光触媒活性
MBCF分解の超音波触媒活性(SCA)および超音波光触媒活性(SPCA)は、固定周波数〜35 kHzで動作するZnOおよびMg:ZnO触媒の超音波浴でテストされました。同様に、可視光照射下で、MBCFに対するZnOおよびMg:ZnOナノ触媒の光触媒分解がテストされています。各実験では、50 mLのモデル色素に光触媒(10 mg)を懸濁し、溶液を10〜15分間暗所に置いて、吸着-脱着平衡を達成しました。可視光(光触媒-PCA)、超音波処理器(ソノカタリシス-SCA)、および可視光照射と超音波処理(ソノ光触媒-SPCA)の組み合わせを、懸濁溶液の下に系統的に配置しました。一定の時間間隔での吸収分析のために、曝露中に3mLの懸濁液を収集しました。 MBCFのλmax=670 nmの差を測定することにより、得られた色素成分を観察しました。ナノ触媒の存在下でのMBCFの分解により、青色の溶液は時間の経過とともに退色しました。最後に、分解度(Ct / Co)を評価しました。ここで、Ctは一時的な染料濃度、Coは初期染料濃度です。各サンプルの劣化率も、式%Degradation =\(\ frac {{\ left({Co --Ct} \ right)}} {Co} \)×100を使用して計算されました。
Sの分離と識別。アウレウス および E。コリ
サーフフィールド乳房炎でテストされた乳製品(牛)のミルクサンプルは、さまざまな農場から収集されました。インキュベートしたサンプル(5%ヒツジ血液寒天培地で培養)に、G + ve S用のMSA(マンニット食塩寒天培地)およびMA(マッコンキー寒天培地)をストリークしました。アウレウス およびG-ve E。コリ 、それぞれ(pH〜7)。特徴的なコロニーは、生化学的分析(カタラーゼおよびコアグラーゼテスト)および形態素解析(グラム染色)によって特定されました。
抗菌作用
合成されたNRの殺菌性能は、1.5×108 CFU / mLの Sを拭くことによる寒天ウェル拡散アプローチを採用したG-veおよびG + ve細菌株で調べられました。 アウレウス および E。コリ それぞれMSAとMAで分離します。綿棒で拭いたMSAおよびMAペトリ皿に滅菌コルクボーラーを使用して、直径6mmのウェルを形成しました。ネガティブコントロール(DI水)およびポジティブコントロール(シプロフロキサシン)と比較して、異なる濃度のMg:ZnO NR(0.5 mg /50μl)および(1.0 mg /50μl)を使用しました。用量を含むペトリ皿を一晩インキュベートし(37°C)、ノギスで阻害ゾーンの直径を測定することにより、NRの抗菌性能を記録しました。 SPSS 20を使用した一元配置分散分析(ANOVA)により、阻害ゾーンに関して統計的に測定された有効性が有意であると見なされました。
分子ドッキング研究
ドープされたZnONRの抗菌活性の背後にある重要な構造的特徴を特定するための効果的なアプローチであるインシリコ分子ドッキング研究は、それらの可能なメカニズムの予測に採用されています。葉酸生合成経路の重要な酵素、すなわちβと並んでジヒドロ葉酸レダクターゼ(DHFR)およびジヒドロプテロイン酸シンターゼ(DHPS) -脂肪酸生合成経路のケトアシル-アシルキャリアタンパク質シンターゼIII(FabH)酵素は、抗生物質発見の魅力的な標的として報告されています。選択した酵素の3D構造特性は、Protein Data Bankから取得され、活性部位内にMgドープZnONRをドッキングするためのタンパク質調製ツールを使用して調製されました。
選択したターゲットのアクセッションコードは次のとおりです。2ANQ(DHFR E.coli )[24]、5U0V(DHPS E.coli )[25]および4Z8D(FabH E.coli )[26]。分子ドッキング研究は、ICM Molsoft(Molsoft L.L.C.、La Jolla、CA)ソフトウェア[27]を使用して実行され、タンパク質構造はエネルギー最小化ツールによって最適化されました。共結晶化したリガンドとともに結晶構造から水分子を除去した後、タンパク質構造の調製のために極性H原子を追加し、グリッドボックスを使用してアクティブポケットを特定しました。最後に、リガンド結合に関与する重要なアミノ酸を観察するための結合相互作用分析のために、最良のドッキング複合体を選択しました。ドッキングされた複合体の分析には、DiscoverystudioビジュアライザーとPymolを使用しました。
結果と考察
ドーパントフリーおよびドープされたZnOの構造特性と相構成は、X線回折を使用して評価されました(図2a)。 31.7°、34.5°、36.3°、47.5°、56.6°、62.9°、68.0°で観測されたピークは、回折面(100)、(002)、(101)、(102)、(110)、( 103)および(112)は、ZnOが空間群P63mcの六角形構造(JCPDS No. 361451)であることを確認しました。 2つのピークは、亜鉛-カルボキシルを含む化合物の不純物を反映しています(黒い矢印でマーク)。これらの亜鉛-カルボキシルの痕跡は、合成中にZn前駆体が他の反応物と反応したために現れた可能性があります[28]。 ZnOの結晶子サイズは、シェラーの式を使用して推定された26nmであり、これは、ドーパントの量が増加するにつれて(8重量%で)23nmまで徐々に減少した。ホスト格子への「Mg」の追加を成功させるために、3つの顕著なピーク位置(100)、(002)、および(101)面が追跡されました[23]。いくつかの研究では、Mg、Fe、AlなどのドーパントをZnOに添加すると、結晶子サイズが徐々に減少することが報告されていますが、ZnOのピークはMgをドープすると高い2θにシフトすると考えられています[29、30]。 Znイオン半径とドーパントイオンの違いによって引き起こされる圧縮応力、結晶成長の妨害、および/またはドーピング時の結晶の欠陥生成を含むいくつかの要因が、ZnO成長を抑制する可能性がある。ドープされたZnONRで観察されたピークシフトは、Mg 2+ 間のイオン半径の違いによりZnイオンを置換したMgイオンに起因する可能性があります。 (0.57Å)およびZn 2+ (0.60Å)[23、29]。

a MgドープZnOのXRDパターン、 b–d ZnOのSAEDパターン、4%、8%のMgドープZnOおよび e それぞれFTIRスペクトル
ドープされたZnOのSAEDパターンは、電子線回折のために明るいスポットを示しました。各スポットは、ブラッグ回折条件に影響を与える合成生成物の結晶構造内に見られる一連の平行面に由来します。図2b–dに示すように、ミラー指数はそれに応じて割り当てられています。パターンは、[101]ゾーン軸[31]に沿って電子ビームが投射されたZnOの六角形構造に接続された平面(002)、(100)、(101)、および(102)でインデックス付けされています。一般に、ZnOの異方性成長方向は、界面自由エネルギーと水溶解ポテンシャルの両方によって決定されます。異なる平面の成長の相対速度も成長を制御します。成長は、さまざまな平面の相対的な成長速度によっても制御されます[32]。
FTIR分析を実行して、サンプルに存在する化学結合の官能基の存在、表面化学、および振動モードを調査しました(図2e)。 400〜560cmのバンド -1 は、ZnOの形成を確認したZn–O–Zn振動モードの伸縮に指定されています。低周波数/指紋領域のバンドは、M–O並進振動(590、670 cm -1 )に起因していました。 )およびO–M–O(430 cm -1 )[33]。 Mgの濃度を増加させても、Zn-Oの吸収帯および強度に有意な変化は観察されなかった。 1651cmのバンド -1 対称C =O伸縮モードに対応します。これは、硝酸マグネシウムの負荷率の増加に伴って高度に強化されますが、約1362 cm -1 バンドは非対称C–Oストレッチモードに対応します。出発物質からの炭素が誤ってNRに組み込まれた可能性がありますが、3456 cm -1 で広い透過帯域が出現します。 表面吸着水分子のO–H伸縮に対応します[34]。
ドーピング時の吸収挙動の変化を確認するために、ドープされたサンプルとドープされていないサンプルにUV-Vis分光法を導入しました。合成されたNRのUV-Vis吸収スペクトルは、波長の関数として250〜600 nmの範囲で記録されました(図3a)。サンプルは、370〜395 nm付近で最大吸収を示し、さまざまなドーピング濃度で吸収端がより低い波長にシフトしました。ドーピング時の吸収とシフトのこの増加は、酸素欠乏、粒子サイズ効果、および粒子構造の欠陥に現れます[35]。図3aから抽出した値を使用して、ZnOの光学バンドギャップ(Eg)を計算しました(Taucプロットを使用)。これは、Mgドーピング時に3.32から3.72 eVに増加しました(図3b)[36、37]。たとえば、この青方偏移は、バースタイン-モス効果現象を支持することができます。金属酸化物法では、粒子サイズの減少により、量子閉じ込め効果(QCE)によりバンドギャップの青方偏移が生じることが報告されています。ただし、QCEだけが理由ではありません。ドーピングはまた、局所的な対称性に影響を及ぼし、バンドの構造を変化させ、光学特性に大きな変化を引き起こす格子欠陥中心を生成する可能性があります[38]。 XRD分析で前述したように、ZnOにドープされたMgは、ホスト結晶に酸素空孔を生成します。これは、システム内のドナーとして機能し、電子をCBに放出することによって正に帯電したイオンとして動作します。電子キャリアの濃度がCBの状態密度を超えると、フェルミエネルギーのレベルがCBに押し込まれます。 Zn 2+ Mg 2+ に置き換えます 両方の材料のイオン半径と電気陰性度の違いにより、電子濃度と酸素空孔が増加します。したがって、ZnOは最も縮退した半導体の1つであるため、キャリア密度の増加により、フェルミ準位が縮退半導体CBに上昇します。 。この作用により、フェルミ準位とその位置は、自由電子の集中とVBからフェルミ準位への電子の励起に依存し、その結果、自由電子の密度が増加し、バンドギャップが広がります[39]。このバースタイン-モスシフトは、MgをドープしたZnONRの観測されたEgの広がりに寄与します。
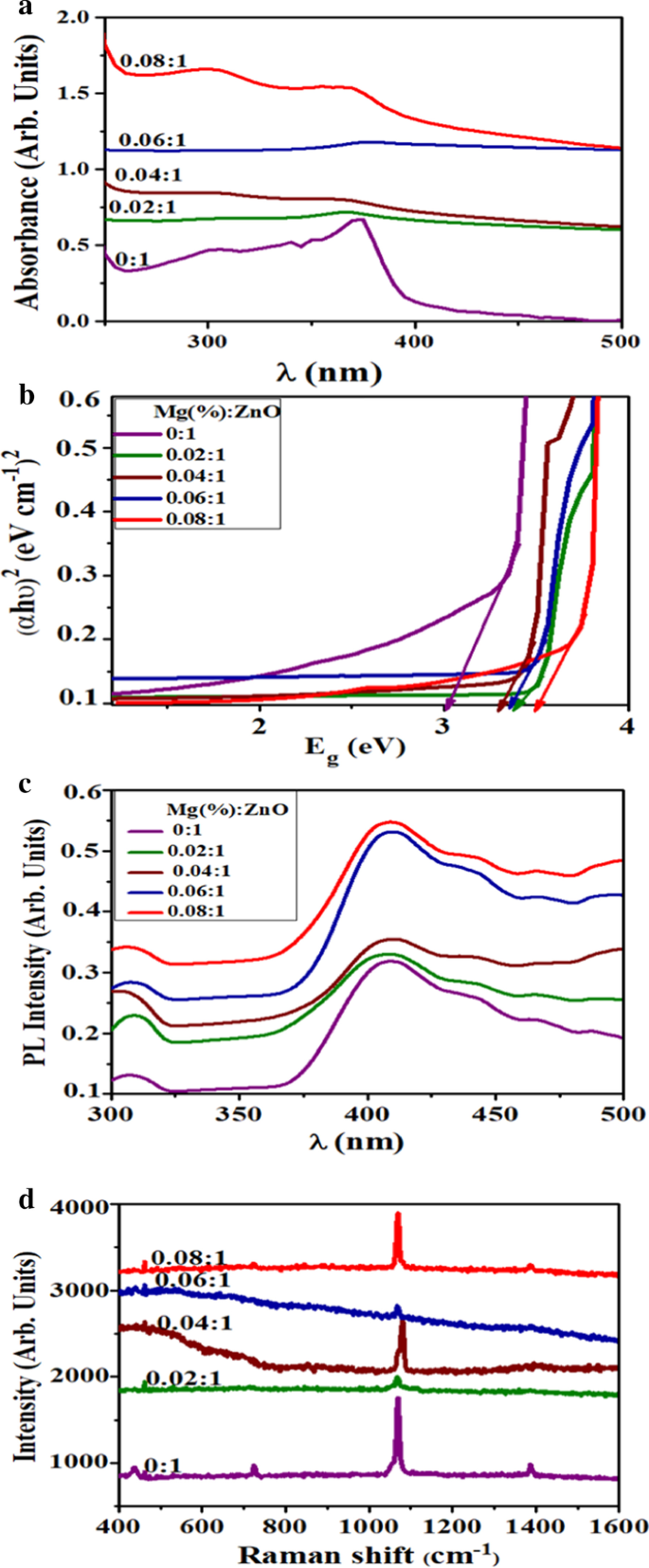
a MgをドープしたZnO、 b のサンプルの吸収スペクトル タウクプロット、 c PLスペクトルと d MgをドープしたZnOナノロッドのラマンスペクトル
PL分析は、発光スペクトルを研究することにより、不純物、遷移、およびドーパントに関するより良い情報を取得するための貴重なツールです。量子サイズの影響は、ナノスケールで半導体材料の物理的特性に影響を与えます。たとえば、ZnOは、PLから観察される量子閉じ込めの増加によって光学的挙動を変化させました[40]。 ZnOに組み込まれたさまざまな濃度のMgのPLスペクトルを、室温で励起λ〜325 nmで測定しました(図3c)。ドープされていないZnOとドープされたZnOの場合、広い深層レベルと近帯域の放出が検出されました。すべてのサンプルは、励起子の再結合に起因するUV領域での発光ピークを示しました。可視領域で観察されるピークは、O 2 などの欠陥状態(ドナー)が原因で表示されます。 欠員-V o 、Znインタースティシャル-Zn i 、亜鉛空孔からの欠陥状態(アクセプター)-V z および酸素格子間原子-O i [39]。結晶化度の増幅に伴って欠陥密度が減少するため、UV領域と可視領域のピーク強度比は、ドープされた材料の結晶品質に大きく影響されます。サンプルは、ZnOの近バンドエッジ-NBE遷移に起因する408nm付近の発光ピークを示しました[39]。 408、442、467、488 nmに見られるピークは青色の発光につながり、Zn格子間原子に起因するものは408nmに主要な紫色の発光を示します。 442、467、および488 nmで観察された弱い発光は、サンプルのさまざまな欠陥レベルを伴うドナー-アクセプター(D / A)ペアの再結合に起因します。 488 nmでの発光は、単一イオン化されたO 2 の電子によるものです。 VBに光励起された穴がある空孔[41]。 NBE発光のピークがより高いエネルギー領域に移動する一方で、幅広い深部レベルの発光の強度はドーピング時に増加しました。 NBE放出のこの青方偏移は、バースタイン-モス効果に基づいて解釈できます。 ZnOはn型材料であり、高濃度にドーピングすると、そのフェルミ準位は伝導帯の内側にシフトします。したがって、吸収はバースタインによって提案されたように青方偏移を示さなければなりません。満たされた領域は、光または熱励起をブロックします[42]。 PL強度の増加は、ドープされたサンプルで観察され、電子移動効率の低下を意味します。
ラマン散乱は、微細構造を調べ、ナノ材料の振動状態に関連する特性を分析するための高感度で非破壊的な手法です。 2つの式単位を含む原始セルを持つウルツ鉱型酸化亜鉛はC6ν空間群に配置されます。逆格子空間の原始セルに存在する光学フォノンは、既約関係から正当化されます:Гopt=1A 1 + 2B 1 + E 1 + 2E 2 ここで、B 1 ラマンサイレントモードを表し、A 1 およびE 1 極性モード(長距離クーロン力)であり、縦光学(LO)フォノンと横光学(TO)フォノンに分割されます。さらに、2周波フォノンモードE 2 (無極性)、E 2 (低)およびE 2 (高)、Zn副格子およびO 2 に対応 原子[43]。ラマンスペクトルでは、波数が高くなる方向と低くなる方向にシフトするピークは、分子間の結合長の変化に依存します。結合長の増加は、低波数へのシフトを支配し、その逆も同様です。 1300 cm -1 を超えると、これ以上高次のピークは観察されません。 (図3d)。 〜1069 cm -1 で観察される主要なピーク E 2 を表します 六角形のZnOのH(特性)モード[44]。さらに、436、723、1386 cm -1 付近にも3つの小さなピークが観察されました。 これは、高い蛍光バックグラウンドが原因で発生しました。さらに、8 wt%ドープされたZnOのラマンスペクトルはブルーシフトされました。これは、Mg 2+ の置換に起因します。 Zn 2+ 格子ダイナミクスで役割を果たすと考えられているZnO格子[45]。通常、ラマンピークシフトは、フォノン閉じ込め効果、格子ひずみ、および酸素空孔の3つの理由で発生します。 XRDおよびラマン分光法から取得したスペクトルにより、ウルツ鉱型-ZnO構造はMgの取り込みによる影響を受けないことが確認されました。ただし、水晶の品質は大幅に低下します。
ドープされていないZnOとドープされたZnOの形態を確認するために、HR-TEMを実行して(図4a–e)、ZnO:Mgの六角形の棒状の形態を描写しました。 Mgはドーピングとともに成長するにつれて核形成の役割を示したようです[39]。ドープされていないおよびドープされたZnOの層間d間隔値は、〜0.464、0.183、0.333、0.27、および0.232 nm HR-TEM画像で計算されました(図4a'–e ')。 d間隔の値は、XRD分析で得られた平面とよく一致しています。不純物/二次相が存在しないことは、クラスター化することなく、ドーパント原子がZnOナノロッドに適切に組み込まれていることを示唆しています[46]。さらに、d間隔の変化は、ZnO格子へのMgの取り込みに起因していました。
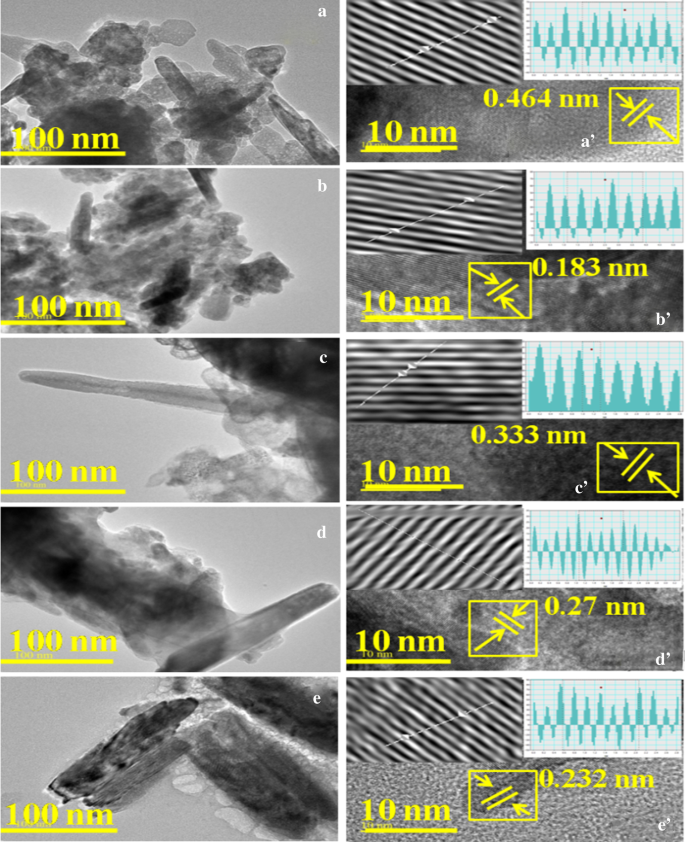
a–e さまざまな濃度のMgドープZnOのHR-TEM画像とMg-ZnOのHR-TEM画像を使用して計算されたd間隔 a ′ –e 'Mg含有量(2、4、6、および8 wt%)
EDSを使用して元素分析を行い、ZnOナノ粉末中の亜鉛と酸素の存在を確認しました(図5a–e)。平均原子比(67.6:23.6)は、ドーパントとともにZnOの形成を定量的に確認しました。金(Au)のピークは、帯電効果を低減するためにサンプル上に金のコーティングがスパッタされたためにスペクトルに表示されます。 Cuのピークは、サンプルホルダーで使用されたCuテープに由来する場合があります。いくつかの追加のピーク(Cl、Si)は、汚染を示している可能性があります。 Naピークは、合成中に塩基性pHを維持するために使用されたNaOHに由来する可能性があります。ただし、NaのピークはZnと重なっているため、サンプル中の存在を確認することはできません。
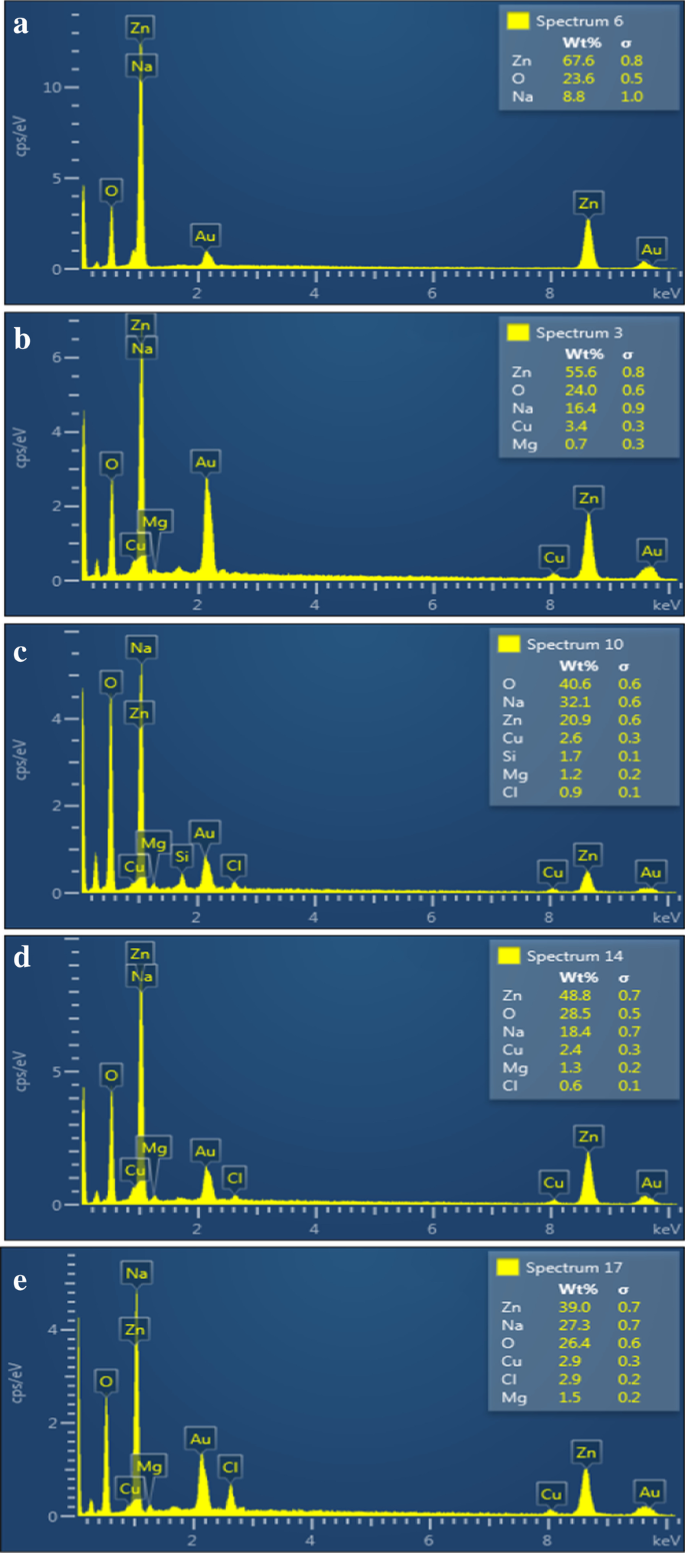
a ZnOおよびさまざまな濃度(2、4、6、および8 wt%)のMgドープZnO( b–e )のEDS分析 )、それぞれ
光触媒プロセスでは、電子と正孔のペア(e-、h +)が生成され、電子と正孔の分離と再結合が続き(図6)、次の酸化還元反応が示されます[35]。
$$ \ begin {aligned}&{\ text {ZnO}} + h \ nu \ to {\ text {ZnO}} \、({\ text {e}} _ {{{\ text {CB}}}} + {\ text {h}} _ {{{\ text {VB}}}})\\&{\ text {e}} _ {{{\ text {CB}}}} + {\ text {O} } _ {2} \ to {\ text {O}} _ {2} ^ {\ cdot-} \\&{\ text {O}} _ {2} ^ {\ cdot- \、} + {\ text {dye}} \、{\ text {degraded}} \、{\ text {products}} + {\ text {CO}} _ {2} + {\ text {H}} _ {2} {\ text { O}} \\&{\ text {OH}} ^ {\ cdot} + {\ text {dye}} \、{\ text {degraded}} \、{\ text {products}} + {\ text {CO }} _ {2} + {\ text {H}} _ {2} {\ text {O}} \\ \ end {aligned} $$
MgをドープしたZnOナノロッドの光触媒メカニズムの概略図
準備されたすべてのサンプルは、対象となる汚染物質としてのMBCFに対する光触媒、超音波触媒、および超音波光触媒活性について評価されました。合成されたナノ触媒によるUV光照射下で光触媒されたMBCF色素の分解プロファイルを図7a–cに示します。
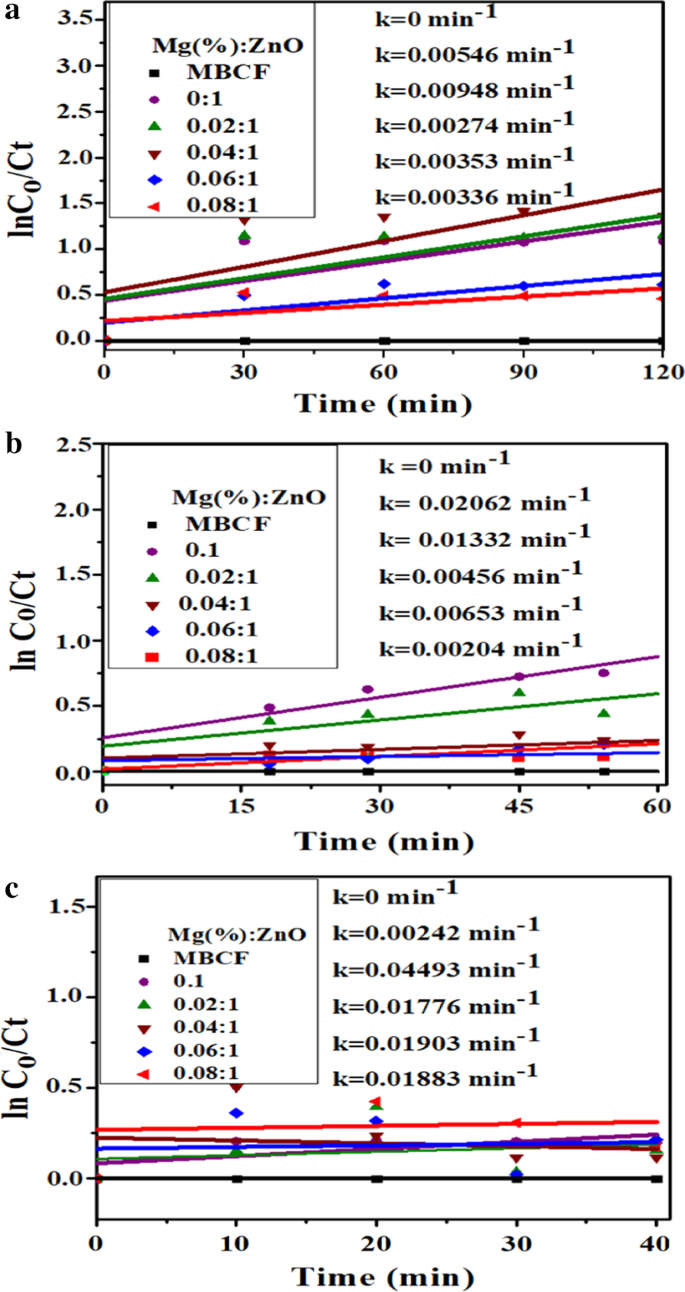
a 光触媒、 b ソノカタリシスと c MgをドープしたZnOナノロッドのMBCF色素分解の超音波光触媒反応速度論
疑似一次反応速度に基づくk(速度定数)は、曝露時間tに対してln(Ct / Co)の線形曲線をプロットすることによって決定されました。ドープされていないおよびドープされたZnO(2、4、6、および8 wt%)の分解速度定数kは、0.00546、0.00948、0.00274、0.00353、および0.00336 min -1 と計算されました。 、それぞれ(図7a)。ドープされたZnOは、純粋なZnOよりも優れた光触媒効率を示し、ドープされたZnO(8 wt%)の最大劣化は26%でした(図8a–c)。表面酸素空孔が存在するため、表面積の増加が、ドープされたZnOの光触媒活性の増加の背後にある説明でした[35]。 VBに正の正孔が残っている半導体のCBでの光誘起電子移動は、光触媒作用の基本的なメカニズムです[15]。励起子が消滅するまで、励起子は触媒表面の周囲の色素分子との酸化還元反応に関与し、分解生成物をもたらします。光誘起電子は強力な還元剤として機能し、周囲のO 2 と相互作用します。 反応性O 2 を生成する分子 ・− 種族。一方、光誘起正孔は、反応性の高いOHを生成する強力な酸化剤として機能します ・ ヒドロキシル基からの種。結果として生じるラジカル種(O 2 ・− およびOH ・ )周囲の染料分子と相互作用して、それらを無毒の製品またはミネラルに分解します。
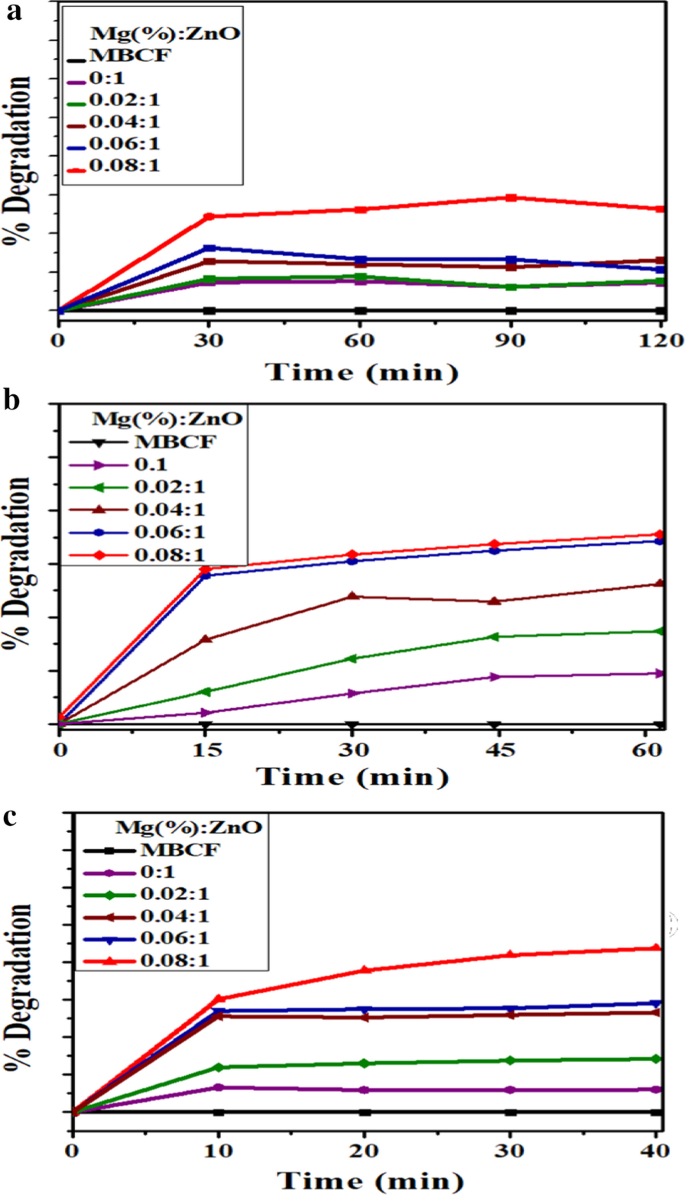
a 光触媒、 b ソノカタリシスと c MgをドープしたZnOナノロッドのMBCFの超音波光触媒光分解
水中の有機性廃棄物を効率的に分解するための代替アプローチは、超音波触媒作用(SC)です[15]。 MBCFの劣化に対する超音波の影響を、ドープされていないZnOとドープされたZnOを使用して調べました。 (図7b)。 MBCF色素濃度に関しては、ドープされたZnOによるMBCFのSC分解は、疑似一次速度論に従いました。ドープされていないおよびドープされたZnO(2、4、6、および8 wt%)の分解速度定数は、0.02062、0.01332、0.00456、0.00653、および0.00204 min -1 でした。 、 それぞれ。最近、さまざまな触媒の存在下でのホットスポットメカニズムとソノルミネッセンスに基づくSC色素の分解に関するいくつかの研究が報告されました。溶液中のキャビテーション気泡の形成は、気泡の非対称核形成によってホットスポットを作成することによって促進できます。これらのホットスポットは、OHがH 2 によって形成されるきっかけとなる可能性があります。 熱分解するO分子。ソノケミカルメカニズムは、通常、崩壊するキャビテーション気泡内の高圧および高温下での溶媒である水のソノリシスを必要とします。 MBCFとナノ触媒溶液では、超音波は水の超音波分解を引き起こすだけでなく、触媒の結合によって電荷担体を生成します。 OH radicals and superoxide anions · O 2− can be generated by electron–hole pairs, which decompose dyes into non-toxic species [15, 47]. Sonophotocatalysis (SPC) also appears to follow pseudo-first-order kinetics, similar to photocatalysis and sonocatalysis. Degradation rate constants for undoped and doped ZnO (2, 4, 6 and 8 wt %) were 0.00242, 0.04493, 0.1776, 0.01903 and 0.01883 min −1 , respectively (Fig. 7c). Degradation performance of doped ZnO was 12, 29, 53, 58 and 87%, respectively (Fig. 8c).
These results suggest that doping plays a crucial role in the efficiency of ZnO photocatalytic. At identical operating conditions, SPC has a higher degradation rate than the corresponding individual mechanisms. The combined process reaction rate constant is greater than the sum of individual processes' rate constants, i.e., photo of Ksono > Kphoto + Ksono, which can be attributed to (i) increase in OH production in mixture, (ii) raised transfer of mass between solution and catalyst surface, and (iii) enhanced activity related to ultrasound disaggregation, consequently enhancing the area of surface [15, 48]. In order to estimate the reusability as well as sample steadiness, Fig. 9a indicates that photocatalytic switches off MBCF colorant degradation under similar conditions after back to back (four cycling experiments). In this way, sample’s degradation efficiency reduced from to 82 to 75%. Herein (Fig. 9b), there is some depletion of nanomaterial by centrifugation or washing while doing recycling experiment. Following the recycling results, it was concluded that the product lasts stable and possesses remarkable ability and acceptance for dangerous wastewater treatment. Anyhow, Table 2 shows the comparison of photocatalytic degradation efficiency of present work with other reported materials.
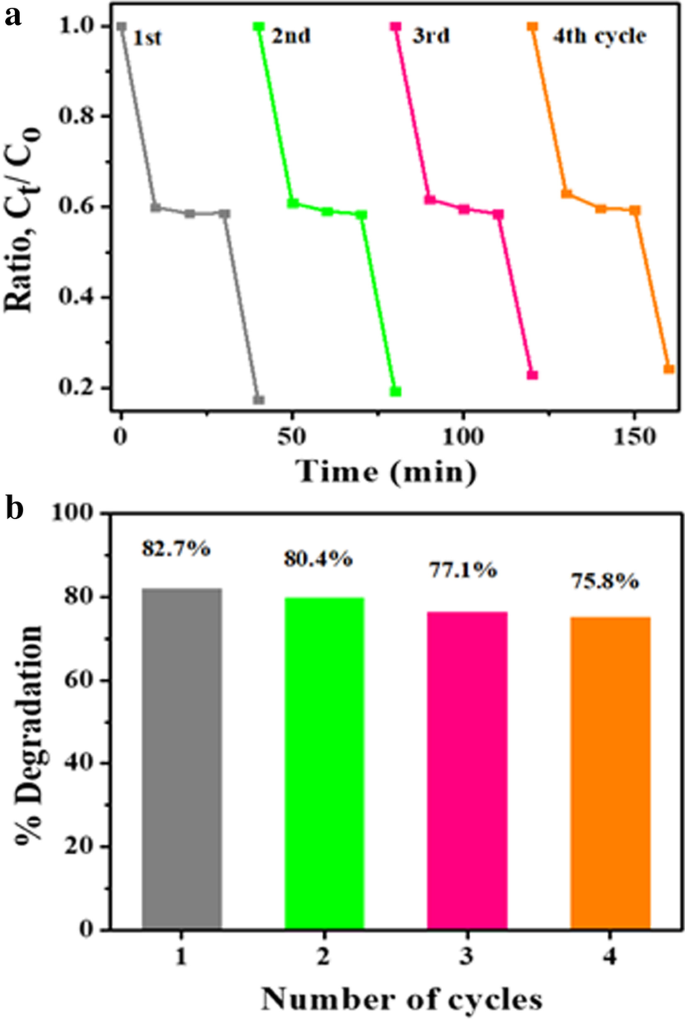
a Photocatalysis reusability performance of Mg-doped ZnO and b %degradation bar graph
In vitro bactericidal action of undoped and doped ZnO NRs for G-ve and G+ve bacteria is given in Table 1. Results depict improved bactericidal synergism and action of doped ZnO against E.コリ in contrast to S.アウレウス 。 Inhibition zones were recorded as (1.05–2.05 mm) and (2.10–4.15 mm) for S.アウレウス and (0–6.15 mm) to (0–8.65 mm) for E.コリ , respectively, while ZnO showed negligible efficacy for E.コリ as compared to S.アウレウス 。 Moreover, control + ve depicted inhibition zone (9.00 mm) against E.コリ および S。アウレウス parallel to control -ve (0 mm). Overall, Mg-doped ZnO exhibited substantial (P < 0.05) efficacy against G-ve as compared to G+ve bacteria.
Oxidative stress induced by prepared doped ZnO depends upon concentration, shape and size of NRs, while increment in NRs size reduces antibacterial activity. Nanosized rods generate oxygen species (ROS) to produce bacterial cell membrane as a result of extrusion of cytoplasmic content, which cause bacteria death as shown in Fig. 10. Another possible phenomenon involves strong interaction between negatively charged cell membrane and cations (Mg 2+ およびZn 2+ ) that results in crumbling of micro-pathogens [49].
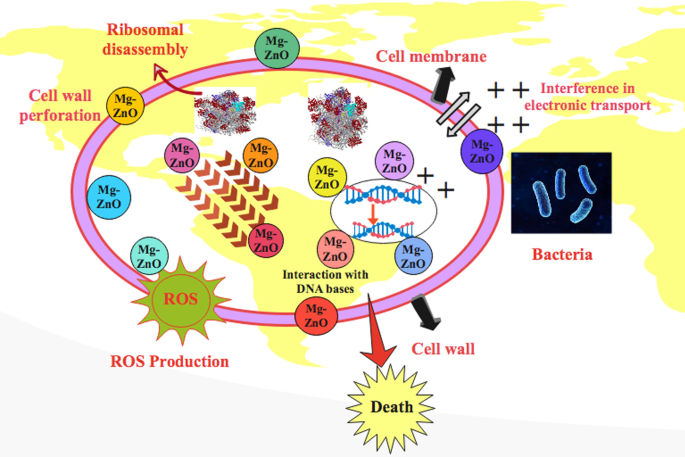
Schematic illustration of bactericidal mechanism of Mg-doped ZnO nanorods
Drug resistance has been considered as major threat to mankind, and there is continuous need for discovery of more compatible antibiotics. Bactericidal activity of metal NRs is well documented, and their role as possible candidate for new antibiotic discovery has been suggested previously [50]. In silico molecular docking studies facilitate to get insight into mechanism behind their antibacterial activity. Dihydrofolate reductase (DHFR) and dihydropteroate synthase (DHPS) enzyme belonging to folate biosynthetic pathway have been reported as well-known target for trimethoprim and sulfonamide drugs, respectively [51, 52]. Here, we evaluated binding tendency of Mg-doped ZnO NRs against DHFR, DHPS and FabH enzymes from E.コリ 。 Docked complexes revealed their binding pattern inside active site and suggested them as possible inhibitor against selected enzyme targets.
For DHFRE.coli , the best docked complex revealed H-bonding interaction with Ile94 (3.1 Å), Tyr100 (3.1 Å) and metal–contact interaction with Met20 and Ala7 with overall binding score -7.518 kcal/mol. Binding interactions with key amino acids of active pocket and orientation of Mg-doped ZnO NP are depicted in Fig. 11a.

Binding interaction pattern of Mg-doped ZnO NRs inside active pocket a Dihydrofolate reductase (DHFR), b Dihydropteroate synthase (DHPS) from E.コリ
For DHPSE.coli , docking complexes showed H-bonding with Leu21 (3.1 Å), Asp56 (3.4 Å), Gly59 (2.9 Å), Thr62 (2.8 Å) and Arg255 (2.8 Å). In addition, the Asn22 and Ile20 interacted with NRs through metal contact inside active site as shown in Fig. 11b. These Mg-doped ZnO NPs blocked active site (binding score:-6.973 kcal/mol) and are suggested to be possible inhibitors against DHPS enzyme.
Similarly, docking of Mg-doped ZnO NRs against the β -ketoacyl-acyl carrier protein synthase III (FabH) enzyme of fatty acid biosynthetic pathway showed H-bonding interaction with Glu302 (3.3 Å), Leu220 (2.9 Å), Thr254 (3.2 Å), and Gln245 (2.7 Å) having binding score -6.548 kcal/mol (Fig. 12). Furthermore, Mg-doped ZnO NPs involved metal contact interaction with Ile250 and His241.
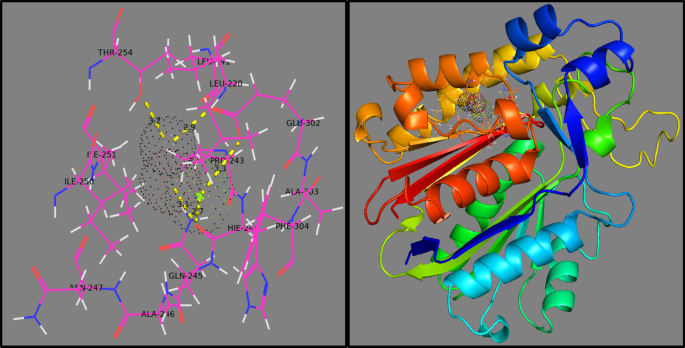
Binding interaction pattern of Mg-doped ZnO NRs inside active pocket β -ketoacyl-acyl carrier protein synthase III (FabH) from E.コリ
Blockage of active site through binding of ligands prevents entry of substrate and thus leads to loss of enzyme activity. Owing to better antibacterial activity of Mg-doped ZnO NRs against E.コリ as compared to S.アウレウス , in silico predictions against selected enzyme targets revealed their possible binding patterns inside active pocket and suggested them potential inhibitors of given enzymes.
A comparison of present sonophotocatalytic study with the literature is shown in Table 2.
結論
Using co-precipitation technique, Mg-doped ZnO NRs were successfully synthesized, and the influence of Mg doping on the phase constitution, elemental composition, morphology and optical properties of ZnO was investigated. Using XRD analysis, the ZnO has hexagonal wurtzite phase, while the estimated crystallite size was less than 100 nm. Crystalline structure of ZnO was also improved by Mg doping, which in turn led to increased luminescence and an increase in the band gap. UV–Vis absorption spectra revealed blueshift indicating band gap widening, while ZnO rod formation was confirmed by EDS study, where an average atomic ratio of 67.6:23.6 was observed. Raman spectrum was blueshifted for higher values of doping (8 wt%) caused by substitution of Mg 2+ for Zn 2+ in ZnO lattice. PL results indicated increased visible emissions with Mg, leading to an increase in electron hole pair delocalization. Dye degradation performance of synthesized NRs was evaluated against MBCF, and best results were obtained via sonophotocatalysis with maximum degradation efficiency of 87% for Mg-doped ZnO. Inhibition zones were recorded as (1.05–2.05 mm) and (2.10–4.15 mm) for S.アウレウス and (0–6.15 mm) to (0–8.65 mm) for E.コリ 、 それぞれ。 Therefore, doped nanorods may be imposed as a control material to minimize antibiotic resistance. Furthermore, in silico molecular docking studies predicted Mg-doped ZnO NRs as potential inhibitor of DHFR, DHPS and FabH enzyme. The inhibition of given enzymes is suggested as possible mechanism behind bactericidal activity of Mg-doped ZnO NRs against E.コリ 。
データと資料の可用性
すべてのデータは制限なしで完全に利用可能です。
略語
- DHFR:
-
Dihydrofolate reductase
- DHPS:
-
Dihydropteroate synthase
- EDS:
-
エネルギー分散型X線分光法
- FTIR:
-
フーリエ変換赤外分光法
- FESEM:
-
電界放出型走査電子顕微鏡
- G+ve:
-
グラム陽性
- G-ve:
-
グラム陰性
- HR-TEM:
-
高分解能透過型電子顕微鏡
- JCPDS:
-
粉末回折基準に関する合同委員会
- Mg:
-
Magnesium
- UV–Vis:
-
紫外可視分光法
- XRD:
-
X線回折
- ZnO:
-
酸化亜鉛
ナノマテリアル
- ナイロン6、66およびPOMと競合するポリケトンベースの化合物
- Escherichia coliに対する酸化銅ナノ粒子の生体合成、特性評価、および抗菌力の評価
- 窒化処理を施したHfO2ベースのRRAMの伝導メカニズムと耐久性の向上
- 光触媒性能を改善するための階層的ZnO @ NiOコア-シェルヘテロ構造の製造
- 色素分解のための新規p-Ag3PO4 / n-BiFeO3ヘテロ接合複合材料の容易な合成と強化された可視光光触媒活性
- アルゴンプラズマ処理によるZnOの挿入による金属とn-Ge間の接触抵抗の低減
- 強化された光触媒評価と抗菌分析のためのZnOナノ粒子に対するMgドーピングの影響
- 水熱法によって調製されたZnOナノスピアアレイの微細構造とドーピング/温度依存フォトルミネッセンス
- 不揮発性メモリのスイッチング特性に及ぼす二分子膜CeO2-x / ZnOおよびZnO / CeO2-xヘテロ構造と電鋳極性の影響
- 太陽照射下での電荷分離と高い光触媒活性を強化するための部分的な表面改質を備えたZnO多孔質ナノシート
- 促進された光触媒抗生物質分解のためのWO3 / p-Type-GR層状材料およびメカニズム洞察のための装置



