強化された光触媒評価と抗菌分析のためのZnOナノ粒子に対するMgドーピングの影響
要約
この研究では、簡単な共沈法を使用して、純粋なMgドープZnOナノ粒子(NP)を合成しました。合成されたナノ粒子(NP)の構造、形態、化学組成、および光学的および抗菌活性を、純粋なMgドープZnO濃度(0〜7.5モル(M)%)に関して研究しました。 X線回折パターンにより、ZnOの結晶性の六方晶ウルツ鉱相の存在が確認されました。走査型電子顕微鏡(SEM)画像は、純粋でMgをドープしたZnO NPが、約30〜110nmの六角形の結晶形態を持つナノスケール領域にあることを明らかにしました。サンプルの光学的特性評価により、バンドギャップエネルギー( E g )Mg 2+ の増加に伴い、3.36から3.04eVに減少しました。 ドーピング濃度。 ZnOの光吸収スペクトルは、Mg濃度が2.5から7.5 Mに変化するにつれて赤方偏移しました。フォトルミネッセンス(PL)スペクトルは、400nm付近にUV発光ピークを示しました。 Mg 2+ による430〜600nmの可視発光の強化 ドーピングは、Zn 2+ を占有することにより、ZnOの欠陥密度を示しました。 Mg 2+ の空孔 イオン。光触媒研究により、7.5%のMgドープZnO NPは、UV-Vis照射下でローダミンB(RhB)色素に対して最大の分解(78%)を示すことが明らかになりました。抗菌研究は、グラム陽性菌とグラム陰性菌を使用して実施されました。結果は、ZnOマトリックス内にMgイオンをドープすると、すべてのタイプの細菌に対する抗菌活性が向上し、ZnONP内のMgイオン濃度が連続的に増加するにつれてその性能が向上することを示しました。
背景
ナノ粒子は、そのサイズ、形状、および形態に依存する新しい特性を示し、植物、動物、および微生物との相互作用を可能にします[1]。商業的に重要なナノ粒子は、いくつかの有機材料または植物抽出物の存在下で、金属または金属塩から直接合成されています。クリーパーや他の多くの植物は、有機物、おそらく樹脂を含む多糖類をしみ出させます。これは、植物が垂直に登ったり、不定根を通って存在する微量元素のナノ粒子を生成し、吸収されるのを助けます[2]。ナノサイズの無機化合物は、表面積対体積比が高く、独特の化学的および物理的特徴があるため、非常に低濃度で顕著な抗菌活性を示しています[3]。さらに、これらの粒子は高温高圧でもより安定しています[4]。それらのいくつかは無毒であると認識されており、人体に不可欠なミネラル要素さえ含んでいます[5]。最も抗菌性のある無機材料は、金属ナノ粒子と、銀、金、銅、酸化チタン、酸化亜鉛などの金属酸化物ナノ粒子であると報告されています[6、7]。亜鉛は、炭酸脱水酵素、カルボキシペプチダーゼ、アルコールデヒドロゲナーゼなどの多くの酵素が不活性になる人間のシステムに不可欠な微量元素ですが、同じ電子構成を持つ同じ元素グループに属する他の2つのメンバーであるカドミウムと水銀は有毒[8]。ナノ粒子の生合成には、アルカロイド、フラボノイド、フェノール、テルペノイド、アルコール、糖、およびナノ粒子を生成する還元剤として機能するタンパク質などの代謝物が含まれているため、植物のさまざまな部分が使用されます。それらはまたそれらのためのキャッピング剤および安定剤として機能します。それらは、技術だけでなく、医学、農業、および他の多くの分野で使用されています。したがって、ナノ粒子の合成のために葉、花、または根に香りまたは色のいずれかを有するすべての植物種に注意が向けられます。これらはすべて、金属イオンを金属ナノ粒子に還元するような化学物質を含むからです[9]。最近、ナノ粒子は、その独特の機械的、光学的、磁気的、電気的、およびその他の特性のために関心を集め始めています[10]。これらの新たな特徴により、エレクトロニクス、医療、その他の分野での使用に有望な候補となっています。ナノ材料は、従来の形態と比較して、表面積対体積比が大きいことが観察されています[11]。これが、ナノマテリアルがより大きな化学反応性を示す理由です。基本的にナノスケールでは、量子効果は、新しい光学的、磁気的、および電気的挙動につながるそれらの最終特性を決定するために、より顕著になります。さまざまな金属酸化物半導体ナノ構造の中で、ZnOナノ構造は、その低コスト、高い化学的安定性、および大量生産のためにかなりの関心を集めています[12]。 ZnOの研究は、現在のナノ調査の妥当な部分を構成しているにすぎません。しかし、それがナノテクノロジーの拡大する部分を際限なく推定する重要な材料の1つであると考えられるすべての要因。 ZnOは、これまでで最も一般的に関連する局所薬の1つです。それはほとんどの日焼け止めに利用されており、苦痛やかゆみを和らげるための多くの治療法への道を発見しています[13]。それは、本質的にZnOとドープされたZnOでの光触媒の機能に見られます。光触媒表面で発生する可能性のある潜在的な化学的、光化学的、および電気化学的応答の大きなクラスターがあります[14]。 ZnOは、環境汚染の分解と完全な鉱化作用において多くの考慮を集めてきました[15]。 ZnOの最も好ましい観点は、いくつかの半導体金属酸化物よりも多種多様な太陽光発電の光範囲とより多くの光量子を引き付ける能力です。 ZnOは、その斬新な属性により、グリーンエコロジー管理構造の主要な材料であり、熟練した有望な候補として開発されました[16]。
基本的に2つの要因、すなわち表面積と表面欠陥は、半導体金属酸化物の光触媒活性を決定するための最も重要な変数です。その高い表面活性、結晶性、形態学的特徴、およびテクスチャーのために; ZnOナノ粒子は、有機汚染物質の分解に最も適した触媒と見なされています[17]。最近の文献では、MgをドープしたZnOナノ構造がデバイス用途に優れた特性を示す可能性があることが報告されています[18]。グループII元素にZnOをドープすることに関する調査では、ドーパントがバンドギャップエネルギー( E )を変更できることが示されました。 g )UV-Visible発光強度の増加に伴い[19]。
ZnOへのMgのドーピングは、ZnOの吸収、物理的、および化学的特性を変更すると予想されます[20]。金属イオンをドープしたZnOナノ構造は、その光学特性が向上しているため、さまざまな汚染物質の分解に最も有望な触媒です[21]。細菌によって引き起こされるさまざまな種類の感染症は、世界中の公衆衛生に深刻な脅威をもたらします。 ZnOの抗菌活性を高めるには、粒子サイズ、結晶化度指数、光学特性などのさまざまな種類の物理化学的特性を、金属または非金属のドーピングによって変更する必要があります[22]。
ZnOの表面により多くの欠陥を誘発することにより、光吸着特性を向上させることができます。基本的に微量のドーパントは、半導体結晶格子内でドナーまたはアクセプターとして機能するのに十分であり、これにより、半導体の特性が大幅に変化します。サイズの量子化により、伝導帯の電子と価電子帯の正孔の間のエネルギーギャップが変化し、ドープされた金属酸化物ナノ構造の光学特性が変化します[23]。以前の文献では、ZnOナノ粒子は細菌に抵抗でき、紫外線を遮断する能力があると報告されています[24]。酸化亜鉛NPには、 Escherichia coli のグラム陰性菌の細胞膜構造を破壊する能力があります。 [25、26]。正電荷を持つナノ粒子は、静電引力を使用してグラム陰性菌の細胞膜に結合できることも報告されています[27]。異なる金属イオンでドープされたZnONPは、 Eに対して評価されました。コリ 、および黄色ブドウ球菌 は、結晶サイズとともに抗菌活性が増加することを示しました[28]。蒸気輸送プロセス[29]、スプレー加水分解[30]、熱分解[31]、その形態とサイズを調整するための電気化学的方法[32]、ゾル-ゲル法[33]、加水分解[34]、化学的沈殿[35]、および熱水法[36]。これらすべての方法の中で、共沈法は比較的単純で安価です。さらに、純粋でドープされたZnONPの合成に室温で高収率をもたらすことができます[37]。
ここでは、単純な化学共沈法を使用して、Mgドーパントの濃度が異なるZnOナノ粒子の調製と特性評価を調査しました。 Mg 2+ の効果 ZnO格子内のイオン濃度は、構造的、形態学的、光学的、および光触媒的研究の観点から評価されています。さらに、Mg 2+ の効果 抗菌活性のイオンを(グラム陽性およびグラム陰性) Sに対して研究した。アウレウス 、 E。コリ 、およびプロテウス 文化。
メソッド
分析グレードの試薬はすべてSigma-Aldrichから購入し、さらに精製することなく受け取ったまま使用しました。フローチャート(図1)は、純粋なMgドープZnONPの調製方法を示しています。この方法では、1 Mの水酸化ナトリウム(NaOH)溶液を1 Mの塩化亜鉛(ZnCl 2 ) 解決。最終的な溶液は、6時間一定の攪拌下に保たれます。水酸化ナトリウムのアルカリ性溶液は、遷移金属水酸化物の沈殿を助けます。それは還元プロセスを加速し、それによってZnOおよびMgをドープしたZnOナノ粒子の形成を引き起こします。さらに、水酸化ナトリウムはZnCl 2 を変換します Zn(OH) 2 加熱後、ZnOナノ粒子が生成されます。沈殿後、ビーカーを取り出し、最終製品を沈殿させるのに十分な時間を与えます。得られた生成物を濾過し、脱イオン水およびアセトンで数回洗浄する。最後に、サンプルを100°Cで5時間乾燥させた後、瑪瑙乳鉢で粉砕して微粉末に変換します。このようにして得られた粉末を300°Cで4時間焼成して、ナノサイズのZnO粒子を生成します。
MgをドープしたZnONPの合成を説明するフローチャート
MgをドープしたZnOを合成するには、ZnCl 2 のモル比 およびMgCl 2 Zn 1 − x として測定されました Mg x O( x =0.025、0.050、および0.075)、同じ手順を繰り返しました。純粋なMgドープZnOを合成するための化学式を式(1)に示します。 (1–4)
$$ {\ mathrm {ZnCl}} _ 2 + 2 \ mathrm {NaOH} \ to \ mathrm {Zn} {\ left(\ mathrm {OH} \ right)} _ 2 + 2 \ mathrm {NaCl} \ left(\ mathrm {aq} \ right)$$(1)$$ \ mathrm {Zn} {\ left(\ mathrm {OH} \ right)} _ 2 \ to \ mathrm {Sintering} \ to \ mathrm {Mg} \ hbox {- } \ mathrm {ドープ} \ \ mathrm {ZnO} + {\ mathrm {H}} _ 2 \ mathrm {O} $$(2)$$ {\ mathrm {MgCl}} _ 2 + {\ mathrm {ZnCl}} _ 2 + 2 \ mathrm {NaOH} \ to \ mathrm {ZnMg} {\ left(\ mathrm {OH} \ right)} _ 2 + 2 \ mathrm {NaCl} \ left(\ mathrm {aq} \ right)$$(3) $$ \ mathrm {ZnMg} {\ left(\ mathrm {OH} \ right)} _ 2 \ to \ mathrm {Sintering} \ to \ mathrm {Mg} \ hbox {-} \ mathrm {ドープ} \ \ mathrm {ZnO } + {\ mathrm {H}} _ 2 \ mathrm {O} $$(4)電気化学シリーズでは、MgはZnよりも反応性が高いため、還元を受けてZn格子を占有します。
特性評価
サンプルの結晶構造は、Cukα放射線(λ)を使用したX線回折(XRD)Bruker D8高度X線回折計によって調査されました。 =1.54Å)および表面形態の特徴は、電界放出型走査電子顕微鏡(FESEM、ZEISS)によって研究されました。サンプルの光吸収スペクトルは、200〜1200nmの範囲でHitachiU-3900Hを使用してダブルビームUV-Visible分光光度計で記録されました。フォトルミネッセンス(PL)発光の研究は、波長325 nmのHe-Cdレーザー光源を使用した分光計(JOB HR800 IN Yoon Horbe)によって実施されました。合成されたサンプルの抗菌活性は、寒天ディスク拡散技術によってさまざまな生物に対してテストされました。
光触媒活性の測定
実験は、150mlの容量を持つ光触媒石英反応器で実施されました。原子炉には、一定の温度を確保するための水循環設備がありました。 UV照射は、125 W(311 nm)の中圧Hgアークランプ(SAIC、インド)を使用して実行されました。 150ミリリットルの望ましい初期濃度(20 ppm)のRhB色素溶液を、自然のpH(6.2)で一定量のZnO NP(50 mg / L)と混合しました。溶液をUV照射下に置き、磁気的に攪拌した。光反応器からのサンプルを異なる時間間隔で取り出し、遠心分離した。 UV-Vis分光光度計を使用して、上澄みの最大吸収(554 nm)を分析しました。同様の手順が、RhB色素溶液を使用したMgドーパント(2.5、5、および7.5%)-ZnONPに採用されました。触媒表面によって分解されたRhBのパーセンテージは、次の式から計算されました。
$$ \ mathrm {Percentage} \ \ mathrm {of} \ \ mathrm {degradation} =\ left({C} _0- {C} _t \ right)/ {C} _0 \ times 100 \%$$(5)ここで C 0 吸収の初期時間を表し、 C t さまざまな時間間隔(0、30、60、90、120分)後の吸収を表します。
抗菌研究
E。コリ (グラム陰性)、 S。アウレウス (グラム陽性)、およびプロテウス (グラム陰性菌)は、使用前にブロス培地で4°Cに維持されました。栄養寒天培地を調製し、121°Cで15分間滅菌しました。 25ミリリットルの栄養寒天培地を滅菌ペトリ皿に注ぎ、硬化させた。各ペトリ皿に0.2mlの異なる細菌種( E.coli )を広げました 、 S。アウレウス 、およびプロテウス )。ディスクを準備し、滅菌ループを使用してプレートに配置し、プレートごとに2枚のディスクを細菌培養物を含むセット寒天に作成しました。
結果と考察
構造研究
図2は、純粋なZnOサンプルとMgをドープしたZnOサンプルのX線回折(XRD)パターンを示しています。この図では、31.8°、34.5°、36.3°、47.5°、56.7°、62.9°、68°に7つの主要なピークが見られ、(100)、(002)、(101)、格子定数がa =b =3.24Åおよびc =5.2066Åの場合、それぞれ(102)、(110)、(103)、および(112)平面[38]。 XRDパターンは、純粋なZnOナノ粒子(JCPDS:36-1451)の六角形のウルツ鉱相結晶構造の存在を明確に反映しています[39]。また、回折から、ZnO結晶格子へのMgドーパントではそれ以上の二次相は観察されず、MgドープZnONPのXRDパターンに有意な変化は観察されないことに注意してください。また、Mgドーピング濃度の増加に伴ってXRDピークの強度が低下することにも注意してください(図2a〜dを参照)。これにより、格子の歪みによる結晶化度の細長い損失が確認されます。 ZnOの周期的結晶格子内にMgイオンがドーピングされているため、少量の歪みが発生します。これにより、格子が入れ替わり、結晶の規則性が連続的に変化します。しかし、非常に注意深い推論は、ZnOマトリックスへのMgのより高いドーピングで観察されるように、ピーク位置がより低い角度値に向かってシフトすることを示しています。特に(101)面35°.84に位置するピークの場合、ドーピング濃度の増加に伴って低い値にシフトすることがわかります。これは、Zn 2+ の置換に起因する可能性があります。 Mg 2+ によるイオン イオン[40]。ドーパント材料の組み込みにより、ホスト材料の格子特性が変化することが文献でよく報告されています。これは、原子半径のばらつきが原因で発生します。さらに、ドーパントイオンは、ホスト格子内のZnイオン(Mgイオン)に置き換わる可能性があります[41]。したがって、ZnO NPの基本構造は変更されておらず、元のウルツ鉱構造を保持しています。これは、Mg 2+ のほとんどが イオンは、Zn 2+ を置き換える置換イオンとして格子に入ります。 イオンとボイドスペースに入らないでください。置換されたMg 2+ のイオン半径から ( R Mg 2+ =0.057 nmは0.57Å)Zn 2+ よりも小さい ( R Zn 2+ =0.06 nmは0.60Å)[42]、Mg 2+ のため、シフトは少量の格子ひずみに対応することが観察されています。 ZnO環境に。
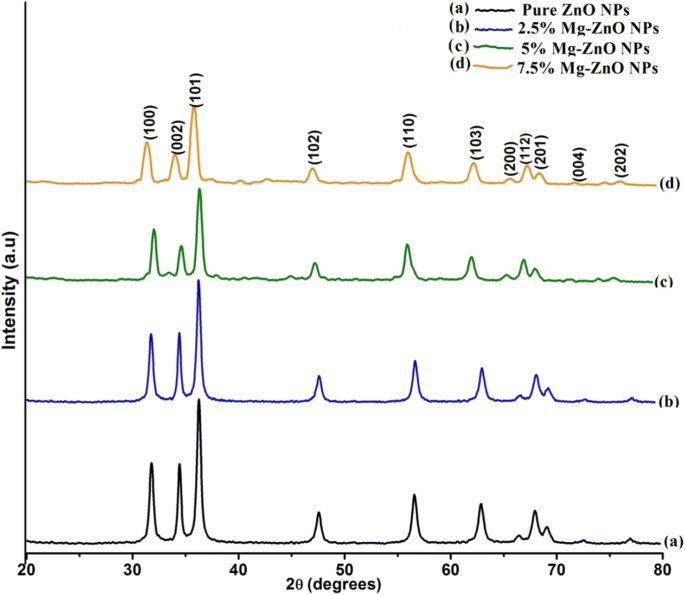
純粋なMg-ZnONPのXRDパターン。 a 純粋なZnONP。 b 2.5%Mg-ZnONP。 c 5%Mg-ZnONP。 d 7.5%Mg- ZnO NP
平均結晶子サイズは、シェラーの式[43]を使用して計算されます。
$$ d =\ frac {0.89 \ lambda} {\ beta \ cos \ theta} $$(6)ここで、λ は放射の波長(1.54056Å)、β は半値全幅であり、θ は回折角です。計算値から、Mgドーピング濃度の増加に伴って平均結晶子サイズが増加することが観察されます(表1)。
<図>格子定数に対するドーピングの影響
結晶サイズ、格子パラメーター、原子充填率(APF)、格子ひずみ、および体積は、純粋なZnONPとドープされたZnONPの物理的特性を示しています[44]。ウルツ鉱相の場合、格子定数は式(1)を使用して計算されます。 (7–9)ここで、a =b、cは格子定数 d hkl はミラー指数(hkl)に対応する面間距離です。
$$ \ frac {1} {d_ {hkl}} =\ frac {\ left({h} ^ 2 + {k} ^ 2 \ right)} {a ^ 2} + \ frac {l ^ 2} {c ^ 2} $$(7)$$ a =\ frac {\ lambda} {\ sqrt {3 \ sin {\ theta} _ {100}}} $$(8)$$ c =\ frac {\ lambda} {\ sin {\ theta} _ {002}} $$(9)$$ D =\ frac {1} {APF} $$計算された格子定数を表1に示します。表1から、Mg 2+ として格子定数値に変化があることがわかります。 イオンがZn 2+ に置き換わる 格子内のイオン。ドーピング濃度が増加すると、組み込まれたドーパント原子が置換格子サイトを占有します。表1から、式(1)に示すように、結晶子サイズ(D)が原子充填率(APF)に反比例して変化することもわかります。 (10)。
誘発されるひずみは、式(1)を使用して計算されます。 (10)。
$$ \ varepsilon ={\ beta} _ {hkl} \ cos \ theta / 4 $$(10)さらに、Mg 2+ により格子ひずみが減少することに注意してください。 ZnOマトリックス内にイオンがドーピングされると(表1)、結晶構造に局所的な歪みが生じます。これは明らかであり、原子半径とドーピング濃度の違いについても文献で以前に指摘されています[45]。
電界放出型走査電子顕微鏡(FESEM)およびEDS分析
図3a〜dは、さまざまなMgモル濃度でのMgドープZnONPの形態を示しています。 FESEM画像から、ほとんどの粒子がナノスケール領域にあることが観察されます。粒子がそれらの表面に凝集することにも注意されたい。表面上の粒子の凝集は、合成されたNPの高い表面エネルギーに起因している可能性があります[46]。興味深いことに、ドーピング濃度が5 M%および7.5 M%の場合、六角形の結晶形でよく分布したナノ構造の粒子が観察され、ZnOマトリックスの表面に高濃度のMgがドープされていることを示しています。 ZnOマトリックス内のMgイオンの濃度が高くなると、最終粒子の粒子サイズは30nmから110nmに増加しました。図3c、dは、XRD分析によって得られた結晶子サイズに準拠しています。

純粋なMgドープZnONPのFESEM写真。 a 純粋なZnONP。 b 2.5%Mg-ZnONP。 c 5%Mg-ZnONP。 d 7.5%Mg- ZnO NP
図4a〜dは、EDSを使用して実行された純粋なMgドープZnOナノ粒子の化学組成分析を示しています。得られたEDSスペクトルから、Zn、Mg、Oなどのさまざまな元素の存在が観察されます。図4c、dは、MgをZnO環境に注入するとMgの強度がわずかに増加することを明確に示しています。 Mgイオンの取り込みは、構造的および光学的特性に大きな影響を及ぼしました。また、EDSスペクトルから、合成されたサンプルには他の異物は存在しないと結論付けられました。
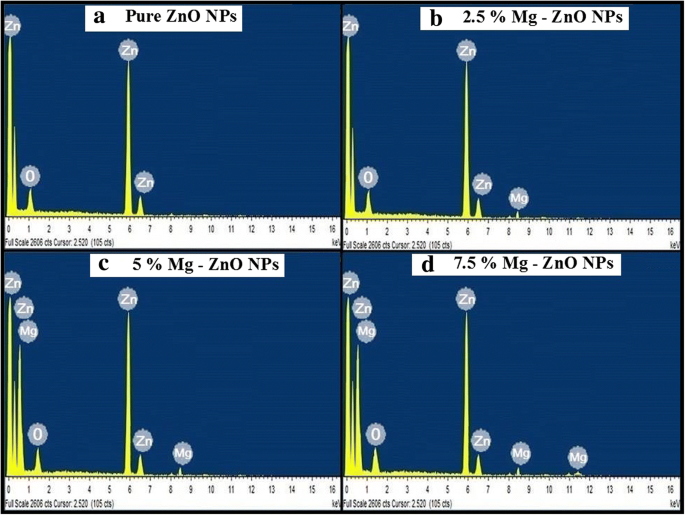
エネルギー分散型X線(EDS)スペクトル。 a 純粋なZnONP。 b 2.5%Mg-ZnONP。 c 5%Mg-ZnONP。 d 7.5%Mg-ZnO NP
光学研究
200〜1200nmの範囲の波長の関数としての純粋なMgドープZnONPのUV-Vis吸収スペクトルを図5aに示します。図から、ドーピング濃度とともに吸収ピークが増加することがわかります。吸光度の増加は、粒子サイズ、酸素欠乏、粒子構造の欠陥などのさまざまな要因が原因である可能性があります[47]。図5aから観察されるように、MgをドープしたZnOナノ粒子の380 nm未満の波長で強い吸光度が見られますが、可視領域では非常に低い吸光度が観察されます。これは、低エネルギー状態で存在する分子が高エネルギーレベルに励起されることにより、入射光子エネルギーの吸収が大きくなることに起因します。
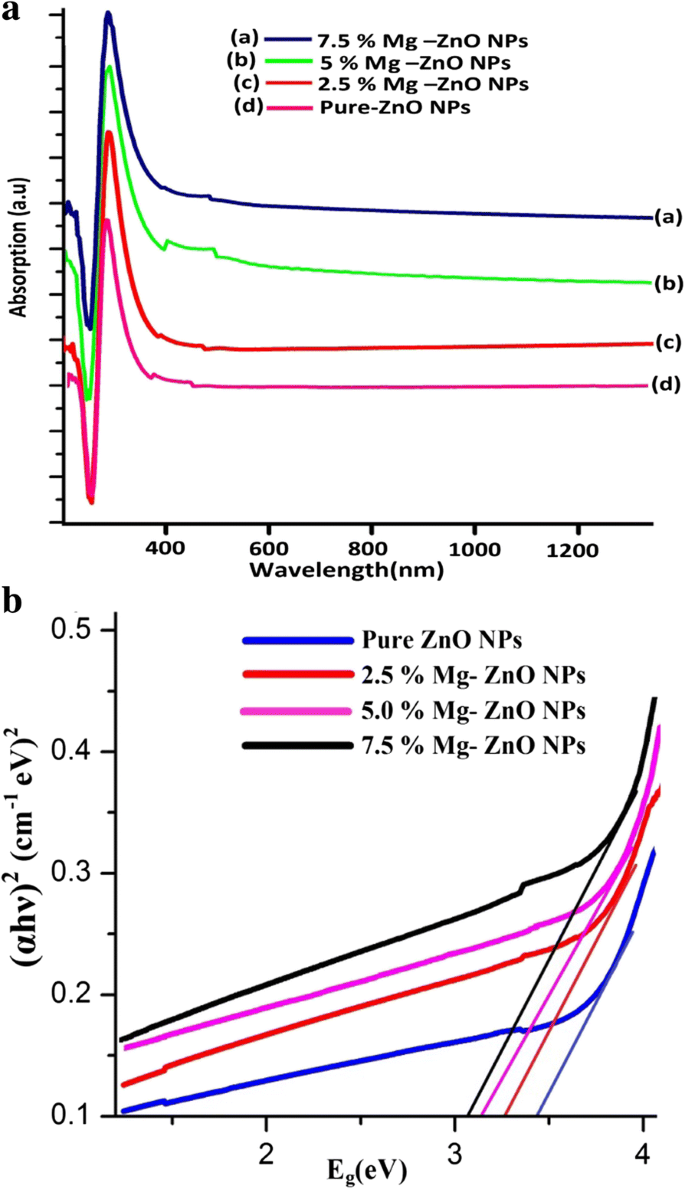
a 吸光度と b バンドギャップエネルギー( E g )純粋なMgドープZnONPの場合
Mg含有量が2.5から7.5M%に変化すると、MgをドープしたZnO NPの吸収端がより長い波長にシフトする(赤方偏移)ことが観察されます。これは、ZnOに対するMgドーパントの結果としてサンプルに存在する少量の格子ひずみが原因である可能性があります。この赤方偏移の振る舞いは、バンドギャップ( E )で減少すると予想されます。 g ) 価値。光学バンドギャップ( E g )は、次の関係(11)のTaucプロットから決定されます。
$$ \ alpha =\ frac {A {\ left(h \ nu- {E} _ {\ mathrm {g}} \ right)} ^ {1/2}} {hv} $$(11)ここでα は吸収係数、 h プランク定数ν は光放射の周波数であり、 E g はバンドギャップエネルギーです。ここで、「 n 」は、許可された直接遷移に対して½の値を取ります[48]。 (αhν) 2 のプロット 対(hν)は、純粋なMgドープZnONPに対して作成されます。バンドギャップエネルギー( E g )は、プロットの線形部分を x に外挿することで得られます。 -軸。
図5bから、バンドギャップエネルギー( E g )純粋なZnONPの場合は約3.36eVであり、Mgドーパント(3.36〜3.04 eV)とともに減少します。バンドギャップは、強力な量子閉じ込めと表面積対体積比の向上により減少します[49]。赤方偏移の強化とバンドギャップエネルギーの減少( E g )Mg 2+ の存在を確認します Zn 2+ の内部 ZnO格子のサイト。
フォトルミネッセンス研究
図6は、純粋なMg 2+ のフォトルミネッセンススペクトルを示しています。 325nmの波長でドープされたZnONP。可視スペクトル領域では、400 nm付近の比較的頑丈なUV発光バンドと、450〜620nmの広いバンドが観察されます。強いUV放射は、励起子の放射再結合(励起子放射)に起因します[50]。 450〜620 nmの広い可視発光バンドの起源は、表面の陰イオン空孔によるものです[51]。これは、既存のトラップされた正孔を介した表面結合電子のトンネリングが原因である可能性があります[52]。また、390および525 nmで観察される発光バンドの強度は、Mg含有量のドーピングが高くなると(7.5%)減少することが観察されます。 ZnO NP内のドーピング率が高いと、光生成された電子と正孔の再結合が妨げられます。さらに、Mg(7.5%)イオンは、ZnO格子内に追加のアクティブな欠陥サイトを生成し、これらのアクティブな欠陥サイトを介した可視光の吸着をさらに促進します[53]。
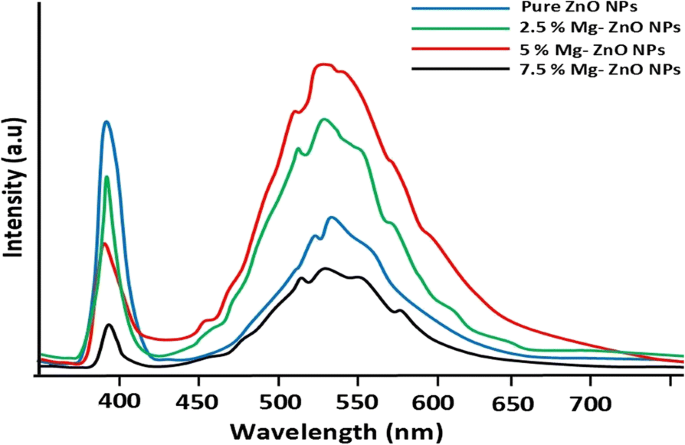
純粋なMg-ZnONPのフォトルミネッセンススペクトル
光触媒研究
ローダミンB(Rh B)色素溶液を使用した純粋なMgドープZnOの光触媒分解研究を、さまざまな時間間隔(0〜120分)で研究しました。さまざまな時間間隔(0〜120分)でのRhB色素溶液の光吸収スペクトルを記録し、同じことを図7に示します。時間の経過とともにピーク高さが減少し、ローダミンBの劣化が大きいことを示しています。 ZnOの光触媒活性に。 120分後に純粋なZnOを使用して分解された染料の量はごくわずかですが、7.5%のMgドープサンプルはより高い分解効率を示しました。これは、ZnOマトリックス内のMgドーピングによって生成された欠陥と酸素空孔の存在のために予想されます[54]。図8は、純粋なZnONPとMgをドープしたZnONPの劣化の割合を示しています。 7.5%のMgドープZnOは、他のドーピング濃度と比較して78%の最大劣化を示したことが観察されています(表2)。 ZnOへのより高いMg(10%以上)のドーピング濃度は、光触媒活性を低下させることにも留意されたい。これは、陽イオンの酸化状態の増加だけでなく、物理的な欠陥のために理解できます。この現象は、ドーピングプロセス中に生成された過剰な陽イオンが正孔と電子のトラップサイトとして機能することを説明した文献の初期に観察されました。その後、これは光生成された荷電種の再結合を刺激します。これにより、•OH(ヒドロキシル)とO• 2 の生成が徐々に妨げられます。 − (酸素)スーパーオキシドラジカル。この現象は、光触媒活性を低下させます。同様の結果がLeeらによって報告されています。 [55]およびYousefietal。 [56]。さらに、我々の共沈技術では、熱力学的溶解度は、ZnOへのMgのドーピング濃度が高いほど低くなります。このような結果と同様に、Javed Iqbal et al [57]によって報告されています。
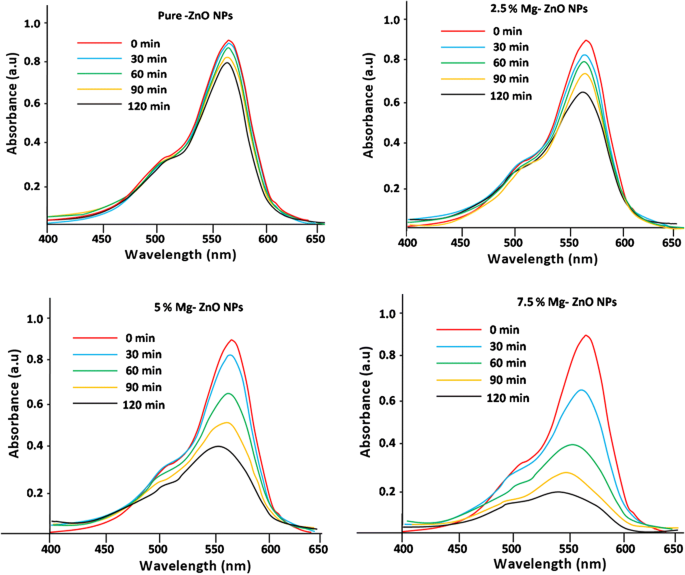
(0〜120分)から分解されたローダミンB色素水溶液の吸収スペクトルの減少
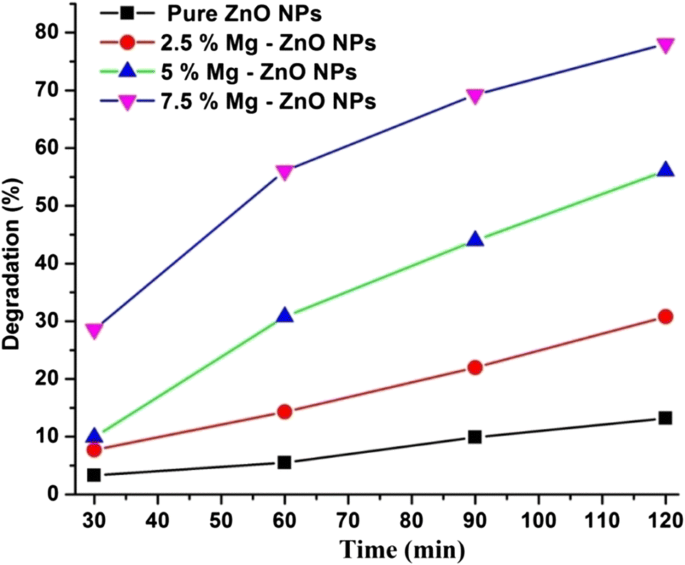
純粋およびIZ-NP下でのローダミンBの光分解
MgをドープしたZnONPは電子シンクと同様に機能し、その結果、光生成された電子正孔対の分離を大幅に強化し、それらの再結合を阻害して、光触媒活性を向上させることができるようです[58]。
反応速度は、濃度比ln(C / C o の線形曲線をプロットすることで観察できます。 )、照射時間に対して「 t 」。グラフ(図9a)から、ZnOマトリックス内に2.5〜7.5%のMgイオンが存在することで、実際に光触媒プロセスが活性化されていることが明らかにわかります。図9bから、RhB分解速度定数kが評価され、1.09×10 − 3 でした。 、2.76×10 − 3 、5.72×10 − 3 、および1.26×10 − 2 純粋なZnONPの場合、それぞれ2.5%Mg-ZnO NP、2.5%Mg-ZnO NP、および2.5%Mg-ZnONPです。その中で、7.5%のMg-ZnO NPは、最も高い分解速度定数(k)値を示し、純粋なZnO NPと比較してかなり大幅に増加しています(表2)。この光触媒実験の結果は、特定の限界までのMgイオンのドーピングが、ZnO光触媒の光触媒活性を効果的に高めることができることを明確に示しています。
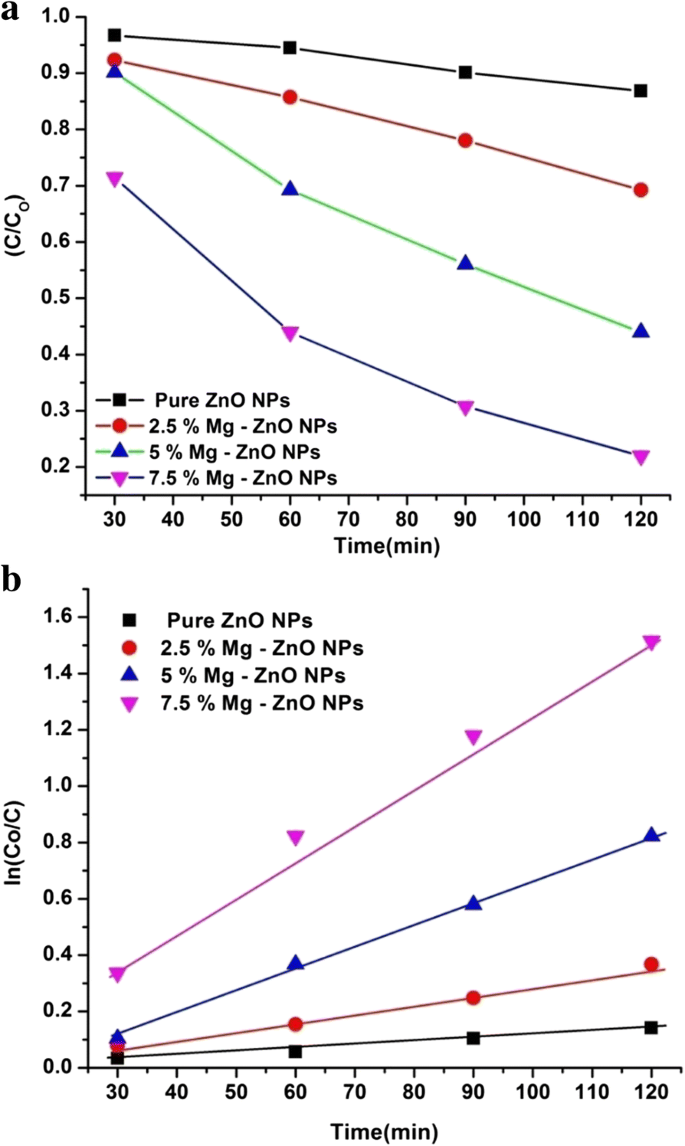
( a )純粋なMg-ZnO NP( b )の時間の関数としてのRhBの相対濃度の変化 )純粋なMg-ZnONPのRhB染料分解の反応速度論
MgをドープしたZnONPの光触媒活性が向上する理由は、表面の酸素空孔が存在することで表面積が拡大することです[59]。半導体材料の光触媒メカニズムは、電子正孔対(e - )の形成を通じて進行します。 、h + )その後の分離と電子と正孔の再結合[60]。 Photocatalytic activity for pure ZnO is attributed both to the donor states caused by a large number of defect sites such as oxygen vacancies and interstitial zinc atoms and to the acceptor states which arise from zinc vacancies and interstitial oxygen atoms [61]. But for Mg-doped ZnO NPs for the degradation of RhB under UV-Visible irradiation, initially electron–hole pairs are created and then the species such as •OH and •O − 2 are formed as shown in the equation.
$$ ZnO+ h\nu \to ZnO\left({e}_{CB}+{h}_{VB}\right) $$ (12)The photo-induced electrons are easily trapped by electronic acceptors like adsorbed (O2 ), in order to produce a superoxide radical anion (O• − 2 ) Eq. (13)
$$ {e}_{CB}+{O}_2\to {O}_2^{\bullet -} $$ (13)Further, the photo-induced holes are easily trapped by negative OH − ions to errand the production of hydroxyl radical species (OH•) Eq. (14)
$$ {OH}^{-}+{h}^{+}\to {OH}^{\bullet } $$ (14)Thus produced OH − radical and superoxide radical anion will carry out the total photocatalytic reaction. However, •OH radical is a particularly strong oxidant which can cause fractional or complete mineralization of organic molecules. The high oxidative potential of the hole in the valence band causes the oxidation of organic compounds to form some reactive intermediates [62] as shown by Eq. (15–16).
$$ {O}_2^{\bullet -}+\mathrm{RhB}\ \mathrm{degradation}\ \mathrm{products}+{CO}_2+{H}_2O $$ (15) $$ {OH}^{\bullet }+\mathrm{RhB}\ \mathrm{degradation}\ \mathrm{products}+{CO}_2+{H}_2O $$ (16)Thus, it is necessary to prevent the recombination of electron–hole pairs to have better photocatalytic activity of semiconductor based NPs. Controlled doping of Mg over the ZnO NPs up to a certain limit can enhance the photocatalytic activities. All the Mg-doped ZnO NPs show a significant enhancement of the photo-degradation of RhB dye compared with the pure ZnO NPs. In this research, 7.5% Mg-doped ZnO NPs show better photocatalytic properties after 120 min compared with pure ZnO sample. This might be due to the change in their particle size and band gap effects [63].
Antibacterial Studies
The zone of inhibition by using Mg-doped ZnO NPs for E.コリ (Gram-negative), S.アウレウス (Gram-positive bacteria), and Proteus (Gram-negative strains) is displayed by Fig. 10. It was carried out using disc diffusion method to observe their ability as a potential antimicrobial agent. The prepared NPs were highly reactive due to their high surface to volume ratio. From Fig. 10, it is clear that the Mg 2+ -doped ZnO NPs inhibit the growth of both Gram-negative and Gram-positive bacteria. It was observed that the zone of inhibition is proportional with the amount of Mg doping in ZnO NPs. The results obtained to show the effect of Mg doping in ZnO NPs are illustrated in Table 3. This might be attributed to the reduction in their band gap values. Due to reduction in the band gap, there is a possibility of exciton generation. Overall, this enhances the photocatalyst activities for improved bactericidal activity of Mg-doped ZnO NPs [64]. Furthermore, due to the various surface-interface characteristics may have different chemical-physical, adsorption-desorption abilities in the direction towards bacteria, make sure in different antibacterial performances [65].

Zones of Inhibition of ZnO and Mg-doped ZnO NPs against the given bacteria
The interaction between the NPs and the cell wall of bacteria was changed due to doping of Mg. The growth of S.アウレウス and the other two bacteria was more commendably affected by Mg 2+ -doped ZnO nanostructures compared with pure ZnO NPs. From Table 3, it is noted that Gram-negative and Gram-positive have different inhibition zones. This difference in the antibacterial activity of Mg-doped ZnO nanostructures against Gram-negative and Gram-positive bacterial strains may be due to the difference in cell wall structure of those respective bacteria. It was also reported earlier that various bacterial strains had considerably different infectivity and tolerance levels towards the different agents including antibiotics [66]. Also differences in the antibacterial activity might be due to different particle dissolution.
Basically, the antibacterial efficiency of pure and Mg-doped ZnO NPs is mainly dependent on the increased levels of reactive oxygen species (ROS), mostly hydroxyl radicals (OH) and singlet oxygen [67]. This is mainly due to the enlarged surface area which causes increase in oxygen vacancies as well as the diffusion capacity of the reactant molecules inside the NPs [68]. The reactive oxygen group contains superoxide radical and hydrogen peroxide. Both of them can damage the DNA and cellular protein leading to cell death [69]. Moreover, the presence or addition of the nanostructures on the surface or cytoplasm of the bacteria can cause the disruption of cellular function as well as disorganization of the cell membranes [70]. The doping of Mg with ZnO may lead to the variation in grain size, morphology, and solubility of Zn 2+ イオン。 All these factors combined together have a robust impact on the antibacterial activity of ZnO [71, 72]. The results have revealed that Mg-doped ZnO nanostructures will be a promising candidate to be used for potential drug delivery systems to cure some significant infections in the near future.
結論
To conclude, pure and Mg-doped ZnO structures were successfully synthesized by co-precipitation method. The XRD patterns revealed the wurtzite structure for all the nanosamples and no impurity phase was noted. The maximum crystallite size obtained from XRD was less than 100 nm. FE-SEM studies confirmed that the crystallite size increased with increase in Mg content. The UV-Visible results revealed that absorption underwent a redshift with Mg into ZnO as compared to pure ZnO exhibiting strong quantum confinement effects. Optical band gap energy was found to decrease from 3.36 to 3.04 eV with Mg doping, resulting in the increment in their crystallite size as a result of Mg doping. PL results confirmed the enhanced visible emissions with Mg-doped ZnO leading to the increase in delocalization of electron-hole pairs. Photocatalytic measurements revealed the increase in Mg doping in the ZnO nanoparticles that caused higher photocatalytic activity. The antibacterial activities of the synthesized nanosamples were tested against E.コリ (Gram-negative), S.アウレウス (Gram-positive bacteria), and Proteus (Gram-negative strains).
ナノマテリアル
- ドラッグデリバリーを強化するためのナノファイバーとフィラメント
- 癌治療のためのナノ粒子:現在の進歩と課題
- Escherichia coliに対する酸化銅ナノ粒子の生体合成、特性評価、および抗菌力の評価
- Sb /パリゴルスキー石(PAL)ナノ粒子の調製と強化された接触水素化活性
- アルミノシリケートミネラルおよび優れた水分解性能のための代替ドーピング
- HT29およびSPEV細胞株に対するAuナノ粒子の影響のinvitro研究
- 光触媒活性と安定性を強化するためのIn2O3ナノ粒子ハイブリッド双晶六角形ディスクZnOヘテロ構造の水熱合成
- In VivoCTイメージングおよび腎クリアランス特性のための新しい生体適合性AuNanostars @PEGナノ粒子
- 光触媒活性が強化されたAgナノ粒子/ BiV1-xMoxO4の相乗効果
- ナノ粒子の跳ね返りに及ぼす弾性剛性と表面接着の影響
- 強化された細胞内在化のためのFe3O4磁性ナノ粒子の葉酸とgH625ペプチドベースの機能化の比較



