溶融塩合成により合成された球形および棒状のPbTiO3粉末の構造特性と誘電特性
要約
PbC 2 の反応による O 4 およびTiO 2 共晶NaCl-KCl塩では、球形と棒状の両方のPbTiO 3 (PTO)粉末は、それぞれ溶融塩合成(MSS)およびテンプレートMSS法によって合成されました。 X線回折パターンは、すべてのPTO粉末が正方晶相構造で結晶化することを示しています。 PbC 2 のモル比を上げる O 4 :TiO 2 MSSプロセスの1:1:10:10から1:1:60:60までの:NaCl:KClは、950°Cで5時間合成されたPTO粉末の球形の形態にほとんど影響を与えません。直径480nm〜1.50μm、長さ10μmまでの大規模な多結晶棒状PTO粉末を、800°Cで5時間、テンプレートMSS法により合成しました。この方法では、棒状アナターゼTiO 2 前駆体をテンプレートとして使用し、PbC 2 のモル比を使用しました O 4 :TiO 2 :NaCl:KClは1:1:60:60に等しかった。 X線エネルギー分散型分光スペクトルは、すべてのPTO粉末がPb、Ti、およびO元素で構成されており、測定されたPb:Ti原子比が1:1に近いことを示しています。テンプレートMSSプロセスでは、溶融塩含有量が棒状のPTO粉末の形成に重要な役割を果たします。溶融塩含有量が少ないと、棒状のTiO 2 であっても、棒状のPTO粉末を合成することはできません。 テンプレートが使用されます。さらに、反応時間を延長すると、棒状のPTO粉末の形成が抑制されましたが、球形のPTOナノ粒子の形成が促進されました。球形および棒状のPTO粉末の誘電特性を比較調査しました。室温で、PbC 2 のモル比でMSS法によって合成された球状PTO粉末の誘電率と誘電損失 O 4 :TiO 2 1:1:30:30に等しい:NaCl:KClは〜340および0.06(10 6 で測定) Hz)、それぞれ。 PbC 2 のモル比でテンプレートMSS法によって合成された棒状PTO粉末の対応する値 O 4 :TiO 2 1:1:60:60に等しい:NaCl:KClは、それぞれ140と0.08でした。今回の結果は、球形のPTO粉末の誘電特性が優れていることを示しており、多層コンデンサや共振器の分野で有望な用途があります。
はじめに
一般式ABO 3 のペロブスカイト酸化物 は、固体化学において最も重要なクラスの材料の1つであり、強誘電性、磁性、オプトエレクトロニクス、およびエネルギー変換の分野で広く使用されています[1,2,3]。ペロブスカイト酸化物ファミリーのすべてのメンバーの中で、PbTiO 3 (PTO)は、正方晶の歪みが最も高くなります( c / a 〜1.064)、これは他の人よりも注目に値します。この大きな正方晶歪みは、すべての強誘電性ペロブスカイト酸化物の中で最も高い自発分極に対応します。ペロブスカイト強誘電性酸化物のパラダイムとして、PTOは優れた誘電特性、圧電特性、および焦電特性を備えています[4、5]。しかし、純粋なPTOセラミックは、PTOセラミックの熱膨張の不一致、機械的伸縮力、マイクロクラックなどの問題があるため、高密度のモノリシックセラミックとして調製することは困難です。過去10年間で、固相反応[6]、ゾル-ゲル法[7、8]、水熱法[9、10]など、さまざまな経路によるPTO粉末の合成に多くの研究が費やされてきました。 Pechini法[11]、共沈[12]など。ただし、これらすべての方法で、純粋な結晶化強誘電体PTOを得るには、多かれ少なかれ高温での煆焼が必要です。残念ながら、高温での煆焼は通常、粒子サイズが粗い凝集粉末を生成するため、追加の粉砕プロセスが必要になります。フライス盤加工中の汚染やその他の望ましくない特徴により、製造された製品に欠陥が生じ、PTOセラミックの電気的特性が損なわれる可能性があります。
溶融塩合成(MSS)法は、ペロブスカイト酸化物電子セラミック粉末を調製する効果的な方法です。これは、構成材料(酸化物と炭酸塩)から純粋なペロブスカイト酸化物を比較的低温で短時間で合成するための媒体として使用される溶融塩を含みます。従来の固相反応と比較した反応時間[13]。最近、ペロブスカイトPTO粉末は、反応媒体としてNaClとNaCl-KClを使用した溶融フラックス反応によって合成されています[14、15、16]。球状のPTO粉末の形成は、溶解したPbOがTiO 2 に拡散することによって達成されました。 溶融塩の表面とその場で反応してPTOナノ粒子を形成し、次にPTOナノ粒子の核形成と成長を追跡します。 PTO粉末と比較して、MSS法によるPTO 1Dナノ材料(ナノロッド、ナノワイヤー、ナノチューブなど)の合成ははるかに遅れています。主な理由は、ペロブスカイト構造の対称性が高いためにPTOが立方体ブロックに成長しやすいため、高品質のPTO1Dナノ材料を合成する際の課題によるものです。現在まで、MSS法によるPTO1Dナノ材料の合成に関するいくつかの研究のみが文献で利用可能です。 Deng etal。 [17] NaCl溶融塩媒体中で界面活性剤(ポリオキシエチレン(9)ノニルフェニルエーテル、NP-9)支援アプローチを使用して、700°Cで直径50〜80 nm、長さ数マイクロメートルのPTOナノロッドを合成しました。 PTOナノロッドの成長は、微細なPTOナノ粒子の分散と、より大きな粒子への再堆積に起因し、NP-9界面活性剤とNaClのフラックスの複合効果の下で軸方向に沿ってナノロッドが形成されました。カイら[15]は、テンプレートMSS法による、直径0.1〜1.0μm、長さ数マイクロメートルまでの単結晶PTOナノロッドの合成について報告しました。ここでは、NP-9を界面活性剤として使用し、棒状のTiO 2 前駆体はチタン源のテンプレートとして使用されました。棒状のTiO 2 のサイズと形態 テンプレートは、合成されたPTO粒子に保持されました。同様に、針状のPTO粉末も、テンプレートMSS法を使用して合成されました。この方法では、純粋な針状のTiO 2 テンプレートとして粒子を使用しました[18]。テンプレートMSS法により800°Cで合成された針状のPTO粒子は、長さが30〜100μm、直径が500 nm〜2.0μmでした。
MSS法およびテンプレートMSS法によるPTOナノ材料の合成に関する上記の報告にもかかわらず、PTO粉末の誘電特性に関するデータはほとんどありません。さらに、テンプレートMSS法によるPTOナノロッドの形成メカニズムはよく理解されていません。この作業では、PbC 2 の反応による(テンプレート)MSS法による球形および棒状のPTO粉末の合成について報告します。 O 4 およびTiO 2 NP-9界面活性剤を使用せずに共晶NaCl-KCl塩で。棒状のPTO粉末の形成に及ぼす反応時間や溶融塩含有量などのテンプレートMSS法の処理パラメータの影響を詳細に調査した。結果は、溶融塩含有量が棒状のABO 3 の形成に重要な役割を果たしていることを示しています。 テンプレートMSSプロセスで立方晶または疑似立方晶の結晶構造を持つ化合物。溶融塩含有量が少ないと、棒状のTiO 2 であっても、PTOナノロッドを合成できません。 テンプレートは、テンプレートMSSプロセスで使用されます。 MSS法とテンプレートMSS法で合成された球形および棒状のPTO粉末の誘電特性も比較研究され、その結果、球形のPTO粉末がより優れた誘電特性を示すことが実証されました。
メソッド
資料
PbC 2 の分析グレード試薬 O 4 およびTiO 2 (アナターゼとルチルの球形の形態と混合相構造を持つ)は、Sigma-Aldrich(Shanghai)Trading Co.、Ltdから購入しました。NaClおよびKCl塩の分析グレードの試薬、K 2 CO 3 、AgNO 3、 およびHCl溶液は、Shanghai Chemical Reagent Co.、Ltd。から入手しました。
MSS法による球形のPTO粉末の合成
球形のPTO粉末は、PbC 2 の反応によるMSS法によって合成されました。 O 4 およびTiO 2 共晶NaCl-KCl塩中。 PbC 2 のモル比 O 4 :TiO 2 :NaCl:KClは、1:1:10:10、1:1:20:20、1:1:30:30、1:1:40:40、および1:1:60:60として選択されました。 PbC 2 の混合物 O 4 、TiO 2 、NaCl、およびKClを乳鉢と乳棒で30分間粉砕した後、アルミナるつぼで950°Cに5時間加熱しました。最後に、生成物を炉内で自然に室温まで冷却し、AgNO 3 で遊離塩化物イオンが検出されなくなるまで、脱イオン水で数回洗浄しました。 塩の完全な除去を確実にするための解決策。洗浄後、構造特性を明らかにするために、製品を120°Cで4時間乾燥させました。
テンプレートMSS法によるロッド状PTO粉末の合成
棒状のPTO粉末は、テンプレートMSS法を使用して合成されました。この方法では、棒状のアナターゼTiO 2 チタン源として粒子を使用した。棒状のTiO 2 テンプレートは棒状のK 2 から作成されました Ti 4 O 9 、林らによって以前に報告された手順に従う。 [19]。まず、K 2 CO 3 酸化物はTiO 2 と混合されました モル比が1:3の酸化物、次に混合物を1000℃で加熱し、18時間保持した。最後に、生成物を炉内で自然に室温まで冷却し、脱イオン水で数回洗浄して、残留するK 2 を除去した。 CO 3 。得られたK 2 の主産物 Ti 4 O 9 70°CのHCl溶液(1 Mの濃度)で2時間洗浄し、K 2 を抽出しました。 O、そして得られた相はTiO 2 でした ・nH 2 棒状のTiO 2 を得るために、それぞれ600°C、700°C、および800°Cで1時間アニールされたO 化合物。そして、PbC 2 O 4 棒状のTiO 2 と混合しました テンプレートとPbC 2 のモル比のNaCl-KCl溶融塩 O 4 :TiO 2 (テンプレート):NaCl:KClはそれぞれ1:1:20:20と1:1:60:60に等しい。 2つの混合物を800°Cで異なる時間(たとえば、1時間、5時間、および10時間)アニーリングしました。最終製品は、上記と同様の手順で洗浄および乾燥しました。
微細構造の特性評価
調製されたままのPTO粉末の相構造は、X線粉末回折(Rigaku D / Max-RA、CuKα放射線)によって特徴づけられました。ステップサイズは毎秒0.01°で、2θの範囲は15〜70°でした。 PTO製品の表面形態は、元素のX線エネルギー分散型分光法(EDS)(EX-250分光法、HORIBA Corporation)を備えた走査型電子顕微鏡(SEM、Hitachi S-3400 N II、30 kV)を使用して調べました。検出。 SEMサンプルは、カーボンテープに粉末を振りかけた後、必要に応じて金でコーティングして作成しました。
誘電測定
誘電特性の測定では、乾燥した球形および棒状のPTO粉末を、7 MPaの圧力下で、直径12 mm、厚さ1.0 mmのペレットにプレスし、空気中で1150°Cで2時間アニールしました。続いて、焼きなましされたペレットの表面を粉砕および研磨し、続いて両方の表面に銀ペーストを塗装した。次に、銀ペーストを550℃で60分間焼成しました。アニールされたPTO粉末の誘電率と誘電損失は、Agilent 4192Aインピーダンスアナライザーを使用して室温で10Hzから1MHzまで測定されました。
結果と考察
MSS法で合成されたPTO粉末の相構造と形態
さまざまな溶融塩含有量の下で950°Cで5時間MSS法によって合成されたPTO粉末のXRDパターンを図1に示します。すべてのXRD回折ピークが正方晶PTO(JCPDS No. 06–0452、 P 4 mm 空間群、格子定数 a =0.390nmおよび c =0.415 nm)、他の不純物相は検出されません。通常、2θ=45°領域のXRDパターンは、立方晶または正方晶のペロブスカイト構造の存在に特徴的です。この場合、約2θ=45 ° での立方(200)の正方晶(200)と(002)反射への分割 はっきりと観察され、純粋な正方晶強誘電相の形成を示しています。格子定数( a および c )正方晶PTO粉末は、次の式で計算できます。
$$ \ frac {1} {d ^ 2} =\ frac {h ^ 2 + {k} ^ 2} {a ^ 2} + \ frac {l ^ 2} {c ^ 2} $$(1)ここで d 隣接する( hkl )平面、および a および c 正方晶相構造の格子定数です。格子定数 a XRDパターンから計算されたPTO粉末の割合は、0.3905〜0.3911 nmの範囲であり、 c 0.4077〜0.4089nmの範囲で。詳細を表1に示します。 c / a 比率は1.043〜1.047の範囲で、平均値は1.045で、PTO単結晶の1.064よりも小さかった。図1に示すXRDパターンから、PTO粉末の相構造は溶融塩含有量の影響を受けないことがわかります。すべてのPTO粉末は、 P の空間群を持つ正方晶相構造で結晶化しました。 4 mm 。最近、密度汎関数理論計算と組み合わせたCALYPSO(粒子群最適化による結晶構造解析)構造探索法による0Dクラスターから3D結晶へのペロブスカイトPTOの構造進化に関する理論的研究により、PTOの基底状態構造が明らかになりました。周囲圧力での P 4 mm PTOクラスターと2DPTO二重層の相と準平面構造も周囲圧力で安定しています[20]。 PTO粉末のSEM-EDS検査を図2に示します。図2a〜eに示すSEM画像は、PTO粉末が、少数の棒状粒子のみを除いて、主に多くの球形ナノ粒子で構成されていることを示しています。 PbC 2 のモル比を上げると O 4 :TiO 2 :NaCl:KCl 1:1:10:10から1:1:60:60まで、図2a–eに示すように、PTO粉末の形態は明らかに変化しませんでした。つまり、同じ溶融塩の量が異なると、反応媒体としてのみ機能し、反応イオンの拡散速度に影響を与えるだけです。共晶NaCl-KCl溶融塩(共晶融点650°C)は、MSSプロセス中の反応物イオンの輸送を支援する比較的低温の液相反応環境を提供します。溶融塩への反応物の溶解度はMSSプロセスで重要な役割を果たし、合成されたままの生成物の反応速度と形態に重大な影響を与えることが報告されています[13]。本研究では、PbOはPbC 2 から分解されます。 O 4 400〜500°Cの温度での化学反応を介して[14]
$$ {\ mathrm {PbC}} _ 2 {\ mathrm {O}} _ 4 \ to \ mathrm {PbO} + \ mathrm {CO} \ uparrow + {\ mathrm {CO}} _ 2 \ uparrow $$(2)これは、TiO 2 よりもNaCl-KClの溶融塩への溶解度が高い(NaCl-KCl塩への溶解度は900°Cで30μmol/ g塩化物[21])。 (これは塩化アルカリへの溶解度が非常に低い[22])。したがって、溶融塩に溶けやすい反応物PbOは、球のようなTiO 2 の表面に拡散する可能性があります。 前駆体をその場で反応させ、溶液沈殿プロセスによって球形のPTO粉末を形成します。図2fに示す典型的なEDSスペクトルは、サンプルがPb、Ti、およびO元素で構成されていることを示しており、EDS分析により、化学組成が公称値とほぼ同じであることが確認されています。
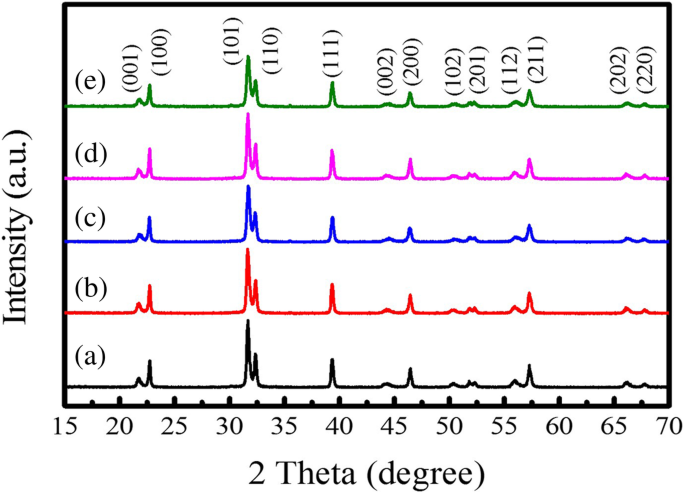
PbC 2 のモル比で950°Cで5時間MSS法によって合成された球形のPTO生成物のXRDパターン O 4 :TiO 2 :NaCl:KClは(a)1:1:10:10、(b)1:1:20:20、(c)1:1:30:30、(d)1:1:40:40、および(e)それぞれ1:1:60:60

PbC 2 のモル比で950°Cで5時間MSS法によって合成された球形のPTO製品のSEM画像 O 4 :TiO 2 :NaCl:KClは a に等しい 1:1:10:10、 b 1:1:20:20、 c 1:1:30:30、 d 1:1:40:40、および e それぞれ1:1:60:60。 f PbC 2 のモル比で950°Cで5時間合成された球形のPTO生成物から取得された典型的なEDSスペクトル O 4 :TiO 2 :NaCl:KClは1:1:10:10に等しい
テンプレートMSS法で合成されたロッド状PTO粉末の相構造と形態
テンプレートMSS法で棒状PTO粉末を合成する前に、TiO 2 の相構造と形態 テンプレートが最初に調査されました。図3は、TiO 2 のXRDパターンを示しています。 テンプレートをさまざまな温度で1時間アニーリングしました。 TiO 2 の主なアナターゼ相が観察されます 600°C(図3a)および700°C(図3b)でアニーリングした後、生成物に形成されました。ただし、一定量のK 2 Ti 4 O 9 まだ製品に保持されています。星で示されるXRD回折ピークは、K 2 に由来します。 Ti 4 O 9 フェーズ(ICDD番号32-0861)。焼きなまし温度を800°Cまで上げると(図3c)、不純なK 2 Ti 4 O 9 フェーズはほとんど消えました。図3cに示されているすべてのXRD回折ピークは、アナターゼ型TiO 2 に適切にインデックス付けできます。 (JCPDS No. 021–1272)、純粋なアナターゼ相TiO 2 の形成を示します 。 TiO 2 の結晶品質も注目されました。 (101)メイン回折ピークの強度が大幅に増加したため、テンプレートが大幅に改善されました。図4は、TiO 2 のSEM画像を示しています。 さまざまな温度でアニーリングされたテンプレート。すべてのTiO 2 テンプレートは棒状の形態を示し、平均長さを約12.0μmに保ちながら、アニーリング温度が上昇するにつれて、平均直径は490nmから570nm、次に500nmまで変化しました。 TiO 2 のアスペクト比 600°C、700°C、および800°Cでアニーリングされたテンプレートは、それぞれ約25、23、および24でした。アニールされたTiO 2 の棒状の形態 テンプレートは、アニーリングされたプロセスにおけるアナターゼ相構造の異方性成長に起因します。上記の実験結果に基づいて、TiO 2 800°Cで1時間アニーリングされたアナターゼ相のテンプレートは、高い結晶化度と棒状の形態を持ち、テンプレートMSS法を介して棒状のPTO粉末を合成する傾向があります。
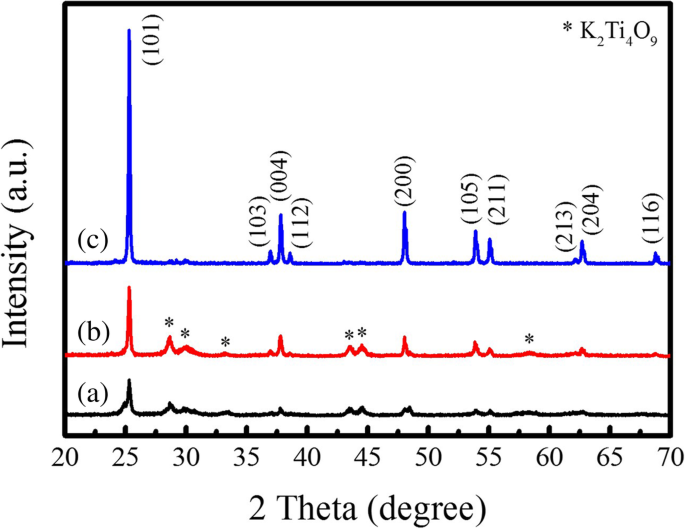
TiO 2 のXRDパターン テンプレートは、(a)600°C、(b)700°C、および(c)800°Cで1時間アニーリングされました

TiO 2 のSEM画像 a でアニーリングされたテンプレート 、 b 600°C; c 、 d 700°C;および e 、 f 800°Cで1時間
図5は、800°Cでさまざまな反応時間でテンプレートMSS法によって合成されたPTO粉末のXRDパターンを示しています。ここで、棒状のTiO 2 テンプレート(800°Cで1時間アニールしたアナターゼ相)をチタン源およびPbC 2 のモル比として使用しました。 O 4 :TiO 2 (テンプレート):NaCl:KClは1:1:20:20に等しかった。 XRD回折パターンは、すべてのPTO粉末が正方晶相構造(JCPDS No. 06–0452)で結晶化し、他の不純物相が検出されないことを示しており、純粋な正方晶相構造の形成を示しています。 PTO粉末の格子定数はXRDパターンから推定されました。詳細は表2に示されています。PTO粉末の対応するSEM画像を図6に示します。図6aに示すように、アニールされたPTO粉末の形態800°Cで1時間は、いくつかの棒状の粒子と大量の球状のPTO粒子の組み合わせです。棒状PTO粒子の定性体積分率はわずか約3%であり、棒状PTO粒子の平均直径は約860 nm、長さは4.50μmでした。しかし、反応時間を1hから5hに増やすと、棒状PTO粒子の体積分率は約2.4%に減少し(図6c)、棒状PTO粒子の平均直径は約930でした。 nmおよび6.0μmの長さ。反応時間をさらに10時間まで延長すると(図6e)、PTO製品では棒状のPTO粒子はほとんど観察されませんでしたが、球状のPTO粒子が大量に形成されました(図6e-fを参照)。つまり、反応時間を長くすると、球状のPTO粒子の形成が促進され、棒状のPTO粒子の形成が抑制されます。 800°Cで10時間アニールした球状PTO粒子の平均粒子サイズは約550nmであり(図6e)、棒状のTiO 2 の直径よりわずかに大きかった。 テンプレート(480 nm)(図4e)。 800°Cで10時間アニールした製品に大量の球状PTO粒子が形成されたのは、棒状のTiO 2 が原因である可能性があります。 テンプレートは、テンプレートMSSプロセス中に小さな球状粒子に分解され、溶解したPbO(PbC 2 から分解)と反応します。 O 4 )NaCl-KCl溶融塩中で、溶液沈殿メカニズムを介して球状のPTO粉末を形成します。 TiO 2 の壊れた痕跡 テンプレートは図6bおよびdで観察され、いくつかの球状PTO粒子が互いに結合して、瓢箪糸の形状を形成しました。棒状のPTO粉末は、溶融塩含有量が少ない場合、テンプレートMSS法ではうまく合成されないようです。
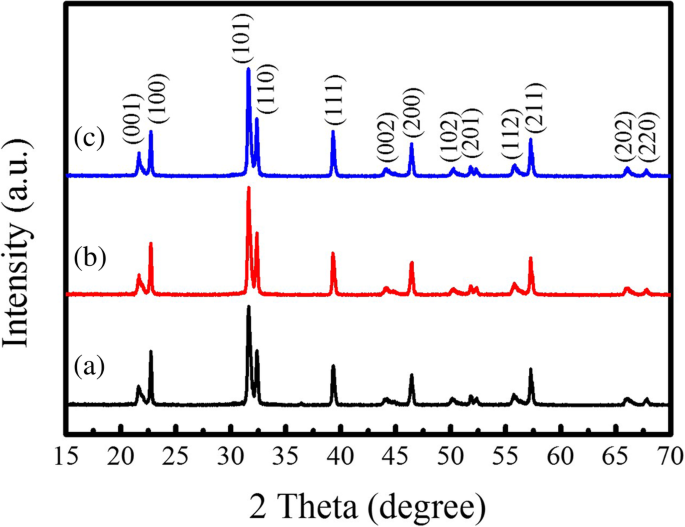
PbC 2 のモル比でテンプレートMSS法を介して合成されたPTO粉末のXRDパターン O 4 :TiO 2 (テンプレート):NaCl:KClは1:1:20:20に等しく、800°Cで(a)1 h、(b)5 h、および(c)10 h

PbC 2 のモル比でテンプレートMSS法を介して合成されたPTO製品のSEM画像 O 4 :TiO 2 (テンプレート):NaCl:KClは1:1:20:20に等しく、 a の間800°Cでアニーリングされます 、 b 1 h; c 、 d 5 h;および e 、 f 10 h
MSSプロセスでは、高温で溶融塩フラックスを介して粒子が成長し、溶融塩含有量が粒子成長速度と最終製品の形態を制御することが知られています[23]。溶融塩含有量を増やすと、高温で大量の溶融塩液が形成されます。したがって、溶解した反応イオン(例えば、鉛イオン)は、溶融塩液中で効果的に分離され、それらの濃度は、飽和濃度を達成するためにより長い時間を必要とする。したがって、不溶性TiO 2 の表面でのPTOナノクリスタライトの核形成速度 テンプレート粒子を減らす必要があります。形成されたPTOナノクリスタライトは、溶融塩含有量の高い環境で棒状のPTO粒子に再結合するのに十分な時間があります。つまり、高い溶融塩含有量の環境は、テンプレートMSSプロセスで棒状のPTO粒子を合成するのに役立ちます。そのため、PbC 2 のモル比を上げました。 O 4 :TiO 2 (テンプレート):NaCl:KClは1:1:60:60までで、それらの混合物は800°Cでさまざまな時間アニーリングされました。図7は、高い溶融塩含有量の下でテンプレートMSS法によって800°Cで合成されたPTO粉末のXRDパターンを示しています。 800°Cで5時間(図7b)および10時間(図7c)アニーリングしたPTO粉末は、純粋な正方晶相を持っていることがわかりました。ただし、800°Cで1時間アニールしたPTO粉末(図7a)は、Ti 3 の小さな不純相を除いて、主な正方晶相を持っていました。 O 5 およびTiO 2 。格子定数 a および c 800°Cでさまざまな時間アニールしたPTO粉末の割合を計算し、表2に示します。 c / a 比率は約1.050でした。対応するPTO粉末の表面形態を図8に示します。図8aでは、800°Cで1時間アニールしたPTO粉末が棒状および球状の粒子で構成されていることが観察されます。 SEM画像から推定された棒状粒子の定性体積分率は約70%でした。棒状粒子の直径は480nmから1.50μmまで変化し、長さは3.0–7.0μmの範囲でした。図8bに示す局所的な拡大SEM画像は、棒状のPTO粉末が非常に小さなPTOナノ結晶で構成されていることを示しており、棒状のTiO 2 の痕跡が壊れていることを示しています。 テンプレートMSSプロセス中のテンプレート。反応時間を1時間から5時間に増やすと、最終製品中の棒状PTO粉末の体積分率は約97%まで増加しました(図8c)。棒状のPTO粉末の長さは、7.0〜10.0μmの範囲でした。ただし、反応時間をさらに10時間まで延長すると(図8e)、最終製品中の棒状PTO粒子の体積分率は約85%であり、PTO棒の長さは3.5〜の範囲でした。 6.5μm。棒状のPTO粉末の直径は、970 nm〜1.50μmの範囲でした。
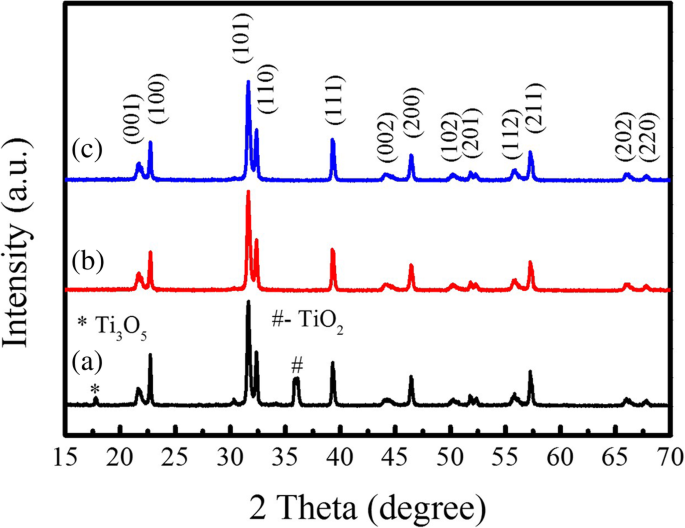
PbC 2 のモル比でテンプレートMSS法を介して合成されたPTO粉末のXRDパターン O 4 :TiO 2 (テンプレート):NaCl:KClは1:1:60:60に等しく、800°Cで(a)1 h、(b)5 h、および(c)10 h
の間アニーリングされます。
PbC 2 のモル比でテンプレートMSS法を介して合成されたPTO粉末のSEM画像 O 4 :TiO 2 (テンプレート):NaCl:KClは1:1:60:60に等しく、 a の場合は800°Cで 、 b 1 h; c 、 d 5 h;および e 、 f 10 h
テンプレートMSS法による高溶融塩含有量下での棒状PTO粉末の形成は、以下のプロセスによって理解することができます。テンプレートMSSプロセスでは、PbC 2 O 4 最初にPbO、CO、およびCO 2 に分解されます 400〜500°Cの温度範囲で、PbOは800°Cで溶融塩液に溶解します(NaCl-KCl塩への溶解度は800°Cで14μmol/ g塩化物です[21])。溶解したPbOは棒状のTiO 2 の表面に拡散します テンプレートを作成し、TiO 2 と反応します 800°Cでの化学反応を介してその場でPTOナノクリスタライトを形成する
$$ \ mathrm {PbO} + {\ mathrm {TiO}} _ 2 \ to {\ mathrm {PbTiO}} _3 $$(3)溶融塩含有量が非常に高いため(PbC 2 のモル比 O 4 :TiO 2 (テンプレート):NaCl:KClは1:1:60:60に等しい)、したがって、溶解した鉛イオンは溶融塩液中で効果的に分離されるため、その濃度が飽和濃度に達するまでに長い時間が必要です。棒状のTiO 2 テンプレートは、NaCl-KCl塩への溶解度が非常に低く、小さなTiO 2 に分解されます。 高溶融塩含有環境下での高温での球状粒子。したがって、溶解したPbOは壊れたTiO 2 と反応します。 それらの表面に粒子があり、PTOナノクリスタライトを形成します。これらのPTOナノクリスタライトは、溶融塩含有量の高い環境下で棒状のPTO粒子に再結合するのに十分な時間があります。図8cに示すように、直径が480 nm〜1.50μmの範囲で長さが10μmまでの大規模な多結晶棒状PTO粉末が合成されました。それらは、図8dに見られるように、小さなナノクリスタライトで構成されています。 MSSプロセスでのPTO粒子とテンプレートMSSプロセスでの棒状PTO粉末の形成を示す概略図を図9に示します。現在の作業は、溶融塩含有量が棒状の形成に重要な役割を果たしていることを示しています。 ABO 3 テンプレートMSSプロセスで立方晶または疑似立方晶の結晶構造を持つ化合物。つまり、溶融塩含有量が少ないと、棒状のTiO 2 であっても、棒状のPTO粉末は合成できません。 テンプレートは、テンプレートMSSプロセスで使用されます。単結晶PTOロッドではなく、砂糖ひょうたんストリングの形をした多結晶ロッド状PTO粉末の形成には、さらに調査が必要です。
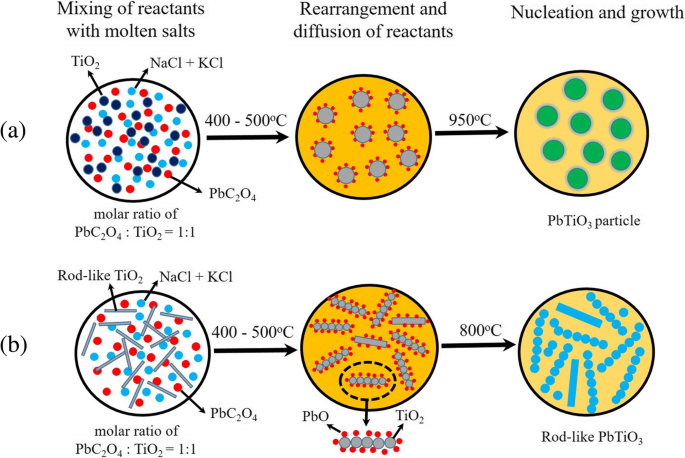
Schematic diagrams illustrating the formation of (a) PTO particles in the MSS process and (b) rod-like PTO powders in the template MSS process
Dielectric Properties of Spherical and Rod-Like PTO Powders
The dielectric constants (εr ) and dielectric losses (tanδ ) of the spherical and rod-like PTO powders synthesized by MSS and template MSS methods are shown in Fig. 10, which are measured at room temperature as a function of the frequency. Similar frequency-dependent dielectric behaviors are observed in the spherical and rod-like PTO powders. As shown in Fig. 10a, the sphere-like PTO powders (a) and (b) synthesized by MSS method at 950 °C for 5 h with the molar ratios of PbC2 O 4 :TiO2 :NaCl:KCl equal to (a) 1:1:30:30 and (b) 1:1:60:60, respectively, have much higher dielectric constants than the rod-like PTO powders (c) and (d) synthesized by template MSS method at 800 °C for (c) 5 h and (d) 10 h with the molar ratio of PbC2 O 4 :TiO2 (template):NaCl:KCl equal to 1:1:60:60. It is noticed that the dielectric constants of the sphere-like PTO powders (a) and (b) have decreased fast (from ~ 3000 to ~ 700) in the frequency range below 10 3 Hz, then reduced slowly with further increasing the frequency over 10 3 Hz, and finally become a constant value of ~ 340 at a higher frequency over 10 5 Hz. The fast decrease of the dielectric constant at lower frequencies is ascribed to the space charge polarization effect, which is correlated to the non-uniform charge accumulation at grain boundaries within the sphere-like PTO powders. The slow reduction of the dielectric constant is due to that the dipoles present in the PTO powders could not reorient themselves as fast as the frequency of an alternating electric field, resulting in a decrease of the dielectric constants [24]. In contrast, the rod-like PTO powders (c) and (d) synthesized by template MSS method exhibit a slight frequency-dependent dielectric behavior, their dielectric constants are slightly reduced with increasing frequency below 10 3 Hz, and then become a constant value of ~ 140. It is observed in Fig. 10b that all the dielectric losses of the spherical and rod-like PTO powders are decreased with increasing frequency due to the existence of the space charge polarization in all the PTO powders. The dielectric loss of the PTO powder (b) has the highest value, which has reduced fast with increasing frequency below 10 5 Hz, and then it becomes constant. The dielectric losses of the PTO powder (a) are reduced slowly with increasing frequency, which has the lowest value as compared with the other three PTO samples. The dielectric losses of the spherical PTO powders (c) and (d) synthesized by template MSS method exhibit very similar dielectric behavior, their dielectric losses are reduced slowly as the frequency increases. At room temperature, the dielectric constant and dielectric loss of the spherical PTO powders (a) measured at 10 6 Hz were ~ 340 and 0.06, respectively. The corresponding values for the spherical PTO powders (b) were 155 and 0.12, 140 and 0.08 for the rod-like PTO powders (c), and 130 and 0.07 for the rod-like PTO powders (d). Therefore, the sphere-like PTO powders (a) have high dielectric constant and low dielectric loss, and these dielectric data are better than that reported previously for the PTO nanoparticles synthesized via sol-gel process and annealed at 600 °C for 6 h (the dielectric constant and dielectric loss at 10 6 Hz were about 15 and 0.40) [25], and for the PTO nanoparticles synthesized by stearic acid gel method and annealed at 400 °C for 1 h (the dielectric constant and dielectric loss at 10 6 Hz were about 50 and 0.002) [26]. Normally, to measure the dielectric properties of PbTiO3 ceramics prepared from the nanopowders synthesized by chemical methods such as the sol-gel method [27], hydrothermal method [28, 29], or by physical method such as high-energy ball milling technique [30], PbTiO3 powder samples are usually pressed into pellets under a hydraulic press (using 1 cm diameter die). For making dense PbTiO3 ceramics, the samples are needed to be sintered at high temperatures (e.g., 900 °C or 1000 °C for 2 h in air) followed by furnace cooling. Leonarska et al. [28] synthesized the PTO nanopowders at 490 K for 2 h by hydrothermal method and then prepared the PTO ceramics from the as-synthesized PTO nanopowders and sintered it at 1240 K for 1.5 h. They checked the impact of high-temperature process on the morphology or crystallization degree of the PTO ceramics by SEM observations and found that the PTO ceramics had slightly larger and rounded ceramic grains in comparison with the nanoparticles obtained directly from hydrothermal method. Similarly, Hu et al. [29] also reported the preparation of PTO nanoceramics (with grain sizes of ~ 200 nm) under sintering process (at 950 °C for 2 h in air) using the hydrothermal PTO nanopowders (with average grain size of ~ 100 nm) as the raw materials. This result indicates the sintering process of the hydrothermal PTO nanopowders can increase the grain size. Kong et al. [30] prepared the PTO nanopowders (with average grain size of ~ 10 nm) by high-energy ball milling technique, and pressed them directly into green pellets and sintered at 1100 °C for 1 h. Crack-free PTO ceramics with 95% of the theoretical density were successfully obtained. SEM images revealed that the average grain size of the sintered samples were < 1.5 μm. In the present work, we have prepared dense PbTiO3 ceramic samples under a sintering process (at 1150 °C for 2 h) by using the as-synthesized sphere-like PTO powders via MSS method and the as-synthesized rod-like PTO powders via template MSS method. The high-temperature process has improved the crystallized quality and the grain sizes of the PTO powders but has few effects on the morphology. The best dielectric properties of the PTO ceramics prepared the as-synthesized spherical PTO powders by MSS method are attributed to their larger average particle size (~ 2.0 μm).
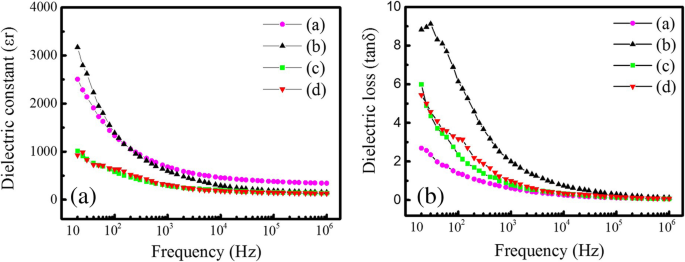
a Dielectric constants (εr ) and b dielectric losses (tanδ ) of the PTO powders synthesized by MSS method and template MSS method. Samples (a) and (b) were synthesized by MSS method at 950 °C for 5 h with the molar ratios of PbC2 O 4 :TiO2 :NaCl:KCl equal to 1:1:30:30 and 1:1:60:60, respectively. Samples (c) and (d) were synthesized by template MSS method with the molar ratio of PbC2 O 4 :TiO2 (rod-like template):NaCl:KCl equal to 1:1:60:60 and annealed 800 °C for 5 h and 10 h, respectively
Conclusions
Both sphere- and rod-like PTO powders were synthesized by MSS and template MSS methods, respectively. XRD patterns reveal that all the PTO powders are crystallized in a tetragonal phase structure. SEM images demonstrated that increasing the molar ratio of PbC2 O 4 :TiO2 :NaCl:KCl from 1:1:10:10 to 1:1:60:60 in the MSS process had little effect on the sphere-like morphology of the PTO powders synthesized by MSS method. Large-scale polycrystalline rod-like PTO powders with length up to 10 μm and diameters in the range of 480 nm–1.50 μm were successfully synthesized by template MSS method at 800 °C for 5 h, where the rod-like anatase TiO2 precursors were used as a titanium source and the molar ratio of PbC2 O 4 :TiO2 :NaCl:KCl was equal to 1:1:60:60. It is found that under low molten salt content, extending the reaction time promoted the formation of sphere-like PTO particles whereas the formation of rod-like PTO particles was suppressed. In addition, the rod-like PTO powders cannot be synthesized even if the rod-like TiO2 templates are used. Dielectric measurements demonstrated that the dielectric constants of the sphere-like PTO powders synthesized by MSS method decreased fast from ~ 3000 to ~ 700 at low frequencies below 10 3 Hz, and at high frequencies over 10 5 Hz they became a constant value of ~ 340. The fast decrease of the dielectric constant at low frequencies is ascribed to the space charge polarization due to the non-uniform charges accumulated within the PTO powders. The rod-like PTO powders synthesized by template MSS method exhibited slight frequency-dependent dielectric behavior, their dielectric constants decreased slowly at the frequencies below 10 3 Hz and then remained a constant value of ~ 140 as the frequency increased up to 10 6 Hz. At room temperature, dielectric constant and dielectric loss (measured at 10 6 Hz) of the sphere-like PTO powders synthesized by MSS method at 950 °C for 5 h with low molten salt content (the molar ratio of PbC2 O 4 :TiO2 :NaCl:KCl equal to 1:1:30:30) were 340 and 0.06, respectively, and the corresponding values were 155 and 0.12 for the sphere-like PTO powders synthesized by MSS method with high molten salt content (the molar ratio of PbC2 O 4 :TiO2 :NaCl:KCl equal to 1:1:60:60). The dielectric constant and dielectric loss for the rod-like PTO powders synthesized by template MSS method at 800 °C for 5 h and 10 h under high molten salt content (the molar ratio of PbC2 O 4 :TiO2 (rod-like template):NaCl:KCl equal to 1:1:60:60) were 140 and 0.08, and 130 and 0.07, respectively. The higher dielectric constant and lower dielectric loss of the sphere-like PTO powders synthesized at 950 °C for 5 h by MSS method with the molar ratio of PbC2 O 4 :TiO2 :NaCl:KCl equal to 1:1:30:30 are ascribed to their large average particle size (~ 2.0 μm), which have promising applications in multilayer capacitors and resonators.
略語
- CALYPSO:
-
Crystal Structure AnaLYsis by Particle Swarm Optimization
- EDS:
-
Energy Dispersive Spectroscopy
- MSS:
-
Molten Salt Synthesis
- NP-9:
-
Polyoxyethylene (9) Nonylphenyl Ether
- PTO:
-
PbTiO3
- SEM:
-
Scanning Electron Microscopy
- XRD:
-
X-ray Diffraction
ナノマテリアル
- 小さなセレンナノ結晶とナノロッドの容易な合成と光学的性質
- ゾル-ゲル法によるナノ構造シリカ/金-セルロース結合アミノ-POSSハイブリッド複合材料とその特性
- 脂肪族エポキシ樹脂と過塩素酸リチウムの塩に基づくイオン伝導性有機-無機ポリマー複合材料の構造的特異性
- MnХFe3−XО4スピネルの構造的および磁気的特性に及ぼす接触非平衡プラズマの影響
- 微結晶およびナノセルロースの構造と誘電特性に及ぼす水の影響
- 水溶性α-NaGdF4/β-NaYF4:Yb、Erコアシェルナノ粒子の合成と発光特性
- 着色された低温顔料用のCrドープTiO2の構造的および可視近赤外光学特性
- 水溶性硫化アンチモン量子ドットの合成とそれらの光電特性
- 蒸発誘起自己組織化と強化されたガス検知特性によるワームホールのようなメソポーラス酸化スズの容易な合成
- Ag n V(n =1–12)クラスターの構造的、電子的、および磁気的特性の調査
- グラフェン/ Ag3PO4量子ドット複合材料の簡単なワンステップソノケミカル合成と光触媒特性



