蛍光ナノバイオマスドット:超音波支援抽出およびFe3 +検出用のナノプローブとしてのそれらの応用
要約
持続可能で再生可能な資源としてのバイオマスは、人間の生命にとって重要なエネルギー源の1つです。ここで、発光ナノバイオマスドット(NBD)は、バイオマスに蛍光特性を与える超音波法によって大豆から抽出されました。調製されたままのNBDは、平均直径2.4 nmのアモルファス構造であり、16.7%の量子収率で明るい青色の蛍光を示します。食用原料と加熱のない合成プロセスの恩恵を受けて、細胞毒性試験は、NBDの濃度が800μg/ mlに達しても細胞生存率が100%を維持することを示し、NBDの良好な生体適合性を示しています。さらに、NBDの蛍光はFe 3+ に非常に敏感です。 、Fe 3+ に使用できます それらの健康上の優位性の観点からの検出。提案されたセンサーの検出限界(LOD)は2.9μMと決定されました。これはFe 3+ の最大許容レベルよりも低い値です。 (5.37μM)飲料水中。
背景
発光ナノ材料は、特に発光ダイオード、検出器、バイオイメージング、および金属イオン検出において、その独自の光学特性により、さまざまな用途に使用されています[1,2,3,4,5,6]。これまで、半導体量子ドット(QD)、カーボンナノドット、硫黄QDなど、さまざまな発光ナノ材料が報告されており、多くの分野で多くの進歩を遂げてきました[7,8,9,10,11,12]。 。発光ナノ材料の優れた代表としてのQDは、その優れた光学的および電気的特性により、多くの分野で使用されてきました。これらすべてにもかかわらず、QDの毒性は依然としてそれらのアプリケーションを大幅に制限します[13、14]。発光を備えた、より環境に優しく、より持続可能なナノ材料を見つけることは常に非常に重要です。バイオマスは、光合成によって生成できる独自の有機物であり、その持続可能で再生可能な特性が強調されています。具体的には、バイオマスは、生物の生成物、廃棄物、および残留物の生分解性画分として定義されます[15、16]。ナノテクノロジーの文脈では、バイオマスは通常、前駆体として使用され、特別な処理の後、いくつかの特定の光学特性を備えたナノドットに変えることができます。化学的前駆体と比較して、バイオマス、特に食用バイオマスの主成分は糖とタンパク質であり、これらはその後の処理で無害です。したがって、ナノバイオマスドット(NBD)は生体適合性が高く、有害物質を生成することなく生物学および環境分野でのアプリケーションを保証する必要があります。
これまで、バイオマス由来の蛍光カーボンナノドットのみが報告されています。基本的に、葉、卵白、レモン果汁などの一部の天然バイオマスは、蛍光カーボンナノ粒子を合成するために水熱法で処理されました[17、18、19]。食用食品に存在する別の種類のカーボンナノドットもあり、これらは天然バイオマスのさらなる処理で生成されます[20、21]。例外なく、それらはすべて高温炭化の典型的なプロセスを含んでいました。この工程は長時間と高温を伴う可能性があり、大規模なバッチ生産を達成することは困難です[22]。高温と比較して、室温または低温条件は実行が容易であり、バイオマス自体の本来の特性を維持します。
ナノプローブは、発光ナノ材料の重要な用途の1つです[23]。明るい蛍光と高い生体適合性を考慮すると、NBDは生物学と環境の分野で一種のナノプローブとして使用される可能性があります。 Fe 3+ は人体の重要な金属イオンであり、ヘモグロビンとミオグロビンの合成に重要な役割を果たします[24]。しかし、過剰なFe 3+ 体内に蓄積すると、組織の損傷や臓器不全につながる可能性があります。 Fe 3+ の定性的および定量的測定のための効果的で環境に優しいセンシングシステムの開発 臨床、医療、および環境問題にとって非常に重要です。これにより、バイオマスを処理せずに、天然の食用バイオマスから直接、望ましい特性を備えたナノドットに調整できるかどうかを検討できます。しかし、そのような発光NBDはどれも私たちの知る限り報告されていません。したがって、望ましい特性と高い生体適合性を備えたNBDを取得するために、より天然のバイオマス前駆体を探すことは、より環境に優しい発光ナノ材料とFe 3+ に向けた一歩を踏み出す可能性があります。 検出。
ここでは、発光ナノバイオマスドット(NBDs)は、大豆からの超音波抽出戦略(UES)を介して初めて実証されました。調製されたままのNBDのフォトルミネッセンス(PL)量子収率(QY)は16.7%に達する可能性があり、NBDは固体状態で明るい発光を示します。細胞毒性試験は、NBDが高い生体適合性を持っていることを示しています。さらに、NBDはFe 3+ に採用されています Fe 3+ への線形依存性の蛍光強度の検出 濃度、および検出限界(LOD)は2.9μMに達する可能性があります。
メソッド
資料
中華人民共和国の国家基準( GB1352-2009 )に準拠した北東部の大豆の品種 )地元のスーパーマーケットから購入し、使用前に蒸留水で数回洗浄しました。塩化カルシウム(CaCl 2 )、塩化マンガン(MnCl 2 )、塩化第二銅(CuCl 2 )、塩化コバルト(CoCl 2 )、硝酸鉛(Pb(NO 3 ) 2 )、および硝酸クロム(Cr(NO 3 ) 3 )はAladdin Ltd.(上海、中国)から購入しました。塩化第二鉄(FeCl 3 )、塩化第一鉄(FeCl 2 )、塩化カドミウム(CdCl 2 )、二塩化水銀(HgCl 2 )、塩化ナトリウム(NaCl)、および塩化亜鉛(ZnCl 2 )は、Sinopharm Chemical Reagent Co.、Ltd。(Shanghai、China)から入手しました。すべての化学物質は分析試薬(純度> 99.0%)であり、さらに精製することなく受け取ったままの状態で使用されます。
NBDの合成
まず、100個の大豆をアルコールと蒸留水の混合物で3回洗浄して不純物を除去しました。次に、大豆を50 mlの蒸留水を入れたビーカーに入れ、2時間超音波処理しました。この過程で、溶液の色が透明から濃い黄色に変化し、大豆の皮がナノサイズに調整されてNBDを形成したことを示しています。次に、暗黄色の溶液を遠心分離管に移し、7000rpmで3分間2回遠心分離して大きなサイズの粒子を除去した後、上澄みを0.22μMの膜で濾過して大きな粒子または凝集した粒子をさらに除去した。その後、溶液を冷蔵庫に入れ、-5 ° で凍結処理した。 6時間C。次に、-50 ° の凍結乾燥機に移しました。 粉末を得るために12時間C。凍結した粉末を水に分散させてNBDを形成し、さらに塗布しました。
特性評価
NBDのX線回折(XRD)パターンは、X'PertPro回折計を使用して記録されました。X線はCu-Kα源によって生成されました。 JEM-2010透過型電子顕微鏡(TEM)を使用して、NBDのサイズと結晶化度を特性評価しました。 NBDの蛍光スペクトルはF-7000蛍光分光光度計で得られました。 NBDのUV-Vis吸収スペクトルは、UH4150分光光度計を使用して取得しました。サンプルのフーリエ変換赤外(FTIR)スペクトルは、Thermo Scientific Nicolet iS10FTIR分光計によって記録されました。サンプルのX線光電子分光法(XPS)スペクトルは、Al-KαX線放射源を備えたThermo Fisher Scientific ESCALAB250Xi分光計を使用して収集されました。
フォトルミネッセンス量子収率測定
PL QYは、積分球を備えたF-9000分光蛍光光度計を使用してテストされました。まず、NBD水溶液を0.1未満の吸収強度に希釈しました。次に、この水溶液を蛍光キュベットに加え、積分球に入れ、370nmの単色光で励起しました。蛍光スペクトルは、430〜450nmの範囲で収集されました。一方、純水の同じ蛍光スペクトルも同じ条件下で記録されました。最後に、PL QYは、サンプルと水の両方のPLスペクトルに基づいて蛍光ソフトウェアを使用して計算されました。
細胞毒性試験
NBDの細胞毒性は、MTT(3-(4,5)-ジメチルチアヒアゾ(-z-y1)-3,5-ジフェニルテトラゾリューモルミド)法によって評価されます。細胞は、5%CO 2 中の10%ウシ胎児血清を含む通常のRPMI-1640で培養されました。 そして37 ° で95%の空気 加湿インキュベーター内のC。細胞生存率を測定するために、HeLa細胞を96ウェルプレートに入れ、72時間インキュベートしました。 Hela細胞をさまざまな濃度のNBDおよびCDと72時間インキュベートした後、細胞の生存率を記録しました。
Feの検出 3+
さまざまな濃度のFe 3+ を含む1mlの溶液 PL測定の前に、3 g / lの溶液を含む1mlのNBDに添加しました。溶液を完全に混合し、室温で1分間反応させた後、関連する蛍光スペクトルを記録しました。 PL測定は370nmの励起下で実行されました。
結果と考察
形態と化学組成
NBDは、UESメソッドを介して作成されています。すべてのプロセスはスキーム1に示されています。図1aおよびbに示すように、NBDのサイズと形態は透過型電子顕微鏡(TEM)によって特徴づけられました。 TEM画像は、NBDの形状がほぼ球形であることを示しています。 NBDの直径は1〜3 nmの範囲で、平均直径は2.4 nmであり、対応するサイズ分布を図1cに示します。 NBDの格子縞は、高解像度TEM画像(図1bの挿入図)からは観察できません。これは、NBDのアモルファス性を示しています。高角度環状暗視野走査透過電子顕微鏡(HAADF-STEM)の画像と、それに対応するNBDの元素マッピング(炭素、窒素、酸素)を図1d–gに示します。 NBDの主要な元素は炭素、窒素、および酸素であることがわかります。さらに、ソリッドステート 13 NBDのC核磁気共鳴(NMR)測定を図1hに示します。シグナルの範囲は160〜180 ppmで、164ppmと170ppmのピークはC =O結合に対応しており、sp 2 を示しています。 炭素原子[25、26]。
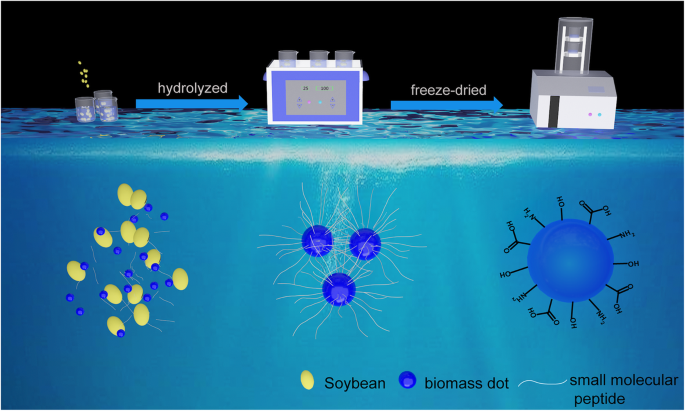
大豆からのNBDの調製プロセスの概略図
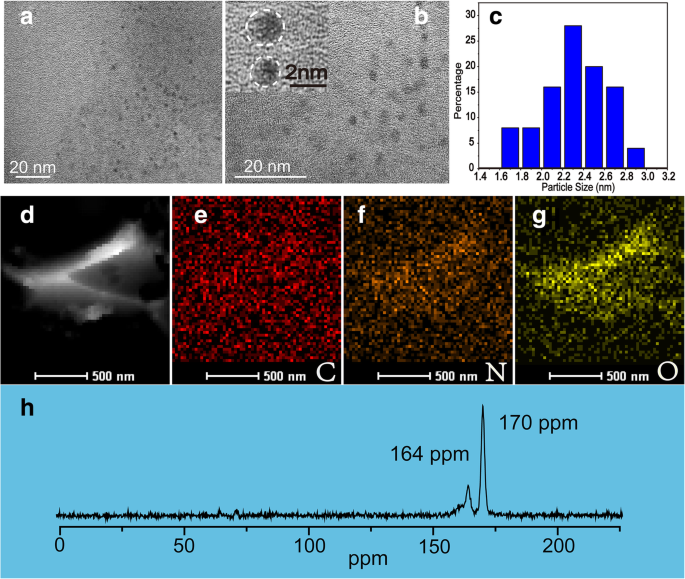
NBDのTEM画像( a )および( b )。 c NBDの粒度分布。 HAADF画像( d )および対応する炭素の元素分布マッピング( e )、窒素( f )、および酸素( g )
NBDの構造特性をさらに研究するために、X線回折(XRD)パターンを記録しました。図2aに示すように、典型的なXRDパターンは、約21.5 o にある広いピークを示しています。 ショルダーピークは約41.0 o 、これはアモルファスカーボン相に起因する可能性があります[27]。さらに、図2(b)に示すように、大豆とNBDの特徴的な吸収ピークをフーリエ変換赤外(FTIR)分光法で調べました。約3380cm -1 の吸収帯 O–H / –N–Hの伸縮振動、約2906 cm -1 のバンドに割り当てることができます。 C–H伸縮振動、および約1650 cm -1 のバンド C =O伸縮振動に。 1400 cm -1 のピーク および1071cm -1 それぞれC–HおよびC–O曲げ振動に対応します[28]。大豆とNBDのスペクトルには、約1750 cm -1 で明らかな違いがあります。 、これは大豆の脂質からのC =O結合の伸縮振動に属します[29、30]。水溶液に不溶性の脂質は、水に浸したときにサンプルから分離され、NBDのFTIRスペクトルの結合が消失しました。サンプルの還元されたC =O結合は、タンパク質のカルボキシル基に由来します。ピークは約1543cm -1 を中心としました 大豆の浸漬過程でのタンパク質分解に起因する可能性もあります。超音波プロセスの前後のすべてのピークを比較すると、NBDの表面に–OH、–C =O(アミドI)、および–NH基が形成されていることがわかります[31]。上記の結果は、NBDの表面にヒドロキシル、アミドゲン、およびカルボキシル基が存在することを示しており、これらの官能基は、水溶液中のNBDの親水性と安定性に重要な役割を果たします。図2cに示すように、X線光電子分光法(XPS)スペクトルを実行して、NBDの成分をさらに解明しました。 XPSスペクトルは、532.0、401.1、および286.1 eVに3つの強いピークを示しています。これは、それぞれO 1s、N 1s(図2d)、およびC 1s(図2e)に起因する可能性があります[32]。これらの結果は、NBDには主にC(64.33%)、O(32.34%)、N(2.72%)、および限られた量のPが含まれており、P元素は大豆のリン脂質に由来する可能性があることを示しています[33]。 。高分解能XPSスペクトルでは、C 1sスペクトルは287.6、285.8、および284.6 eVに3つのピークを表示します。これは、C =O、C–O / C–N、およびC–C / C =Cに割り当てることができます。図2cに示すように、グループ。 C =O結合は可溶性カルボキシル基に由来します[24]。 C–O / C =NおよびC–C / C =Cは、亜酸化窒素およびsp 2 に由来します。 / sp 3 それぞれ炭素[34]。図2dに示すN1sスペクトルは、399.5eVと401.6eVの2つの主要なバンドを確認し、FTIR分析と一致するピリジニックNとピロリックNの存在を示しています。図2fに示されているO1sスペクトルには、531.4eVと533.0eVに2つのピークがあり、それぞれC–OH / C–O–CグループとC =Oグループに起因する可能性があります[9]。
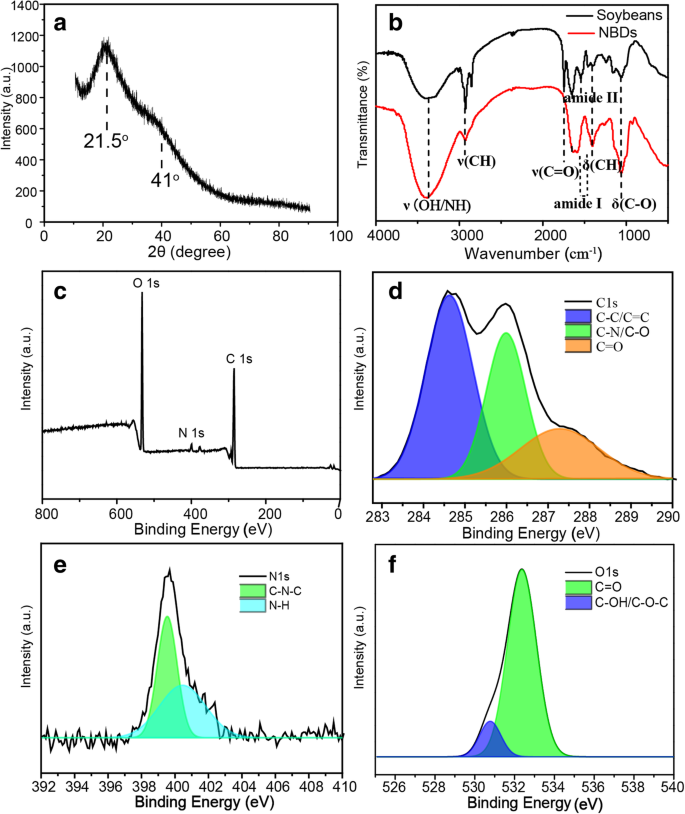
a NBDのXRDパターン。 b 大豆とNBDのFTIRスペクトル。 c NBDのXPS調査スペクトル。 C 1sの高分解能XPSスペクトル( d )、N 1s( e )、およびO 1s( f )
上記の分析に基づいて、大豆からのNBDの形成の可能なメカニズムが提案された。まず、溶液中に浮遊しているバイオマスのいくつかの大きな粒子は、超音波脳震盪によってナノメートルサイズに分解されます。超音波抽出処理前後の溶液の変化は、追加ファイル1:図S1に示されています。次に、上記の過程で大豆中のタンパク質を低分子ペプチドとアミノ酸に加水分解し、ナノサイズのバイオマスに多くの小分子ペプチド鎖を結合させて、表面機能性の高いバイオマスドットを形成します。バイオマスドットの表面の官能基は、蛍光の主な原因です。メカニズムによると、リョクトウも前駆体として使用され、追加ファイル1:図S2に示すように、青色蛍光NBDも取得されました。
光学特性
NBDは励起に依存する蛍光特性を示し、励起波長が320から520 nmに変化すると、発光ピークは徐々に赤方偏移します。これは、図3aに示すように、励起波長を変更することでNBDの発光を調整できることを示しています。 NBD水溶液は、図3bの挿入図に示すように、屋内照明下では透明で、UV照明下では青色の蛍光を示します。 NBDのフォトルミネッセンス励起(PLE)スペクトルは、追加ファイル1:図S3に示されています。光励起波長は、360〜420nmの範囲です。 NBDのPL起源を調べるために、さまざまな濃度のNBDのUV-Vis吸収スペクトルを室温で記録しました(下から上へのNBDの濃度は0.03、0.06、0.13、0.25、0.25、0.50、0.50です)。 、0.75、1.00、および1.50 g / l)、図3bに示すように。 NBDのUV-Vis吸収スペクトルは、それぞれ270nmと330nmに2つの明確な吸収ピークを示します。前者はπ-π * に起因する可能性があります C–C / C =C結合の遷移、後者はn-π * への遷移 C =O / N結合の遷移[35、36]。これらの官能基は、NBDの蛍光に寄与する主要な発色基です[37、38]。超音波抽出中の大豆のPLスペクトルは、追加ファイル1:図S4に示され、PL強度は時間とともに増加し、その後最大に達します。図3cは、80〜300 Kで測定されたNBDのPLスペクトルを示しています。NBDは典型的な熱消光挙動を示し、温度の上昇とともにすべてのピークの強度が単調に減少します。このPLの振る舞いは、温度の上昇に伴う非放射再結合の増加と放射再結合の減少に起因する可能性があります[39、40]。 NBDの安定性を評価するために、図3dに示すように、NBDの光安定性と熱安定性が特徴付けられています。光安定性については、測定設定画像を追加ファイル1:図S5に示します。蛍光強度の値は、追加ファイル1:図S6およびS7に示されています。 NBDの発光強度は、UVランプ照明下で6時間90%を超えたままであり、良好な光安定性を示しています。熱安定性のために、温度が20から80 ° に変化したとき、NBDの蛍光強度はほとんど減少しません。 C、高い熱安定性を示しています。
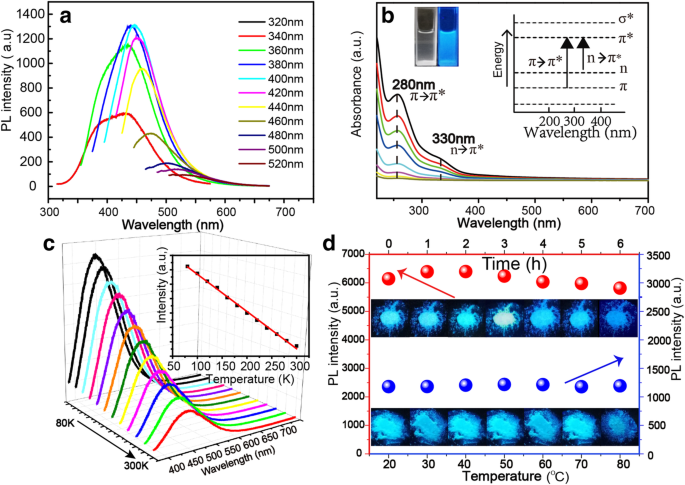
a 励起波長が320から520nmに変化するNBDの蛍光スペクトル。 b NBDのUV-Vis吸収スペクトル。 c 異なる温度でのNBDの蛍光スペクトル。挿入図は、温度の関数としてのNBDの蛍光強度のプロットです。 d さまざまな持続時間の365nmランプの照明下でのNBD粉末の蛍光強度と画像、およびさまざまな測定温度でのNBD粉末の蛍光強度と画像
細胞毒性評価
MTTアッセイは、NBDの細胞毒性を評価するために使用されました。図4に示すように、水熱法で合成されたNBDおよび他の2種類のCDとインキュベートしたHeLa細胞の生存率。図に示すように、NBD溶液を導入した場合、 NBDは800μg/ mlに達します。 HeLa細胞を他の2種類のCDと800μg/ mlの濃度でインキュベートした場合の細胞生存率は70%と67%でした。明らかに、NBDは化学試薬から調製されたCDよりも優れた生体適合性を示します。
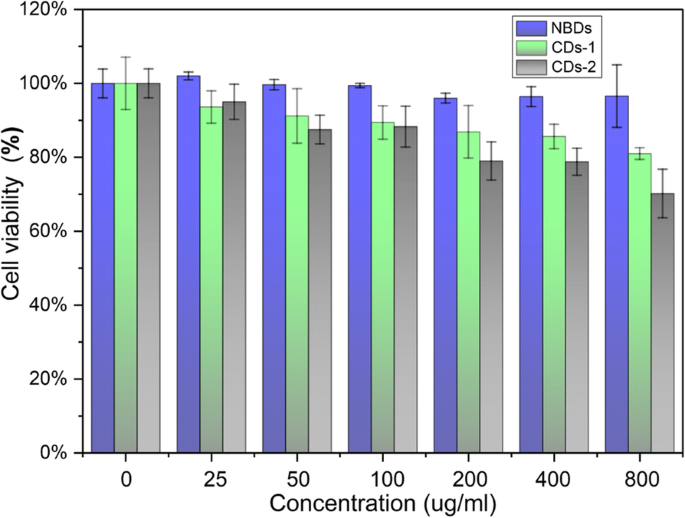
さまざまな濃度のNBDおよびCDとの72時間のインキュベーション後のHeLa細胞の生存率
Fe 3+ に向けたNBDのセンシングプロパティ
興味深いことに、NBDの蛍光はFe 3+ によって効果的に消光することができます。 、図5aに示すように、NBDのPL強度は、Fe 3+ の増加とともに大幅に減少します。 集中。さらに、F 0 の間に良好な線形関係をプロットできます。 / FとFe 3+ 0から30μMの範囲の濃度( R 2 =0.99)、ここでF 0 およびFは、Fe 3+ の非存在下および存在下でのex / em 370 / 445nmでのNBDのPL強度でした。 、図5bに示すように。消光効率は、シュテルン-フォルマー方程式によって適合されました:
$$ \ frac {{\ mathrm {F}} _ 0} {\ mathrm {F}} =1 + {K} _ {\ mathrm {SV}} \ left [Q \ right] $$(1)<図>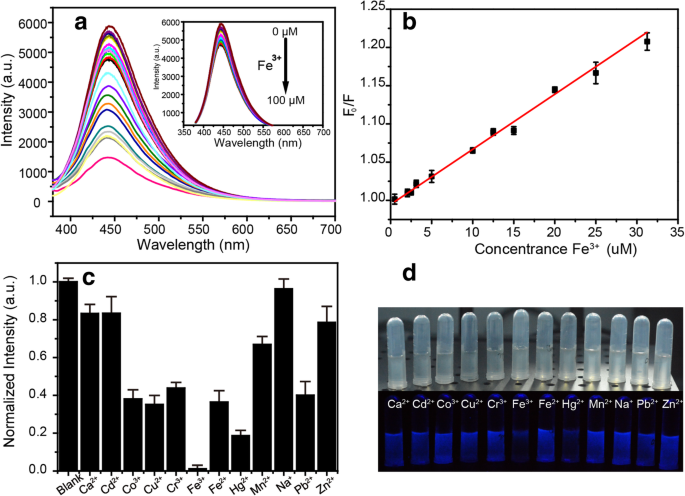
a 異なる濃度のFe 3 の存在下でのNBDのPLスペクトル + 。 b Fe 3 の関数としてのセンサーの検量線 + 集中。 c 異なるイオンの存在下でのNBDの蛍光強度。 d 屋内およびUV照明下でのさまざまな金属イオンを含むNBDソリューションの写真画像
ここで K sv はシュテルン-フォルマー消光定数であり、[ Q ]はFe 3+ です 集中。線形回帰方程式は Y です。 =0.0072 X + 0.99479、 R 2 =0.99。提案されたセンサーの検出限界(LOD)は2.9μMと決定されました。これはFe 3+ の最大許容レベルよりも低い値です。 (5.37μM)米国環境保護庁(USEPA)によって設定された飲料水中[24]。選択性は、化学センサーのもう1つの重要なパラメーターです。したがって、Ca 2+ を含む、いくつかの干渉金属イオンに対するセンサーの蛍光応答が調査されました。 、Cd 2+ 、Co 2+ 、Cu 2+ 、Cr 3+ 、Fe 3+ 、Fe 2+ 、Hg 2+ 、Mn 2+ 、Na + 、Pb 2+ 、およびZn 2+ 。それぞれ10 -2 の濃度の金属イオン Mを3g / lの濃度で1mlのNBD溶液に加えました。図5cでは、NBDの蛍光強度がFe 3+ に対してより敏感に反応することがわかります。 他の金属イオンより。図5dの写真は、屋内およびUV照明下でさまざまなイオンを含むNBDの画像であり、金属イオンの濃度は100μMでした。明らかに、NBDはFe 3+ の存在下で消光しています。 、視覚的検出に使用できることを示します。
消光メカニズム
Fe 3+ の存在下でのNBDの消光メカニズム NBDのUV-Vis吸収スペクトルと蛍光寿命に基づいて議論されました。追加ファイル1:図S8に示されているUV-Vis吸収スペクトルから、Fe 3+ を導入しても、270nmと340nmの吸収ピークに変化はありません。 、Fe 3+ NBDの構造には影響しません[41]。 UV-Vis吸収スペクトルとは別に、Fe 3+ の効果 NBDの寿命についても研究されました。図6aでは、Fe 3+ を添加すると、蛍光寿命が短くなります。 、これには、NBDの d への部分的な電子移動が含まれる場合があります。 Fe 3+ の軌道 したがって、NBDの放射再結合を減らします[42]。 Fe 3+ によって引き起こされるNBDの蛍光消光メカニズム 図6bに示します。 Fe 3+ の存在下でのNBDの高感度蛍光消光効果 Fe 3+ 間の強い相互作用に起因する可能性があります およびNBDの表面グループ。 Fe 3+ NBDの表面にあるアミノ基とカルボキシル基との結合親和性が強く、キレート化の速度が速くなります。 Fe 3+ 間の特別な調整 イオンおよびNBDのフェノール性ヒドロキシル/アミン基は、Fe 3+ の検出に広く使用されています。 従来の有機化学におけるイオンまたは着色反応[43、44]。さらに、Fe 3+ の酸化還元電位 / Fe 2+ (Ф =0.77)は、NBDの最低空軌道(LUMO)と最高空軌道(HOMO)の間に位置し、LUMOからFe 3+ の複雑な状態への光誘起電子移動を引き起こします。 [45]。これらの結果は、NBDがFe 3+ に非常に敏感であることを示しています。 他の金属イオンの上に。
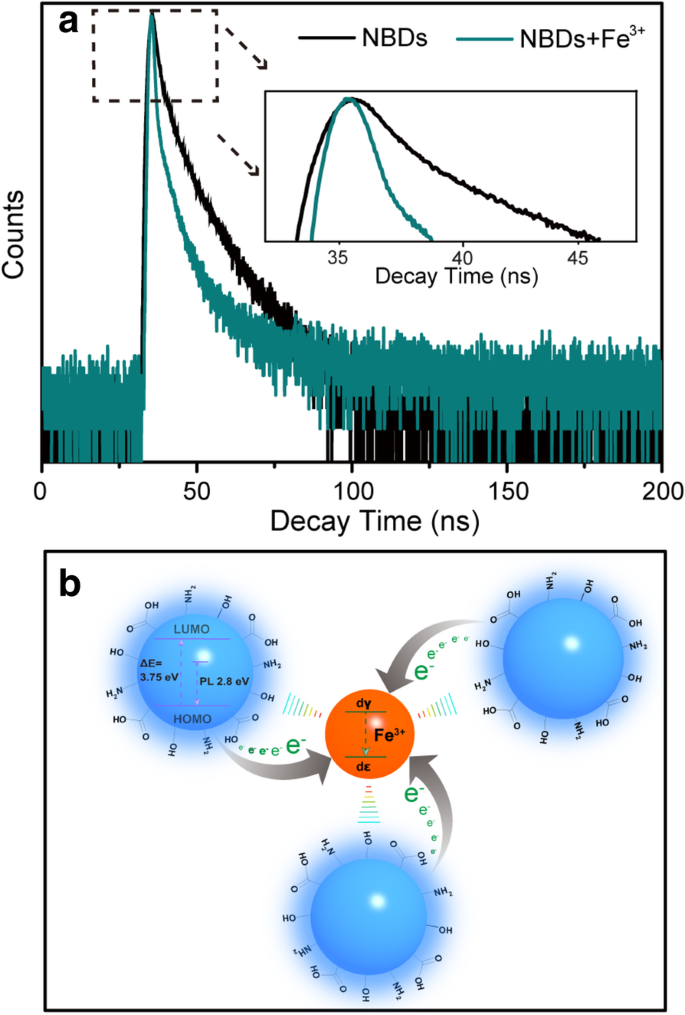
a Fe 3 の非存在下および存在下でのNCDの蛍光減衰トレース + 370nmで励起し、445nmで発光します。 b Fe 3 の存在下でのNBDの可能な蛍光消光メカニズムの概略図 + イオン
結論
要約すると、発光NBDは、大豆から加熱のないUESアプローチによって調製されています。 NBDはPLQYが16.7%の明るい青色の蛍光を示し、食用バイオマスと加熱のない合成プロセスの恩恵を受けて、NBDの濃度が800μg/ mlに達しても細胞生存率は100%を維持します。さらに、NBDの蛍光はFe 3+ に対して特定の感度を示します 、およびLODは2.9μMに達する可能性があります。毒性が低く、検出限界が高いことは、NBDが生物学的および環境的システムで潜在的な用途を見つけることが期待されていることを示しています。
略語
- FTIR:
-
フーリエ変換赤外
- HAADF-STEM:
-
高角度環状暗視野走査透過電子顕微鏡法
- LOD:
-
検出限界
- NBD:
-
ナノバイオマスドット
- NMR:
-
核磁気共鳴
- PL:
-
フォトルミネッセンス
- QD:
-
量子ドット
- QY:
-
量子収率
- TEM:
-
透過型電子顕微鏡
- UES:
-
超音波抽出戦略
- USEPA:
-
米国環境保護庁
- XPS:
-
X線光電子分光法
- XRD:
-
X線回折
ナノマテリアル
- 卵巣癌細胞の高感度かつ迅速な検出のための柔軟なグラフェンベースのバイオセンサーのデモンストレーション
- 改善された診断および治療用途のための多機能金ナノ粒子:レビュー
- 合成および生物医学的応用のための蛍光ナノ材料の進歩と挑戦
- Fe3 +の高感度測定のためのMXene量子ドットの蛍光を制御するN、N-ジメチルホルムアミド
- 再吸収抑制タイプII /タイプIZnSe / CdS / ZnSコア/シェル量子ドットの合成と免疫吸着アッセイへのそれらの応用
- 豆腐廃水から蛍光炭素量子ドットを合成するための簡単なアプローチ
- 水溶性硫化アンチモン量子ドットの合成とそれらの光電特性
- Fe3 +用の再開可能な蛍光プローブBHN-Fe3O4 @ SiO2ハイブリッドナノ構造とそのバイオイメージングへの応用
- Co3O4ナノワイヤの環境にやさしく簡単な合成とリチウムイオン電池でのグラフェンによるそれらの有望な応用
- 修飾BiOClの合成と特性評価および水溶液からの低濃度染料の吸着におけるそれらの応用
- 基板反りの原因と対策



