高い触媒活性と耐水性を備えたCO酸化とメタン燃焼のためにPdOナノ粒子で修飾されたロッド状のナノポーラスCeO2
要約
PdO / CeO 2 Al-Ce-Pd合金リボンの脱合金化と煆焼を組み合わせることにより、棒状のナノポーラス骨格構造を持つ複合材料を調製しました。 CO酸化およびCH 4 燃焼、ナノポーラスPdO / CeO 2 複合材料は優れた触媒活性を示し、COとCH 4 の完全な反応温度を示します。 それぞれ80°Cと380°Cです。さらに、この複合材料は優れたサイクル安定性、CO 2 を備えています。 毒性、耐水性、および水蒸気(2×10 5 )の存在下での100時間の長期安定性試験後の触媒活性の低下はほとんどありません。 ppm)。一連の特性評価の結果は、触媒活性の向上は、PdOナノ粒子の良好な分散、大きな比表面積、強力なレドックス容量、PdOとCeO 2 間の相互作用に起因する可能性があることを示しています。 、およびPdO上のより多くの表面活性酸素。特性評価と実験の結果は、脱合金化と焼成を組み合わせて調製されたPdOナノ粒子が、Pdナノ粒子よりも強力な触媒活性を持っていることも示しています。最後に、単純なモデルを使用して、PdO / CeO 2 の触媒メカニズムを要約します。 複合。この研究が高活性触媒の開発への洞察を提供することが期待されています。
背景
現在、環境問題に注目し、排気ガスや地球温暖化などのいくつかの重要な環境問題の緩和に焦点を当てる人が増えています[1、2]。特に、有毒なCOと温室効果ガスの除去CH 4 たくさんの研究の焦点です。そのような調査の中で、低温触媒作用はこれらの汚染ガスを排除する効果的な方法であることが証明されています[3,4,5,6]。
多くの研究により、安価な金属とその金属酸化物(遷移金属と酸化物、希土類金属と酸化物など)をCO酸化とCH 4 の触媒として使用できることが証明されています。 燃焼の場合、貴金属を使用すると通常、触媒性能が大幅に向上することは否定できません[7、8]。近年、PdおよびPdO触媒が広く研究されており、CO酸化およびCH 4 に最も効果的な触媒のいくつかであると考えられています。 燃焼。それらは、高温での低い揮発性だけでなく、低温での高い触媒活性も示します[9、10]。
しかし、用途の観点からは、地球中の貴金属の存在量は比較的少ないため、実際の工業用途で一般的に使用されるPdおよびPdO触媒は、金属酸化物、ゼオライト、炭素材料、および金属有機フレームワーク。この構成は、貴金属を保存し、サポートと貴金属の相互作用を使用して触媒活性を向上させることにより、持続可能な触媒作用を開発する傾向とも一致しています[11、12]。サポートの種類の中で、CeO 2 強力な酸素貯蔵/放出特性と優れた熱安定性により、有望なサポートと見なされています。たとえば、MacLachlan etal。ナノ構造のPdO / CeO 2 を作成するために、初期湿潤含浸と表面支援還元の組み合わせを使用しました 煆焼後のメタン燃焼の触媒として優れた活性を示した複合材料[13]。羅らPdO-CeO 2 の準備を報告しました 溶液燃焼法による触媒であり、PdOとCeO 2 の相乗効果が証明されました 強化された触媒活性の理由です[14]。
多くの良い結果が達成されましたが、まだいくつかの課題があります。たとえば、多くの有機化学物質または界面活性剤がナノ材料を汚染し、湿式化学で一般的な不十分な触媒活性をもたらす可能性があります[15]。さらに、液体前駆体の老化の方法に基づいて触媒を調製するプロセスは複雑であり、収率は低い[16]。したがって、非汚染、高収率、高触媒活性の材料の開発は依然として課題です。
この作業では、PdO / CeO 2 の作成方法を開発しました。 Al-Ce-Pd合金リボンを脱合金化してから焼成することによる複合材料。調製方法は簡単で、材料の構造は制御しやすく、有機試薬は必要ありません[17、18]。これは特に大規模な工業生産と持続可能な未来に適しています[19、20]。しかし、私たちが知る限り、メタン燃焼用の触媒を調製するための脱合金化の使用に関する文献報告はありません。したがって、この研究がナノ材料の合成と調製に関する洞察を提供し、支援することが期待されています。
メソッド
資料
すべての化学物質と金属は、さらに精製することなく、分析グレードの受け取ったままの状態で使用されました。純粋なAl(99.90 wt%)、純粋なCe(99.90 wt%)、および純粋なPd(99.90 wt%)はSino-Platinum Metals Co.、Ltdから入手しました。粒状NaOH(AR)はShanghai Aladdin Biochemical Technology Co.、Ltdから入手しました。 。高純度アルゴンはXi'anJiahe Co.、Ltd。から入手しました。
PdO / CeO 2 の合成 コンポジット
Al 92- X Ce 8 Pd X ( X =0、0.1、0.3、0.5、0.7、0.9、および1.1)前駆体合金は、アルゴン雰囲気下で純粋なAl、純粋なCe、および純粋なPdをアーク溶解することによって調製されました。得られたAl-Ce-Pd前駆体合金は、アルゴン保護下で石英管内で高周波誘導加熱により再溶解されました。溶融合金を高速回転銅ロールにアルゴンで吹き付けて急速凝固させ、幅約3〜4mm、厚さ約20〜30μmのAl-Ce-Pd合金リボンを得た。
調製したAl-Ce-Pd合金リボンを20wt%の水酸化ナトリウム溶液に入れ、周囲温度で2時間脱合金した後、80°Cに加熱して10時間脱合金しました。脱合金化したサンプルを脱イオン水で繰り返しすすぎ、室温で空気中で乾燥させた。乾燥したサンプルをO 2 で煆焼しました。 200〜600°Cで2時間、O 2 の流量 は18mLmin -1 。 PdO / CeO 2 の調製方法と構造進化 コンポジットを図1に示します。
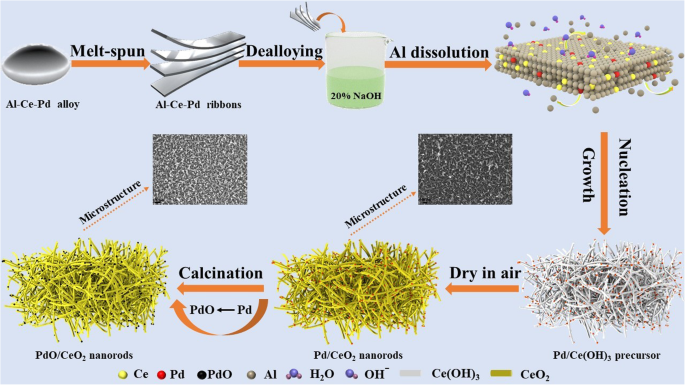
棒状のナノポーラスPdO / CeO 2 の調製の概略図 コンポジット
サンプルの特性評価
X線回折(XRD)パターンは、島津XRD-6100回折計とCuKα線(20kVおよび40mA)を使用して得られました。サンプルの形態と元素組成は、JSM-7000F走査型電子顕微鏡(SEM)とINCA X-Sight Oxfordエネルギー分散型分光計(EDS)から得られました。透過型電子顕微鏡(TEM)画像、高解像度透過型電子顕微鏡(HRTEM)画像、およびエネルギー分散型X線スペクトル(STEM-EDX)と組み合わせた走査型透過型電子顕微鏡画像をJEOLJEM-200電子顕微鏡で記録しました。比表面積( S ベット )、ポアサイズ( D p )、および細孔容積( V p )のサンプルは、Micromeritics ASAP2020装置を使用して77.4Kで測定しました。X線光電子分光法(XPS)分析は、多機能分光計モデルAxis UltraKratosを使用して実行しました。水素温度プログラム還元(H 2 -TPR)は、Quantachrome Autosorb-iQC-TPXで実行され、50mgのサンプルが10vol%H 2 <で10°C /分のランプ速度で50から800°Cに加熱されました。 / sub> / Ar混合ガスは40mL min -1 の速度で流れます 。
触媒テスト
サンプルの触媒活性は、CO酸化とCH 4 によって評価されました。 燃焼。触媒(100 mg)をステンレス鋼管状反応器に投入し、反応器を正確な温度制御を備えた管状炉に配置した。 1 vol%CO、10 vol%O 2 のいずれかで構成される供給ガス 、および89 vol%N 2 または1vol%CH 4 、10 vol%O 2 、および89 vol%N 2 総流量50mLmin -1 で反応器に導入しました。 (空間速度=30000 h -1 )、反応ガスの流量は、質量流量計(Brooks 5850E)によって制御および調整されました。 20 vol%H 2 を使用した供給ガスの調製の詳細 Oは追加ファイル1に示されています:図S1。 COとCH 4 加熱プロセス中の濃度は、水素炎イオン化検出器(FID)を備えたAgilentGC-7890Bガスクロマトグラフによってインラインで分析されました。 COとCH 4 の変換 式に従って計算されました。 (1):
$$ X =\ frac {C _ {\ mathrm {in}}-{C} _ {\ mathrm {out}}} {C _ {\ mathrm {in}}} \ times 100 \%$$(1)ここで X COまたはCH 4 の変換を表します 、 C in COまたはCH 4 の入口濃度を表します 、および C out COまたはCH 4 の出口濃度を表します 。
COとCH 4 の反応速度 式を使用して計算されました。 (2)[14、21]:
$$ {r} _ {\ mathrm {CO} / {\ mathrm {CH}} _ 4} =\ frac {C _ {\ mathrm {CO} / {\ mathrm {CH}} _ 4} \ cdot {X} _ { \ mathrm {CO} / {\ mathrm {CH}} _ 4} \ cdot P \ cdot V} {m _ {\ mathrm {cat}} \ cdot {W} _ {\ mathrm {Pd}} \ cdot R \ cdot T } \ left(\ mathrm {mol} \ cdot {\ mathrm {s}} ^ {-1} \ cdot {\ mathrm {g}} _ {\ mathrm {Pd}} ^ {-1} \ right)$$ (2)ここで r CO / CH4 COまたはCH 4 の反応速度を表します; COまたはCH 4 の濃度 C として表されます CO / CH4 供給ガス中; COまたはCH 4 の変換 X として表されます CO / CH4 ; P は大気圧で、101.3KPaです。 V は総流量です。 m cat 反応器内の触媒の質量です。 W Pd Pdの負荷です。 R はモルガス定数で、8.314 Pa m 3 です。 mol -1 K -1 ;および T は周囲温度(293 K)です。
結果と考察
触媒の特性評価
サンプルのXRDスペクトルを図2に示します。CeO 2 の回折ピークの明確なセット (JCPDSNO。34-0394)は、図2aに示すように検出されましたが、Pdに関連する回折ピークは、400°Cで煆焼されたすべての脱合金サンプルで検出されませんでした。解雇されたAl 91.3 Ce 8 Pd 0.7 図2bに示すように、合金はさまざまな温度で焼成されました。温度が徐々に上昇するにつれて、CeO 2 の回折ピーク 徐々に鋭く狭くなりました。しかし、800℃の煆焼後でも、Pdに関連する回折ピークは検出できませんでした。この結果は、サンプル中のPdの濃度が比較的低いためである可能性があり、アモルファス相または小さな結晶粒のいずれかの形でサンプル中に高度に分散している可能性があります。どのサンプルのXRDスペクトルにも、Alに関連する回折ピークは観察されませんでした。これは、脱合金化後のサンプルの残留Al含有量が非常に低いか、Alがアモルファスの形でサンプルに存在することを示しています。
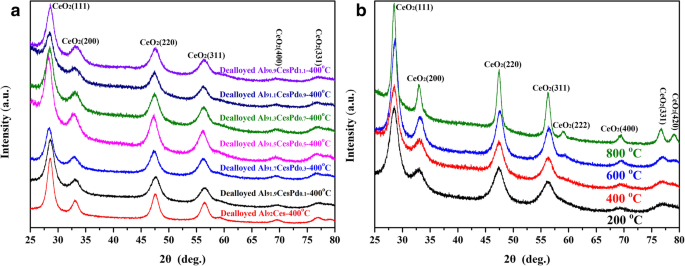
Al 92- X のXRDパターン Ce 8 Pd X ( X =0.1、0.3、0.5、0.7、0.9、および1.1)400°Cで脱合金化( a )および脱合金化されたAl 91.3 のXRDパターン Ce 8 Pd 0.7 異なる温度で焼成された合金( b )
脱合金化されたAl 91.3 のEDS結果と微細構造 Ce 8 Pd 0.7 400℃で煆焼したものを図3に示します。脱合金後のサンプル中のCeとPdの含有量は、図3aに示すように前駆体合金の含有量に非常に近く、CeとPdの損失が脱合金化プロセス中は小さい。脱合金されたAl 91.3 の残留Al Ce 8 Pd 0.7 400°Cで焼成された合金は非常に低く、わずか2.73%であり、XRDの結果と一致しています。図3bおよびcは、サンプルの表面SEM画像を示しています。サンプルは、直径が約10nmの多数のナノロッドで構成される均一で無秩序な織り多孔質構造を示しています。ナノロッドは互いに積み重ねられて、いくつかのミクロポアとメソポアを形成します。サンプルの断面SEM画像を図3dに示します。ナノロッドは互いに接続されて、大きな接触面積を通じてナノ粒子の安定化を促進する3次元骨格構造を形成し、よりナノスケールの相互作用をもたらします。インターフェース。
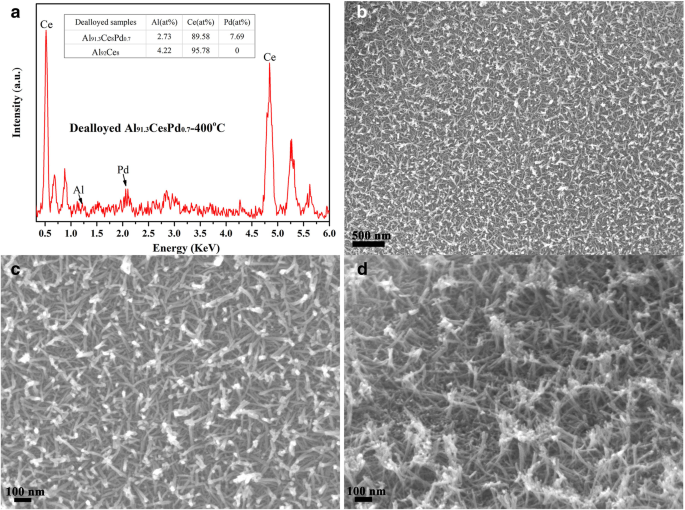
EDSパターン( a )、表面SEM画像( b 、 c )、および断面SEM画像( d )解雇されたAl 91.3 の Ce 8 Pd 0.7 400°Cで焼成された合金
図4に示すように、TEM画像とTEM-EDXマッピングをさらに使用して、サンプルの構造と粒子分布を特徴付けました。脱合金化されたAl 91.3 Ce 8 Pd 0.7 図4aに示すように、400°Cで焼成されたナノロッドは多数のナノロッドで構成され、ナノロッドは互いに積み重ねられて多数のミクロポアとメソポアを形成します。これはSEMの結果と一致しています。図4aの赤いボックスに示されているように、ナノロッドの表面にはいくつかの暗い粒子が分布しています。図4bは、サンプルのHRTEM画像を示しています。ナノロッドの格子間隔の値は約0.314nmと0.193nmであり、CeO 2 の(111)面と(220)面に対応します。 、 それぞれ。図4bの赤いボックスは、図4aに見られる暗い粒子のHRTEM画像です。この粒子は、直径が約5 nmで、CeO 2 の表面に分布しています。 ナノロッド。ただし、暗い粒子の格子間隔の値(0.201 nm)は、CeO 2 の(220)面の格子間隔の値と似ています。 (0.193 nm)であり、区別するのは困難です。これらの粒子を特定するために、TEM-EDXマッピングの特性評価が実施されました。図1と図2に示すように。 4cおよびd、CeO 2 に分布する粒子 ナノロッドはPdに関連しており、格子間隔の値が0.201 nmであることを考慮すると、暗い粒子はCeO 2 の表面に均一に分散しているPdOナノ粒子であると判断されます。 ナノロッド(図4d)、多数の粗い界面を形成します。
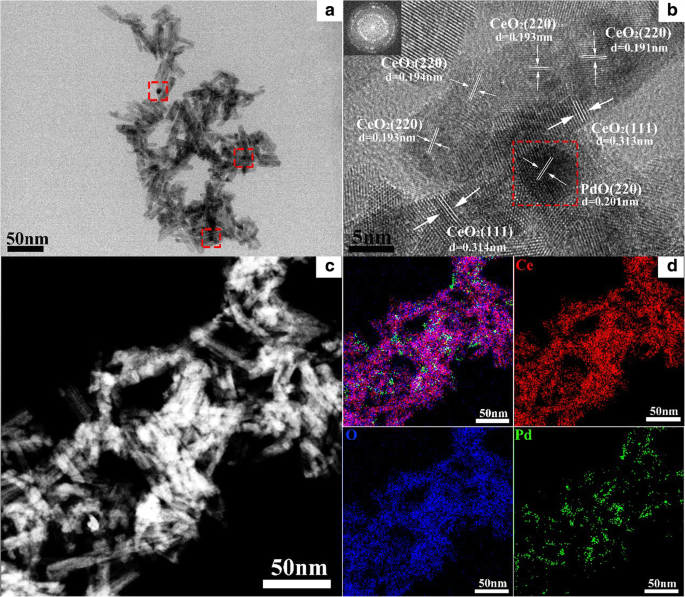
TEM( a )、HRTEM( b )、およびTEM-EDSマッピング( c 、 d )解雇されたAl 91.3 の画像 Ce 8 Pd 0.7 400°Cで焼成された合金
BETおよびBJHテストは、脱合金化されたAl 91.3 で実行されました。 Ce 8 Pd 0.7 さまざまな温度で煆焼し、対応する結果を図5と表1に示します。すべてのサンプルは、H 2 のタイプIV等温線を示しました。 およびH 3 図5aに示すように、ヒステリシスループ。この結果は、サンプルがメソポーラス構造であることを示しており、SEMおよびTEMの結果と一致しています。さらに、図5bに示す細孔径分布曲線は、すべてのサンプルがメソポーラス構造を持っていることをさらに証明しており、焼成サンプルは、平均細孔径が約12〜14nmの同様に狭い細孔径分布を示しました。比表面積( S ベット )、ポアサイズ( D p )、および細孔容積( V p )対応する煆焼温度でのサンプルを表1に示します。400°Cの煆焼サンプルは、最大の比表面積と約102 m 2 に等しい最大の細孔容積を示します。 g -1 および0.362cm 3 g -1 、 それぞれ。煆焼温度が連続的に上昇するにつれて、比表面積はわずかに減少しました。ただし、600°Cの煆焼後でも、サンプルの比表面積は84 m 2 でした。 g -1 。これらの結果は、棒状のナノポーラスCeO 2 骨格構造は優れた焼結防止能力を持っています。この結論は、追加ファイル1:表S1の結晶サイズと、追加ファイル1:図S2のSEMおよびTEM画像によっても確認されます。
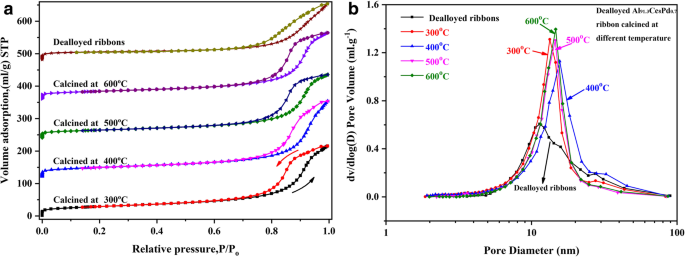
窒素の吸脱着等温線( a )および細孔径分布曲線( b )脱合金化されたAl 91.3 Ce 8 Pd 0.7 さまざまな温度で煆焼されたリボン
脱合金化されたAl 91.3 のXPSスペクトル Ce 8 Pd 0.7 サンプルと煆焼された脱合金Al 91.3 Ce 8 Pd 0.7 サンプルの表面元素の原子価組成をさらに特徴づけるために、サンプルを図6に示します。 Ce 3dのXPSスペクトルを図6aに示します。ここで、UはCe 4+ を表します。 VはCe 3+ を表します [22]。一般的に、Ce 3+ の存在 酸素空孔と密接に関連しています。計算結果は、Ce 3+ の濃度が 解雇されたAl 91.3 Ce 8 Pd 0.7 サンプルと煆焼された脱合金Al 91.3 Ce 8 Pd 0.7 表2に示すように、サンプルはそれぞれ21.15%と23.33%であり、ほとんど差がありませんでした。この結果は、煆焼が表面酸素空孔の濃度にほとんど影響を与えないことを示しています。サンプルの酸素空孔濃度に対するPdO負荷の影響を理解するために、脱合金化されたAl 92 のXPSスペクトル Ce 8 400°Cで煆焼したサンプル(純粋なCeO 2 )は追加ファイル1に示されています:図S3。 Ce 3+ 濃度は約14.27%と計算されました。これは、PdOをロードしたサンプルの濃度よりもはるかに低い値です。この現象は、PdOとCeO 2 の間に相互作用があることを示しています。 また、PdOの存在により、CeO 2 の原子価状態が変化する可能性があること 表面元素と表面酸素空孔の濃度を増加させます。
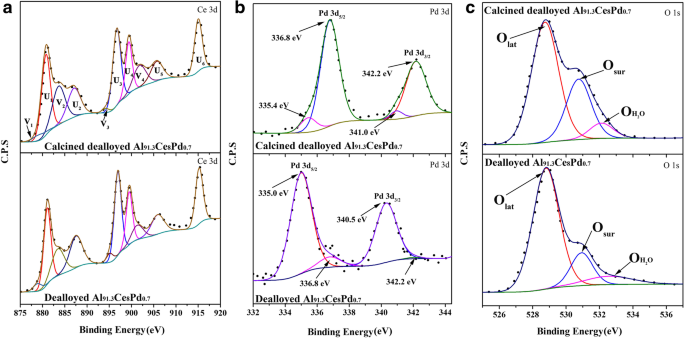
Ce 3dのXPSスペクトル( a )、Pd 3d( b )、およびO 1s( c )脱合金化されたAl 91.3 の地域 Ce 8 Pd 0.7 サンプルと脱合金化されたAl 91.3 Ce 8 Pd 0.7 400°Cで煆焼したサンプル
表面のPdOナノ粒子に対する焼成の影響をさらに調査するために、脱合金化されたAl 91.3 のPd3dXPSスペクトル Ce 8 Pd 0.7 サンプルと煆焼された脱合金Al 91.3 Ce 8 Pd 0.7 サンプルを図6bに示します。煆焼された脱合金Al 91.3 には2つの形態のPdがあります Ce 8 Pd 0.7 リボン; 336.8eVと342.2eVの強いピークは、PdO(Pd 2+ )に起因する可能性があります。 )[23]、335.4eVと341.0eVの弱いピークは金属Pd(Pd 0 )[24]。表2は、Pd 2+ の濃度を示しています。 およびPd 0 それぞれ約91.25%と8.75%でした。ただし、脱合金化されたAl 91.3 の分析結果 Ce 8 Pd 0.7 サンプルは反対で、Pd 2+ の濃度 およびPd 0 それぞれ約6.45%と93.55%でした。この発見は、Pdが脱合金化されたサンプルに金属Pdの形で存在するのに対し、煆焼後、PdはPdOに酸化され、CeO 2 の表面に均一に分散したことを示しています。 、これはHRTEM画像の結果と一致しています。
表面活性酸素(O sur )は通常、触媒反応の活性酸素種です。図6cは、2つの触媒のO 1sXPSスペクトルを示しています。煆焼された脱合金Al 91.3 Ce 8 Pd 0.7 サンプルでは、528.9 eV、530.6 eV、および532.1 eVのピークが格子酸素(O lat )に対応します。 )、表面活性酸素(O sur )、および弱く吸着されたH 2 O(O H2O )、それぞれ[25、26]。 O sur の比率 (O sur /(O lat + O sur + O H2O ))が計算され、表2にリストされています。O sur の比率 解雇されたAl 91.3 Ce 8 Pd 0.7 サンプルと煆焼された脱合金Al 91.3 Ce 8 Pd 0.7 サンプルはそれぞれ約16.2%と29.3%であり、煆焼された脱合金化されたAl 91.3 に表面活性酸素種がより多く存在することを示しています。 Ce 8 Pd 0.7 サンプル。 Ce 3+ の濃度 これら2つの触媒は類似しており(図6a)、PdOがO 2 を吸着して活性化するより強力な能力を持っていることを示唆しています。 金属Pdナノ粒子よりも。別の実験(追加ファイル1)は、追加ファイル1:図S4に示すように、実験結果に対する熱活性化の干渉を排除するように設計されており、得られた結果も上記の結論を裏付けています。
煆焼前後のサンプルの還元性の違いを比較するために、H 2 -TPRを使用して、煆焼された脱合金Al 91.3 の両方をテストしました。 Ce 8 Pd 0.7 サンプルと脱合金化されたAl 91.3 Ce 8 Pd 0.7 2つのTPR曲線には3つの主要なピークがありますが、それらの強度と位置は異なります。 2セットのピーク、P 2 、P 2 ′およびP 3 、P 3 '、高温範囲(> 300°C)では、表面CeO 2 の還元に起因します。 およびバルクCeO 2 、それぞれ[27]、P 1 およびP 1 低温範囲(<300°C)の 'ピークは、PdO種とPd 2+ の還元に起因します。 -O-Ce 4+ 構造[28]。 P 1 の面積 ピークはP 1 のピークよりも大幅に大きい 'ピーク。これは、煆焼された脱合金化されたサンプルがより多くのPdO種を含んでいたことを示しており、XPSの結果と一致しています。 P 1 という事実 ピーク面積がP 1 よりも大きい 'ピークは、煆焼された脱合金サンプルの場合、Ce 4+ が多いことも示しています。 PdO種に結合したイオンは低温で還元することができ、これは接触酸化反応に有利です。 P 2 およびP 2 470°C付近にある 'ピークもこの推測を証明しています。 P 2 の面積 'ピークはP 2 のピークよりも大幅に大きい ピーク。これは、煆焼された脱合金サンプルの場合、表面CeO 2 の濃度を示しています。 高温でのみ還元できる種は、脱合金化されたサンプルの種よりも少なかった。つまり、Ce 4+ の一部 PdOに接続されたイオンは低温で還元されました。 XPS分析と組み合わせると、PdO / CeO 2 の酸化還元能力 コンポジットはPd / CeO 2 よりも高い 、これは、PdO / CeO 2 複合材料はより高い触媒性能を示します。
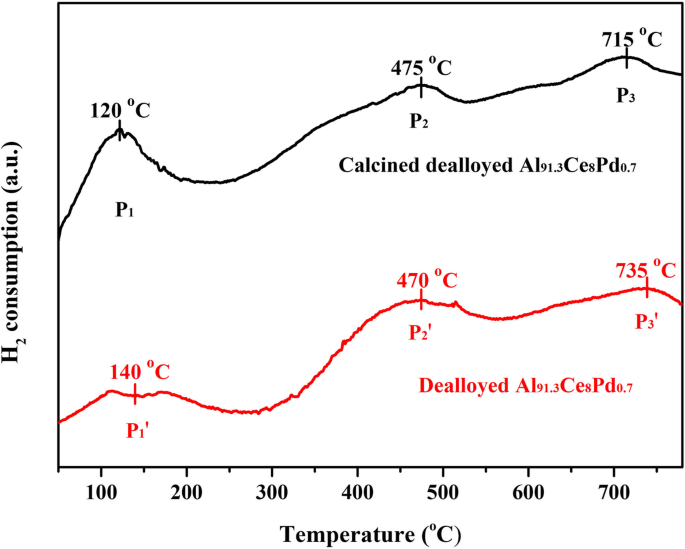
H 2 -脱合金化されたAl 91.3 のTPR曲線 Ce 8 Pd 0.7 リボンと脱合金化されたAl 91.3 Ce 8 Pd 0.7 400°Cで煆焼したリボン
上記の特性評価の結果に基づいて、PdO / CeO 2 の可能な形成メカニズム コンポジットが提案されています(図1)。まず、NaOH溶液にAlを溶解し、CeをOH - と反応させます。 80°Cで棒状のナノポーラスCe(OH) 3 を形成します Ce(OH) 3 の異方性による骨格構造 成長。同時に、Pd原子はCe(OH) 3 の表面に拡散します。 ナノロッド。 Ce(OH) 3 非常に不安定で、容易に脱水および酸化されてCeO 2 になります。 空気中での乾燥中。 O 2 での煆焼後 、CeO 2 の表面にあるほとんどのPdナノ粒子 ナノロッドは酸化されてPdOを形成し(図6b)、CeO 2 に部分的に埋め込まれました。 ナノロッド(図4)を高温で使用すると、強力な金属酸化物と支持体の相互作用が生じます。その結果、PdO / CeO 2 複合材料が形成されました。
触媒活性テスト
前駆体中のPdの含有量と触媒の触媒活性との関係を図1および2に示します。 8aおよびb。図8aに示すように、CeO 2 ナノロッドは、CO(挿入図)の酸化に対して不十分な触媒活性を示し、 T 99 (変換率が99%の場合の対応する反応温度)は280℃と高い。 PdOの負荷により、CO酸化の触媒活性が大幅に向上しました。脱合金化されたAl 91.3 のサンプル Ce 8 Pd 0.7 最高のCO触媒活性を示し、 T 50 (変換率が50%の場合の対応する反応温度)および T 99 それぞれ15°Cと80°Cでした。着火温度も−20℃以下でした。しかしながら、前駆体中のPdの含有量がさらに増加すると、触媒活性はわずかに低下した。 CH 4 に対する触媒活性 異なるPd含有量の前駆体から生成された触媒の燃焼を図8bに示します。CO酸化で見られるものと同様に、純粋なCeO 2 ナノロッドは、CH 4 に対して不十分な触媒活性を示します 燃焼し、600°Cでの転化率はわずか65%でした。 PdOの添加後、触媒活性は大幅に改善されました。同様に、解雇されたAl 91.3 Ce 8 Pd 0.7 サンプルはCH 4 に対して最高の触媒活性を示しました 燃焼、約250°Cの着火温度、および T 50 および T 99 それぞれ305°Cと380°Cでした。
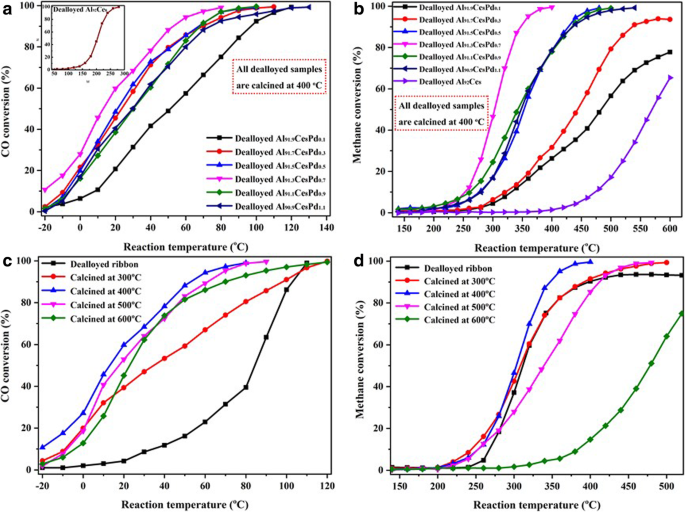
CO変換( a )およびCH 4 変換( b )脱合金化したAl 90 の反応温度の関数として Ce 10 リボンおよび400°Cで焼成された異なるPd含有量の脱合金化されたAl-Ce-Pdリボン。 CO変換( c )およびCH 4 変換( d )脱合金化したAl 91.3 の反応温度の関数として Ce 8 Pd 0.7 さまざまな温度で煆焼
COとCH 4 脱合金化されたAl 91.3 に対する反応温度の関数としての変換 Ce 8 Pd 0.7 異なる温度で煆焼されたリボンを図8cおよびdに示します。図8cに示すように、脱合金化されたリボン(煆焼なし)は、煆焼されたサンプルのCO触媒活性と比較して低いCO触媒活性を示しました。 XPS分析と組み合わせると、これらの結果は、PdOがCeO 2 でサポートされていることを示しています。 ナノロッドは、Pdよりも優れたCO触媒活性を示します。これは、H 2 と一致しています。 -TPR分析。 400°C未満では、COに対する触媒活性は煆焼温度とともに徐々に増加しました。しかし、400℃を超える温度で煆焼すると、COに対する触媒活性は煆焼温度の上昇とともに低下しました。 CH 4 の場合 同様に、燃焼では、図8dに示すように、400°Cで焼成されたサンプルが最高の触媒活性を示しました。ただし、脱着したリボンは着火温度と T を示しました 50 煆焼したサンプルと同様で、CH 4 の変換 常に93%未満でした。異なるO 2 の下での脱合金化リボンと焼成脱合金化リボンの触媒活性の実験結果と分析によると、 大気(追加ファイル1:図S5)の場合、この現象の理由は、CH 4 の着火温度が原因である可能性があります。 高く(> 240°C)、Pdの一部が酸化されてPdOになりました。したがって、サンプルは良好なCH 4 を示します。 触媒活性。ただし、複合材料は純粋なO 2 では煆焼されないため 大気中では、酸化が不十分で、CH 4 を完全に変換することができませんでした。 。解雇されたAl 91.3 の場合 Ce 8 Pd 0.7 さまざまな温度で煆焼され、CH 4 に対する触媒活性の順序 脱合金サンプル(煆焼なし)<600°Cで煆焼<500°Cで煆焼<300°Cで煆焼<400°Cで煆焼。実験結果は、煆焼温度がサンプルの触媒活性に重要な影響を与えることを示しています。
サイクル安定性テストは、脱合金化されたAl 91.3 でも実行されました。 Ce 8 Pd 0.7 図1および2に示すように、400°Cで焼成したリボン。 9aおよびb。 COの酸化用かCH 4 の燃焼用か 、結果は、これらの3つの連続した活性試験で同様の曲線が得られ、触媒が安定しており、失活していないことを示しています。この結果は、脱合金化したAl 91.3 を煆焼して得られた触媒であることを示しています。 Ce 8 Pd 0.7 400°Cのリボンは実用的な用途があり、複数回繰り返し使用できます。
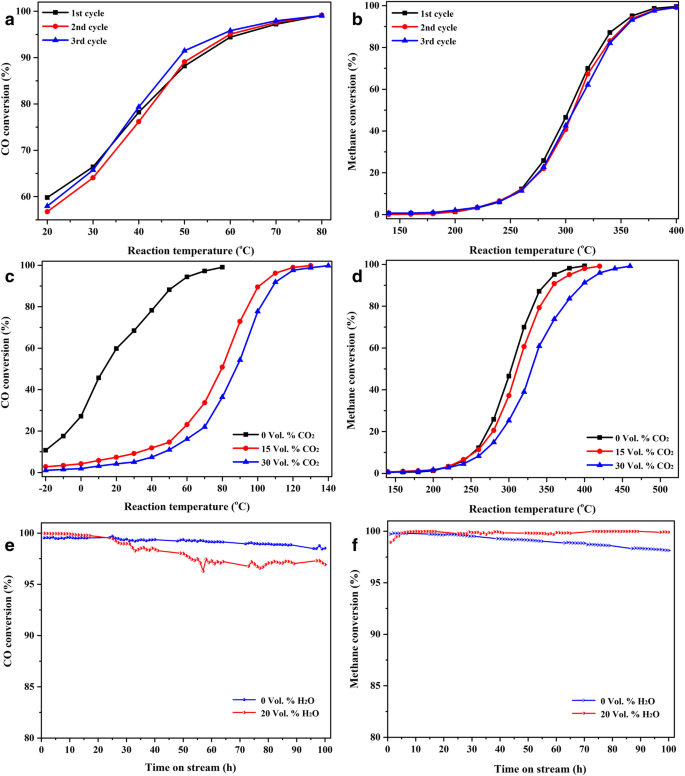
周期的安定性試験( a 、 b )、CO 2 に対する耐性 毒性試験( c 、 d )、および耐水性テスト( e 、 f )解雇されたAl 91.3 の Ce 8 Pd 0.7 400°Cで煆焼したリボン
一般に、実用的な用途価値のある触媒の場合、CO 2 の存在下で安定している必要があります。 およびH 2 O. CO 2 を含む反応ガス またはH 2 Oを触媒に通してCO 2 を調べた およびH 2 脱合金化されたAl 91.3 のO公差 Ce 8 Pd 0.7 図1および2に示すように、400°Cで焼成したリボン。 9c–f。 CO 2 がない場合の応答と比較 反応ガスに15vol%CO 2 を添加 図9cに示すように、 T を使用すると、CO酸化に対する触媒の活性が低下しました。 50 および T 99 それぞれ80°Cと130°Cの。ただし、CO 2 をさらに増やすと 30 vol%まで、CO酸化に対する触媒の活性はわずかに低下し、 T 50 および T 99 それぞれ88°Cと140°Cです。メタン燃焼の場合、15 vol%CO 2 の存在 反応ガス中の触媒活性にはほとんど影響がなく、 T 50 および T 99 CO 2 がない場合と比較して、それぞれ5°Cと30°Cだけ上昇しました。 、図9dに示すように。 CO 2 の濃度が 2倍になりました(30 vol%CO 2 )、 T で、触媒活性は低下し続けます 50 および T 99 それぞれ350°Cと460°Cです。したがって、反応物の濃度が一定の場合、CO 2 の濃度を上げます。 製品はCOおよびCH 4 と強力な競争関係を形成します PdOナノ粒子とその界面への吸着により、COまたはCH 4 の量を削減します。 単位時間あたりに吸着され、その結果、変換率。ただし、メタンの燃焼に必要な反応温度が高いため、CO 2 の脱着 CO 2 メタン燃焼への影響は、CO酸化への影響よりも弱いようです。
触媒の長期安定性および耐水性試験を図1および2に示します。 9eおよびf。 CO酸化の場合、高濃度の水蒸気(20 vol%)の有無にかかわらず、100時間の試験後、触媒活性はほとんど低下せず、CO酸化に対して優れた長期安定性と耐水性を備えていることを示しています。 。高転化率(99%)でのメタン燃焼の場合、触媒はCO酸化に関して同様の特性を持っています。同時に、低変換率(30%、50%、および85%)でのメタン燃焼に対する水蒸気の影響についても、追加ファイル1:図S6で説明しています。低転化率での触媒活性に対する水蒸気の影響は、高転化率でのそれよりも大きい。詳細な説明と説明は、追加ファイル1:図S6に示されています。得られた結論は、Burchらによって報告されたものと同様です。 [29]。最近報告されたメタン燃焼用のPdベースの触媒の耐水性(追加ファイル1:表S2)と比較すると、PdO / CeO 2 この研究で調製された触媒は、より高い水蒸気濃度(20 vol%)とより長い反応時間(100 h)の後、比較的優れた触媒活性を保持します。これは、メタン燃焼の実用化を促進するのに非常に役立ちます。
反応ガスの流量とO 2 の濃度 触媒の触媒活性に重要な影響を与えることが知られています。ここでは、脱合金化されたAl 91.3 の触媒性能に対する流量の影響 Ce 8 Pd 0.7 図1および2に示すように、400°Cで焼成されたリボンが最初に研究されました。 10aおよびb。図10aに示すように、CO酸化の場合、総流量を20 mL min -1 から増加させた場合 (空間速度12,000 h -1 )〜100 mL min -1 (空間速度60,000 h -1 )、COの変換は最初の78%から31%に徐々に減少しました。ただし、COの変換は流量の増加とともに減少しましたが、反応速度( r CO )徐々に増加しました。この現象は、ガスの流量を増やすと、ガスと活性部位との接触時間が短くなり、変換率が低下するために発生しました。しかしながら、単位時間あたりに活性部位上を流れる反応物の実際の量が増加し、それにより反応速度が増加した。メタン燃焼でも同様の現象が見られました。ただし、CH 4 の変換に対する流量の影響はわずかに小さいようです。 COの変換よりも。流量が20から100mLに増加するにつれてmin -1 、メタンの変換率は初期値の84%から53%に減少しました。さらに、メタン燃焼の反応速度( r CH4 )は、 r で見られるのと同様に、安定したままになる傾向ではなく、流量とともに直線的な増加を示しました。 CO 。これは、CO酸化よりもメタン燃焼の方が触媒の流量範囲が広いことを示しています。この研究では、 r の計算値 CO および r CH4 さまざまなテスト条件下で、1.40〜2.87の範囲でした\(\ left(\ times {10} ^ {-5} \ mathrm {mol} \ cdotp {\ mathrm {g}} _ {\ mathrm {Pd}} ^ {-1} \ cdotp {\ mathrm {s}} ^ {-1} \ right)\)および1.51〜4.70 \(\ left(\ times {10} ^ {-5} \ mathrm {mol} \ cdotp {それぞれ\ mathrm {g}} _ {\ mathrm {Pd}} ^ {-1} \ cdotp {\ mathrm {s}} ^ {-1} \ right)\)。
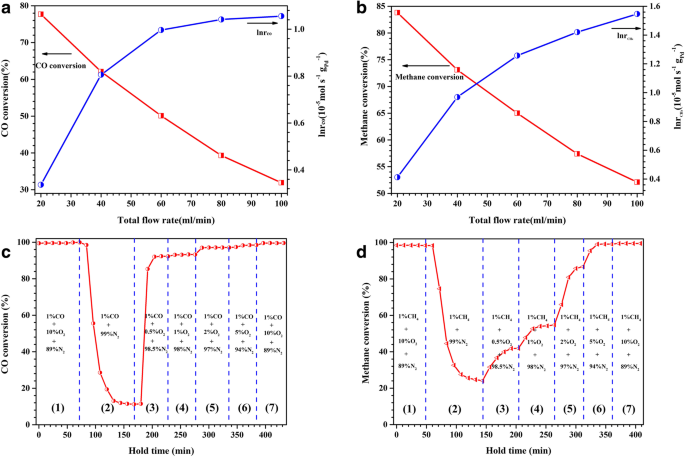
脱合金化したAl 91.3 の触媒活性と反応速度 Ce 8 Pd 0.7 20°Cで異なる流量でCO酸化のために400°Cで焼成されたリボン( a )および320°Cでのさまざまな流量のメタン燃焼用( b )(反応ガス1 vol%CO / CH 4 、10 vol%O 2 、および89%vol%N 2 。)。脱合金化したAl 91.3 の触媒活性 Ce 8 Pd 0.7 さまざまなO 2 の存在下でCO酸化のために400°Cで焼成されたリボン 80°Cでの濃度( c )および異なるO 2 の存在下でのメタン燃焼用 380°Cでの濃度( d )
次に、O 2 の効果 触媒の触媒活性に対する反応ガス中の濃度を調べた。 CO酸化の場合、図10cに示すように、酸素が豊富な条件下(10 vol%O 2 )、CO変換は99%に維持され、O 2 濃度が突然0(嫌気性条件)に減少すると、CO変換は急速に減少し、最終的には約12%で安定しました。この現象の理由は、表面格子酸素がCOの酸化反応に関与したためでした。一般に、支持体の表面に格子酸素が関与するCO酸化経路は、O の直接吸着活性化と比較して遅く、非効率的です。 2 分子[30]。したがって、この研究では嫌気性条件下でCO変換は低いレベルにとどまりました。この結果は、CeO 2 キャリアは酸素を貯蔵/放出する強力な能力を持っています。続いて、0.5%O 2 反応ガスに導入され、CO転化率は90%まで急速に回復しました。 O 2 として 濃度は増加し続け、CO変換は最終的に最初の99%に達し、新しい定常状態が確立されました。メタン燃焼(図10d)については、CO酸化の結果と同様の結果が観察されましたが、2つの異なる点があります。最初のポイントは、嫌気性環境では、CH 4 の変換でした 最終的に25%で安定し、COの嫌気性変換よりも高くなりました。これは、高い反応温度が表面格子酸素の移動を加速し、変換効率を向上させる可能性があることを示しています。 2番目のポイントは、O 2 として 濃度が増加し、CH 4 の増加率 変換と定常状態の最終的な確立は、CO変換の場合よりも遅くなりました。これは、酸素の少ない条件下(0.5〜2 vol%O 2 )でのメタンの不完全燃焼が原因である可能性があります。 )。この結果は、メタンの燃焼がCO酸化に比べてより複雑で困難な反応であることも示しています。
特性評価と実験の結果に基づいて、図11に示すように、CO酸化とメタン燃焼の簡単なメカニズムが提案されます。
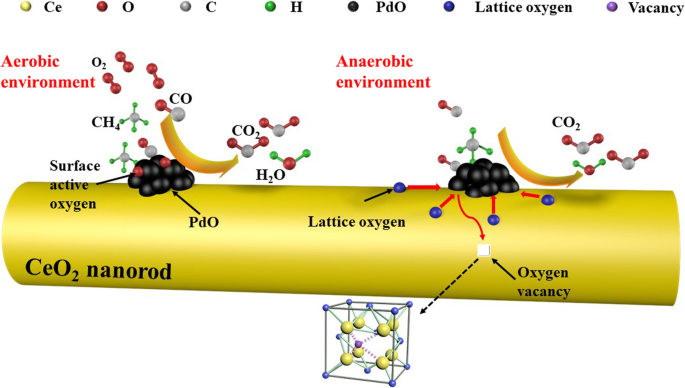
棒状のナノポーラスPdO / CeO 2 でのCO酸化とメタン燃焼の概略図 触媒
まず、COとCH 4 反応ガス中の分子はPdOの表面に吸着され、PdOの表面に吸着され活性化された酸素と急速に反応し、次にCO 2 およびH 2 Oが生成され、脱着されます。活性部位が再び利用可能になり、CO酸化とCH 4 の反応速度が高くなります 燃焼が維持されます。触媒酸化反応は嫌気性条件下でもゆっくりと進行する可能性があることは注目に値します。これは、図10c、dに示すように、ナノロッドの表面格子酸素が触媒反応に関与することに関連していることが示されています。 。11。
多数の実験結果は、PdO / CeO 2 脱合金化と煆焼を組み合わせて調製した触媒は、CO酸化とメタン燃焼に対して優れた触媒活性を示し、優れたサイクル安定性、CO 2 に対する耐性を備えています。 毒性、および耐水性。その固有の単純さに加えて、脱合金化の「グリーン」調製法は、湿式化学合成法に一般的な有機化学物質や他の界面活性剤によるナノ材料の汚染を効果的に回避することができます。さらに、PdO / CeO 2 脱合金化と煆焼を組み合わせて調製された触媒は優れた再現性を示し、追加ファイル1:図S7〜S10、表S3およびS4に詳述されている繰り返しの実験はこの点を非常によく証明しました。したがって、この作業は他の新しい触媒の準備への洞察を提供することができます。
結論
要約すると、煆焼と組み合わせたAl-Ce-Pdリボンの脱合金化の簡単な方法が、PdO / CeO 2 の調製のために開発されました。 棒状のナノポーラス複合材料。実験結果は、Al 91.3 の脱合金化によって調製されたサンプルを示しています。 Ce 8 Pd 0.7 20 wt%溶液でリボンを使用し、400°Cで煆焼すると、COの酸化とメタンの燃焼、およびCOとCH 4 の完全な変換の反応温度に対して最高の触媒活性が示されました。 それぞれ80°Cと380°Cです。高い触媒活性は、PdOナノ粒子の良好な分散に起因する可能性があります(102 m 2 の大きな比表面積を持っています g -1 )、強力なレドックス能力、PdOとCeO 2 間の相互作用 、およびPdO上のより多くの表面活性酸素。さらに、この触媒は優れたサイクル安定性、CO 2 に対する耐性も示しました。 毒性、および耐水性。100時間の試験後、H 2 の存在下で触媒活性はほとんど低下しませんでした。 O.さらに、触媒反応は嫌気性条件下でも発生する可能性があります。これらの結果は、新しい触媒の調製のための複合脱合金煆焼法の実現可能性を示しています。この方法は、同様の複合材料の調製に適用できることが期待されます。
データと資料の可用性
この記事の結論を裏付けるデータセットは、記事に含まれています。
略語
- CH 4 :
-
メタン
- CO:
-
一酸化炭素
- D p :
-
ポアサイズ
- EDS:
-
エネルギー分散型分光計
- EDX:
-
エネルギー分散型X線スペクトル
- FID:
-
水素炎イオン化検出器
- H 2 -TPR:
-
水素温度プログラムによる還元
- S ベット :
-
比表面積
- SEM:
-
走査型電子顕微鏡
- TEM:
-
透過型電子顕微鏡
- V p :
-
細孔容積
- XPS:
-
X線光電子分光法
- XRD:
-
X線回折
ナノマテリアル
- 癌治療のためのナノ粒子:現在の進歩と課題
- Sb /パリゴルスキー石(PAL)ナノ粒子の調製と強化された接触水素化活性
- 非常に効果的な標的膵臓腫瘍治療のための、血液循環が延長され、生体適合性が改善されたレスベラトロール負荷アルブミンナノ粒子
- 炭化水素中の金ナノ粒子のサイズ制御と安定化のための分散剤としての修飾ハイパーブランチポリグリセロール
- 光触媒活性が強化されたAgナノ粒子/ BiV1-xMoxO4の相乗効果
- 6-メルカプトプリンとニューロン透過性ペプチドで修飾された金ナノ粒子によるSH-SY5Y細胞増殖の促進
- Auナノ粒子で調整されたシリカ珪藻殻により、生物学、安全、環境アプリケーション向けの分子の高感度分析が可能になります
- ナノ粒子と超音波によって制御される水の過冷却
- 酸化亜鉛ナノ粒子の特性と微生物に対するそれらの活性
- 非常に濃縮された亜鉛源を用いた水/グリセロール中のナノサイズの酸化亜鉛の調製のための簡単なアプローチ
- 膀胱癌細胞を阻害するための疎水性修飾プルランナノ粒子を用いたミトキサントロンの新規送達および阻害効率に対するナノ薬物サイズの影響



